Стадии болезни паркинсона по хен яру: Болезнь Паркинсона – причины возникновения, признаки и симптомы, лечение болезни Паркинсона
Стадии болезни Паркинсона — гимнастика: упражнения и инвентарь
1
Что такое болезнь Паркинсона и сколько стадий выделяют?
Это серьёзное нейродегенеративное заболевание. В данной статье мы обсудили:
- причины и факторы риска;
- двигательные нарушения;
- недвигательные симптомы;
- виды заболевания;
- методы лечения.
Болезнь Паркинсона влияет на людей по-разному, но на каждой стадии можно отметить ряд общих симптомов. Врачи обычно используют классификацию по Хен-Яру, введённую ещё в 1967 году, согласно которой двигательные нарушения оценивают по шкале от 1 до 5 и выделяют, соответственно, пять стадий болезни. Сегодня мы поговорим о каждой отдельно.
2
Что происходит на первой стадии?
На данном этапе симптомы болезни практически незаметны и не влияют на качество жизни. Пациента могут беспокоить:
- скованность в конечностях;
- лёгкий тремор при волнении;
- подавленное настроение;
- бессонница и усталость.

Отличительной особенностью начальной стадии является то, что двигательные нарушения затрагивают только одну сторону тела. Важно вовремя начать лечение, чтобы отсрочить прогрессирование заболевания и уменьшить симптомы. В этом пациенту помогут лекарства и физиотерапия.
3
Что происходит на второй стадии?
На данном этапе симптомы ухудшаются и охватывают уже обе стороны тела.
- снижается подвижность суставов;
- возникают сложности с передвижением;
- тремор рук становится более заметным;
- появляются трудности с речью;
- снижается подвижность мышц лица;
- меняется осанка;
- возникают проблемы с потоотделением;
Большинство пациентов на второй стадией болезни всё ещё могут самостоятельно выполнять повседневные задачи, хотя это занимает больше времени. Лечение на данном этапе включает процедуры физиотерапии, специальную диету и приём лекарственных препаратов, которые помогают замедлить развитие болезни и облегчить симптомы.
4
Что происходит на третьей стадии?
На данном этапе развития заболевания пациент уже нетрудоспособен. Ему требуется помощь в выполнении многих простых действий, таких как одевание и приём пищи. Человеку всё сложнее координировать движения и удерживать равновесие, поэтому пациенты часто получают травмы при падении.
Из симптомов выделяют те же, что и на второй стадии, а также:
- ещё большее снижение подвижности суставов;
- передвижение мелкими шагами;
- сильное замедление речи, повторение слов;
- постоянные подёргивания головой.
К уже указанным методам лечения на данном этапе подключается трудотерапия, чтобы помочь пациенту улучшить качество жизни и выполнять повседневные действия.
5
Что происходит на четвёртой стадии?
Пациенты на данной стадии развития болезни уже не могут обойтись без посторонней помощи. Им требуются ходунки или инвалидное кресло. Все двигательные нарушения заметно усиливаются, но к ним добавляются также недвигательные симптомы, такие как:
Все двигательные нарушения заметно усиливаются, но к ним добавляются также недвигательные симптомы, такие как:
- проблемы с вниманием;
- проблемы с памятью, деменция;
- тревожность, апатия и раздражительность;
- развитие депрессии.
В этот период необходимо, чтобы рядом с больным постоянно находился кто-то из близких, чтобы уберечь от травм и морально поддержать.
6
Что происходит на пятой стадии?
Основной признак — серьёзная обездвиженность. Пациент не способен ходить и стоять, прикован к постели. Ему необходима инвалидная коляска и круглосуточная помощь.
Характерные симптомы 5 стадии болезни Паркинсона:
- потеря когнитивных способностей;
- неразборчивая речь;
- проблемы с дефекацией и мочеиспусканием;
- неспособность принимать пищу из-за тремора и нарушения глотательной функции — пациентов кормят с помощью специальной ложки или зонда;
До 30% людей на пятой стадии заболевания страдают от спутанности сознания, галлюцинаций и бредовых идей. Деменция поражает до 75% больных. Кроме того, побочные эффекты от лекарств на данном этапе могут перевешивать пользу от них.
Деменция поражает до 75% больных. Кроме того, побочные эффекты от лекарств на данном этапе могут перевешивать пользу от них.
7
Какие ещё выделяют особенности течения болезни?
Несмотря на универсальность классификации по Хен-Яру, развитие болезни Паркинсона индивидуально для каждого пациента.
- У кого-то определённая стадия может длиться несколько месяцев, у других — несколько лет.
- Симптомы могут иметь разную степень тяжести в зависимости от программы физиотерапии, назначенных препаратов, диеты и индивидуальных особенностей организма.
- Иногда наблюдаются резкие переходы между стадиями. Например, первая сменяется третьей, а третья — пятой.
- В некоторых случаях больному может стать лучше, и он вернётся к предыдущей стадии заболевания.
Источники: Stages of Parkinson’s, The 5 Stages of Parkinson’s Disease, The 5 Stages of Parkinson’s
Особенности клинического течения болезни Паркинсона при отложении железа в базальных ганглиях | Буряк А.
 Б., Труфанов А.Г.Введение
Б., Труфанов А.Г.ВведениеБолезнь Паркинсона (БП) — хроническое прогрессирующее заболевание нервной системы, сопровождающееся развитием ряда двигательных нарушений, таких как гипокинезия, мышечная ригидность и тремор, а также группы немоторных симптомов [1]. До сих пор как один из ведущих патофизиологических процессов при БП рассматривается патологическое накопление альфа-синуклеина и формирование телец Леви в черной субстанции (ЧС) и других отделах головного мозга (ГМ). Многообразие современных методов исследования позволяет изучить вклад в нейродегенеративный процесс других механизмов, таких как феномен эксайтотоксичности, избыточное отложение железа и окислительный стресс [2–4].
В 2012 г. группой американских ученых был описан новый тип регулируемой клеточной гибели с участием железа, который получил название ферроптоз [5]. Особенностями данного процесса являются истощение внутриклеточного глутатиона и уменьшение активности фермента глутатионпероксидазы-4, с последующим развитием перекисного окисления липидов, обусловленного снижением антиоксидантной защиты клеток и накоплением активных форм кислорода.
Ряд современных исследований [4, 7, 8] рассматривают повышенное депонирование железа и ферроптоз как один из механизмов, приводящих к нейродегенерации при БП. В то же время важным вопросом остается выбор методики оценки распределения металла в ГМ, и в частности в структурах экстрапирамидной системы. Возм ожность неинвазивно in vivo изучать характер отложения железа предоставляет магнитно-резонансная томография (МРТ) в режиме изображений, взвешенных по магнитной восприимчивости (susceptibility weighted imaging — SWI), которая с каждым годом все активней применяется у пациентов с БП и другими заболеваниями нервной системы [9, 10]. В то же время для комплексной оценки клинических проявлений заболевания применяются специализированные шкалы, позволяющие с высокой точностью охарактер e8зовать разнообразные симптомы БП и степень их выраженности.
Цель исследования: оценить взаимосвязь отложения железа в структурах экстрапирамидной системы с особенностями клинической картины у пациентов с различными стадиями БП.
Материал и методы
В исследование было включено 92 пациента с диагнозом БП, установленным согласно критериям MDS (International Parkinson and Movement Disorder Society) [11]. В зависимости от стадии заболевания пациенты были разделены на 2 группы. В 1-ю вошли 42 пациента со II стадией по Хен — Яру, средний возраст которых составил 60,4±4,5 года, а продолжительность заболевания — 2,3±1,2 года. При этом у 24 (57,1%) больных данной группы на основании клинических данных была установлена смешанная форма заболевания, а у 18 (42,9%) пациентов — акинетико-ригидная.
Всем пациентам выполнялось клиническое и нейропсихологическое обследование по специализированным шкалам, таким как унифицированная шкала оценки болезни Паркинсона (UPDRS), шкала ходьбы и равновесия (GABS), шкала застываний (FOGQ), краткая шкала оценки психического статуса (MMSE), тест «Батарея лобной дисфункции» (FAB), а также шкала депрессии Бека. Затем всем пациентам проводилась МРТ ГМ на МР-томографе Magnetom Trio A Tim 3,0 Тесла (SIEMENS, Германия) с применением импульсной последовательности SWI. На полученных аксиальных SWI-изображениях выделялись области интереса, такие как: ЧС, красное ядро (КЯ), бледный шар (БШ), головка хвостатого ядра (ХЯ), скорлупа и зубчатое ядро мозжечка. В проекции каждой изучаемой структуры экстрапирамидной системы при помощи программы SPIN (signal processing in NMR) Software (SpinTechMRI, США) вручную измерялся уровень интенсивности сигнала с получением числовых значений.
Статистическая обработка данных проводилась с использованием программного обеспечения Statistica 12 (StatSoft, США). Количественные показатели представлены в виде медианы и нижнего и верхнего квартилей (Me [LQ; UQ]). Для выявления статистически значимых различий применялся непараметрический те ст Манна — Уитни, а для определения корреляционных связей — критерий Спирмена.
Результаты исследованияСравнительный анализ групп пациентов с БП II и III стадий по Хен — Яру продемонстрировал статистически значимые различия по результатам обследования по шкале UPDRS, ее разделам UPDRS II, UPDRS III и UPDRS IV, шкалам нарушений ходьбы FOGQ, GABS, а также тестам для оценки когнитивных функций MMSE и FAB (табл. 1).
У пациентов c III стадией БП были выявлены более высокие баллы по шкале UPDRS и ее разделам, что свидетельствует о большей выраженности клинических симптомов заболевания, как моторных, так и немоторных.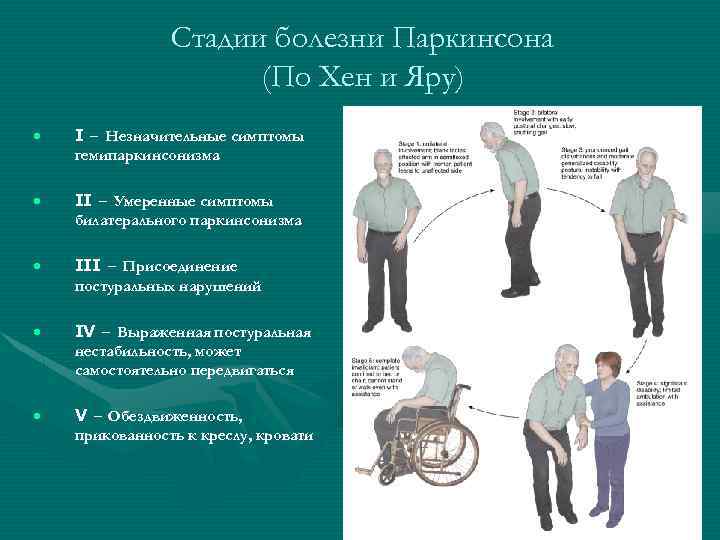
Шкалы GABS и FOGQ позволяют оценить тяжесть нарушений ходьбы, равновесия, а также наличие и выраженность застываний у пациентов с БП. В нашем исследовании обнаружено, что в группе больных с III стадией БП данные расстройства имели заметно более выраженные проявления. Стоит отметить отсутствие застываний у пациентов со II стадией заболевания, что согласуется с общепринятыми представлениями о стадийном прогрессировании клинической симптоматики при БП.
При оценке когнитивных функций исследуемых групп также были выявлены статистически значимые различия. Пациенты с III стадией БП характеризовались более выраженными познавательными расстройствами, в структуру которых входили как нейродинамические, так и регуляторные нарушения. При этом у 13 человек с развернутой стадией заболевания диагностирована деменция, чего не наблюдалось ниодного обследуемого со II стадией по Хен — Яру.
Согласно результатам сравнительного анализа накопления железа в базальных ганглиях у больных исследуемых групп обнаружены статистически значимые различия показателей интенсивности сигнала от таких структур, как правая и левая ЧС, правая и левая скорлупа, левыЦ 9 БШ, а также правое и левое ХЯ (табл.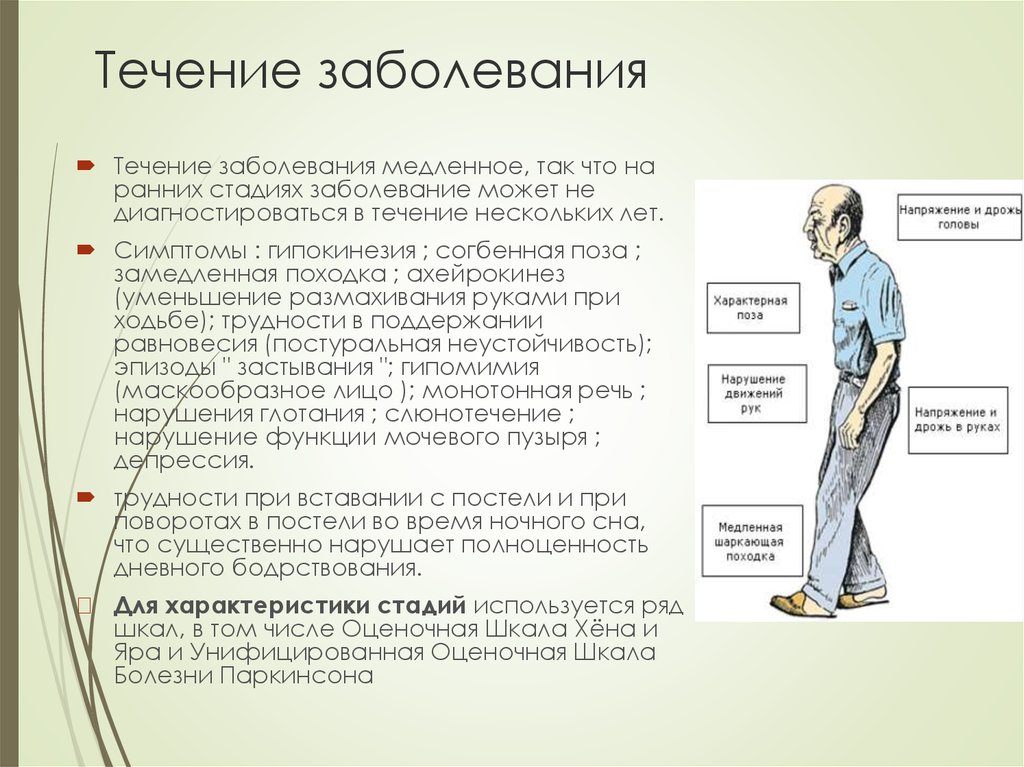 2).
2).
Более низкий сигнал на SWI-изображениях отражает более высокое содержание железа, что свидетельствует о преобладании его депонирования практически во всех структурах экстрапирамидной системы у больных с III стадией БП.
Согласно результатам корреляционного анализа у пациентов со II стадией по Хен — Яру были выявлены множественные взаимосвязи отложения железа в базальных ганглиях с данными обследования по шкале UPDRS и ее разделам (табл. 3).
У пациентов с III стадией по Хен — Яру была обнаружена единственная статистически значимая корреляция (r=-0,57) накопления железа с результатами обследования по разделу UPDRS III (29,00 [28,00; 35,00]), которую продемонстрировал минимальный уровень сигнала от правого БШ (60,00 [26,00; 92,00]).
При анализе корреляционных связей между результатами клинической оценки расстройств ходьбы по шкалам GABS и FOGQ и накоплением железа в структурах экстрапирамидной системы была выявлена единственная связь (r=-0,86) уровня интенсивности сигнала от левого БШ min (90,00 [79,00; 108,00]) и баллов по шкале FOGQ (2,00 [1,00; 2,00]) у пациентов со II стадией по Хен — Яру. В то же время статистически значимых корреляций со шкалой нарушения ходьбы и равновесия у данной группы обследованных обнаружено не было.
В то же время статистически значимых корреляций со шкалой нарушения ходьбы и равновесия у данной группы обследованных обнаружено не было.
У пациентов с III стадией БП единственной структурой, которая продемонстрировала значимую корреляцию с баллами по шкале FOGQ, оказалась левая скорлупа. В то же время оценка по шкале GABS имела множество статистически значимых связей с накоплением железа в базальных ганглиях (табл. 4).
Корреляционный анализ уровня интенсивности сигнала от структур экстрапирамидной системы и результатов оценки когнитивных функций у пациентов со II стадией по Хен — Яру продемонстрировал влияние накопления железа в правом БШ на развитие познавательных расстройств (табл. 5).
У пациентов с III стадией БП нами было выявлено значительное большее влияние избыточного депонирования железа в структурах экстрапирамидной системы на развитие когнитивных нарушений (см. табл. 5).
В проведенном нами исследовании не было установлено статистически значимых корреляционных связей значений интенсивности сигнала от изучаемых областей и результатов обследования по шкале депрессии Бека у пациентов со II стадией БП.
Согласно гипотезе H. Braak et al. [2] отложение альфа-синуклеина при БП носит стадийный характер, последовательно вовлекая в патологический процесс множество различных структур ГМ. В то же время клиническое течение заболевания также характеризуется последовательным прохожд ением через несколько стадий, каждая из которых имеет свои особенности. В нашем исследовании пациенты с III стадией БП характеризовались более тяжелыми моторными и немоторными нарушениями, что нашло отражение в результатах комплексного клинико-нейропсихологического обследования. Кроме того, у данной группы пациентов было обнаружено более высокое
‘f1одержание железа в ЧС, скорлупе, БШ и ХЯ, чем у пациентов со II стадией по Хен — Яру. Исходя из этого, можно сделать предположение, что процесс развития заболевания и эволюция клинической картины сопровождаются накоплением металла в базальных ганглиях и, возможно, являются отчасти и его следствием. Для определения связи депонирования железа в конкретных структурах экстрапирамидной системы с отдельными симптомами и синдромами БП был проведен корреляционный анализ, который продемонстрировал множество статистически значимых связей.
Для определения связи депонирования железа в конкретных структурах экстрапирамидной системы с отдельными симптомами и синдромами БП был проведен корреляционный анализ, который продемонстрировал множество статистически значимых связей.
Так как дегенерация нейронов компактной части ЧС, по современным представлениям, занимает центральное место в теории патогенеза БП, то взаимосвязь накопления железа в данной структуре среднего мозга с тяжестью моторных и некоторых немоторных проявлений заболевания весьма закономерна и может объясняться развитием ферроптоза и окислительного стресса в дофаминпродуцирующих клетках. Уровень интенсив ности сигнала от ЧС продемонстрировал статистически значимые корреляционные связи со шкалой UPDRS, разделами UPDRS II, UPDRS III у пациентов со II стадией БП и шкалами GABS и FAB у обследуемых с III стадией по Хен — Яру. Однако нами были обнаружены взаимосвязи, требующие углубленного анализа в силу своей неочевидности. Например, с накоплением железа в КЯ оказались взаимосвязаны не только клинические проявления БП, оцениваемые по шкале UPDRS и ее разделам у пациентов со II стадией по Хен — Яру, но и когнитивные нарушения у лиц с III стадией заболевания.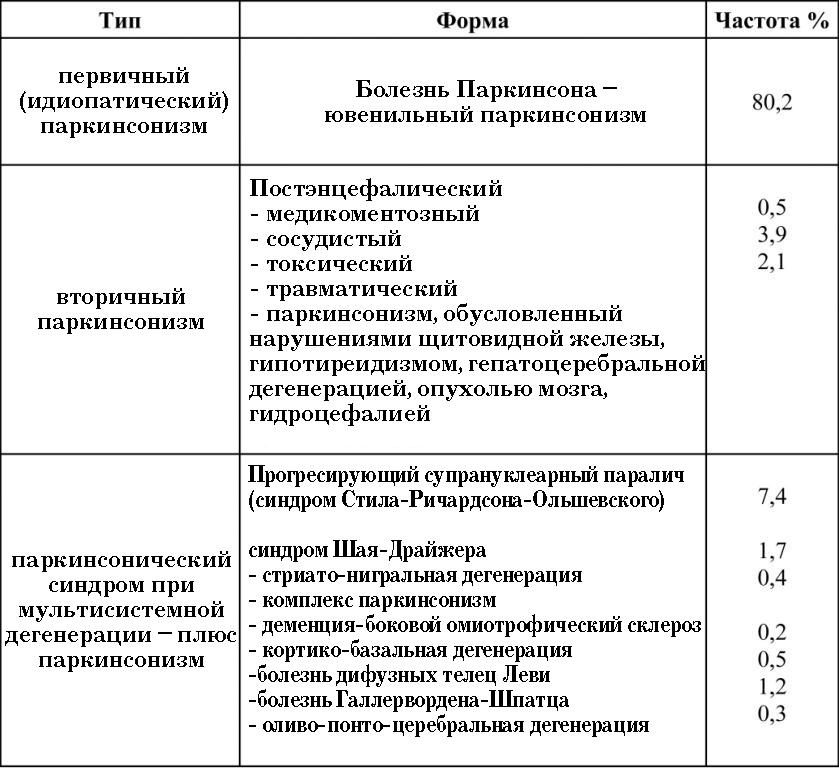 Если представление об участии КЯ в формировании двигательных актов уже является общепринятым, то их возможный вклад в осуществление сенсорных, познавательных и психических функций за счет обширных связей с префронтальной, поясной и инсулярной корой изучается только сегодня [12, 13].
Если представление об участии КЯ в формировании двигательных актов уже является общепринятым, то их возможный вклад в осуществление сенсорных, познавательных и психических функций за счет обширных связей с префронтальной, поясной и инсулярной корой изучается только сегодня [12, 13].
Помимо ЧС с выраженностью нарушений ходьбы и застываниями у пациентов с III стадией БП были связаны отложения железа в скорлупе. Данные структуры экстрапирамидной системы находятся в тесном физиологическом взаимодействии посредством нигростриарного дофаминергического пути, который обеспечивает достижение дофамином дофаминовых рецепторов, экспрессирующихся на поверхности нейронов стриатума [14]. Дегенерация нигростриарного тракта и снижение уровня нейромедиатора лежат в основе патогенеза БП и являются причиной развития двигательных проявлений заболевания. Возможно, именно прогрессирующее накопление железа в ЧС и скорлупе с последующим ферроптозом и гибелью во влеченных нейронов вносит существенный вклад в формирование нарушений ходьбы у пациентов с развернутой клинической картиной БП.
Депрессия является одним из аффективных расстройств, характерных для БП, причем ее развитие может происходить еще во время продромального периода и на много лет опережать дебют двигательных проявлений заболевания [15–17]. В нашем исследовании была обнаружена статистически значимая связь накопления железа в левом ХЯ с результатами обследования по шкале депрессии Бека у пациентов с III стадией по Хен — Яру, что можно объяснить тесными взаимосвязями стриатума с различными отделами ГМ, включая лимбическую систему [18].
Стадии Хена и Яра — Клиническая эффективность и экономическая эффективность физиотерапии и трудотерапии по сравнению с отсутствием терапии при болезни Паркинсона легкой и средней степени тяжести: крупное прагматическое рандомизированное контролируемое исследование (PD REHAB)
NCBI Bookshelf. Служба Национальной медицинской библиотеки, Национальных институтов здоровья.
Clarke CE, Patel S, Ives N, et al.; от имени совместной группы PD REHAB. Клиническая эффективность и экономическая эффективность физиотерапии и трудотерапии по сравнению с отсутствием терапии при болезни Паркинсона легкой и средней степени тяжести: большое прагматическое рандомизированное контролируемое исследование (PD REHAB). Саутгемптон (Великобритания): Библиотека журналов NIHR; 2016 г., август (Оценка технологий здравоохранения, № 20.63.)
Клиническая эффективность и экономическая эффективность физиотерапии и трудотерапии по сравнению с отсутствием терапии при болезни Паркинсона легкой и средней степени тяжести: большое прагматическое рандомизированное контролируемое исследование (PD REHAB). Саутгемптон (Великобритания): Библиотека журналов NIHR; 2016 г., август (Оценка технологий здравоохранения, № 20.63.)
Клиническая эффективность и экономическая эффективность физиотерапии и трудотерапии по сравнению с отсутствием терапии при болезни Паркинсона легкой и средней степени тяжести: большое прагматическое рандомизированное контролируемое исследование (PD REHAB).
Показать подробности
- Содержание
Критерий поиска
Стадия 1.0: Только одностороннее участие.
Стадия 1.5: Одностороннее и осевое поражение.
Стадия 2.0: Двустороннее поражение без нарушения равновесия.
Стадия 2.5: Легкая двусторонняя вовлеченность с восстановлением при тесте на ретропульсию (натяжение).
Стадия 3.0: Легкое или умеренное двустороннее поражение, некоторая постуральная нестабильность, но физически независимый.
Стадия 4.0: Тяжелая инвалидность, способность ходить и стоять без посторонней помощи.
Стадия 5.0: Прикованный к инвалидной коляске или прикованный к постели без посторонней помощи.
Copyright © Queen’s Printer and Controller of HMSO 2016. Эта работа была подготовлена Clarke et al. в соответствии с условиями контракта на ввод в эксплуатацию, выданного министром здравоохранения. Этот выпуск может свободно воспроизводиться в целях частного исследования и изучения, а выдержки (или даже полный отчет) могут быть включены в профессиональные журналы при условии, что будет сделано соответствующее признание и воспроизведение не связано с какой-либо формой рекламы. Заявки на коммерческое воспроизведение следует направлять по адресу: Библиотека журналов NIHR, Национальный институт исследований в области здравоохранения, Координационный центр оценки, испытаний и исследований, Alpha House, Научный парк Университета Саутгемптона, Саутгемптон, SO16 7NS, Великобритания.
Включено в соответствии с условиями некоммерческой государственной лицензии Великобритании.
Идентификатор книжной полки: NBK379751
Содержание
- PubReader
- ПЕЧАТЬ ВИДОВАЯ
- СИДА ЭТА СТРАНИЦА
- PDF Версия этого названия
- 1111111111111111111111111111111111111111111111111111113.
Последние действия
ClearTurn OffTurn On
Ваша активность в Интернете пуста.
Запись активности отключена.
Включить запись
Подробнее…
Прогрессирование болезни Паркинсона по оценке времени перехода между стадиями Хена и Яра
. 2010 30 апреля; 25 (6): 710-6.
doi: 10.1002/mds.22875.
Ин Цзяо Чжао 1 , Хви Лин Ви, Йонг-Хуак Чан, Су Хун Сеа, Винг Лок Ау, Пуай Нгох Лау, Эммануэль Камара Пика, Шу Чуен Ли, Нан Луо, Луи Си Тан
Принадлежности
принадлежность
- 1 Факультет фармации, Национальный университет Сингапура, Республика Сингапур.

- PMID: 20213822
- DOI: 10.1002/мдс.22875
Ин Цзяо Чжао и др. Мов Беспорядок. .
. 2010 30 апреля; 25 (6): 710-6.
doi: 10.1002/mds.22875.
Авторы
Ин Цзяо Чжао 1 , Хви Лин Ви, Йонг-Хуак Чан, Су Хун Сеа, Винг Лок Ау, Пуай Нгох Лау, Эммануэль Камара Пика, Шу Чуен Ли, Нан Луо, Луи Си Тан
принадлежность
- 1 Факультет фармации, Национальный университет Сингапура, Республика Сингапур.

- PMID: 20213822
- DOI: 10.1002/мдс.22875
Абстрактный
Это исследование было проведено для оценки прогрессирования болезни Паркинсона (БП) путем анализа времени, необходимого для перехода от одной стадии Хена и Яра (H&Y) к следующей стадии, и для изучения переменных, которые будут связаны со временем перехода H&Y с использованием большого PD. базу данных, содержащую проспективно собранную информацию. Данные были получены из базы данных двигательных расстройств Национального института неврологии в Сингапуре. Анализ выживаемости Каплана-Мейера (KM) был принят для изучения времени, необходимого для прохождения различных стадий H&Y. Регрессионный анализ Кокса использовался для изучения связи между исходными переменными в начальной точке каждого этапа H&Y и переходом к следующему этапу. Всего 69Было обследовано 5 пациентов (средний возраст: 65,2 года, мужчины: 57,3%). Используя анализ КМ, среднее время, необходимое для перехода от стадии H&Y 1 к стадии 2, от 2 к стадии 2,5, от 2,5 к стадии 3, составило 20, 62 и 25 месяцев соответственно; тогда как среднее время, необходимое для перехода от стадии 3 к стадии 4 и от стадии 4 к 5, составляло 24 и 26 месяцев соответственно. Регрессионный анализ Кокса показал, что более старший возраст при постановке диагноза, более длительная продолжительность БП и более высокие двигательные показатели по унифицированной шкале оценки болезни Паркинсона (UPDRS) на исходном уровне были связаны со значительно более быстрым прогрессированием через различные стадии H&Y. Пол и этническая принадлежность не были связаны с прогрессированием заболевания. В заключение, время перехода H&Y является полезной мерой прогрессирования заболевания при БП и может использоваться в клинических исследованиях, оценивающих терапевтические вмешательства и прогностические факторы при БП.
Всего 69Было обследовано 5 пациентов (средний возраст: 65,2 года, мужчины: 57,3%). Используя анализ КМ, среднее время, необходимое для перехода от стадии H&Y 1 к стадии 2, от 2 к стадии 2,5, от 2,5 к стадии 3, составило 20, 62 и 25 месяцев соответственно; тогда как среднее время, необходимое для перехода от стадии 3 к стадии 4 и от стадии 4 к 5, составляло 24 и 26 месяцев соответственно. Регрессионный анализ Кокса показал, что более старший возраст при постановке диагноза, более длительная продолжительность БП и более высокие двигательные показатели по унифицированной шкале оценки болезни Паркинсона (UPDRS) на исходном уровне были связаны со значительно более быстрым прогрессированием через различные стадии H&Y. Пол и этническая принадлежность не были связаны с прогрессированием заболевания. В заключение, время перехода H&Y является полезной мерой прогрессирования заболевания при БП и может использоваться в клинических исследованиях, оценивающих терапевтические вмешательства и прогностические факторы при БП.
2010 Общество двигательных расстройств
Похожие статьи
Использование селегилина связано с более медленным прогрессированием болезни Паркинсона на ранних стадиях, что оценивается временем перехода стадии Хена и Яра.
Чжао Ю.Дж., Ви Х.Л., Ау В.Л., Сеах С.Х., Луо Н., Ли С.К., Тан Л.К. Чжао Ю.Дж. и др. Расстройство, связанное с паркинсонизмом. 2011 март; 17(3):194-7. doi: 10.1016/j.parkreldis.2010.11.010. Epub 2010 14 декабря. Расстройство, связанное с паркинсонизмом. 2011. PMID: 21159539
Прогрессирование двигательных нарушений и инвалидности при болезни Паркинсона: популяционное исследование.
Алвес Г., Вентцель-Ларсен Т., Аарсланд Д., Ларсен Д.П. Алвес Г. и соавт. Неврология.
 2005 8 ноября; 65 (9): 1436-41. doi: 10.1212/01.wnl.0000183359.50822.f2.
Неврология. 2005.
PMID: 16275832
2005 8 ноября; 65 (9): 1436-41. doi: 10.1212/01.wnl.0000183359.50822.f2.
Неврология. 2005.
PMID: 16275832Клинически значимое различие по единой шкале оценки болезни Паркинсона.
Шульман Л.М., Грубер-Бальдини А.Л., Андерсон К.Е., Фишман П.С., Райх С.Г., Вайнер В.Дж. Шульман Л.М. и соавт. Арх Нейрол. 2010 Январь; 67 (1): 64-70. doi: 10.1001/archneurol.2009.295. Арх Нейрол. 2010. PMID: 20065131
Совокупная оценка генетического риска предсказывает прогрессирование болезни Паркинсона.
Пильстрём Л., Морсет К.Р., Гримстад Э., Вителли В., Тофт М. Pihlstrøm L, et al. Мов Беспорядок. 2016 апр; 31 (4): 487-90. doi: 10.1002/mds.26505. Epub 2016 8 февраля. Мов Беспорядок. 2016. PMID: 26853697 Обзор.

Естественная история болезни Паркинсона.
Поу В. Поу В. Дж Нейрол. 2006 декабрь; 253 Приложение 7:VII2-6. doi: 10.1007/s00415-006-7002-7. Дж Нейрол. 2006. PMID: 17131223 Обзор.
Посмотреть все похожие статьи
Цитируется
Адаптация и валидация сингальской версии Опросника оральной моторики Radbound (ROMP) для болезни Паркинсона.
Gamage PDMH, Mohideen MS, Galhena P, Weerasinghe N, Kumbukage MP, Herath T, Senanayake S, Sirisena D, Senanayake SJ, Gooneratne IK. Gamage PDMH и др. Энн Индиан Академик Нейрол. 2022 июль-август; 25 (4): 688-691. doi: 10.4103/aian.aian_953_21. Epub 2022 5 мая. Энн Индиан Академик Нейрол. 2022. PMID: 36211170 Бесплатная статья ЧВК.

Экономическая эффективность добавления эксенатида к обычному лечению у пациентов с болезнью Паркинсона с учетом сопутствующих эффектов сахарного диабета.
Chen HC, Wang CY, Chen HH, Liou HH. Чен ХК и др. ПЛОС Один. 11 августа 2022 г .; 17 (8): e0269006. doi: 10.1371/journal.pone.0269006. Электронная коллекция 2022. ПЛОС Один. 2022. PMID: 35951654 Бесплатная статья ЧВК.
Метаболитные изменения в префронтальных долях и передней поясной коре коррелируют со скоростью обработки и исполнительной функцией у пациентов с болезнью Паркинсона.
He C, Rong S, Zhang P, Li R, Li X, Li Y, Wang L, Zhang Y. Он С и др. Quant Imaging Med Surg. 2022 авг; 12 (8): 4226-4238. doi: 10.21037/qims-21-1126. Quant Imaging Med Surg.




 2005 8 ноября; 65 (9): 1436-41. doi: 10.1212/01.wnl.0000183359.50822.f2.
Неврология. 2005.
PMID: 16275832
2005 8 ноября; 65 (9): 1436-41. doi: 10.1212/01.wnl.0000183359.50822.f2.
Неврология. 2005.
PMID: 16275832

