Шкала рэнкина описание: Шкала Рэнкина — описание методики, фотографии, стоимость
Шкала Рэнкина | CardioNeurology.ru
Шкала Рэнкина позволяет оценить степень инвалидизации после инсульта и включает пять степеней инвалидизации после инсульта
| 0 | Нет симптомов |
| 1 | Отсутствие существенных нарушений жизнедеятельности, несмотря на наличие некоторых симптомов: способен выполнять все повседневные обязанности. |
| 2 | Легкое нарушение жизнедеятельности: неспособен выполнять некоторые прежние обязанности, однако справляется с собственными делами без посторонней помощи. |
| 3 | Умеренное нарушение жизнедеятельности: требуется некоторая помощь, однако способен ходить без посторонней помощи. |
| 4 | Выраженное нарушение жизнедеятельности: неспособен ходить без посторонней помощи, неспособен справляться со своими физическими потребностями без посторонней помощи. |
| 5 | Тяжелое нарушение жизнедеятельности: прикован к постели, недержание мочи и кала, требует постоянной помощи и присмотра персонала. |
- Первая степень предполагает отсутствие признаков инвалидности, больной в состоянии выполнять без посторонней помощи все действия по уходу за собой. Однако это не исключает у больного наличия мышечной слабости, расстройств чувствительности, нарушений речи или других неврологических функций. Эти нарушения выражены в незначительной степени и не ведут к ограничению активности.
- Вторая степень инвалидизации по Рэнкину предполагает наличие легких признаков инвалидности, но больной в состоянии ухаживать за собой без посторонней помощи. Например, не может вернуться к прежней работе, но способен обслуживать себя без постороннего присмотра.
- Третья степень умеренно выраженные признаки инвалидности, больной нуждается в некоторой посторонней помощи при одевании, гигиеническом уходе за собой; больной не в состоянии внятно читать или свободно общаться с окружающими.
 Больной может пользоваться ортопедическими приспособлениями или тростью.
Больной может пользоваться ортопедическими приспособлениями или тростью. - Четвертая степень предполагает наличие выраженных признаков инвалидности. Больной не в состоянии ходить и ухаживать за собой без посторонней помощи, он нуждается в круглосуточном присмотре и в ежедневной посторонней помощи. При этом он в состоянии самостоятельно или при минимальной помощи со стороны выполнять какую-то часть мероприятий по уходу за собой.
- Пятая степень сильно выраженные признаки инвалидности. Больной прикован к постели, неопрятен и нуждается в постоянном уходе и наблюдении.
Вконтакте
Одноклассники
Вебинар «Шкалы для оценки состояния пациентов с острым инсультом (NIHSS, Рэнкин, Ривермид). Тромболитическая терапия при ишемическом инсульте»
Время начала: 15:00
Место проведения: Платформа Вебинар ру
Адрес проведения: https://events.webinar.ru/integriti/6127087
Инициатор: Шамалов Николай Анатольевич
Специализация: неврология
Краткое описание: Знакомство слушателей с методологией оценки тяжести состояния пациентов с инсультом по шкалам NIHHS, Рэнкин и Ривермид и результатами современных исследований по проблеме реперфузионной терапии при ишемическом инсульте.
Описание: Программа семинара включает образовательные видеоролики и интерактивные презентации с обсуждением клинических случаев оценки тяжести состояния пациентов с инсультом. В рамках теоретической части участникам также будут прочитаны лекции о реперфузионной терапии больных с ишемическим инсультом и порядке оказания помощи больным с данной патологией.
Контактное лицо: Шамалов Николай Анатольевич +7 (499) 936-99-37 [email protected]
Планируемое количество участников: 30
Цель и ожидаемый результат: Образовательная цель вебинара — ознакомление врачей с современными подходами к обследованию, тромболитической терапии, консервативному и хирургическому лечению, подходам к реабилитации пациентов после инсультов. Программа весьма актуальна, сформирована с учетом потребностей врачей, а также по данным Пилотного проекта «Развитие системы медицинской реабилитации в Российской Федерации» (Иванова Г.И., 2015). Ожидаемые образовательные результаты: Совершенствование компетенций врачей неврологов, анестезиологов-реаниматологов, нейрохирургов, специалистов по функциональной диагностике и врачей скорой помощи — по актуальным вопросам, связанным с инсультами: диагностике, терапии, реабилитации и профилактике, отработка междисциплинарного и комплексного подхода к консервативному и хирургическому лечению, реабилитации и профилактике инсультов.
Описание и использование шкалы Рэнкина
Первая версия шкалы Рэнкина появилась в 80-х годах. Ее основным предназначением была правильная оценка состояния больного после перенесенного инсульта. Шкала Рэнкина также помогала в выборе соответствующих мер по восстановлению организма человека. Данная методика и сейчас широко используется врачами, занимающимися реабилитацией пациентов, пострадавших от нарушений мозгового кровообращения.
В дальнейшем была выпущена модифицированная шкала Рэнкина. Она не только отражает степень функциональных нарушений, но и позволяет объективно оценить результативность реабилитационных мероприятий. Также с ее помощью можно выявить необходимость применения различных дополнительных приспособлений для инвалидов.
Описание шкалы Рэнкина
Метод базируется на проведении изучения картинки Нихс, анализа Ривермид. Диагностика в каждой клинике индивидуальна. По шкале Рэнкина специалистом определяется дальнейшая жизнедеятельность и уровень инвалидности человека, перенесшего инсульт. На основе полученных исследований проводится тромболитическая терапия.
При помощи шкалы диагностируют:
- качество речевой деятельности;
- изменения в функционировании опорно-двигательной системы;
- уровень осознанности;
- чувствительность;
- возможность контролировать движения тела.
Шкала определяет степень тяжести состояния пациента. Таблица оценки уровня здоровья состоит из шести пунктов. В каждом дается подробная характеристика состояния больного с нарушениями мозгового кровообращения.
Высокая оценка уровня здоровья по Рэнкину
Первые два пункта описывают практически не пострадавшего от патологии, сохранившего дееспособность пациента, не нуждающегося в реабилитации:
- Нулевой.
 Дееспособность не нарушена. Проблемы, возникающие после инсульта, отсутствуют, ограничений нет.
Дееспособность не нарушена. Проблемы, возникающие после инсульта, отсутствуют, ограничений нет. - Первый. Наблюдаются небольшие изменения речи, письма и быстроты чтения. Бывают расстройства в эмоциональном плане. Человек ведет привычный самостоятельный образ жизни, но не может выполнять действия, связанные с мелкой моторикой и усиленным вниманием.
Низкая оценка уровня здоровья
В остальных пунктах описывается состояние пациента, частично или полностью потерявшего дееспособность и нуждающегося в посторонней помощи:
- Второй. Пациент частично теряет дееспособность. Возможна жизнь без посторонней поддержки, если не требуется выполнять сложные действия. Ограничения в некоторых видах деятельности: управление транспортом, танцы, бег, физический труд.
- Третий. Инвалидизация средней степени. Человеку нужна помощь со стороны, но передвигается он самостоятельно, возможно с использованием вспомогательных средств. Необходима психологическая и моральная поддержка.
- Четвертый. Среднетяжелый уровень потери двигательных функций. Больному необходима посторонняя поддержка. Уход за собой не осуществляет.
- Пятый. Самое тяжелое состояние пациента, последняя степень инвалидности. Нужен круглосуточный присмотр и уход. Человек пожизненно прикован к постели, происходит неконтролируемое мочеиспускание.
В первоначальной версии шкалы присутствовал шестой уровень — смерть больного. В модифицированной системе его нет.
Польза метода
Главной составляющей врачебной помощи после лечения критического состояния при инсульте является реабилитация. В этот период необходимо максимально избавиться от неврологических отклонений.
Большую роль при восстановлении играют индивидуальные особенности организма человека. Шкала Рэнкина позволяет значительно облегчить работу невролога, составляющего последовательный план реабилитации.
Помимо этого, полученные значения шкалы используются и врачами, занимающимися восстановительными процедурами. Для оценки необходимости самого процесса реабилитации также применяется этот метод. Еще можно выделить то, что шкала Рэнкина выявляет целесообразность использования и разновидность средств для перемещения пациента (коляска, ходунки, трость).
Для оценки необходимости самого процесса реабилитации также применяется этот метод. Еще можно выделить то, что шкала Рэнкина выявляет целесообразность использования и разновидность средств для перемещения пациента (коляска, ходунки, трость).
Шкала температуры. Шкала Цельсия, Фаренгейта, Кельвина, Реомюра
ИсторияСлово «температура» возникло в те времена, когда люди считали, что в более нагретых телах содержится большее количество особого вещества — теплорода, чем в менее нагретых. Поэтому температура воспринималась как крепость смеси вещества тела и теплорода. По этой причине единицы измерения крепости спиртных напитков и температуры называются одинаково — градусами.
Из того, что температура — это кинетическая энергия молекул, ясно, что наиболее естественно измерять её в энергетических единицах (т.е. в системе СИ в джоулях). Однако измерение температуры началось задолго до создания молекулярно-кинетической теории, поэтому практические шкалы измеряют температуру в условных единицах — градусах.
Шкала Кельвина
В термодинамике используется шкала Кельвина, в которой температура отсчитывается от абсолютного нуля (состояние, соответствующее минимальной теоретически возможной внутренней энергии тела), а один кельвин равен 1/273.16 расстояния от абсолютного нуля до тройной точки воды (состояния, при котором лёд, вода и водяной пар находятся в равновесии). Для пересчета кельвинов в энергетические единицы служит постоянная Больцмана. Используются также производные единицы: килокельвин, мегакельвин, милликельвин и т.д.
Шкала Цельсия
В быту используется шкала Цельсия, в которой за 0 принимают точку замерзания воды, а за 100° точку кипения воды при атмосферном давлении. Поскольку температура замерзания и кипения воды недостаточно хорошо определена, в настоящее время шкалу Цельсия определяют через шкалу Кельвина: градус Цельсия равен кельвину, абсолютный ноль принимается за −273,15 °C. Шкала Цельсия практически очень удобна, поскольку вода очень распространена на нашей планете и на ней основана наша жизнь. Ноль Цельсия — особая точка для метеорологии, поскольку замерзание атмосферной воды существенно всё меняет.
Ноль Цельсия — особая точка для метеорологии, поскольку замерзание атмосферной воды существенно всё меняет.
Шкала Фаренгейта
В Англии и, в особенности, в США используется шкала Фаренгейта. В этой шкале на 100 градусов раздёлен интервал от температуры самой холодной зимы в городе, где жил Фаренгейт, до температуры человеческого тела. Ноль градусов Цельсия — это 32 градуса Фаренгейта, а градус Фаренгейта равен 5/9 градуса Цельсия.
В настоящее время принято следующее определение шкалы Фаренгейта: это температурная шкала, 1 градус которой (1 °F) равен 1/180 разности температур кипения воды и таяния льда при атмосферном давлении, а точка таяния льда имеет температуру +32 °F. Температура по шкале Фаренгейта связана с температурой по шкале Цельсия (t °С) соотношением t °С = 5/9 (t °F — 32), то есть изменение температуры на 1 °F соответствует изменению на 5/9 °С. Предложена Г. Фаренгейтом в 1724.
Шкала Реомюра
Предложенна в 1730 году Р. А. Реомюром, который описал изобретённый им спиртовой термометр.
Единица — градус Реомюра (°R), 1 °R равен 1/80 части температурного интервала между опорными точками — температурой таяния льда (0 °R) и кипения воды (80 °R)
1 °R = 1,25 °C.
В настоящее время шкала вышла из употребления, дольше всего она сохранялась во Франции, на родине автора.
|
Пересчёт температуры между основными шкалами |
|||
|
|
Кельвин |
Цельсий |
Фаренгейт |
|
Кельвин (K) |
= K |
= С + 273,15 |
= (F + 459,67) / 1,8 |
|
Цельсий (°C) |
= K − 273,15 |
= C |
= (F − 32) / 1,8 |
|
Фаренгейт (°F) |
= K · 1,8 − 459,67 |
= C · 1,8 + 32 |
= F |
Сравнение температурных шкал
|
Описание |
Кельвин | Цельсий |
Фаренгейт |
Ньютон | Реомюр |
|
Абсолютный ноль |
0 |
−273. |
−459.67 |
−90.14 |
−218.52 |
|
Температура таяния смеси Фаренгейта (соли и льда в равных количествах) |
255.37 |
−17.78 |
0 |
−5.87 |
−14.22 |
| Температура замерзания воды (нормальные условия) |
273.15 |
0 |
32 |
0 |
0 |
|
Средняя температура человеческого тела¹ |
310.0 |
36.8 |
98.2 |
12.21 |
29.6 |
|
Температура кипения воды (нормальные условия) |
373.15 |
100 |
212 |
33 |
80 |
| Температура поверхности Солнца |
5800 |
5526 |
9980 |
1823 |
4421 |
¹ Нормальная температура человеческого тела — 36.6 °C ±0.7 °C, или 98.2 °F ±1.3 °F. Приводимое обычно значение 98.6 °F — это точное преобразование в шкалу Фаренгейта принятого в Германии в XIX веке значения 37 °C. Поскольку это значение не входит в диапазон нормальной температуры по современным представлениям, можно говорить, что оно содержит избыточную (неверную) точность.
Сопоставление шкал Фаренгейта и Цельсия
(oF — шкала Фаренгейта, oC — шкала Цельсия)
|
oF |
oC |
|
oF |
oC |
|
oF |
oC |
|
oF |
oC |
|
-459.67 |
-273.15 |
|
-60 |
-51.1 |
|
-4 |
-20.0 |
|
20 |
-6.7 |
Для перевода градусов цельсия в кельвины необходимо пользоваться формулой T=t+T0 где T- температура в кельвинах, t- температура в градусах цельсия, T0=273.15 кельвина. По размеру градус Цельсия равен Кельвину.
Шкала Ренкина — Энциклопедия по машиностроению XXL
Шкала Ренкина — температурная шкала, в которой размер градуса равен градусу Фаренгейта, но отсчет ведется от абсолютного нуля температуры. [c.92]По шкале Ренкина О °F равен 459,67 °Ra, точка таяния льда 491,67 °Ra и точка кипения воды 671,67 °Ra. [c.93]
Шкала Ренкина сохраняется в США и в некоторых странах, где принято измерение температуры в градусах Фаренгейта. [c.93]
Помимо шкал Кельвина и Цельсия в некоторых странах используют шкалы Ренкина, Фаренгейта и Реомюра. Между единицами температуры по этим шкалам и кельвином справедливы соотношения
[c.172]
Между единицами температуры по этим шкалам и кельвином справедливы соотношения
[c.172]
Шкала Ренкина имеет такую же цену деления шкалы (1 °К), что и шкала Фаренгейта (1 °Р), только начало отсчета выбрано при абсолютном нуле температур. Поэтому 7 =7 °Р/1,8, где Т — температура, К. [c.79]
Температуру в идеально-газовой шкале можно отсчитывать яе только в градусах Цельсия или Кельвина, но и в других единицах свойства шкалы не изменяются от цены деления шкалы. В отдельных странах находят применение шкалы Фаренгейта (°Ф), Рен-кина (°Ra) н Реомюра ( R), уже упоминавшиеся ранее в 1-1 эти шкалы различаются только выбором вида функций. Переход от одной шкалы к другой производится обычным математическим пересчетом. В отличие от шкалы Цельсия у шкал Фаренгейта и Реомюра интервал от точки таяния льда до точки кипения воды делится не на 100 частей, а соответственно на 180 и 80 частей. Кроме того, точка таяния льда по шкале Фаренгейта соответствует температуре 32° Ф. Шкала Ренкина является абсолютной шкалой, подобной шкале Кельвина значения температуры по шкале Ренкина равны 9/5 значений температуры по шкале Кельвина. Таким образом, основной температурный интервал по шкале Ренкина, так же как и но шкале Фаренгейта, делится на 180 частей. Соотношения для пересчета значений температуры по шкале Фаренгейта, Ренкина п Реомюра в значения по шкале Цельсия и обратно были приведены в табл. 1-1. [c.74]
Градус по температурной шкале Ренкина (термоди- [c.493]
В США употребляется абсолютная шкала Ренкина , в которой за нуль принята температура абсолютного нуля, а цена деления такая же, как и цена деления шкалы Фаренгейта. [c.9]
Какова температура по абсолютной шкале Ренкина, если в градусах Цельсия она равна 520 °С [c.9]
Градус Ренкина — см. температурные шкалы.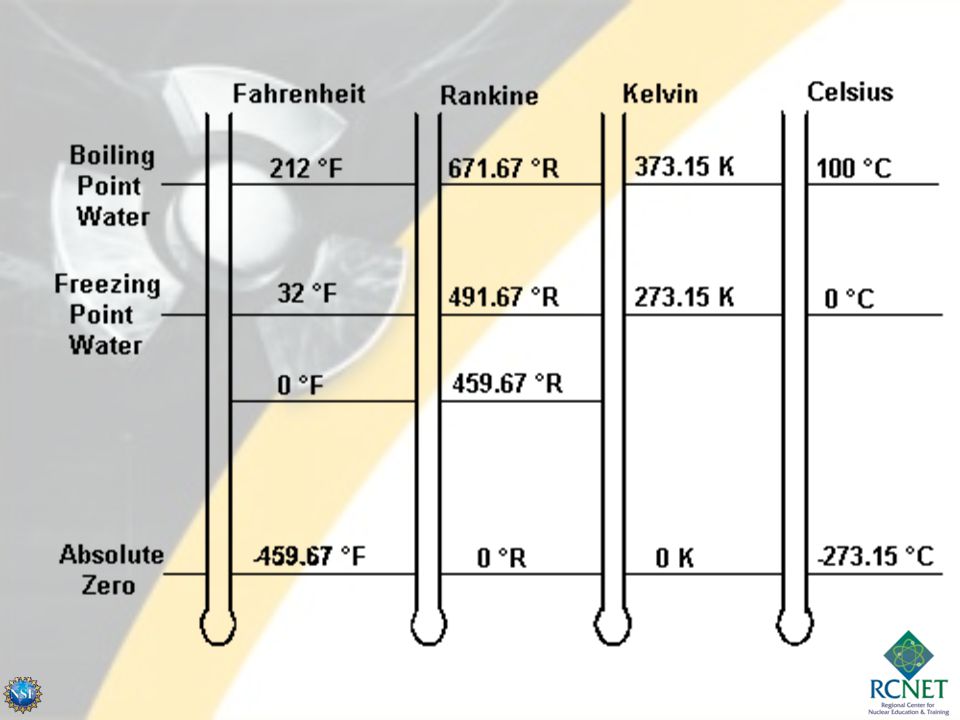 Шкала Ренкина.
[c.253]
Шкала Ренкина.
[c.253]
Шкала Ренкина, в сущности, является той же самой шкалой температуры по ней равны /5 значения температуры по шкале Кельвина. [c.24]
В Англии, США и некоторых других странах применяют шкалу Фаренгейта (°Р) с двумя реперными точками — температурой таяния льда при давлении 760 л л рт. ст. (32° Р) и кипения воды при давлении 760 мм рт. ст. (212° Р) абсолютную термодинамическую шкалу Ренкина (°Ва) с нижней границей — точкой абсолютного нуля (0° На), соответствующей —459,67° Р, и точкой таяния льда (491,67° Ка), соответствующей 32° Р, [c.133]
Шкала Ренкина (°К) имеет началом отсчета абсолютный нуль температур, а цена ее деления одинакова со шкалой Фаренгейта, поэтому Т°К==1,8Т. [c.22]
Шкалу Фаренгейта, отсчитанную от абсолютного нуля, называют шкалой Ренкина (°К). В этой шкале точка плавления льда составляет 491,67° К, а точка кипения воды 671,67° К. [c.7]
В настоящее время применяются различные температурные шкалы Цельсия, Фаренгейта, Реомюра, Ренкина. Наиболее употребительной является температурная шкала Цельсия, в которой интервал температур от точки плавления льда до точки кипения воды при атмосферном давлении разбит на сто равных частей, называемых градусами 1( X2). [c.8]
Помимо температурных шкал Кельвина (Т) и Цельсия (t), вошедших в Международную систему (СИ), были широко распространены также температурные шкалы Реомюра (Tr), Фаренгейта (Тр) и Ренкина (Тка). Приведение этих внесистемных температур к шкалам Кельвина и Цельсия производится по формулам t = T-273,15 [c.217]
В ряде стран используют температурные шкалы Фаренгейта и Ренкина. Пересчет температуры, заданной в градусах Фаренгейта С Р), в [c.22]
Британская тепловая единица (Бте) = 0,25198 ккал= 1,05506 10 дж Формулы перехода от температур в шкалах Фаренгейта (г . ) и Ренкина (/р) к температурам в шкале Цельсия (/ ) и в абсолютной шкале Кельвина ( р -)
[c.12]
) и Ренкина (/р) к температурам в шкале Цельсия (/ ) и в абсолютной шкале Кельвина ( р -)
[c.12]
F/9 = (Т — 491,67)° Rank/9, где Г, К — абс. термодинамическая тем-ра Кельвина t, С — тем-ра, выраженная в градусах Цельсия i, ° F — тем-ра по шкале Фаренгейта t, °R — тем-ра по шкале Реомюра Г, ° Rank — тем-ра по шкале Ренкина (Ранкина) — см. табл. 1.10. [c.345]
Шкала Ренкина. Температурная шкала, в которой размер градуса равен градусу Фарангейта, но отсчет ведется от абсолютного нуля температуры, называется шкалой Ренкина. Она сохраняется в США и в некоторых странах, где принято измерение температуры в градусах Фаренгейта. [c.118]
Обе шкалы — термодинамическая и МПТШ-68 могут градуироваться и в кельвинах, и в градусах Цельсия. Для. ШТТШ-68 температура тройной точки воды принята равной точно по определению 273,16 К или 0,01 °С температура таяния льда равна 273,15 К или о °С (реально воспроизводится с погрешностью примерно 10 К). Находит применение также выражение температуры в градусах Фаренгейта (°Р) и градусах Ренкина (°Р), которые равны (1°Р = = 1°Р). Соотношения между различными единицами измерения температуры даются формулами [c.89]
Термический к. п. д. цикла Ренкина удобно определять, пользуясь диаграммой s — t (рис. 10-18). На пересечении изобары pi и изотермы ti находят точку 7, соответствующую состоянию пара перед входом в турбину. Энтальпию I l пара, состояние которого отображается этой точкой, определяют по шкале на оси ординат. Затем из точки 1 проводят вертикальную прямую — адиабату до ее пересечения в точке 2 с изобарой / 2 и находят энтальпию /г пара, состояние которого отображается точкой 2. Энтальпию конденсата i k определяют по таблице или по диаграмме s—i, учитывая, однако, что в ней i выражается в кдж1кг, а не в ккал/кг. [c.119]
Каждый прибор, используемый для измерения температуры, должен быть отградуирован (оттарирован) в соответствии с твердо установленной телшературной шкалой. В настоящее время применяются различные температурные шкалы — Цельсия, Фаренгейта, Реомюра, Ренкина, соотно-
[c.6]
В настоящее время применяются различные температурные шкалы — Цельсия, Фаренгейта, Реомюра, Ренкина, соотно-
[c.6]
Температуру измеряют различными приборами жидкостными и газовыми термометрами, термоэлектрическими пирометрами (термопарами), оптическими пирометрами, в которых используется зависимость излучения тела от температуры и длины волны, и т. д. В практике измерения температуры распространение получили различные температурные шкалы—Иельсия, Фаренгейта, Реомюра, Ренкина. Наиболее употребительной является температурная шкала Цельсия, в которой интервал температур от точки плавления льда до точки кипения воды при атмосферном давлении разбит на сто равных частей, называемых градусами (°С). [c.10]
В зарубежной литературе наряду с выражением температуры в кельвинах (К) и градусах Цельсия (°С) используется иногда градус Фаренгейта (°Р) и градус Ренкина (°Ка). Следует иметь в виду, что раньше градус Фаренгейта был характерен для шкал ртутностеклянных термометров, а в данное время, так же как и градус Цельсия, он обозначает, что температура выражена по МПТШ, но с другим числовым значением. Пересчет числовых значений температуры, выраженной в градусах одной шкалы, в градусы другой производят по следующим формулам [c.61]
Клинические исследование Инсульт: Anti-platelets and statin, альтеплаза, внутриартериальное вмешательство — Реестр клинических исследований
Критерии включения:
Критерии включения: чтобы иметь право на участие в этом исследовании, кандидаты должны соответствовать всем следующие критерии отбора на момент обращения в отделение неотложной помощи:
1. Возраст: 18-80 лет
2. Ишемический инсульт (время начала неизвестно, но прошло менее 24 часов с момента последнего посещения). нормальный)
3. Шкала инсульта Национального института здоровья (NIHSS) 8–22
4. Признаки полутени при компьютерной томографии перфузии (ВКТ), как указано выше.
5. Оценка ранней компьютерной томографии (КТ) программы инсульта Альберты (ASPECTS 7 или выше)
6. Подписанное информированное согласие
Критерий исключения:
Критерии исключения: Потенциальные пациенты будут исключены из исследования, если следующие критерии исключения существуют на момент проверки:
1. Признаки внутричерепного кровоизлияния (внутримозговая гематома, внутрижелудочковая кровоизлияние, субарахноидальное кровоизлияние (САК), эпидуральное кровотечение, острое или хроническое субдуральная гематома (SDH)) на исходной КТ
2. Историческая модифицированная шкала Ренкина (mRS) ≥2
3. Шкала инсульта Национального института здоровья (NIHSS)
4. Положительный тест на беременность у женщин детородного возраста.
5. Внутричерепная или интраспинальная хирургия в течение 3 месяцев.
6. Инсульт или серьезная травма головы в течение 3 месяцев.
7. История внутричерепного кровоизлияния.
8. Неконтролируемая артериальная гипертензия во время лечения (например, систолическое давление> 185 мм рт. Ст. Или> 110 мм рт. Ст. диастолический)
9. Судороги в начале инсульта.
10. Активное внутреннее кровотечение.
11. Внутричерепное новообразование.
12. Артериовенозная мальформация или аневризма.
13. Клинические проявления перикардита после перенесенного ИМ.
14. Известный кровоточащий диатез, включая, но не ограничиваясь, текущее использование пероральных антикоагулянты с международным нормализованным отношением (INR)> 1,7
15. Международное нормализованное отношение (INR)> 1,7
16. Введение гепарина в течение 48 часов до начала инсульта с повышенное активированное частичное тромбопластиновое время (АЧТВ) при поступлении
17. Количество тромбоцитов
18. Крупная операция в течение 2 недель.
19. Желудочно-кишечное (ЖКТ) или мочевыводящее кровотечение в течение 3 недель.
20. Для снижения артериального давления требуется агрессивное лечение.
21. Уровень глюкозы 400 мг / дл
Уровень глюкозы 400 мг / дл
22. Артериальная пункция в несжимаемом месте или люмбальная пункция в течение 1 недели.
ВЕДУЩИЕ ФАКТОРЫ РИСКА ИНСУЛЬТА И ИХ КОНТРОЛЬ У ПАЦИЕНТОВ МАЛОГО ГОРОДСКОГО ПОСЕЛЕНИЯ МОСКОВСКОЙ ОБЛАСТИ | Козяйкин
1. Колчу ИГ, Волченкова ТВ, Исакова ЕВ, Котов СВ. Влияние предшествующей антигипертензивной терапии на течение церебрального инсульта. Бюллетень сибирской медицины. 2010;(4):145–7. Kolchu IG, Volchenkova TV, Isakova EV, Kotov SV. Vliyanie predshestvuyushchey antigipertenzivnoy terapii na techenie tserebral’nogo insul’ta [Influence of the previous antihypertensive therapy on the course of cerebral stroke]. Bulletin of Siberian Medicine. 2010;(4):145–7 (in Russian).
2. Колчу ИГ, Романова МВ, Козяйкин ВВ, Котов СВ, Исакова ЕВ. Влияние приверженности к антигипертензивной терапии на течение и исход церебрального инсульта.
3. Клиническая геронтология. 2013;(5–6):22–7. Kolchu IG, Romanova MV, Kozyaykin VV, Kotov SV, Isakova EV. Vliyanie priverzhennosti k antigipertenzivnoy terapii na techenie i iskhod tserebral’nogo insul’ta [Influence of adherence to antihypertensive therapy on the course and outcome of ischemic stroke]. Klinicheskaya gerontologiya. 2013;(5–6):22–7 (in Russian).
4. Котов СВ, Исакова ЕВ, Верещагина ЕВ. Приверженность к антигипертензивной терапии у лиц из группы риска инсульта. Лечение и профилактика. 2012;(2):27–30. Kotov SV, Isakova EV, Vereshchagina EV. Priverzhennost’ k antigipertenzivnoy terapii u lits iz gruppy riska insul’ta [The compliance to antihypertension therapy in patients from the stroke risk group]. Disease treatment and prevention. 2012;(2):27–30 (in Russian).
5. Стаховская ЛВ, Котова СВ, ред. Инсульт. Руководство для врачей. М.: МИА; 2014. 400 с. Stakhovskaya LV, Kotov SV, editors. Insul’t: rukovodstvo dlya vrachey [Stroke: Manual for doctors]. Moscow: MIA; 2014. 400 p. (in Russian).
Стаховская ЛВ, Котова СВ, ред. Инсульт. Руководство для врачей. М.: МИА; 2014. 400 с. Stakhovskaya LV, Kotov SV, editors. Insul’t: rukovodstvo dlya vrachey [Stroke: Manual for doctors]. Moscow: MIA; 2014. 400 p. (in Russian).
6. Гудкова ВВ, Стаховская ЛВ, Шанина ТВ, Мешкова КС, Шеховцова КВ. Антитромботическая терапия во вторичной профилактике ишемического инсульта: вопросы стратегии и тактики. Журнал неврологии и психиатрии им. C.C. Корсакова. 2011;(11):87–94. Gudkova VV, Stakhovskaya LV, Shanina TV, Meshkova KS, Shekhovtsova KV. Antitromboticheskaya terapiya vo vtorichnoy profilaktike ishemicheskogo insul’ta: voprosy strategii i taktiki [The antithrombotic treatment in the secondary prevention of ischemic stroke: strategy and tactic issues]. Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2011;(11):87–94 (in Russian).
7. Paciaroni M, Bogousslavsky J. Primary and secondary prevention of ischemic stroke. Eur
8. Neurol. 2010;63(5):267–78.
9. Мисникова ИВ, Древаль АВ, Ковалева ЮА, Исакова ЕВ, Козяйкин ВВ. Риск развития ост- рых нарушений мозгового кровообраще- ния у больных сахарным диабетом второго типа. Проблемы стандартизации в здраво- охранении. 2011;(11–12):35–8.
10. Goldstein LB, Bushnell CD, Adams RJ, Appel LJ, Braun LT, Chaturvedi S, Creager MA, Culebras A, Eckel RH, Hart RG, Hinchey JA, Howard VJ, Jauch EC, Levine SR, Meschia JF, Moore WS, Nixon JV, Pearson TA; American Heart Association Stroke Council; Council on Cardiovascular Nursing; Council on Epidemiology and Prevention; Council for High Blood Pressure Research; Council on Peripheral Vascular Disease, and Interdisciplinary Council on Quality of Care and Outcomes Research./48-1.jpg) Guidelines for the primary prevention of stroke: a guideline for healthcare professionals from the American Heart Association/ American Stroke Association. Stroke. 2011;42(2):517–84.
Guidelines for the primary prevention of stroke: a guideline for healthcare professionals from the American Heart Association/ American Stroke Association. Stroke. 2011;42(2):517–84.
11. Marso SP, Kennedy KF, House JA, McGuire DK. The effect of intensive glucose control on allcause and cardiovascular mortality, myocardial infarction and stroke in persons with type 2 diabetes mellitus: a systematic review and meta-analysis. Diab Vasc Dis Res. 2010;7(2): 119–30. Misnikova IV, Dreval’ AV, Kovaleva YuA, Isakova EV, Kozyaykin VV. Risk razvitiya ostrykh narusheniy mozgovogo krovoobrashcheniya u bol’nykh sakharnym diabetom vtorogo tipa [Risk of acute stroke in patients with diabetes mellitus type II]. Problemy standartizatsii v zdravookhranenii. 2011;(11–12):35–8 (in Russian).
12. Hackam DG, Khan NA, Hemmelgarn BR, Rabkin SW, Touyz RM, Campbell NR, Padwal R, Campbell TS, Lindsay MP, Hill MD, Quinn RR, Mahon JL, Herman RJ, Schiffrin EL, Ruzicka M, Larochelle P, Feldman RD, Lebel M, Poirier L, Arnold JM, Moe GW, Howlett JG, Trudeau L, Bacon SL, Petrella RJ, Milot A, Stone JA, Drouin D, Boulanger JM, Sharma M, Hamet P, Fodor G, Dresser GK, Carruthers SG, Pylypchuk G, Burgess ED, Burns KD, Vallee M, Prasad GV, Gilbert RE, Leiter LA, Jones C, Ogilvie RI, Woo V, McFarlane PA, Hegele RA, Tobe SW; Canadian Hypertension Education Program. The 2010 Canadian Hypertension Education Program recommendations for the management of hypertension: part 2 – therapy. Can J Cardiol. 2010;26(5):249–58.
Шкала Рэнкина— обзор
Шкалы для оценки исходов (глобальных или гандикапных) после инсульта
Доступны несколько шкал для оценки глобальных (гандикапных) результатов после инсульта. Эти шкалы относительно короткие и включают несколько четко определенных клинических степеней. Наиболее часто используемые шкалы — это mRS и шкала результатов Глазго (GOS). 5,6,202 Это действенные и действенные способы оценки результатов клинических испытаний и эпидемиологических исследований. 183,203 Шкалы показали высокую степень достоверности, а воспроизводимость внутри эксперта высока. 204
MRS считается лучшей в настоящее время доступной шкалой для оценки результатов после инсульта. 17 Ее следует рассматривать не только как шкалу гандикапа, а скорее как показатель глобального результата. У него есть ограничения. Определения несколько произвольны. Оценка 0 по шкале mRS может быть труднодостижимой, поскольку у пациента не должно быть никаких остаточных симптомов, связанных с инсультом (таблица 21-12). Это строгое определение проблематично, потому что пациент, возможно, полностью выздоровел, но если минимальные проблемы сохраняются, ему необходимо присвоить 1 балл.В результате оценка 1 охватывает широкий спектр пациентов. Как правило, в клинических испытаниях использовалось дихотомическое или трихотомическое деление оценок, при этом оценка 0–1 считалась очень благоприятным исходом, 2–3 — благоприятным и 4–6 — неблагоприятным. В некоторых случаях оценка 2 считается положительной, а в других — отрицательной. Согласие между экспертами в дифференциации смежных баллов, особенно среди пациентов с легким поражением, может быть затруднено. 205 MRS продемонстрировала умеренную межэкспертную надежность, которая улучшается с помощью структурированных интервью. 204 Обучение использованию весов, ведущее к сертификации, также повышает их надежность. 206 Использование централизованного вынесения решений по результатам посредством передачи видеозаписей — еще одна стратегия, повышающая надежность шкал. 16,207,208 Конструктивная валидность mRS демонстрируется его тесной взаимосвязью с другими показателями тяжести инсульта, включая баллы NIHSS и изображения головного мозга. 204 Адамс и др. 126 предложила скорректировать определения благоприятных исходов по mRS исходя из исходной тяжести неврологических нарушений, оцененных по шкале NIHSS.Saver 209 выступал за то, чтобы изменение распределения баллов по шкале mRS использовалось как способ оценки успешности лечения. Последний подход подвергался критике. 210 Mandava et al. 211 обнаружил, что использование дихотомизации конечных точек было более надежным, чем использование стратегии распределения.
GOS был разработан для оценки исходов у пациентов с травмами головы, но теперь он используется для оценки исходов у пациентов с инсультом, в частности с кровотечениями. 202 212 213 Состоит из пяти ступеней с подразделениями в рамках трех высших категорий (Таблица 21-13). Разделение баллов на 2 (умеренная инвалидность) и 3 (тяжелая инвалидность) может быть трудным. Тем не менее, GOS имеет хорошее согласование между экспертами и воспроизводимость результатов внутри эксперта. Использование GOS, по-видимому, лучше всего подходит для пациентов с субарахноидальным кровоизлиянием из-за связи GCS со шкалой WFNS. Спектр оценок по шкале GOS может отражать серьезное диффузное или многоочаговое повреждение головного мозга, которое может возникнуть при субарахноидальном кровоизлиянии.GOS включает степень постоянного вегетативного состояния, которое не очень часто встречается у выживших после ишемического инсульта. Кроме того, GOS не делает различий между пациентами с более легкой степенью поражения. Таким образом, использование GOS снизилось в исследованиях ишемического инсульта, поскольку mRS стала более широко использоваться.
Все общие критерии оценки исходов включают некоторое объединение групп пациентов с широким спектром неврологических последствий; они могут не дать адекватного определения многих тонких или разнообразных, но важных неврологических последствий инсульта.Однако весы относительно просты в использовании, доступны образовательные и сертификационные программы для повышения их достоверности и надежности, и они успешно использовались в многочисленных клинических испытаниях. Весы используются клиницистами и все чаще группами, которые сертифицируют или контролируют качество помощи в медицинских центрах. Врачи, работающие с пациентами с инсультом, знакомы с этими инструментами, и они широко используются. Были предложены другие шкалы результатов, но они широко не используются. 214 Также были оценены детские шкалы исходов инсульта. 215 До тех пор, пока не появятся более совершенные рейтинговые инструменты, следует продолжать использовать mRS или GOS. 17
Средство просмотра отчетов | Общие элементы данных NINDS
Бруно А., Акинвунтан А.Е., Лин С., Клоуз Б., Дэвис К., Бауте В., Ариал Т., Брукс Д., Хесс, округ Колумбия, Свитцер Д.А., Николс Ф.Т. Упрощенная анкета с модифицированной шкалой ранкина: воспроизводимость по телефону и подтверждение качества жизни.Гладить. 2011; 42 (8): 2276-2279.
Бруно А., Шах Н., Лин С., Клоуз Б, Хесс, округ Колумбия, Дэвис К., Бауте В., Свитцер Дж. А., Уоллер Дж. Л., Николс Ф. Т. Улучшение оценки по модифицированной шкале Рэнкина с помощью упрощенной анкеты. Гладить. 2010; 41 (5): 1048-1050.
Cheng B, Forkert ND, Zavglia M, Hilgetag CC, Golsari A, Siemonsen S, Fiehler J, Pedraza S, Puig J, Cho T, Alawneh J, Baron J, Ostergaard L, Gerloff C, Thomalla G. Влияние инсульта Расположение на функциональном выходе, измеряемом по модифицированной шкале Рэнкина.Инсульт; 45 (6): 1695-1702.
Фаррелл Б., Годвин Дж., Ричардс С., Варлоу С. Испытание аспирина в Соединенном Королевстве при транзиторной ишемической атаке (UK-TIA): окончательные результаты. J Neurol Neurosurg Psychiatry. 1991; 54 (12): 1044-1054.
Lansberg M, Schrooten M, Bluhmki E, Thijs VN, Saver JL. Зависящее от времени количество лечения, необходимое для лечения, оценки для лечения тканевым активатором плазминогена при остром инсульте, основанные на сдвигах по всему диапазону модифицированной шкалы Рэнкина.Гладить. 2009; 40 (6): 2079-2084.
Ранкин Дж. Сосудистые нарушения мозгового кровообращения у пациентов старше 60 лет. II. Прогноз. Скотт Мед Дж. 1957; 2 (5): 200-215.
van Swieten JC, Koudstaal PJ, Visser MC, Schouten HJ, van Gijn J. Соглашение между наблюдателями по оценке инвалидности у пациентов с инсультом. Гладить. 1988; 19 (5): 604-607.
Uyttenboogaart M, Stewart RE, Vroomen CAJ, De Keyser J, Luijckx G. Оптимизация пороговых значений индекса Бартеля и модифицированной шкалы ранжирования для определения исходов в испытаниях острого инсульта.Гладить. 2005; 36: 1984-1987.
Wilson JT, Hareendran A, Hendry A, Potter J, Bone I, Muir KW. Надежность модифицированной шкалы Рэнкина для нескольких оценщиков: преимущества структурированного интервью. Гладить. 2005; 36 (4): 777-781.
Определение порогового значения для модифицированного индекса Бартеля и модифицированной шкалы Рэнкина для оценки функциональной независимости и остаточной инвалидности после инсульта
Abstract
Оценка функциональной независимости и остаточной нетрудоспособности очень важна для оценки результатов лечения после инсульта.Модифицированная шкала Рэнкина (mRS) и модифицированный индекс Бартеля (MBI) обычно используются для измерения инвалидности или зависимости в повседневной жизни (ADL) выживших после инсульта. Отсутствие консенсуса в отношении категорий баллов MBI вызвало путаницу в интерпретации исходов инсульта. Целью этого исследования было определение оптимальных соответствующих оценок MBI и модифицированной шкалы Рэнкина (mRS) для категоризации MBI. Корейские версии MBI (K-MBI) и mRS были собраны у 5759 пациентов с инсультом через 3 месяца после начала инсульта.Чувствительность и специфичность рассчитывались по пороговым значениям K-MBI для каждой степени mRS, чтобы получить оптимально соответствующие оценки K-MBI и оценки mRS. Мы также построили кривые чувствительности и специфичности рабочих характеристик приемника (ROC) и определили площадь под кривой (AUC). Пороговые значения K-MBI с наивысшей суммой чувствительности и специфичности составили 100 (чувствительность 0,940; специфичность 0,612), 98 (чувствительность 0,904; специфичность 0,838), 94 (чувствительность 0,885; специфичность 0,937), 78 (чувствительность 0.946; специфичность 0,973) и 55 (чувствительность 937; специфичность 0,986) для оценок mRS 0, 1, 2, 3 и 4 соответственно. Исходя из этого результата, можно получить диапазон отсечки K-MBI для каждой степени mRS. Для степени 0 по шкале mRS пороговая оценка K-MBI составляет 100, что указывает на отсутствие соответствующего диапазона оценок. Для классов mRS 1, 2, 3, 4 и 5 оценка K-MBI составляет от 99 до 98, 97 до 94, 93 до 78, 77 до 55 и ниже 54 соответственно. составил 0,791 для mRS степени 0, 0,919 для mRS степени 1, 0,970 для mRS степени 2, 0.0 для степени 3 mRS и 0,991 для степени 4 mRS. Диапазоны оценки K-MBI для представления оценок mRS были переменными; Оценки mRS 0, 1 и 2 имели узкие диапазоны оценок K-MBI, тогда как оценки mRS 3, 4 и 5 демонстрировали широкие диапазоны оценок K-MBI. Степень mRS, по-видимому, чувствительно дифференцирует легкую остаточную инвалидность выживших после инсульта, тогда как K-MBI предоставляет более конкретную информацию о функциональном статусе выживших после инсульта с умеренными и тяжелыми резидуальными нарушениями.
Образец цитирования: Lee SY, Kim DY, Sohn MK, Lee J, Lee S-G, Shin Y-I, et al.(2020) Определение порогового значения для модифицированного индекса Бартеля и модифицированной шкалы Рэнкина для оценки функциональной независимости и остаточной инвалидности после инсульта. PLoS ONE 15 (1): e0226324. https://doi.org/10.1371/journal.pone.0226324
Редактор: Ona Wu, Массачусетская больница общего профиля, США
Поступила: 3 декабря 2018 г .; Одобрена: 25 ноября 2019 г .; Опубликовано: 29 января 2020 г.
Авторские права: © 2020 Lee et al.Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Исследование KOSCO продолжается, и внутренние правила Корейского центра по контролю и профилактике заболеваний (KCDC) запрещают открывать данные для общественности до тех пор, пока исследование не будет завершено. Данные доступны по запросу для исследователей, соответствующих критериям доступа к конфиденциальным данным.Контактная информация комитета по доступу к данным: Сынчхан Ким, Департамент статистики, Университет Халлим, Чхунчхон, Канвон; Телефон: + 82-10-3749-2622; Электронная почта: [email protected].
Финансирование: Эта работа была поддержана грантом Корейских центров по контролю и профилактике заболеваний (2016E-33003-02; www.cdc.go.kr) и Национальным исследовательским фондом Кореи правительством Кореи (MSIP). (NRF-2017R1A2A1A05000730; www.nrf.re.kr) в YHK. Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Авторы заявили об отсутствии конкурирующих интересов.
Сокращения: ADL, Деятельность в повседневной жизни; MBI, Модифицированный индекс Бартеля; Миссис, Модифицированная шкала Ренкина; К-МБИ, Корейская версия Модифицированного индекса Бартеля; PPV, Положительные прогнозные значения; ЧПС, Отрицательные прогностические значения; РПЦ, Рабочие характеристики приемника; AUC, Площадь под кривой
Введение
Инсульт — основная глобальная причина серьезной длительной инвалидности и функциональной зависимости [1].Таким образом, снижение инвалидности, вызванной инсультом, и повышение независимости выживших после инсульта являются первоочередными задачами постинсультной реабилитации [2]. Повседневная деятельность (ADL) оценивается как мера функциональной независимости и результатов реабилитационного процесса. Хотя существует множество инструментов для измерения инвалидности и зависимости у выживших после инсульта, индекс Бартеля (BI) и модифицированная шкала Рэнкина (mRS) являются наиболее широко используемыми инструментами оценки в клинике и в исследованиях [3].
Первоначальная версия Индекса Бартеля состоит из 10 пунктов, каждый из которых оценивается в три этапа [4]. Значения, присвоенные каждому элементу, основаны на объеме физической помощи, необходимой для выполнения задачи. Модифицированный индекс Бартеля (MBI) с пятиступенчатой системой оценки был разработан Шахом и др. [5] и имеет большую чувствительность и надежность по сравнению с исходной версией. MBI и его переведенные версии на разные языки обеспечивают надежную меру базового ADL для оценки эффективности реабилитации.Поэтому он часто использовался в крупномасштабных исследованиях исходов [6–10]. Несмотря на то, что MBI проверен и используется во всем мире, он имеет ограничения в применении и интерпретации. В то время как MBI предоставляет широкий диапазон оценок для функции ADL, интерпретация результатов ограничивается числовыми изменениями в общей оценке. Неясно, насколько изменение общей оценки клинически значимо. Определение клинически различных степеней ADL у пациентов с инсультом является важным вопросом не только для оценки исходов отдельных пациентов, но и для оценки исходов на уровне популяции.Однако нет единого мнения о том, сколько уровней ADL можно значимо классифицировать в MBI или пороговых значениях для этих уровней в каждой категории.
Для сравнения, оценка mRS представляет собой клиническое измерение глобальной инвалидности с использованием 7-балльной шкалы в диапазоне от 0 (нет симптомов) до 6 (мертвый). В то время как mRS изначально была разработана как шкала инвалидности, теперь она больше считается шкалой инвалидности [11]. mRS и MBI часто рассматриваются как аналогичные измерения, и mRS широко применяется для оценки восстановления после инсульта и в качестве первичной конечной точки в клинических испытаниях [12].Однако между двумя измерениями есть существенная разница. Ключевое отличие состоит в том, что mRS — это глобальная шкала инвалидности, тогда как MBI — это количественное измерение базового ADL. Утверждалось, что mRS состоят из субъективных категорий и трудно детально отразить степень инвалидности. Фактически, инвалидность, измеряемая с помощью mRS, и ADL, измеряемая с помощью MBI, часто выявляла несоответствия в объяснении функционального исхода выживших после инсульта [13]. Таким образом, понимание взаимосвязи между mRS и MBI может помочь клиницистам интерпретировать результаты лечения и планировать клинические испытания с использованием обоих показателей.
Целью этого исследования было определение оптимальных значений отсечки для баллов MBI для дифференциации клинически различных классов в ADL, тем самым выявив соответствие между баллом mRS и баллом MBI и переносимость этих двух измерений при оценке остаточного функционального статуса выживших после инсульта. .
Материалы и методы
Сбор данных
Данные были получены из Корейской когорты пациентов с инсультом по функционированию и реабилитации (KOSCO), когорты пациентов с острым, первым в истории инсультом, которые были госпитализированы в участвующие больницы в 9 различных районах Кореи [14, 15].Исследование KOSCO было разработано как 10-летнее продолжительное наблюдение пациентов с инсультом. Это перспективный многоцентровый проект, который исследует остаточную инвалидность, ограничения активности и долгосрочное качество жизни пациентов, впервые перенесших инсульт. Все подходящие пациенты были набраны с августа 2012 г. по май 2015 г. Пациенты официально участвовали в исследовании после того, как они дали письменное информированное согласие. Если пациент не мог принять решение на основании информированного согласия, оно было получено от законного представителя пациента.Протокол исследования был одобрен Наблюдательным советом медицинского центра Самсунг (номер разрешения 2012-06-016). В исследование KOSCO было включено 7 858 пациентов с первым инсультом (6 254 ишемических и 1 604 геморрагических). Через три месяца после начала инсульта 5 759 пациентов прошли индивидуальную оценку последующего наблюдения.
MBI, разработанный Шахом и др. [5] представляет собой 100-балльную шкалу оценки способности пациента выполнять 10 видов ADL. Каждому действию присваивается числовое значение в соответствии с потребностями пациента в помощи.Более низкие баллы указывают на меньшую независимость, тогда как более высокие баллы указывают на большую независимость. Таким образом, максимальная оценка 100 представляет пациента, полностью независимого в выполнении базового ADL, тогда как самая низкая оценка (0) представляет полностью зависимое состояние. MBI был переведен на корейский язык (K-MBI) 6 корейскими физиотерапевтами, специализирующимися на инсульте. Содержание тестовых заданий было пересмотрено, чтобы отразить корейскую культуру и образ жизни, и его достоверность и надежность были ранее проверены. (9) mRS определяет 6 различных степеней инвалидности и 1 степень смерти [16].Уровень 6 mRS не был включен в этот анализ, поскольку настоящее исследование сосредоточено на взаимосвязи между K-MBI и mRS, а пациенты с инвалидностью 6 степени mRS были недоступны для прохождения оценки K-MBI.
K-MBI и mRS были получены в результате личных бесед оценщика с пациентами. Для поддержания оптимальной валидности и межэкспертной надежности все оценки выполнялись квалифицированными оценщиками, имеющими лицензию профессиональных терапевтов или физиотерапевтов и прошедших стандартную программу обучения, предусмотренную исследованием KOSCO.Стандартизированная программа обучения проводилась в начале и каждые 3 месяца в течение периода обучения. Программа первоначального обучения с однодневным семинаром была проведена трижды перед зачислением. Оценщики прошли стандартизированный экзамен для функциональной оценки, включая онлайн-тесты K-MBI и mRS, чтобы получить разрешение на участие в сборе данных. Программа обучения состояла из однодневного семинара и индивидуального обучения опытным специалистом по оценке в течение одной недели. То же правило применялось и к дополнительным оценщикам, принимавшим участие в сборе данных.
Методы анализа
Все подтверждающие данные доступны в статье. Статистический анализ проводили с использованием программного пакета SPSS 24.0 (SPSS Inc., Чикаго, Иллинойс, США). Поскольку данные не удовлетворяют предположению о нормальном распределении, все применяемые статистические тесты были непараметрическими. Описательная статистика использовалась для изучения распределения оценок K-MBI в соответствии с оценкой mRS. Тест хи-квадрат был проведен для определения значимости доли пола среди оценок по шкале mRS. Тест Краскала-Уоллиса применялся для изучения средней разницы в возрасте и показателей K-MBI для оценок по шкале mRS.Для проверки того, какие пары существенно различаются, использовались тесты Манна-Уитни.
Чувствительность, специфичность, а также положительные и отрицательные прогностические значения (PPV и NPV) оценок K-MBI для каждой степени mRS были рассчитаны во всех возможных точках отсечения. Оценки mRS были разделены на две категории. Например, для расчета соответствующих баллов K-MBI для уровня 1 mRS, mRS 0 или 1 были установлены как «благоприятные исходы», а mRS 2–4 были установлены как «неблагоприятные исходы». Чувствительность относится к доле случаев, которые были выше или равны пороговому значению K-MBI среди благоприятных исходов.Специфичность относится к доле случаев, которые были ниже порогового значения K-MBI среди неблагоприятных исходов. PPV — это доля благоприятных исходов согласно mRS среди случаев выше порогового значения K-MBI. NPV — это доля неблагоприятных исходов среди случаев, которые ниже порогового значения K-MBI. Оптимальная граничная оценка была определена как оценка с наивысшей суммой чувствительности и специфичности [17].
Был проведен анализ рабочих характеристик приемника (ROC) и рассчитана площадь под кривой (AUC) для исследования взаимосвязи между чувствительностью и специфичностью.Кривые ROC отображают чувствительность в зависимости от специфичности 1, что позволяет визуализировать оптимальную пороговую оценку K-MBI для каждой степени mRS. AUC указывает на дискриминационный потенциал показателя отсечки K-MBI в оценке mRS, при этом более высокая AUC отражает лучшую производительность [18]. Для оценки значимости значения AUC был проведен тест перестановки.
Результаты
Характеристика населения
Из 5759 пациентов 3332 (57,9%) были мужчинами. Средний возраст — 64 года.1 год (СО 13,2 года). Средний балл K-MBI составил 65 с межквартильным диапазоном от 55 до 74. На рис. 1 показано распределение частот K-MBI для каждой степени MRS и показаны медиана, межквартильный размах, минимум и максимум оценок K-MBI. Распределение баллов по шкале mRS показано в таблице 1.
Рис. 1. Распределение баллов K-MBI по оценкам mRS. Центральный прямоугольник охватывает с первого по третий квартили.
Сегмент внутри прямоугольника показывает медиану, а усы над и под прямоугольником показывают положения максимума и минимума, соответственно.K-MBI, корейская версия модифицированного индекса Бартеля; mRS, модифицированная шкала Ренкина.
https://doi.org/10.1371/journal.pone.0226324.g001
Соотношение пола и среднего возраста между оценками mRS значительно различались ( p <0,05). При ретроспективном анализе доли пола в оценках mRS значительно отличались друг от друга, за исключением mRS степени 2 и mRS степени 3, а также для mRS степени 4 и mRS степени 5. Средний возраст mRS степени значительно отличался друг от друга, кроме MRS степени 2 и mRS степени 3.
Диапазон оценок K-MBI был небольшим в категориях mRS 0, 1 и 2, а медианы были аналогичными (100, 100 и 96 соответственно). Напротив, диапазон оценок K-MBI в категориях mRS 3, 4 и 5 был широким, со средним баллом 83, 48 и 2, соответственно. Наблюдалось значительное совпадение оценок K-MBI между оценками mRS.
Для определения наличия статистически значимой разницы ( P <0,05) в средних показателях K-MBI между оценками mRS применялисьтестов Краскела-Уоллиса.Результаты показали, что существуют значительные различия в показателях K-MBI между классами mRS ( P <0,0001). Тест Манна-Уитни был проведен как апостериорный анализ теста Краскела-Уоллиса. Все оценки mRS статистически отличались друг от друга ( P <0,01).
Оптимальные пороговые значения K-MBI для классов mRS
Оптимальные пороговые значения K-MBI по отношению к классам mRS, а также чувствительность, специфичность, PPV и NPV каждого порога показаны в таблице 2.
Для степени 0 по шкале mRS оптимальный пороговый балл K-MBI составлял 100 с чувствительностью 0,940 и специфичностью 0,612. Для степени 1 по шкале mRS оптимальный пороговый балл K-MBI составлял 98 с чувствительностью 0,904 и специфичностью 0,838. Для степени 2 по шкале mRS оптимальная граничная оценка K-MBI составила 94 с чувствительностью 0,885 и специфичностью 0,937. Для степени 3 по шкале mRS оптимальный пороговый балл K-MBI составлял 78 с чувствительностью 0,946 и специфичностью 0,973. Для 4 степени mRS оптимальная граничная оценка K-MBI составила 55 с чувствительностью 0.937 и специфичность 0,986. Исходя из этого результата, был получен диапазон отсечки K-MBI для каждой степени mRS. Для степени 0 по шкале mRS пороговая оценка K-MBI составляла 100, что указывает на отсутствие соответствующего диапазона оценок. Для 1, 2, 3, 4 и 5 классов mRS диапазон оценок K-MBI составлял от 99 до 98, от 97 до 94, от 93 до 78, от 77 до 55 и до 54 соответственно.
AUC для порогового значения K-MBI составляло 0,791 для mRS степени 0, 0,919 для mRS степени 1, 0,970 для mRS степени 2, 0,994) для mRS степени 3 и 0,991 для mRS степени 4 (таблица 3).
Во всех классах mRS асимптотическая значимость для всех AUC была очень значимой (p <0,0001), что указывает на то, что все пороговые значения K-MBI являются подходящими измерениями для различения дихотомических степеней mRS (AUC более 50%). На рис. 2 показаны кривые ROC.
Обсуждение
В этом исследовании мы проанализировали соответствие между mRS и K-MBI, вычислив оптимальные значения отсечки K-MBI для mRS. Пороговые баллы K-MBI были определены как 100 для mRS степени 0, 98 для mRS степени 1, 94 для mRS степени 2, 78 для mRS степени 3 и 55 для mRS степени 4.Насколько нам известно, это первое исследование, в котором определялись пороговые значения K-MBI, соответствующие классам mRS у пациентов с инсультом. K-MBI позволяет оценить базовый уровень ADL пациента с различных точек зрения и все чаще используется в качестве основной конечной точки в клинических исследованиях инсульта [14, 19–22]. Результаты этого исследования могут иметь последствия для определения результатов исследований инсульта. Например, изменение категории K-MBI предполагает клинически значимое улучшение функции ADL у пациентов с инсультом.Таким образом, исследователи могут решить, указывает ли изменение оценки в группе на пользу вмешательства. Кроме того, также можно разделить результаты испытаний инсульта на благоприятные и неблагоприятные. Хотя нет согласованной точки дихотомизации для mRS [23]. в большинстве исследований инсульта благоприятный исход определяется как степень mRS ≤ 1 или ≤ 2 ([24, 25]. Согласно нашим результатам, если испытания определяют благоприятный исход, целевой балл после вмешательства или время восстановления составляет степень mRS ≤ 1 с соответствующий показатель отсечения K-MBI ≥ 98.Если испытания определяют благоприятный исход как степень mRS ≤ 2, соответствующий пороговый балл K-MBI будет ≥ 94. Более того, перевод результатов испытаний может позволить провести метаанализ в испытаниях острого инсульта.
Интересный вывод из этого исследования состоит в том, что диапазоны отсечки K-MBI, представляющие оценки по шкале mRS, были переменными. В частности, оценки по шкале mRS 0, 1 и 2 имели узкий диапазон оценок K-MBI. Хотя средние значения K-MBI для оценок mRS 0, 1 и 2 значительно различались, разница между оптимальными пороговыми значениями K-MBI для mRS степени 0 и mRS степени 1 и для mRS степени 1 и mRS степени 2 составила 2 балла. и 4 балла соответственно.Эти значения отсечки K-MBI близки к максимальным, что указывает на эффект потолка K-MBI. Хотя об эффекте потолка для K-MBI ранее не сообщалось, такой эффект часто наблюдается для BI [26, 27]. Поскольку K-MBI основан на BI и сильно коррелирует с ним, было бы неудивительно, если бы эффект потолка также наблюдался в K-MBI. K-MBI фокусируется на базовом ADL и не имеет информации о многих инструментальных ADL. Следовательно, многие задачи, которые не измеряются с помощью K-MBI, могут сыграть важную роль в потере трудоспособности после инсульта.100 баллов по шкале K-MBI (независимо от всех 10 видов деятельности) не означает, что пациент может самостоятельно выполнять расширенные ADL. Эти результаты показывают, что K-MBI не может быть чувствительным инструментом оценки при обнаружении изменений в инвалидности у пациентов с легким инсультом.
Напротив, оценки mRS 3, 4 и 5 показали широкий диапазон оценок K-MBI, а оценки K-MBI перекрывались между оценками mRS. Это может быть связано с низкой репрезентативностью mRS у пациентов с умеренной и тяжелой инвалидностью, что позволяет предположить, что mRS не является чувствительным показателем для пациентов этих категорий.Скорее, K-MBI может иметь более высокую дискриминационную способность у пациентов со средними и тяжелыми формами инвалидности. Эти результаты согласуются с предыдущими исследованиями. У пациентов с инсультом с легкой и средней степенью инвалидности mRS лучше реагирует, поскольку BI испытывает эффект потолка. Однако у пациентов с тяжелой инвалидностью BI был более полезен для различения пациентов [28]. Точно так же глобальные шкалы, такие как mRS, были гораздо менее чувствительны к изменениям инвалидности, чем шкалы ADL [29].
mRS очень проста и не требует специальных инструментов или обучения, что делает ее пригодной для использования в больших испытаниях. Хотя внутриэкспертная надежность mRS относительно удовлетворительна, межэкспертная надежность оказалась низкой, особенно в исследованиях с большим размером выборки [30]. Это может быть связано с субъективным характером оценки и отсутствием четких критериев, что снижает надежность измерений [31–33]. Кроме того, 7-балльной порядковой шкалы может быть недостаточно для точной оценки инвалидности пациента.Оценка mRS определяется ограничениями в активности и мобильности пациентов. Однако ограничение повседневной активности и подвижности пациентов с инсультом не всегда проявляется на типичных стадиях. Были попытки повысить надежность mRS. В предыдущих исследованиях сообщалось, что структурированное интервью может повысить надежность между экспертами [31, 32), и даже было высказано предположение, что использование контрольного списка ADL для оценки mRS может повысить надежность результатов между экспертами [34].
В этом исследовании мы использовали mRS в качестве ориентира для классификации K-MBI.Основная цель этого исследования состояла в том, чтобы предложить клинически различимые категории K-MBI со статистическими доказательствами. Хотя mRS не является золотым стандартом для измерения инвалидности у пациентов с инсультом, мы считаем, что он подходит для этой цели. Во-первых, mRS — это самая популярная оценка глобальной инвалидности при инсульте с хорошо изученной достоверностью и надежностью. Во-вторых, 6 уровней mRS четко определены и клинически различны.
Это исследование имеет несколько ограничений. Во-первых, всего 2099 (26.7%) пациенты пропустили контрольный визит через 3 месяца после начала инсульта. Исключение этих пациентов могло повлиять на результаты. Однако целью этого исследования было определение пороговых значений K-MBI для mRS. Для этого требуется большое количество показателей K-MBI и mRS, оцененных в один и тот же момент времени у одного и того же пациента. В исследовании KOSCO K-MBI и mRS оценивались в начальной временной точке, через 7 дней после инсульта, и наблюдались через 3 месяца в одно и то же время у тех же пациентов.Хотя значительное количество пациентов было потеряно в течение 3 месяцев наблюдения, данные этого периода соответствуют цели данного исследования. Во-вторых, в этом исследовании результаты представляют весь размер выборки. Результаты не были стратифицированы по полу, возрастным категориям, сопутствующим заболеваниям и различным временным точкам (на исходном уровне и через несколько месяцев). Несмотря на установленную надежность mRS и K-MBI, полученные результаты не могут быть распространены на другой пол или возрастную группу. Кроме того, в исследовании использовался K-MBI исключительно в корейской популяции.Дальнейшие исследования должны изучить валидность пороговых значений этого исследования для разных групп населения.
Выводы
В целом, хотя mRS и K-MBI часто классифицируются как шкала функциональных результатов в исследованиях инсульта, они имеют существенно разные характеристики. Ни mRS, ни K-MBI не дают полной картины функциональных возможностей у пациентов с инсультом. mRS кажется более чувствительным, чем K-MBI у выживших после инсульта с более легкой остаточной инвалидностью, тогда как K-MBI может быть более чувствительным у выживших после инсульта с тяжелой остаточной инвалидностью, предоставляя более конкретную информацию о ADL.Таким образом, следует уделять особое внимание использованию одного из этих измерений для оценки остаточной инвалидности выживших после инсульта.
Ссылки
- 1. Мукерджи Д., Патил К.Г. Эпидемиология и глобальное бремя инсульта. World Neurosurg. 2011; 76 (6 доп.): S85–90. pmid: 22182277
- 2. Лангхорн П., Бернхардт Дж., Кваккель Г. Реабилитация после инсульта. Ланцет. 2011. 377 (9778): 1693–702. pmid: 21571152
- 3. Куинн Т.Дж., Доусон Дж., Уолтерс М.Р., Лис К.Р.Функциональные критерии исходов в современных исследованиях инсульта. Int J Stroke. 2009. 4 (3): 200–5. pmid: 19659822
- 4. Махони Ф.И., Бартел Д.В. Функциональная оценка: индекс Бартеля. Md State Med J. 1965; 14: 61–5.
- 5. Шах С., Ванклай Ф., Купер Б. Повышение чувствительности индекса Бартеля для реабилитации после инсульта. J Clin Epidemiol. 1989. 42 (8): 703–9. pmid: 2760661
- 6. Кучукдевечи А.А., Явузер Г., Теннант А., Сулдур Н., Сонель Б., Арасил Т.Адаптация модифицированного индекса Бартеля для использования в физической медицине и реабилитации в Турции. Scand J Rehabil Med. 2000. 32 (2): 87–92. pmid: 10853723
- 7.
Шах С., Купер Б., Маас Ф. Индекс Бартеля и оценка ADL в реабилитации после инсульта в Австралии, Японии, Великобритании и США. Aust Occup Ther J. 1992; 39 (1): 5–13. pmid: 217
- 8. Леунг С.О., Чан С.К., Шах С. Разработка китайской версии модифицированного индекса Бартеля — валидность и надежность.Clin Rehabil. 2007. 21 (10): 912–22. pmid: 17981850
- 9. Jung HY, Park BK, Shin HS, Kang YK, Pyun SB, Paik NJ и др. Разработка корейской версии модифицированного индекса Бартеля (K-MBI): многоцентровое исследование для пациентов с инсультом. J Korean Acad Rehabil Med. 2007. 31 (3): 283–97.
- 10. Охура Т., Хигаси Т., Ишизаки Т., Накаяма Т. Оценка достоверности и внутренней согласованности инструмента оценки эффективности на основе японской версии модифицированного индекса Бартеля для пожилых людей, живущих дома.J Phys Ther Sci. 2014; 26 (12): 1971–4. pmid: 25540510
- 11. de Haan R, Limburg M, Bossuyt P, van der Meulen J, Aaronson N. Клиническое значение «инвалидности» Ранкина после инсульта. Гладить. 1995. 26 (11): 2027–2030. pmid: 7482643
- 12. Sulter G, Steen C, De Keyser J. Использование индекса Бартеля и модифицированной шкалы Рэнкина в испытаниях острого инсульта. Гладить. 1999. 30 (8): 1538–41. pmid: 10436097
- 13. Uyttenboogaart M, Luijckx GJ, Vroomen PC, Swewart RE, De Keyser J.Измерение инвалидности при инсульте: взаимосвязь между модифицированной шкалой Рэнкина и индексом Бартеля. J Neurol. 2007; 254 (8): 1113–7 pmid: 17668259
- 14. Чанг У.Х., Сон М.К., Ли Дж., Ким Д.Й., Ли С.Г., Шин И.И. и др. Корейская когорта инсульта для функционирования и реабилитации (KOSCO): обоснование и протокол многоцентрового проспективного когортного исследования. BMC Neurol. 2015; 15:42. pmid: 25886039
- 15. Чанг У.Х., Сон М.К., Ли Дж., Ким Д.Й., Ли С.Г., Шин И.И. и др. Предикторы функционального уровня и качества жизни через 6 месяцев после первого инсульта: исследование KOSCO.J Neurol. 2016; 263 (6): 1166–77. pmid: 27113602
- 16. Ранкин Дж. Сосудистые нарушения мозгового кровообращения у пациентов старше 60 лет. II. Прогноз. Скотт Мед Дж. 1957; 2 (5): 200–15. pmid: 13432835
- 17. Коннелл Ф.А., Кёпселл Т.Д. Меры повышения достоверности диагностического теста. Am J Epidemiol. 1985. 121 (5): 744–53. pmid: 4014166
- 18. Хаджиан-Тилаки К. Анализ кривой рабочих характеристик приемника (ROC) для оценки медицинских диагностических тестов.Caspian J Intern Med. 2013. 4 (2): 627–35. pmid: 24009950
- 19. Kim DY, Lim JY, Kang EK, You DS, Oh MK, Oh BM и др. Влияние транскраниальной стимуляции постоянным током на восстановление моторики у пациентов с подострым инсультом. Am J Phys Med Rehabil. 2010. 89 (11): 879–86. pmid: 20962598
- 20. Бхасин А., Шривастава М.В., Моханти С., Бхатиа Р., Кумаран С.С., Бозе С. Терапия стволовыми клетками: клиническое испытание инсульта. Clin Neurol Neurosurg. 2013. 115 (7): 1003–8. pmid: 23183251
- 21.Kong KH, Chua KS, Lee J. Симптоматическая спастичность верхних конечностей у пациентов с хроническим инсультом, посещающих реабилитационную клинику: частота, клинические корреляты и предикторы. J Rehabil Med. 2010. 42 (5): 453–7. pmid: 20544156
- 22. Franceschini M, Agosti M, Cantagallo A, Sale P, Mancuso M, Buccino G. Зеркальные нейроны: лечение наблюдения за действием как инструмент в реабилитации после инсульта. Eur J Phys Rehabil Med. 2010. 46 (4): 517–23. pmid: 20414184
- 23. Новый PW, Buchbinder R.Критическая оценка и обзор шкалы Рэнкина и ее производных. Нейроэпидемиология. 2006; 26 (1): 4–15. pmid: 16272826
- 24. Квятковски Т.Г., Либман Р.Б., Франкель М., Тилли BC, Моргенштерн Л.Б., Лу М. и др. Эффекты тканевого активатора плазминогена при остром ишемическом инсульте через год. Национальный институт неврологических заболеваний и инсульта Группа по изучению инсульта, рекомбинантного тканевого активатора плазминогена. N Engl J Med. 1999. 340 (23): 1781–7. pmid: 10362821
- 25. Сальгадо А.В., Ферро Дж.М., Гувейя-Оливейра А.Долгосрочный прогноз первых в истории лакунарных инсультов. Больничное исследование. Гладить. 1996. 27 (4): 661–6. pmid: 8614926
- 26. Uyttenboogaart M, Stewart RE, Vroomen PC, De Keyser J, Luijckx GJ. Оптимизация оценок отсечки для индекса Бартеля и модифицированной шкалы Рэнкина для определения исходов в испытаниях острого инсульта. Гладить. 2005; 36 (9): 1984–7. pmid: 16081854
- 27. Квон С., Хартзема А.Г., Дункан П.В., Мин-Лай С. Меры инвалидности при инсульте: взаимосвязь между индексом Бартеля, показателем функциональной независимости и модифицированной шкалой Рэнкина.Гладить. 2004. 35 (4): 918–23. pmid: 14976324
- 28. Веймар К., Курт Т., Крайвинкель К., Вагнер М., Буссе О., Хаберл Р.Л. и др. Оценка функционирования и инвалидности после ишемического инсульта. Гладить. 2002. 33 (8): 2053–9. pmid: 12154262
- 29. Дромерик А.В., Эдвардс Д.Ф., Дирингер М.Н. Чувствительность к изменениям инвалидности после инсульта: сравнение четырех шкал, используемых в клинических испытаниях. J Rehabil Res Dev. 2003. 40 (1): 1–8. pmid: 15150715
- 30. Куинн Т.Дж., Доусон Дж., Уолтерс М.Р., Лис К.Р.Надежность модифицированной шкалы Рэнкина: систематический обзор. Гладить. 2009. 40 (10): 3393–5. pmid: 19679846
- 31. Уилсон Дж. Т., Хариендран А., Грант М., Бэрд Т., Шульц Ю. Г., Мьюир К. В. и др. Улучшение оценки исходов при инсульте: использование структурированного интервью для выставления оценок по модифицированной шкале Рэнкина. Гладить. 2002. 33 (9): 2243–6. pmid: 12215594
- 32. Уилсон Дж. Т., Хариендран А., Хендри А., Поттер Дж., Боун I, Мьюир К. В.. Надежность модифицированной шкалы Рэнкина для нескольких оценщиков: преимущества структурированного интервью.Гладить. 2005; 36 (4): 777–81. pmid: 15718510
- 33. Куинн Т.Дж., Доусон Дж., Уолтерс М.Р., Лис К.Р. Надежность модифицированной шкалы Рэнкина. Гладить. 2007; 38 (11): e144; ответ автора e5. pmid: 17885254
- 34. Вулф CD, Тауб Н.А., Вудро Э.Дж., Берни П.Г. Оценка шкал инвалидности и инвалидности для больных, перенесших инсульт. Гладить. 1991. 22 (10): 1242–4. pmid: 1833860
Анализ модифицированной шкалы Рэнкина в рандомизированных контролируемых исследованиях острого ишемического инсульта: систематический обзор
Предпосылки .Исторически сложилось так, что большинство клинических исследований острого инсульта были нейтральными статистически, с испытаниями, как правило, дихотомическими порядковыми шкалами, такими как модифицированная шкала Рэнкина. Исследования, опубликованные до 2007 года, показали, что сохранение порядкового характера этих шкал увеличивает статистическую мощность. Систематический обзор испытаний, опубликованных с 2007 года, был проведен для переоценки используемых статистических методов и оценки того, изменилась ли практика. Методы . Поиск в электронных базах данных выявил РКИ, опубликованные в период с января 2007 г. по июль 2014 г. по острому ишемическому инсульту, с использованием порядковой шкалы зависимости в качестве первичного результата. Выводы . Было выявлено 42 РКИ. Большинство использовали дихотомический анализ (25, 59,5%), восемь (21,4%) сохранили порядковую шкалу, а девять (19,0%) использовали другой тип анализа. Выводы . В исследованиях, опубликованных с 2007 г., по-прежнему предпочтение отдавалось дихотомическому анализу, а не порядковому. При испытаниях инсульта, где это уместно, следует рассмотреть вопрос о сохранении порядкового характера шкал зависимости.
1. Введение
Модифицированная шкала Ренкина (mRS) представляет собой 7-уровневую упорядоченную категориальную шкалу, отражающую уровни функциональной независимости пациента после инсульта, с оценками от 0 (полностью независимый) до 6 (мертвый) [1].Сообщается, что mRS является достоверной и надежной конечной точкой в рандомизированных клинических испытаниях [2] и, как таковая, является распространенным и рекомендуемым критерием оценки результатов в исследованиях острого ишемического инсульта [3].
Исторически сложилось так, что клинические испытания острого ишемического инсульта в основном не могли продемонстрировать статистическое преимущество терапии над контролем [4]. Эта неудача объясняется множеством причин, включая соответствие лабораторных данных клиническому инсульту [5], неадекватный размер выборки [6], выбор первичного результата и его статистический анализ.Большинство исследований ранее отдавали предпочтение дихотомическому анализу показателей исходов с использованием порядковой шкалы [7]. Однако предыдущие обзоры исходов инсульта показали, что выбор аналитических методов был неоптимальным [8]. Коллаборация OAST опубликовала в 2007 году повторный анализ исходов инсульта с использованием альтернативных статистических методов и показала, что методы, сохраняющие порядковый характер исходных данных, были наиболее оптимальными [7]. Было показано, что порядковая логистическая регрессия (OLR) обеспечивает наиболее статистически эффективный анализ шкал порядковых результатов, когда соблюдается предположение о пропорциональных шансах, что позволяет уменьшить размер пробной выборки по сравнению с дихотомическим анализом [7, 9].Это наряду с другими соответствующими работами привело к тому, что рабочая группа Европейской организации по инсульту порекомендовала исследователям отойти от дихотомических исходов и выбрать подход к анализу, основанный на типе набираемых пациентов и вероятном механизме вмешательства, которое необходимо протестировать [10] .
Основная цель этого систематического обзора — предоставить обновленную оценку статистических методов, используемых при анализе mRS в клинических испытаниях острого ишемического инсульта, опубликованных с 2007 по 2014 год.Принимая во внимание рекомендации, сделанные коллаборацией OAST в 2007 году, уместно оценить, повлияли ли эти результаты на более поздние тенденции в анализе порядковых исходов в исследованиях острого инсульта.
2. Материалы и методы
2.1. Стратегия поиска
Перекрывающиеся стратегии поиска были проведены для определения полного списка испытаний для систематического обзора. Доступ к электронным базам данных Национального центра биотехнологической информации (NCBI) PubMed, Ovid MEDLINE и Cochrane Collaboration Trials был получен в июле 2014 года.Публикации, цитирующие результаты сотрудничества OAST, также были просмотрены для выявления потенциально подходящих исследований. Были приняты меры для записи только исходной публикации результатов испытаний, а последующие публикации и анализы подгрупп не были включены.
Были использованы ключевые слова «инсульт», «ишемический», «рандомизированный» и «Ранкин» с учетом различий в написании и комбинациях в зависимости от используемой базы данных. Систематический обзор стремился включить проспективные рандомизированные исследования III фазы острого ишемического инсульта с использованием mRS в качестве первичного результата исследования.Были также включены испытания с использованием Оксфордской шкалы гандикапов (OHS), очень близкого варианта mRS. В дальнейшем поиск был ограничен исследованиями, опубликованными на английском языке с 2007 по июль 2014 года. Из обзора были исключены исследования по профилактике инсульта, геморрагического инсульта и те, которые не включали mRS в первичный результат.
2.2. Скрининг и соответствие критериям
Названия и отрывки исследований были проверены на предмет выявления потенциально подходящих исследований. Впоследствии были получены полные тексты соответствующих публикаций и проанализированы, чтобы окончательно составить полный список подходящих исследований, за исключением тех, которые не соответствовали всем критериям включения.
2.3. Сбор данных
Данные для основной цели обзора были собраны из полного текста каждой публикации и включали название испытания, год публикации, количество рандомизированных участников, протестированное вмешательство и время наблюдения. Кроме того, был записан названный метод анализа, использованный для оценки первичного результата, определения благоприятного результата mRS, где это применимо, и изложение результата исследования.
3. Результаты
3.1. Выборка исследования
Всего с помощью методов поиска после удаления дубликатов было идентифицировано 192 публикации. Скрининг резюме исследований выявил 76 потенциально релевантных клинических испытаний ишемического инсульта с использованием mRS в качестве основного результата (рис. 1). Восемнадцать исследований были исключены как нерандомизированные, наблюдательные, ретроспективные или пилотные, первоначально опубликованные до 2007 г .; испытания по профилактике инсульта; или те, кто не использует mRS в первичном исходе.
3.2. Характеристики 42 идентифицированных клинических испытаний
В целом подходили 42 публикации клинических испытаний с участием 32 432 участников, размер исследований варьировался от 37 до 4071 рандомизированных лиц (таблица 1). Девять (21,4%) испытаний были положительными, в то время как подавляющее большинство исследований (31 исследование, 73,8%) не смогли продемонстрировать преимущество изучаемого вмешательства над контролем. Два испытания (4,8%) по оценке отмены кандесартана и статинов показали доказательства вредного вмешательства.
Клиническое исследование (год публикации) Вмешательство Кол-во пациентов. Первичный результат
(благоприятная оценка)Метод анализа Результат исследования CATIS (2014) Антигипертензивный 4,071 мес. тест (нескорректированный), ИЛИ логистической регрессией Нейтрально URICO-ICTUS (2014) Мочевая кислота 421 mRS через 90 дней (0-1 (оценка 2, если было 2)) Лог-биномиальная регрессия (скорректированная) Нейтрально ALIAS Part 2 (2013) Альбумин 848 mRS и NIHSS при 90 d GLM с логической связью (отрегулированной) Нейтрально AXIS-2 (2013) Filgrastim (G-CSF) 328 mRS при 90 d Наименьший квадратнейтральный CERE-LYSE-1 (2013) Церебролизин + альтеплаза 119 mRS через 90 дней Порядковая логистическая регрессия Нейтрально, испытание прекращено MLC601 1,100 mRS в 3 мес. Порядковая логистическая регрессия (скорректированная) Нейтрально ECCS-AIS33 (2013) Edaravone через 3 месяца ANOVA (средний балл mRS) Положительный результат на эдаравон IMS III (2013) Эндоваскулярная терапия 656 mRS через 3 месяца (0–328) Тест CMH (скорректированный) Нейтрально, испытание прекращено досрочно Комплексная реабилитация (2013) Комплексная реабилитация 69 mRS при 90 d (0-1) Дихотомический (недоступно) Нейтральный MAC SI (2013) DP-b99 44633 d Тест CMH с модифицированными оценками ридита Нейтральный () NBP (2013) dl-3-n-Бутилфталид 573 dRS и BI 1) тест положительный () NEST 1 и 2, объединенный (2013) Транскраниальная лазерная терапия 780 mRS при логарифмической регрессии 90 d (0–2) (скорректировано) Положительный Расширение СИНТЕЗА (2013) Эндоваскулярная терапия 362 mRS через 3 мес. (0-1) Точный тест Фишера , OR по методу MHНейтральныйCASTA (2012) Церебролизин 1070 Общий тест: mRS, NIHSS и BI при 90 д Глобальный направленный тест (тест Уилкокситона, , Манна) Ранний аспирин (2012) Аспирин + альтеплаза 642 mRS через 3 месяца (0–2) Дихотомия повышенная (неуточненная ранняя) Ginsenoside-Rd (2012) Ginsenoside-Rd 390 mRS, NIHSS, BI на 90 d (0–2) Тестирование OR (с корректировкой по логистической регрессии), Положительный Домашняя реабилитация (2012) Домашняя реабилитация 60 mRS, BI и EQ-5D в возрасте 2 лет (0-1) Дихотомия (u nspecified) Положительный ICTUS (2012) Citicoline 2,298 глобальный тест: mRS, NIHSS, BI через 90 дней Логистическая регрессия с поправкой IST-3 (2012) rt-PA 3,035 OHS в течение 6 мес. (0–2) Логистическая регрессия (скорректированная) Нейтральная
903 Миноциклин (2012)Миноциклин 50 mRS, NIHSS, BI на 90 дн -тест и тест Манна-Уитни Положительный Скальпунктурный электрическая акупунктура 62 NIHSS, mRS, BI при постакупунктуре Точный тест Фишера нейтральный ALIAS Part 1 (2011) Альбумин 316 Составные mRS и NIHSS при 90 d (0-1) Дихотомические (не указаны) Нейтральные Пирацетам 49 Показатели mRS, GAT, NIHSS и BI через 24 недели -тест и тест Манна-Уитни Нейтральный CA 458 mRS через 90 дней (0–2) Нормальное приближение к биномиальному Сравнимо с аспирином (эффективность и безопасность) QASC (2011) Оценка mRS, BI, SF-36, PSC через 90 дней (0-1) Логистическая регрессия с GEE Положительно SCAST (2011) 90 333 Кандесартан 2,029 mRS в 6 мес. Порядковая логистическая регрессия Отрицательная SENTIS (2011) Устройство NuroF328 ,NuroF328, Global Endpoint 9033 и GOS в 90 дней (0-1) Логистическая регрессия (скорректированная) Нейтрально t-PA у пожилых людей (2011 г.) t-PA 97 mRS at разряд (0–2) Дихотомический (недоступен) Нейтральный COSSACS (2010) Антигипертензивный 763 мкс по скорректированной логистической регрессии) Нейтрально, исследование прекращено раньше РАННЕЕ (2010) Аспирин + дипиридамол <24 ч 548 9032 8 мРС через 90 дней (0-1)Тест CMH (скорректированный), ИЛИ с помощью логистической регрессии Нейтрально ASP I и II промежуточные (2009) Ancrod 508 508 mRS через 90 дней (в зависимости от оценки до инсульта)Логистическая регрессия (скорректированная) Neutral CHHIPS (2009) Манипуляция АД 180 mRS через 2 недели ) Логистическая регрессия Нейтрально, исследование недостаточно мощное DIAS-2 (2009) 90 & 125 µ г / кг десмотеплазы 193 при 90 днях Глобальный статистический тест Нейтральный EDO (2009) Edaravone 401 mRS через 3 месяца (0-1) Dichotomous (недоступно) Нейтрально NEST-2 (2009) Транскраниальная лазерная терапия 660 mRS и NIHSS через 9033 (0–2) Логистическая регрессия Нейтральный () PAIS (2009) Парацетамол 1,400 mRS через 3 мес. ) Абциксимаб 801 mRS в 3 месяца Скользящая дихотомия (mRS 0, если NIHSS 4–7, 0-1, если 8–14, и 0–2, если 15–22) Нейтрально ECASS III (2008) Alteplase (RT-PA) 821 mRS на 90 дней (0-1) тест (OR и RR) Положительный
7903 28 TCCS под контролем УЗИ (2008) Транскраниальная сонография с цветовой кодировкой 37 mRS, BI и смерть через 90 дней Тест Манна-Уитни Нейтральный mRS, общая польза от терапии TCCS MELT (2007) Урокиназа 114 mRS через 90 дней (0–2) Точный тест Фишера Нейтральный, испытание прекращено рано (2007) (2007) SAINT II NXY-059 3,306 mRS при 90 d Тест CMH (скорректированный) нейтральный отмена статина (2007) отмена статина 8 mo (0–2) Логистическая регрессия Отрицательный Порядковый анализ.CMH: Cochran-Mantel-Haenszel, GEE: общее уравнение оценки, GLM: обобщенная линейная модель, OR: отношение шансов и RR: относительный риск. Нейропротекторные или нейротрофические соединения составили большую часть изученных вмешательств в 17 (40,5%) опубликованных клинических исследованиях. Антитромбоцитарная или тромболитическая терапия наблюдалась в 11 (26,2%) исследованиях, в то время как пять (11,9%) исследований были направлены на улучшение физических симптомов с помощью контроля артериального давления или контроля температуры тела и лихорадки.В трех (7,1%) исследованиях изучалась эндоваскулярная терапия или катетерные устройства, а в двух (4,8%) последовательных исследованиях оценивалась транскраниальная лазерная терапия. Три (7,1%) исследования касались пользы инициатив по реабилитации после инсульта, а одно (2,4%) исследование изучало влияние лечения электрической иглоукалыванием кожи головы.
3.3. Сравнение показателей первичного результата
Показатели первичного результата значительно различались в опубликованных исследованиях. Использование только mRS наблюдалось более чем в половине включенных исследований (24 исследования, 57.1%). В тринадцати (31,0%) клинических испытаниях mRS (или OHS) использовался наряду с другими показателями результатов, включая индекс Бартеля (BI), шкалу инсульта NIH (NIHSS), показатели качества жизни EQ-5D и SF-36, шкалу результатов Глазго (GOS). ), Тест на афазию Гюльхане (GAT) или время в Центре первичного инсульта (PCS). В пяти (11,9%) исследованиях использовалась составная конечная точка, включающая баллы mRS плюс BI, NIHSS или GOS, при этом в трех из этих пяти исследований описывалась глобальная конечная точка с порогом результата, который должен быть достигнут по нескольким шкалам.
Результат был признан благоприятным при оценке mRS 0–1 и 0–2 в равном количестве исследований, по 10 (23,8%) в каждом. Только одно (2,4%) исследование определило благоприятный исход как 0–3 балла по шкале mRS. В трех (7,1%) дальнейших испытаниях были определены оценки благоприятных исходов, которые различались в зависимости от исходной оценки NIHSS, в которой используется скользящая дихотомия. Восемнадцать (35,7%) исследований не указали желаемый результат.
3.4. Сводка статистических методов, использованных в отдельных исследованиях
Всего 25 (59.5%) исследований использовали дихотомический анализ по сравнению с восемью (19,0%) исследованиями с использованием порядкового анализа и девятью (21,4%) исследованиями, которые не попали ни в одну из категорий (таблица 1). Тесты различий в пропорциях (точный критерий Фишера, тест или альтернатива) использовались в 14 (33,3%) исследованиях, в то время как бинарная логистическая регрессия использовалась в девяти (21,4%) исследованиях, что дает преимущество получения отношения шансов 95%. доверительный интервал и значение. Альтернативные подходы к моделированию использовались в двух (4,8%) исследованиях.Скользящая дихотомия использовалась в двух (4,8%) исследованиях, а глобальная статистика использовалась в двух (4,8%) дальнейших исследованиях. Статистические методы с использованием исходных порядковых баллов включали OLR (три исследования, 7,1%) и тест Кокрана-Мантеля-Хензеля (CMH) (пять исследований, 11,9%). В четырех (9,5%) исследованиях использовались тесты, основанные на нормальном распределении (-тест или обычная регрессия наименьших квадратов), и в одном (2,4%) исследовании использовался тест Манна-Уитни.
3.5. Распространенность порядковых методов во вторичных анализах
Из 11 статистически значимых исследований порядковые методы использовались в двух (18.2%) учеба. Двенадцать (28,6%) исследований сообщили об использовании порядковых методов в качестве вторичного анализа или анализа чувствительности. В семи (16,7%) исследованиях использовался тест Кокрана-Мантеля-Хензеля (CMH) или тест Ван Элтерена (скорректированный критерий Манна-Уитни), а в пяти (11,9%) исследованиях применялся OLR. В двух (4,8%) исследованиях сообщалось о количестве, необходимом для лечения (NNT), наряду с основным результатом исследования.
4. Обсуждение
Более половины опубликованных исследований острого ишемического инсульта использовали дихотомический анализ порядковой шкалы с большим расхождением в пороге благоприятного исхода.Этот результат аналогичен открытию, сделанному коллаборацией OAST в 2007 году, что почти половина из 55 выявленных исследований использовала дихотомический анализ (49%), что указывает на то, что дихотомический анализ по-прежнему является преобладающим выбором для анализа порядковой шкалы [7]. Напротив, коллаборация OAST обнаружила, что около 45% исследований использовали анализ среднего или медианного значения, по сравнению с гораздо меньшим процентом, использующим тот же анализ в этом более позднем обзоре (9,5%) [7]. Только пятая часть исследований в этом обзоре показала значительное преимущество вмешательства над контролем, тогда как Duncan et al.(2000) сообщили о систематическом обзоре 51 исследования, в котором гораздо больший процент исследований позволил получить значительную пользу (21 исследование, 41%), хотя ни одно из них не оказало впоследствии влияния на клиническую практику [8].
Менее четверти клинических испытаний выбрали использование анализов, соответствующих порядковой шкале; однако в одной трети испытаний сообщалось об использовании порядкового анализа вторичного анализа и анализа чувствительности, что указывает на то, что исследователи испытаний были осведомлены об этих методах. Только в двух исследованиях сообщалось о NNT вместе с основным результатом исследования, несмотря на рекомендацию OAST о том, что этот показатель помогает клинической интерпретации основного результата исследования [11].Одним из возможных объяснений этого открытия является то, как регулирующие органы, такие как FDA, авторы и журналы, рассматривают порядковый анализ. FDA только недавно приняло недихотомические подходы к анализу порядковых шкал. Следовательно, исследователи, возможно, не хотели менять свои планы анализа, в то время как FDA неохотно принимало такие подходы. Существуют неофициальные данные, позволяющие предположить, что людям трудно интерпретировать результаты порядкового анализа с точки зрения клинической важности, что также может привести к нерешительности в отношении применения этих методов.Наконец, поддержка использования таких методов может возрасти по мере публикации крупномасштабных испытаний с использованием таких методов. После завершения этого обзора было опубликовано несколько исследований с использованием порядкового метода анализа [12–15], что может способствовать принятию в случае необходимости.
Хотя здесь это не показано, мы также провели краткий обзор опубликованных протоколов текущих исследований инсульта. Из оцененных опубликованных работ 56% предлагают использовать анализ с сохранением порядковой шкалы, при этом в шести исследованиях конкретно указывается, что анализ первичного результата будет OLR, что уже численно больше, чем в трех опубликованных исследованиях, наблюдаемых в ходе систематического обзора.Хотя это высокоселективная выборка, можно предположить, что распространенность таких методов увеличивается.
С момента публикации исследования OAST в 2007 году наблюдается постоянный интерес как к разработке, так и к тестированию новых методов анализа порядковых исходов инсульта. Использование метода OLR основано на соблюдении предположения о пропорциональных шансах; то есть есть общий сдвиг по точкам разреза. Исследователи должны использовать данные предыдущих исследований, чтобы оценить, разумно ли предполагать это для оцениваемого вмешательства.Это предположение может не выполняться для некоторых методов лечения инсульта; например, тромболизис увеличивает шансы на хороший исход, но при определенных обстоятельствах может увеличить шансы смерти. В этих ситуациях была рекомендована модель частичных пропорциональных шансов, в которой допущение пропорциональных шансов ослаблено. Было показано, что этот метод имеет некоторые преимущества перед OLR при сравнении с использованием данных исследования тромболизиса NINDS [16]. Также предлагались альтернативы, свободные от предположений, такие как метод перестановки [17].Некоторые утверждали, что еще одним ограничением перехода к порядковому методу анализа является интерпретируемость обычного отношения шансов [18, 19]. Поэтому были предложены альтернативные меры лечебного эффекта [20, 21], хотя они имели ограниченное применение. NNT — это общепризнанный показатель абсолютного лечебного эффекта; Было предложено расширение этого метода для порядковых данных, которое может решить эту проблему [11]. Ограничением этих исследований является то, что они, как правило, повторно анализируют данные одного исследования, что затрудняет обобщение более широких исследований инсульта.Дальнейшие исследования должны быть сконцентрированы на обобщении имеющихся на сегодняшний день обширных данных по большому количеству разнообразных исследований, таких как набор данных OAST.
Хотя этот обзор сосредоточен на исследованиях инсульта, аналогичная работа и результаты были опубликованы в других областях, таких как черепно-мозговые травмы [22] и рак [23]. Несмотря на то, что результаты исследований черепно-мозговой травмы и рака основаны на различных шкалах результатов, в целом они совпадают с данными, наблюдаемыми при инсульте. На сегодняшний день не было обзора практики испытаний в этих областях, чтобы оценить, были ли предложены методы.
Имеются некоторые ограничения для представленных здесь работ. Во-первых, рекомендуется провести систематический обзор и собрать данные двумя независимыми авторами с последующей перекрестной проверкой и разрешением разногласий [24]. Этот обзор был проведен единственным автором под наблюдением старшего статистика, и поэтому он не пользуется такой проверкой вторым независимым автором. Во-вторых, публикации не на английском языке были исключены из обзора и, как таковые, могут ограничивать обобщаемость результатов.Однако в первоначальном списке из 192 результатов поиска было обнаружено только восемь неанглоязычных статей, а работа Моррисона и др. [25] не обнаружили доказательств систематической предвзятости в метаанализах с ограничением языка; таким образом, маловероятно, что ограничение поиска публикациями на английском языке внесет предвзятость в этом обзоре. В этот систематический обзор мы включили только результаты опубликованных испытаний. Более полный поиск также мог бы включать данные завершенных, но неопубликованных исследований, путем поиска в реестрах испытаний, таких как ClinicalTrials.gov и ISRCTN [26]. Есть данные, позволяющие предположить, что опубликованные исследования, как правило, больше и демонстрируют больший лечебный эффект, чем неопубликованные [27]. Поэтому включенные здесь исследования могут не быть репрезентативными для всех испытаний, проведенных за это время, и к результатам следует относиться с некоторой осторожностью.
5. Выводы
Результаты этого систематического обзора не указывают на резкий сдвиг в анализе первичных функциональных исходов после острого ишемического инсульта, несмотря на рекомендации OAST; однако, похоже, есть понимание использования этих методов, и может появиться тенденция к более порядочному анализу в текущих и будущих исследованиях.
Конкурирующие интересы
Авторы заявляют, что нет конкурирующих интересов относительно публикации этой статьи
Вклад авторов
Эми Нанн провела систематический обзор, проанализировала результаты и подготовила документ. Филип М. Бат был главным исследователем проекта «Оптимизирующий анализ исследований инсульта», внес клинический вклад и отредактировал документ. Лаура Дж. Грей разработала проект, руководила систематическим обзором и анализом и подготовила документ.Все авторы рассмотрели и согласились с окончательной представленной версией.
Преобразование результатов самооценки из регистра инсультов в модифицированную шкалу Ренкина: перекрестное исследовательское исследование
Выборка исследования и процедура
Это перекрестное исследовательское исследование на основе регистров, являющееся частью Физического исследования. Активность до инсульта в ГОТеБорге проект 11 . Были использованы два регистра качества: Väststroke, местный регистр инсульта в Гетеборге, Швеция, и Riksstroke, шведский национальный регистр инсульта.Были извлечены данные об оказании неотложной помощи и трехмесячном последующем наблюдении, зарегистрированные с 1 января 2015 г. по 31 августа 2018 г. Данные по неотложной помощи регистрировались персоналом больницы. Данные трехмесячного последующего наблюдения были собраны с использованием почтовых анкет, заполняемых самостоятельно, а также телефонных интервью с обученными медсестрами. Регистры Väststroke и Riksstroke были связаны статистиком Riksstroke с использованием уникальных личных идентификационных номеров пациентов.
Критерии включения, применявшиеся в этом исследовании, были следующими: пациенты с первым в истории инсультом, диагностированным в соответствии с кодами Международной классификации болезней (МКБ-10), пациенты в возрасте> 18 лет, полные данные о пациентах с mRS. данные, зарегистрированные в регистре Väststroke, и ответы на вопросы Riksstroke, которые должны были использоваться в алгоритме, как показано в дополнительной таблице S1.
Этика и информированное согласие
Файл данных, который использовался в исследовании, был анонимным, и отдельные пациенты не могли быть идентифицированы. Исследование было одобрено региональным советом по этике в Гетеборге (№ 346-16) и Шведским органом по этике (поправка № 2019-01251 / 346-16). Была соблюдена Хельсинкская декларация. Информированное согласие : согласно Управлению по защите данных Швеции, обработка данных, созданных в рамках регистров качества, представляет собой исключение из общего правила, требующего письменного информированного согласия пациентов.Кроме того, Закон о личных данных (шведский закон № 1998: 204 от 29 апреля 1998 г.) позволяет собирать данные из медицинских карт для клинических целей и контроля качества без письменного информированного согласия.
Переменные
Переменные, использованные для разработки модифицированного алгоритма шкалы Рэнкина-Риксстрока (mRS-RS)
Контрольная переменная mRS была получена из данных трехмесячного наблюдения Вестстрока. Данные mRS были собраны опытными врачами или медсестрами. Рекомендации по телефонному интервью, описанные Bruno et al. 8,12 отслеживались. MRS используется для определения уровня функциональной инвалидности пациента после инсульта; в нем используется 7-уровневая порядковая шкала, где 0 = «нет симптомов» и 6 = «смерть» 5 .
Переменные индекса были получены из данных трехмесячного наблюдения Riksstroke . Семь вопросов были выбраны профессионалами здравоохранения на основе клинических соображений для процедуры картирования. Были заданы следующие вопросы: 1. «Зависимы ли вы сегодня от помощи / поддержки члена семьи / ближайшего родственника?» 2.»Где ты сейчас остановился?» 3. «Как ваша подвижность сейчас?» 4. «Получают ли вы помощь от кого-нибудь, чтобы сходить в туалет?» 5. «Вам нужна помощь, чтобы одеться и раздеться?» 6. «У вас все еще есть проблемы после инсульта?» 7. «Смогли ли вы вернуться к жизни и занятиям, которые у вас были до инсульта?» (Дополнительная таблица S1).
Переменные, использованные для описания образца исследования
От Väststroke: тяжесть инсульта при поступлении в больницу оценивалась по шкале инсульта Национального института здравоохранения (NIHSS) 13 .Когнитивные функции во время пребывания в больнице оценивались с помощью Монреальской когнитивной оценки (MoCA) 14 .
Из Riksstroke: были получены пол пациентов, возраст, факторы риска инсульта, статус активности до инсульта, реперфузионное лечение, продолжительность пребывания в больнице и место выписки. Тип инсульта классифицировался согласно кодам МКБ-10: отсутствие травматического внутримозгового кровоизлияния (I61), инфаркт мозга (I63) и неуточненный инсульт (I64). Уровень сознания по прибытии в больницу оценивался по шкале уровня реакции (RLS).Оценки RLS варьировались от 1 до 8, где «1» означало полное бодрствование / бдительность 15 .
Статистический анализ
Характеристики исследуемой выборки описаны как средние (SD), медианы (диапазон), количества (%) и квартили (Q 1 –Q 3 ). Анализ выпадения проводился с помощью критерия Пирсона χ 2 для номинальных переменных и критерия Манна – Уитни U для порядковых и непрерывных переменных с асимметричным распределением.
Разработка модифицированного алгоритма шкалы Ренкина-Риксстрака (mRS-RS)
Предварительная работа и картирование
Многопрофильная группа специалистов здравоохранения (три автора: Т.A., M.R., K.S.S.) с 8–30-летним опытом реабилитации после инсульта (исследования, а также клиническая работа) выполнили ручное сопоставление вопросов Riksstroke с оценками mRS. Семь вопросов от Riksstroke были определены как возможные кандидаты для алгоритма mRS-RS. Кроме того, категории ответов на вопросы Riksstroke были сопоставлены с оценками mRS, индивидуально каждым специалистом в области здравоохранения. Варианты ответа «Не знаю» и «Не имею родственников / друзей или не контактирую с родственниками / друзьями» были исключены из анализа.
Результаты ручного картирования обобщены в SPSS. Общее согласие между mRS-RS и mRS, а также согласие по отдельным классам оценивалось с помощью каппа Коэна. Поскольку mRS является порядковой шкалой, был рассчитан квадратичный вес типа Флейсса-Коэна (K w ). Уровень согласия интерпретировался как слабый (K w ≤ 0,20), удовлетворительный (K w = 0,21–0,40), умеренный (K w = 0,41–0,60), существенный (K w = 0,61– 0.80) и почти идеальный (≥ 0,81) 16 . Результаты описываются перекрестной таблицей, значениями K и , значениями p и 95% доверительным интервалом.
Деревья принятия решений
Справочная переменная mRS (Väststroke) была порядковой. Были и порядковые, и номинальные индексные переменные — это семь вопросов от Riksstroke. Таким образом, для построения деревьев решений был использован непараметрический метод. Набор данных был разделен на обучающий (80%) и тестовый (20%) наборы. Несколько измерений были использованы для оценки производительности деревьев решений.Точность классификации использовалась для определения общего количества правильно классифицированных пациентов. Точность классификации дополнительно сравнивалась со скоростью отсутствия информации, чтобы определить удобство использования модели. Квадратичный K w был использован для изучения соответствия между истинными и предсказанными значениями mRS. Для каждого дерева классификации были созданы матрицы неточностей.
Были построены три отдельных дерева решений:
Дерево 1. Для проверки алгоритма mRS-RS, который был разработан на основе ручного сопоставления, мы использовали mRS с оценками 0–2, 3, 4 и 5 в качестве целевой переменной.
Дерево 2. Чтобы отличить оценки mRS 0, 1 и 2 друг от друга, в качестве целевой переменной использовалась полномасштабная оценка mRS.
Дерево 3. Из-за клинического обоснования и проблем с ручным картированием целевой переменной была mRS с оценками 0–1, 2–3 и 4–5, что указывало на отсутствие инвалидности, умеренную инвалидность и тяжелую инвалидность, соответственно.
Описательный статистический анализ исследуемой выборки и анализ согласованности выполнялись в SPSS Statistics 26.0 (IBM SPSS Statistics для Windows, Армонк, Нью-Йорк: IBM Corp). Деревья решений были построены с использованием подхода условных деревьев вывода (ctree) из набора инструментов для рекурсивного разбиения (partykit) из пакета 17,18 (R, версия 3.6.2). Все тесты были двусторонними и проводились с уровнем значимости 5%.
(PDF) Модифицированная шкала Рэнкина при остром инсульте имеет хорошую надежность в разных оценках, но сомнительная достоверность
Надежность mRS при остром инсульте Cerebrovasc Dis 2010; 29: 188–193
193
Ссылки
1 van Swieten JC, Koudstaal PJ, Visser MC,
Schouten HJ, va n Gijn J: Interobserver a gree-
ment для оценки инвалидности у
пациентов, перенесших инсульт.Stroke 1988;
19: 604–607.
2 de Haan R, Limburg M, Bossuyt P, van der
Meulen J, Aaronson N: клиническое значение
ранга в «инвалидности» после инсульта.
Stroke 1995;
26: 2027–2030.
3 Комитета по критериям Нью-Йоркской кардиологической ассоциации
: Номенклатура и критерии для
Диагностика заболеваний сердца и крупных сосудов
. Бостон, Литтл Браун, 1994, стр. 253–
256.
4 Wang DZ, Rose JA, Honings DS, Garwacki
DJ, Milbrandt JC: Лечение пациентов с острым инсультом
пациентов с внутривенным tPA: инсульт OSF
сетевой опыт. Stroke 2000;
31: 77–81.
5 Weimar C, Ziegler A, König IR, Diener HC:
Прогнозирование функционального исхода и выживаемости
после острого ишемического инсульта. J Neurol 2002;
249: 888–895.
6 Johnston SC, Wilson CB, Halbach VV, Hi-
gashida RT, Dowd CF, McDermott MW, Ap-
Plebury CB, Farley TL, Gress DR: Endovas-
куларное и хирургическое лечение неразорвавшихся участков
аневризмы головного мозга: сравнение рисков.
Ann Neurol 2000;
48: 11–19.
7 Ferguson GG, Eliasziw M, Barr HW, Clagett
GP, Barnes RW, Wallace MC, Taylor DW,
Haynes RB, Finan JW, Hachinski VC, Bar-
nett HJ: The North American Symptomatic
Каротидная эндартерэктомия Испытание: хирургическое повторение —
сеанса у 1415 пациентов. Stroke 1999;
30: 1751–
1758.
8 Q uinn TJ, Le es KR, Hardem ark HG, Dawson
J, Walters MR: Первоначальный опыт использования цифрового обучающего ресурса
для оценки модификации Rankin Sale
в клинических испытаниях.Stroke 2007;
38:
2257–2261.
9 Hand PJ, Haisma JA, Kwan J, Lindley RI,
Lamont B, Dennis MS, Wardlaw JM: In-
Соглашение о наблюдении за больным для клинической оценки подозрения на инсульт. Инсульт
2006 г .;
37: 776–780.
10 Инсульт — 1989. Рекомендации по профилактике, диагностике и лечению инсульта
. Отчет
Целевой группы ВОЗ по инсульту и другим
Цереброваскулярным заболеваниям.Инсульт 1989 г .;
20:
140 7–1431.
11 Brot t T, Adams HP Jr, Olinge r CP, M arler JR,
Barsan WG, Biller J, Spilker J, Holleran R,
Eberle R, Hertzberg V, et al: Измерения
острых мозговых инфаркт: клинический осмотр — шкала
. Инсульт 1989 г .;
20: 864–870.
12 Bamford J, Sandercock P, Dennis M, Burn J,
Warlow C: Классификация и естественная история
клинически идентифицируемых подтипов церебрального инфаркта
.Lancet 1991;
337: 1521–1526.
13 T ELEform 쏐 Elite Version 9. Саннивейл, Ver-
ity, 2005.
14 Shrout PE, Fleiss JL: Внутриклассовые корреляции:
используется для оценки надежности оценщика. Psychol
Bull 1979;
86: 420–428.
15 Коэн Дж .: Взвешенная каппа: номинальная шкала
Соглашение с резервом на масштабную скидку
Соглашение или частичное зачисление. Psychol Bull
1968;
70: 213.
16 Wilson JT, Hareendran A, Grant M, Baird T,
Schulz UG, Muir KW, B one I: Улучшение
оценки результатов инсульта: использование структурированного интервью
для выставления оценок по
модифицированная шкала Ренкина. Stroke 2002;
33:
2243–2246.
17 Ладбрук Дж .: Обнаружение систематической систематической ошибки между двумя двумя оценками. Clin Exp Pharmacol Physi-
ol 2004;
31: 113–115.
18 Статистика Статистическое программное обеспечение версии 10.0. Col-
lege Station, StataCorp, 2007.
19 Thrift AG, Dewey HM, Macdonell RA, Mc-
Neil JJ, Donnan GA: Заболеваемость инсультом на
восточном побережье Австралии: северо-восток Mel-
Исследование заболеваемости инсультом по Борну (NEMESIS).
Ход 200 0;
31: 2087–2092.
20 Dewey HM, Sturm J, Donnan GA, Mac-
donell RA, McNeil JJ, Thrift AG: Заболеваемость
и исходы подтипов ИСК гемического инсульта:
первоначальные результаты из Северо-Восточного Мел-
Исследование заболеваемости инсультом Борна (NEMESIS).
Cerebrovasc Dis 2003;
15: 133–139.
21 Ландис Дж. Р., Кох Г. Г.: Измерение
соблюдает согласие для категориальных данных. Био-
метрики 1977;
33: 159–174.
22 Wilson JT, Hareendran A, Hendr y A, Potter
J, Bone I, Muir KW: Надежность модифицированной шкалы Ранкина
у нескольких оценщиков:
Преимущества структурированного интервью. Инсульт
2005 г .;
36: 777–781.
23 Shinohara Y, Minematsu K, Amano T,
Ohashi Y: Модифицированная шкала Рэнкина со схемой руководства ex-
и интервью
Анкета: межэкспертное соглашение и повторная оценка производительности оценки
. Цереброваск Дис
2006;
21: 271–278.
24 Bland M, Altman G: Статистические заметки: валидированные шкалы и указатели
. BMJ 2002;
324: 606–
607.
Надежность и достоверность новой китайской версии упрощенной модифицированной анкеты по шкале Рэнкина (2011) | BMC Neurology
Нашей основной целью в этом исследовании было проверить клинические свойства новой китайской версии smRSq (2011).Мы оценили надежность теста smRSq (2011) между экспертами и проверили его по сравнению с обычным интервью mRS. Мы протестировали конструктную валидность smRSq (2011) по сравнению с NIHSS и BI. Мы пришли к выводу, что китайская версия smRSq (2011 г.) отличается надежностью от хорошей до отличной, а также с хорошей достоверностью. Китайские вопросы smRSq (2011) были понятны большинству пациентов и лиц, осуществляющих уход, с небольшими пояснениями или без них, а шкалу было легко применять. Время для оценки smRSq было относительно коротким (в среднем 70 с).
Межэкспертная надежность нового китайского smRSq (2011) была от хорошей до отличной ( κ = 0,84, κ w = 0,96) и несколько лучше, чем у обычного интервью mRS ( κ = 0,76, κ w = 0,93). Сравнение китайского smRSq (2011) с традиционным mRS-интервью показало меньшую степень согласия ( κ = 0,47), но расхождения были относительно небольшими, о чем свидетельствует отличная взвешенная каппа, равная 0.91. Об аналогичной межэкспертной надежности и сравнении с обычным mRS сообщалось с использованием различных других средств, включая структурированное интервью [4, 5, 7, 13].
Проверка достоверности конструкции показала хорошие корреляции между новым китайским smRSq (2011) и NIHSS (0,82–0,83) и BI (-0,86). Этот результат согласуется с другими исследованиями валидности с использованием обычного mRS [14], английской версии smRSq (2011) [15] и нашего предыдущего исследования китайского smRSq (2010, 10).
Наши результаты показывают, что новый китайский smRSq (2011) может быть подходящим подспорьем для оценки mRS у китайских пациентов с инсультом.

 Больной может пользоваться ортопедическими приспособлениями или тростью.
Больной может пользоваться ортопедическими приспособлениями или тростью. Дееспособность не нарушена. Проблемы, возникающие после инсульта, отсутствуют, ограничений нет.
Дееспособность не нарушена. Проблемы, возникающие после инсульта, отсутствуют, ограничений нет./047/047.jpg) 15
15 2
2