Реабилитация больных перенесших инсульт: Особенности реабилитации пациентов после инсульта
Реабилитация больных, перенесших инсульт, в условиях городской поликлиники | Бугрова С.Г.
Церебральный инсульт (острое нарушение мозгового кровообращения – ОНМК) является серьезной медицинской и социальной проблемой, сопровождающейся высокой летальностью, значительной инвалидизацией и социальной дезадаптацией перенесших его пациентов [4]. Степень, характер и длительность восстановления функций, утраченных вследствие инсульта, вариабельны. Наиболее существенное улучшение в состоянии больного отмечается в первые 6 мес., в 5% случаев положительная динамика может наблюдаться в течение года. Ранняя диагностика инсульта, лечение и реабилитация больных, перенесших ОНМК, отнесены к приоритетным направлениям государственной политики в области здравоохранения. Постановлением Правительства Ивановской области утвержден план мероприятий по снижению смертности населения области от инсульта и инфаркта. Одной из поставленных задач является обретение полной независимости в каждодневной жизни в течение 3 мес. более 70% больных, выживших в 1–й месяц заболевания. Ранняя реабилитация пациентов с инсультом начинается уже в региональных сосудистых центрах, имеющих в штатах кинезотерапевта, физиотерапевта, социального работника. Каждому больному разрабатывается индивидуальная реабилитационная программа. Основная нагрузка по реабилитации больных с инсультом приходится на амбулаторно–поликлиническое звено. Более чем у половины больных, перенесших ОНМК, развиваются двигательные нарушения в виде спастических парезов. Постинсультная спастичность рассматривается как комбинированное поражение пирамидных и экстрапирамидных структур внутри головного мозга, сопровождающееся ослаблением тормозных влияний преимущественно на a–мотонейроны, которые обеспечивают движение антигравитационных мышц [6]. Характерны приведение плеча, сгибание руки в локтевом и лучезапястном суставах, приведение бедра, разгибание колена и подошвенное сгибание в голеностопном суставе. Спастичность обычно нарастает в паретичных конечностях в течение нескольких недель и месяцев, ухудшает двигательные функции, способствует развитию контрактуры и деформации конечности, затрудняет уход за обездвиженным больным и иногда сопровождается болезненными мышечными спазмами.
более 70% больных, выживших в 1–й месяц заболевания. Ранняя реабилитация пациентов с инсультом начинается уже в региональных сосудистых центрах, имеющих в штатах кинезотерапевта, физиотерапевта, социального работника. Каждому больному разрабатывается индивидуальная реабилитационная программа. Основная нагрузка по реабилитации больных с инсультом приходится на амбулаторно–поликлиническое звено. Более чем у половины больных, перенесших ОНМК, развиваются двигательные нарушения в виде спастических парезов. Постинсультная спастичность рассматривается как комбинированное поражение пирамидных и экстрапирамидных структур внутри головного мозга, сопровождающееся ослаблением тормозных влияний преимущественно на a–мотонейроны, которые обеспечивают движение антигравитационных мышц [6]. Характерны приведение плеча, сгибание руки в локтевом и лучезапястном суставах, приведение бедра, разгибание колена и подошвенное сгибание в голеностопном суставе. Спастичность обычно нарастает в паретичных конечностях в течение нескольких недель и месяцев, ухудшает двигательные функции, способствует развитию контрактуры и деформации конечности, затрудняет уход за обездвиженным больным и иногда сопровождается болезненными мышечными спазмами.
Материал и методы. Проведен анализ лечения 145 больных в возрасте 54–72 лет (в среднем 65,9±8,7 года), перенесших ОНМК и выписанных на долечивание в поликлинику №5 г. Иваново в 2007–2009 гг. Обследование включало оценку выраженности неврологического дефицита по оригинальной шкале Гусева Е.И., Скворцовой В.И. [2], степени утраты способности к самообслуживанию (шкала Бартела, шкала Ривермида).
Лечение больных с инсультом проводилось в соответствии со стандартами [4,5]. Для уменьшения выраженности двигательных нарушений у 53 больных (34 женщины,19 мужчин) применялся толперизон (Мидокалм) – мышечный релаксант центрального действия, который близок к лидокаину по химической структуре и стабилизирует мембраны нервных клеток, снижает активность спинальных нейронов, участвующих в формировании спастичности, путем ограничения потока натрия через мембрану нервных клеток. Препарат применялся в дозе 150 мг внутрь 3 раза/сут. в течение 3 мес. Для сравнения больные были подразделены на 3 группы в зависимости от выраженности двигательных расстройств при первичном осмотре. 1–ю группу (14 человек) составили пациенты с выраженными нарушениями (выраженный гемипарез), 2–ю группу (29 человек) – больные с умеренными нарушениями (моноплегия, умеренный гемипарез), 3–ю группу (10 человек) – пациенты с легкими двигательными расстройствами (легкий гемипарез, пирамидная недостаточность без слабости).

Наряду с медикаментозной терапией проводился комплекс мероприятий в условиях реабилитационного отделения поликлиники.
Обследование проводилось в 1–й день, на 45–е сутки лечения, на 90–е сутки. Полученные результаты были обработаны статистически с использованием программного пакета Statistica 6.0
Наряду с гипертонической болезнью у 6,89% пациентов в анамнезе перенесенный инфаркт миокарда, у 10,35% имелись нарушения сердечного ритма, у 12,4% – сахарный диабет, заболевания легких диагностированы у 28,97%, эндокринные нарушения – у 13,4%, заболевания суставов и позвоночника – у 78%, атеросклероз сосудов нижних конечностей и варикозная болезнь – у 26,1%, онкопатология – у 9,66%. 0,69% больных ранее перенесли каротидную эндартэктомию, 1,38% – коронарное стентирование.
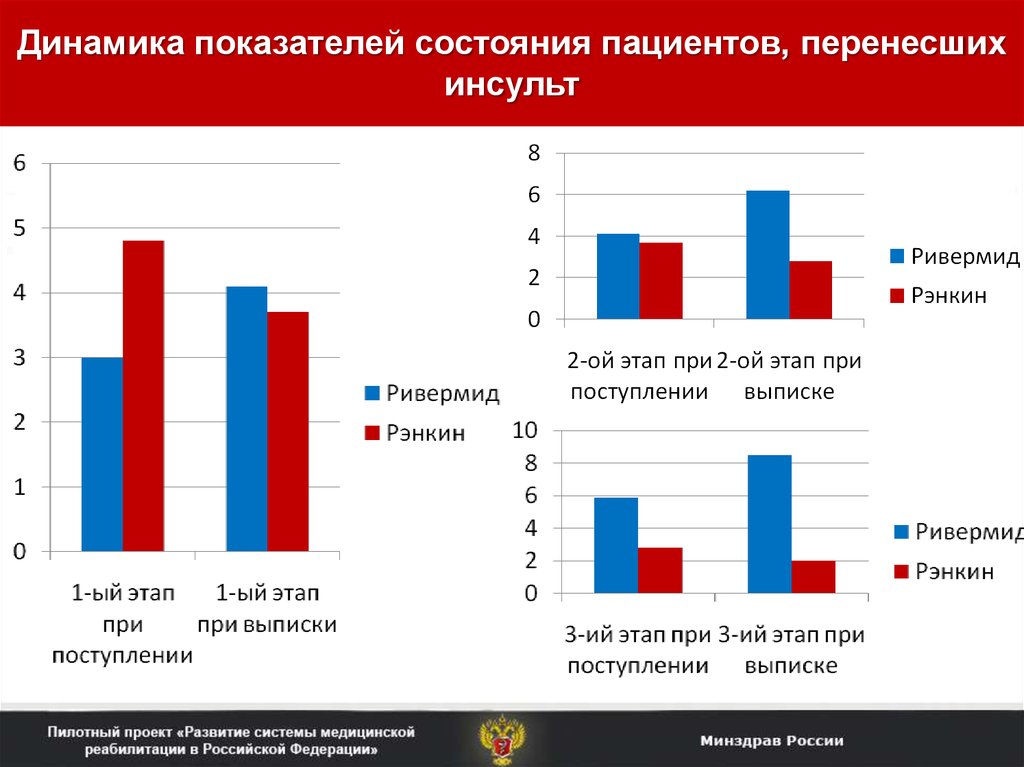
Результаты, приведенные на рисунках 1 и 2, свидетельствуют, что среди больных, принятых на амбулаторное лечение в условиях поликлиники, преобладали пациенты с атеротромботическим ишемическим инсультом.
 В клинической картине ведущее место занимали двигательные нарушения в виде спастических парезов различной степени выраженности.
В клинической картине ведущее место занимали двигательные нарушения в виде спастических парезов различной степени выраженности.В результате лечения Мидокалмом у больных всех групп отмечалось уменьшение выраженности неврологического дефицита (табл. 1). Более значительным улучшение было у больных с умеренными и легкими двигательными нарушениями (2–я и 3–я группы), достоверное различие показателей неврологического дефицита и способности к самообслуживанию выявлено уже на 45–й день лечения по сравнению с исходными (табл. 2). Достоверных различий показателей у больных в зависимости от варианта перенесенного инсульта, локализации очага и возраста больных выявлено не было. В 2 случаях отмечались побочные эффекты в виде головокружения, тошноты в начале лечения, которые постепенно ослабли и позволили продолжить лечение, не меняя дозировки. У 3 пациентов в возрасте старше 65 лет отмечено незначительное снижение АД, что было скорректировано изменением дозы гипотензивных препаратов.
 У больных 2–й и 3–й групп положительный эффект отмечался к 45–му дню лечения, у больных с выраженными двигательными нарушениями – к концу лечения.
У больных 2–й и 3–й групп положительный эффект отмечался к 45–му дню лечения, у больных с выраженными двигательными нарушениями – к концу лечения.Результаты Опросника качества жизни у больных, получавших лечение Мидокалмом, приведены на рисунке 3. Отмечено достоверное улучшение показателей шкал физического функционирования, общего здоровья, жизнеспособности, ролевого физического и социального функционирования.
Специалистами реабилитационного отделения поликлиники разработан комплекс лечебной гимнастики, направленный на тренировку движений в паретичных конечностях и предотвращение контрактур. В группе пациентов с умеренными и легкими двигательными нарушениями (51,6%) представилось возможным использование тренажеров (степпер, беговая дорожка). В группе больных с выраженными гемипарезами лечение проводилось на дому (48,4%). Использовалось лечение положением, обучение пациентов стоянию, сидению, ходьбе (с помощью дополнительных средств и самостоятельно). Одной из проблем в организации реабилитационных мероприятий, с которой мы столкнулись, явился недостаток методических рекомендаций по ЛФК в домашних условиях, наглядных материалов, памяток для больных.
 Обучение проводилось в рамках школы для больных, перенесших инсульт, как пациентов, так и их родственников в виде групповых и индивидуальных занятий.
Обучение проводилось в рамках школы для больных, перенесших инсульт, как пациентов, так и их родственников в виде групповых и индивидуальных занятий. Из физиопроцедур использовались тепловые воздействия на спастичные мышцы, а также электрическая стимуляция определенных мышечных групп. Физиолечение было проведено у 33,8% больных с учетом имеющейся сопутствующей патологии и наличия противопоказаний. Массаж мышц паретичных конечностей проводился по щадящей методике в сочетании с растиранием и неглубоким разминанием в мышцах–антагонистах в более быстром темпе. В результате реабилитационных мероприятий удалось добиться полной независимости в самообслуживании у 47% пациентов с постинсультными двигательными расстройствами. Вернулись к трудовой деятельности 18,3% больных.
Анализ результатов исследования показал высокий удельный вес двигательных расстройств у больных с инсультами, находящихся на амбулаторном лечении. Полученные результаты свидетельствуют об эффективности Мидокалма в раннем восстановительном периоде инсульта.
 Применение препарата способствует снижению выраженности спастического пареза и нормализации мышечного тонуса, увеличению степени независимости пациента в повседневной жизни. Эффективность Мидокалма сопоставима у больных как с геморрагическим, так и с ишемическим инсультом. При умеренных и легких двигательных нарушениях рекомендуется курс лечения в дозе 450 мг/сут. в 3 приема длительностью не менее 3 мес. При выраженных парезах (более 3 баллов по шкале Ashworth), по–видимому, необходимо более длительное применение препарата в более высоких дозах. В работе Stamenova P., Koytchev R., Kuhn K. et al. [8] приведены результаты исследования 97 пациентов, страдающих связанной с инсультом спастичностью (51 больной получал толперизон и 46 плацебо). В 45% случаев использовалась доза толперизона 600 мг/сут., 15% пациентов получали 900 мг/сут. В среднем пациенты получали терапию толперизоном в течение 88,3±17,1 дня и плацебо в течение 88,1±16,4 дня. По завершении исследования средние изменения исходных значений Индекса Бартела составили 5,3 в группе толперизона и 1,7 в группе плацебо, достоверно более значительное снижение степени спастичности по показателям 5–пунктовой шкалы Ашворта отмечалось в группе толперизона.
Применение препарата способствует снижению выраженности спастического пареза и нормализации мышечного тонуса, увеличению степени независимости пациента в повседневной жизни. Эффективность Мидокалма сопоставима у больных как с геморрагическим, так и с ишемическим инсультом. При умеренных и легких двигательных нарушениях рекомендуется курс лечения в дозе 450 мг/сут. в 3 приема длительностью не менее 3 мес. При выраженных парезах (более 3 баллов по шкале Ashworth), по–видимому, необходимо более длительное применение препарата в более высоких дозах. В работе Stamenova P., Koytchev R., Kuhn K. et al. [8] приведены результаты исследования 97 пациентов, страдающих связанной с инсультом спастичностью (51 больной получал толперизон и 46 плацебо). В 45% случаев использовалась доза толперизона 600 мг/сут., 15% пациентов получали 900 мг/сут. В среднем пациенты получали терапию толперизоном в течение 88,3±17,1 дня и плацебо в течение 88,1±16,4 дня. По завершении исследования средние изменения исходных значений Индекса Бартела составили 5,3 в группе толперизона и 1,7 в группе плацебо, достоверно более значительное снижение степени спастичности по показателям 5–пунктовой шкалы Ашворта отмечалось в группе толперизона.
Необходимо дальнейшее совершенствование мероприятий по реабилитации больных с инсультом в амбулаторно–поликлинических условиях.
Литература
1. Белова А.Н.Шкалы, тесты и опросники в неврологии инейрохирургии.М.–2004.–433 с.
2. Гусев Е.И., Скворцова В.И., Бурд Г.С., Гехт А.Б., и др. Метаболическая терапия ишемического инсульта: применение ноотропила // Ж. неврол. и психиатр. – 1997. – Т.97.№5–С.24–29.
3. Дамулин И.В. Постинсультные двигательные расстройства.// Consilium Medicum, 2003, т.5, №2, с.64–70.
4. Инсульт: диагностика, лечение, профилактика. Под.ред. З.А.Суслиной, М.А. Пирадова.–М.:МЕДпресс–информ,2008.–288с.
5. Снижение заболеваемости, смертности и инвалидности от инсультов в Российской Федерации.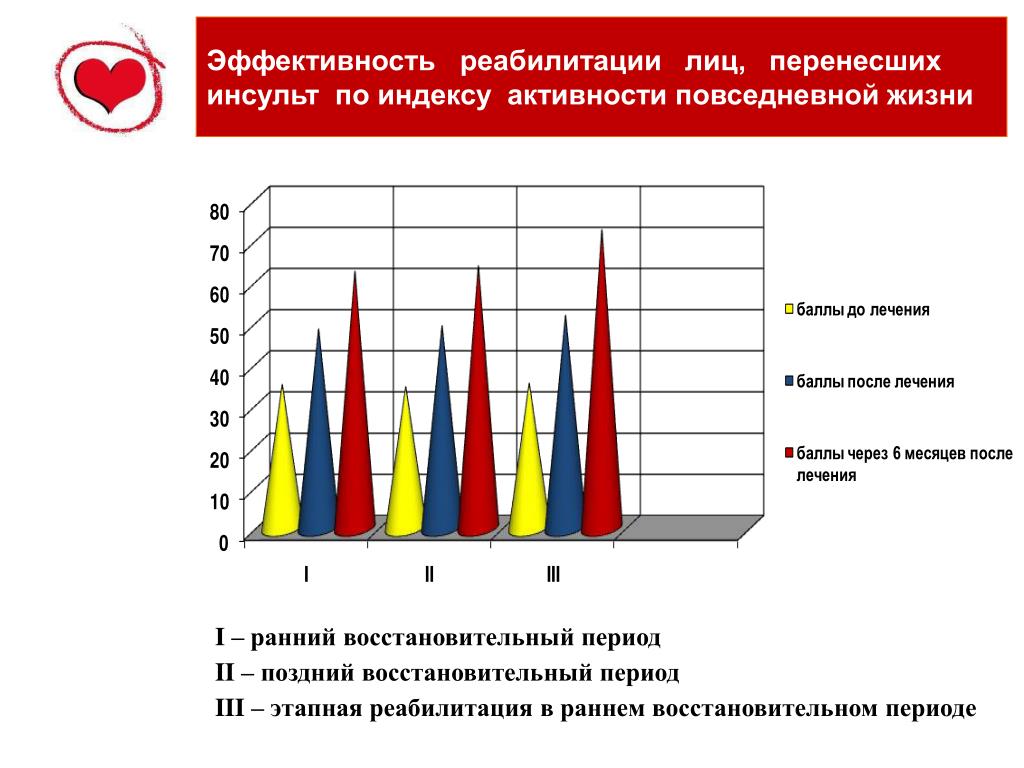 Сборник методических рекомендаций, программ, алгоритмов. Под.ред.В.И.Скворцовой.–М.:Литерра,2007.–192с.
Сборник методических рекомендаций, программ, алгоритмов. Под.ред.В.И.Скворцовой.–М.:Литерра,2007.–192с.
6. Парфенов В. А. Спастичность. В кн.: Применение ботокса (токсина ботулизма типа А) в клинической практике: руководство для врачей / под ред. О. Р. Орловой, Н. Н. Яхно. М.: Каталог, 2001. С. 91–122.
7. Feher M., Juvancz P., Szontagh M. Effect of Mydocalm in the rehabilitation of hemiparesis // Balneologia Rehailitdcio Gyogyfurdougy. 1985. Vol. 6. P. 201–205.
8. Stamenova P., Koytchev R., Kuhn K. et al. A randomized, double–blind, placebo–controlled study of the efficacy and safety of tolperisone in spasticity following cerebral stroke. European Journal of Neurology. 2005; 12: 453–461.
9. Gallichio J. E. Pharmacologic management of spasticity following stroke. // Phys Ther. 2004. Vol. 84. P. 973–981.
Реабилитация больных, перенесших инсульт, в поликлинике восстановительного лечения | #03/03
Каких пациентов следует направлять в поликлинику восстановительного лечения?
Когда следует начинать кинезотерапию?
В чем заключается профилактика повторного инсульта?
В России ежегодно фиксируется более 400 тыс. инсультов, которые подразделяются на ишемические инсульты, или церебральные инфаркты (они встречаются чаще и составляют 70—85%) и геморрагические, то есть кровоизлияние в мозг и субарахноидальное кровоизлияние. В течение первого месяца умирает 15—30% больных ишемическим инсультом и 40—60% больных геморрагическим инсультом. Таким образом, можно сказать, что через месяц в живых остается в среднем 65—80% людей, пораженных инсультом. В целом же количество пациентов, перенесших инсульт (или выживших в течение первого месяца заболевания), в России ежегодно составляет около 300 тыс. человек.
инсультов, которые подразделяются на ишемические инсульты, или церебральные инфаркты (они встречаются чаще и составляют 70—85%) и геморрагические, то есть кровоизлияние в мозг и субарахноидальное кровоизлияние. В течение первого месяца умирает 15—30% больных ишемическим инсультом и 40—60% больных геморрагическим инсультом. Таким образом, можно сказать, что через месяц в живых остается в среднем 65—80% людей, пораженных инсультом. В целом же количество пациентов, перенесших инсульт (или выживших в течение первого месяца заболевания), в России ежегодно составляет около 300 тыс. человек.
Лечение больных, перенесших инсульт, проводится в поликлиниках восстановительного лечения (реабилитационных центрах), санаториях и на дому под наблюдением врачей поликлиник. Это очень актуальная медицинская и социальная проблема, в решении которой участвуют неврологи, терапевты, физиотерапевты, логопеды, медицинские психологи и социальные работники.
Основные задачи, которые приходится решать в период лечения больных, перенесших инсульт, можно распределить следующим образом:
- восстановление (улучшение) нарушенных функций;
- бытовая и социальная адаптация к имеющемуся дефекту;
- профилактика повторного инсульта и других сердечно-сосудистых заболеваний;
- лечение сопутствующих заболеваний;
Восстановительному лечению в условиях специализированной поликлиники (реабилитационного центра) подлежат больные, которые после инсульта имеют двигательные, чувствительные или речевые нарушения. Длительность лечения определяется сроками восстановления нарушенных функций: максимальное улучшение двигательных функций отмечается в течение 6 месяцев, восстановление бытовых навыков и трудоспособности — в течение года, речевых функций — на протяжении 2—3 лет с момента развития инсульта.
Длительность лечения определяется сроками восстановления нарушенных функций: максимальное улучшение двигательных функций отмечается в течение 6 месяцев, восстановление бытовых навыков и трудоспособности — в течение года, речевых функций — на протяжении 2—3 лет с момента развития инсульта.
В поликлинику восстановительного лечения направляются пациенты, сохранившие способность к самообслуживанию и самостоятельному передвижению и не имеющие соматических противопоказаний, а также выраженных когнитивных нарушений, которые затрудняют активную реабилитацию или даже делают ее невозможной.
Двигательные нарушения — одно из наиболее частых и тяжелых последствий инсульта. Восстановление двигательных функций наблюдается у большинства больных; при адекватной лечебной гимнастике пациенты даже с грубыми двигательными дефектами начинают самостоятельно стоять и ходить, по крайней мере, через 3—6 месяцев после заболевания. Отсутствие положительного эффекта через 3—6 месяцев может быть вызвано утратой глубокой чувствительности в паретичных конечностях и (или) низкой мотивацией больного к реабилитации, что часто наблюдается при поражении недоминантного (правого у правшей) полушария головного мозга и сочетается с недооценкой тяжести заболевания или его игнорированием (анозогнозией).
Огромное значение при утрате двигательной активности имеет кинезотерапия, которая в виде пассивных движений в парализованных конечностях должна проводиться уже в первые дни после инсульта, после стабилизации неврологических нарушений и при отсутствии противопоказаний к физическим нагрузкам. Активные движения в паретичных конечностях необходимо тренировать сразу после их появления, постепенно увеличивая нагрузку. В дальнейшем следует обучать больных ходьбе, используя сначала специальные приспособления, а затем палочку. Если восстановительные упражнения дают хороший результат, то сначала надо освоить ходьбу по комнате, а затем спуск и подъем по лестнице, прогулки вне дома. Очень важно уделять внимание обучению самостоятельному приему пищи, одеванию и раздеванию, чистке зубов и другим навыкам, необходимым в быту. При проведении кинезотерапии необходимо постепенно увеличивать физические нагрузки. Если у больного имеется сочетанная кардиальная патология (например, аритмия или стенокардия), то реабилитационная программа должна быть составлена с кардиологом.
Если существенного восстановления двигательных функций в руке не происходит, больному рекомендуется носить фиксирующую косынку, во избежание свободного свисания руки, которое может привести к подвывиху в плечевом суставе и развитию периартериита. Для предупреждения контрактуры и деформации лучезапястного и(или) голеностопного суставов (а также при их развитии) можно использовать ортопедическое приспособление для голени и специальную шину, удерживающую лучезапястный сустав и кисть в правильном положении.
Для больных, перенесших инсульт, характерно резкое снижение моторной активности, обусловленное наличием парезов и частыми сочетанными заболеваниями сердечно-сосудистой системы. Гипокинезия приводит к уменьшению проприоцептивной импульсации и утрате двигательных навыков, что способствует дальнейшему ухудшению функции сердечно-сосудистой системы, снижению общей адаптационной способности организма. Поэтому трудно переоценить роль кинезотерапии, которая может включать как групповые, так и индивидуальные занятия.
Для диагностики патологии двигательной сферы в условиях поликлиники восстановительного лечения можно использовать комплекс «Биомеханика», с помощью которого проводятся функциональные исследования опорно-двигательной системы. Комплекс дает возможность исследовать двигательную составляющую по классическим методам с использованием таких двигательных тестов, как ходьба или основная стойка. Полученная функциональная информация позволяет оценить двигательный стереотип больного, перенесшего инсульт. На основании двигательных параметров пациента составляется индивидуальная программа восстановления нарушенной двигательной функции. В составе комплекса «Биомеханика» имеются специализированные тренажеры и мультимедийные игры, основанные на биологической обратной связи по зрительному и слуховому каналу. Пациент управляет «картинкой» на экране компьютера, совершая определенные телодвижения. Врач-оператор со своего рабочего места может менять режим работы, чтобы помочь больному справиться с определенной реабилитационной задачей. Сложность реабилитационной задачи повышается автоматически по мере ее выполнения.
Сложность реабилитационной задачи повышается автоматически по мере ее выполнения.
При двигательных нарушениях, если нет выраженной спастичности, можно использовать электромиостимуляцию паретичных мышц синусоидальными модулированными токами, а также их избирательный массаж.
У большинства больных после перенесенного инсульта наблюдается повышение мышечного тонуса по типу спастичности в паретичных конечностях. Во многих случаях спастичность ухудшает двигательные функции и нередко сопровождается болезненными мышечными спазмами в паретичных конечностях, способствует развитию контрактуры и деформации конечности, затрудняет уход за обездвиженным больным. В таких случаях снижение спастичности может улучшить двигательные функции, предупредить или уменьшить контрактуры и деформации конечностей, облегчить уход за больным.
Для лечения спастичности можно использовать пероральные антиспастические средства. Курс начинают с минимальной дозы препарата, постепенно ее повышая до появления результата. Баклофен применяют по 10—50 мг/сут., тизанидин (сирдалуд) — по 6—30 мг/сут. и толперидон (мидокалм) — по 150—300 мг/сут. Антиспастические средства в большинстве случаев снижают мышечный тонус в паретичных конечностях и снимают болезненные мышечные спазмы, способствуя проведению физиотерапии и предупреждая развитие контрактур. Однако повышение дозы антиспастических средств с целью уменьшения спастичности нередко приводит к значительной мышечной слабости и седативному действию, что ограничивает их применение у многих ходячих больных.
Баклофен применяют по 10—50 мг/сут., тизанидин (сирдалуд) — по 6—30 мг/сут. и толперидон (мидокалм) — по 150—300 мг/сут. Антиспастические средства в большинстве случаев снижают мышечный тонус в паретичных конечностях и снимают болезненные мышечные спазмы, способствуя проведению физиотерапии и предупреждая развитие контрактур. Однако повышение дозы антиспастических средств с целью уменьшения спастичности нередко приводит к значительной мышечной слабости и седативному действию, что ограничивает их применение у многих ходячих больных.
В последние годы для лечении спастичности практикуется внутримышечное введение ботулинического токсина типа А (ботокс или диспорт). Локальное введение препарата вызывает частичную блокаду нервно-мышечного синапса и расслабление мышцы в течение 3—6 месяцев, что обеспечивает возможности для успешной физиотерапии.
В качестве физиотерапевтических методов также используют:
- парафиновые или озокеритовые аппликации на паретичную конечность в виде носка, чулка или перчатки;
- постоянное магнитное поле на мышцы сгибатели руки и разгибатели ноги, по 15-20 мин;
- точечный массаж по тормозной методике, ежедневно или через день;
- иглорефлексотерапию по методике, направленной на снижение спастичности.

В ряде случаев положительный эффект достигается после придания определенного положения паретичной конечности (например, с помощью лангетки, специальных приспособлений для ходьбы, ортопедической обуви).
У 5—10% больных с постинсультным гемипарезом развивается боль и отек в паретичной руке или реже в ноге, что обычно обусловлено поражением суставов и (или) периферическими сосудистыми нарушениями. Если движения в суставах паретичной конечности сопровождаются болью, то рекомендуют активные и пассивные движения в суставе, вызывающие только минимальные болевые ощущения, постепенно увеличивая их объем. Для уменьшения болевых ощущений перед гимнастикой можно использовать локально обезболивающие мази и гели (финалгель) или компрессы с новокаином и димексидом, массаж и рефлексотерапию. При длительных и выраженных болях назначают курс нестероидных анальгетиков (мовалис — для быстрого снятия болевого синдрома 1,5 мл (15 мг) в/м 1—2 дня, затем переход на таблетированную форму — 7,5 мг 1 раз в день), сочетая их с антидепрессантами в небольших дозах (например, амитриптилин по 25—75 мг на ночь или 2—3 раза в сутки) и (или) противоэпилептическими средствами (например, карбамазепин по 200—600 мг/сут. или клоназепам по 0,5—2 мг/сут.). Для уменьшения отека паретичной конечности рекомендуют лечение положением (периодический подъем руки или ноги), применяют пневматические перчатки или носки.
или клоназепам по 0,5—2 мг/сут.). Для уменьшения отека паретичной конечности рекомендуют лечение положением (периодический подъем руки или ноги), применяют пневматические перчатки или носки.
Боль в паретичных конечностях после инсульта может иметь и центральное происхождение вследствие поражения чувствительных проводников и центров головного мозга, чаще всего зрительного бугра. Центральные боли обычно появляются спустя некоторое время после развития инсульта. Они, как правило, постоянны, усиливаются при эмоциональном напряжении, сочетаются с измененным восприятием чувствительности (дизестезией) в заинтересованных отделах тела. Облегчение при сильной центральной боли достигается введением раствора тиопентал-натрия в дозе 75—300 мг. Иногда помогают антидепрессанты (например, 25—75 мг амитриптилина на ночь), противоэпилептические средства (например, клоназепам 0,5—2 мг/сут.) и рефлексотерапия.
Если у больного после инсульта имеются речевые нарушения (афазия, дизартрия), его направляют на логопедические занятия. Такой человек должен слышать речь других людей, слушать радио, телевизор и иметь возможность общаться с окружающими. Необходимо стимулировать больного к самостоятельной речи даже при грубом ее нарушении. Большое значение имеет чтение вслух, письмо, рисование и другие занятия, стимулирующие речевые функции. Эффективность восстановления речевых функций во многом определяется мотивацией больного и его активным участием в реабилитационном процессе, поэтому так важны для него положительные отзывы врача и окружающих людей относительно его успехов.
Такой человек должен слышать речь других людей, слушать радио, телевизор и иметь возможность общаться с окружающими. Необходимо стимулировать больного к самостоятельной речи даже при грубом ее нарушении. Большое значение имеет чтение вслух, письмо, рисование и другие занятия, стимулирующие речевые функции. Эффективность восстановления речевых функций во многом определяется мотивацией больного и его активным участием в реабилитационном процессе, поэтому так важны для него положительные отзывы врача и окружающих людей относительно его успехов.
В условиях поликлиники восстановительного лечения проводятся индивидуальные и (или) групповые занятия с логопедом не реже 3 раз в неделю. При любой афазии необходимо работать над пониманием речи, чтением, письмом и над восстановлением свободного высказывания и смысловой структуры речи. Желателен постоянный контакт логопеда с семьей больного, чтобы члены семьи, следуя рекомендациям логопеда, могли помогать больному в выполнении домашних заданий и в освоении некоторых видов речевой деятельности.
Нарушение когнитивных функций, снижение памяти и интеллекта наблюдается у значительной части больных после перенесенного инсульта, они сильно затрудняют занятия в реабилитационном центре, а также бытовую и социальную адаптацию больного после инсульта.
С целью улучшения речевых и когнитивных функций можно использовать средства, повышающие метаболические процессы и кровоснабжение в головном мозге. В этом случае применяют один из нейротропных препаратов или комбинацию нескольких лекарственных средств, однако следует избегать комбинации двух или нескольких вазоактивных препаратов. Эти курсы целесообразно проводить в условиях дневного стационара, входящего в состав поликлиники восстановительного лечения. Церебролизин рекомендуется в больших дозах (10—50 мл/сут.), вводимых на 100—200 мл физиологического раствора в/в капельно (в течение 60—90 мин) на протяжении 10—15 дней. Пирацетам (ноотропил) используется внутрь по 1,2—4,8 г/сут. Гаммалон — по 20 мл 5%-ного раствора на 300 мл физиологического раствора в/в капельно в течение 10—15 дней. Глиатилин назначается внутрь по 0,8—2,4 г/сут. Семакс — эндоназально в дозе 12—24 мг (по 2—4 капли раствора). Нимодипин (нимотоп) — внутрь по 30—60 мг 3—4 раза в сутки. Винпоцетин (кавинтон) применяется внутрь по 5 мг 3 раза в сутки. Ницерголин (сермион) используется внутрь по 5 мг 3—4 раза в сутки. Циннаризин (стугерон) назначается внутрь по 25 мг 3—4 раза в сутки. Инстенон — по 2—4 мл в/в капельно (в течение 3 часов) на протяжении 3—5 суток. Никардипин используется внутрь по 20 мг 2 раза в сутки.
Глиатилин назначается внутрь по 0,8—2,4 г/сут. Семакс — эндоназально в дозе 12—24 мг (по 2—4 капли раствора). Нимодипин (нимотоп) — внутрь по 30—60 мг 3—4 раза в сутки. Винпоцетин (кавинтон) применяется внутрь по 5 мг 3 раза в сутки. Ницерголин (сермион) используется внутрь по 5 мг 3—4 раза в сутки. Циннаризин (стугерон) назначается внутрь по 25 мг 3—4 раза в сутки. Инстенон — по 2—4 мл в/в капельно (в течение 3 часов) на протяжении 3—5 суток. Никардипин используется внутрь по 20 мг 2 раза в сутки.
Депрессия возникает более чем у половины больных после перенесенного инсульта. Она значительно затрудняет процесс реабилитации пациента, осложняет уход за ним и его контакт с окружающими людьми. Депрессия может проявляться головными болями и другими неврологическими нарушениями, которые иногда ошибочно расцениваются как прогрессирование сосудистого поражения головного мозга. Для лечения депрессивного синдрома используются психотерапия и (или) антидепрессанты, например амитриптилин по 25—75 мг/сут. на ночь или 2—3 раза в день, тианептин (коаксил) по 25—37,5 мг/сут. или флуоксетин (прозак) по 20 мг 1 раз в день.
на ночь или 2—3 раза в день, тианептин (коаксил) по 25—37,5 мг/сут. или флуоксетин (прозак) по 20 мг 1 раз в день.
Большое значение имеет психологическая атмосфера в семье. Родственникам больного или лицам, осуществляющим уход за ним, рекомендуется поощрять больного в его занятиях — тренировке движений, речи, бытовых и профессиональных навыков, стимулировать его к выполнению всего того, что он может сделать, дать ему почувствовать свою самостоятельность, возможность бытовой и социальной реабилитации. Если вследствие неврологических нарушений больной не может вернуться к прежней профессии, то нужно помочь ему овладеть новыми навыками и интересами, учитывая его возможности. Это важное условие социальной адаптации больного при его наблюдении в поликлинике восстановительного лечения.
Психотерапия направлена на уменьшение психических расстройств, повышение устойчивости к стрессам и формирование адекватного отношения к болезни, способствующего улучшению самочувствия. Проводятся индивидуальные собеседования с больным и его родственниками, динамическое наблюдение за поведением больного, которые позволяют определить уровень и характер эмоционально-волевых расстройств, выбрать методы их коррекции.
Проводятся индивидуальные собеседования с больным и его родственниками, динамическое наблюдение за поведением больного, которые позволяют определить уровень и характер эмоционально-волевых расстройств, выбрать методы их коррекции.
У части больных после инсульта развиваются эпилептические припадки, что чаще наблюдается после перенесенного лобарного внутримозгового кровоизлияния, субарахноидального кровоизлияния или коркового ишемического инсульта. В этих случаях назначают противоэпилептические средства; обычно начинают лечение с карбамазепина (финлепсина) по 600 мг/сут. или фенитоина (дифенина) по 300 мг/сут., возможно использование и других препаратов.
Одним из важных направлений лечения больных, перенесших инсульт, является профилактика повторного инсульта, риск которого составляет 10—16% в течение первого года, что в 15 раз выше, чем в общей популяции той же возрастной группы. Через год вероятность повторного инсульта снижается до 5% на последующие четыре года. Риск повторного инсульта повышен при наличии артериальной гипертонии, аритмии, патологии клапанов сердца, застойной сердечной недостаточности, сахарного диабета.
Риск повторного инсульта повышен при наличии артериальной гипертонии, аритмии, патологии клапанов сердца, застойной сердечной недостаточности, сахарного диабета.
Профилактика повторного инсульта должна начинаться как можно скорее и продолжаться постоянно. Она направлена на корригируемые факторы риска развития инсульта. Большую роль здесь играет здоровый образ жизни, предусматривающий отказ от курения или уменьшение количества выкуриваемых сигарет, отказ от употребления наркотиков и злоупотребления алкоголем, адекватную физическую активность и снижение избыточного веса. Необходимо уменьшить потребление продуктов, содержащих большое количество холестерина (сливочное масло, яйца, жирный творог и др.), и включить в рацион свежие овощи и фрукты.
Артериальная гипертония — наиболее значимый корригируемый фактор риска инсульта. Для больных, перенесших инсульт на фоне артериальной гипертонии, необходима длительная гипотензивная терапия с целью вторичной профилактики инсульта и других сердечно-сосудистых заболеваний. В последние годы убедительно доказана эффективность гипотензивной терапии, основанной на периндоприле, в профилактике повторного инсульта, инфаркта миокарда, когнитивных нарушений и инвалидности. Комбинация периндоприла (4 мг/сут.) и индапамида (2,5 мг/сут.), применяемая в течение 5 лет, предупреждает 1 повторный инсульт у 14 больных, перенесших инсульт или транзиторную ишемическую атаку.
В последние годы убедительно доказана эффективность гипотензивной терапии, основанной на периндоприле, в профилактике повторного инсульта, инфаркта миокарда, когнитивных нарушений и инвалидности. Комбинация периндоприла (4 мг/сут.) и индапамида (2,5 мг/сут.), применяемая в течение 5 лет, предупреждает 1 повторный инсульт у 14 больных, перенесших инсульт или транзиторную ишемическую атаку.
При этом гипотензивную терапию следует проводить с осторожностью, во избежание значительного снижения артериального давления и гипоперфузии головного мозга, особенно у пожилых больных с окклюзирующим поражением церебральных и прецеребральных артерий. В поликлинике восстановительного лечения до начала гипотензивной теарпии целесообразно исследовать прецеребральные и церебральные артерии методом дуплексного сканирования и транскраниальной допплерографии, чтобы установить наличие и степень окклюзирующего поражения и на основании этого оценить риск церебральных осложнений гипотензивной терапии. Повторные исследования церебральной гемодинамики на фоне приема гипотензивных препаратов позволяют определить оптимальный уровень снижения артериального давления, который у больных, перенесших инсульт на фоне длительной артериальной гипертонии, может быть существенно выше обычных нормальных значений АД. Однако в целом гипотензивная терапия рекомендуется даже пожилым больным при повышении артериального давления и атеросклеротического поражения церебральных артерий.
Повторные исследования церебральной гемодинамики на фоне приема гипотензивных препаратов позволяют определить оптимальный уровень снижения артериального давления, который у больных, перенесших инсульт на фоне длительной артериальной гипертонии, может быть существенно выше обычных нормальных значений АД. Однако в целом гипотензивная терапия рекомендуется даже пожилым больным при повышении артериального давления и атеросклеротического поражения церебральных артерий.
Одно из ведущих направлений во вторичной профилактике ишемического инсульта занимает антиагрегантная терапия. Для профилактики инсульта больным, перенесшим транзиторную ишемическую атаку или ишемический инсульт, рекомендуется в течение 1—2 лет или постоянно принимать ангиагреганты: ацетилсалициловую кислоту (аспирин), клопидогрель (плавикс), дипиридамол (курантил) или тиклопидин (тиклид).
Ацетилсалициловую кислоту можно использовать в дозе от 80 до 1300 мг/сут., дозы от 80 до 325 мг/сут. считаются более предпочтительными из-за меньшего риска осложнений со стороны желудочно-кишечного тракта. Регулярный прием ацетилсалициловой кислоты снижает риск развития инсульта, инфаркта миокарда или сосудистой смерти в среднем на 13%. При использовании малых (менее 160 мг), средних (160—325 мг) и высоких (500—1500 мг) доз ацетилсалициловой кислоты не отмечено существенных различий в частоте развития инсульта, но при использовании малых доз реже встречались осложнения со стороны желудочно-кишечного тракта.
Регулярный прием ацетилсалициловой кислоты снижает риск развития инсульта, инфаркта миокарда или сосудистой смерти в среднем на 13%. При использовании малых (менее 160 мг), средних (160—325 мг) и высоких (500—1500 мг) доз ацетилсалициловой кислоты не отмечено существенных различий в частоте развития инсульта, но при использовании малых доз реже встречались осложнения со стороны желудочно-кишечного тракта.
Тиклопидин (тиклид) применяется по 250 мг 2 раза в сутки. Сравнение эффективности тиклопидина и ацетилсалициловой кислоты показало, что при использовании тиклопидина отмечается тенденция к более значительному снижению инсульта, инфаркта миокарда или сосудистой смерти. Сопоставление побочных эффектов этих препаратов показало, что прием ацетилсалициловой кислоты чаще осложняется желудочно-кишечным дискомфортом и кровотечением, использование тиклопидина — угнетением функции костного мозга (кроветворения), сыпью и диареей. Поскольку лечение тиклопидином часто приводит к лейкопении, при его приеме требуется регулярный контроль общего анализа крови (каждые 2 недели в течение первых 3 месяцев лечения) и отмена препарата при развитии осложнений. Из-за возможности угнетения функции костного мозга тиклопидин сегодня редко назначается, однако его не следует отменять у тех пациентов, которые уже принимают препарат в течение длительного времени без побочных эффектов.
Из-за возможности угнетения функции костного мозга тиклопидин сегодня редко назначается, однако его не следует отменять у тех пациентов, которые уже принимают препарат в течение длительного времени без побочных эффектов.
Клопидогрель (плавикс) представляет собой новое производное тиенопиридина, химически сходное с тиклопидином, но не имеющее негативных воздействий на функцию костного мозга. 75 мг клопидогреля более эффективно снижает частоту инсульта, инфаркта миокарда или острой сосудистой смерти, чем 325 мг ацетилсалициловой кислоты. Проспективное наблюдение почти 20 тыс. больных, перенесших ишемический инсульт, инфаркт миокарда или имеющих заболевание периферических артерий, показало, что в группе пациентов, получавших 75 мг клопидогреля в сутки, инсульт, инфаркт миокарда или острая сосудистая смерть возникают достоверно реже (5,32% в год), чем в группе, получавшей 325 мг ацетилсалициловой кислоты (5,83%). При этом установлено, что клопидогрель сравнительно безопасен при длительном приеме и хорошо переносится больными. В частности, нейтропения, часто возникающая как осложнение от приема тиклопидина, наблюдалась только в 0,10% случаев при приеме клопидогреля и в 0,17% случаев при приеме ацетилсалициловой кислоты.
В частности, нейтропения, часто возникающая как осложнение от приема тиклопидина, наблюдалась только в 0,10% случаев при приеме клопидогреля и в 0,17% случаев при приеме ацетилсалициловой кислоты.
В настоящее время клопидогрель, как и ацетилсалициловая кислота, представляют собой препараты выбора среди антиагрегантов для вторичной профилактики инсульта. Клопидогрель необходим в тех случаях, когда противопоказана ацетилсалициловая кислота или имеются побочные эффекты от ее использования либо сердечно-сосудистое заболевание возникло у больного, принимавшего ацетилсалициловую кислоту.
Еще одним антиагрегантом, используемым для вторичной профилактики инсульта, является дипиридамол (курантил). Комбинация ацетилсалициловой кислоты по 50 мг/сут. и дипиридамола по 400 мг/сут. снижает риск развития инсульта на 22,1%, однако при этом достоверно не уменьшается частота развития инсульта со смертельным исходом.
Для больных с мерцательной аритмией, внутрижелудочковым тромбом, искусственным клапаном сердца и другой патологией, опасной повторением кардиоэмболического инсульта, при отсутствии противопоказаний рекомендуется прием непрямого антикоагулянта варфарина в дозе, обеспечивающей существенное снижение уровня протромбина в крови (снижение протромбинового индекса до 50—60% или повышение международного нормализующего коэффициента до 3,0—4,0). Средние дозы варфарина составляют около 5 мг/сут. В тех случаях когда использование варфарина противопоказано или невозможно регулярное исследование уровня протромбина в крови, рекомендуется прием антиагрегантов.
Средние дозы варфарина составляют около 5 мг/сут. В тех случаях когда использование варфарина противопоказано или невозможно регулярное исследование уровня протромбина в крови, рекомендуется прием антиагрегантов.
Вопрос о каротидной эндартерэктомии обсуждается при выявлении стеноза внутренней сонной артерии с целью предупреждения повторного инсульта. В настоящее время каротидная эндартерэктомия рекомендуется при выраженном (сужении 70—99% диаметра) стенозе внутренней сонной артерии у больных, перенесших транзиторную ишемическую атаку или малый инсульт. Она целесообразна и при умеренной степени (сужении 30—69% диаметра) стеноза внутренней сонной артерии у больных малым инсультом, а также при выраженной либо умеренной степени ее стеноза у больных с легким или умеренным неврологическим дефицитом после перенесенного инсульта. При выборе хирургической или консервативной тактики ведения больного, перенесшего инсульт и имеющего стеноз внутренней сонной артерии, следует учитывать поражение другой сонной и церебральных артерий, выраженность патологии коронарных артерий и наличие других соматических заболеваний.
Над больными, перенесшими инсульт, довлеет в два раза более высокий риск смерти, чем в общей популяции той же возрастной группы. Это вызвано не только высокой частотой повторного инсульта со смертельным исходом, но и риском соматических заболеваний (инфаркта миокарда, пневмонии, заболеваний почек и др.), которые возникают у больных после инсульта вследствие артериальной гипертонии, патологии коронарных артерий, нарушений сердечного ритма, сахарного диабета. Развитие соматических заболеваний чаще приводит к смерти больного, чем повторный инсульт, поэтому их предупреждение и лечение составляет не менее важное направление ведения больных, перенесших инсульт. Поэтому при реабилитации больного, перенесшего инсульт, в условиях поликлиники восстановительного лечения назначение лекарственных препаратов и реабилитационные мероприятия должны быть согласованы с терапевтом и кардиологом. Лечение соматических заболеваний может существенно улучшить качество жизни больных и уменьшить риск различных заболеваний сердечно-сосудистой системы.
Т. Т. Батышева, кандидат медицинских наук
В. А. Парфенов, доктор медицинских наук
Поликлиника восстановительного лечения № 7, ММА им. И. М. Сеченова, Москва
Обратите внимание!
- Несмотря на выраженные речевые нарушения, пациент должен иметь возможность общаться с окружающими. Положительные отзывы врача и окружающих людей являются очень важной мотивацией к его активному участию в реабилитационном процессе.
- Риск развития повторного инсульта у больных, уже перенесших сосудистую катастрофу, в 15 раз выше, чем в общей популяции той же возрастной группы.
- Гипотензивная терапия пациентам, перенесшим инсульт, должна проводиться очень осторожно во избежание гипоперфузии головного мозга, особенно у пожилых больных с окклюзирующим поражением церебральных и прецеребральных артерий.
Услуги по реабилитации после инсульта — Emory Healthcare
Healthconnection℠ 404-778-7777
Зарегистрированные медсестры могут помочь вам найти подходящее место или специалиста.
Звоните по телефону 404-778-7777
с 7:30 до 18:00. ЭСТ (пн-пт)
- Домашний
- Центры и программы
- Реабилитационные услуги
- Восстановление и последующие действия
- Реабилитация после инсульта
Мы знаем, что восстановление после инсульта — одна из самых сложных задач, с которыми когда-либо сталкивался человек. Исследования показывают, что то, какое лечение и реабилитация человек решит пройти, может иметь решающее значение для того, насколько хорошо и как быстро он выздоровеет.
Центр лечения инсульта Эмори является сертифицированным Совместной комиссией комплексным центром лечения инсульта, что делает реабилитационную больницу Эмори лучшим выбором для пациентов, перенесших инсульт, в штате. Как специализированная реабилитационная больница, мы известны и высоко ценим наш медицинский опыт и заботу о сострадании.
Как специализированная реабилитационная больница, мы известны и высоко ценим наш медицинский опыт и заботу о сострадании.
Наши программы предлагают следующее, чтобы помочь вам или близкому вам человеку оправиться от инсульта:
- Экспертное медицинское обслуживание: Наша медицинская команда имеет опыт лечения всех типов инсульта, от легких до самых сложных.
- Специализированная реабилитационная команда: наши пациенты работают с преданной и всесторонней командой специализированного и сертифицированного медицинского и реабилитационного персонала, включая врачей; медсестры; физические, профессиональные и респираторные терапевты; логопеды; кейс-менеджеры; диетологи; нейропсихологи; и другие медицинские работники по мере необходимости.
- Бригады под руководством врачей: Каждую медицинскую бригаду возглавляет физиотерапевт — врач, специализирующийся на физической медицине (лечение нервов, мышц, костей и головного мозга) и реабилитации.
 Кроме того, физиотерапевт ежедневно посещает каждого пациента.
Кроме того, физиотерапевт ежедневно посещает каждого пациента. - Индивидуальные планы лечения: Наше медицинское обслуживание и реабилитация адаптированы к конкретным потребностям и целям каждого человека.
- Таргетная терапия: наши специализированные программы помогают пациентам восстановить сильные стороны и навыки, в том числе уверенность и независимость
- .
Пациенты, перенесшие инсульт, могут рассчитывать на нас в следующем:
- Плавный переход к реабилитации: Наши сотрудники тесно сотрудничают с пациентами, их семьями и направляющей больницей, чтобы обеспечить плавный переход в нашу реабилитационную больницу.
- Заботливая среда: уход предоставляется в безопасной, поддерживающей и сочувствующей среде, в которой потребности наших пациентов всегда стоят на первом месте.
- Образование и обучение: Чтобы подготовить пациентов и их семьи к будущей жизни, мы предлагаем ряд программ обучения и поддержки.

- Исключительные результаты: В целом, согласно национальным показателям, наши пациенты имеют больше шансов на улучшение состояния во время пребывания у нас и могут работать на более высоком уровне по возвращении домой.
- социальная информация, если применимо
Реабилитация после инсульта | Техасская реабилитационная больница Арлингтона
Дом | Виды ухода | Реабилитация после инсульта
Наша программа лечения инсульта состоит из опытной команды профессионалов, которые оказывают специализированную помощь, чтобы помочь людям восстановить функции после физических и психологических последствий инсульта. Благодаря интенсивной терапии наша команда стремится обеспечить максимально полное и оптимальное восстановление.
Элементы программы лечения инсульта включают, но не ограничиваются:
- Профилактика, распознавание, оценка и лечение состояний, связанных с инсультом и его осложнениями.

- Состояния могут включать дисфункцию кишечника и мочевого пузыря, тревогу, депрессию, снижение физической формы, дисфагию, трудности с преодолением трудностей, падения, проблемы с кровяным давлением, пролежни и повторный инсульт.
Чтобы помочь пациентам максимально восстановить функциональные возможности после инсульта, наша междисциплинарная команда клиницистов работает с каждым пациентом индивидуально. Мы реализуем план лечения, предназначенный для максимизации потенциала и дополнения медицинских вмешательств, обеспечивая междисциплинарный командный подход к лечению.
Наша специализированная программа лечения инсульта сертифицирована Комиссией по аккредитации реабилитационных учреждений (CARF)
Стационарная реабилитация играет важную роль в восстановлении после инсульта
Мы стремимся предоставлять квалифицированную и сострадательную помощь для восстановления после инсульта.
Ранние действия имеют решающее значение, если у пациента случился инсульт. Реабилитация после инсульта должна начинаться как можно раньше после инсульта, когда состояние здоровья пациента стабилизируется и врачи принимают профилактические меры против повторных инсультов и осложнений.
Реабилитация после инсульта должна начинаться как можно раньше после инсульта, когда состояние здоровья пациента стабилизируется и врачи принимают профилактические меры против повторных инсультов и осложнений.
Наша интенсивная стационарная программа предусматривает индивидуальный план лечения для каждого пациента и постоянный уход с целью подготовки людей к возвращению домой самостоятельно или с помощью членов семьи или других медицинских работников.
Исследования показывают, что стационарная реабилитация приводит к:
- Быстрому возвращению домой
- Кратковременное пребывание
- Минимизация повторной госпитализации
Рекомендации Американской ассоциации по борьбе с инсультом (ASA)
Основные рекомендации Руководства по реабилитации и восстановлению после инсульта у взрослых ASA содержат передовой клинический опыт для взрослых, выздоравливающих после инсульта. Прежде всего, в рекомендациях говорится, что, когда это возможно, выздоровление должно происходить в реабилитационном стационаре неотложной помощи в учреждении квалифицированного сестринского ухода (SNF).
Руководство предполагает, что существуют убедительные доказательства того, что организованная междисциплинарная помощь при инсульте, например, предоставляемая стационарным реабилитационным центром (IRF), не только снижает уровень смертности и вероятность стационарного ухода и длительной нетрудоспособности, но также ускоряет выздоровление. и повышает независимость в повседневной жизни. С этой целью все пациенты, которые могут соответствовать требованиям, должны быть оценены клиницистами IRF, чтобы можно было обеспечить надлежащий уровень ухода за каждым пациентом. Согласно самим руководящим принципам, «постоянство результатов в пользу направления IRF предполагает, что перенесшие инсульт, которые имеют право на услуги IRF, должны получать эту помощь, а не помощь на основе SNF».
К каждому пациенту относятся с достоинством, уважением и сочувствием. Пациенты, госпитализированные в IRF, получают специализированную интенсивную терапию и сестринскую помощь для медицинских и функциональных нужд, что должно предотвратить возможность перевода на менее интенсивный уровень помощи.
Наша программа по борьбе с инсультом помогает улучшить навыки, уделяя особое внимание:
- Повышению вашей независимости, здоровья и мобильности
- Повседневная деятельность, такая как прием пищи, одевание, уход за собой, купание и ведение домашнего хозяйства
- Лечение кишечника и мочевого пузыря
- Общение через устную и письменную речь
- Проглатывание
- Улучшение памяти и суждения
- Речь и язык
- Баланс и координация
- Психологическая коррекция
- Самообраз
Предоставление лечения и интенсивность обслуживания определяются как часть индивидуального плана лечения и обычно включают комбинацию 30–60-минутных сеансов терапии в течение трех или более часов в большинстве дней.
Therapy Team
Пациент, его семья, близкие и лица, осуществляющие уход, являются самой важной частью нашей реабилитационной команды. Наша команда медицинских работников будет работать вместе с пациентом и лицами, ухаживающими за пациентом, над восстановлением после инсульта.
Наша команда медицинских работников будет работать вместе с пациентом и лицами, ухаживающими за пациентом, над восстановлением после инсульта.
Наша междисциплинарная реабилитационная команда, специализирующаяся на реабилитации после инсульта, включает:
- Врачи, специализирующиеся на реабилитации, обеспечивающие ежедневное наблюдение
- Медсестры реабилитации
- Физиотерапевты, работающие над проблемами движения, ходьбы, равновесия и координации
- Эрготерапевты, которые помогают пациентам восстановить независимость при приеме пищи, купании, одевании, письме и других повседневных задачах
- Сертифицированные логопеды, которые помогают пациентам восстановить речь, язык, когнитивные навыки и навыки глотания
- Специалисты по ортопедическому/адаптивному оборудованию
- Консультанты по питанию
- Кейс-менеджеры/социальные работники
- Нейро/клинические психологи
Caregiver Support
Поскольку семья часто является важной частью процесса выздоровления, персонал реабилитационного центра проводит обучение и обучение близких членов семьи после инсульта.