Продолжительность жизни при аритмии сердца: Как жить с мерцательной аритмией?
сложные случаи из практики кардиолога uMEDp
Российский национальный конгресс кардиологов прошел в Москве с 6 по 8 октября 2009 года в здании Российской академии наук. В рамках конгресса при поддержке компании Dr.Reddy`s состоялся научный симпозиум, посвященный проблемам современной клинической кардиологии.
Н.А. Мазур, д.м.н., профессор, РМАПО
Таблица 1. Тактика ведения и лечения больных с аритмией
Таблица 2. Группы риска тромбоэмболии
С.Ф. Соколов, ведущий научный сотрудник Института кардиологии им. А.Л. Мясникова РКНПК Росздрава
Таблица 3. Важнейшие исследования по изучению стратегии контроля частоты сердечных сокращений при ФП
Рисунок 1. Отклонения частот ритма в группе обследованных пациентов от средних почасовых значений ЧСС для здоровых лиц с синусовым ритмом в контроле и под действием Корбис
О.Л. Барбараш, профессор, Кузбасский кардиологический центр
Рисунок 2. Динамика ЧСС во время операции
Динамика ЧСС во время операции
А.И. Мартынов, д.м.н., профессор, академик РАМН
Рисунок 3. Дизайн исследования препаратов Корбис и Конкор
Стратегия ведения пациентов с фибрилляцией предсердий
Наиболее частой формой аритмий является фибрилляция предсердий (ФП) – ее распространенность среди населения старше 60 лет составляет от 3% до 12%.
Средняя продолжительность жизни больных после возникновения фибрилляции предсердий не превышает 6 лет. Особенно важно то, что эти больные, кроме нарушения ритма сердца и развития сердечной недостаточности, имеют угрозу развития тромбоэмболий. Практика показывает, что при диагностике инсульта процент ошибок минимален, в то время как тромбоэмболию порой определить сложно. Особенно высок риск тромбоэмболии при наличии ревматического порока сердца. Однако в настоящее время основными причинами ФП стали артериальная гипертония, сердечная недостаточность различной этиологии и сахарный диабет.
Стратегия лечения больных с ФП должна включать купирование и предупреждение приступов, а в связи с высоким риском тромбообразования и тромбоэмболии – также и их профилактику. Кроме того, при наличии такой возможности проводится этиологическое лечение, например хирургическая коррекция порока сердца.
В настоящее время нет согласованных подходов в лечении больных с артериальной гипертонией, имеющих фибрилляцию предсердий. Поэтому сотрудниками кафедры кардиологии РМАПО проведено исследование, в котором было изучено влияние на артериальное давление и нарушения ритма сердца некоторых препаратов, принадлежащих к разным группам.
В нашем исследовании лечение больных проводилось с помощью индивидуально подобранной дозы Верапамила (от 240 до 480 мг в сутки). Терапия в течение 3 месяцев привела к достоверному снижению частоты пароксизмов (до применения препарата в данной группе больных отмечалось от 3 до 12 пароксизмов в месяц). У четверых больных для достижения целевого уровня АД (ниже 140/90 мм рт. ст.) к терапии Верапамилом были добавлены ингибиторы АПФ. При более подробном анализе оказалось, что в подгруппе больных, у которых Верапамил обеспечивал снижение систолического АД до уровня ниже 130-120 мм рт. ст., наблюдалось полное исчезновение пароксизмов на период наблюдения.
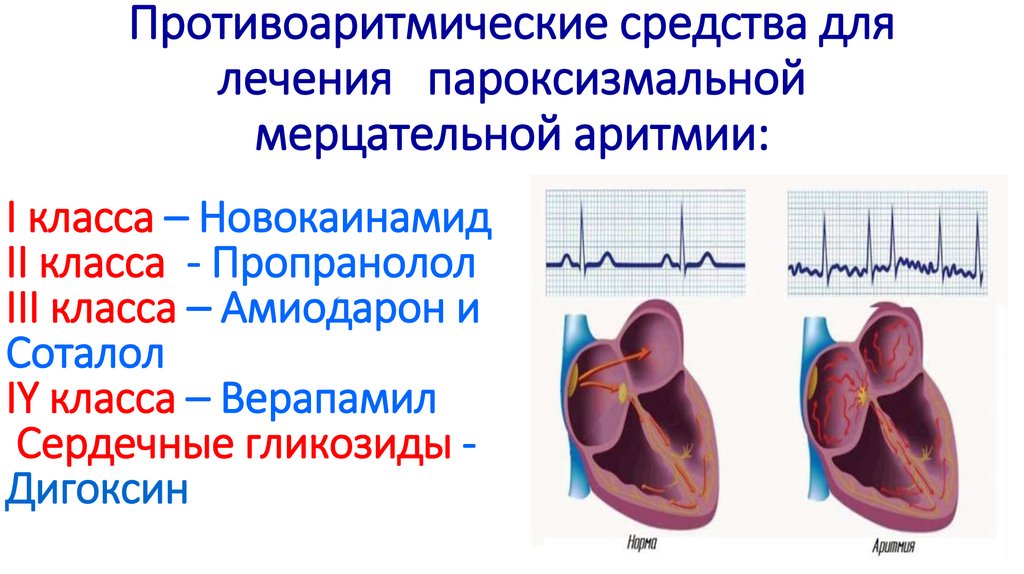
В Рекомендациях Европейского общества кардиологов в представленной последней классификации подчеркивается, что пароксизмальная форма ФП самостоятельно купируется в течение первых суток. В то время как при персистирующей форме самостоятельное купирование не происходит как минимум в течение 7 дней. При пароксизмальной форме тактика ведения больного зависит от тяжести течения приступов (таблица 1).
Если пароксизм протекает легко, то можно ограничиться препаратом, который снижает частоту сердечного ритма или который ускоряет его купирование. В случаях, когда пароксизм протекает тяжело, то кроме купирования необходимо лечение антиаритмическими препаратами с целью предупреждения рецидивирования аритмии. При персистирующей форме можно придерживаться тактики восстановления синусового ритма или лишь урежения частоты ритма желудочков, так как различий в отдаленных исходах при той или другой тактике их ведения не отмечено. Но в обоих случаях показано проведение антитромботической терапии с целью профилактики тромбообразования.
В случаях, когда пароксизм протекает тяжело, то кроме купирования необходимо лечение антиаритмическими препаратами с целью предупреждения рецидивирования аритмии. При персистирующей форме можно придерживаться тактики восстановления синусового ритма или лишь урежения частоты ритма желудочков, так как различий в отдаленных исходах при той или другой тактике их ведения не отмечено. Но в обоих случаях показано проведение антитромботической терапии с целью профилактики тромбообразования.
При купировании пароксизма с помощью препаратов, не замедляющих время проведения импульсов в АВ узле, обязательно предварительное назначение препарата уменьшающего ЧСС. По нашим данным, у больных с пароксизмальной формой ФП с исходной ЧСС более 75 в 1 мин. предпочтение для урежения частоты сердечного ритма должно быть отдано β-блокатору, а при исходном ритме 60 и меньше, урежать ЧСС во время пароксизма лучше с помощью Верапамила.
При выборе антитромботической терапии следует учитывать, к какой группе риска тромбоэмболии относится больной (таблица 2).
Больным из группы низкого риска профилактика тромбоэмболии может осуществляться с помощью аспирина (предпочтительнее в дозе около 325 мг), в группе умеренного риска – с помощью аспирина или антагониста витамина К (Варфарина) или прямого антагониста тромбина – Дабигатрана, а в группе высокого риска – с помощью одного из двух последних препаратов.
Влияние бисопролола (Корбис) на урежение сердечного ритма у больных с фибрилляцией предсердий
Фибрилляция предсердий имеет четыре основных непосредственных последствия:
- исчезновение сокращений предсердий;
- нерегулярность сердечного ритма;
- нарушение коронарного кровотока;
- развитие тахикардии.
Лекарственные препараты, которые применяются для урежения ритма, прежде всего оказывают влияние на функцию атриовентрикулярного узла. Необходимо учитывать последствия высокой частоты сердечных сокращений при фибрилляции предсердий.
Таким образом, при лечении данных пациентов необходимо устранить высокую частоту сердечных сокращений при фибрилляции предсердий. Существуют рекомендации, изданные Американским колледжем кардиологов и Американской ассоциацией сердца. Согласно документу, пациентам с персистирующей или перманентной формой ФП рекомендуется измерение частоты ритма в покое и при физической нагрузке, а также контроль частоты с использованием фармакологических препаратов (в большинстве случаев β-блокаторов и кальциевых антагонистов).
Тем не менее вопрос о критериях адекватного урежения ритма сердца при фибрилляции предсердий окончательно не решен. В настоящий момент существует 5 основных исследований, которые позволяют провести анализ адекватности критериев при урежении ритма (таблица 3). Следует обратить внимание, что в двух из представленных в таблице исследований не указываются критерии, оценивалась только величина снижения ЧСС в среднем. Однако три исследования дают вполне определенные критерии.
В настоящий момент существует 5 основных исследований, которые позволяют провести анализ адекватности критериев при урежении ритма (таблица 3). Следует обратить внимание, что в двух из представленных в таблице исследований не указываются критерии, оценивалась только величина снижения ЧСС в среднем. Однако три исследования дают вполне определенные критерии.
Для выявления наиболее оптимальных методов при урежении сердечного ритма у больных с ФП было предпринято ретроспективное сравнение двух исследований (см. таблицу): RACE и AFFIRM. На основании сопоставлений данных работ в 2005 году было инициировано новое исследование, которое получило название RACE-2, цель которого сопоставить 2 подхода: на основе снисходительных критериев и подход на основе жестких критериев.
Теперь можно определить медикаментозные средства для урежения ритма сердца. Пациентам с ФП прием Дигоксина внутрь является эффективным средством контроля ЧСС в покое и показан больным с сердечной недостаточностью, с дисфункцией левого желудочка или малоподвижным пациентам. Пациентам с ФП является разумным назначение Дигоксина в комбинации либо с β-блокаторами, либо с кальциевыми антагонистами для контроля частоты сердца как в покое, так и при физических нагрузках. Выбор препаратов должен быть индивидуализирован и при выборе дозировок следует избегать брадикардии. Суммируя результаты разрозненных многочисленных исследований, были выделены фармакологические средства для приема внутрь с целью контроля ЧСС при ФП. При неострых состояниях и хронической поддерживающей терапии рекомендуется: Метопролол, Пропранолол, Дилтиазем, Верапамил. При сердечной недостаточности: Дигоксин, Амиодарон.
Пациентам с ФП является разумным назначение Дигоксина в комбинации либо с β-блокаторами, либо с кальциевыми антагонистами для контроля частоты сердца как в покое, так и при физических нагрузках. Выбор препаратов должен быть индивидуализирован и при выборе дозировок следует избегать брадикардии. Суммируя результаты разрозненных многочисленных исследований, были выделены фармакологические средства для приема внутрь с целью контроля ЧСС при ФП. При неострых состояниях и хронической поддерживающей терапии рекомендуется: Метопролол, Пропранолол, Дилтиазем, Верапамил. При сердечной недостаточности: Дигоксин, Амиодарон.
Для выявления эффективности β-блокаторов при лечении пациентов с ФП нами начато исследование, которое направлено на изучение эффективности бисопролола в форме препарата Корбис в контроле частоты сердечного ритма при персистирующей и перманентной ФП. В данное исследование предполагалось включить 20 пациентов. Изначальная доза препарата 5 мг при отсутствии эффекта или недостаточном урежении ритма могла быть увеличена. Эффект оценивался путем измерения ЧСС в покое. А также на основе результатов холтеровского мониторирования, во время которого проводился тест с 6-минутной ходьбой. Пациентов отбирали с персистирующей и перманентной формой ФП с одним или несколькими из следующих признаков, устранение которых в ходе лечения считали критерием эффективности:
Эффект оценивался путем измерения ЧСС в покое. А также на основе результатов холтеровского мониторирования, во время которого проводился тест с 6-минутной ходьбой. Пациентов отбирали с персистирующей и перманентной формой ФП с одним или несколькими из следующих признаков, устранение которых в ходе лечения считали критерием эффективности:
- ЧСС в покое более 80/мин.;
- ЧСС средняя за сутки более 100/мин.;
- ЧСС максимальная за сутки более (220 – возраст) + 10%;
- ЧСС максимальная при тесте с 6-минутной ходьбой более 140/мин.
Данное исследование еще не закончено. Согласно текущим результатам, было проведено обследование 8 пациентов (5 мужчин и 3 женщины) в возрасте 41-71 года с органическими заболеваниями сердца, тиреотоксикозом и идиопатической аритмией. Препарат Корбис назначался 5 пациентам в дозе 5 мг/сут., 3 больным – в дозе 10 мг/сут. Препарат достоверно снижал среднюю частоту сердечных сокращений за сутки по результатам холтеровского мониторирования. Эффективность терапии составила 62,5% (5 из 8).
Эффективность терапии составила 62,5% (5 из 8).
В ходе исследования была отмечена динамика почасовых значений средней ЧСС на протяжении суток в контроле и под действием Корбиса. Частоты достаточно высоки в дневное время суток, а на фоне приема Корбиса (однократный прием в 8:00), отмечается значительное и достоверное снижение ЧСС и достоверные изменения сохраняются с 8-го по 20-й час суток. Причем препарат целенаправленно ориентирован на действие в дневное время суток, именно тогда, когда требуется действие β-блокаторов.
Кроме того, был проанализирован результат отклонения частот ритма в группе обследованных пациентов от средних почасовых значений ЧСС для здоровых лиц с синусовым ритмом в контроле и под действием Корбиса. На фоне лечения препаратом в дневное время суток отмечается достоверное снижение частот (рисунок 1).
Таким образом, можно сделать предварительное заключение данного исследования. Бисопролол (Корбис) обладает способностью снижать частоту сердечных сокращений при фибрилляции предсердий преимущественно в период дневной активности. Препарат обладает фармакокинетическими свойствами, делающими его удобным для применения в условиях длительной поддерживающей терапии (длительный, равномерный эффект после однократного приема внутрь).
Препарат обладает фармакокинетическими свойствами, делающими его удобным для применения в условиях длительной поддерживающей терапии (длительный, равномерный эффект после однократного приема внутрь).
Сердечно-сосудистые осложнения у пациентов, подвергшихся не кардиохирургическим вмешательствам. Место β-адреноблокаторов
Достижения в области анестезиологии и хирургии привели к неуклонному росту количества хирургических вмешательств, в связи с чем терапевтам, врачам общей практики и кардиологам все чаще приходится решать вопрос переносимости пациентом хирургического вмешательства. Инфаркт миокарда (ИМ), нестабильная стенокардия являются основными причинами смерти после оперативных вмешательств. Так, у пациента в возрасте более 50 лет вероятность развития периоперационного ИМ приближается к 1%, а если у пациента имеется известный анамнез ишемической болезни сердца (ИБС), то риск развития периоперационного ИМ увеличивается в 5 раз.
Периоперационные сердечно-сосудистые события повышают вероятность развития последующих осложнений, драматически увеличивают госпитальную летальность.
Во многих странах мира процедура предоперационного обследования достаточно четко регламентирована и основана на принципах доказательной медицины. В России, к сожалению, данному вопросу уделяется мало внимание, что наряду с целым рядом других проблем приводит к увеличению продолжительности госпитализации, стоимости лечения и высокой частоте отказа от проведения операций в категориях высокого риска.
В 2009 г. вышли в свет Европейские рекомендации по оценке риска и профилактики сердечно-сосудистых осложнений при проведении операций некардиологического профиля. Эти рекомендации требуют оценки с позиции реальности выполнения в российских условиях, однако ценны с позиции доказательной медицины для обоснования необходимости тех или иных диагностических и лечебных процедур у хирургических пациентов.
Предоперационное лечение – подготовка пациентов к хирургической травме-стрессу явилась причиной очень серьезных дебатов последнего десятилетия. Операция, с ее травмой, анестезией, аналгезией, интубацией и экстубацией, болью, гипотермией, кровотечением и анемией, голоданием – аналог стресс-теста. Известно, что классическим атрибутом стресса является повышение артериального давления и частоты сокращений сердца (ЧСС). Эти гемодинамические параметры повышаются параллельно увеличению в крови адреналина, норадреналина, кортизола и отражают интенсивность хирургической травмы. Таким образом, создаются условия, при которых дестабилизируется имеющаяся атеросклеротическая бляшка и повышается потребность миокарда в кислороде, что закономерно повышает риск развития острого коронарного синдрома.
Операция, с ее травмой, анестезией, аналгезией, интубацией и экстубацией, болью, гипотермией, кровотечением и анемией, голоданием – аналог стресс-теста. Известно, что классическим атрибутом стресса является повышение артериального давления и частоты сокращений сердца (ЧСС). Эти гемодинамические параметры повышаются параллельно увеличению в крови адреналина, норадреналина, кортизола и отражают интенсивность хирургической травмы. Таким образом, создаются условия, при которых дестабилизируется имеющаяся атеросклеротическая бляшка и повышается потребность миокарда в кислороде, что закономерно повышает риск развития острого коронарного синдрома.
В исследовании DECREASE II была доказана взаимосвязь между ЧСС и риском развития инфаркта миокарда (ИМ) у пациентов, подвергающихся некардиологическим операциям. Доказано: чем выше ЧСС перед операцией, тем выше риск инфаркта миокарда. Относительный риск развития ИМ повышается в 1,5 раза при увеличении ЧСС на каждые 5 ударов в минуту. С учетом этого β-блокаторы являются важным компонентом предоперационной подготовки пациента. Для пациента, находящегося на предоперационной подготовке, важны не только известные гемодинамические эффекты данного класса препаратов, но и снижение потребности миокарда в кислороде, увеличение продолжительности диастолы и время перфузии миокарда, а также антиаритмический эффект. Известно, что β-блокаторы имеют массу метаболических положительных эффектов, очень важных для пациентов, подвергающихся некардиологическим операциям, снижают продукцию свободных радикалов, металлопротеиназную активность и процессы воспаления; снижают экспрессию рецепторов, ответственных за клеточный апоптоз и др.
С учетом этого β-блокаторы являются важным компонентом предоперационной подготовки пациента. Для пациента, находящегося на предоперационной подготовке, важны не только известные гемодинамические эффекты данного класса препаратов, но и снижение потребности миокарда в кислороде, увеличение продолжительности диастолы и время перфузии миокарда, а также антиаритмический эффект. Известно, что β-блокаторы имеют массу метаболических положительных эффектов, очень важных для пациентов, подвергающихся некардиологическим операциям, снижают продукцию свободных радикалов, металлопротеиназную активность и процессы воспаления; снижают экспрессию рецепторов, ответственных за клеточный апоптоз и др.
В исследовании, которое было проведено в Кузбасском кардиологическом центре, проанализирована частота выявления синдрома артериальной гипертензии в хирургической клинике: ретроспективно проведена оценка 554 пациентов, которые подвергались плановой лапароскопической холецистэктомии с едиными подходами в анестезиологическом пособии. Выяснилось, что 47% пациентов пришли в клинику с ранее диагностированной артериальной гипертензией; у 28% в клинике впервые диагностировали артериальную гипертензию. Интересно то, что пациенты с артериальной гипертензией демонстрировали не только сердечно-сосудистые осложнения во время послеоперационного периода, но и большую частоту гнойно-септических осложнений. Данный анализ был проведен в уравненных по возрасту, по индексу массы тела группах пациентов. Следующий этап исследования был направлен на оценку возможности бисопролола снижать риск развития периоперационных гемодинамических нарушений. Было выделено 2 группы пациентов с артериальной гипертензией. I группе была назначена терапия амбулаторным терапевтом, и она была стандартной (ингибиторы ангиотензин-превращающего фермента, диуретики, антагонисты кальция). Пациентам II группы была назначена антигипертензивная терапия, основанная на приеме β-блокатора – бисопролола. Обе группы были абсолютно идентичны по гемодинамическим показателям.
Выяснилось, что 47% пациентов пришли в клинику с ранее диагностированной артериальной гипертензией; у 28% в клинике впервые диагностировали артериальную гипертензию. Интересно то, что пациенты с артериальной гипертензией демонстрировали не только сердечно-сосудистые осложнения во время послеоперационного периода, но и большую частоту гнойно-септических осложнений. Данный анализ был проведен в уравненных по возрасту, по индексу массы тела группах пациентов. Следующий этап исследования был направлен на оценку возможности бисопролола снижать риск развития периоперационных гемодинамических нарушений. Было выделено 2 группы пациентов с артериальной гипертензией. I группе была назначена терапия амбулаторным терапевтом, и она была стандартной (ингибиторы ангиотензин-превращающего фермента, диуретики, антагонисты кальция). Пациентам II группы была назначена антигипертензивная терапия, основанная на приеме β-блокатора – бисопролола. Обе группы были абсолютно идентичны по гемодинамическим показателям. Из препаратов бисопролола был выбран Корбис. В течение 14 дней доза бисопролола тщательно титровалась, и в последующем данная терапия продолжалась в течение 30 дней.
Из препаратов бисопролола был выбран Корбис. В течение 14 дней доза бисопролола тщательно титровалась, и в последующем данная терапия продолжалась в течение 30 дней.
Бисопролол действительно показал свою эффективность и безопасность. Пациенты во время лечения демонстрировали стабильность по гемодинамическим показателям, в частности в период интубации (самый травматичный период). Пациенты, принимавшие бисопролол, вошли в операцию на относительной нормокардии, данный показатель в процессе хирургического вмешательства не изменялся (рисунок 2). В то время как у пациентов, которые получали стандартную терапию, фиксировалась тахикардия.
Таким образом, артериальная гипертензия в хирургической клинике – это большая проблема, которая ассоциируется с высоким риском осложнений, поэтому, согласно результатам исследования, можно констатировать, что терапия бисопрололом, в частности препаратом Корбис, эффективна и безопасна.
Разбор клинического случая
Признаки избыточной реакции пульса на нагрузку и значительное повышение артериального давления (АД) не только опасны с точки зрения развития сердечно-сосудистой патологии, но и с точки зрения развития нарушений ритма, и в частности, таких, как фибрилляция предсердий. Учитывая частое наличие сочетанной патологии у больных, β-блокаторы в последнее время приобретают особое значение при нарушении ритма сердца, и, в частности, фибрилляции предсердий. Из представленных на фармацевтическом рынке β-блокаторов многие специалисты остановили свой выбор на бисопрололе. Ранее в клинической практике широко применяли метопролол, потому что данный препарат был самым изученным в России, хорошо себя зарекомендовавшим. Однако, с появлением бисопролола начали активно проводиться исследования этого препарата. Бисопролол – высокоселективный β-блокатор без собственной симпатомиметической активности. Биодоступность препарата составляет 85-90%, Cmax в плазме крови достигается через 1-3 часа.
Учитывая частое наличие сочетанной патологии у больных, β-блокаторы в последнее время приобретают особое значение при нарушении ритма сердца, и, в частности, фибрилляции предсердий. Из представленных на фармацевтическом рынке β-блокаторов многие специалисты остановили свой выбор на бисопрололе. Ранее в клинической практике широко применяли метопролол, потому что данный препарат был самым изученным в России, хорошо себя зарекомендовавшим. Однако, с появлением бисопролола начали активно проводиться исследования этого препарата. Бисопролол – высокоселективный β-блокатор без собственной симпатомиметической активности. Биодоступность препарата составляет 85-90%, Cmax в плазме крови достигается через 1-3 часа.
На нашем фармрынке представлено несколько зарубежных и отечественных дженериков. В частности, можно рассмотреть такой дженерик, как Корбис. Представляем клиническое наблюдение. Больной 58 лет поступил в блок интенсивной терапии с фибрилляцией предсердий в течение 3 суток. Нарушение ритма пациент переносил относительно благоприятно, однако отметил постепенное нарастание одышки. За полгода до последней госпитализации он перенес на фоне гипертонической болезни субэндокардиальный инфаркт миокарда, после которого появилась стенокардия и начальные проявления недостаточности кровообращения в виде одышки при нагрузке. В постинфарктном периоде больной принимал Корбис 5 мг/сут. и Нолипрел форте 1 таблетку в день. Пароксизм нарушения ритма возник на фоне эмоционального напряжения и повышения АД. Суточная доза Корбиса была удвоена (10 мг/сут.). Через 2,5 часа после приема лекарств восстановился синусовый ритм и нормализовалось АД. Таким образом, восстановление ритма сердца с большой долей вероятности можно связать с увеличением дозы Корбиса.
Нарушение ритма пациент переносил относительно благоприятно, однако отметил постепенное нарастание одышки. За полгода до последней госпитализации он перенес на фоне гипертонической болезни субэндокардиальный инфаркт миокарда, после которого появилась стенокардия и начальные проявления недостаточности кровообращения в виде одышки при нагрузке. В постинфарктном периоде больной принимал Корбис 5 мг/сут. и Нолипрел форте 1 таблетку в день. Пароксизм нарушения ритма возник на фоне эмоционального напряжения и повышения АД. Суточная доза Корбиса была удвоена (10 мг/сут.). Через 2,5 часа после приема лекарств восстановился синусовый ритм и нормализовалось АД. Таким образом, восстановление ритма сердца с большой долей вероятности можно связать с увеличением дозы Корбиса.
Нами было проведено исследование, в котором анализировалось действие 2 препаратов: дженерика Корбис и оригинального препарата Конкор. В исследовании приняли участие 12 больных ишемической болезнью сердца, которые были разбиты на 2 рандомизированные группы по 6 человек. В I группе был назначен Корбис 5-10 мг 1 раз в сутки, во II – Конкор в той же дозе в течение 14 дней. После 2 недель лечения препараты поменяли. В результате, проанализировав ряд показателей (уменьшение ЧСС, урежение стенокардии и экстрасистолии), пришли к заключению, что Корбис по клиническому эффекту идентичен Конкору (рисунок 3). Отмечено, что Корбис оказывает противоаритмический эффект преимущественно у больных с признаками симпатикотонии.
В I группе был назначен Корбис 5-10 мг 1 раз в сутки, во II – Конкор в той же дозе в течение 14 дней. После 2 недель лечения препараты поменяли. В результате, проанализировав ряд показателей (уменьшение ЧСС, урежение стенокардии и экстрасистолии), пришли к заключению, что Корбис по клиническому эффекту идентичен Конкору (рисунок 3). Отмечено, что Корбис оказывает противоаритмический эффект преимущественно у больных с признаками симпатикотонии.
Следует отметить, что Корбис и Конкор включены во все государственные программы: ДЛО, ЖВНЛС, СМПА, СМПС. В аннотации отмечены следующие показания к назначению бисопролола: артериальная гипертензия, ИБС (профилактика приступов стенокардии, ХСН). В национальные клинические рекомендации включены: перенесенный ИМ, ХСН, нарушения ритма, мигрень, предоперационная гипертензия, гипертиреоз, эссенциальный тремор. Исследования бисопролола продолжаются. Однако уже на этом этапе можно сказать, что Корбис (бисопролол) показал хорошую клиническую эффективность и сопоставим с Конкором.
Вернуть здоровый ритм — kldcardio
Фибрилляция предсердий – сложное заболевание. Как правило, в наш Центр обращаются пациенты, которые уже долгое время находятся в нескончаемых поисках диагноза, нужного специалиста, современного и адекватного лечения. Каждому больному, пришедшему на первичный прием с фибрилляцией предсердий, я и мои коллеги всегда рассказываем о том, что написано ниже.
Во-первых, важно, чтобы с момента консультации человек понимал — он теперь не один на пути борьбы с аритмией, и у него есть надежные союзники. Во-вторых, пациенту с такой сложной аритмией, как фибрилляция предсердий, крайне необходимы знания об этом заболевании. Что происходит с сердцем и что будет происходить в дальнейшем. Как аритмия развивается со временем и что будет, к примеру, если не принимать никаких лекарств. Какие есть риски, и конечно же, какие методики позволяют действительно избавиться от аритмии.
Что такое фибрилляция предсердий?
Прежде всего, надо понимать, что «аритмия» это очень общее понятие, включающее в себя огромное множество различных по механизму и, соответственно, по способам лечения (и их эффективности) нарушений ритма сердца. Мерцательная аритмия или фибрилляция предсердий (а это синонимы) — самая сложная из всех.
Мерцательная аритмия или фибрилляция предсердий (а это синонимы) — самая сложная из всех.
Врачи выделяют три формы ФП (фибрилляции предсердий):
-пароксизмальная — когда у пациента время от времени случаются приступы внезапной аритмии;
-персистирующая — это когда ФП существует уже дольше и, как правило, не проходит сама. Приступы «затягиваются», и пациент живет с аритмией длительно, например, несколько месяцев;
-длительно-персистирующая — когда о нормальном ритме напоминают только старые ЭКГ, и ФП существует больше года.
*Справедливости ради нужно сказать, что есть ещё одна форма – постоянная ФП, но это скорее диагноз не для больного, а для врача и нашего сегодняшнего понимания механизмов этой сложной аритмии. Речь идет о состоянии, когда уже не предпринимаются никакие попытки восстановить нормальный ритм. Надеюсь, уже в недалеком будущем наступит время, когда такого диагноза не будет.
Можно сказать, что три формы фибрилляции предсердий — это стадии естественного течения процесса. Если лечение отсутствует, что заболевание пройдет все три этапа — у кого-то быстрее, у кого-то медленнее.
Если лечение отсутствует, что заболевание пройдет все три этапа — у кого-то быстрее, у кого-то медленнее.
Но ключевой момент в том, что при фибрилляции предсердий прогрессирование заболевания происходит постоянно с каждой минутой работы сердца в режиме аритмии.
Как лечить?
Если говорить о методах лечения и его эффективности, то пароксизмальная (приступы) форма мерцательной аритмии и длительно-существующая форма — это вообще разные болезни с разными механизмами, разной эффективностью лечения. И путь, который должны пройти пациент и врач для достижения свободы от аритмии, по времени тоже разный.
Например, если при приступах ФП часто достаточно воздействовать на очаги аритмии в легочных венах (выполняется электрическая изоляция легочных вен), то когда ФП существует уже много лет, а пациент не получает хирургического лечения, происходят вторичные изменения в сердце, сами по себе поддерживающие аритмию. Как говорят аритмологи в такой ситуации — мерцательная аритмия рождает мерцательную аритмию. Соответственно, на данном этапе и лечение другое, более сложное, длительное, зачастую многоступенчатое.
Соответственно, на данном этапе и лечение другое, более сложное, длительное, зачастую многоступенчатое.
Но и в запущенных случаях многолетней ФП есть шанс вылечиться полностью. За этот шанс мы всегда боремся. К счастью, в нашем центре сложилась уникальная не только для России, но для зарубежных клиник практика совместной командной работы с такими пациентами. К каждому случаю подходим индивидуально. Мы используем так называемый «гибридный подход» — когда для устранения мерцательной аритмии сочетаются высокоэффективные методики открытых операций на сердце с малоинвазивными (доступ через прокол вены) операциями РЧА (радиочастотной аблации). Отмечу, что наши кардиохирурги имеют самый большой опыт в России выполнения торакоскопических процедур (через небольшой разрез) для лечения мерцательной аритмии.
И мне, как специалисту, очень приятно работать в такой команде. Я вижу результат, ради которого мы все «живём на работе», вижу пациентов, которые когда-то пришли с вердиктом «неизлечим», а в итоге длительных и часто многоэтапных процедур удается добиться у них нормального здорового ритма сердца без мерцательной аритмии. Это наш «наркотик» и удовольствие от этого — сумасшедший стимул для всей нашей команды центра.
Это наш «наркотик» и удовольствие от этого — сумасшедший стимул для всей нашей команды центра.
Конечно, не все так просто, и особенно в запущенных случаях длительно-существующей фибрилляции предсердий для получения такого результата необходимо несколько операций, сочетание методик, регулярные осмотры, четкое соблюдение рекомендаций доктора. Но самое главное — это желание пациента вылечиться. И если это желание есть, конечно, весь этот длинный путь он проходит в тесном взаимодействии с нами. И мы всегда делаем все возможное, чтобы помочь вернуть нормальный здоровый ритм.
Ожидаемая продолжительность жизни при мерцательной аритмии увеличилась, но раннее выявление по-прежнему имеет решающее значение, говорят исследователи
12 августа 2020 г.
Исследователи говорят, что достижения в области профилактики «необходимы» для достижения большего результата
Трейси Ромеро
Персонал PhillyVoice
Здоровье взрослых Здоровье сердца
Источник/изображение по лицензии Ingram Image
Более 2 миллионов американцев страдают мерцательной аритмией, нерегулярным сердечным ритмом, который сокращает продолжительность жизни примерно на два года.
Подробнее
Уровень смертности, связанной с мерцательной аритмией, за последние 45 лет снизился, но незначительно.
Продольное исследование показало, что мерцательная аритмия снижает ожидаемую продолжительность жизни в среднем на два года, что является небольшим улучшением по сравнению с трехлетним сокращением, ожидаемым в 1970-х и 80-х годах.
- БОЛЬШЕ ЗДОРОВЬЯ
- Тяжелые исходы COVID-19 в Филадельфии резко упали ниже апрельского пика
- Даже один алкогольный напиток на ранних сроках беременности увеличивает риск выкидыша тестирование еще
Мерцательная аритмия — это нерегулярное сердцебиение или аритмия, которая может привести к таким осложнениям, как образование тромбов, инсульт и сердечная недостаточность. По данным Американской кардиологической ассоциации, более 2 миллионов американцев живут с этим заболеванием.
Раннее выявление и лечение по-прежнему имеют решающее значение, говорят исследователи.
«Прогноз для людей с фибрилляцией предсердий со временем улучшился, но фибрилляция предсердий по-прежнему связана с большим разрывом в ожидаемой продолжительности жизни по сравнению с людьми без фибрилляции предсердий», — сказал старший автор Людовик Тринкварт, доцент биостатистики в Бостоне. Университет.
Тринкварт и его команда из Бостонского университета и Дании основывали свои выводы на данных Фрамингемского исследования сердца нескольких поколений. Их исследование было опубликовано в Интернете во вторник в журнале BMJ.
Исследователи проанализировали данные о здоровье трех поколений участников Framingham с 1972 по 2015 год, отслеживая вероятность того, что люди умрут через 10 лет после диагноза фибрилляции предсердий. Их ожидаемая продолжительность жизни сравнивалась с ожидаемой продолжительностью жизни участников того же возраста и пола, у которых не было этого заболевания.
«Исследование сердца во Фрамингеме — одно из немногих исследований в мире, которое позволяет изучать такие временные тенденции», — сказал Никлас Винтер, врач региональной больницы Силькеборга и докторант Орхусского университета в Дании.
Через десять лет после постановки диагноза первое поколение с мерцательной аритмией, охватывающее период с 1972 по 1985 год, прожило в среднем на 2,9 года меньше по сравнению с участниками без мерцательной аритмии. Этот разрыв сократился до 2,1 года в период с 1986 по 2000 год и до 2,0 лет в период с 2001 по 2015 год9.0003
Несмотря на то, что профилактические меры в отношении сердечно-сосудистых заболеваний и высокого кровяного давления также могут снизить вероятность развития мерцательной аритмии, не все случаи мерцательной аритмии можно предотвратить. Вот почему раннее выявление и лечение важны, говорят исследователи.
Кардиологи могут использовать различные тесты для выявления мерцательной аритмии. Они включают в себя электрокардиограмму, которая измеряет электрическую активность сердца, и эхокардиограмму, которая использует звуковые волны для получения картины работы сердца.
После постановки диагноза для лечения мерцательной аритмии можно использовать такие лекарства, как препараты, разжижающие кровь и бета-блокаторы, а также катетерную абляцию — процедуру, используемую для устранения электрических сигналов, вызывающих аномальное сердцебиение.
Исследователи приписали снижение смертности, наблюдаемое в их исследовании, улучшениям в раннем выявлении, управлении и лечении, но подчеркнули, что это все еще потенциально смертельное состояние.
«Достижения в области профилактики будут необходимы, чтобы остановить эпидемию мерцательной аритмии и снизить связанную с ней смертность», — добавил Тринкварт.
Трейси Ромеро
Персонал PhillyVoice
Подробнее Здоровье взрослых Здоровье сердца Филадельфия Ожидаемая продолжительность жизни Исследования Исследования
Подпишитесь на нас
Видео о здоровье
Включите JavaScript для просмотра комментариев с помощью Disqus.
Ожидаемая продолжительность жизни при застойной сердечной недостаточности: прогноз и стадии
Застойная сердечная недостаточность — это хроническое прогрессирующее состояние, которое влияет на функцию сердца. Это может быть опасно для жизни, если его не лечить.
Застойная сердечная недостаточность (ЗСН), или просто сердечная недостаточность, влияет на способность сердца перекачивать кровь по телу. Несмотря на свое название, ХСН не означает, что сердце полностью отказало.
Ожидаемая продолжительность жизни человека с застойной сердечной недостаточностью зависит от множества факторов, включая возраст, стадию заболевания и силу сердечной функции.
Многие заболевания, ослабляющие сердце, могут способствовать развитию ЗСН, в том числе:
- сердечные приступы
- ишемическая болезнь сердца
- врожденные пороки сердца
- пороки клапанов сердца
- высокое кровяное давление сердечная мышца
- Употребление наркотиков или токсинов.

Однако в некоторых случаях продолжительность жизни человека можно увеличить за счет изменения образа жизни, приема лекарств и хирургического вмешательства.
Ожидаемая продолжительность жизни с ХСН может быть нелинейной и зависеть от нескольких переменных. Обзор показал, что многие врачи не чувствуют, что могут уверенно предсказать клиническую траекторию пациента в течение 6 месяцев.
Мета-анализ 2019 года показал, что 1-, 2-, 5- и 10-летняя выживаемость при всех типах сердечной недостаточности составляет 87%, 73%, 57% и 35% соответственно, хотя ожидаемая продолжительность жизни для человека с CHF значительно улучшилось с течением времени.
Возраст человека на момент постановки диагноза может повлиять на прогноз. Авторы сообщили, что 5-летняя выживаемость для людей моложе 65 лет составляет около 78%, а для лиц в возрасте 75 лет и старше — 49%.
Кроме того, на ожидаемую продолжительность жизни может влиять сила, с которой сердце человека выталкивает кровь за удар, его фракция выброса. Врачи отмечают фракцию выброса пациента в процентах, при этом нормальный выброс составляет 50-70%.
Врачи отмечают фракцию выброса пациента в процентах, при этом нормальный выброс составляет 50-70%.
Пациенты с фракцией выброса менее 40% могут подвергаться большему риску смерти от ХСН. Однако исследование 2017 года показало, что 5-летняя ожидаемая продолжительность жизни была низкой среди всех пациентов, поступивших в больницу с сердечной недостаточностью, независимо от фракции выброса, а предполагаемая 5-летняя смертность составила 75,4%. Вышеупомянутый 2019мета-анализ также не обнаружил существенной разницы в выживаемости между пациентами с фракцией выброса ниже 40% и пациентами с фракцией выброса выше.
Наличие сопутствующих заболеваний или сопутствующих заболеваний, таких как ишемическая болезнь сердца, может повлиять на ожидаемую продолжительность жизни человека. Исследование с поправкой на возраст показало, что сопутствующие заболевания были обычным явлением у пациентов с сердечной недостаточностью и способствовали более высокому уровню смертности. Диабет присутствовал в 28% случаев смерти, а хроническая обструктивная болезнь легких — в 16%.
Факторы риска, такие как ожирение, гипертония и неправильное питание, также могут негативно повлиять на прогноз.
ХСН неизлечима, но раннее выявление и лечение могут помочь увеличить продолжительность жизни человека. Соблюдение плана лечения, включающего изменение образа жизни, может помочь улучшить качество их жизни.
У человека с сердечной недостаточностью мышцы сердца могут стать слишком жесткими или слишком слабыми, чтобы эффективно перекачивать кровь. Это заставляет кровь оставаться в желудочке, а не выталкивать его наружу. Кровь, оставшаяся в сердце, может вызвать задержку жидкости.
Врачи часто оценивают функциональные возможности пациента по системе классификации Нью-Йоркской кардиологической ассоциации. Классы:
- Класс 1: У человека нет ограничений физической активности и побочных симптомов.
- Класс 2: Есть небольшое ограничение физической активности, но человеку комфортно в покое.
- Класс 3: Человек имеет заметное ограничение физической активности, но сохраняет комфорт в состоянии покоя.

- Класс 4: Человек не может заниматься физическими упражнениями без дискомфорта и испытывает симптомы сердечной недостаточности в покое.
Вторая система классификации, разработанная Американским колледжем кардиологов и Американской кардиологической ассоциацией, подробно описывает четыре стадии сердечных заболеваний. Это:
- Стадия A: У человека высокий риск сердечной недостаточности, но в настоящее время у него нет идентифицируемых заболеваний.
- Стадия B: У человека структурное заболевание сердца, но симптомы отсутствуют.
- Стадия C: У человека есть текущие или предшествующие симптомы сердечной недостаточности, связанные с основным заболеванием.
- Стадия D: У человека в настоящее время прогрессирующее структурное заболевание сердца, проявляются явные симптомы, и ему требуется специализированное медицинское вмешательство.
Общие симптомы сердечно-сосудистых заболеваний включают:
- отек ног и ступней или увеличение веса, вызванное скоплением избыточной жидкости
- вздутие живота
- одышка или пробуждение по ночам с одышкой
- Неспособность лежать ровно или необходимость спать на дополнительных подушках.

- усталость
- тошнота
- боль в груди
Другие состояния, влияющие на сердце, также могут вызывать ЗСН. Ранняя диагностика ХСН может помочь людям справиться со своими симптомами и внести профилактические изменения в образ жизни.
Медикаментозное лечение сердечной недостаточности может включать лечение, направленное на уменьшение количества жидкости в организме. Это может снизить нагрузку на сердце и улучшить его способность перекачивать кровь. Врачи могут прописать мочегонные средства, чтобы помочь организму избавиться от лишней жидкости. Общие диуретики включают гидрохлоротиазид, буметанид и фуросемид.
Врачи могут также назначить ингибиторы ангиотензинпревращающего фермента (АПФ), блокаторы рецепторов ангиотензина (БРА) или блокаторы рецепторов ангиотензина ингибиторы неприлизина (АРНИ), чтобы помочь сердцу более эффективно перекачивать кровь.
Согласно обзорам, эти методы лечения могут снизить заболеваемость у пациентов со сниженным выбросом левого желудочка.
Другие ключевые компоненты терапии ЗСН включают блокаторы минералокортикоидных рецепторов (MRA) и ингибиторы натрий-глюкозного котранспортера 2 (SGLT2).
MRA рекомендуются пациентам с фракцией выброса 35% или менее и могут помочь улучшить кровоток и работу сердца. Ингибиторы SGLT2 могут помочь контролировать уровень глюкозы у пациентов с диабетом и снизить риск сердечных осложнений.
Врачи также назначат бета-блокаторы для поддержки этих усилий и контроля частоты сердечных сокращений.
Некоторым пациентам также может потребоваться физическое вмешательство для лечения ХСН. Врачи могут рекомендовать использование имплантируемых сердечных дефибрилляторов (ИКД) и сердечную ресинхронизирующую терапию (СРТ), когда это необходимо. Оба они включают в себя прикрепление небольших электрических устройств к сердцу пациента для защиты от внезапной остановки сердца и регулирования сердечного ритма соответственно.
На более поздних стадиях сердечной недостаточности врачи могут порекомендовать операцию по установке в сердце вспомогательного устройства для левого желудочка (LVAD). LVAD — это насос, который помогает сердечной мышце сокращаться. Эти устройства могут быть постоянным решением для пациентов с сердечной недостаточностью.
LVAD — это насос, который помогает сердечной мышце сокращаться. Эти устройства могут быть постоянным решением для пациентов с сердечной недостаточностью.
Полная пересадка сердца также может быть вариантом, если человек является хорошим кандидатом на операцию.
Врачи, скорее всего, порекомендуют изменить образ жизни, чтобы свести к минимуму воздействие ХСН. Это часто происходит независимо от стадии, на которой находится человек, или других методов лечения, которым он будет следовать. Согласно медицинским обзорам, эти изменения могут помочь замедлить прогрессирование сердечной недостаточности и повысить качество жизни человека. Среди них:
Диета и физические упражнения
Здоровое, разнообразное питание и регулярные физические упражнения — это всегда хорошая идея, но это может быть необходимо для людей с ХСН.
Врачи могут порекомендовать людям с ЗСН исключить из рациона избыток соли (натрия), так как это приводит к задержке жидкости в организме. Они также могут предложить уменьшить потребление алкоголя и ограничить потребление жидкости.
Регулярные аэробные упражнения могут улучшить здоровье сердца и улучшить качество жизни пациентов с ХСН. В руководстве говорится, что физическая подготовка может улучшить качество жизни, толерантность к физической нагрузке и снизить частоту госпитализаций у пациентов с сердечной недостаточностью. Однако увеличение физической активности может быть целесообразным не для всех пациентов.
Аэробные упражнения — это любая деятельность, повышающая частоту сердечных сокращений и частоту дыхания. Мероприятия включают плавание, езду на велосипеде или бег трусцой. Если у вас ЗСН, проконсультируйтесь с врачом, прежде чем выполнять какие-либо упражнения.
Ограничение жидкости
Люди с застойной сердечной недостаточностью склонны задерживать жидкость в организме. Чтобы смягчить это, врачи иногда рекомендуют пациентам ограничивать ежедневное потребление жидкости в безопасных пределах.
Потребление слишком большого количества жидкости может свести на нет действие мочегонных препаратов. Хотя важно избегать обезвоживания, врач порекомендует, сколько жидкости человек может безопасно потреблять в день.
Хотя важно избегать обезвоживания, врач порекомендует, сколько жидкости человек может безопасно потреблять в день.
Вес
Ожирение является известным фактором риска сердечной недостаточности. Исследования показывают, что потеря веса и последующее лечение могут быть эффективными для предотвращения сердечной недостаточности.
Однако пациентам с ЗСН снижение массы тела не всегда может быть рекомендовано. В некоторых случаях быстрая потеря веса может быть признаком других заболеваний, таких как кахексия.
Врачи часто просят людей ежедневно следить за своим весом, чтобы выявить внезапное или быстрое увеличение веса, которое может быть признаком задержки жидкости. Кроме того, ежедневное наблюдение за весом человека может помочь врачу назначить правильный уровень диуретиков, чтобы помочь организму высвободить жидкость.
У каждого человека с ХСН разный опыт заболевания, и ожидаемая продолжительность жизни при этом заболевании значительно различается у разных людей.