Препараты при деменции: Лечение деменции у пожилых людей: методы и средства терапии
Not Found (#404)
скрыть меню
Выпуски текущего года
7-8 (136)
5-6 (135)
3-4 (134)
2 (133)
1 (132)
7-8 (136)
Содержание выпуска 7-8 (136), 2022
-
Виклики війни: допомога у кризових ситуаціях
-
Етичні та правові проблеми психічного здоров’я: Україна у фокусі міжнародної уваги
Ю.А. Крамар
-
Скринінг, діагностика та лікування діабетичної сенсомоторної полінейропатії: консенсусні рекомендації
-
Вплив засобів масової інформації на делінквентну поведінку підлітків
Р.
 І. Ісаков
І. Ісаков -
Застосування програм рухової реабілітації у нормалізації психоемоційної сфери пацієнтів з хворобою Паркінсона
Н.П. Волошина, І.В. Богданова, І.К. Волошин-Гапонов, С.В. Федосєєв, Л.П. Терещенко, Т.В. Богданова
-
Алгоритм роботи з травмою
-
Типи нейропатичного болю за Міжнародною класифікацією ротолицевого болю
-
Ведення пацієнтів із деменцією: ключові положення щодо діагностики, лікування та догляду наприкінці життя
-
Відчайдушні прерафаеліти: Джон Раскін та Еффі Грей
5-6 (135)
3-4 (134)
2 (133)
1 (132)
Другие проекты издательского дома «Здоровье Украины»
Спеціалізований медичний портал
Дитячий лікар
Медичні аспекти здоров’я жінки
Клінічна імунологія, Алергологія, ІнфектологіяРаціональна фармакотерапія
3.
 1.4.2. Лечение деменции при болезни Паркинсона \ КонсультантПлюс
1.4.2. Лечение деменции при болезни Паркинсона \ КонсультантПлюс3.1.4.2. Лечение деменции при болезни Паркинсона
Основой терапии является применение базисных препаратов для лечения деменции, к которым относятся два типа препаратов — антихолинэстеразные средства (ИХЭ) и мемантин** (по химическому действию представляющий собой антагонист глутаматных NMDA-рецепторов). Данные препараты не только влияют на ключевые проявления КР [286], но также способствуют улучшению общего функционального статуса пациента, качества жизни как самого пациента, так и окружающих его людей, оказывают положительное влияние на выраженность сопутствующих нервно-психических нарушений.
Оценка эффективности противодементной терапии должна осуществляться на регулярной основе не реже одного раза в 6 месяцев или в зависимости от изменения состояния пациента.
— Рекомендуется применение антихолинэстеразных средств (#донепезила (5, 10 мг в сут) или #ривастигмина** (3 — 12 мг в сут) для лечения легкой и среднетяжелой степени деменции [286 — 289].
Уровень убедительности рекомендаций B (уровень достоверности доказательств — 2).
— Рекомендуется возможное применение #галантамина** (8 — 24 мг/сут) при неэффективности и непереносимости других антихолинэстеразных средств для лечения легкой и среднетяжелой степени деменции [290].
Уровень убедительности рекомендаций — C (уровень достоверности доказательств — 2).
Комментарии: Холинергический дефицит — один из факторов развития деменции при БП. Поэтому холинергическая терапия может считаться базовой в лечении когнитивных нарушений при болезни Паркинсона, а ИХЭ — препаратами выбора. ИХЭ оказывают значительное влияние на внимание, скорость обработки информации, регуляторные функции, память и речь по сравнению с плацебо. Для лечения деменции при болезни Паркинсона официально одобрен только один препарат из группы антихолинэстеразных средств — ривастигмин**, представляющий собой селективный ингибитор ацетил- и бутирилхолинэстераз головного мозга, имеющий наибольшую доказательную базу [291]. А галантамин менее хорошо изучен. В отношении других ингибиторов ацетилхолинэстеразы (донепезил и галантамин**) также проводились КИ с целью оценки эффективности и безопасности применения в лечении пациентов с деменцией при болезни Паркинсона. Результата клинических исследований в отношении применения донепезила носят противоречивый характер, что затрудняет оценку его эффективности в лечении деменции при болезни Паркинсона [287]. Оценка эффективности и безопасности применения галантамина** проведена в одном открытом контролируемом исследовании [290]. Тем не менее, многие эксперты, считают возможным назначение галантамина** для лечения деменции при болезни Паркинсона в связи доказанной антидементной активностью при других нейродегенеративных заболеваниях [290]. По данным мета-анализа при применении ривастигмина** отмечено большее количество нежелательных явлений по сравнению с донепезилом, в частности усиление тремора [286]. Однако, долгосрочные данные по безопасности из 76-недельного проспективного открытого рандомизированного исследования у пациентов с деменцией легкой и средней степени тяжести (n = 583) показали, что лечение ривастигмином** в капсулах (12 мг/день) или пластыре (пластырь 9,5 мг/24 ч) хорошо переносится [291].
А галантамин менее хорошо изучен. В отношении других ингибиторов ацетилхолинэстеразы (донепезил и галантамин**) также проводились КИ с целью оценки эффективности и безопасности применения в лечении пациентов с деменцией при болезни Паркинсона. Результата клинических исследований в отношении применения донепезила носят противоречивый характер, что затрудняет оценку его эффективности в лечении деменции при болезни Паркинсона [287]. Оценка эффективности и безопасности применения галантамина** проведена в одном открытом контролируемом исследовании [290]. Тем не менее, многие эксперты, считают возможным назначение галантамина** для лечения деменции при болезни Паркинсона в связи доказанной антидементной активностью при других нейродегенеративных заболеваниях [290]. По данным мета-анализа при применении ривастигмина** отмечено большее количество нежелательных явлений по сравнению с донепезилом, в частности усиление тремора [286]. Однако, долгосрочные данные по безопасности из 76-недельного проспективного открытого рандомизированного исследования у пациентов с деменцией легкой и средней степени тяжести (n = 583) показали, что лечение ривастигмином** в капсулах (12 мг/день) или пластыре (пластырь 9,5 мг/24 ч) хорошо переносится [291]. Не отмечено отрицательного влияния на выраженность двигательных нарушений ни у одного из препаратов из группы ИХЭ [284]. Титрация антихолинэстеразных средств должна осуществляться постепенно с начальных доз до достижения «целевой» дозы. При недостаточном эффекте целевой дозы возможно увеличение ее до максимальной (Приложение А3).
Не отмечено отрицательного влияния на выраженность двигательных нарушений ни у одного из препаратов из группы ИХЭ [284]. Титрация антихолинэстеразных средств должна осуществляться постепенно с начальных доз до достижения «целевой» дозы. При недостаточном эффекте целевой дозы возможно увеличение ее до максимальной (Приложение А3).
— Рекомендуется применение #мемантина** у пациентов с БП для лечения деменции [292 — 299].
Уровень убедительности рекомендаций — B (уровень достоверности доказательств — 2).
Комментарии: Деменция при болезни Паркинсона не относится к зарегистрированным показаниям для #мемантина**, однако эффективность и безопасность #мемантина** в дозе 20 мг в сутки у пациентов доказана по результатам РКИ [294, 296]. #Мемантин** оказывает значительное влияние на внимание, скорость обработки и регуляторные функции [295]. Сравнительных исследований мемантина с антихолинэстеразными средствами не проводилось. В ряде исследований показан положительный эффект #мемантина** на качество жизни у пациентов с деменцией при болезни Паркинсона [298].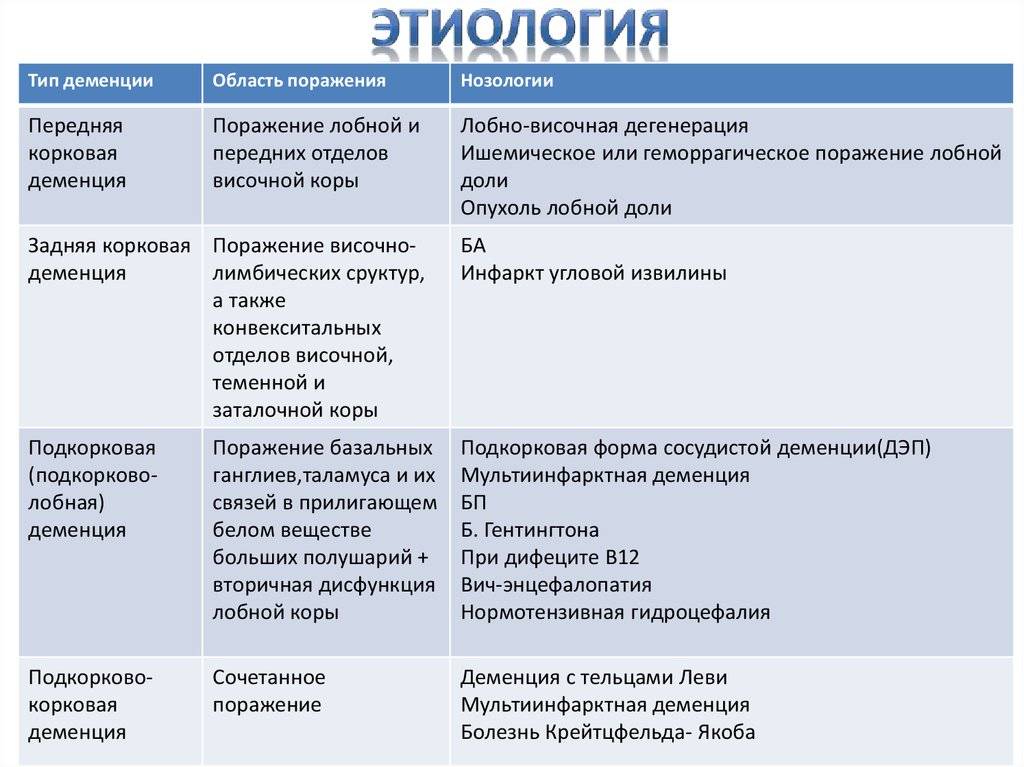
Болезнь Альцгеймера: экспериментальный препарат Леканемаб, по-видимому, замедляет прогрессирование в клинических испытаниях, но вызывает опасения по поводу безопасности
Си-Эн-Эн —
Экспериментальный препарат леканемаб показывает «потенциал» в качестве лечения болезни Альцгеймера, согласно новым результатам испытаний фазы 3, но эти результаты вызывают некоторые опасения по поводу безопасности из-за его связи с некоторыми серьезными побочными эффектами.

Деменция Альцгеймера Hispanos Vive La Salud Азарет Суеньо Хабитос cnnee_00015014.jpg
Эксперты говорят, что после многообещающих данных остается много вопросов по поводу экспериментального лекарства от болезни Альцгеймера.
Долгожданные данные испытаний, опубликованные во вторник в Медицинском журнале Новой Англии, появились примерно через два месяца после того, как производители лекарств Biogen и Eisai объявили, что леканемаб снижает когнитивные и функциональные нарушения на 27% в их испытаниях фазы 3.
Исследование фазы 2 не показало существенной разницы между леканемабом и плацебо у пациентов с болезнью Альцгеймера через 12 месяцев, но данные исследования фазы 3 показывают, что через 18 месяцев леканемаб ассоциировался с более высоким клиренсом амилоида и меньшим снижением когнитивных функций.
«У людей с ранней болезнью Альцгеймера леканемаб снижал уровень амилоида в головном мозге и был связан с меньшим снижением клинических показателей когнитивных функций и функций, чем плацебо, через 18 месяцев, но был связан с побочными эффектами», — пишут исследователи. «Для определения эффективности и безопасности леканемаба на ранних стадиях болезни Альцгеймера необходимы более длительные испытания».
Во вторник Ассоциация Альцгеймера заявила, что приветствует и воодушевлена полными данными Фазы 3.
«Эти рецензируемые опубликованные результаты показывают, что леканемаб предоставит пациентам больше времени для участия в повседневной жизни и самостоятельной жизни.
Испытание фазы 3 проводилось в 235 центрах в Северной Америке, Европе и Азии с марта 2019 года по март 2021 года. В нем приняли участие 1795 взрослых в возрасте от 50 до 90 лет с легкими когнитивными нарушениями из-за ранней стадии болезни Альцгеймера или слабоумия, связанного с болезнью Альцгеймера.

МРТ головного мозга
ШаттерстокЛекарство от болезни Альцгеймера замедляет прогрессирование снижения когнитивных функций в клинических испытаниях, говорят производители лекарств
Исследователи обнаружили, что участники обеих групп имели «клинический рейтинг деменции» или показатель CDR-SB около 3,2 в начале испытания. Такая оценка соответствует ранней стадии болезни Альцгеймера, при этом более высокое число связано с более выраженными когнитивными нарушениями. К 18 месяцам показатель CDR-SB увеличился на 1,21 балла в группе леканемаба по сравнению с 1,66 балла в группе плацебо.
«Значительные различия проявляются уже через шесть месяцев», — заявил во вторник во время презентации на конференции «Клинические испытания болезни Альцгеймера» в Сан-Франциско доктор Кристофер ван Дайк, автор исследования и директор Йельского исследовательского центра болезни Альцгеймера. Франциско.
Франциско.
«Лечение леканемабом соответствовало первичным и вторичным конечным точкам», — сказал он.
Леканемаб, моноклональное антитело, связывается с бета-амилоидом, что является признаком дегенеративного заболевания головного мозга. В начале исследования средний уровень амилоида у участников составлял 77,9.2 сантилоида в группе леканемаба и 75,03 сантилоида в группе плацебо.
Исследователи обнаружили, что к 18 месяцам средний уровень амилоида снизился на 55,48 сантилоида в группе леканемаба и повысился на 3,64 сантилоида в группе плацебо.
Основываясь на этих результатах, «леканемаб может иметь клинически значимое значение для людей, живущих с болезнью Альцгеймера на ранних стадиях, и их семей за счет замедления когнитивного и функционального упадка», — говорит доктор Линн Крамер, главный клинический специалист по болезни Альцгеймера и мозгу. здоровье в Eisai, говорится в сообщении для печати.
Около 6,9% участников исследования в группе леканемаба прекратили исследование из-за нежелательных явлений по сравнению с 2,9% участников в группе плацебо. В целом серьезные нежелательные явления были отмечены у 14% пациентов из группы леканемаба и 11,3% пациентов из группы плацебо.
Наиболее частыми побочными эффектами в группе препаратов были реакции на внутривенные инфузии и аномалии на их МРТ, такие как отек мозга и кровоизлияние в мозг, называемые аномалиями визуализации, связанными с амилоидами, или АВСА.
«Леканемаб в целом хорошо переносился. Большинство нежелательных явлений были связаны с инфузионными реакциями, ARIA-H и ARIA-E, а также головной болью», — заявил на конференции во вторник доктор Марван Саббах, автор исследования и профессор Неврологического института Барроу. Он добавил, что такие события разрешаются в течение нескольких месяцев.
com/_components/paragraph/instances/paragraph_8D06379F-45E0-7DA6-5F03-C56BAC2CEF83@published» data-editable=»text» data-component-name=»paragraph»> Кровоизлияние в мозг при ВСС наблюдалось у 17,3% пациентов, получавших леканемаб, и у 9% пациентов в группе плацебо; Согласно данным исследования, отек головного мозга при АВСА был зарегистрирован у 12,6% пациентов, получавших леканемаб, и у 1,7% пациентов, получавших плацебо. У некоторых людей, получающих АВСА, симптомы могут отсутствовать, но иногда это может привести к госпитализации или стойким нарушениям. И частота АВСА оказалась выше у людей с геном под названием APOE4, который может увеличить риск болезни Альцгеймера и других деменций. Исследователи написали, что ARIA «были численно менее распространены» среди неносителей APOE4.
Болезнь Альцгеймера Мозг Санджай Гупта orig _00002103.png
CNNСогласно сообщениям, экспериментальное лекарство от болезни Альцгеймера могло способствовать смерти участника исследования
Исследователи также написали, что около 0,7% участников в группе леканемаба и 0,8% участников в группе плацебо умерли, что соответствует шести случаям смерти, зарегистрированным в группе леканемаба, и семи в группе плацебо. «Исследователи не сочли, что смертельные случаи связаны с леканемабом или произошли с ARIA», — написали они.
Согласно пресс-релизу, компания намерена подать заявку на одобрение препарата в США к концу марта. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США предоставило леканемабу «приоритетное рассмотрение».
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США предоставило леканемабу «приоритетное рассмотрение».
По сообщению компании, в июле FDA приняло заявку Eisai на получение лицензии Biologics для леканемаба в рамках ускоренного процесса утверждения. Программа позволяет раньше одобрять лекарства, которые лечат серьезные заболевания и «восполняют неудовлетворенные медицинские потребности», в то время как лекарства изучаются в более крупных и длительных испытаниях.
Если испытания подтвердят, что препарат обеспечивает клиническую пользу, FDA выдает традиционное одобрение. Но если подтверждающее исследование не покажет пользы, у FDA есть регуляторные процедуры, которые могут привести к изъятию препарата из продажи.
«Ожидается, что FDA примет решение о предоставлении ускоренного одобрения леканемаба к 6 января 2023 года», — говорится в заявлении Ассоциации по борьбе с болезнью Альцгеймера. «Если FDA сделает это, текущая политика [Центра услуг Medicare и Medicaid] не позволит тысячам и тысячам получателей Medicare с неизлечимой прогрессирующей болезнью получить доступ к этому лечению в течение ограниченного периода времени, который у них будет для доступа к нему. Если пациент решает вместе со своим поставщиком медицинских услуг, что лечение ему подходит, Medicare должна поддержать его, как это происходит в случае с любым другим заболеванием».
«Если и когда это лекарство будет одобрено FDA, врачам потребуется некоторое время, чтобы понять, как это лекарство может или не может быть эффективным у их собственных пациентов», особенно с учетом того, что носители гена АРОЕ4 могут быть в опасности. более высокий риск побочных эффектов, сказал доктор Ричард Исааксон, адъюнкт-профессор неврологии Weill Cornell Medicine, который не участвует в изучении леканемаба или его разработке.
более высокий риск побочных эффектов, сказал доктор Ричард Исааксон, адъюнкт-профессор неврологии Weill Cornell Medicine, который не участвует в изучении леканемаба или его разработке.
«Хотя это исследование, безусловно, обнадеживает, еще предстоит увидеть, как оно отразится на клинической практике, реальной клинической практике», — сказал он о данных исследования фазы 3.
Борьба с болезнью Альцгеймера: где мы сейчас?
В целом, «врачи жаждут любой возможной терапии, которая может помочь нашим пациентам. У меня четверо членов семьи с болезнью Альцгеймера. Если бы член моей семьи пришел ко мне и спросил: «Должен ли я принимать это лекарство?» У правильного пациента, в правильной дозе, в нужной продолжительности, при адекватном и тщательном наблюдении за побочными эффектами, да, я бы предполагают, что этот препарат является жизнеспособным вариантом», — сказал Исааксон. — Я бы сказал, даже важная опция.
— Я бы сказал, даже важная опция.
Он добавил, что экспериментальный препарат служит примером важной потребности в персонализированной медицине в Соединенных Штатах, особенно когда речь идет о болезни Альцгеймера, такой как использование генетического тестирования в клинической практике для идентификации гена АРОЕ, чтобы лучше индивидуализировать подход к лечению. забота о пациенте.
«Это только первая глава в том, что, как я надеюсь, станет действительно длинной книгой о модифицирующих болезнь методах лечения болезни Альцгеймера», — сказал он.
Болезнь Альцгеймера с поздним началом Старческое слабоумие. Симметричное увеличение борозд головного мозга свидетельствует о поражении серого вещества коры головного мозга. Осевой вид в разрезе. (Фото BSIP/UIG через Getty Images)
Симметричное увеличение борозд головного мозга свидетельствует о поражении серого вещества коры головного мозга. Осевой вид в разрезе. (Фото BSIP/UIG через Getty Images)
видео
FDA одобрило лекарство от болезни Альцгеймера
По данным Ассоциации Альцгеймера, более 300 методов лечения болезни Альцгеймера проходят клинические испытания.
Болезнь Альцгеймера была впервые зарегистрирована в 1906, когда доктор Алоис Альцгеймер обнаружил изменения в тканях головного мозга женщины, у которой была потеря памяти, языковые проблемы и непредсказуемое поведение. Изнурительная болезнь в настоящее время поражает более 6 миллионов взрослых в Соединенных Штатах.
Изнурительная болезнь в настоящее время поражает более 6 миллионов взрослых в Соединенных Штатах.
Болезнь Альцгеймера неизлечима, но есть несколько лекарств, отпускаемых по рецепту, которые помогают справиться с симптомами. В прошлом году FDA одобрило Aduhelm для лечения ранних стадий болезни Альцгеймера. До этого FDA не одобряло новую терапию этого состояния с 2003 года.
CNN
видео
Врач говорит, что общее понимание болезни Альцгеймера меняется
Хотя леканемаб тестируется как лекарство от болезни Альцгеймера, это не лекарство, сказала Тара Спайрес-Джонс, заместитель директора Центра научных исследований мозга в Эдинбургском университете, которая не участвовала в испытаниях.
«У обеих групп в испытании симптомы ухудшались, но у людей, принимавших препарат, не так сильно снижались когнитивные способности», — говорится в письменном заявлении Спайрес-Джонс, распространенном британским Центром научных СМИ. «Потребуются более длительные испытания, чтобы убедиться, что преимущества этого лечения перевешивают риски».
В целом болезнь Альцгеймера продолжает оставаться «сложным» заболеванием, заявил в заявлении, распространенном Science Media Center, директор Британского научно-исследовательского института деменции Барт де Струпер.
«Нам еще многое предстоит узнать об основных причинах. Поэтому крайне важно, чтобы мы продолжали инвестировать в научные исследования, и благодаря этому мы также можем определить новые мишени, для которых мы можем разработать методы лечения, которые мы могли бы использовать в сочетании с антиамилоидными препаратами, такими как леканемаб», — сказал Де Струпер, который консультант ряда фармацевтических компаний, включая Eisai, но не консультировал по леканемабу.
Поэтому крайне важно, чтобы мы продолжали инвестировать в научные исследования, и благодаря этому мы также можем определить новые мишени, для которых мы можем разработать методы лечения, которые мы могли бы использовать в сочетании с антиамилоидными препаратами, такими как леканемаб», — сказал Де Струпер, который консультант ряда фармацевтических компаний, включая Eisai, но не консультировал по леканемабу.
«Это испытание доказывает, что болезнь Альцгеймера можно лечить», — сказал он. «Я надеюсь, что мы начнем наблюдать изменение ситуации с хроническим недофинансированием исследований деменции. Я с нетерпением жду будущего, когда мы будем лечить это и другие нейродегенеративные заболевания набором лекарств, адаптированных к индивидуальным потребностям наших пациентов».
Препарат от болезни Альцгеймера леканемаб замедляет снижение когнитивных функций в борьбе с деменцией
- Испытание экспериментального препарата от болезни Альцгеймера было провозглашено «новой эрой» в затянувшейся борьбе за поиск лекарства от деменции.

- Было показано, что леканемаб удаляет скопления белка из мозга пациентов с болезнью Альцгеймера на ранней стадии.
- Болезнь Альцгеймера – это наиболее распространенная форма слабоумия, общий термин для обозначения потери памяти, речи и других мыслительных способностей.
Болезнь Альцгеймера — наиболее распространенная форма деменции, общий термин для обозначения потери памяти, речи и других мыслительных способностей
Брайан Б. Беттанкур | Торонто Стар | Getty Images
Испытание экспериментального лекарства от болезни Альцгеймера было провозглашено «новой эрой» в затянувшейся борьбе за поиск лекарства от деменции.
Результаты клинических испытаний показали, что лекарство леканемаб удаляет скопления белка, называемого бета-амилоидом, которые накапливаются в мозгу людей с болезнью Альцгеймера.
Болезнь Альцгеймера — это наиболее распространенная форма слабоумия, общий термин для обозначения потери памяти, речи и других мыслительных способностей, которые настолько серьезны, что мешают повседневной жизни.
Открытие было названо крупным прорывом в многолетних усилиях исследователей по борьбе с изнурительной болезнью.
Однако авторы отчета предупреждают, что препарат наиболее эффективен у людей с более ранней стадией заболевания, и необходимы дальнейшие испытания для определения его долгосрочных эффектов.
«Леканемаб снижал маркеры амилоида на ранних стадиях болезни Альцгеймера и приводил к умеренно меньшему снижению показателей когнитивных функций и функций», — пишут исследователи в исследовании, опубликованном в Медицинском журнале Новой Англии.
«Для определения эффективности и безопасности леканемаба на ранних стадиях болезни Альцгеймера необходимы более длительные испытания», — добавил он.
«Большой шаг вперед»
Исследование проводилось среди 1795 добровольцев с ранней стадией болезни Альцгеймера в течение 18 месяцев.
Половине раз в две недели вводили леканемаб — антитело, которое заставляет иммунную систему избавляться от амилоида, — а другой половине давали плацебо.
Результаты показали, что ухудшение памяти и умственной активности замедлилось на 27% у пациентов, принимавших леканемаб.
Эти впечатляющие результаты представляют собой важный шаг вперед в исследованиях деменции и могут стать предвестниками новой эры для людей с болезнью Альцгеймера.
Dr Susan Kohlhaas
директор по исследованиям Alzheimer’s Research UK
Важно отметить, что препарат удалил достаточное количество амилоидного белка, поэтому у пациентов не было бы достаточно доказательств болезни Альцгеймера, чтобы претендовать на участие в испытании.
Исследование Alzheimer’s Research UK охарактеризовало результат как «большой шаг вперед» в снижении снижения когнитивных функций у пациентов.
«Эти захватывающие результаты представляют собой важный шаг вперед в исследованиях деменции и могут провозгласить новую эру для людей с болезнью Альцгеймера. испытаний», — сказала директор по исследованиям доктор Сьюзен Кольхас.
Однако она предупредила, что неблагоприятные побочные эффекты препарата доказывают, что это не чудодейственное лекарство.
«Леканемаб был связан с серьезными побочными эффектами, и для регулирующих органов будет важно понять профиль безопасности препарата, прежде чем он получит полную лицензию на использование», — добавила она.
Риск серьезных побочных эффектов
Результаты были представлены на конференции «Клинические испытания болезни Альцгеймера» в Сан-Франциско во вторник. Они последовали за выходом ранее осенью первоклассных результатов от производителей препарата Eisai и Biogen.
Во вторник акции Eisai упали более чем на 6%, а Biogen — примерно на 3,7% после сообщения о том, что 65-летняя женщина умерла от кровотечения после ее включения в исследование леканемаба.
Неясно, была ли смерть непосредственно связана с наркотиками. Женщине дали дополнительное лекарство, известное как активатор тканевого плазминогена (tPA), для очистки от сгустков крови, образовавшихся в результате кровотечения.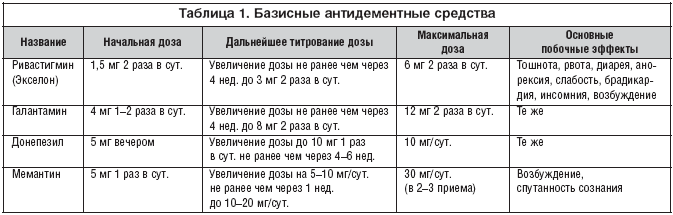

 І. Ісаков
І. Ісаков