Паркинсона симптомы первые: Болезнь Паркинсона – причины возникновения, признаки и симптомы, лечение болезни Паркинсона
Паркинсонизм с ранним началом | Официальный сайт Научного центра неврологии
Паркинсонизм с ранним началом.
На протяжении почти двух веков, прошедших с описания идиопатического паркинсонизма, данная проблема всегда оставалась в фокусе активного интереса со стороны специалистов из самых разных областей нейронаук. Это обусловлено высокой распространенностью заболевания, а также теснейшей взаимосвязью между успехами фундаментальных медико-биологических дисциплин (от патонейроморфологии до биохимии и молекулярной генетики) и прогрессом в разработке новых методов диагностики и лечения паркинсонизма, понимании тонких механизмов его развития.
В настоящее время все случаи паркинсонизма могут быть подразделены на:
- первичный (идиопатический) паркинсонизм. К нему относятся болезнь Паркинсона и особая генетически обусловленная форма раннего паркинсонизма — так называемый ювенильный паркинсонизм;
- вторичный паркинсонизм. Данный синдром развивается в качестве одного из клинических проявлений (осложнений) ряда самостоятельных заболеваний и поражений ЦНС. Наиболее известными вариантами вторичного паркинсонизма являются сосудистый, токсический (в том числе лекарственный), посттравматический и др.;
- паркинсонизм при мультисистемных нейродегенеративных заболеваниях (так называемый паркинсонизм «плюс»). Среди заболеваний, закономерно проявляющихся синдромами паркинсонизма «плюс», следует в первую очередь назвать прогрессирующий надъядерный паралич, множественную системную атрофию, деменцию с тельцами Леви, кортико-базальную дегенерацию;
- паркинсонизм при наследственных заболеваниях ЦНС. Это весьма обширная группа самых разных по генезу заболеваний, которая включает гепатолентикулярную дегенерацию, болезнь Галлервордена-Шпатца, дофачувствительную дистонию, ригидную форму болезни Гентингтона, ряд форм липидозов, митохондриальных энцефалопатий и т.д.
Свыше 70% всех случаев синдрома паркинсонизма в популяции приходится на долю первичного паркинсонизма и, в первую очередь, болезни Паркинсона. Заболевание встречается повсеместно, его частота варьирует от 150 до 300 на 100000 населения, резко увеличиваясь с возрастом. В возрастной группе старше 60 лет данное заболевание встречается у 1-2% лиц, что делает болезнь Паркинсона вторым по распространенности нейродегенеративным заболеванием после болезни Альцгеймера.
Заболевание встречается повсеместно, его частота варьирует от 150 до 300 на 100000 населения, резко увеличиваясь с возрастом. В возрастной группе старше 60 лет данное заболевание встречается у 1-2% лиц, что делает болезнь Паркинсона вторым по распространенности нейродегенеративным заболеванием после болезни Альцгеймера.
В последние годы установлено, что при постепенном, многолетнем развитии болезни Паркинсона наиболее ранние и тонкие изменения (тельца и невриты Леви) обнаруживаются в проекционных нейронах каудальных ядер мозгового ствола, и лишь затем процесс закономерно распространяется на вышележащие отделы мозга. Тем не менее основные симптомы заболевания (тремор покоя, брадикинезия, мышечная ригидность, постуральные нарушения и др.) являются результатом гибели крупных дофамин-продуцирующих нейронов в компактной части черной субстанции среднего мозга, нарушения нигростриарных и других связей и недостаточности дофаминергической трансмиссии в базальных ганглиях. Благодаря механизмам нейропластичности симптоматика появляется лишь в случае гибели >70% пигментных клеток черной субстанции, что соответствует снижению уровня дофамина на 80-85%. В норме в результате процессов естественного старения организма начиная с 5-го десятилетия жизни гибнет от 4,7 до 6% клеток черной субстанции в каждое десятилетие, что и определяет возрастзависимый характер болезни Паркинсона.
В то же время в ряде случаев паркинсонизм может развиваться и в молодом возрасте. Этому аспекту проблемы всегда уделялось гораздо меньше внимания и, более того, сложившаяся многолетняя практика почти гарантированно исключала постановку диагноза «болезнь Паркинсона» при манифестация симптомов до 40 лет. Сегодня наши подходы и сама клиническая практика кардинально изменились, так что появление различных форм первичного паркинсонизма у молодых лиц стало повседневной реальностью врача-невролога.
Интересно, что для ранних случаев паркинсонизма характерны определенные особенности чувствительности к тем или иным группам противопаркинсонических препаратов, свидетельствующие о существовании отличий в патогенезе данных форм по сравнению с «классической» болезнью Паркинсона.
Ранним паркинсонизмом (паркинсонизмом с ранним началом) принято называть случаи первичного паркинсонизма, развившегося в возрасте до 45 лет. В рамках этой возрастной группы нередко выделяется самостоятельная подгруппа лиц с юношеским (ювенильным) паркинсонизмом, у которых первичный паркинсонизм манифестировал в первые два десятилетия жизни (по некоторым авторам — до 25 лет). Подавляющая часть случаев юношеского паркинсонизма связана с рецессивными мутациями недавно открытых генов паркина, DJ.1 и PINK1, продукты которых контролируют процессинг нейрональных белков и особенности окислительного метаболизма нигральных нейронов; эти случаи обозначаются как аутосомно-рецессивный ювенильный паркинсонизм.
Наконец, в молодом возрасте могут манифестировать разнообразные паркинсоновские синдромы, обусловленные некоторыми специфическими токсинами, системными метаболическими расстройствами и другими причинами. Среди токсических паркинсоновских синдромов отметим марганцевый паркинсонизм, ставший в последние годы серьезной проблемой в связи с употреблением лицами преимущественно молодого возраста суррогатных марганецсодержащих наркотических соединений, а также паркинсонизм при употреблении синтетических героинов.
Таким образом, ранний паркинсонизм является чрезвычайно гетерогенным. Далее в настоящем обзоре речь пойдет о первичном паркинсонизме у лиц молодого возраста.
Несколько последних десятилетий охарактеризовались определенной тенденцией к «омоложению» паркинсонизма. Среди причин этого указывают:
- реализацию эффекта ряда генетических факторов;
- растущую подверженность населения развитых стран неблагоприятным эколого-средовым воздействиям;
- улучшение диагностики болезни в ее начальных стадиях, связанное с общим технологическим прогрессом в клинической медицине.
Все эти факторы заслуживают детального рассмотрения.
Возможность развития «истинной» болезни Паркинсона в молодом возрасте подтверждается обнаружением на секции типичной «Леви-патологии» (в том числе с использованием иммуногистохимической окраски на a-синуклеин) в соответствующих отделах головного мозга у лиц, у которых симптоматика асимметричного леводопачувствительного паркинсонизма впервые появилась на 4-5-м десятилетии жизни.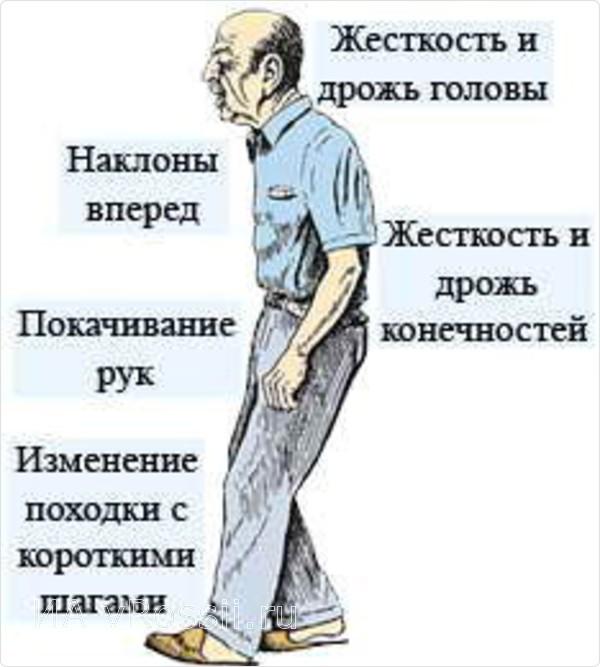 Эти случаи ранней болезни Паркинсона могут носить как спорадический, так и семейный характер. Раннее начало болезни Паркинсона принято связывать, в первую очередь, с генетическими факторами, многие из которых раскрыты и достаточно хорошо изучены благодаря интенсивному прогрессу последних лет в области молекулярной генетики. Показана ассоциация болезни Паркинсона с рядом полиморфизмов в генах детоксикации ксенобиотиков, системы антиоксидантной защиты клетки, транспорта и метаболизма дофамина, липидного обмена, митохондриального цикла. Гены предрасположенности к болезни Паркинсона представлены ниже:
Эти случаи ранней болезни Паркинсона могут носить как спорадический, так и семейный характер. Раннее начало болезни Паркинсона принято связывать, в первую очередь, с генетическими факторами, многие из которых раскрыты и достаточно хорошо изучены благодаря интенсивному прогрессу последних лет в области молекулярной генетики. Показана ассоциация болезни Паркинсона с рядом полиморфизмов в генах детоксикации ксенобиотиков, системы антиоксидантной защиты клетки, транспорта и метаболизма дофамина, липидного обмена, митохондриального цикла. Гены предрасположенности к болезни Паркинсона представлены ниже:
Гены систем клеточной детоксикации и антиоксидантной защиты
- параоксоназа-1
- убиквитин-С-концевая гидролаза L1
- цитохром Р450 (CYP2D6)
- N-ацетилтрансфераза-2
- семейство ферментов глутатин-трансферазы гемоксигеназа-1
- ферменты a-кетоглутарат-дегидрогеназного комплекса
- супероксид-дисмутаза
Гены транспорта и метаболизма дофамина
- моноаминоксидазы А и B
- катехол-О-метилтрансфераза
- тирозингидроксилаза
- транспортеры дофамина
- дофаминовые рецепторы D2, D3, D4 и D5
Митохондриальный геном
- тРНКГлу
- митохондриальная ДНК (отдельные полиморфизмы)
- комплекс I электронной дыхательной цепи
Другие гены
- NO-синтазы (nNOS, iNOS)
- аполипопротеин Е
- нейротрофические факторы
Носительство неблагоприятных аллельных вариантов данных генов достоверно повышает риск заболевания, т.е. формирует генетическую предрасположенность к болезни Паркинсона, которую можно оценить количественно — например, путем стандартного расчета соотношения шансов (показатель OR). Нами и другими исследователями установлено, что выявленные ассоциации (как и семейная кластеризация болезни) значительно выше в группе паркинсонизма молодого возраста. Более того, комбинация нескольких неблагоприятных полиморфизмов усиливает предрасположенность к болезни Паркинсона и ведет к более ранней манифестации симптомов (аддитивный эффект «генов риска»). Таким образом, соотношение генетических и средовых факторов в развития болезни Паркинсона неодинаково в различных возрастных группах больных: в молодой группе пациентов наиболее значим удельный вес генетической составляющей, тогда как у пожилых пациентов роль генетики становится менее четкой, и на первый план выходят средовые и иные факторы.
Более того, комбинация нескольких неблагоприятных полиморфизмов усиливает предрасположенность к болезни Паркинсона и ведет к более ранней манифестации симптомов (аддитивный эффект «генов риска»). Таким образом, соотношение генетических и средовых факторов в развития болезни Паркинсона неодинаково в различных возрастных группах больных: в молодой группе пациентов наиболее значим удельный вес генетической составляющей, тогда как у пожилых пациентов роль генетики становится менее четкой, и на первый план выходят средовые и иные факторы.
Говоря о генетическом грузе, нельзя забывать и о накоплении мутаций митохондриальной ДНК, скорость которого в современных условиях может быть более высокой, а последствия в виде нарушения энергообеспечения нейронов — более драматичными и ранними. Отметим в этой связи, что более чем у половины лиц с болезнью Паркинсона отмечается снижение активности комплекса I митохондрий в различных тканях, в том числе в мозге.
Известным модификатором возраста начала болезни Паркинсона и ряда других нейродегенеративных заболеваний является генетический полиморфизм аполипопротеина Е (ароЕ) — белка, имеющего отношение к репарации клеточных мембран и мобилизации «строительного» холестерина. Как в нашей работе, так и в ряде работ зарубежных авторов было установлено, что наличие аллеля ароЕ-e4 способствует более раннему началу болезни Паркинсона.
В наибольшей степени этот эффект проявляется при гомозиготности по данному варианту ароЕ (генотип e4/e4): в таких случаях, согласно нашим наблюдениям, возраст начала болезни составил 35-37 лет.
По разным данным, от 5 до 10% всех случаев болезни Паркинсона имеют не мультифакторную, а моногенную природу, представляя собой заболевания с аутосомно.доминантным наследованием. Они обусловлены передачей в поколениях патогенетически значимых мутаций в генах a-синуклеина, UCH.L1, LRRK2 и некоторых других. Последний, совсем недавно открытый ген (LRRK2) имеет особое значение, поскольку он может обусловливать до 1% всех случаев болезни Паркинсона в популяции — в том числе (поскольку пенетрантность гена не превышает 70%) при отсутствии четкого семейного анамнеза.
Можно заключить, что в общем ряду случаев «обычной» спорадической болезни Паркинсона нередко «маскируются» те или иные наследственные формы, что подчеркивает гетерогенность данной патологии. Для наследственных случаев болезни Паркинсона характерно относительно раннее появление симптомов: так, в серии на ших случаев заболевание у носителей мутации в гене LRRK2 могло проявиться уже в 39 лет, описаны и более ранние варианты LRRK2.формы болезни Паркинсона.
В ряду факторов, способствующих развитию болезни Паркинсона, большое значение придается подверженности населения развитых стран мира неблагоприятным эколого.средовым воздействиям и, в первую очередь, потенциальным нейротоксинам. Наиболее вероятными кандидатами на роль экзогенных «каузативных» токсинов при болезни Паркинсона являются некоторые пестициды: показано, что в условиях in vitro пестициды способны провоцировать конформационные изменения молекулы a-синуклеина (это ключевой этап патогенеза болезни Паркинсона) и ускорять формирование патологических включений в нейронах. Хроническое системное воздействие пестицидов воспроизводит в эксперименте клинические характеристики болезни Паркинсона. Эпидемиологические исследования подтверждают эти заключения. Так, распространенность болезни Паркинсона в сельских популяциях среди фермеров оказалась почти в 1,4 раза выше по сравнению с городским населением, а риск болезни Паркинсона у работников плантаций — в 1,5-2 раза выше общепопуляционного, что может служить подтверждением роли в развитии заболевания пестицидов и других агентов, контакт с которыми по определению выше у работников, занятых в сельском хозяйстве. Предполагается, что агрессивное агрохимическое производство и соответствующая экологическая обстановка, характерные для ряда регионов мира, могут явиться серьезным фактором, способствующим общему росту заболеваемости болезнью Паркинсона и, при особенно неблагоприятном развитии событий, накоплению более ранних случаев болезни в определенных субпопуляциях. Вероятность манифестации раннего паркинсонизма в такой ситуации особенно возрастает у лиц — носителей неблагоприятных аллельных вариантов «предрасполагающих» генов, отвечающих в организме за процессы клеточной детоксикации (см. выше). Интересно, что ассоциации болезни Паркинсона с аллельными вариантами генов.детоксикантов (CYP2D6, GSTP1 и др.) особенно значимы именно в в группе лиц, имевших контакт с пестицидами. Этот пример наглядно иллюстрирует взаимодействие генетических и средовых факторов в развитии болезни Паркинсона.
Вероятность манифестации раннего паркинсонизма в такой ситуации особенно возрастает у лиц — носителей неблагоприятных аллельных вариантов «предрасполагающих» генов, отвечающих в организме за процессы клеточной детоксикации (см. выше). Интересно, что ассоциации болезни Паркинсона с аллельными вариантами генов.детоксикантов (CYP2D6, GSTP1 и др.) особенно значимы именно в в группе лиц, имевших контакт с пестицидами. Этот пример наглядно иллюстрирует взаимодействие генетических и средовых факторов в развитии болезни Паркинсона.
Определенная роль в увеличении доли молодых пациентов с болезнью Паркинсона принадлежит совершенствованию методов диагностики и улучшению распознавания наиболее ранних случаев болезни (и даже «предболезни»). Отметим, во-первых, внедрение в практику понятия группа риска, к которой принадлежат, в частности, ближайшие родственники пациентов, имеющие в несколько раз более высокую вероятность развития болезни Паркинсона по сравнению с общей популяцией. Именно в этой группе лиц, хорошо осведомленных об имеющейся семейной отягощенности, становится возможным тщательный мониторинг, ориентированный на выявление максимально ранних нарушений в двигательной сфере. Во-вторых, определенное значение имела разработка новейших методов нейровизуализации (КТ и МРТ, ОФЭКТ, ПЭТ), позволяющих осуществлять более точный дифференциальный диагноз и объективизировать тонкие нарушения дофаминового обмена в базальных ганглиях. Наконец, нельзя не отметить роль разработанных международным сообществом унифицированных критериев клинической диагностики болезни Паркинсона, позволивших усовершенствовать и стандартизировать подходы к раннему выявлению и постановке диагноза данного заболевания.
На приведенном ранее рисунке в левой части спектра представлено особое генетически детерминированное заболевание — аутосомно-рецессивный ювенильный паркинсонизм (АР.ЮП), который обусловливает значительную часть случаев «молодого» паркинсонизма и характеризуется рядом своеобразных клинико-морфологических проявлений. Данное заболевание встречается практически во всех изученных популяциях мира.
Данное заболевание встречается практически во всех изученных популяциях мира.
Основное значение в развитии АР-ЮП имеет ген, локализованный на хромосоме 6q и кодирующий новый белок с убиквитин-лигазной функцией — паркин. Показано, что паркин является важнейшим звеном системы клеточной защиты и, в частности, непосредственно участвует в деградации a-синуклеина — классического белкового маркера болезни Паркинсона в составе характерных интранейрональных включений (телец Леви).
Морфологическая картина АР.ЮП характеризуется гибелью нейронов и глиозом в компактной части черной субстанции и голубоватом пятне, отличаясь от «классической» болезни Паркинсона отсутствием телец Леви в дегенерирующих нейронах.
Дебют симптомов АР-ЮП чаще всего приходится на 2-3.е десятилетие жизни, первым проявлением заболевания может быть постепенно развивающийся синдром паркинсонизма либо дистония стоп. Для синдрома паркинсонизма в развернутой стадии АР.ЮП типично сочетание брадикинезии, мышечной ригидности, постуральных нарушений с пирамидными симптомами, а также нередкое отсутствие стадии гемипаркинсонизма.
Особенностью тремора при АР-ЮП является его статокинетический характер, который может сочетаться с типичным паркинсоновским тремором покоя. Проявления дистонии при АР-ЮП, появившись у ряда пациентов в дебюте болезни, могут сохраняться на протяжении многих лет. Важной особенностью болезни, имеющей существенное дифференциально-диагностическое значение, является весьма раннее появление разнообразных и нередко сложных по своей структуре леводопа-индуцированных дискинезий, которые могут возникнуть уже при приеме чрезвычайно низких доз препарата (30-70 мг леводопы). Еще одной отличительной чертой АР-ЮП, отмечаемой у большинства больных, является наличие флуктуаций в выраженности симптомов паркинсонизма и дистонии на протяжении дня: наилучшее состояние отмечается утром или после дневного сна, а к вечеру тяжесть клинических проявлений нарастает. Это сближает клинику АР-ЮП с проявлениями дофачувствительной торсионной дистонии.
Это сближает клинику АР-ЮП с проявлениями дофачувствительной торсионной дистонии.
Гомозиготные мутации гена паркина при первичном паркинсонизме с началом болезни до 20 лет выявляются более чем в 70% семейных и в 15% спорадических случаев. Заметно реже при АР-ЮП выявляются гомозиготные мутации в генах PINK1 и DJ-1. Изредка у гомозиготных носителей мутаций гена паркина описывается начало болезни в более позднем возрасте (вплоть до 6-го десятилетия жизни!), и такие случаи могут быть неотличимы от «классической» болезни Паркинсона [30]. Это демонстрирует определенную условность термина «ювенильный паркинсонизм» применительно к паркин-ассоциированным формам патологии (для обозначения этих синдромов более адекватным представляется получающий всё большее признание термин «паркинопатии»).
Совсем недавно появились основания предполагать, что гетерозиготное носительство мутации в гене паркине иногда достаточно для развития доминантной формы паркинсонизма — наиболее вероятно, в результате падения ниже критического «порога» лигазной активности белкового продукта гена (механизм гаплонедостаточности). Прижизненное ПЭТ-исследование показало отчетливое снижение захвата флюородопы в стриатуме у лиц, имеющих мутантный и нормальный аллель паркина, что является четким нейровизуализационным свидетельством дофаминергической дисфункции у гетерозигот.
С учетом этих данных нами был проведен поиск структурных перестроек в гене паркине у 107 пациентов с ранним паркинсонизмом (возраст начала до 45 лет). При этом мутации паркина были выявлены у 13,1% больных (14 пациентов), в том числе в 12 случаях из 14 — гетерозиготные делеции и дупликации. Аналогичные данные получены и другими исследователями.
Таким образом, гаплонедостаточность по паркину действительно может определять гибель дофаминовых нейронов и служить значимым фактором риска первичного паркинсонизма в молодом возрасте. Подчеркнем, что заболевание у гетерозиготных носителей паркин. мутаций отличается от АР-ЮП по своим генетическим и клиническим характеристикам, являясь самостоятельным и пока еще мало изученным вариантом паркин-ассоциированного паркинсонизма.
мутаций отличается от АР-ЮП по своим генетическим и клиническим характеристикам, являясь самостоятельным и пока еще мало изученным вариантом паркин-ассоциированного паркинсонизма.
Раннее начало первичного паркинсонизма предъявляет повышенные требования к рационализации назначаемой терапии, поскольку такая терапия должна быть ориентирована на длительную перспективу, в идеале — на десятилетия вперед.
Большинство исследователей предпочитает начинать лечение раннего паркинсонизма с агонистов дофаминовых рецепторов (АДР). Целесообразность их использования в данной группе пациентов обусловлена лучшей переносимостью АДР у молодых по сравнению с пожилыми больными, а также необходимостью принимать во внимание возможность быстрого появления выраженных дискинезий у молодых пациентов в случае назначение леводопы (это наиболее типично для различных вариантов ювенильного паркинсонизма). Кроме того, именно для пациентов молодого возраста в начальной стадии болезни важен оказываемый препаратами из группы АДР нейропротекторный эффект (подтвержденный в эксперименте и в некоторых клиниконейровизуализационных исследованиях), что позволяет в определенной степени пролонгировать течение болезни. АДР-опосредованную нейропротекцию связывают с уменьшением синаптического кругооборота дофамина, стимуляцией D1-рецепторов, синтезом белков с антиоксидантными свойствами, стимуляцией аутотрофической активности нейронов, уменьшением секреции эксайтотоксина глутамата.
При необходимости у пациентов молодого возраста АДР можно комбинировать с ингибиторами МАО-В, а также амантадинами (мидантан, ПК-Мерц и др.). Последняя группа препаратов достаточно перспективна для лечения именно молодых случаев паркинсонизма, поскольку имеющиеся данные свидетельствуют о наличии у них свойств антагонистов NMDA-рецепторов глутамата; таким образом, амантадины способны реализовывать свое предполагаемое нейропротекторное действие на уровне «эксайтотоксического каскада».
В молодой возрастной группе для борьбы с тремором (весьма резистентным к терапии симптомом болезни Паркинсона) более свободно могут быть назначены центральные холинолитики, обычно не рекомендуемые у пожилых лиц в связи с большим числом общесоматических противопоказаний, опасностью нарастания когнитивных нарушений и риском развития психотических состояний на фоне атрофии мозга. Следует помнить, что у молодых больных центральные холинолитики назначаются в минимально возможной дозировке, а общая продолжительность непрерывного лечения данными препаратами не должна превышать 3-5 лет.
На определенном этапе болезни при нарастании двигательных нарушений возникает необходимость приема препаратов леводопы. Согласно современным представлениям, «опасность» леводопы с точки зрения ее неблагоприятного влияния на течение болезни Паркинсона остается недоказанной, а несвоевременное (чрезмерно отсроченное) назначение леводопы может нивелировать имеющийся терапевтический потенциал заместительной терапии и, тем самым, оказать негативное влияние на прогноз болезни и качество жизни. Избегая необоснованной «леводопофобии», следует помнить, что у молодых пациентов требуется особенно тщательное «титрование» разовых и суточных доз леводопы, минимизирующее проявления нередко весьма мучительных для больного дискинезий.
Контроль двигательных осложнений леводопа-терапии предполагает назначение разнообразных патогенетических и симптоматических корректоров (АДР, ингибиторы КОМТ и новый комбинированный препарат леводопы Сталево — см. далее, бензодиазепины и др.).
Согласно нашему опыту, не менее чем у половины пациентов с ювенильным паркинсонизмом применение леводопасодержащих препаратов было невозможным без их сочетания с АДР. С учетом ожидаемой продолжительности жизни и необходимости максимального отсрочивания двигательных флуктуаций, у молодых больных стратегически обоснованным представляется начало терапии леводопой с ее пролонгированных форм.
В последние годы появился ряд новых направлений лечения паркинсонизма, связанных как с функциональной нейрохирургией (высокочастотная электростимуляция базальных ганглиев), так и с оригинальными методами трансдермальной доставки противопаркинсонических средств и технологиями малоинвазивной хирургии. Заслуживает внимания так называемая концепция постоянной дофаминергической стимуляции, которая может быть реализована, в частности, посредством дозируемого введения леводопы через постоянную дуоденальную помпу; это позволяет эффективно купировать тяжелые двигательные флуктуации у пациентов в развернутой стадии болезни. Еще один подход, позволяющий пролонгировать и «физиологизировать» эффект леводопы, изящно реализован в новой и чрезвычайно перспективной лекарственной форме, представляющей собой комбинацию леводопы, карбидопы и энтакапона (препарат Сталево). Имеющийся к настоящему времени опыт показывает высокую эффективность Сталево в уменьшении выраженности двигательных флуктуаций и снижении риска развития дискинезий как в клинике, так и в эксперименте, что связывают с улучшенной фармакокинетикой леводопы (одновременное ингибирование периферической дофа-декарбоксилазы и катехол-О-метилтрансферазы). Обсуждается потенциальный протективный эффект Сталево при раннем назначении препарата.
Использование вышеуказанных и ряда других новых технологий при различных формах первичного паркинсонизма показано, в первую очередь, у молодых пациентов, имеющих меньшее число противопоказаний и неблагоприятных прогностических факторов. Это существенно расширяет имеющиеся возможности эффективной помощи людям трудоспособного возраста, страдающим ранним паркинсонизмом, что имеет не только медицинский, но и несомненный социально-экономический эффект.
Иллариошкин С.Н. Атмосфера. Нервные болезни, 3, 2006
Невролог рассказала, как распознать первые признаки болезни Паркинсона
demenciya. ru
ru
Они начинаются задолго до тремора.
Таким мнением поделилась в эфире радиостанции «Говорит Москва» заведующая неврологическим отделением для больных с нарушениями мозгового кровообращения больницы №52 Вера Пшеничникова. По её словам, в первую очередь нужно обращать внимание на обоняние.
«Считается, что всё начинается с моторных форм, когда трясётся одна рука. На самом деле заболевание начинается за 10 лет, иногда за 20 лет. Это постепенно прогрессирующий процесс, люди его не замечают, и начинается он с нарушения обоняния. Болезнь Паркинсона — это системная болезнь головного мозга. Начинается с нарушения обоняния, сна, снижения работоспособности. Эти симптомы могут длиться несколько лет. А затем пациент чувствует ощущение тяжести в плечах. Они часто ходят к неврологам и лечатся с диагнозом остеохондроз. На самом деле это всё стадии болезни Паркинсона, на которых лучше начинать лечение, потому что это продлевает качество жизни больных».
Можно проводить домашние тесты, проверяя чувствительность своего обоняния на кофе или знакомых духах, отметила врач.
«После того, как у пациента развиваются все эти жалобы — обоняние, ощущение, что кто-то сидит на плечах — появляется тремор в одной руке, это уже первая стадия болезни Паркинсона. Потом присоединяется тремор второй половины, больной начинает хуже двигаться, но выполняет свои функции. Затем наступает третья стадия, когда пациенту всё тяжелее двигаться и выражено снижение когнитивных функций. Четвёртая, когда он нуждается в посторонней поддержке, и пятая, когда он полностью обездвижен».
По словам Пшеничниковой, предпосылками к развитию болезни Паркинсона считается не только генеалогическая предрасположенность, но и плохая экологическая обстановка, а также неправильное питание и сопутствующие болезни, например, ожирение или гипертония. Для профилактики заболевания она порекомендовала заниматься физической активностью: спортом или танцами.
Для профилактики заболевания она порекомендовала заниматься физической активностью: спортом или танцами.
Болезнь Паркинсона — методы лечения
Доктор Дитер Фольц,
Руководитель центра лечения болезни Паркинсона в частной клинике «Конфратернитет»
Доктор Фольц, что такое паркинсонизм?
Болезнь Паркинсона — одно из наиболее распространенных заболеваний нервной системы. Паркинсонизм — медленно прогрессирующее неврологическое заболевание, которое поражает в основном определенные части мозга. В этих областях мозга проявляется недостаток нейротрансмиттера дофамина, поскольку нервные клетки, содержащие дофамин, по еще необъяснимым причинам, постепенно отмирают.
Области мозга с нервными клетками, содержащими дофамин, контролируют произвольные и непроизвольные движения. Таким образом, двигательные расстройства являются одним из наиболее частых проявлений болезни Паркинсона.
С 1990 года количество заболеваний во всем мире возросло больше, чем в два раза, что также связано с увеличением продолжительности жизни. Также существенную роль играют ядовитые вещества, использующиеся повсеместно в сельском хозяйстве и промышленности. Это тоже является причиной массового роста заболеваемости в последние годы. Вероятность заболеть болезнью Паркинсона возрастает с возрастом: 1 процент людей после 60 лет больны этим заболеванием, после 80 лет это количество составляет 3 процента.
Каковы первые симптомы болезни Паркинсона?
Снижение содержания дофамина начинается медленно и постепенно, проходит несколько лет или даже десятилетий, пока начинают проявляться симптомы.
Для ранней диагностики заболевания необходимо ответить на 12 вопросов:
- Трясется ли рука в состоянии покоя и успокаивается ли, если что-то взять в руку?
- Согнута ли рука и прижата к телу или она качается при ходьбе?
- Находится ли ваше тело в согнутой позе?
- Вы передвигаетесь небольшими шагами, шаркаете или тянете ногу при ходьбе?
- Ухудшилось ли чувство обоняния по сравнению с прошлым?
- Часто ли вы страдаете от запоров по непонятным причинам?
- Часто ли вы ощущаете боли напряжения в плечах/спине?
- Быстро ли вы отстраняетесь и избегаете социальных контактов?
- Стал ли ваш голос более монотонным, тихим или хриплым?
- Изменился ли ваш почерк? Стал ли он более мелким и неразборчивым?
- Страдаете ли вы от «внутреннего дрожания» или «внутреннего беспокойства»?
- Видите ли вы беспокойные сны, которые сопровождаются движением, разовариваете ли во сне?
Если появляются описанные симптомы, необходимо сразу же обратиться к специалисту-неврологу! Он назначит дополнительные обследования и сможет подтвердить или опровергнуть наличие болезни Паркинсона.
Нефармакологические меры
Физиотерапия, эрготерапия, логопедия, психологическое консультирование и, не в последнюю очередь, обучение и поддержка членов семьи — играют огромную роль в удовлетворительном лечении болезни Паркинсона. Рекомендуется также использование вспомогательных услуг и групп самопомощи.
Какие симптомы типичны для заболевания на прогрессирующей стадии?
- Затруднение движений. Например, сложности вставать из сидячего положения, держать осанку, ходить. Также может затрагиваться артикуляция.
- Оцепенение: длительное напряжение различных мышц ведет к скованности и затрудненным движениям.
- Дрожь (тремор): обычно это начинается с кистей, рук и ног одной стороны тела. Если симптомы проявляются с обеих сторон, чаще всего речь идет не о болезни Паркинсона.
Важно отметить, что заболевший Паркинсонизмом теряет лишь часть коммуникативных навыков, умственные способности полностью сохраняются!
Какими методами проводится терапия?
Медикаментозная терапия
Цель медикаментозной терапии — восстановить недостаток дофамина, замедлить его потерю и скорректировать баланс других нейротрансмиттеров. Помимо этого, следует замедлить развитие заболевания и сохранить нервные клетки мозга как можно дольше (нейропротекция). Дополнительно рекомендуется применение физио- и эрготерапии, а также логопедии и рекомендаций по питанию.
В случаях, когда медикаментозная терапия не приносит нужного эффекта, есть еще одна возможность — глубокая стимуляция мозга. При этой процедуре в мозг внедряются небольшие зонды, через которые поступают импульсы, которые обычно у здорового человека передаются дофамином. В настоящее время этот метод очень хорошо зарекомендовал себя.
Ежедневные физические тренировки также необходимы — потеря выносливости у пациентов с болезнью Паркинсона чаще всего связана с недостаточной физической активностью. Это происходит из-за ограничений движения в связи с течением заболевания.
Это происходит из-за ограничений движения в связи с течением заболевания.
Каковы шансы на излечение?
Полное излечение на данный момент, к сожалению, невозможно. Однако, благодаря новым формам терапии, развитие болезни возможно значительно замедлить. По статистике Паркинсонизм диагностируется только через 10-13 лет после начала болезни. Чем раньше поставлен диагноз, тем лучше можно поддерживать качество жизни.
Каковы шансы на излечение?
Полное излечение на данный момент, к сожалению, невозможно. Шансы генотерапии все еще слишком низки и для применения в клинической практике запрещены. В 2012 году, мы первыми во всем мире провели вакцинацию против болезни Паркинсона. Результаты будут доступны в ближайшее время, но и здесь приходится ждать широкого применения в клинической практике.
Чем раньше поставлен диагноз, тем лучше можно поддерживать качество жизни. Для постановки комплексного диагноза и назначения терапии пациенту нужно пройти расширенное клиническое обследование. Врачебные проверки требуются минимум 1 раз в квартал и могут осуществляться также при помощи телемедицины (видеоконсультации), так как при обследовании не требуется телесный контакт. Терапия должна контролироваться ежегодно.
В частной клинике «Конфратернитет» пациентам предлагается дополнительная возможность для обследования и профилактики. С приложением Encephalog Home Prescription, которое устанавливается на смартфоне (без дополнительного сенсора), вы можете ежедневно измерять подвижность, тремор и ходьбу. Данные генерируются сами по себе и отбражаются в личном кабинете вашего лечащего врача. Таким образом, все изменения могут диагностироваться очень оперативно, считываются тренды развития, и возможно дальнейшее планирование лечения.
Если у Вас появились вопросы или Вы хотите записаться на онлайн консультацию, пожалуйста, свяжитесь с нашим международным отделом!
Контакт
Мы говорим по-русски!
Отправить запрос
У Вас есть вопросы? − Напишите нам!
Вы можете задать вопрос на русском языке. Ответ Вам будет направлен также на русском языке.
Ответ Вам будет направлен также на русском языке.
Болезнь Паркинсона — Американская Медицинская Клиника
Болезнь Паркинсона — это заболевание, которое вызывает гибель нейронов — двигательных нервных клеток, которые вырабатывают медиатор дофамин. По этой причине нарушается координация движений и мышечного тонуса. Основными симптомами болезни Паркинсона являются дрожь, общая скованность, нарушение движений и позы.
Для предотвращения возникновения и развития заболевания обращайтесь в Американскую Медицинскую Клинику. Наши специалисты проведут комплексную диагностику Вашего мозга и ЦНС и обеспечат эффективное лечение. Это гарантирует Вам сохранение бодрости и тонуса тела до преклонных лет!
Симптомы болезни Паркинсона
Первые симптомы и признаки болезни Паркинсона могут проявиться уже после 40 лет, в возрасте старше 65 лет ей подвержен каждый сотый человек.
Основная симптоматика на начальном этапе:
- Общее недомогание — больной ощущает упадок сил и слабость.
- Нарушения походки — больной пошатывается при ходьбе, делает неуверенные и короткие шаги.
- Нарушения речи — больной говорит с неприятным носовым призвуком, теряет мысль, не может закончить предложение.
- Изменения в почерке — больной пишет мелкими и угловатыми «дрожащими» буквами.
- Беспричинные перепады настроения — больной начинает плакать или смеяться, становится агрессивным и раздражительным без видимых причин.
- Нарушения мимики — больной становится менее эмоциональным, создается впечатление, что он надел маску на лицо.
- Ригидность мышц — мышцы больного болезненно напряжены.
-
Дрожь — больной не может контролировать движение мышц — они начинают быстро и ритмично двигаться.
 Поначалу этому подвержена лишь одна рука, затем дрожь распространяется на все конечности.
Поначалу этому подвержена лишь одна рука, затем дрожь распространяется на все конечности.
Отсутствие медицинской помощи в дальнейшем приведет к переходу болезни Паркинсона на следующую стадию. Это обусловит возникновение постоянной боли во всех мышцах и отсутствие их согласованного движения, постоянной сутулости, потере контроля над мочеиспусканием и многим другим осложнениям. Поэтому крайне важно обратиться за медицинской помощью при первых же симптомах болезни Паркинсона.
Врачи Американской Медицинской Клиники проведут комплексную диагностику Вашего мозга и ЦНС и обеспечат эффективное лечение. Это гарантирует Вам сохранение бодрости и тонуса тела на долги года!
Лечение болезни Паркинсона
На ранней стадии болезни Паркинсона возможно медикаментозное лечение. Основным ее компонентом является препарат леводопа (леводофа).
В запущенной ситуации необходимо хирургическое лечение, которое заключается в пересадке больному клеток, которые вырабатывают дофамин.
Помните, что эффективное и безвредное лечение болезни Паркинсона обеспечит только врач! Обращайтесь в Американскую Медицинскую Клинику — мы гарантируем Вам наиболее щадящее и эффективное лечение с наименьшей степенью хирургического вмешательства.
Болезнь Паркинсона | вопросы и ответы
Благодаря современным противопаркинсоническим препаратам, ожидаемая продолжительность жизни пациентов с БП не меньше, чем у их здоровых сверстников.
На начальных стадиях, лечение контролирует моторные симптомы: устраняет или резко уменьшает скованность и замедленность, оказывает умеренный эффект на дрожание и неустойчивость. Качество жизни пациента может нарушаться из-за немоторных симптомов: депрессии, нарушений сна, запоров, нарушений потенции. Лечение этих расстройств не столь эффективно.
В дальнейшем, двигательные симптомы прогрессируют, а возможности лечения ограничиваются осложнениями терапии и усилением флуктуаций (колебания эффективности препарата — выраженности двигательных нарушений, феномен «включения-выключения», феномен «невключения», непроизвольные движения, связанные с уровнем препарата в крови — дискинезии), осложнения лекарственной терапии через 5 лет после начала заболевания развиваются приблизительно у половины пациентов, а через 10 лет — доля таких пациентов достигает 80%. Вероятность осложнений зависит от правильности выбора групп и доз препаратов на каждой стадии болезни.
Вероятность осложнений зависит от правильности выбора групп и доз препаратов на каждой стадии болезни.
Пациенты страдают от симптомов, плохо поддающихся лекарственной коррекции — нарушений ходьбы, постуральной неустойчивости, а также прогрессированием немоторных симптомов, прежде всего апатии и депрессии, в меньшей степени — когнитивных нарушений.
У существенной части пациентов интеллект не страдает даже на поздних стадиях болезни с грубыми двигательными нарушениями. Однако, у большинства пациентов есть характерные личностные черты: «застреваемость» внимания, педантизм, тревожность. Они испытывают страх перед сменой обстановки, изменением схемы лечения, что часто является причиной жалоб и ухудшения самочувствия при радикальной коррекции терапии.
Темп прогрессирования заболевания индивидуален.
Довольно часто, смерть наступает от причин, общих для всех пожилых людей, не связанных с БП, например, онкологического заболевания, инфаркта или инсульта.
Болезнь Паркинсона » Медвестник
Причины и механизмы
развития БП
Согласно современным представлениям в развитии БП имеет значение специфическое взаимодействие генетических и средовых факторов. Для БП имеется четкая тенденция к внутрисемейному накоплению случаев болезни, а ближайшие родственники больных имеют в 2—7 раз более высокий риск развития БП по сравнению с общепопуляционным. С помощью позитронно-эмиссионной томографии (ПЭТ), позволяющей верифицировать пресимптоматическую дисфункцию нигростриарной дофаминергической системы, у клинически здоровых братьев и сестер была установлена более высокая конкордантность по БП среди монозиготных близнецов (55%) по сравнению с дизиготными (18%). Результаты анализа генетических ассоциаций показали определенную роль «аллелей риска» ряда кандидатных генов, имеющих значение в функционировании нигральных нейронов.
Надо отметить, что семейные формы БП отличаются высокой генетической гетерогенностью. На сегодняшний момент идентифицировано как минимум 11 хромосомных локусов и 7 самостоятельных генов. Из наследственных форм БП наиболее частым является аутосомно-рецессивный паркинсонизм (мутации на 6 хромосоме в гене белка паркина) с ранним началом (более 50—70% случаев с дебютом до 25 лет). В позднем возрасте чаще встречаются варианты с аутосомно-доминантным типом наследования в результате мутации в гене LRRK2.Вместе с тем на долю наследственно-семейных форм приходится не более 5—10% случаев БП. Генетический фактор имеет наибольшее значение при дебюте заболевания в молодом возрасте.
На сегодняшний момент идентифицировано как минимум 11 хромосомных локусов и 7 самостоятельных генов. Из наследственных форм БП наиболее частым является аутосомно-рецессивный паркинсонизм (мутации на 6 хромосоме в гене белка паркина) с ранним началом (более 50—70% случаев с дебютом до 25 лет). В позднем возрасте чаще встречаются варианты с аутосомно-доминантным типом наследования в результате мутации в гене LRRK2.Вместе с тем на долю наследственно-семейных форм приходится не более 5—10% случаев БП. Генетический фактор имеет наибольшее значение при дебюте заболевания в молодом возрасте.
БП относится к числу заболеваний пожилого возраста. С увеличением возраста происходит потеря части пула дофаминергических нейронов в компактной части черной субстанции. Каждое десятилетие число нигральных нейронов снижается на 10%. К 60 годам их количество при естественном старении сокращается в 1,5—2 раза. С возрастом снижается активность фермента тирозин-гидроксилазы, регулирующего синтез дофамина. В процессе старения в дофаминергических нейронах накапливается так называемый пигмент старения — меланин, метаболиты которого обладают нейротоксическими свойствами. Увеличивается уязвимость нейронов черной субстанции к воздействию свободных радикалов, которые образуются в процессе окисления дофамина. Активность антиоксидантной системы с возрастом падает, и накапливающиеся свободные радикалы оказывают повреждающее воздействие на нейрональные структуры.
Кроме того, с возрастом повышается чувствительность дофаминсинтезирующих нейронов к пропаркинсоническим агентам. Пропаркинсонические свойства обнаружены у многих экзогенных токсинов: моно- и дисульфид углерода, марганец, цианиды, гербициды, пестициды, продукты кобальтовой и ртутной промышленности, пиридиновые производные органических растворителей. Вероятнее всего, имеет значение длительная интоксикация токсическими препаратами, часто в сочетании с нарушением детоксицирующих свойств печени.
Изучается роль эмоционального стресса в развитии заболевания. Клинический опыт показывает, что многие пациенты связывают развитие заболевания с психологическим стрессом. Доказано, что чрезмерные психологические и физические нагрузки могут истощать резервы компенсации дофаминергических структур и приближать момент дебюта заболевания.
Клинический опыт показывает, что многие пациенты связывают развитие заболевания с психологическим стрессом. Доказано, что чрезмерные психологические и физические нагрузки могут истощать резервы компенсации дофаминергических структур и приближать момент дебюта заболевания.
В основе БП лежит нейродегенеративный процесс, приводящий к прогрессирующей гибели нейронов черной субстанции. С течением заболевания дегенеративный процесс становится более распространенным, выходит за рамки черной субстанции и захватывает ядра ствола, лимбические структуры, кору головного мозга. Повреждение нигральных нейронов происходит по механизму апоптоза и связано с нарушением внутриклеточного метаболизма — оксидантным стрессом, эксайтотоксическим действием возбуждающих аминокислот — глутамата и аспартата, запуском механизмов кальциевого каскада, дисфункцией митохондрий.
Дофамин является медиатором нигростриарного, мезолимбического и мезокортикального путей. Дефицит дофамина в нигростриарном пути приводит к развитию основных моторных проявлений БП, дисфункции мезолимбического и мезокортикального путей к когнитивным и аффективным нарушениям при этом заболевании. Первые симптомы БП появляются, когда содержание стриарного дофамина падает на 60—80% от возрастной нормы. Дефицит дофамина в стриатуме ведет к относительному переизбытку ацетилхолина. Дисбаланс нейромедиаторов приводит к нарушению соотношения между возбуждающими и тормозными влияниями внутри базальных ганглиев. Развивается чрезмерная тормозная активность базальных ганглиев по отношению к коре, что является причиной брадикинезии и ригидности. Возникновение тремора связывают с усилением спонтанной осцилляторной активности нейронов полосатого тела и зрительного бугра.
Основные клинические
проявления БП
Заболевание развивается преимущественно в возрасте 55—70 лет. Ядро клинической картины составляет триада симптомов — брадикинезия, тремор покоя, мышечная ригидность. Болезнь может начаться с каждого из этих симптомов, а в дальнейшем к нему присоединяются другие. Четвертый важнейший признак заболевания — постуральная неустойчивость?— обычно присоединяется на более поздней стадии заболевания.
Четвертый важнейший признак заболевания — постуральная неустойчивость?— обычно присоединяется на более поздней стадии заболевания.
Брадикинезия представляет собой снижение спонтанной двигательной активности. Первые жалобы больных могут быть связаны с нарушением мелкой моторики — неловкость при застегивании пуговиц, завязывании шнурков, при нарезании продуктов, замедление письма. Эти изменения возникают, как правило, в одной руке или ноге и постепенно прогрессируют. Скованность переходит на проксимальные отделы, распространяется на другую конечность той же стороны, а затем и на другую сторону. У больных с БП, прежде всего, затруднено начало движения. Больному бывает трудно встать со стула, сделать первый шаг, изменить положение тела в постели. Походка становится замедленной, шаркающей. Впоследствии присоединяются пропульсии и латеропульсии. Распространение гипокинезии на мышцы лица приводит к гипомимии, лицо становится маскообразным. К проявлениям гипокинезии относятся частые поперхивания во время еды, монотонность речи, микрография.
Тремор. Для БП характерен тремор покоя в дистальных отделах руки или ноги. В мышцах кисти наблюдаются движения по типу «скатывания пилюль» или «счета монет». При прогрессировании заболевания тремор может распространяться на проксимальные отделы конечностей и приобретать более сложный рисунок. Амплитуда тремора может меняться в зависимости от эмоционального состояния пациента, но его частота остается неизменной — 4—6 Гц. У некоторых больных при генерализации процесса отмечается тремор головы, нижней челюсти, губ, языка. По мере прогрессирования заболевания часто присоединяется постуральный тремор (т.е. тремор вытянутых рук или ног) и нередко интенционный компонент. Статическое напряжение в ряде случаев ведет к ослаблению тремора. Некоторые больные стремятся постоянно носить что-либо в руке, подавляя или уменьшая, таким образом, дрожание. Обнаруживается связь тремора с уровнем бодрствования: непосредственно после сна и во время расслабленного бодрствования интенсивность тремора уменьшается. Во время сна тремор исчезает.
Во время сна тремор исчезает.
Мышечная ригидность — представляет собой пластическое повышение мышечного тонуса, обусловленное одновременным сокращением агонистов и антагонистов. Мышечная ригидность затрудняет произвольные движения. При наложении тремора на пластический тонус появляется симптом «зубчатого колеса». Преобладание ригидности в вентральных мышечных группах приводит к сгибанию головы и сгорбленной позе. Так же как и другие симптомы БП, ригидность выявляется сначала на одной стороне, а затем носит двусторонний характер.
Постуральные нарушения складываются из нарушения позы, статики, походки. Больные с БП имеют характерный внешний вид: голова опущена, туловище наклонено вперед, руки согнуты в локтях, лицо маскообразно. Ходьба мелкими шагами, шаркающая, при этом руки не совершают синергичных движений во время ходьбы (ахейрокинез). При попытке начать движение возникает симптом «топтания», нередко в этот момент возникают спонтанные падения. Тело больного наклоняется вперед, а ноги остаются «прилипшими» к полу.
Вегетативная недостаточность. Для больных с БП характерны такие вегетативные нарушения, как слюнотечение, запоры, расстройства мочеиспускания, импотенция, ортостатическая гипотензия, сальность кожных покровов.
Заболевание носит неуклонно прогрессирующий характер. Стадию гемипаркинсонизма неизбежно сменяет стадия двусторонних нарушений. На поздних стадиях болезни наступает тяжелая обездвиженность, требующая постоянного постороннего ухода. В большинстве случаев смерть больных БП наступает от соматических осложнений — бронхопневмонии, уросепсиса и других инфекционных осложнений.
Развитие БП нередко осложняется присоединением когнитивных нарушений. Когнитивные нарушения различной тяжести встречаются у 80—90% больных и имеют тенденцию к прогрессированию. В некоторых случаях деменция развивается уже в первые годы заболевания, в других — через 10—20 лет. Наиболее часто присоединение когнитивных нарушений наблюдается через 5—7 лет от начала болезни. Самым значимым фактором риска развития деменции при БП является пожилой и старческий возраст. Успехи современной фармакотерапии БП привели к увеличению продолжительности жизни пациентов, но в то же время обострилась проблема деменции при этом заболевании. Определенный вклад в развитие деменции вносят лекарственные препараты, в частности холинолитики, способствующие нарастанию ацетилхолинергического дефицита в коре головного мозга. Когнитивные, психотические нарушения при адекватно подобранной терапии двигательных расстройств становятся наиболее дезадаптирующим фактором и значительно осложняют проблему ухода за такими больными.
Самым значимым фактором риска развития деменции при БП является пожилой и старческий возраст. Успехи современной фармакотерапии БП привели к увеличению продолжительности жизни пациентов, но в то же время обострилась проблема деменции при этом заболевании. Определенный вклад в развитие деменции вносят лекарственные препараты, в частности холинолитики, способствующие нарастанию ацетилхолинергического дефицита в коре головного мозга. Когнитивные, психотические нарушения при адекватно подобранной терапии двигательных расстройств становятся наиболее дезадаптирующим фактором и значительно осложняют проблему ухода за такими больными.
Психотические нарушения, как правило, провоцируются приемом противопаркинсонических средств и бывают представлены в виде зрительных, реже слуховых галлюцинаций, иллюзиями, бредом. У большинства больных галлюцинации носят обратимый характер и проходят при снижении дозы или отмене того или иного дофамиметического средства. Предиктором галлюцинаций нередко являются яркие сновидения.
Аффективные нарушения в виде депрессии, тревоги, апатии, обсессивно-компульсивного синдрома часто встречаются при БП. Депрессия может появиться на любом этапе заболевания, а в ряде случаев предшествует моторным проявлениям болезни. У большинства больных выраженность депрессивной симптоматики бывает легкой или умеренной. Частыми признаками депрессии при БП являются угнетенный фон настроения, ангедония (неспособность испытывать удовольствие), быстрая утомляемость, снижение аппетита, тревожность, раздражительность, нарушения сна. В то же время такие частые проявления депрессии, как чувство вины, тоски, а также суицидальные мысли и попытки, встречаются нечасто. Распространенность депрессии выше у лиц женского пола, с ранним дебютом заболевания. Ряд авторов отмечает корреляцию между депрессией и выраженностью акинетико-ригидного синдрома. Обычно более выраженные аффективные нарушения встречаются в первые три года заболевания, затем происходит адаптация к заболеванию, а с появлением осложнений дофасодержащей терапии вновь нарастает частота депрессий.
Диагностика БП
Диагностика БП базируется на клинических критериях. Чаще всего используются критерии Hughes A. J. (1992 г.). Необходимым условием является наличие брадикинезии в сочетании не менее чем с одним из следующих основных симптомов паркинсонизма — тремором покоя, ригидностью и постуральной неустойчивостью. Важным дополнительным критерием служит прогрессирующий характер заболевания в сочетании с положительной реакцией на терапию дофасодержащими препаратами.
К дополнительным методам диагностики можно отнести ПЭТ с использованием радиофармпрепарата 6-(18F)флюродопы. Изменения в виде снижения накопления флюродопы, выявляемые этим методом, опережают по времени клинические проявления болезни. Кроме того, ПЭТ позволяет отдифференцировать БП от других форм паркинсонизма (при мультисистемной атрофии, прогрессирующем надъядерном параличе, сосудистом паркинсонизме). Вместе с тем стоимость ПЭТ с данным радиоизотопом очень высока и используется во всем мире нечасто. В России такие исследования до настоящего времени не проводились. Методы томографии могут быть использованы лишь для исключения некоторых форм вторичного паркинсонизма (сосудистого, гидроцефального, на фоне объемного образования), но не для диагностики БП. Информативность методов функциональной диагностики на сегодняшний день не подтверждена.
Лечение БП
Лечение должно быть непрерывным и начинаться с момента появления бытовой и профессиональной дезадаптации. На самых начальных стадиях болезни (например, при легком треморе одной руки) можно не назначать специфической терапии, ограничиваясь рекомендациями по соблюдению высокой двигательной активности. Имеются данные о положительном влиянии физических упражнений на выраженность брадикинезии, постуральных нарушений. Особое значение должно уделяться упражнениям на разгибательную группу мышц для предотвращения развития сгибательной установки туловища.
Оптимальными препаратами для старт-терапии БП считаются препараты с потенциально нейропротективным действием.
Агонисты дофаминовых рецепторов (АДР) наиболее часто рекомендуют в качестве средств начальной терапии БП. Противопаркинсонический эффект этой группы препаратов связан со стимуляцией дофаминовых рецепторов. Эффективность применения АДР на ранних стадиях БП сопоставима с препаратами леводопы. Их раннее назначение приводит к снижению риска возникновения моторных флуктуаций и лекарственных дискинезий. АДР эффективны в отношении основных симптомов болезни — брадикинезии, ригидности, тремора. Обладают умеренным антидепрессивным эффектом, некоторые способствуют улучшению когнитивных функций.
Амантадины являются антагонистами глутамата и снижают патологическое действие глутамата на нигральные нейроны, в связи с чем предполагается наличие у них нейропротективного эффекта. Кроме того, амантадины увеличивают синтез дофамина в пресинаптических терминалях, его высвобождение в синаптическую щель и уменьшают обратный захват дофамина в синаптической щели. Назначение амантадинов приводит к уменьшению мышечной ригидности, акинезии; в меньшей степени влияют на тремор. Особенностью действия амантадинов является их антидискинетический эффект. В связи с этим препараты этой группы назначают как на ранней стадии БП, так и в сочетании с препаратами леводопы для уменьшения дискинезий. Инфузионная форма амантадинов может использоваться для лечения тяжелых форм заболевания (акинетических кризов), у больных с дисфагиями, а также в качестве начальной терапии амантадинами, позволяющей добиться быстрейшего улучшения симптоматики.
Ингибиторы моноаминооксидазы (МАО) типа В блокируют фермент, способствующий метаболизму дофамина по пути окислительного дезаминирования, в результате чего способствуют увеличению содержания нейромедиатора. Кроме того, повышают чувствительность дофаминовых рецепторов, что ведет к увеличению высвобождения дофамина. В эксперименте был показан антиоксидантный эффект этой группы препаратов. Ингибиторы МАО типа В являются мягкими противопаркинсоническими препаратами и рекомендуются к применению на ранней стадии заболевания, а также в комбинированной терапии с препаратами леводопы для коррекции моторных флуктуаций.
Холинолитики — старейшая группа противопаркинсонических препаратов. В настоящее время они обычно назначаются относительно молодым пациентам (до 55 лет), без когнитивных нарушений, имеющих тремор покоя, резистентный к терапии леводопой и АДР. Ограничением к применению этих препаратов является большое количество побочных эффектов — галлюцинации, дезориентация, повышение внутриглазного давления, нарушение аккомодации, нарушение сердечного ритма, задержка мочеиспускания. Их нельзя назначать пациентам старше 55—60 лет, поскольку они усиливают когнитивную дисфункцию и способствуют развитию деменции.
При неэффективности моно- или комбинированной терапии препаратами вышеуказанных групп переходят к назначению препаратов леводопы.
Леводопа является предшественником дофамина и в головном мозгу превращается в дофамин (сам дофамин не проникает через гематоэнцефалический барьер). Она назначается в комбинации с ингибитором декарбоксилазы — ингибиторами периферического распада леводопы. Леводопа до сих пор считается «золотым стандартом» лечения БП с точки зрения эффективности и переносимости. Больным старше 70—75 лет можно назначать препараты леводопы в качестве старт-терапии, т.к. и ожидаемая продолжительность жизни, и риск развития лекарственных дискинезий у них меньше.
Новым направлением дофатерапии, позволяющим повысить биодоступность леводопы и реализовать стратегию постоянной дофаминергической терапии, является применение интрадуоденальной формы леводопы. С помощью чрескожной эндоскопической гастротомии с установкой дуоденального зонда или гастротомии устанавливается постоянный доступ к кишечнику, и препарат дозированно вводится через индивидуально программируемую помпу. Эти операции уже получили широкое распространение в странах Европы и в ближайшем будущем планируется их проведение в РФ.
Нейрохирургическое направление также имеет большое значение и перспективы для лечения БП. Деструктивные стереотаксические операции применяются все меньше и меньше. Наиболее часто используется глубинная стимуляция мозга, предпочтительной точкой стимуляции является субталамическое ядро. Показаниями к проведению подобной операции являются тяжелые формы БП, не поддающиеся адекватной коррекции антипаркинсоническими препаратами, тяжелые моторные флуктуации и лекарственные дискинезии, выраженный интактный к медикаментозной коррекции тремор. При успешной операции состояние пациентов в период «выключения» улучшается на 70%. Причем эффект от операции может сохраняться длительное время.
Наиболее часто используется глубинная стимуляция мозга, предпочтительной точкой стимуляции является субталамическое ядро. Показаниями к проведению подобной операции являются тяжелые формы БП, не поддающиеся адекватной коррекции антипаркинсоническими препаратами, тяжелые моторные флуктуации и лекарственные дискинезии, выраженный интактный к медикаментозной коррекции тремор. При успешной операции состояние пациентов в период «выключения» улучшается на 70%. Причем эффект от операции может сохраняться длительное время.
Отдельно разрабатываемым направлением в лечении БП является использование стволовых клеток и генной терапии с применением трофических пептидных факторов.
В заключение хочется отметить, что эффективность долгосрочного лечения БП определяется тесным взаимодействием лечащего врача, пациента и его родственников. Постоянная коррекция терапии позволяет избежать возможных побочных явлений и сохранить высокий уровень двигательной активности. Не надо забывать о коррекции сопутствующих когнитивных и эмоционально-аффективных расстройств. Развившаяся депрессия может явиться причиной стойкого ухудшения симптомов заболевания и снизить комплаентность больного. Важным дополнительным методом терапии БП является лечебная физкультура. Сохранение высокого уровня физической активности положительно влияет на выраженность симптомов болезни, предотвращает развитие вторичных костно-мышечных изменений. Сбалансированной должна быть диета больных с БП. В рацион питания должна быть включена волокнистая пища и достаточное количество жидкости для профилактики нарушений перистальтики кишечника. Если у пациента снижается масса тела или он вынужден снижать количество белковой пищи (для улучшения адсорбции препаратов леводопы), необходимо увеличить содержание углеводов и ненасыщенных жиров.
Е.А.КАТУНИНА, доктор медицинских наук, доцент кафедры неврологии и нейрохирургии лечебного факультета РГМУ
Результаты проведенного в 2006 г.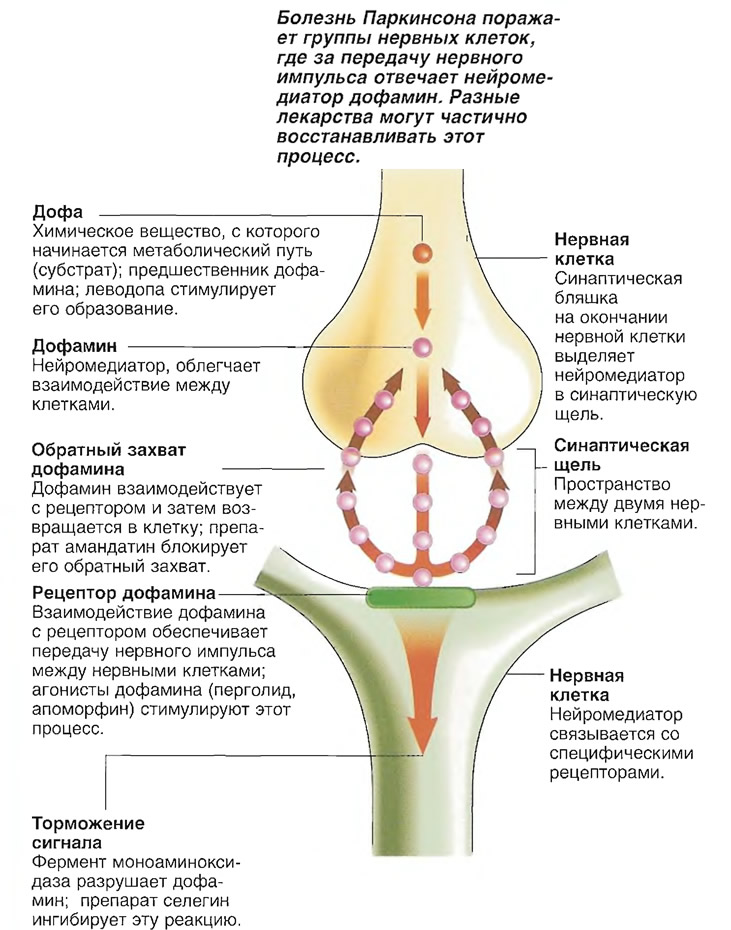 эпидемиологического исследования в 15 странах Западной и Восточной Европы, Азии, Африки позволили сделать прогноз по распространенности БП к 2030 г. В 14 странах из 15 (кроме Нигерии) прогнозируется повышение распространенности БП. В РФ численность больных с БП увеличится с 0,21 до 0,34 млн.
эпидемиологического исследования в 15 странах Западной и Восточной Европы, Азии, Африки позволили сделать прогноз по распространенности БП к 2030 г. В 14 странах из 15 (кроме Нигерии) прогнозируется повышение распространенности БП. В РФ численность больных с БП увеличится с 0,21 до 0,34 млн.
Описание заболевания принадлежит английскому врачу Джеймсу Паркинсону. В 1817 г. вышла его книга «Эссе о дрожательном параличе», в которой он обобщил свои клинические наблюдения.
Эффективность долгосрочного лечения БП определяется тесным взаимодействием лечащего врача, пациента и его родственников. Постоянная коррекция терапии позволяет избежать возможных побочных явлений и сохранить высокий уровень двигательной активности.
11 апреля — Всемирный день борьбы с болезнью Паркинсона
11 апреля — Всемирный день борьбы с болезнью Паркинсона
По данным Европейской ассоциации болезни Паркинсона (EPDA), от этого заболевания страдает около 10 миллионов человек во всем мире. Однако эти цифры могут быть сильно занижены из-за несвоевременного обращения пациентов к врачу и поздней диагностики патологии, которая до сих пор изучена недостаточно хорошо. Что нам известно на сегодняшний день? Врач-невролог Международного медицинского центра «СОГАЗ», к.м.н. Ольга Александровна Амелина ответила на 7 вопросов о болезни Паркинсона.
— В каком возрасте обычно возникает болезнь Паркинсона?
— Болезнь Паркинсона чаще развивается во второй половине жизни, обычно её диагностируют у пациентов старше 50-60 лет. Однако заболевание может начаться и раньше, что, как правило, обусловлено генетической предрасположенностью.
— Из-за чего возникает болезнь?
— Болезнь Паркинсона — это прогрессирующее нейродегенеративное заболевание головного мозга. Оно развивается вследствие гибели нервных структур, отвечающих за выработку нейромедиаторов — биологически активных веществ, с помощью которых осуществляется передача нервных импульсов в мозге.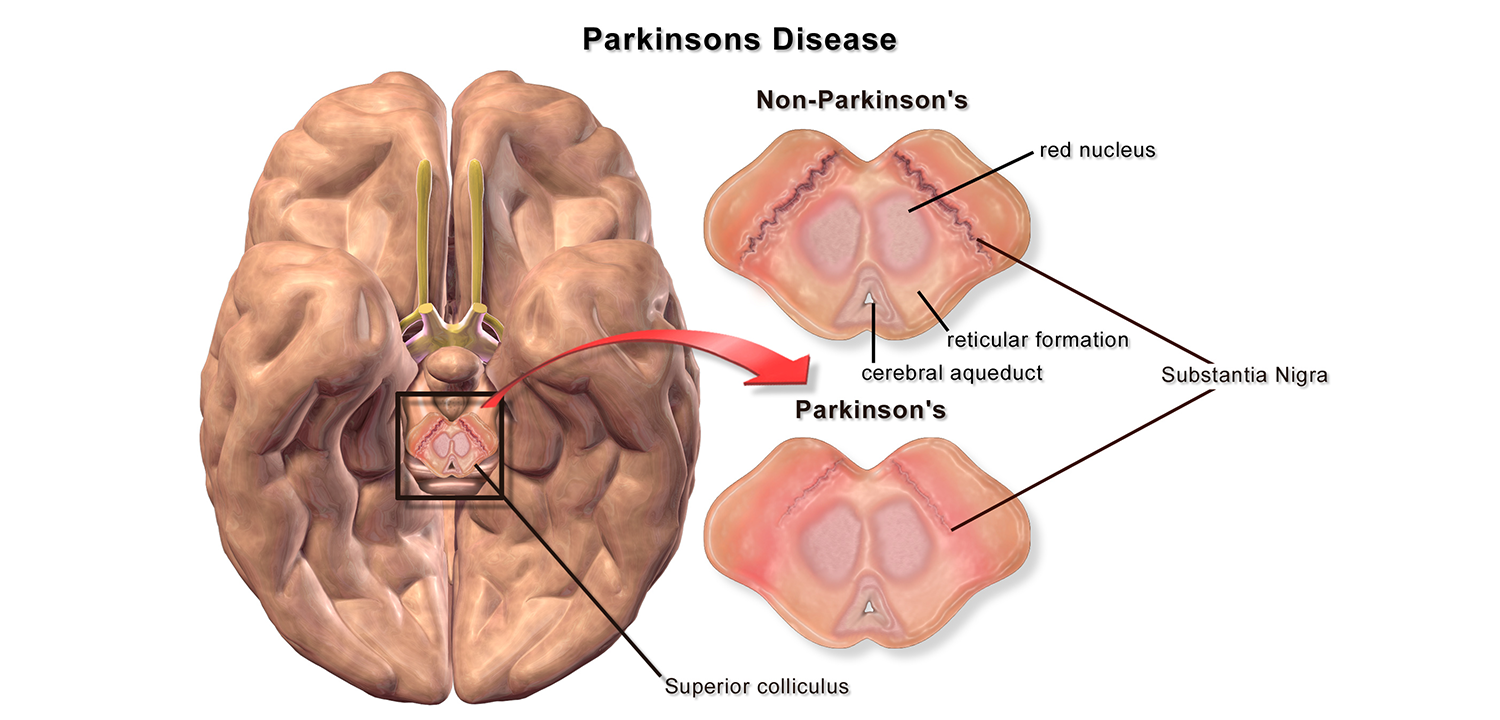
Одним из важнейших нейромедиаторов, регулирующих работу нервной системы, является дофамин. Он отвечает за плавность и координацию движений. У больных паркинсонизмом дофамин не продуцируется в достаточном количестве, поэтому происходят нарушения двигательной активности. Этот процесс называется первичным паркинсонизмом (собственно, болезнью Паркинсона).
Развитие вторичного, симптоматического паркинсонизма возможно из-за отравления, например, угарным газом, и злоупотребления некоторыми лекарственными средствами.
Существует и посттравматический синдром паркинсонизма, вызванный повторяющимися травмами головы, например, у профессиональных боксеров.
— Какие первые симптомы указывают на развитие болезни?
— Первые симптомы развиваются постепенно, не всегда заметно для окружающих и самого пациента. Среди них:
- снижение двигательной активности — общая мышечная скованность
- нарушение мимики — малоподвижное, маскообразное лицо
- замедленная, тихая речь
- нарушение осанки (т.н. «поза просителя»), возникающее по причине изменения мышечного тонуса
Нередко заболевание начинается со специфического гиперкинеза — мелкого размашистого тремора рук. Движения большого и указательного пальцев напоминают «счет монет» или «скатывание пилюль». Тремор начинается чаще с правой руки в виде ритмичных медленных самопроизвольных движений кисти, постепенно он распространяется на правую, а затем и на левую половину тела.
— Какие методы помогут обнаружить болезнь Паркинсона?
— В первую очередь, необходимо исключить другие заболевания нервной системы, сопровождающиеся синдромом паркинсонизма. Для этого выполняют МРТ головного мозга. На нем при хорошей визуализации можно увидеть атрофию (уменьшение размера) глубоких подкорковых структур мозга. Пожалуй, это единственный объективный критерий наличия болезни Паркинсона. Как правило, вместе с этим выявляют признаки хронической ишемической болезни мозга.
Пожалуй, это единственный объективный критерий наличия болезни Паркинсона. Как правило, вместе с этим выявляют признаки хронической ишемической болезни мозга.
Клиническая диагностика болезни Паркинсона состоит из осмотра, опроса, выявления типичной неврологической картины и сопутствующих когнитивных нарушений в разной степени выраженности. Указывать на болезнь может и снижение артериального давления.
— Почему у больных возникает тремор?
— Паркинсонизм даже называют «дрожательный паралич». Ритмичный гиперкинез развивается из-за повышения мышечного тонуса и неравномерной выработки медиатора движения — дофамина. Тремор при паркинсонизме обычно не затрагивает голову.
— Расскажите, пожалуйста, о лечении болезни Паркинсона.
— Терапия этого заболевания направлена на стимуляцию выработки собственных нейромедиаторов — стимуляторов дофаминовых рецепторов. Лечение проводится пожизненно и включает прием препаратов Леводопы в различных комбинациях с блокаторами декарбоксилазы. Дополнительно применяют ингибиторы ферментов, разрушающих дофамин. Используют и препараты для коррекции настроения, памяти, улучшения метаболических процессов головного мозга.
Немедикаментозная терапия включает в себя массаж, лечебную гимнастику, физиотерапевтические процедуры, эрготерапию (регулярные тренировки навыков, необходимых для самообслуживания в повседневной жизни).
— Если у моего близкого человека болезнь Паркинсона, чем я могу помочь, чтобы облегчить его состояние?
— Паркинсонизм развивается по стадиям. Прогрессируя, он проявляется уже не только в виде мышечно-двигательных расстройств. Постепенно происходит замедление мыслительной деятельности, а затем и интеллектуальное снижение.
Если ваш близкий человек страдает паркинсонизмом, наберитесь терпения: у пациентов могут развиваться специфические личностные изменения, проще говоря «портиться характер» — они могут постоянно жаловаться, плохо спать, часто падать из-за сниженного артериального давления, также у них нередко возникает депрессия.
Рекомендации по уходу за человеком, страдающим болезнью Паркинсона:
-
Попробуйте завести дневник и ежедневно записывать в него симптомы и проблемы, с которыми сталкивается больной, чтобы сообщить о наиболее частых трудностях лечащему врачу.
-
Важно поддерживать физическую активность больного. Для этого стоит согласовать программу ежедневных физических упражнений с инструктором по лечебной физкультуре. Регулярные тренировки не только помогут увеличить объем движений в суставах, но и уменьшить боли в мышцах, восстановить осанку, равновесие, улучшить механизм ходьбы.
-
Снизить риски падений и облегчить передвижения помогут поручни, прикрепленные на стены по периметру квартиры.
-
Пациенту следует выбирать удобную одежду, которую он бы смог снимать и надевать без труда. Лучше отказаться от изделий с пуговицами, а использовать вместо них липучки или молнии.
-
Целесообразно сделать ручки мебели более массивными, чтобы больному проще было браться за них руками.
-
Для облегчения приема пищи приобретите ложки, ножи и вилки с увеличенной рукояткой (их можно сделать и самостоятельно, просто обмотав ручки тканью), тарелки и блюда с высокими краями. Процесс питья облегчат трубочки или кружки с двумя ручками.
Помните, что при первых признаках заболевания важно обратиться к врачу. Своевременная и правильно подобранная терапия поможет значительно отдалить и сгладить осложнения паркинсонизма.
11 Апреля 2021
Tremor | Фонд Паркинсона
Типичный тремор Паркинсона возникает в основном в состоянии покоя («тремор покоя») и ослабевает во время сна и когда часть тела активно используется. Например, ваша рука может дрожать, пока вы сидите или даже идете, но когда вы протягиваете руку, чтобы пожать кому-то руку, тремор менее заметен или полностью проходит.
Тремор, как правило, возникает в руках и часто описывается как «катание таблетки»: представьте, что вы держите таблетку между большим и указательным пальцами и непрерывно катите ее.Но он также может появиться на других частях тела, включая нижнюю губу, челюсть или ногу. Этот тремор может мешать рутинным действиям, таким как бритье, одевание, письмо и многие другие задачи, требующие мелкой моторной координации.
Некоторые люди сообщают о внутреннем треморе, ощущении тряски внутри груди, живота или конечностей, которые не видны.
Тремор обычно поражает только одну сторону тела, особенно на ранних стадиях заболевания. По мере прогрессирования болезни могут пострадать обе стороны.Усталость, стресс или сильные эмоции могут временно усилить тремор.
Кто страдает от тремора?
Около 70% людей с болезнью Паркинсона испытывают тремор в какой-то момент болезни. Тремор, по-видимому, немного реже встречается у молодых людей с БП, хотя он по-прежнему является одним из самых неприятных симптомов. У людей с тремором в покое болезнь обычно прогрессирует медленнее, чем у людей без тремора.
Тремор при других состояниях
Хотя тремор является распространенным симптомом болезни Паркинсона, он также может быть симптомом других состояний, в первую очередь эссенциального тремора.Основное различие между тремором Паркинсона и большинством других типов тремора заключается в том, что тремор в состоянии покоя встречается чаще всего. Другие состояния обычно характеризуются «тремором действия», который имеет тенденцию уменьшаться в состоянии покоя и усиливаться, когда вы что-то делаете, например, пытаетесь позвонить или выпить.
Тремор головы и голоса также часто встречается при эссенциальном треморе, но редко при болезни Паркинсона.
Управление тремором
Леводопа — это лекарство, которое чаще всего назначают для контроля двигательных симптомов болезни Паркинсона, а тремор обычно — хотя и не всегда — поддается лечению леводопой.
Если дофаминергические препараты не помогают контролировать тремор, иногда используются другие препараты. Например, при треморе могут помочь холинолитики. Однако они могут вызывать серьезные психические и физические побочные эффекты, поэтому их использование следует тщательно продумать. Антихолинергические препараты наиболее эффективны у молодых людей с преобладанием тремора на БП (когда тремор является основным симптомом, требующим лечения).
Если лекарства не эффективны, глубокая стимуляция мозга (DBS) обычно помогает контролировать тремор, даже тремор, не отвечающий на лечение.
Лечение внутреннего тремора такое же, как и при видимом треморе.
Для получения дополнительной информации о лекарствах и глубокой стимуляции мозга от тремора прочтите наши книги «Болезнь Паркинсона: лекарства» и «Руководство по глубокой стимуляции мозга».
Помимо лекарств и хирургического лечения, существуют вспомогательные устройства, которые могут помочь в различных повседневных делах. Одним из них является Liftware, посуда со стабилизирующей ручкой для противодействия тремору, связанному с БП.Он доступен с насадками для ложки и вилки и помогает стабилизировать руку, облегчая захват еды и поднос ее ко рту.
И последнее, но не менее важное: упражнения так же важны, как лекарства и другие методы лечения, для облегчения симптомов Паркинсона и обеспечения наилучшего образа жизни.
Насколько распространено снижение когнитивных функций при болезни Паркинсона?
Новое исследование показало, что когнитивные нарушения являются частым и быстро прогрессирующим симптомом болезни Паркинсона (БП).Около половины участников, которые имели БП в среднем в течение пяти лет и имели нормальные когнитивные функции в начале исследования, развили умеренное когнитивное нарушение (MCI) в течение шести лет — примерно через 11 лет после постановки диагноза БП. Те немногие, у кого развился MCI, развились до слабоумия в течение еще пяти лет. Результаты появятся в онлайн-выпуске журнала Neurology от 11 сентября.
При диагнозе БП большинство людей и их врачи сосредотачиваются на лечении и преодолении двигательных симптомов.Тем не менее, даже на ранней стадии болезни люди с БП могут испытывать трудности с одновременным выполнением нескольких задач или чувствовать, что их мыслительные способности «совсем не такие».
Чтобы лучше понять скорость развития когнитивных нарушений и определить факторы риска развития когнитивных нарушений, исследователи во главе с Дэниелом Вайнтраубом, доктором медицины, приняли участие в исследовании 141 человека с болезнью Паркинсона. Все они проходили лечение в Центре исследований болезни Паркинсона Университета Пенсильвании в Удалле.В среднем им было 69 лет, и они жили с БП в течение пяти лет; 63 процента составляли мужчины. У всех участников было нормальное познание, основанное на серии стандартных тестов для людей с болезнью Паркинсона. Исследователи ежегодно переоценивали познавательные способности участников исследования на срок до шести лет.
Результаты
- С каждым годом наблюдения все больший процент участников достигал уровня MCI, достигнув 47,4 процента через шесть лет.
- Каждый участник, которому в ходе исследования был поставлен диагноз MCI, развил деменцию в течение пяти лет.
- Мужчины были подвержены повышенному риску когнитивных нарушений, как и те, кто имел более высокие баллы по шкалам оценки двигательных симптомов БП (более высокие оценки Хоэна и Яра и UPDRS), дольше жили с БП и депрессией.
Что это значит?
Многие люди десятилетиями живут с БП и обладают хорошими когнитивными способностями. Тем не менее, это исследование дополняет растущий объем литературы, в которой когнитивные нарушения определяются как распространенный немоторный симптом БП. Это исследование также является одним из первых, в котором собрана группа участников с нормальным познанием и отслеживается прогрессирование их когнитивных проблем с течением времени. По сравнению с другими исследованиями, это исследование выявило более высокую скорость снижения когнитивных функций среди участников.
По сравнению с другими исследованиями, это исследование выявило более высокую скорость снижения когнитивных функций среди участников.
Лучшее понимание того, как БП влияет на познание, может помочь людям с БП несколькими способами. Проведя тестирование на выявление этих трудностей на ранней стадии заболевания, большему количеству людей потенциально может помочь ривастигмин (Экселон®) — единственный препарат, одобренный для лечения деменции при БП.
Кроме того, результаты исследования подчеркивают необходимость в более эффективных методах лечения для замедления или остановки развития MCI и прогрессирования болезни Паркинсона в целом.Большинство клинических исследований БП сосредоточено на двигательных симптомах, и это исследование (и другие) подчеркивает острую необходимость исследований, посвященных вмешательствам для замедления скорости когнитивных изменений при БП. Кроме того, оценка когнитивных способностей на ранних стадиях болезни Паркинсона может дать людям возможность участвовать в клинических исследованиях. Повышение осведомленности о MCI также может помочь людям в принятии более информированных решений об уходе за ними в будущем.
Эксперты предупреждают, что такие симптомы болезни Паркинсона, как депрессия и апатия, могут влиять на память и способность сосредотачивать свое мышление; Перед оценкой когнитивных функций важно вылечить эти симптомы.
Недостатком исследования является то, что все участники были очень похожи — почти все были белыми, с высоким уровнем образования (в среднем 16 лет) и в узком возрастном диапазоне (62-73 года). По этой причине результаты могут не отражать реальность в большей популяции людей с БП, исследования которой показывают, что возраст является самым большим фактором риска развития деменции. Для подтверждения результатов необходимы исследования с большим количеством участников. Одно из таких исследований, в котором принимают участие 8000 человек с БП в 20 различных центрах, уже проводится.
Номер ссылки
Кара Пиготт, Жаклин Рик, Шарон X. Се, Ховард Хуртиг, Элис Чен-Плоткин, Джон Э. Дуда, Джеймс Ф. Морли, Лама М. Чахин, Набила Даходвала, Ризван С. Ахтар, Эндрю Сидеровф, Джон К. Трояновски , и Даниэль Вайнтрауб. (2015). Продольное исследование нормального познания при болезни Паркинсона. Неврология, 85 (15), 1276–1282. http://doi.org/10.1212/WNL.0000000000002001
Се, Ховард Хуртиг, Элис Чен-Плоткин, Джон Э. Дуда, Джеймс Ф. Морли, Лама М. Чахин, Набила Даходвала, Ризван С. Ахтар, Эндрю Сидеровф, Джон К. Трояновски , и Даниэль Вайнтрауб. (2015). Продольное исследование нормального познания при болезни Паркинсона. Неврология, 85 (15), 1276–1282. http://doi.org/10.1212/WNL.0000000000002001
Симптомов болезни Паркинсона | Stanford Health Care
Каковы симптомы болезни Паркинсона?
Симптомы болезни Паркинсона у разных людей различаются.Они также меняются по мере прогрессирования болезни. Симптомы, которые у одного человека появляются на ранних стадиях болезни, у другого могут появиться позже — или не появиться вовсе.
Симптомы чаще всего возникают в возрасте от 50 до 60 лет. Они развиваются медленно. Они часто остаются незамеченными для семьи, друзей и даже для человека, у которого они есть.
Заболевание вызывает двигательные симптомы и немоторные симптомы. Двигательные симптомы связаны с тем, как вы двигаетесь. Самый частый из них — тремор.
Тремор и другие двигательные симптомы
Тремор или дрожь, часто в руке, руке или ноге, возникает, когда вы бодрствуете, сидите или стоите на месте (тремор покоя).Становится лучше, когда вы двигаете этой частью тела.
- Тремор часто является первым симптомом, который замечают люди с болезнью Паркинсона или члены их семей.
- Сначала тремор может появиться только в одной руке или ноге или только на одной стороне тела. Тремор также может затронуть подбородок, губы и язык.
- По мере прогрессирования болезни тремор может распространяться на обе стороны тела. Но в некоторых случаях тремор остается только с одной стороны.
Эмоциональное и физическое напряжение делает тремор более заметным.Сон, полное расслабление и намеренное движение или действие обычно уменьшают или останавливают тремор.
Тремор — один из наиболее частых признаков болезни Паркинсона. Но не у всех с тремором есть болезнь Паркинсона. В отличие от тремора, вызванного болезнью Паркинсона, тремор, вызванный другими состояниями, проходит, когда ваша рука или кисть не движется, и усиливается, когда вы пытаетесь пошевелить ими.
Но не у всех с тремором есть болезнь Паркинсона. В отличие от тремора, вызванного болезнью Паркинсона, тремор, вызванный другими состояниями, проходит, когда ваша рука или кисть не движется, и усиливается, когда вы пытаетесь пошевелить ими.
Наиболее частой причиной непаркинсонического тремора является эссенциальный тремор. Это излечимое заболевание, которое часто ошибочно диагностируется как болезнь Паркинсона.
Помимо тремора, наиболее частыми симптомами являются:
- Скованность мышц (ригидность) и боли в мышцах.
Одним из наиболее распространенных ранних признаков болезни Паркинсона является уменьшение размаха руки на одну сторону при ходьбе. Это вызвано жесткими мышцами. Жесткость также может влиять на мышцы ног, лица, шеи или других частей тела. Это может вызвать чувство усталости и боли в мышцах.
- Слабость мышц лица и горла.
Говорить и глотать может стать труднее.Вы можете подавиться, кашлять или пускать слюни. Речь становится мягче и однообразнее. Потеря подвижности мускулов лица может вызвать неподвижное, пустое выражение лица, которое часто называют «маской Паркинсона».
- Проблемы с ходьбой и равновесием.
Человек с этим заболеванием, скорее всего, будет делать маленькие шаги и шаркать, ставя ноги близко друг к другу. Человек может немного наклониться вперед в талии и с трудом повернуться. Проблемы с равновесием и осанкой могут стать причиной частых падений.Но эти проблемы обычно не возникают позже.
- Замораживание.
Это внезапная кратковременная невозможность двигаться. Чаще всего поражает ходьба.
Немоторные симптомы
Болезнь Паркинсона может вызывать множество других симптомов, не связанных с тем, как вы двигаетесь. Их можно отключить. Они могут включать запоры, проблемы со сном и депрессию.
Есть много других состояний с симптомами, похожими на болезнь Паркинсона.Некоторые из них могут быть обратимыми.
Ранние симптомы Паркинсона, очевидные за годы до постановки диагноза, говорится в исследовании
Это важный вывод, потому что он может помочь врачам диагностировать болезнь Паркинсона на более раннем этапе и может помочь лучше справиться с этим заболеванием.
Исследование « Траектории преддиагностического функционирования при болезни Паркинсона » — первое, в котором описывается порядок возникновения моторных и немоторных нарушений, влияющих на повседневное функционирование пациентов с болезнью Паркинсона.
Группа исследователей, возглавляемая Арфаном Икрамом, доктором медицины, из Медицинского центра Университета Эразмус MC в Роттердаме, Нидерланды. изучал траекторию повседневного функционирования, моторных и немоторных функций за 23 года до постановки диагноза болезни Паркинсона. Он сделал это, выполнив вложенное исследование случай-контроль в рамках Роттердамского исследования, в котором проанализировано почти 8000 человек, проживающих в Оммурде в Нидерландах, в возрасте 55 лет и старше.
Исследователи неоднократно оценивали повседневное функционирование участников в период с 1990 по 2013 год, используя Стэнфордский опросник для оценки состояния здоровья и Шкалу инструментальной активности повседневной жизни Лоутона.
Для оценки потенциальной преддиагностической двигательной функции исследователи использовали медленность или потерю мышечных движений, тремор, ригидность, дисбаланс или неправильную осанку.
Наконец, они оценили немоторные особенности болезни Паркинсона, включая когнитивные способности, настроение и вегетативную функцию, используя несколько стандартизированных тестов, в том числе краткую оценку психического состояния, тест Струпа, тест на замену букв и цифр, тест беглости слов. , Центр эпидемиологических исследований — Шкала депрессии, Шкала тревоги и депрессии Гамильтона, артериальное давление и использование слабительных.
Исследователи также наблюдали за участниками с повторными личными обследованиями и путем доступа к их медицинским записям.
За это время у 109 человек была диагностирована болезнь Паркинсона. Исследователи сопоставили каждого из них с 10 людьми того же возраста и пола без болезни Паркинсона в качестве контроля.
Когда они сравнили повседневное функционирование людей, у которых позже была диагностирована болезнь Паркинсона, с теми, у кого не была диагностирована болезнь Паркинсона, исследователи обнаружили, что за семь лет до постановки диагноза люди, у которых позже была диагностирована болезнь Паркинсона, чаще имели проблемы в инструментальной повседневной деятельности.У них также чаще наблюдались признаки затруднения и замедления движений, тремора и незначительных когнитивных нарушений.
За пять лет до постановки диагноза у людей, у которых позже была диагностирована болезнь Паркинсона, развились дополнительные двигательные проблемы, такие как дисбаланс, ригидность и неправильная осанка, и они все чаще сообщали о проблемах в основной повседневной деятельности.
Наконец, люди, у которых позже была диагностирована болезнь Паркинсона, все чаще сообщали о симптомах тревоги, депрессивных симптомах и использовании слабительных средств на протяжении всего периода наблюдения за исследованием.Однако различия с людьми, которым впоследствии не диагностировали болезнь Паркинсона, стали статистически значимыми только в последние годы перед постановкой диагноза.
Уже было известно, что у некоторых пациентов, у которых была диагностирована болезнь Паркинсона, были симптомы, предшествующие постановке диагноза. Однако это первое исследование, в котором подробно описывается последовательность этих так называемых продромальных симптомов.
Ранние симптомы болезни Паркинсона
Зная о ранних симптомах болезни Паркинсона, наши физиотерапевты в North Boulder Physical Therapy в Голдене могут начать лечение, которое поможет вам справиться с этим заболеванием.Мы предлагаем терапию LSVT BIG ® , которая может быть персонализирована в соответствии с вашими потребностями, областями дефицита или нарушения, а также прогрессированием и серьезностью заболевания.
Это прогрессирующее нейродегенеративное заболевание, вызванное потерей дофамин-продуцирующих клеток мозга. Хотя точные причины этого заболевания неизвестны, они могут быть результатом генетики и факторов окружающей среды.
У большинства людей первые симптомы болезни Паркинсона появляются в возрасте 50 лет и старше.Но есть так называемая болезнь Паркинсона с молодым началом (YOPD), которая возникает у людей моложе 50 лет. От него страдают около 2-10 процентов из миллиона заболевших в нашей стране. Симптомы болезни Паркинсона могут появиться даже у детей и подростков. Эта форма расстройства называется ювенильным паркинсонизмом и часто связана со специфическими генетическими мутациями, имеющими риск возникновения болезни Паркинсона.
ЭтапыПервый этап
Пациент испытывает легкие симптомы, которые обычно не мешают повседневной деятельности.На одной стороне тела могут возникать тремор и другие двигательные симптомы. Ранние симптомы болезни Паркинсона могут также включать изменения в ходьбе, осанке и мимике.
Второй этап
Симптомы ухудшаются. Тремор, ригидность и другие симптомы движения начинают влиять на обе стороны тела. Проблемы с ходьбой и плохая осанка становятся более очевидными. Ежедневные задачи сложнее и длительнее, но пациент все равно может жить самостоятельно.
Третий этап
У пациента наблюдаются признаки потери равновесия и замедленности движений.Они могут падать. Хотя человек все еще может жить независимо, такие вещи, как одевание и еда, являются трудными.
Четвертый этап
Симптомы болезни Паркинсона сейчас тяжелые и ограниченные. Пациент может стоять без посторонней помощи, но для передвижения могут потребоваться ходунки. Им потребуется помощь в повседневной жизни, а это значит, что они больше не могут жить одни.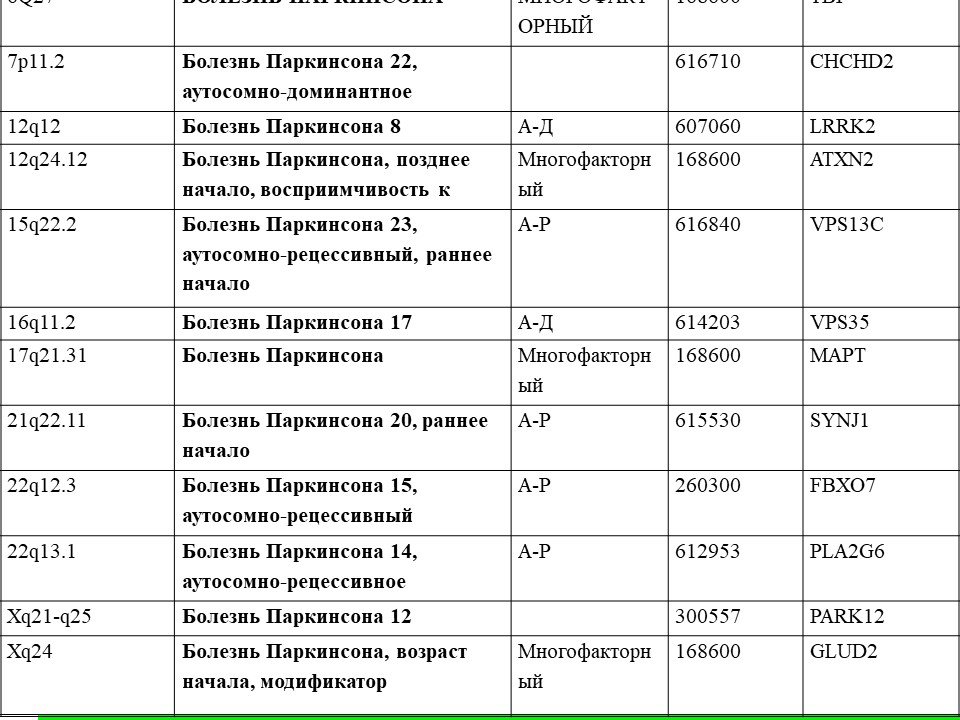
Пятый этап
Этот этап самый сложный. Скованность в ногах пациента может помешать ему стоять или ходить.Им может потребоваться инвалидная коляска или они могут быть прикованы к постели и могут нуждаться в уходе. Эта стадия также может включать галлюцинации и бред.
СимптомыПоскольку симптомы Паркинсона со временем ухудшаются, они в конечном итоге мешают выполнять повседневные задачи. Главное — знать о ранних симптомах болезни Паркинсона и немедленно обращаться за медицинской помощью. Если вы считаете, что у вас более одного из этих симптомов, поговорите со своим врачом о том, что вас беспокоит.
Акинезия или неспособность двигаться
Люди с болезнью Паркинсона могут испытывать проблемы с так называемым «замораживанием» или , когда после остановки трудно ходить.Сдвиг веса или инерции без соответствующего движения конечностей может привести к падению и травмам. Они также могут испытывать брадикинезию, то есть замедленность движений.
Головокружение или обморок
Еще один симптом болезни Паркинсона — головокружение или обморок, например, когда вы встаете со стула. Ощущение головокружения или обморока также может быть признаком низкого кровяного давления.
Осанка
Еще один знак — изменение позы, включая наклоны, наклоны или сутулости, когда вы стоите, и шаркающие ворота.Если вы травмированы, больны или у вас проблемы с костями, это также может вызвать у вас сутулость. Опять же, врач сможет лучше всего диагностировать то, что вы испытываете.
Депрессия, беспокойство и нарушения сна
Если у вас депрессия, беспокойство или беспокойный сон, который может включать в себя дергание в постели или удары кулаком во время глубокого сна, это может быть болезнь Паркинсона. Если вы начали падать с кровати после того, как заснули, или просто при внезапных движениях во время сна, вам следует поговорить с врачом. Это больше, чем просто ворочание или случайные кошмарные движения.
Это больше, чем просто ворочание или случайные кошмарные движения.
Потеря обоняния
Если вы больше не чувствуете запах некоторых продуктов или вам труднее нюхать такие продукты, как бананы, маринованные огурцы или солодка, это может быть симптомом. Это отличается от изменения обоняния, вызванного простудой, гриппом или заложенным носом, которое вернется, когда вы поправитесь.
Проблемы с глотанием, жеванием и речью
Если ваш голос недавно изменился, например, теперь вы говорите очень тихим голосом или звучите хрипло, или у вас проблемы с глотанием и жеванием, это может быть симптомом болезни Паркинсона.Изменения голоса могут быть вызваны простудой или другим вирусом, но когда вы выздоравливаете, ваш голос становится нормальным.
Маскировка
Людям с болезнью Паркинсона часто говорят, что у них серьезный, подавленный или сумасшедший вид, или что они смотрят пустым взглядом или редко моргают. Это серьезное лицо обозначается кодом , маскирующим . Есть некоторые лекарства, которые также могут вызвать такое же выражение лица, но прекратят свое действие после того, как лекарства перестанут использоваться.
Проблемы с мочеиспусканием и запоры
Если вы замечаете, что у вас часто возникают проблемы с опорожнением кишечника без напряжения, и это не связано с другими проблемами со здоровьем, вам следует обратить на это внимание. Недостаток воды или клетчатки и некоторых лекарств также может вызвать запор.
Тремор или тряска
Типичный симптом — легкая дрожь или тремор в конечностях, пальцах, большом пальце, челюсти, кистях, подбородке или губах во время отдыха.Иногда ваша нога будет дрожать, когда вы садитесь или расслабляетесь. Ваши конечности могут подергиваться или подергиваться. Имейте в виду, что не все указывает на болезнь Паркинсона. Иногда дрожь является нормальным явлением, например, после интенсивных упражнений или травмы. Тряска также может быть результатом приема некоторых лекарств.
Тряска также может быть результатом приема некоторых лекарств.
Нарушение баланса и координации
Еще один симптом — жесткость или скованность в конечностях и туловище. Вы можете заметить, что ваши руки не качаются, когда вы идете, или вы чувствуете скованность или боль в плече или бедрах.Люди часто сообщают, что их ноги прилипают к полу. Многие люди могут испытывать небольшую скованность, но она проходит после того, как они начинают двигаться. В противном случае это может быть признаком болезни Паркинсона. Кроме того, скованность могут быть вызваны травмой руки или плеча или артритом.
Мелкий почерк
Если вы заметили, что ваш почерк недавно изменился, это может быть признаком. Например, если буквы меньше или слова сдвинуты вместе. Конечно, некоторые люди нередко изменяют свой стиль письма по мере взросления, если у них затекли пальцы или руки или они больше не видят.Но такого рода изменения произойдут со временем, а не внезапно.
Физическая терапия симптомов болезни ПаркинсонаЕсли у вас есть два или более из этих симптомов, вам следует поговорить со своим врачом. Но что делать после диагностики болезни Паркинсона? Пока вы испытываете первые симптомы болезни Паркинсона, лучше сразу обратиться за помощью для решения определенных проблем. Вы можете работать с одним из наших физиотерапевтов, чтобы улучшить качество своей жизни.
ФизиотерапияNorth Boulder может помочь вам с проблемами равновесия и вестибулярного аппарата, вызванными болезнью Паркинсона. Мы предлагаем терапию LSVT BIG. Эта процедура направлена на увеличение амплитуды движений конечностей и тела за счет повторяющихся основных движений, которые часто используются в повседневной жизни.
Эта терапия основана на Голосовой Технике Ли Сильвермана, которая впервые была использована для терапии сосредоточенного голоса и глотания Паркинсона под названием LSVT LOUD. LSVT BIG подчеркивает сенсорную интеграцию моделей движений и включает:
- Четыре одночасовых занятия в неделю в течение 4 недель подряд — всего 16 занятий
- Домашние упражнения и установление режима домашних упражнений на всю жизнь
- Улучшение походки, скорости, равновесия и общего качества жизни пациента
Физиотерапевтическое лечение фокусируется на разделении каждого основного действия (например, ходьбы) на более мелкие части, которые практикуются и в конечном итоге объединяются для выполнения более крупных движений. С помощью LSVT BIG терапии мы работаем с сильно амплитудными, преувеличенными моделями движений, что приводит к более плавным и безопасным двигательным функциям и улучшает качество вашей жизни.
С помощью LSVT BIG терапии мы работаем с сильно амплитудными, преувеличенными моделями движений, что приводит к более плавным и безопасным двигательным функциям и улучшает качество вашей жизни.
Терапия LSVT BIG финансировалась Национальным институтом здоровья и тщательно исследовалась, а методы лечения разрабатывались более двадцати лет. Документированные улучшения у пациентов с болезнью Паркинсона включают:
- Более быстрая ходьба и улучшение равновесия
- Возможность большего шага (по сравнению с перемешиванием)
- Увеличена возможность поворота ствола
- Повышение мобильности в повседневной деятельности
- Улучшенный единый рейтинг болезни Паркинсона
Знание ранних симптомов болезни Паркинсона может дать вам толчок к решению этой сложной болезни.Наши физиотерапевты в North Boulder Physical Therapy в Голдене начнут лечение, чтобы помочь вам справиться с этим состоянием. Они начнут с полной оценки ваших сильных сторон и проблем, а затем сформируют ваше лечение LSVT BIG в соответствии с вашими конкретными целями.
В то время как раннее лечение дает наилучшие результаты, LSVT BIG может быть эффективным средством лечения на всех стадиях болезни Паркинсона, затрагивая как грубую, так и мелкую моторику. В North Boulder Physical Therapy в Вестминстере мы прошли полную сертификацию, чтобы предложить этот вариант лечения пациентам с болезнью Паркинсона.Чтобы записаться на прием, позвоните нам сегодня.
Ранние признаки и симптомы болезни Паркинсона
Болезнь Паркинсона обычно считается заболеванием позднего среднего возраста со средним возрастом начала около 60 лет. Есть случаи болезни Паркинсона с «ранним началом», но только у небольшого процента людей в возрасте до 50 лет, примерно от 5 до 10 процентов, это заболевание разовьется раньше.
Причина болезни неизвестна.Хотя некоторые данные указывают на генетику, у большинства пациентов нет известных отклонений в генах. Некоторые исследования показывают, что факторы окружающей среды могут вызвать заболевание у людей с генетической предрасположенностью. Эти факторы включают воздействие пестицидов и гербицидов, особенно для тех, кто живет в сельской местности, питьевую воду из частного колодца, работу на ферме или сварщиком. Но даже эти исследования неубедительны.
Некоторые исследования показывают, что факторы окружающей среды могут вызвать заболевание у людей с генетической предрасположенностью. Эти факторы включают воздействие пестицидов и гербицидов, особенно для тех, кто живет в сельской местности, питьевую воду из частного колодца, работу на ферме или сварщиком. Но даже эти исследования неубедительны.
Симптомы болезни Паркинсона
Вы можете связать симптомы болезни Паркинсона с дефицитом химического вещества в вашем мозгу, называемого дофамином.Четыре классических моторных симптома болезни Паркинсона включают:
- Дрожь и тремор
- Медленное движение, известное как брадикинезия
- Необычно жесткие или жесткие мышцы лица, шеи, ног или других мышц
- Проблемы с поддержанием баланса
Дрожь и тремор во время отдыха обычно являются первым признаком болезни Паркинсона, но около трети пациентов не испытывают этих симптомов. Эти симптомы обычно усугубляются эмоциональным и физическим стрессом.Сон или движение могут помочь уменьшить эти проблемы.
Болезнь Паркинсона носит хронический и прогрессирующий характер, с течением времени симптомы обычно ухудшаются. По мере развития могут развиваться другие виды инвалидности, в том числе:
- Затруднения при разговоре и глотании
- Внезапная невозможность двигаться, называемая «замирание».
- Снижение подвижности и координации, затрудняющее выполнение повседневных дел, например одевание.
У некоторых больных также есть симптомы, не влияющие на их двигательные навыки, в том числе:
- Проблемы с психическим здоровьем, такие как беспокойство, депрессия и потеря памяти
- Потеря запаха
- Проблемы со сном, включая взбучку и другие резкие движения
- Изменение артериального давления
Некоторые варианты лечения болезни Паркинсона
Болезнь Паркинсона неизлечима, но существуют варианты лечения, позволяющие контролировать симптомы и улучшать качество жизни, в том числе:
- Лекарства.
 Леводопа (синемет) и другие лекарства, которые пытаются повысить уровень дофамина (химического вещества с низким содержанием в вашем мозгу). Есть ряд лекарств, которые можно использовать по отдельности или в комбинации. Хотя многие из этих лекарств могут помочь вам значительно контролировать двигательные симптомы (медлительность, тремор, жесткость), со временем вы также можете испытывать побочные эффекты и снижать эффективность.
Леводопа (синемет) и другие лекарства, которые пытаются повысить уровень дофамина (химического вещества с низким содержанием в вашем мозгу). Есть ряд лекарств, которые можно использовать по отдельности или в комбинации. Хотя многие из этих лекарств могут помочь вам значительно контролировать двигательные симптомы (медлительность, тремор, жесткость), со временем вы также можете испытывать побочные эффекты и снижать эффективность. - Физическая терапия, профессиональная терапия и логопедия обычно являются частью вашего плана лечения и могут улучшить ваше равновесие, подвижность, способность выполнять повседневные задачи и речь.
- Глубокая стимуляция мозга — это операция, выполняемая нейрохирургом, и у определенных пациентов может помочь с двигательными симптомами, хотя немоторные симптомы, такие как падение, запор, низкое кровяное давление и недержание мочи, не улучшаются.
- Тай Чи — это китайское боевое искусство, которое может помочь пострадавшим частично восстановить равновесие и силу, а также снизить риск падения. Также могут помочь танцы, такие как зумба, велотренажер и рок-бокс.
Многие варианты лечения болезни Паркинсона наиболее эффективны, когда используются вместе с другими, такими как прием лекарств и физиотерапия.
Возможные факторы снижения риска
Хотя возраст, генетика и мужское начало повышают вероятность развития болезни Паркинсона, некоторые факторы делают ее менее вероятной. Принято считать, что американцы азиатского происхождения и афроамериканцы имеют более низкий риск развития болезни Паркинсона по сравнению с европейцами.Употребление кофе может снизить риск, поскольку 30-летнее исследование американцев японского происхождения показало, что чем больше кофе они пьют, тем ниже становится их риск болезни Паркинсона.
Симптомы и диагностика болезни Паркинсона
Немоторные симптомы болезни Паркинсона не влияют на движение, но они могут влиять на ваше настроение, чувства и способность думать. (2)
(2)
Общие немоторные симптомы включают:
Когнитивные проблемы и слабоумиеПроблемы с мышлением, памятью, многозадачностью и оценкой расстояния, по оценкам, возникают у 40 или более процентов людей с болезнью Паркинсона.
Психоз и галлюцинацииПсихоз — мысли и убеждения, не связанные с реальностью, — могут возникать у 20-40 процентов людей из-за самого заболевания, а также из-за побочных эффектов лекарств. (3)
Визуальные галлюцинации — видение нереальных вещей — являются наиболее частым психотическим симптомом болезни Паркинсона. По мере прогрессирования болезни галлюцинации часто становятся более частыми и тяжелыми.
У некоторых людей с болезнью Паркинсона также есть заблуждения, в том числе ложные убеждения, что они в опасности, что их украли или обманул супруг.
Расстройства настроенияНекоторые люди с болезнью Паркинсона становятся депрессивными, тревожными или апатичными — им не хватает мотивации ходить, говорить или выражать эмоции.
Расстройства снаПроблемы с засыпанием и сном — обычное явление при болезни Паркинсона. (4)
Эти проблемы могут быть вызваны или усугублены трудностями при переворачивании в постели, мышечными судорогами или болью, частым мочеиспусканием или яркими сновидениями и кошмарами.
Дневная сонливостьЧрезмерная дневная сонливость поражает до 75 процентов людей с болезнью Паркинсона. Это может усугубиться лекарствами от болезни.
Некоторые люди с болезнью Паркинсона могут внезапно заснуть, что может быть очень опасно, если они водят машину.
Поговорите со своим врачом о корректировке приема лекарств, если вы испытываете этот симптом.
Вегетативная дисфункция Вегетативная нервная система контролирует автоматические функции организма, такие как частота сердечных сокращений, артериальное давление, дыхание, пищеварение, потоотделение, мочеиспускание и сексуальное возбуждение.

 Поначалу этому подвержена лишь одна рука, затем дрожь распространяется на все конечности.
Поначалу этому подвержена лишь одна рука, затем дрожь распространяется на все конечности. Леводопа (синемет) и другие лекарства, которые пытаются повысить уровень дофамина (химического вещества с низким содержанием в вашем мозгу). Есть ряд лекарств, которые можно использовать по отдельности или в комбинации. Хотя многие из этих лекарств могут помочь вам значительно контролировать двигательные симптомы (медлительность, тремор, жесткость), со временем вы также можете испытывать побочные эффекты и снижать эффективность.
Леводопа (синемет) и другие лекарства, которые пытаются повысить уровень дофамина (химического вещества с низким содержанием в вашем мозгу). Есть ряд лекарств, которые можно использовать по отдельности или в комбинации. Хотя многие из этих лекарств могут помочь вам значительно контролировать двигательные симптомы (медлительность, тремор, жесткость), со временем вы также можете испытывать побочные эффекты и снижать эффективность.