Как справится с психозомпри паркинсоне: Психозы при болезни Паркинсона — Центр Экстрапирамидных Заболеваний
Психозы при болезни Паркинсона — Центр Экстрапирамидных Заболеваний
Психозы при болезни Паркинсона
Психические расстройства являются одними из наиболее частых немоторных проявлений болезни Паркинсона (БП). Психозы являются «позитивными» (продуктивными) психическими расстройствами, в противоположность «негативным» симптомам дефицита [1]. Среди психотических симптомов при БП встречаются зрительные галлюцинации, бред, а также галлюцинации, связанные с другими органами чувств (обонятельные, слуховые, вкусовые и тактильные галлюцинации) [2].
Факторами риска развития психозов при БП является пожилой возраст, быстрый темп прогрессирования болезни, микроваскулярные изменения, атрофия головного мозга, когнитивные нарушения, депрессия, нарушения сна, а также полифармакотерапия [3].
Зрительные галлюцинации — наиболее распространенный нейропсихиатрический симптом при БП (22-38% случаев среди пациентов с БП) [4, 5]. Галлюцинации представляют собой неадекватное восприятие окружающей среды в отсутствие внешних стимулов.
К малым галлюцинациям относятся экстракампильные галлюцинации и иллюзии. Экстракампильные галлюцинации подразделяются на галлюцинации прохождения и галлюцинации присутствия. Галлюцинации присутствия (или ощущение присутствия) — яркое ощущение, что рядом кто-то находится, обычно позади плеч пациента, при отсутствии каких-либо сенсорных признаков, подтверждающих присутствие. Галлюцинации прохождения — мимолетные тень или образ человека, животного или объекта, пролетающего сбоку, в пределах бокового поля зрения [7].
Зрительные иллюзии — короткие ошибочные представления объектов или живых существ, отличающихся от реальной действительности (например, принятие стоящей лампы в углу комнаты за человека, ветки дерева — за кошку) [8].
Большие, структурированные галлюцинации состоят из периодически повторяющихся образов людей, животных или неодушевленных объектов [9].
Как правило, психотические симптомы развиваются по мере прогрессирования БП в определенной последовательности. Так, на ранних стадиях болезни у пациентов могут отмечаться галлюцинации прохождения, присутствия или иллюзии. Иногда появление малых галлюцинаций даже предшествует манифестации моторных симптомов БП [8]. На более поздних стадиях галлюцинации становятся сформированными, однако критика к ним пациента сохранена. Наконец, по мере прогрессирования БП критика к галлюцинациям может утрачиваться, появляется бред, а также галлюцинации, связанные с другими органами чувств (мультимодальные галлюцинации). Примером слуховых галлюцинаций при БП является голос, который не может быть понят, либо невербальные звуки, такие как шаги или музыка [10]. Одновременно с утратой критики к галлюцинациям отмечается когнитивное снижение [11].
Литература
- Fénelon G, Soulas T, Zenasni F, De Langavant LC.
 The changing face of Parkinson’s disease-associated psychosis: a cross-sectional study based on the new NINDS-NIMH criteria. Mov Disord 2010;25(6):763-766. https://doi.org/10.1002/mds.22839
The changing face of Parkinson’s disease-associated psychosis: a cross-sectional study based on the new NINDS-NIMH criteria. Mov Disord 2010;25(6):763-766. https://doi.org/10.1002/mds.22839 - Fenelon G, Soulas T, Cleret de Langavant L, Trinkler I, Bachoud-L ́evi AC. Feeling of presence in Parkinson’s disease. J Neurol Neurosurg Psychiatry. 2011;82:1219–1224. https://doi.org/10.1136/jnnp.2010.234799
- Barnes J, David AS. Visual hallucinations in Parkinson’s disease: a review and phenomenological survey. Journal of neurology, neurosurgery, and psychiatry. 2001;70(6):727-733. https://doi.org/10.1136/jnnp.70.6.727
- Schneider RB, Iourinets J, Richard IH. Parkinson’s disease psychosis: presentation, diagnosis and management. Neurodegener Dis Manag. 2017;7(6):365-376. https://doi.org/10.2217/nmt-2017-0028
- Schapira AH, Chaudhuri KR, Jenner P. Non-motor features of Parkinson disease. Nat Rev Neurosci. 2017;18(7):435-50.
 https://doi.org/10.1038/nrn.2017.91
https://doi.org/10.1038/nrn.2017.91 - Ffytche DH, Creese B, Politis M, Chaudhuri KR, Weintraub D, Ballard C, Aarsland D. The psychosis spectrum in Parkinson disease. Nat Rev Neurol. 2017;13(2):81-95. https://doi.org/10.1038/nrneurol.2016.200
- Boubert, L., Barnes, J. Phenomenology of visual hallucinations and their relationship to cognitive
profile in Parkinson’s disease patients: preliminary observations. SAGE Open. 2015.
- Pagonabarraga J, Martinez-Horta S, Fernández de Bobadilla R, Pérez J, Ribosa-Nogué R, Marín J, Pascual-Sedano B, García C, Gironell A, Kulisevsky J. Minor hallucinations occur in drug-naive Parkinson’s disease patients, even from the premotor phase. Mov Disord. 2016;31(1):45-52. https://doi.org/10.1002/mds.26432
- McKinlay A, Grace RC, Dalrymple-Alford JC, Anderson T, Fink J, Roger D. A profile of neuropsychiatric problems and their relationship to quality of life for Parkinson’s disease patients without dementia.
 Park Relat Disord. 2008;14(1):37-42. https://doi.org/10.1016/j.parkreldis.2007.05.009
Park Relat Disord. 2008;14(1):37-42. https://doi.org/10.1016/j.parkreldis.2007.05.009 - Fénelon G, Mahieux F, Huon R, Ziegler M. Hallucinations in Parkinson’s disease: prevalence, phenomenology and risk factors. Brain. 2000;123:733–745.
- Ravina B, Marder K, Fernandez HH, Friedman JH, McDonald W, Murphy D, Aarsland D, Babcock D, Cummings J, Endicott J, Factor S, Galpern W, Lees A, Marsh L, Stacy M, Gwinn-Hardy K, Voon V, Goetz C. Diagnostic criteria for psychosis in Parkinson’s disease: report of an NINDS, NIMH work group. Mov Disord. 2007;22:1061–1068. https://doi.org/10.1002/mds.21382
Автор: Верюгина Н.И.
Психоз при болезни Паркинсона: отзывы, рекомендации
Паркинсонический психоз: причины, симптомы и варианты лечения
Hubert H. Fernandez, MD
Эпидемиология
Психоз при болезни Паркинсона переносят до 60% пациентов, независимо от их когнитивного статуса. [7-9] Длительное 20 -летнее исследование группы больных с диагнозом болезни Паркинсона показало, что к концу исследования 74% пациентов имели в анамнезе галлюциноз. [10] Другое исследование обнаружило, что в группе численностью 191 человек 21,5% имели психотические симптомы, несмотря на отсутствие когнитивных нарушений. [11] То же исследование описало варианты психической патологии при болезни Паркинсона: зрительные галлюцинации (13,6%), иллюзии или ложные узнавания людей (7,3%), слуховые галлюцинации (6,8%) и параноидные идеи (4,7%). Кроме того, для пациентов с болезнью Паркинсона, депрессией и нарушениями поведения во время REM — стадии сна, вероятность развития психотических симптомов оказалась выше в 5 раз.
[10] Другое исследование обнаружило, что в группе численностью 191 человек 21,5% имели психотические симптомы, несмотря на отсутствие когнитивных нарушений. [11] То же исследование описало варианты психической патологии при болезни Паркинсона: зрительные галлюцинации (13,6%), иллюзии или ложные узнавания людей (7,3%), слуховые галлюцинации (6,8%) и параноидные идеи (4,7%). Кроме того, для пациентов с болезнью Паркинсона, депрессией и нарушениями поведения во время REM — стадии сна, вероятность развития психотических симптомов оказалась выше в 5 раз.
В целом, психотические расстройства чаще возникают у пациентов с когнитивным дефицитом, то есть положительно коррелируют с языковыми и мнестическими нарушениями, нарушениями внимания, исполнительного функционирования и снижением способности к зрительно — пространственной ориентации.[12] Распространенность психотических расстройств при болезни Паркинсона еще выше, когда долгосрочное лечение характеризуется полипрагмазией (см. Таблицу).
Таблица. Причины, связанные с развитием психоза при болезни Паркинсона
| Причины, связанные с болезнью Паркинсона | Причины, не связанные с болезнью Паркинсона |
| Когнитивное ухудшение | Снижение мозговой перфузии |
| Деменция | Дисбаланс электролитов |
| Депрессия | Боль |
Нарушения сна
| Психосоциальный стресс |
| Тяжелые двигательные нарушения | Дисфункция зрительного анализатора
|
| Выраженная вегетативная дисфункция | |
Инфекции
| |
Лекарства
|
Прим. : REM — стадия = стадия «быстрого сна».
: REM — стадия = стадия «быстрого сна».
From Hubert H. Fernandez, MD
Клинические симптомы и факторы риска
Психоз при болезни Паркинсона характеризуется собственной совокупностью клинических симптомов, которые отличаются от таковых при других психических расстройствах, таких, как шизофрения. Несмотря на то, что эти проявления хорошо описаны, до сих пор не существует официальных критериев для подтверждения диагноза паркинсонического психоза. Диагностическое и Статистическое Руководство по Психическим Расстройствам четвертого выпуска, пересмотренное (DSM-IV-TR) и Структурированное Клиническое Интервью для Оси 1 DSM-IV-TR (SCID) включают только общие категории, такие как «психоз вследствие соматического заболевания» или «медикаментозный психоз». [13]
Психоз при болезни Паркинсона чаще всего проявляется в виде зрительных галлюцинаций, которые могут возникать в любое время суток, хотя чаще всего появляются в вечерние часы, и вообще при снижении внешней стимуляции. [8] Зрительные галлюцинации обычно включают людей или животных, но могут также содержать и неодушевленные объекты. Как правило, эти обманы восприятия длятся от нескольких секунд до нескольких минут с частотой от одного раза в неделю и выше. Слуховые галлюцинации, если они возникают при паркинсоническом психозе, как правило, не бывают изолированными, а сопровождаются зрительными. В целом, при болезни Паркинсона слуховые обманы восприятия обнаруживаются реже, чем, например, при шизофрении; если они присутствуют, то, как правило, представляют из себя шепот или музыку, а не угрожающие голоса, о которых сообщают шизофренические пациенты. Тем не менее, в научной литературе имеются сведения о случаях угрожающих слуховых галлюцинаций и при болезни Паркинсона. [14] Тактильные, обонятельные, и висцеральные галлюцинации при болезни Паркинсона редки, и также обычно сопровождаются зрительными. [3]
[8] Зрительные галлюцинации обычно включают людей или животных, но могут также содержать и неодушевленные объекты. Как правило, эти обманы восприятия длятся от нескольких секунд до нескольких минут с частотой от одного раза в неделю и выше. Слуховые галлюцинации, если они возникают при паркинсоническом психозе, как правило, не бывают изолированными, а сопровождаются зрительными. В целом, при болезни Паркинсона слуховые обманы восприятия обнаруживаются реже, чем, например, при шизофрении; если они присутствуют, то, как правило, представляют из себя шепот или музыку, а не угрожающие голоса, о которых сообщают шизофренические пациенты. Тем не менее, в научной литературе имеются сведения о случаях угрожающих слуховых галлюцинаций и при болезни Паркинсона. [14] Тактильные, обонятельные, и висцеральные галлюцинации при болезни Паркинсона редки, и также обычно сопровождаются зрительными. [3]
В литературе содержатся сведения и о других феноменах, возникающих при паркинсоническом психозе, таких как иллюзии, галлюцинации присутствия или периферические галлюцинации. [8] Иллюзия — это ошибка перцептивного опыта, например, принятие объекта за животное или человека. Галлюцинации присутствия включают чувство, что кто-то находится в непосредственной физической близости к пациенту. Периферические галлюцинации — обычно мимолетные видения образов или теней, возникающие на периферии поля зрения пациента. Пациенты редко сами сообщают врачу о наличии у них этих феноменов. Скорее всего потому, что наличие или отсутствие этих обманов обычно никак не влияет на течение их повседневной жизни.
[8] Иллюзия — это ошибка перцептивного опыта, например, принятие объекта за животное или человека. Галлюцинации присутствия включают чувство, что кто-то находится в непосредственной физической близости к пациенту. Периферические галлюцинации — обычно мимолетные видения образов или теней, возникающие на периферии поля зрения пациента. Пациенты редко сами сообщают врачу о наличии у них этих феноменов. Скорее всего потому, что наличие или отсутствие этих обманов обычно никак не влияет на течение их повседневной жизни.
Бред и дезорганизация мышления также описаны в структуре психотических расстройств при болезни Паркинсона, однако они не настолько характерны, как зрительные галлюцинации. Наиболее часто содержанием бредовых идей оказываются ситуации супружеской неверности, хотя грандиозные, ипохондрические, персекуторные и религиозные бредовые идеи, чаще, впрочем, описываемые при шизофрении, при болезни Паркинсона также встречаются.
Психоз при болезни Паркинсона, как правило, развивается на поздних стадиях заболевания. О симптомах психоза пациенты, в среднем, сообщают спустя 10 и более лет после постановки диагноза паркинсонизма. [15] Первоначально психоз возникает на фоне сохранных сенсорики и критики. [15,16] Тем не менее, возникнув однажды, психотические симптомы имеют тенденцию к повторению, а их течение — к ухудшению со временем, и критика в конечном итоге может быть утеряна. [16] Психоз при болезни Паркинсона принято рассматривать как текущий параллельно основному заболеванию процесс, в котором незначительные симптомы, такие как яркие сновидения и иллюзии предваряют более откровенные галлюцинации и бред, в конечном счете приводя к цветущему психозу и деменции. [17] Другие данные, однако, свидетельствуют, что это понимание предварительно, и может не соответствовать истине. [18]
О симптомах психоза пациенты, в среднем, сообщают спустя 10 и более лет после постановки диагноза паркинсонизма. [15] Первоначально психоз возникает на фоне сохранных сенсорики и критики. [15,16] Тем не менее, возникнув однажды, психотические симптомы имеют тенденцию к повторению, а их течение — к ухудшению со временем, и критика в конечном итоге может быть утеряна. [16] Психоз при болезни Паркинсона принято рассматривать как текущий параллельно основному заболеванию процесс, в котором незначительные симптомы, такие как яркие сновидения и иллюзии предваряют более откровенные галлюцинации и бред, в конечном счете приводя к цветущему психозу и деменции. [17] Другие данные, однако, свидетельствуют, что это понимание предварительно, и может не соответствовать истине. [18]
Существует несколько шкал, подходящих для оценки паркинсонического психоза. [19] Такие шкалы, как Психоневрологический Опросник (NPI-Q), Краткая Психиатрическая Оценочная Шкала (BPRS), Рейтинговая Шкала Паркинсонического Психоза (PPRS), Шкала Позитивных Симптомов (SAPS), Анкетный опросник паркинсонического психоза (PPQ), Первая часть Объединенной рейтинговой шкалы болезни Паркинсона (UPDRS), Шкала Позитивных И Негативных Синдромов (PANSS), а также некоторые другие, используются в исследованиях и клинической практике. Однако эти шкалы не разрабатывались специально для применения при болезни Паркинсона, и поэтому не в состоянии оценить весь спектр феноменологии паркинсонического психоза. [19] Ни одна из вышеприведенных шкал не является оптимальной для оценки этой психической патологии. Необходимо создание новой шкалы, которая упростит и будет учитывать уникальные особенности психоза при болезни Паркинсона. [19] Рекомендации по использованию имеющихся шкал: если у пациента есть когнитивное ухудшение, то необходимо использовать шкалу NPI; если такого снижения нет, то возможно применение шкал SAPS, PANSS или BPRS , возможно совместно со Шкалой Общей Клинической Оценки (CGIS), чтобы исследовать также изменения и реакцию на долгосрочное лечение.
Однако эти шкалы не разрабатывались специально для применения при болезни Паркинсона, и поэтому не в состоянии оценить весь спектр феноменологии паркинсонического психоза. [19] Ни одна из вышеприведенных шкал не является оптимальной для оценки этой психической патологии. Необходимо создание новой шкалы, которая упростит и будет учитывать уникальные особенности психоза при болезни Паркинсона. [19] Рекомендации по использованию имеющихся шкал: если у пациента есть когнитивное ухудшение, то необходимо использовать шкалу NPI; если такого снижения нет, то возможно применение шкал SAPS, PANSS или BPRS , возможно совместно со Шкалой Общей Клинической Оценки (CGIS), чтобы исследовать также изменения и реакцию на долгосрочное лечение.
Дофаминергическая медикаментозная терапия, особенно использование дофаминомиметиков, является серьезным фактором риска развития психоза, однако продолжительность лечения и дозы препаратов, как оказалось, не единственная причина развития психоза. [20] Другие факторы риска включают когнитивное ухудшение, преклонный возраст, длительность течения болезни и ее тяжесть, наличие депрессии, нарушений сна, вегетативное ухудшение и снижение остроты зрения. [3, 8, 21-24] В недавнем геномном исследовании было показано, что психоз у пациентов с болезнью Паркинсона не связан с полиморфизмом аполипопротеинов, альфа синуклеинов или генов тау-белков микроканальцев. Однако исследователи обнаружили сильную корреляцию риска развития психоза с нарушением походки (по типу «застывания» при ходьбе и поворотах). [25] Это исследование также подтвердило ассоциацию между психозом и депрессией, продолжительностью болезни, возрастом, когнитивным снижением и проблемами сна.
[3, 8, 21-24] В недавнем геномном исследовании было показано, что психоз у пациентов с болезнью Паркинсона не связан с полиморфизмом аполипопротеинов, альфа синуклеинов или генов тау-белков микроканальцев. Однако исследователи обнаружили сильную корреляцию риска развития психоза с нарушением походки (по типу «застывания» при ходьбе и поворотах). [25] Это исследование также подтвердило ассоциацию между психозом и депрессией, продолжительностью болезни, возрастом, когнитивным снижением и проблемами сна.
Проблематика
Психоз является основным противопоказанием для помещения человека в интернат или пансионат по уходу, а также в дома престарелых. Это связано с повышенным риском заболеваний и смерти, ухудшением качества жизни, это значительно ограничивает возможности лечения болезни Паркинсона. [26] Бред в большей степени, чем какой-либо другой психоневрологический симптом, может быть причиной серьезного стресса у лиц, ухаживающих за больным. [26]
Даже после купирования психотической симптоматики велик риск рецидива галлюциноза вслед за прекращением терапии атипичными антипсихотиками. [27], Кроме того, использование антипсихотиков иногда не способно полностью улучшить состояние пациентов. [28] Галлюцинации имеют тенденцию сохраняться, если не утяжеляться, на протяжении нескольких лет после их появления. [5]
[27], Кроме того, использование антипсихотиков иногда не способно полностью улучшить состояние пациентов. [28] Галлюцинации имеют тенденцию сохраняться, если не утяжеляться, на протяжении нескольких лет после их появления. [5]
Патофизиология
Не у всех пациентов с болезнью Паркинсона развивается психоз. Создается впечатление, что его возникновению способствуют различные внутренние и внешние факторы.
Роль дофаминергических препаратов
Патофизиология паркинсонического психоза традиционно сосредоточена на дофаминергических лекарствах как его причине. [29] Известно, что дофаминомиметики, такие как кокаин или амфетамин, могут вызвать психотические симптомы. [30] С другой стороны, механизм действия атипичных нейролептиков, используемых для ослабления этих симптомов, как полагают, обусловлен, главным образом, сродством к D2- дофаминовым рецепторам. [31] Все препараты для лечения паркинсонизма могут быть причастны к возникновению психотических симптомов; эти симптомы часто стихают или исчезают после того, как медикаментозное лечение было уменьшено или прекращено.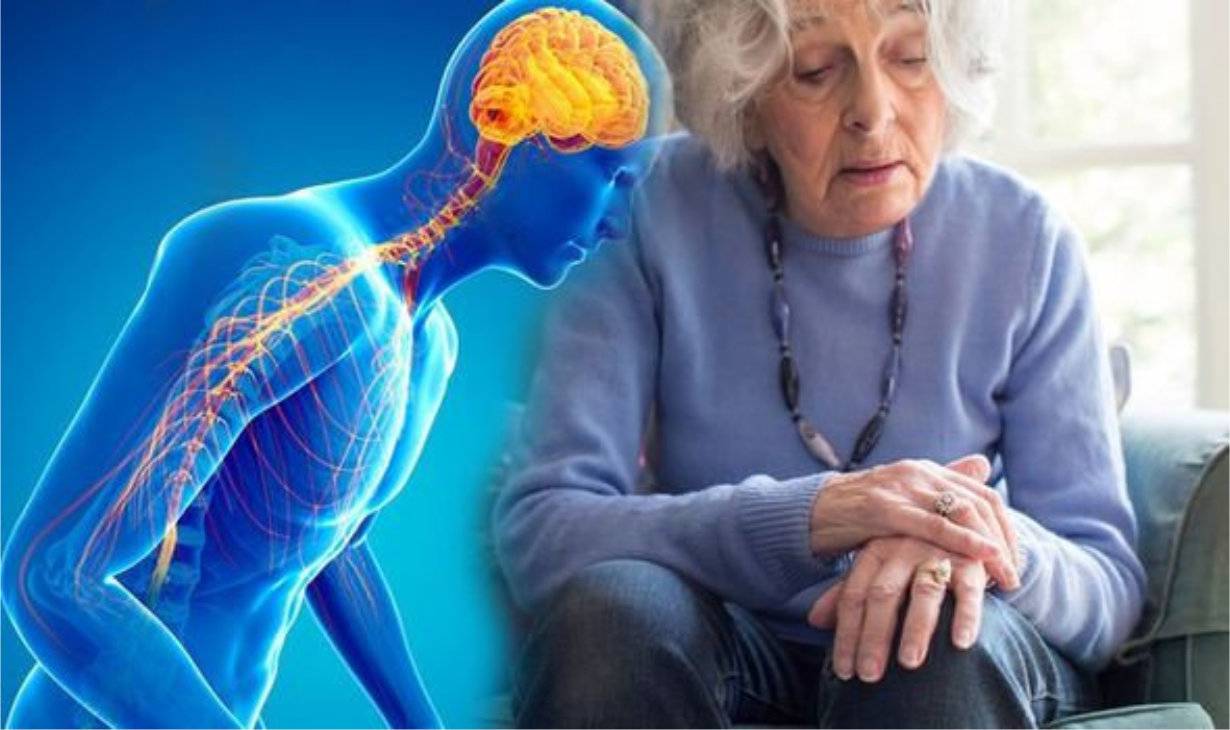 [32] Известная теория, объясняющая механизм развития психотической симптоматики под воздействием антипаркинсонических препаратов, включает гиперчувствительность дофаминовых рецепторов нигростриальной области вследствие их хронической гиперстимуляции, что может привести к дисфункции лимбических структур, ответственных за назначение эмоционального и гедонического значения содержимому сенсорного ввода. Эта дисфункция может привести к ложному узнаванию внутренних раздражителей как внешних. [33]
[32] Известная теория, объясняющая механизм развития психотической симптоматики под воздействием антипаркинсонических препаратов, включает гиперчувствительность дофаминовых рецепторов нигростриальной области вследствие их хронической гиперстимуляции, что может привести к дисфункции лимбических структур, ответственных за назначение эмоционального и гедонического значения содержимому сенсорного ввода. Эта дисфункция может привести к ложному узнаванию внутренних раздражителей как внешних. [33]
Однако не только дофаминергические препараты лежат в основе развития психозов при болезни Паркинсона. Внутренние связанные с болезнью процессы также способствуют появлению психотических симптомов у паркинсонических больных. Действительно, накопленные данные поддерживают представление, что дофаминергические вещества не необходимы и не достаточны для проявления психотики. Существуют отчеты о наличии галлюцинаций, развившихся у больных — паркинсоников еще до введения леводопы. [34] Таким образом, появление психотических симптомов оказывается связано с такими недофаминергическими веществами, как антихолинергические средства [35] амантадин [36] и ингибиторами моноаминоксидазы типа B (MAО-B). [37] Исследователи не обнаружили четкой корреляции между дозировкой препаратов и возникновением или тяжестью психоза у больных с болезнью Паркинсона. [24, 38] В патогенезе развития психоза при болезни Паркинсона также играют роль и факторы, не связанные с лекарственным воздействием, например, патология зрительного анализатора, расстройства сна и структурные или нейрохимические мозговые изменения.
[37] Исследователи не обнаружили четкой корреляции между дозировкой препаратов и возникновением или тяжестью психоза у больных с болезнью Паркинсона. [24, 38] В патогенезе развития психоза при болезни Паркинсона также играют роль и факторы, не связанные с лекарственным воздействием, например, патология зрительного анализатора, расстройства сна и структурные или нейрохимические мозговые изменения.
Дефицит зрительного анализатора
Одной из причин зрительных галлюцинаций, как было обнаружено, является патология зрительного анализатора выражающаяся в трудности адекватной обработки зрительного сигнала. У пациентов, переносящих паркинсонический психоз, присутствовали снижение остроты зрения, [24] дефицит восприятия цветовых и контрастных фигур. [39] Чаще, чем у больных без психоза, обнаруживалась выраженная глазная патология, например катаракта, патология сетчатки и глаукома. [8] Недостаток дофамина на уровне сетчатки был обнаружен исследователями при изучении как болезни Паркинсона, [40] так и деменции с тельцами Леви. [41, 42] Эти факты могут объяснять легкость возникновения зрительных обманов восприятия при болезни Паркинсона. Согласно данным магнитно-резонансной томографии (МРТ), галлюцинирующие при болезни Паркинсона пациенты страдают от снижения интенсивности ретино-стриато-кортикальных сигналов, что может приводить к растормаживанию «нисходящей» обработки и последующего замещения внешних сигналов сгенерированными внутри, это происходит в тех областях мозга, где обычно представлены внешне сгенерированные образы. [43] Барнс и др. сообщает о недостаточном контроле реальности у пациентов с галлюцинациями при болезни Паркинсона. Эти пациенты с большей вероятностью, чем негаллюцинирующие, а также по сравнению с контрольными группами пожилых пациентов, полагали, что сгенерированные внутри картинки были реальными внешними стимулами. [44]
[41, 42] Эти факты могут объяснять легкость возникновения зрительных обманов восприятия при болезни Паркинсона. Согласно данным магнитно-резонансной томографии (МРТ), галлюцинирующие при болезни Паркинсона пациенты страдают от снижения интенсивности ретино-стриато-кортикальных сигналов, что может приводить к растормаживанию «нисходящей» обработки и последующего замещения внешних сигналов сгенерированными внутри, это происходит в тех областях мозга, где обычно представлены внешне сгенерированные образы. [43] Барнс и др. сообщает о недостаточном контроле реальности у пациентов с галлюцинациями при болезни Паркинсона. Эти пациенты с большей вероятностью, чем негаллюцинирующие, а также по сравнению с контрольными группами пожилых пациентов, полагали, что сгенерированные внутри картинки были реальными внешними стимулами. [44]
Расстройства сна
Нарушения сна, особенно у пациентов с большим стажем течения болезни Паркинсона, как обнаружили, были наиболее важным фактором в предсказании развития галлюцинаций. [45] Фрагментация сна и измененные сновидения (яркие сны, кошмары и проявления, нарушения поведения во время быстрой фазы сна (REM behavioral disorder [RBD]), или ночной террор), также связаны с галлюцинациями. [18] Однако 6-летнее проспективное лонгитюдное исследование пришло к заключению, что галлюцинации и нарушения сна показали различные структуры прогрессии. Нарушения сна, присутствующие в течение длительного времени, не обнаруживают увеличения тяжести, тогда как тяжесть зрительных галлюцинаций нарастает со временем, и имеет отчетливую тенденцию к хронификации. [46] В другом исследовании было показано, что нарушения сна, включая RBD, могут присутствовать еще до клинической манифестации двигательных проявлений болезни Паркинсона и не связаны с тяжестью заболевания; и при этом они не являются показателем прогрессирования болезни Паркинсона. [47] Одно недавнее исследование нашло, что яркие сны были связаны с визуальными галлюцинациями и когнитивным ухудшением при болезни Паркинсона. [48]
[45] Фрагментация сна и измененные сновидения (яркие сны, кошмары и проявления, нарушения поведения во время быстрой фазы сна (REM behavioral disorder [RBD]), или ночной террор), также связаны с галлюцинациями. [18] Однако 6-летнее проспективное лонгитюдное исследование пришло к заключению, что галлюцинации и нарушения сна показали различные структуры прогрессии. Нарушения сна, присутствующие в течение длительного времени, не обнаруживают увеличения тяжести, тогда как тяжесть зрительных галлюцинаций нарастает со временем, и имеет отчетливую тенденцию к хронификации. [46] В другом исследовании было показано, что нарушения сна, включая RBD, могут присутствовать еще до клинической манифестации двигательных проявлений болезни Паркинсона и не связаны с тяжестью заболевания; и при этом они не являются показателем прогрессирования болезни Паркинсона. [47] Одно недавнее исследование нашло, что яркие сны были связаны с визуальными галлюцинациями и когнитивным ухудшением при болезни Паркинсона. [48]
Нейрохимическая патология
Среди нейромедиаторов головного мозга именно дофамин наиболее последовательно связан с развитием психоза при болезни Паркинсона. Однако и серотонин, и ацетилхолин, а также их взаимодействие с дофаминергической системой, могут также играть роль в появлении психотических симптомов.
Однако и серотонин, и ацетилхолин, а также их взаимодействие с дофаминергической системой, могут также играть роль в появлении психотических симптомов.
Вклад серотонина подтверждается наблюдением, в котором несколько фармакологических агентов, которые, как известно, снижают серотонинергическую активность (например, атипичные нейролептики и ондансетрон, антагонист серотонин 3 [5-HT3] рецепторов), уменьшают выраженность психотических симптомов. [49,50] С другой стороны, серотонинергические препараты вызывают делирий и психоз. [51] Недавно в клинических испытаниях были проверены новые лекарства, действующие на серотониновые 2 [5-HT2] и 5-HT3 рецепторы.
Давно известно, что болезнь Паркинсона включает холинергический дефицит, особенно в базальном ядре Мейнерта. [52] Этот дефицит еще более очевиден у пациентов-паркинсоников с когнитивным снижением и бредовыми нарушениями. [53] Кроме того, холинергический дефицит связан с развитием психоза у больных деменцией с тельцами Леви. [54] Антихолинергические препараты, используемые для лечения моторных симптомов при болезни Паркинсона, могут привести к появлению психоза, и исследование показывает, что ингибиторы холинэстеразы служат альтернативой атипичным нейролептикам при лечении паркинсонического психоза. [55]
[55]
В целом, кажется, паркинсонический психоз включает нарушения одновременно в нескольких нейромедиаторных системах.
Структурная патология
Выявление телец Леви было идентифицировано как фактор риска паркинсонического психоза. Одно исследование нашло сильную корреляцию между расположением телец Леви в височной доле — особенно в миндалине и парагиппокампе — и истинными зрительными галлюцинациями при деменции с тельцами Леви. [56] Расположение телец Леви в височной доле также связано с более ранним началом галлюцинаций при этой болезни. Крупное исследование 788 случаев паркинсонизма показало высокую специфичность (92,9%) зрительных галлюцинаций для заболевания с наличием телец Леви. [57]
Лечение
Прежде, чем лечить психоз при болезни Паркинсона, важно исключить любую другую патологию, которая может иметь сходные симптомы. Например, мочевые и легочные инфекции, метаболические и эндокринные нарушения, состояния недостаточной мозговой перфузии и психосоциальный стресс могут привести к делирию и психотическим симптомам, особенно у пожилых пациентов с болезнью Паркинсона. [58]
[58]
Если пациент находится на ранних стадиях заболевания, психотические симптомы могут иметь отношение к существовавшему ранее психическому расстройству или могут возникнуть из-за другого паркинсонического синдрома, например деменции с тельцами Леви. В одном исследовании, где все пациенты были идентифицированы как имеющие ранний галлюциноз (терапия леводопой не дольше трех месяцев), как было установлено позже, во всех случаях присутствовала вторая патология кроме, или в дополнение к болезни Паркинсона, которая могла спровоцировать развитие психотических симптомов. [59]
Еще одним заслуживающим внимания моментом при лечении паркинсонического психоза является полипрагмазия, которая, как было показано, является независимым фактором риска развития психотических симптомов при болезни Паркинсона. [60] Недофаминергические вещества, такие как наркотики, снотворные средства, антидепрессанты и транквилизаторы также могут способствовать проявлению психоза.
Снижение дозы препаратов
Принято считать, что самой эффективной стратегией первого ряда в лечении паркинсонического психоза является уменьшение дозировки противопаркинсонических препаратов. Если пациент принимает несколько лекарств, большинство руководств рекомендует постепенную отмену антипаркинсонических препаратов в следующем порядке: антихолинергические средства, ингибиторы MAO-B, амантадин, агонисты дофамина, ингибиторы катехол-O-метилтрансферазы (СOMT), и в последнюю очередь, леводопа. [61] Врачи клиницисты должны также рассмотреть возможность использования препаратов леводопы короткого действия, в противоположность пролонгированным препаратам; короткодействующие препараты леводопы имеют более низкий риск накопления и развития побочных эффектов. Если сокращение антипаркинсонических препаратов до самой низкой допустимой дозы не улучшает симптомов психоза, необходимо рассмотреть вопрос о добавлении в структуру лечения атипичного нейролептика.
Если пациент принимает несколько лекарств, большинство руководств рекомендует постепенную отмену антипаркинсонических препаратов в следующем порядке: антихолинергические средства, ингибиторы MAO-B, амантадин, агонисты дофамина, ингибиторы катехол-O-метилтрансферазы (СOMT), и в последнюю очередь, леводопа. [61] Врачи клиницисты должны также рассмотреть возможность использования препаратов леводопы короткого действия, в противоположность пролонгированным препаратам; короткодействующие препараты леводопы имеют более низкий риск накопления и развития побочных эффектов. Если сокращение антипаркинсонических препаратов до самой низкой допустимой дозы не улучшает симптомов психоза, необходимо рассмотреть вопрос о добавлении в структуру лечения атипичного нейролептика.
Атипичные нейролептики
Для борьбы с паркинсоническим психозом предпочтительно применять атипичные нейролептики (атипичные антипсихотики). Однако управление по контролю за продуктами и лекарствами (FDA, США) распорядилось, чтобы все производители положили в коробки с выпускаемыми препаратами предупреждение о том, что атипичные нейролептики, если они используются у пожилых пациентов с деменцией, связаны с более высоким риском смертности. [62] Метаанализ 15 исследований, в которых участвовало 3 353 пациента, рандомизированно получавших атипичные нейролептики, и 1 757 пациентов, рандомизированно получавших плацебо, не обнаружил доказательств специфических рисков для отдельных препаратов. [62] Этот вывод особенно важен для лечения психоза при болезни Паркинсона, особенно учитывая возраст и слабость пациентов с диагнозом болезни Паркинсона, у которых развился психоз.
[62] Метаанализ 15 исследований, в которых участвовало 3 353 пациента, рандомизированно получавших атипичные нейролептики, и 1 757 пациентов, рандомизированно получавших плацебо, не обнаружил доказательств специфических рисков для отдельных препаратов. [62] Этот вывод особенно важен для лечения психоза при болезни Паркинсона, особенно учитывая возраст и слабость пациентов с диагнозом болезни Паркинсона, у которых развился психоз.
Число атипичных нейролептиков на фармакологическом рынке неуклонно растет. Этот класс препаратов включает такие вещества, как арипипразол (Абилифай), клозапин (Азалептин, Лепонекс), оланзапин (Зипрекса), кветиапин (Сероквель), рисперидон (Рисполепт), зипрасидон (Зелдокс), а также более молодые препараты, такие как палиперидон (Инвега). Различия между этими веществами заключаются в профилях их связей с рецепторами, которые могут объяснить их относительно слабую тенденцию влиять на моторную сферу, а также и их уникальные профили побочных эффектов. Учитывая негативные последствия, связанные с использованием нейролептиков, очень важно четко определять продолжительность лечения. При болезни Паркинсона галлюцинации имеют свойство сохраняться с течением болезни, а наличие галлюцинаций до развития болезни как правило означает их постоянное присутствие при всех последующих оценках. [63]
При болезни Паркинсона галлюцинации имеют свойство сохраняться с течением болезни, а наличие галлюцинаций до развития болезни как правило означает их постоянное присутствие при всех последующих оценках. [63]
Согласно сведениям, распространенным Подкомиссией по Стандартам качества американской Академии Неврологии (AAN), у пациентов с паркинсоническим психозом клозапин снижает симптомы психоза и в некоторых случаях улучшает двигательные функции; кветиапин, возможно, улучшает течение психоза, а оланзапин, вероятно, не улучшает течения психоза и ухудшает двигательные функции. [64]
Интересно, что несмотря на многочисленные предупреждения о потенциальном ухудшении моторных симптомов при использовании других (кроме кветиапина и клозапина) атипичных нейролептиков у пациентов с болезнью Паркинсона, и несмотря на непротиворечивые отчеты, доказывающие, что клозапин — это золотой стандарт лечения при паркинсоническом психозе, недавний обзор использования лекарственных средств при лечении большого контингента ветеранов США с диагнозом болезни Паркинсона показал, что врачи клиницисты все еще 1) часто прописывали другие атипичные нейролептики, которые могут вызвать моторное ухудшение, — такие как рисперидон, оланзапин, арипипразол или зипрасидон; 2) периодически прописывали типичные нейролептики (первого поколения) с высокой вероятностью развития экстрапирамидной побочной симптоматики; и 3) редко прописывали клозапин, являющийся в настоящее время самым эффективным средством для лечения психозов при болезни Паркинсона. [65]
[65]
Ниже представлено краткое резюме по различным терапевтическим подходам, использовавшимся в лечении психоза при болезни Паркинсона.
Клозапин
Это производное дибензодиазепина является единственным атипичным нейролептиком, полностью рекомендуемым для лечения лекарственного психоза при болезни Паркинсона согласно метаанализу, опубликованному в 2007 году. [66] (Примечание: клозапин не одобрен в США для использования при паркинсоническом психозе). Многочисленные двойные слепые плацебо-управляемые и открытые исследования продемонстрировали его эффективность и высокую переносимость у больных с болезнью Паркинсона. Пациенты с болезнью Паркинсона могут испытывать улучшение при суточной дозе всего 6.25 мг. [67] Два рандомизированных, двойных слепых, плацебо-контролируемых исследования, посвященных использованию низких доз клозапина у больных паркинсонизмом — одно в США [68] и одно во Франции [67] — были опубликованы в 1999 году. Испытание, проведенное в США, продемонстрировало существенное улучшение симптомов, которое было выявлено путем оценки по четырем различным шкалам, рекомендованным для оценки тяжести психоза; в исследовании также не сообщалось о сколь-нибудь заметном ухудшении в двигательной сфере. [68] Кроме того, отмечалось значительное снижение выраженности тремора. Только 1 пациент был вынужден прекратить лечение из-за снижения количества лейкоцитов (белых кровяных телец). Сходные результаты были получены и в том исследовании, которое проводилось во Франции. [67] Метаанализ сообщил о 85% среднем уровне улучшения и приемлемой переносимости терапии. [69]
[68] Кроме того, отмечалось значительное снижение выраженности тремора. Только 1 пациент был вынужден прекратить лечение из-за снижения количества лейкоцитов (белых кровяных телец). Сходные результаты были получены и в том исследовании, которое проводилось во Франции. [67] Метаанализ сообщил о 85% среднем уровне улучшения и приемлемой переносимости терапии. [69]
Относительно долгосрочной эффективности и безопасности 1 ретроспективный анализ сообщил, что в течение 60 месяцев, 33 из 39 пациентов с болезнью Паркинсона (85%) имели продолжительную частичную/хорошую реакцию на клозапин, а у 5 пациентов (13%) психоз редуцировался полностью. [70] Данные последующего 5-летнего наблюдения показали, что 9 из 32 пациентов с болезнью Паркинсона (28%) прекратили лечение клозапином, потому что у них улучшились психотические симптомы, в то время как 3 пациента (9%) прекратили лечение из-за чрезмерной сонливости. [71]
Несмотря на то, что клозапин демонстрирует настолько высокую эффективность, его назначения часто избегают из-за возможного развития агранулоцитоза при его применении. В 1 исследовании (выборка> 99 000 пациентов США с шизофренией) подобное побочное явление зафиксировано у 0,38% пациентов, принимавших препарат, [72] поэтому производители препарата предупреждают, что использование клозапина должно сопровождаться еженедельным анализом количества лейкоцитов крови в течение первых шести месяцев; в течение последующих 6 месяцев анализ должен производиться каждые две недели; после чего контроль должен производиться ежемесячно. Другие неблагоприятные эффекты клозапина включают седацию, ортостатическую гипотензию и гиперсаливацию. [73] Использование атипичных антипсихотиков у пациентов с шизофренией было также связано с развитием метаболического синдрома, включающим инсулинорезистентность, увеличение веса, дислипидемию и нарушение метаболизма глюкозы. [74] Однако об этом синдроме не сообщалось у пациентов с болезнью Паркинсона.
В 1 исследовании (выборка> 99 000 пациентов США с шизофренией) подобное побочное явление зафиксировано у 0,38% пациентов, принимавших препарат, [72] поэтому производители препарата предупреждают, что использование клозапина должно сопровождаться еженедельным анализом количества лейкоцитов крови в течение первых шести месяцев; в течение последующих 6 месяцев анализ должен производиться каждые две недели; после чего контроль должен производиться ежемесячно. Другие неблагоприятные эффекты клозапина включают седацию, ортостатическую гипотензию и гиперсаливацию. [73] Использование атипичных антипсихотиков у пациентов с шизофренией было также связано с развитием метаболического синдрома, включающим инсулинорезистентность, увеличение веса, дислипидемию и нарушение метаболизма глюкозы. [74] Однако об этом синдроме не сообщалось у пациентов с болезнью Паркинсона.
То есть, исследования подтверждают преимущества использования низких доз клозапина для лечения психоза при болезни Паркинсона. Однако, из-за необходимости строгого контроля во время лечения клозапином, применение препарата становится не очень простым, и в настоящее время полным ходом идут исследования, имеющие целью производство более удобного и столь же эффективного как клозапин вещества для лечения паркинсонического психоза.
Однако, из-за необходимости строгого контроля во время лечения клозапином, применение препарата становится не очень простым, и в настоящее время полным ходом идут исследования, имеющие целью производство более удобного и столь же эффективного как клозапин вещества для лечения паркинсонического психоза.
Кветиапин
Среди всех атипичных нейролептиков кветиапин, дибензотиазепин, имеет самое близкое структурное родство с клозапином. Этот препарат — сильный антагонист серотониновых 5-HT2 и умеренный антагонист дофаминовых D2 рецепторов, при этом он показывает очень низкое сродство к мускариновым холинорецепторам. Кветиапин не изменяет уровень пролактина крови, с его применением не связан риск развития агранулоцитоза. Однако он не устраняет вызванную апоморфином стереотипию.
Были опубликованы материалы многочисленных открытых исследований, касавшихся применения кветиапина при лечении паркинсонического психоза, 2 из этих исследований были ретроспективными. В одном исследовании 35 из 43 пациентов с болезнью Паркинсона после назначения им кветиапина обнаружили существенное уменьшение психотических симптомов, и только 5 пациентов (у всех была деменция) отмечали умеренное ухудшение моторных функций. [75] В 2003, Фернандес и др. сообщали, что 78 из 106 пациентов с болезнью Паркинсона проходивших курс терапии кветиапином в центре лечения двигательных расстройств, получали препарат, в среднем, 15 месяцев. У 87 (82%) из них наступило частичное или полное выздоровление от психоза. [76] Об умеренном ухудшении двигательных функций сообщили более чем за 15 месяцев 32% пациентов, у всех них наблюдались тяжелые формы деменции.
[75] В 2003, Фернандес и др. сообщали, что 78 из 106 пациентов с болезнью Паркинсона проходивших курс терапии кветиапином в центре лечения двигательных расстройств, получали препарат, в среднем, 15 месяцев. У 87 (82%) из них наступило частичное или полное выздоровление от психоза. [76] Об умеренном ухудшении двигательных функций сообщили более чем за 15 месяцев 32% пациентов, у всех них наблюдались тяжелые формы деменции.
Два двойных слепых исследования применения кветиапина при болезни Паркинсона не сообщили ни о каком существенном улучшении при психозе. Первое из них, в котором 31 пациенту рандомизированно назначали (2:1) кветиапин или плацебо, не фиксировалось должным образом для обнаружения эффекта лечения. [77] Во втором исследовании 30 пациентам рандомизированно назначали кветиапин, и 28 пациентам рандомизированно назначали на плацебо. [78] Из 15 пациентов, прекративших лечение в группе получавших кветиапин, 10 сообщили о недостаточном терапевтическом эффекте. Авторы предполагают, что этот большой процент отсеявшихся, возможно, повлиял на результаты, не показавшие благоприятного воздействие кветиапина на лекарственный психоз при болезни Паркинсона. В третьем двойном слепом исследовании, изучавшем влияние кветиапина на архитектуру быстрого сна, рандомизированно назначали 16 пациентам с диагнозом болезни Паркинсона, испытывающим визуальные галлюцинации кветиапин либо плацебо. [79] Пациенты проходили обследование методом полисомнографии до и после курса лечения. Во время каждого осмотра пациентов просили заполнить оценочные шкалы CGIS, BPRS и секцию шкалы UPDRS, оценивающую моторную сферу. Средняя доза кветиапина, которая назначалась пациентам, составляла 58.3 мг/сут. Несмотря на то, что не было обнаружено значительной разницы в изменении длительности REM сна ни в одной подгруппе, у пациентов, которым был назначен кветиапин, показали улучшение по шкале CGIS (P =. 03) и по шкале BPRS (P =. 02) в части уменьшения выраженности зрительных галлюцинаций. Не было отмечено никакой статистической разницы по шкале UPDRS (секция, оценивающая моторику). Несмотря на небольшую выборку, это — первое двойное слепое исследование, которое показало эффективность кветиапина по сравнению с плацебо в контроле зрительных галлюцинаций у пациентов с болезнью Паркинсона.
В третьем двойном слепом исследовании, изучавшем влияние кветиапина на архитектуру быстрого сна, рандомизированно назначали 16 пациентам с диагнозом болезни Паркинсона, испытывающим визуальные галлюцинации кветиапин либо плацебо. [79] Пациенты проходили обследование методом полисомнографии до и после курса лечения. Во время каждого осмотра пациентов просили заполнить оценочные шкалы CGIS, BPRS и секцию шкалы UPDRS, оценивающую моторную сферу. Средняя доза кветиапина, которая назначалась пациентам, составляла 58.3 мг/сут. Несмотря на то, что не было обнаружено значительной разницы в изменении длительности REM сна ни в одной подгруппе, у пациентов, которым был назначен кветиапин, показали улучшение по шкале CGIS (P =. 03) и по шкале BPRS (P =. 02) в части уменьшения выраженности зрительных галлюцинаций. Не было отмечено никакой статистической разницы по шкале UPDRS (секция, оценивающая моторику). Несмотря на небольшую выборку, это — первое двойное слепое исследование, которое показало эффективность кветиапина по сравнению с плацебо в контроле зрительных галлюцинаций у пациентов с болезнью Паркинсона.
В еще одном двойном слепом исследовании, касавшемся терапии при болезни Паркинсона, 45 пациентам рандомизированно назначали кветиапин или клозапин. [80] Обе группы испытали существенное улучшение психотических симптомов, и группы не отличались по средней величине этого улучшения.
Другое исследование включало35 пациентов с паркинсоническим психозом, находившихся под наблюдением более 24 месяцев. [81] В течение 24-месячного периода терапевтический ответ на лечение кветиапином наблюдался у 15 пациентов (43%). К концу 24 -го месяца лечения 11 все еще получали кветиапин, 3 прекратил лечение вследствие редукции психоза, а 3 прекратили лечение по причинам, связанным с финансовой сферой. Не было сообщений о каком-либо ухудшении моторики.
Некоторые исследования обнаруживали, что кветиапин может иметь положительное влияние на архитектуру сна. [82] Принимая за основу известную гипотезу о наличии связи между визуальными галлюцинациями при болезни Паркинсона и нарушениями сна (включая бессонницу и дневную сонливость), исследователи в настоящее время пытаются оценить влияние кветиапина на сон и психотические симптомы при этом заболевании.
Иными словами, кветиапин, кажется, несколько менее эффективен при лечении паркинсонического психоза, чем клозапин. Он не устраняет тремор, и в ряде случаев даже может вызвать умеренное моторное ухудшение. [49] Тем не менее, ни в одном исследовании ни разу не сообщалось о том, что кветиапин вызывал какое-либо существенное ухудшение моторной сферы, потребовавшее госпитализации — как это случалось у пациентов, получавших оланзапин или рисперидон. Кроме того, с применением кветиапина не связан риск развития агранулоцитоза, и таким образом его применение не требует постоянного тщательного контроля картины крови, что является обязательным при использовании клозапина.
Пимавансерин
Это новый препарат, обратный агонист 5-HT2A рецепторов, который, как сообщают, смягчает симптомы психоза при болезни Паркинсона, не ухудшая моторных симптомов. [83] В 6-недельном рандомизированном двойном слепом плацебо-контролируемом исследовании 199 пациентов с паркинсоническим психозом получали либо пимавансерин в дозе 40мг/сут, либо плацебо. [84] Основным результатом исследования был антипсихотический эффект препарата, что оценивалось независимыми экспертами по шкале SAPS-PD. С применением пимавансерина было связано снижение на 5,79 пунктов по шкале SAPS-PD, по сравнению с уменьшением на 2,73 пункта для плацебо (difference, ?3.06; 95% CI, ?4·91 to ?1·20; P=.001; Cohen’s d 0.50). В целом, пимавансерин хорошо переносился, был безопасен и не ухудшал двигательных функций. [84] Ученые исследуют и другие лекарства с тем же фармакологическим эффектом, такие как кетансерин и алтансерин.
[84] Основным результатом исследования был антипсихотический эффект препарата, что оценивалось независимыми экспертами по шкале SAPS-PD. С применением пимавансерина было связано снижение на 5,79 пунктов по шкале SAPS-PD, по сравнению с уменьшением на 2,73 пункта для плацебо (difference, ?3.06; 95% CI, ?4·91 to ?1·20; P=.001; Cohen’s d 0.50). В целом, пимавансерин хорошо переносился, был безопасен и не ухудшал двигательных функций. [84] Ученые исследуют и другие лекарства с тем же фармакологическим эффектом, такие как кетансерин и алтансерин.
29 апреля 2016 года имавансерин был одобрен FDA в качестве препарата для лечения психозов, связанных с болезнью Паркинсона.
Препарат имеет торговое наименование Нуплазид, с 2018 года для лечения бреда и галлюцинаций, связанных с болезнью Паркинсона применяются капсулы по 34 мг и таблетки по 10 мг один раз в сутки. Доза 10 мг применяется у лиц, параллельно с пимавансерином принимающих ингибиторы CYP3A4 (например, кетоконазол).
В России препарат в 2019 году проходил клинические испытания, в 2020 году еще не зарегистрирован.
Другие атипичные антипсихотики, иногда используемые при лечении психоза при болезни Паркинсона.
Арипипразол
В отличие от других атипичных нейролептиков, арипипразол является частичным агонистом D2 и 5-HT1A рецепторов. [85] Кроме того, он, как полагают, несет относительно низкий риск экстрапирамидных побочных эффектов из-за его высокого сродства к 5-HT2/D2 рецепторам. Доступные по арипипразолу данные предполагают, что его эффективность и переносимость у пациентов носят непостоянный характер.
До настоящего времени были опубликованы 2 открытых исследования, касающихся применения арипипразола у больных паркинсонизмом. Первое, включавшее 8 пациентов с вероятным диагнозом болезни Паркинсона, исследовало применение арипипразола при лечении индуцированного противопаркинсоническими препаратами психоза. [86] Только 2 из 8 пациентов показали почти полное купирование психоза. Остальные 6 прекратили лечение в связи с моторным ухудшением (2), отсутствием улучшения моторных симптомов, которые ухудшились вследствие применения оланзапина (1), неэффективностью контроля психоза при помощи арипипразола (2), или невыносимой бессонницей, беспокойством и спутанностью (1).
Второе открытое исследование включало 14 пациентов, сообщалось о схожих результатах. [87] В этом исследовании 6 из 14 пациентов испытали улучшение психоза. Остальные 8 пациентов прекратили лечение из-за ухудшения паркинсонизма (3), усиления психоза (2), ухудшения как паркинсонизма, так и психоза (2), и недостаточной эффективности (1).
Предварительные данные свидетельствуют, что в то время как арипипразол может быть эффективен для некоторых пациентов, его применение несет высокий риск побочных эффектов, и результаты являются переменчивыми. Существует потребность в дальнейших контролируемых исследованиях арипипразола у пациентов с болезнью Паркинсона.
Мелперон
Этот атипичный нейролептик не показал эффективности при лечении психоза у паркинсонических больных. Результаты неопубликованного многофокусного двойного слепого плацебо контролируемого исследования показали, что мелперон в дозах 20, 40, и 60 мг не ухудшал моторные симптомы. [88] Однако лекарственное средство оказалось неэффективно в контролировании психотических симптомов.
Оланзапин
Химически близкий к клозапину, оланзапин является более атипичным, чем рисперидон, поскольку дозы, вызывающие каталепсию у мышей выше, чем те, которые требуются для применения у людей; оланзапин также не вызывает значимого увеличения секреции пролактина. [89] опубликованные исследования показывают, что моторное ухудшение происходит приблизительно у 40% пациентов с болезнью Альцгеймера. [49]
Был опубликован ряд двойных слепых исследований применения оланзапина у пациентов с болезнью Паркинсона. Одно из них, в котором сравнивались оланзапин с клозапином, было прервано после того, как 6 из 7 из получавших оланзапин пациентов испытали значительное ухудшение двигательных функций. [90] Плацебо-контролируемые исследования не продемонстрировали ни существенного улучшения психотических симптомов при болезни Паркинсона, ни ухудшения моторных функций. [91-92]
Суммируя вышесказанное, оланзапин оказался неэффективным при лечении психоза у пациентов с болезнью Паркинсона, и способен привести к значительному ухудшению моторных функций даже в низких дозах.
Ондансетрон
Это противорвотный препарат изучался как возможное средство для лечения шизофрении из-за его антагонизма в отношении 5-HT3 рецепторов, однако применение препарата с вышеуказанной целью оказалось неэффективным. Тем не менее, существует несколько публикаций, указывающих на то, что этот препарат эффективен для лечения психоза при паркинсонизме, и не ухудшает моторных симптомов. По-видимому, это связано с его высокой селективностью. Ондансетрон, снимал симптомы психоза у больных с поздними стадиями болезни Паркинсона, не вызывая каких-либо серьезных побочных эффектов. [50] Однако эти положительные результаты не были воспроизведены другими исследователями. [93], Кроме того, высокая стоимость препарата препятствовала его широкому исследованию при лечении паркинсонических психозов.
Рисперидон
Хотя рисперидон химически отличается от клозапина, он был одобрен в США как атипичный нейролептик. Как оказалось, этот препарат ведет себя, в основном, как «типичный» антипсихотик, который вызывает дозозависимые экстрапирамидные побочные эффекты и повышает уровень пролактина. [94-96] Большинство исследований рисперидона у больных с паркинсонизмом являются открытыми. В целом, исследовательские отчеты показывают существенное улучшение при психозе. Однако результаты лечения, касающиеся двигательных побочных эффектов, оказались весьма вариабельны и значительно отличаются от исследования к исследованию. Метаанализ показал, что 27 из 82 леченных рисперидоном пациентов с диагнозом болезни Паркинсона (33%) испытали ухудшение моторных симптомов. [97]
[94-96] Большинство исследований рисперидона у больных с паркинсонизмом являются открытыми. В целом, исследовательские отчеты показывают существенное улучшение при психозе. Однако результаты лечения, касающиеся двигательных побочных эффектов, оказались весьма вариабельны и значительно отличаются от исследования к исследованию. Метаанализ показал, что 27 из 82 леченных рисперидоном пациентов с диагнозом болезни Паркинсона (33%) испытали ухудшение моторных симптомов. [97]
В единственном двойном слепом исследовании рисперидона у паркинсонических больных 10 пациентам рандомизированно дали клозапин или рисперидон. [98] Два пациента в группе клозапина и 1 пациент в группе рисперидона прекратили лечение. Существенное улучшение симптомов психоза наблюдалось в группе рисперидона, но не в группе клозапина, когда результат измерялся по шкале BPRS (кластер психозов). Число умеренных улучшений не отличалось между обеими группами. Средний показатель UPDRS (Unified Parkinson’s disease rating scale), улучшился в группе клозапина и, ухудшился в группе рисперидона; однако, это различие не достигло статистической значимости.
Вариабельность результатов исследований применения рисперидона, в основном, объясняется открытостью большинства исследований. Однако различные клиницисты, возможно, отличались друг от друга по своим оценкам паркинсонизма, а также различные исследования использовали различные графики титрования и длительность наблюдения. Учитывая многочисленные сообщения о моторном ухудшении у пациентов с болезнью Паркинсона, получавших рисперидон, и учитывая его свойства как «типичного» антипсихотика, многие специалисты по двигательным расстройствам по понятным причинам не рекомендуют использовать этот препарат для лечения психоза при болезни Паркинсона.
Зипрасидон
По сравнению с другими атипичными нейролептиками, зипрасидон имеет большее сродство к серотониновым 5-HT2, чем к дофаминовым D2 рецепторам. [99] Его использование было ограничено из-за его влияния на электрическую проводимость сердца, но никогда не сообщалось ни об одном случае, когда применение зипрасидона привело бы к возникновению желудочковой тахикардии по типу «пируэта» вследствие его способности удлинять интервал QT. [100]
[100]
Были опубликованы два исследования применения зипрасидона у пациентов с болезнью Паркинсона. Первое, проводившееся в Испании, исследование, включавшее 12 пациентов с болезнью Паркинсона, являлось открытым. [101] В среднем, отмечалось улучшение психоза на 58,4% (средняя доза 26 мг/сут) после 1 месяца терапии и на 72% (средняя доза, 32 мг/сут) после 12 недель; результат измерялся по шкале NPI. Два пациента прекратили лечение из-за седативного эффекта или ухудшения походки. Моторный кластер UPDRS не выявил значительного ухудшения, несмотря на визуально наблюдаемое ухудшение походки. Второе исследование, проводившееся в Германии, включало 5 пациентов с психозом при болезни Паркинсона, получавших внутримышечные инъекций зипрасидона (от 10 до 20 мг) при острой ажитации. [102] Среднее улучшение симптомов составило 24,6 пункта по шкале BPRS, и ни о каком ухудшении моторики не сообщалось.
Хотя представляется, что зипрасидон может представлять относительно безопасное и эффективное средство для лечение психоза при болезни Паркинсона у некоторых пациентов, после рассмотрения данных относительно применения зипрасидона для лечения шизофрении, группа психиатров экспертов пришла к заключению, что экстрапирамидный профиль побочных эффектов этого препарата более благоприятен по сравнению с рисперидоном, примерно одинаков с оланзапином, но «совсем не так хорош, как у кветиапина или клозапина». [103]
[103]
Ингибиторы холинэстеразы
Донепезил
Рандомизированное, плацебо-контролируемое исследование донепезила у 22 пациентов с паркинсоническим психозом на фоне деменции не выявило различий в тяжести психоза между пациентами, получающими донепезил и пациентами, получающими плацебо, что было измерено с помощью шкалы BPRS. [104] Однако это исследование не включало пациентов с наиболее тяжелыми формами психоза. В 20-недельном двойном слепом, плацебо-контролируемом исследовании донепезила участвовали 14 пациентов с болезнью Паркинсона и когнитивным ухудшением. [105] Ни один пациент не отметил ухудшения моторных функций. Улучшения психотической симптоматики не было статистически значимым, вероятно, из-за низких базовых показателей и небольшого размера выборки.
Галантамин
Этот препарат отличается от других ингибиторов холинэстеразы тем, что он также связывается с никотинзависимыми рецепторами ацетилхолина, что, по-видимому, предотвращает нарушение регуляции обмена ацетилхолина, которое может развиться после применения ингибиторов холинэстеразы. [106] Повышение активности никотиновых рецепторов, расположенных на пресинаптических мембранах дофаминергических нейронов стриатума, в свою очередь, облегчает высвобождение дофамина и оказывает положительное воздействие на моторные симптомы. Одно открытое исследование галантамина у больных с паркинсонической деменцией сообщило, что у 7 из 9 пациентов снизилась тяжесть галлюцинаторной симптоматики, а у 3 из этих 7 галлюцинации полностью исчезли. [106], Кроме того, у 6 из 9 пациентов произошло улучшение двигательных проявлений паркинсонизма. Тем не менее, остальные 3 отметили усиление тремора.
[106] Повышение активности никотиновых рецепторов, расположенных на пресинаптических мембранах дофаминергических нейронов стриатума, в свою очередь, облегчает высвобождение дофамина и оказывает положительное воздействие на моторные симптомы. Одно открытое исследование галантамина у больных с паркинсонической деменцией сообщило, что у 7 из 9 пациентов снизилась тяжесть галлюцинаторной симптоматики, а у 3 из этих 7 галлюцинации полностью исчезли. [106], Кроме того, у 6 из 9 пациентов произошло улучшение двигательных проявлений паркинсонизма. Тем не менее, остальные 3 отметили усиление тремора.
Ривастигмин
Препарат отличается от других ингибиторов холинэстеразы тем, что в дополнение к воздействию на ацетилхолинэстеразу, он также ингибирует бутирилхолинэстеразу. Большое двойное слепое плацебо-контролируемое исследование эффектов ривастигмина при лечении зрительных галлюцинаций у пациентов в состоянии паркинсонического психоза включало 188 больных со зрительными галлюцинациями и 348 без галлюцинаций. [107] Пациенты, испытывавшие галлюцинации, показали значительное повышение общего балла по шкале NPI, особенно это касалось подпункта ажитации/агрессии. Кроме того, для пациентов с галлюцинациями ривастигмин оказался более полезен, чем для тех, кто галлюцинаций не испытывал. Вероятно это произошло из-за более быстрого снижения в группе галлюцинирующих пациентов, получавших плацебо. В настоящее время активно ведутся дополнительные двойные слепые контролируемые исследования применения ривастигмина для лечения зрительных галлюцинаций при паркинсоническом психозе.
[107] Пациенты, испытывавшие галлюцинации, показали значительное повышение общего балла по шкале NPI, особенно это касалось подпункта ажитации/агрессии. Кроме того, для пациентов с галлюцинациями ривастигмин оказался более полезен, чем для тех, кто галлюцинаций не испытывал. Вероятно это произошло из-за более быстрого снижения в группе галлюцинирующих пациентов, получавших плацебо. В настоящее время активно ведутся дополнительные двойные слепые контролируемые исследования применения ривастигмина для лечения зрительных галлюцинаций при паркинсоническом психозе.
Такрин
Первое опубликованное исследование, касавшееся применения ингибиторов холинэстеразы при болезни Паркинсона касалось применения такрина для лечения паркинсонической деменции у больных, испытывающих спутанность и зрительные галлюцинации. [108] В этом открытом исследовании у 5 из 7 дементных пациентов произошла полная редукция психотических симптомов, а состояние остальных двух пациентов улучшилось. Никто не испытал ухудшения моторных функций. Однако исследователи Отт и Ланнон сообщали о том, что на фоне применения такрина у одного паркинсонического пациента наступило ухудшение в моторной сфере. [109] Такрин редко применяется для лечения паркинсонического психоза в связи с его гепатотоксичностью.
Однако исследователи Отт и Ланнон сообщали о том, что на фоне применения такрина у одного паркинсонического пациента наступило ухудшение в моторной сфере. [109] Такрин редко применяется для лечения паркинсонического психоза в связи с его гепатотоксичностью.
Другие терапевтические стратегии
Антидепрессанты
Предшествующие исследования показали, что некоторые антидепрессанты могут вызвать или усиливать психотические симптомы. [110] Тем не менее, существуют отдельные свидетельства того, что ряд антидепрессантов — таких, как кломипрамин или циталопрам действительно могут облегчать психотические симптомы, особенно у пациентов с сопутствующей депрессией. [111, 112] На сегодняшний день все свидетельства этого ограничиваются только отдельными историями болезни.
Электросудорожная терапия (ЭСТ)
ЭСТ может быть эффективным средством для лечения психических расстройств — таких как терапевтически резистентные депрессия и шизофрения. Исследования применения ЭСТ при болезни Паркинсона ограничиваются лишь историями болезни; однако, кажется, ЭСТ могла бы быть полезной в ослаблении психотических симптомов при болезни Паркинсона, особенно при наличии сопутствующей депрессии и/или когда применение медикаментозной терапии оказалось неэффективно. [113] Отчеты также показывают, что ЭСТ может на время снизить тяжесть двигательных расстройств. Однако для применения ЭСТ может потребоваться госпитализация. Побочные эффекты включают когнитивные расстройства и спутанность. По этим причинам ЭСТ, как правило, рассматривают как вариант лечения только тогда, когда попытки фармакологической терапии оказались безуспешными.
[113] Отчеты также показывают, что ЭСТ может на время снизить тяжесть двигательных расстройств. Однако для применения ЭСТ может потребоваться госпитализация. Побочные эффекты включают когнитивные расстройства и спутанность. По этим причинам ЭСТ, как правило, рассматривают как вариант лечения только тогда, когда попытки фармакологической терапии оказались безуспешными.
Мемантин
Мемантин является антагонистом N-метил-D-аспартат (NMDA) рецептора, применяемым для лечения болезни Альцгеймера. Этот препарат использовался в качестве альтернативы атипичным нейролептикам при лечении галлюцинаций у пациентов с болезнью Паркинсона и когнитивными нарушениями. Мемантин, кажется, вызывает меньше побочных эффектов и имеет лучшую переносимость, чем антипсихотики; однако несколько доступных контролируемых исследований сообщили противоречивые данные. [114,115]
Психологические подходы
Немедикаментозная терапия психоза и его поведенческих и эмоциональных последствий всегда должна быть включена в структуру лечения. Психоз при болезни Паркинсона имеет тенденцию к хроническому течению, и может не реагировать даже на агрессивную фармакологическую тактику. Кроме того, психоз может быть связан с наличием параллельно текущей аффективной патологии, например депрессии. Обучение самоконтролю и структурированные психотерапевтические интервенции являются важными стратегиями в оптимизации лечения психоза.
Психоз при болезни Паркинсона имеет тенденцию к хроническому течению, и может не реагировать даже на агрессивную фармакологическую тактику. Кроме того, психоз может быть связан с наличием параллельно текущей аффективной патологии, например депрессии. Обучение самоконтролю и структурированные психотерапевтические интервенции являются важными стратегиями в оптимизации лечения психоза.
Одно исследование показало, что 36 из 46 пациентов с галлюцинациями при болезни Паркинсона сообщили, что самостоятельно используют различные копинг-стратегии: познавательные, интерактивные и визуальные техники с целью справиться со своими симптомами. [116], В то время, как исследование не включало шкал для формальной оценки эффективности этих стратегий, пациенты, использовавшие их, сообщили, что их галлюцинации были «надоедливыми или угнетающими» только 39% времени, по сравнению с 60% времени для тех, кто не использовал копинг-стратегии. Несмотря на то, что это различие не слишком велико, было бы целесообразным проводить дальнейшие исследования для определения наиболее эффективных копинг-стратегий.
Структурированные психотерапевтические вмешательства, включая когнитивно-поведенческую терапию (КПТ), поддерживающую терапию и психологическое обучение в лечении психоза при болезни Паркинсона также могут быть полезны. [117-119], Применение КПТ может оказаться весьма полезным особенно на ранних стадиях психоза при болезни Паркинсона, так как психоз на ранней стадии, как правило, еще включает сохранную критику.
Заключение
Психотические симптомы являются общей чертой PD и связаны с длительностью заболевания и его тяжестью, наличием сопутствующих деменции, депрессии, а также с величиной возраста. Патофизиология психоза, как теперь известно, включает взаимодействие между внешними, связанными с лечением; и внутренними, связанными с болезнью компонентами, такими как нейрохимические нарушения (например, связанные с обменом дофамина, серотонина, ацетилхолина), структурная патология, дисфункция зрительного анализатора и нарушения регуляции сна. Варианты лечения психоза при болезни Паркинсона весьма многочисленны и могут включать различные фармакологические и нефармакологические методы. Первый этап лечения традиционно включает сокращение или отмену противопаркинсонических препаратов; однако, если симптомы сохраняются, это может потребовать назначение дополнительного препарата. В то время как клозапин и кветиапин, кажется, в данном случае являются самыми эффективными атипичными нейролептиками, их побочные эффекты вызвали большой интерес исследователей к тому, чтобы найти альтернативные эффективные препараты, в том числе обратные агонисты/антагонисты 5HT2 рецепторов, такие как пимавансерин, кетансерин и алтансерин, которые могут быть более эффективными при большей безопасности применения.
Первый этап лечения традиционно включает сокращение или отмену противопаркинсонических препаратов; однако, если симптомы сохраняются, это может потребовать назначение дополнительного препарата. В то время как клозапин и кветиапин, кажется, в данном случае являются самыми эффективными атипичными нейролептиками, их побочные эффекты вызвали большой интерес исследователей к тому, чтобы найти альтернативные эффективные препараты, в том числе обратные агонисты/антагонисты 5HT2 рецепторов, такие как пимавансерин, кетансерин и алтансерин, которые могут быть более эффективными при большей безопасности применения.
Литература:
- Witjas T, Kaphan E, Azulay JP, et al. Nonmotor fluctuations in Parkinson’s disease: frequent and disabling. Neurology. 2002;59:408-413.
- Global Parkinson’s Disease Survey Steering Committee. Factors impacting on quality of life in Parkinson’s disease: results from an international survey. Mov Disord. 2002;17:60-67.
- Marsh L, Williams JR, Rocco M, Grill S, Munro C, Dawson TM.
 Psychiatric comorbidities in patients with Parkinson disease and psychosis.
Psychiatric comorbidities in patients with Parkinson disease and psychosis. - Aarsland D, Larsen JP, Tandbert E, Laake K. Predictors of nursing home placement in Parkinson’s disease: a population-based prospective study. J Am Geriatr Soc. 2000;48:938-942.
- Goetz CG, Stebbins GT. Mortality and hallucinations in nursing home patients with advanced Parkinson’s disease. Neurology. 1995;45:669-671
- Goetz CG, Stebbins GT. Risk factors for nursing home placement in advanced Parkinson’s disease. Neurology. 1993;43:2227-2229
- Mack J, Rabins P, Anderson K, et al. Prevalence of psychotic symptoms in a community-based Parkinson disease sample. Am J Geriatr Psychiatry.2012;20:123-132.
- Fenelon G, Mahieux F, Huron R, Ziegler M. Hallucinations in Parkinson’s disease: prevalence, phenomenology and risk factors.
- Forsaa EB, Larsen JP, Wentzel-Larsen T, et al. A 12-year population-based study of psychosis in Parkinson disease. Arch Neurol. 2010;67:996-1001.

- Hely MA, Reid WG, Adena MA, Halliday GM, Morris JG. The Sydney multicenter study of Parkinson’s disease: the inevitability of dementia at 20 years. Mov Disord. 2008;23:837-844.
- Lee AH, Weintraub D. Psychosis in Parkinson’s disease without dementia: common and comorbid with other non-motor symptoms. Mov Disord. 2012;27:858-863.
- Factor SA, Scullin MK, Sollinger AB, et al. Cognitive correlates of hallucinations and delusions in Parkinson’s disease. J Neurol Sci. 2014;347:316-321.
- American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders, Fourth Edition. Washington, DC: American Psychiatric Association; 2000.
- Factor SA, Molho ES. Threatening auditory hallucinations and Cotard syndrome in Parkinson disease. Clin Neuropharmacol. 2004;27:205-207.
- Zahodne LB, Fernandez HH. Parkinson’s psychosis. Curr Treat Options Neurol. 2010;12:200-211.
- Goetz CG, Fan W, Leurgans S, Bernard B, Stebbins GT. The malignant course of «benign hallucinations» in Parkinson disease.
 Arch Neurol. 2006;63:713-716.
Arch Neurol. 2006;63:713-716. - Moskovitz C, Moses H 3rd, Klawans HL. Levodopa-induced psychosis: a kindling phenomenon. Am J Psychiatry. 1978;135:669-675.
- Pappert EJ, Goetz CG, Niederman FG, Raman R, Leurgans S. Hallucinations, sleep fragmentation, and altered dream phenomena in Parkinson’s disease. Mov Disord. 1999;14:117-121.
- Fernandez HH, Aarsland D, F?nelon G, et al. Scales to assess psychosis in Parkinson’s disease: critique and recommendations. Mov Disord.2008;23:484-500.
- Aarsland D, Larsen JP, Cummins JL, Laake K. Prevalence and clinical correlates of psychotic symptoms in Parkinson disease: a community-based study. Arch Neurol. 1999;56:595-601.
- Giladi N, Treves TA, Paleacu D, et al. Risk factors for dementia, depression and psychosis in long-standing Parkinson’s disease. J Neural Transm.2000;107:59-71.10809404″>
- de Maindreville AD, F?nelon G, Mahieux F. Hallucinations in Parkinson’s disease: a follow-up study. Mov Disord. 2005;20: 212-217.

- Papapetropoulos S, Argyriou AA, Ellul J. Factors associated with drug-induced visual hallucinations in Parkinson’s disease. J Neurol. 2005; 252:1223-1228.
- Holroyd S, Currie L, Wooten GF. Prospective study of hallucinations and delusions in Parkinson’s disease. J Neurol Neurosurg Psychiatry. 2001;70:734-738.
- Factor SA, Steenland NK, Higgins DS, et al. Disease-related and genetic correlates of psychotic symptoms in Parkinson’s disease. Mov Disord.2011;26:2190-2195
- Aarsland D, Br?nnick K, Ehrt U, et al. Neuropsychiatric symptoms in patients with Parkinson’s disease and dementia: frequency, profile and associated care giver stress. J Neurol Neurosurg Psychiatry. 2007;78:36-42.
- Fernandez HH, Trieschmann ME, Okun MS. Rebound psychosis: effect of discontinuation of antipsychotics in Parkinson’s disease. Mov Disord.2005;20:104-105.
- Chou KL, Fernandez HH. Combating psychosis in Parkinson’s disease patients: the use of antipsychotic drugs. Expert Opin Investig Drugs.
 2006;15:339-349.
2006;15:339-349. - Factor SA, Molho ES, Brown DL. Combined clozapine and electroconvulsive therapy for the treatment of drug-induced psychosis in Parkinson’s disease. J Neuropsychiatry Clin Neurosci. 1995;7:304-307.
- Glenth?j BY, Hemmingsen R. Dopaminergic sensitization: implications for the pathogenesis of schizophrenia. Prog Neuropsychopharmacol Biol Psychiatry. 1997;21:23-46.
- Kapur S, Zipursky R, Jones C, Remington G, Houle S. Relationship between dopamine D(2) occupancy, clinical response, and side effects: a double-blind PET study of first-episode schizophrenia. Am J Psychiatry. 2000;157:514-520.
- Goetz CG, Tanner CM, Klawans HL. Pharmacology of hallucinations induced by long-term drug therapy. Am J Psychiatry. 1982;139:494-497.
- Wolters EC, Berendse HW. Management of psychosis in Parkinson’s disease. Curr Opin Neurol. 2001;14:499-504.
- F?nelon G, Goetz CG, Karenberg A. Hallucinations in Parkinson disease in the prelevodopa era.
- Tanner CM, Vogel C, Goetz CG, Klawans HL.
 Hallucinations in Parkinson’s disease: a population study. Ann Neurol. 1983;12:136.
Hallucinations in Parkinson’s disease: a population study. Ann Neurol. 1983;12:136. - Postma JU, Van Tilburg W. Visual hallucinations and delirium during treatment with amantadine (Symmetrel). J Am Geriatr Soc. 1975;23:212-215.
- Klein C, K?mpf D, Pulkowski U, Moser A, Vieregge P. A study of visual hallucinations in patients with Parkinson’s disease. J Neurol. 1997;244:371-377.
- Merims D, Shabtai H, Korczyn AD, Peretz C, Weizman N, Giladi N. Antiparkinsonian medication is not a risk factor for the development of hallucinations in Parkinson’s disease. J Neural Transm. 2004;111:1447-1453.
- Diedrich NJ, Goetz CG, Raman R, Pappert EJ, Leurgans S, Piery V. Poor visual discrimination and visual hallucinations in Parkinson’s disease. Clin Neuropharmacol. 1998;21:289-295.
- Bodis-Wollner I. Visual deficits related to dopamine deficiency in experimental animals and Parkinson’s disease patients. Trends Neurosci. 1990;13:296-302.
- Maurage CA, Ruchoux MM, de Vos R, Surguchov A, Destee A.
 Retinal involvement in dementia with Lewy bodies: a clue to hallucinations? Ann Neurol. 2003;54:542-547.
Retinal involvement in dementia with Lewy bodies: a clue to hallucinations? Ann Neurol. 2003;54:542-547. - Onofrj M, Bonanni L, Albani G, Mauro A, Bulla D, Thomas A. Visual hallucinations in Parkinson’s disease: clues to separate origins. J Neurol Sci. 2006;248:143-150.
- Stebbins GT, Goetz CG, Carillo MC, et al. Altered cortical visual processing in PD with hallucinations: an fMRI study. Neurology. 2004;63:1409-1416.
- Barnes J, Boubert L, Harris J, Lee A, David AS. Reality monitoring and visual hallucinations in Parkinson’s disease.
- Pacchetti C, Manni R, Zangaglia R, et al. Relationship between hallucinations, delusions, and rapid eye movement sleep behavior disorder in Parkinson’s disease. Mov Disord. 2005;20:1439-1448.
- Goetz CG, Wuu J, Curgian LM, Leurgans S. Hallucinations and sleep disorders in PD: six-year prospective longitudinal study.
- Lavault S, Leu-Semenescu S, Tezenas du Montcel S, Cochen de Cock V, Vidailhet M, Arnulf I. Does clinical rapid eye movements behavior disorder predict worse outcomes in Parkinson’s disease? J Neurol.
 2010;257:1154-1159.
2010;257:1154-1159. - Gama RL, de Bruin VM, de Bruin PF, et al. Risk factors for visual hallucinations in patients with Parkinson’s disease. Neurol Res. 2015;37:112-116.
- Fernandez HH, Trieschmann ME, Friedman JH. The treatment of psychosis in Parkinson’s disease: safety considerations. Drug Saf. 2003;26:643-659.
- Zoldan J, Friedberg G, Livneh M, Melamed E. Psychosis in advanced Parkinson’s disease: treatment with ondansetron, a 5-HT3 receptor antagonist.
- Van der Mast RC, Fekkes D. Serotonin and amino acids: partners in delirium pathophysiology? Semin Clin Neuropsychiatry. 2000;5:125-131.
- Whitehouse PJ. Clinical and neurochemical consequences of neuronal loss in the nucleus basalis of Meynert in Parkinson’s disease and Alzheimer’s disease. Adv Neurol. 1987;45:393-397.
- Kuhl DE, Minoshima S, Fessler JA, et al. In vivo mapping of cholinergic terminals in normal aging, Alzheimer’s disease, and Parkinson’s disease.Ann Neurol. 1996;40:399-410.

- Perry E, Walker M, Grace J, Perry R. Acetylcholine in mind: a neurotransmitter correlate of consciousness? Trends Neurosci.1999;22:273-280.
- Connolly BS, Lang AE. Pharmacological treatment of Parkinson disease: a review.
- Harding AJ, Broe GA, Halliday GM. Visual hallucinations in Lewy body disease relate to Lewy bodies in the temporal lobe. Brain. 2002;125:391-403.
- Williams DR, Lees AJ. Visual hallucinations in the diagnosis of idiopathic Parkinson’s disease: a retrospective autopsy study. Lancet Neurol. 2005;4:605-610.
- Wint DP, Okun MS, Fernandez HH. Psychosis in Parkinson’s disease. J Geriatr Psychiatry Neurol. 2004;17:127-136.
- Goetz CG, Pappert EJ, Blasucci LM, et al. Intravenous levodopa in hallucinating Parkinson’s disease patients: high-dose challenge does not precipitate hallucinations. Neurology. 1998;50:515-517.
- Henderson MJ, Mellers JDC. Psychosis in Parkinson’s disease: between a rock and a hard place. Int Rev Psychiatry.
 2000;12:319-334.
2000;12:319-334. - Fernandez HH, Friedman JH. The role of atypical antipsychotics in the treatment of movement disorders. CNS Drugs. 1999;11:467-483.
- Schneider LS, Dagerman KS, Insel P. Risk of death with atypical antipsychotic drug treatment for dementia: meta-analysis of randomized placebo-controlled trials.
- Goetz CG, Leurgans S, Pappert EJ, Raman R, Stemer AB. Prospective longitudinal assessment of hallucinations in Parkinson’s disease. Neurology.2001;57:2078-2082.
- Miyasaki JM, Shannon K, Voon V, et al; Quality Standards Subcommittee of the American Academy of Neurology. Practice parameter: evaluation and treatment of depression, psychosis, and dementia in Parkinson disease (an-evidence based review): report of the Quality Standards Subcommittee of the American Academy of Neurology.
- Weintraub D, Chen P, Ignacio RV, Mamikonyan E, Kales HC. Patterns and trends in antipsychotic prescribing for Parkinson disease psychosis. Arch Neurol. 2011;68:899-904.

- Frieling H, Hillemacher T, Ziegenbein M, Neund?rfer B, Bleich S. Treating dopamimetic psychosis in Parkinson’s disease: structured review and meta-analysis. Eur Neuropsychopharmacol. 2007;17:165-171.
- Clozapine in drug-induced psychosis in Parkinson’s disease. The French Clozapine Parkinson Study Group.
- Low-dose clozapine for the treatment of drug-induced psychosis in Parkinson’s disease. The Parkinson Study Group. N Engl J Med. 1999;340:757-763.
- Friedman JH, Factor SA. Atypical antipsychotics in the treatment of drug-induced psychosis in Parkinson’s disease. Mov Disord. 2000;151:201-211.
- Fernandez HH, Donnelly EM, Friedman JH. Long-term outcome of clozapine use for psychosis in parkinsonian patients. Mov Disord. 2004;19:831-833.
- Klein C, Gordon J, Pollak L, Rabey JM. Clozapine in Parkinson’s disease psychosis: 5-year follow-up review. Clin Neuropharmacol. 2003;26:8-11.
- Honigfeld G, Arellano F, Sethi J, Bianchini A, Schein J.
 Reducing clozapine-related morbidity and mortality: 5 years of experience with the Clozaril National Registry. J Clin Psychiatry. 1998;59:3-7.
Reducing clozapine-related morbidity and mortality: 5 years of experience with the Clozaril National Registry. J Clin Psychiatry. 1998;59:3-7. - Pollak P, Tison F, Rascol O, et al. Clozapine in drug induced psychosis in Parkinson’s disease: a randomised, placebo controlled study with open follow up. J Neurol Neurosurg Psychiatry. 2004;75:689-695.
- Holt RI, Peveler RC, Byrne CD. Schizophrenia, the metabolic syndrome and diabetes. Diabet Med. 2004;21:515-523. 15154933″>
- Reddy S, Factor SA, Molho ES, Feustel PJ. The effect of quetiapine on psychosis and motor function in parkinsonian patients with and without dementia. Mov Disord. 2002;17;676-681.
- Fernandez HH, Trieschmann ME, Burke MA, Jacques C, Friedman JH. Long-term outcome of quetiapine use for psychosis among Parkinsonian patients. Mov Disord. 2003;18:510-514.
- Ondo WG, Tintner R, Voung KD, Lai D, Ringholz G. Double-blind, placebo-controlled, unforced titration parallel trial of quetiapine for dopaminergic-induced hallucinations in Parkinson’s disease.
 Mov Disord. 2005;20:958-963.
Mov Disord. 2005;20:958-963. - Rabey JM, Prokhorov T, Miniovich A, et al. The effect of quetiapine in Parkinson’s disease (PD) psychotic patients: A double-blind labeled study of 3 months’ duration. Mov Disord. 2005;20:S46.
- Fernandez HH, Okun MS, Rodriguez RL, et al. Quetiapine improves visual hallucinations in Parkinson disease but not through normalization of sleep architecture: results from a double-blind clinical-polysomnography study. Int J Neurosci. 2009;119:2196-2205.
- Morgante L, Epifanio A, Spina E, et al. Quetiapine and clozapine in parkinsonian patients with dopaminergic psychosis. Clin Neuropharmacol. 2004; 27:153-156.
- Klein C, Prokhorov T, Miniovich A, Dobronevsky E, Rabey JM. Long-term follow-up (24 months) of quetiapine treatment in drug-induced Parkinson disease psychosis. Clin Neuropharmacol. 2006;29:215-219.
- Juri C, Chana P, Tapia J, Kuntsmann C, Parrao T. Quetiapine for insomnia in Parkinson disease: results from an open-label trial.
 Clin Neuropharmacol. 2005;28:185-187.
Clin Neuropharmacol. 2005;28:185-187. - Abbas A, Roth BL. Pimavanserin tartrate: a 5-HT2A inverse agonist with potential for treating various neuropsychiatric disorders. Expert Opin Pharmatother. 2008;9:3251-3259.
- Cummings J, Isaacson S, Mills R, et al. Pimavanserin for patients with Parkinson’s disease psychosis: a randomised placebo-controlled phase 3 trial. Lancet. 2014;383:533-540.
- McGavin JK, Goa KL. Aripiprazole. CNS Drugs. 2002;16:779-786. 12383035″>
- Fernandez HH, Trieschmann ME, Friedman JH. Aripiprazole for drug-induced psychosis in Parkinson disease: preliminary experience. Clin Neuropharmacol. 2004;27:4-5.
- Friedman JH, Berman RM, Goetz CG, et al. Open-label flexible-dose pilot study to evaluate the safety and tolerability of aripiprazole in patients with psychosis associated with Parkinson’s disease. Mov Disord. 2006;21:2078-2081.
- Friedman JH. Melperone is ineffective in treating Parkinson’s disease psychosis. Mov Disord.
 2012;27:803-804.
2012;27:803-804. - Moore NA, Tye NC, Axton MS, Risius FC. The behavioral pharmacology of olanzapine, a novel «atypical» antipsychotic agent. J Pharmacol Exp Ther. 1992;262:545-551.
- Goetz CG, Blasucci LM, Leurgans S, Pappert EJ. Olanzapine and clozapine: comparative effects on motor function in hallucinating PD patients.
- Breier A, Sutton VK, Feldman PD, et al. Olanzapine in the treatment of dopamimetic-induced psychosis in patients with Parkinson’s disease. Biol Psychiatry. 2002;52:438-445.
- Ondo WG, Levy JK, Vuong KD, Hunter C, Jankovic J. Olanzapine treatment for dopaminergic-induced hallucinations. Mov Disord. 2002;17:1031-1035.
- Eichhorn TE, Brunt E, Oertel WH. Ondansetron treatment of L-dopa-induced psychosis.
- Grant S, Fiton A. Risperidone. A review of its pharmacology and therapeutic potential in the treatment of schizophrenia.
- Rosebush PI, Mazurek MF. Neurologic side effects in neuroleptic-naive patients treated with haloperidol or risperidone.

- Rustembegovic A, Sofic E, Wichart I. Serum prolactin, leptin, lipids and lipoprotein levels during antipsychotic treatment in Parkinson’s disease and related psychosis. Med Arh. 2006;60:211-212.
- Factor SA, Molho ES, Friedman JH. Risperidone and Parkinson’s disease. Mov Disord. 2002;17:221-222.
- Ellis T, Cudkowicz ME, Sexton PM, Growdon JH. Clozapine and risperidone treatment of psychosis in Parkinson’s disease. J Neuropsychiatry Clin Neurosci. 2000;12:364-369.
- Stahl SM, Shayegan DK. The psychopharmacology of ziprasidone: receptor-binding properties and real-world psychiatric practice. J Clin Psychiatry. 2003;64:6-12.
- Glassman AH. Schizophrenia, antipsychotic drugs, and cardiovascular disease. J Clin Psychiatry. 2005;66:5-10.
- G?mez-Esteban JC, Zarranz JJ, Velasco F, et al. Use of ziprasidone in parkinsonian patients with psychosis. Clin Neuropharmacol. 2005;28:111-114.
- Oechsner M, Korchounov A. Parenteral ziprasidone: a new atypical neuroleptic for emergency treatment of psychosis in Parkinson’s disease? Hum Psychopharmacol.
 2005;20:203-205.
2005;20:203-205. - Weiden PJ, Iqbal N, Mendelowitz AJ, Tandon R, Zimbroff DL, Ross R. Best clinical practice with ziprasidone: update after one year of experience. J Psychiatr Pract. 2002;8:81-97.
- Ravina B, Putt M, Siderowf A, et al. Donepezil for dementia in Parkinson’s disease: a randomised, double blind, placebo controlled, crossover study. J Neurol Neurosurg Psychiatry. 2005;76:934-939.
- Aarsland D, Laake K, Larsen JP, Janvin C. Donepezil for cognitive impairment in Parkinson’s disease: a randomized controlled study. J Neurol Neurosurg Psychiatry. 2002;72:708-712.
- Aarsland D, Hutchinson M, Larsen JP. Cognitive, psychiatric and motor response to galantamine in Parkinson’s disease with dementia. Int J Geriatr Psychiatry. 2003;18:937-941.
- Burn D, Emre M, McKeith I, et al. Effects of rivastigmine in patients with and without visual hallucinations in dementia associated with Parkinson’s disease. Mov Disord. 2006;21:1899-1907.
- Hutchinson M, Fazzini E.
 Cholinesterase inhibition in Parkinson’s disease. J Neurol Neurosurg Psychiatry. 1996;61:324-325.
Cholinesterase inhibition in Parkinson’s disease. J Neurol Neurosurg Psychiatry. 1996;61:324-325. - Ott BR, Lannon MC. Exacerbation of parkinsonism by tacrine. Clin Neuropharmacol. 1992;15:322-325.
- Normann C, Hesslinger B, Frauenknecht S, Berger M, Walden J. Psychosis during chronic levodopa therapy triggered by the new antidepressive drug mirtazapine.
- Meco G, Bernardi S. Antidepressant use in treatment of psychosis with comorbid depression in Parkinson’s disease. Prof Neuropsychopharmacol Biol Psychiatry. 2007;31:311-313.
- Voon V, Lang AE. Antidepressants in the treatment of psychosis with comorbid depression in Parkinson disease. Clin Neuropharmacol. 2004;27:90-92.
- Ozer F, Meral H, Aydin B, Hanoglu L, Aydemir T, Oral T. Electroconvulsive therapy in drug-induced psychiatric states and neuroleptic malignant syndrome. J ECT. 2005;21:125-127.
- Sleeper RB. Antipsychotic dose-sparing effect with addition of memantine. Ann Pharmacother. 2005;39:1573-1576.

- Ridha BH, Josephs KA, Roosor MN. Delusions and hallucinations in dementia with Lewy bodies: worsening with memantine.
- Diederich NJ, Pieri V, Goetz CG. Coping strategies for visual hallucinations in Parkinson’s disease. Mov Disord. 2003;18:831-832.
- McGorry PD. Psychoeducation in first-episode psychosis: a therapeutic process. Psychiatry. 1995;58:313-328.
- Tarrier N, Wykes T. Is there evidence that cognitive behaviour therapy is an effective treatment for schizophrenia? A cautious or cautionary tale? Behav Res Ther. 2004;42:1377-1401.
- Jenner JA, van de Willige G, Wiersma D. Effectiveness of cognitive therapy with coping training for persistent auditory hallucinations: a retrospective study of atttenders of a psychiatric out-patient department. Acta Psychiatr Scand. 1998;98:384-389.
Источник: http://www .medscape.org/
Все материалы на сайте представлены в ознакомительном порядке, одобрены дипломированным врачом, Васильевым Михаилом, диплом серия 064834, согласно лицензии № ЛО-77-005297 от 17 сентября 2012 г. , сертифицированным специалистом в сфере психиатрия номер сертификата 0177241425770.
, сертифицированным специалистом в сфере психиатрия номер сертификата 0177241425770.
В любых ситуациях связанных с расстройством психики необходимо обращаться к специалисту .
Вирусы могут стать пусковым механизмом многих заболеваний — Российская газета
Впервые в истории столько людей оказались в самоизоляции. И многие, как выяснилось, совершенно не готовы к такому повороту. Скандалы, психозы… Как справиться со стрессом в четырех стенах? Как уберечь себя и своих близких от нервных срывов? Об этом обозреватель «РГ» беседует с главным психиатром Москвы доктором медицинских наук, профессором Георгием Костюком.
Георгий Петрович, существует ли рост психических заболеваний во время пандемии и самоизоляции?
Георгий Костюк: Да, такое происходит впервые… И нам только предстоит узнать, какие психологические последствия таит в себе это явление. Сведения, которые мы имеем сейчас, указывают на обострение проблем, которые уже существуют у человека в семье. Например, увеличение случаев домашнего насилия.
Сведения, которые мы имеем сейчас, указывают на обострение проблем, которые уже существуют у человека в семье. Например, увеличение случаев домашнего насилия.
А если говорить о последствиях пандемии, то мы пока не можем точно сказать, какими они будут для пандемии коронавируса, зато можем вспомнить историю. Мы пережили пандемии свиного, птичьего гриппа, атипичной пневмонии, которые были совсем недавно, 10-20 лет назад. Россию эти пандемии не коснулись так сильно, как некоторые другие страны. Тем не менее мы можем узнать результаты исследований, проведенных в странах, где пандемия была. Сейчас часто вспоминают эпидемию испанки, случившуюся ровно 100 лет назад.
Существуют научные публикации, в которых проводится анализ влияния пандемии на психическое здоровье. Исследования рассматривают три аспекта: непосредственные психологические реакции во время пандемии, психические расстройства у заболевших вирусной инфекцией и отсроченные последствия для нервной системы и психики.
Если говорить про первый аспект, про психологические реакции, то можно привести в пример исследование, проводившееся во время эпидемии свиного гриппа среди жителей Великобритании. Опрос показал, что примерно у 40 процентов людей значительно изменился образ жизни. Формально они соблюдали все рекомендации специалистов: реже выходили из дома, чаще мыли руки, дезинфицировали поверхности. Однако при этом они испытывали высокий уровень тревоги. А часть из них обычные простудные симптомы воспринимала как проявления свиного гриппа.
Опрос показал, что примерно у 40 процентов людей значительно изменился образ жизни. Формально они соблюдали все рекомендации специалистов: реже выходили из дома, чаще мыли руки, дезинфицировали поверхности. Однако при этом они испытывали высокий уровень тревоги. А часть из них обычные простудные симптомы воспринимала как проявления свиного гриппа.
Если говорить про более серьезные нарушения психики, то можно вспомнить американского психиатра Карла Меннингера, который сделал интересное наблюдение во время эпидемии испанки столетие назад.
Георгий Костюк: Да. В клинику, где он работал, стало поступать большое количество пациентов с гриппом, который сопровождался психотическими симптомами. При этом симптомы психоза улетучивались, как только пациенты выздоравливали от гриппа.
С точки зрения долгосрочных последствий рассматривается влияние вирусных инфекций на возникновение тяжелых психических расстройств. Таких как шизофрения, деменция, умственная отсталость. Было замечено, что дети, которые родились в зимние месяцы, то есть месяцы всплесков сезонных заболеваний, чаще страдают шизофренией. Также есть риски и во время беременности: если женщина перенесла во время беременности вирусное заболевание, то у родившегося ребенка возрастает риск развития нарушений нервной системы.
Было замечено, что дети, которые родились в зимние месяцы, то есть месяцы всплесков сезонных заболеваний, чаще страдают шизофренией. Также есть риски и во время беременности: если женщина перенесла во время беременности вирусное заболевание, то у родившегося ребенка возрастает риск развития нарушений нервной системы.
У пожилых людей на фоне вирусной инфекции может возрасти риск делирия, болезни Паркинсона и болезни Альцгеймера. При этом невозможно четко прогнозировать, что у того или иного человека совместно с вирусной инфекцией могут произойти некоторые изменения в психике. Тем не менее вирусы могут выступить пусковым механизмом не только психических заболеваний, но и соматических. Нельзя забывать и об уязвимости каждой личности и генетической предрасположенности к развитию изменений в психике.
Сегодня мы знаем, что влияние вирусов на нервную систему и психику возможно, но прямых корреляций мы не находим. Скорее всего, как и при любых сложных явлениях, есть совокупность факторов: генетическая предрасположенность, уязвимость организма и влияние внешних обстоятельств.
Самоизоляция чревата отдаленными последствиями?
Георгий Костюк: Пока мы не можем дать четкого ответа на вопрос о том, будет ли самоизоляция иметь долгосрочные последствия для каждого из нас. Естественно, все зависит от условий и обстоятельств, в которых изолируется человек. Одна история, если это осознанный выбор человека, у которого есть постоянный заработок, хорошее жилье, благополучные семейные отношения. Если никто из его близких не пострадал от вируса, если есть интересы, которые позволяют не скучать во время изоляции. Совсем другая история, если хотя бы часть жизненных обстоятельств из этого перечня не такая благополучная. Но даже и в этом случае многое будет зависеть от исходных психических особенностей человека, от его адаптивности. Ведь известно, что даже при самых страшных обстоятельствах, во время катастроф, войн далеко не все люди начинают страдать психическими расстройствами.
Как перенести изоляцию людям, живущим в стесненных условиях? Людям с детьми, которым сложно объяснить, что нельзя выходить на улицу?
Георгий Костюк: Действительно, для многих это может стать проблемой. Но нельзя сказать, что эта проблема будет совсем новой, скорее, она будет обостренной. В случае с детьми все изначально зависит от того, как раньше родители выстраивали с ними свои отношения. Если отношения понимающие, любящие, если родителям интересно проводить время с детьми, то вряд ли совместная изоляция будет мучением. Дети же легко превращают необычные жизненные обстоятельства в игру. У них развито воображение, поэтому можно и нужно использовать эти свойства детской психики для преодоления стресса от изоляции. Больше играть, общаться, вместе узнавать что-то новое. Вместе делать зарядку. Нужно разрешать детям иногда побеситься, выплеснуть свою энергию. Общение с родителями чаще всего основная детская потребность. Гораздо большая, чем потребность в прогулках. Если это обеспечить, то вряд ли ребенок будет сильно скучать по улице.
Но нельзя сказать, что эта проблема будет совсем новой, скорее, она будет обостренной. В случае с детьми все изначально зависит от того, как раньше родители выстраивали с ними свои отношения. Если отношения понимающие, любящие, если родителям интересно проводить время с детьми, то вряд ли совместная изоляция будет мучением. Дети же легко превращают необычные жизненные обстоятельства в игру. У них развито воображение, поэтому можно и нужно использовать эти свойства детской психики для преодоления стресса от изоляции. Больше играть, общаться, вместе узнавать что-то новое. Вместе делать зарядку. Нужно разрешать детям иногда побеситься, выплеснуть свою энергию. Общение с родителями чаще всего основная детская потребность. Гораздо большая, чем потребность в прогулках. Если это обеспечить, то вряд ли ребенок будет сильно скучать по улице.
Как правило, в условиях самоизоляции обостряются те проблемы, которые уже существуют у человека в семье
Готова ли наша психиатрическая служба к оказанию помощи в сложившихся условиях?
Георгий Костюк: Медицинские заведения сейчас в срочном порядке перепрофилируются для борьбы с коронавирусом. И психиатрические больницы будут готовы представить свои ресурсы в случае необходимости.
И психиатрические больницы будут готовы представить свои ресурсы в случае необходимости.
В данный момент работа психиатрической службы направлена на оказание максимально возможной психолого-психотерапевтической поддержки. На базе московских психиатрических больниц имени Алексеева, имени Ганнушкина работают службы телефонной психологической помощи населению Москвы. В больнице Алексеева в специально оборудованном помещении с соблюдением всех предписанных мер, направленных на предотвращение распространения нового вируса, организована видеосвязь пациентов с их родственниками. И значит, несмотря на карантин, близкие люди могут увидеться и поговорить друг с другом. В формате видеосвязи проходят и беседы родственников пациентов с лечащими врачами.
Больницы работают в обычном режиме и оказывает помощь пациентам, работают выездные бригады и помощь на дому. Служба готова гибко реагировать на потребности населения.
Психические заболевания не заразны. Они не инфекция. Но в целом они гораздо опаснее. Или?..
Или?..
Георгий Костюк: Психические заболевания чаще всего связаны с качеством жизни и тем, как человек функционирует в обществе, нежели с непосредственной угрозой для жизни. Но косвенные последствия могут быть очень серьезными: с этими расстройствами человек может потерять возможность нормально работать, самостоятельно жить, получать удовольствие от жизни. Да, есть те недуги, которые связаны с вопросами жизни и смерти — суицидальное поведение, расстройства пищевого поведения, психомоторное возбуждение и другие. Психические расстройства являются большим бременем для общества. Они приводят к косвенным долгосрочным последствиям. И особенности этих последствий отличаются от инфекционных заболеваний. Неслучайно ВОЗ считает последствия инфекционных и неинфекционных заболеваний отдельно. Если выделить долю психических заболеваний среди неинфекционных заболеваний, они стабильно оказываются в первой десятке.
В целом люди с психическими расстройствами представляют намного меньшую угрозу для общества, чем люди без очевидных признаков таких расстройств.
Нужно разрешать детям иногда побеситься, выплеснуть свою энергию. Общение с родителями чаще всего основная детская потребность
Возможно, вопрос покажется не уместным, но спрошу: положительные стороны у нынешней ситуации имеются?
Георгий Костюк: Большинство из нас сейчас сфокусированы на опасностях ситуации с коронавирусом и общим негативом. Но есть и позитивные моменты. Мы можем почувствовать важность человеческой жизни, реальность взаимопомощи и поддержки, мы сможем пересмотреть систему своих ценностей.
Для медиков хорошая сторона этой ситуации в том, что сейчас вместо привычных теоретических разговоров о важности медицинской сферы происходит реальное выдвижение медицины и науки на первый план. Медицинские работники воспринимаются как герои, они срывают каждый день аплодисменты во многих странах мира. Вряд ли когда-то раньше они удостаивались таких оваций! А те, кто получает сейчас медицинскую помощь, могут убедиться в том, что медработники готовы выйти из дома, чтобы выполнять свою работу.
Для культуры уникальный момент в том, что музеи, театры, кинотеатры, книжные магазины открывают бесплатный виртуальный доступ к своим сокровищам. Университеты открывают доступ к своим образовательным ресурсам. Могли ли мы подумать, что маститые специалисты будут вести виртуальные уроки для школьников?
Привычный образ жизни с постоянной суетой, избыточным потреблением, развлечениями сейчас для многих невозможен. А что остается, если это убрать из нашей жизни? И так ли велика для нас эта потеря? То, что сейчас происходит, для многих является экзистенциальным кризисом, но именно периоды кризиса дают человеку возможность что-то переосмыслить и что-то изменить в своей жизни.
Лечение и профилактика болезни Паркинсона — Жизнь
Понимание симптомов Причина Диагноз Лечение До сих пор болезнь Паркинсона полностью не излечена. Однако существует несколько методов лечения, которые могут помочь облегчить симптомы и улучшить качест
Содержание
болезнь Паркинсона
Понимание симптомов Причина Диагноз ЛечениеЛечение и профилактика болезни Паркинсона
До сих пор болезнь Паркинсона полностью не излечена.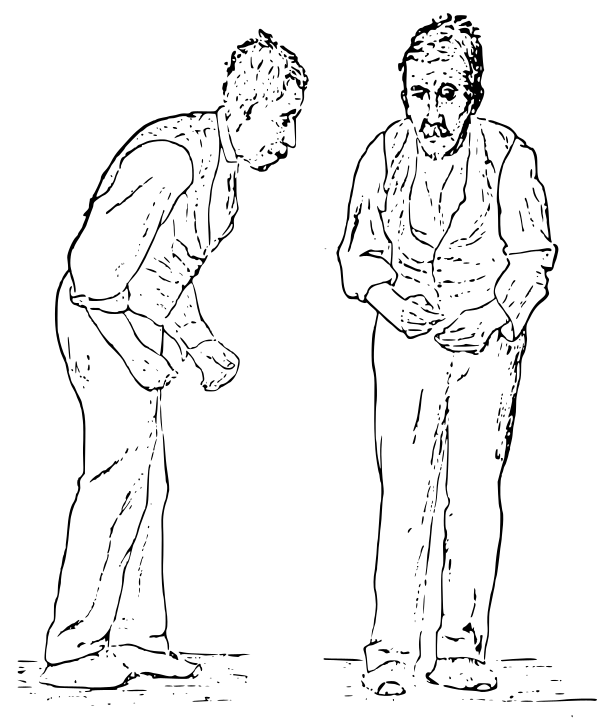 Однако существует несколько методов лечения, которые могут помочь облегчить симптомы и улучшить качество жизни пациента, а именно:
Однако существует несколько методов лечения, которые могут помочь облегчить симптомы и улучшить качество жизни пациента, а именно:
Терапия поддерживающий
Ниже приведены некоторые из рекомендуемых поддерживающих методов лечения симптомов у пациентов с болезнью Паркинсона:
- Физиотерапия. Физиотерапия направлена на то, чтобы помочь пациентам справиться с ригидностью мышц и болями в суставах, чтобы улучшить подвижность и гибкость. Физиотерапия также направлена на повышение выносливости пациента и его способность двигаться независимо от других.
- Изменение меню еды. Одним из симптомов болезни Паркинсона является запор или запор. Это состояние можно преодолеть, выпив много воды и употребляя продукты с высоким содержанием клетчатки. Врачи также могут порекомендовать увеличить потребление соли с пищей, если у пациента пониженное давление, особенно когда он стоит.
- Логопедия.
 Люди с болезнью Паркинсона, как правило, плохо говорят, поэтому логопед необходим для улучшения речи.
Люди с болезнью Паркинсона, как правило, плохо говорят, поэтому логопед необходим для улучшения речи.
Наркотики
Врачи могут назначить несколько видов лекарств, чтобы помочь пациентам справиться с симптомами, которые они испытывают. Приведенные ниже препараты увеличивают или заменяют дофамин в организме:
- Антихолинергические средства. Антихолинергические препараты помогают при треморе. Одним из антихолинергических препаратов, которые можно использовать, является тригексифенидил.
- Леводопа. Этот препарат абсорбируется нервными клетками мозга и превращается в дофамин.. Повышенные уровни дофамин поможет преодолеть двигательные нарушения. LEvodopa может сочетаться с карбидопа, для предотвращения образования дофамина за пределами мозга.
- Агонисты дофамина. Этот препарат действует так же, как леводопа, но не производит дофамин, а только заменяет функцию дофамин в мозгу.
 Агонисты дофамина используется на ранних стадиях болезни Паркинсона, потому что побочные эффекты не такие сильные леводопа. Примеры препаратов-агонистов дофамина: прамипексол, ротиготин, а также ропинироль.
Агонисты дофамина используется на ранних стадиях болезни Паркинсона, потому что побочные эффекты не такие сильные леводопа. Примеры препаратов-агонистов дофамина: прамипексол, ротиготин, а также ропинироль. - Энтакапон. Энтакапон назначают только пациентам с запущенной болезнью Паркинсона. Этот препарат является дополнительным леводопа продлить действие леводопа.
Хирургическая процедура
Пациенты с болезнью Паркинсона обычно лечатся только лекарствами. Тем не менее, хирургические процедуры иногда выполняются пациентам, страдающим болезнью Паркинсона в течение длительного времени. Вот некоторые из возможных процедур:
- Глубокая стимуляция мозга (DBS)
В методе глубокой стимуляции мозга или глубокий мозг sTimulation (DBS), Врач имплантирует электроды в пораженный участок мозга. Эти электроды подключены к имплантированному в грудную клетку генератору, который посылает электрический ток в мозг. DBS рекомендуется пациентам, которые плохо реагируют на лекарства. DBS может уменьшить или остановить дискинезию, уменьшить тремор и ригидность, а также улучшить подвижность.
DBS рекомендуется пациентам, которые плохо реагируют на лекарства. DBS может уменьшить или остановить дискинезию, уменьшить тремор и ригидность, а также улучшить подвижность.
- Операцияпвздох граммамма (граммамма kниф)
У пациентов, которые не могут пройти процедуру DBS, операция гамма-нож может быть вариантом. Эта процедура выполняется в течение 15-40 минут путем фокусировки сильного луча излучения на пораженном участке мозга.
Пока неизвестно, можно ли предотвратить болезнь Паркинсона. Однако считается, что регулярные упражнения и употребление продуктов, богатых антиоксидантами, снижают риск развития этого заболевания. Ряд исследований также показал, что болезнь Паркинсона редко поражает тех, кто регулярно употребляет напитки с кофеином, такие как кофе и чай.
Нарциссизм оказался значительным фактором риска агрессивного и насильственного поведения
Кадр из мультфильма «Сказка о мертвой царевне и о семи богатырях»
Нарциссизм, даже умеренный, значительно связан с агрессивностью, установили американские ученые. Метаанализ 437 независимых исследований показал, что люди с нарциссическими расстройствами личности склонны ко всем видам агрессии, включая физическую, словесную, травлю, троллинг и преследование в интернете. Результаты были одинаковыми независимо от пола, возраста, уровня образования или страны проживания исследуемых. Связь нарциссизма и агрессии усиливалась при провокации, но оставалась значительной и при ее отсутствии. Работа опубликована в журнале Psychological Bulletin.
Нарциссическое расстройство психики — это психическое отклонение, при котором человек чувствует себя уникальным, убежден в своем превосходстве над другими и ожидает безусловного восхищения от окружающих. Нарциссические личности считают себя выше правил, склонны обесценивать все, что не ассоциируют с собой, лишены эмпатии. Люди с нарциссическими чертами личности склонны, например, одобрять социальное неравенство. Ученые предполагают, что нарциссизм имеет как нормальные, так и патологические проявления. Субклинический нарциссизм, характеризующийся такими чертами личности, как, например, ощущение собственной грандиозности, права власти и успеха, считается умеренным. Патологическое нарциссическое расстройство сопровождается клинически значимыми проблемами психического здоровья, такими как депрессия, суицидальные мысли, причинение себе вреда, агрессивность и склонность к насилию.
Нарциссические личности считают себя выше правил, склонны обесценивать все, что не ассоциируют с собой, лишены эмпатии. Люди с нарциссическими чертами личности склонны, например, одобрять социальное неравенство. Ученые предполагают, что нарциссизм имеет как нормальные, так и патологические проявления. Субклинический нарциссизм, характеризующийся такими чертами личности, как, например, ощущение собственной грандиозности, права власти и успеха, считается умеренным. Патологическое нарциссическое расстройство сопровождается клинически значимыми проблемами психического здоровья, такими как депрессия, суицидальные мысли, причинение себе вреда, агрессивность и склонность к насилию.
Существует большое количество исследований, изучающих связь между нарциссизмом и агрессией (например, 1, 2, 3). Люди с нарциссическим расстройством, ожидающие безусловного восхищения, могут быть чрезмерно чувствительны к критике в свой адрес и реагировать на нее с гневом. Люди с патологическим уровнем нарциссизма имеют значительные регуляторные дефициты и дезадаптивные стратегии, чтобы справиться с угрозами собственному образу. Таким образом, люди с патологическим нарциссизмом могут быть особенно склонны нападать на других в агрессивной манере, когда им угрожают.
Таким образом, люди с патологическим нарциссизмом могут быть особенно склонны нападать на других в агрессивной манере, когда им угрожают.
14 знаменитостей с нездоровой психикой — в нашей галерее:
Софи Кьервик (Sophie L. Kjærvik) и Брэд Бушман (Brad J. Bushman) из государственного университета Огайо исследовали в метааналитическом обзоре связь между нормальным и патологическими уровнями нарциссизма и агрессией, и рассмотрели возможную переменную модератора — провокацию. Анализ включил 437 независимых исследования, в том числе 77 не опубликованных, с участием 123 043 человек. Исследования проводились с 1985 по 2020 годы. Средний возраст участников колебался от 8,3 до 61,7 года.
Для поиска соответствующих исследований, опубликованных до 15 ноября 2020 года, ученые использовали пять компьютерных баз данных: Medline, PsycINFO, Информационный центр образовательных ресурсов (ERIC), PubMed и Pro-Quest. Использовались четыре критерия включения: исследование должно было включать определенную степень нарциссизма, изучить нарциссизм на индивидуальном уровне, а не на групповом или коллективном, включать меру агрессии или насилия и не включать участников младше семи лет.
Результаты показали, что нарциссизм является важным фактором риска агрессии и насилия.
Нарциссические расстройства оказались связаны как с агрессией (r = 0,26, [0,24, 0,28]), так и с насилием (r = 0,23, [0,18, 0,27]). Как и ожидалось, связь нарциссизма и агрессии была сильнее в условиях провокации (r = 0,29, [0,23, 0,36]), чем в условиях ее отсутствия (r = 0,12, [0,05, 0,18]), но была значительной и при отсутствии провокации. И «нормальный», и «патологический» нарциссизм были связаны со всеми формами агрессии (косвенной, прямой, вытесненной, физической, вербальной, издевательской). Связь между нарциссизмом и агрессией оказалась одинаково значимой для мужчин и женщин, для людей всех возрастов, уровня образования и страны проживания.
Помимо прочего, люди с нарциссическими расстройствами не умеют учиться на своих ошибках. Неспособность понять, что они что-то делают не так, приводит к тому, что нарциссы не могут оценить альтернативные исходы произошедших событий и сделать выводы.
Читайте также: У мужской скупости нашлось биологическое объяснение
Смотрите наши видео:
Во время загрузки произошла ошибка.Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Советы по уходу за психозом Паркинсона
Если вы ухаживаете за любимым человеком, страдающим болезнью Паркинсона, вам, возможно, придется управлять не только физическими симптомами этого заболевания. Многие люди с болезнью Паркинсона также испытывают психоз, включая галлюцинации и бред — и для тех, кто ухаживает за ними, эти психические симптомы могут быть самой сложной проблемой из всех. Вот несколько стратегий, которые помогут вам и вашему близкому справиться с этими эпизодами.
Поговорим об этом. Некоторые люди не осознают, что психоз связан с болезнью Паркинсона, и в результате страдают в тишине и страхе.Вероника Сантини, доктор медицины, невролог и специалист по двигательным расстройствам из Стэнфордского университета в Пало-Альто, Калифорния, предлагает вам подумать о том, чтобы поднять эту тему самостоятельно, сказав: «Многие пациенты с болезнью Паркинсона видят то, чего нет. С тобой такое когда-нибудь случалось? » Для вашего любимого человека может быть облегчением узнать, что галлюцинации не только нормальны для болезни Паркинсона, но и довольно распространены.
С тобой такое когда-нибудь случалось? » Для вашего любимого человека может быть облегчением узнать, что галлюцинации не только нормальны для болезни Паркинсона, но и довольно распространены.
Сохраняйте спокойствие. Вежливое и приятное поведение поможет расслабиться и вам, и вашему близкому.Во время психотического эпизода также может помочь выключение телевидения или радио; окружающий шум обычно добавляет путаницы.
Попробуйте прикоснуться к галлюцинации. Даже если человек, переживающий это, осознает, что зрительная галлюцинация нереальна, это все равно огорчает: «Что-то такое простое, как протянуть руку [прикоснуться], и она может исчезнуть», — говорит доктор Сантини. «Это помогает людям понять, что это нереально».
Избегайте аргументов. Вместо того, чтобы пытаться исправить или урезонить своего любимого человека, попробуйте прислушаться, — говорит Лори Пуассон, RN, которая помогает клиентам перейти от медицинского обслуживания в учреждении к уходу на дому для компании Right at Home из Бостона. «Позвольте им выразить свои чувства и попытайтесь перенаправить их, если они испытывают что-то негативное, — говорит она. Попытки урезонить человека, страдающего психозом, связанным с болезнью Паркинсона, с большей вероятностью ухудшат ситуацию.
«Позвольте им выразить свои чувства и попытайтесь перенаправить их, если они испытывают что-то негативное, — говорит она. Попытки урезонить человека, страдающего психозом, связанным с болезнью Паркинсона, с большей вероятностью ухудшат ситуацию.
Сосредоточьтесь на том, что вы можете сделать . Возможно, вам не удастся избавиться от галлюцинаций, но вы можете сделать домашнюю обстановку более успокаивающей. Например, если у кого-то галлюцинация, говорит Сантини, сделайте так, чтобы человеку было легче видеть, включив все огни.
Подыгрывайте. Уход за галлюцинациями может быть более полезным, чем попытки убедить любимого человека в том, что они ненастоящие, — говорит Пуассон. Один пример: если кого-то беспокоит галлюцинация детей, играющих во дворе, просто переместите этого человека в другую комнату.
Позаботьтесь о своей безопасности. «Сиделки бесполезны для членов своей семьи или друзей, если они сами травмированы», — говорит Сантини. Не будь героем. Если вам нужно поднять или перевезти любимого человека, вы должны сделать это правильно, .Подумайте о том, чтобы запросить оценку домашней безопасности у эрготерапевта.
Не будь героем. Если вам нужно поднять или перевезти любимого человека, вы должны сделать это правильно, .Подумайте о том, чтобы запросить оценку домашней безопасности у эрготерапевта.
Не ждите, чтобы попросить о помощи. Ожидание обращения за помощью до тех пор, пока вы не рискуете потерять терпение, только усложнит вам управление психотическим поведением. Попробуйте вести список вещей, которые вы легко можете передать кому-то другому. Например, позвольте кому-то купить рецепт, приготовить ужин или провести время с любимым человеком, пока вы делаете перерыв.
Помните, что вы не одиноки. Группа поддержки онлайн или при личной встрече может снять накопившийся стресс. Это дает возможность делиться историями, обмениваться советами и получать поддержку от людей с похожим опытом.
Как справиться с психозом, связанным с болезнью Паркинсона
Если вы страдаете болезнью Паркинсона и испытываете симптомы психоза, вы не одиноки. Около 60 процентов людей с болезнью Паркинсона разовьются симптомы психоза, такие как галлюцинации и бред, показывает долгосрочное исследование, опубликованное в 2010 году в журнале JAMA Neurology .Некоторых людей эти симптомы не беспокоят, но другие считают их беспокоящими.
Около 60 процентов людей с болезнью Паркинсона разовьются симптомы психоза, такие как галлюцинации и бред, показывает долгосрочное исследование, опубликованное в 2010 году в журнале JAMA Neurology .Некоторых людей эти симптомы не беспокоят, но другие считают их беспокоящими.
Галлюцинации действительно являются частью этого состояния, — говорит Мэтью Барретт, доктор медицины, доцент неврологии Университета Вирджинии в Шарлоттсвилле. «Эти симптомы могут усугубляться некоторыми лекарствами, — говорит он, — но если симптомы становятся надоедливыми, есть другие лекарства, которые могут помочь». Поэтому обязательно расскажите врачу о своих симптомах.
Между тем, вот несколько стратегий, которые могут помочь облегчить симптомы психоза, связанного с болезнью Паркинсона.
1. Поговорите со своим врачом о корректировке приема лекарств. Некоторые лекарства могут усугубить психотические симптомы — и в этом случае ваш врач может решить изменить вашу схему лечения. Например, лечение, повышающее уровень дофамина в головном мозге, помогает с двигательными симптомами болезни Паркинсона, но может ухудшить психотическое поведение, — говорит Альберто Дж. Эспай, доктор медицинских наук, профессор неврологии в Университете Цинциннати. По его словам, препараты с антихолинергическим действием, такие как некоторые препараты, контролирующие мочевой пузырь, также могут быть связаны с галлюцинациями или бредом.Ваш врач может также добавить в смесь антипсихотический препарат.
Например, лечение, повышающее уровень дофамина в головном мозге, помогает с двигательными симптомами болезни Паркинсона, но может ухудшить психотическое поведение, — говорит Альберто Дж. Эспай, доктор медицинских наук, профессор неврологии в Университете Цинциннати. По его словам, препараты с антихолинергическим действием, такие как некоторые препараты, контролирующие мочевой пузырь, также могут быть связаны с галлюцинациями или бредом.Ваш врач может также добавить в смесь антипсихотический препарат.
Помните: прекращайте прием лекарств только по указанию врача. Не пытайтесь делать это самостоятельно.
2. Устраните возможные первопричины. Иногда основные проблемы со здоровьем, от острых инфекций до метаболических изменений, могут быть связаны с психозом, говорит доктор Эспей. Когда у людей появляются неожиданные психотические симптомы, Эспей говорит, что иногда он заказывает анализы крови для проверки на наличие инфекций или изменений в функции почек или печени у своих пациентов, которые могут способствовать изменению симптомов.
Темная среда может ассоциироваться с усилением галлюцинаций, говорит доктор Барретт. «Некоторым людям может помочь усиленное освещение», — говорит он. «Тем не менее, это также может иметь негативное влияние на сон, поэтому к этому следует подходить с учетом этого». В конце концов, он говорит, что полноценный сон может помочь вам почувствовать себя лучше. Поговорите со своим врачом о корректировках, которые могут вам помочь.
4. Избегайте триггеров.«Некоторые люди испытывают галлюцинации или бред, связанные с определенным местом», — говорит Барретт.По его словам, хотя это может быть не всегда практично, вам следует избегать обстановки, в которой возникают галлюцинации, где это возможно.
5. Положитесь на свою систему поддержки. Если вам нужна помощь в определении реальности галлюцинаций, спросите своего опекуна, — говорит Барретт. Исследование 2018 года, опубликованное в Международном журнале гериатрической психиатрии , также предполагает, что общение с другими людьми, испытывающими похожие симптомы, может помочь вам справиться с зрительными галлюцинациями, связанными с болезнью Паркинсона.
Знаковое исследование, опубликованное в 2003 году в журнале Movement Disorders , предполагает, что люди с зрительными галлюцинациями при психозе, связанном с болезнью Паркинсона, чаще всего используют когнитивные стратегии совладания, такие как включение света и указание на то, что галлюцинации не настоящие.
Психоз и галлюцинации | Американская ассоциация болезни Паркинсона.
Руководство по пониманию болезни Паркинсона. Психоз Галлюцинации и заблуждения
Что такое психоз при болезни Паркинсона?
Психоз при болезни Паркинсона — это немоторный симптом болезни Паркинсона, который вызывает у пациентов галлюцинации и / или бред. Более чем у половины всех пациентов с болезнью Паркинсона в конечном итоге появляются симптомы на протяжении всего заболевания.1
Диагностика и лечение этого состояния могут быть сложными. Это состояние относится как к неврологии (отрасль медицины, которая занимается нервной системой), так и к психиатрии (отрасль медицины, которая занимается психическим и поведенческим здоровьем). По этой причине психоз при болезни Паркинсона считается нейропсихиатрическим состоянием, поскольку он связан с симптомами психического здоровья (галлюцинациями и бредом), вызванными заболеванием нервной системы (болезнь Паркинсона).
По этой причине психоз при болезни Паркинсона считается нейропсихиатрическим состоянием, поскольку он связан с симптомами психического здоровья (галлюцинациями и бредом), вызванными заболеванием нервной системы (болезнь Паркинсона).
В настоящее время нет четкого понимания точной причины психоза, вызванного болезнью Паркинсона, хотя считается, что определенные химические вещества и рецепторы мозга (например, дофамин и серотонин) играют определенную роль. Обычно считается, что данное состояние вызвано одним из следующих факторов:
Побочный эффект дофаминовой терапии: Хотя точная причинно-следственная связь не установлена, некоторые считают, что это состояние может быть побочным эффектом дофаминергической терапии (дофаминовые препараты являются наиболее распространенным лечением болезни Паркинсона).2
Дофаминергическая терапия повышает уровень дофамина, помогая улучшить двигательные симптомы у пациентов с болезнью Паркинсона. Однако повышение уровня дофамина также может вызывать химические и физические изменения в мозге, которые непреднамеренно приводят к таким симптомам, как галлюцинации или бред.
Однако повышение уровня дофамина также может вызывать химические и физические изменения в мозге, которые непреднамеренно приводят к таким симптомам, как галлюцинации или бред.
Это состояние может быть вызвано изменениями в мозге, которые происходят независимо от приема лекарств, усиливающих дофамин. Некоторые из этих изменений происходят естественным образом по мере прогрессирования болезни Паркинсона.2
Кто подвержен риску психоза?Невозможно с уверенностью предсказать, у каких пациентов с болезнью Паркинсона в дальнейшем разовьются такие симптомы, как галлюцинации или бред. С этим заболеванием связан ряд факторов риска — как внутренних, так и внешних. Некоторые из этих факторов риска включают: возраст, продолжительность и тяжесть болезни Паркинсона; и прием допаминовой терапии .’3-6
Каковы симптомы психоза? Два самых ярких симптома — это галлюцинации и бред.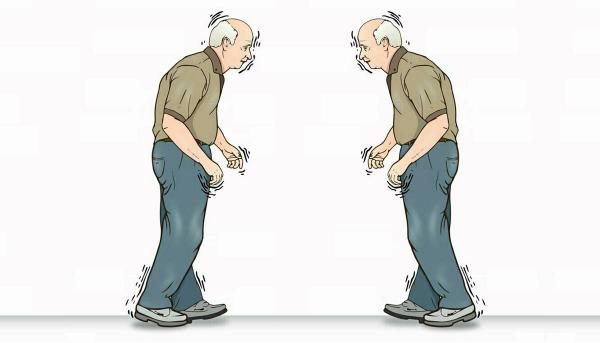 7 Галлюцинации связаны с видением, слушанием, переживанием или ощущением вещей, которых на самом деле нет. Заблуждения — это ложные убеждения, не основанные на реальности. При описании симптомов психоза, связанного с болезнью Паркинсона, пациенты могут использовать такие общие термины, как: видение вещей, паранойя, воспоминания, кошмары, ложные убеждения или отсутствие связи с реальностью8
7 Галлюцинации связаны с видением, слушанием, переживанием или ощущением вещей, которых на самом деле нет. Заблуждения — это ложные убеждения, не основанные на реальности. При описании симптомов психоза, связанного с болезнью Паркинсона, пациенты могут использовать такие общие термины, как: видение вещей, паранойя, воспоминания, кошмары, ложные убеждения или отсутствие связи с реальностью8
Лекарство от психоза
Пимавансерин (PEA-ma-VAN-ser-in) (Nuplazid ™) одобрен для лечения галлюцинаций и бреда, которые могут развиться на поздних стадиях болезни Паркинсона.Это может вызвать отек лодыжек, запор, спутанность сознания. Людям с нарушениями сердечного ритма следует избегать приема этого лекарства.
Почему не знают о психозе, вызванном болезнью Паркинсона? Люди с психозом от болезни Паркинсона нередко хранят молчание о своих переживаниях.2,4,9 На самом деле, только от 10% до 20% действительно сообщают о своих симптомах своим врачам. 4-9 Работа по повышению осведомленности продолжается. этого условия.Здесь вы можете найти дополнительную информацию о немоторных симптомах, связанных с болезнью Паркинсона.
4-9 Работа по повышению осведомленности продолжается. этого условия.Здесь вы можете найти дополнительную информацию о немоторных симптомах, связанных с болезнью Паркинсона.
Первое и самое главное, если вы обнаружите у себя такие симптомы, как галлюцинации или бред, выскажитесь. Очень важно обсудить с вашей лечащей бригадой весь спектр симптомов болезни Паркинсона. Диалог между пациентами, партнерами по уходу и врачами — важнейший компонент эффективного лечения вашего состояния.
Ссылки: 1. Forsaa EB, Larsen JP, Wentzel-Larsen T, et al. 12-летнее популяционное исследование психоза при болезни Паркинсона. Arch Neurol. 2010; 67: 996-1001. 2. Равина Б., Мардер И. (, Фернандес Х. Х. и др. Диагностические критерии психоза при болезни Паркинсона: отчет рабочей группы NINOS, NIMH. Mov Disord. 2007; 22: 1061-1068. 3. Holroyd J, Карри Л., Вутен Г. Ф. Проспективное исследование галлюцинаций и бреда при болезни Паркинсона. ) Нейро-нейрохирургическая психиатрия. 2011; 70: 734-738. 4. Фенелон Г., Махье Ф., Юон М., Зиглер М. Галлюцинации при болезни Паркинсона: распространенность, феноменология и факторы риска. Мозг. 2000; 123: 733-745. 5. Вольтерс ЭЧ. Психоз, связанный с БП: патофизиология с терапевтическими стратегиями. J Neural Transm. 2006; 71: 31-37. 6. Голдман Дж. Г., Холден С. Лечение психоза и деменции при болезни Паркинсона. Варианты лечения Curr Neurol. 2014; 16 (3): 281.7. Гольдман Дж. Г., Воган С., Гетц К. Г.. Обновленное мнение экспертов по ведению и исследованиям психозов при болезни Паркинсона. Expert Opin Pharmacother. 2011; 12 (13): 2009-2024. 8. Данные в досье, ACADIA Pharmaceuticals Inc. 9. Фенелон Г., Алвес Г. Эпидемиология психоза при болезни Паркинсона. } Neurol Sci. 2010; 289: 12-17.
) Нейро-нейрохирургическая психиатрия. 2011; 70: 734-738. 4. Фенелон Г., Махье Ф., Юон М., Зиглер М. Галлюцинации при болезни Паркинсона: распространенность, феноменология и факторы риска. Мозг. 2000; 123: 733-745. 5. Вольтерс ЭЧ. Психоз, связанный с БП: патофизиология с терапевтическими стратегиями. J Neural Transm. 2006; 71: 31-37. 6. Голдман Дж. Г., Холден С. Лечение психоза и деменции при болезни Паркинсона. Варианты лечения Curr Neurol. 2014; 16 (3): 281.7. Гольдман Дж. Г., Воган С., Гетц К. Г.. Обновленное мнение экспертов по ведению и исследованиям психозов при болезни Паркинсона. Expert Opin Pharmacother. 2011; 12 (13): 2009-2024. 8. Данные в досье, ACADIA Pharmaceuticals Inc. 9. Фенелон Г., Алвес Г. Эпидемиология психоза при болезни Паркинсона. } Neurol Sci. 2010; 289: 12-17.
Галлюцинаций / Заблуждений | Фонд Паркинсона
Психоз может быть пугающим словом, которого многие люди просто не понимают.Но что это на самом деле означает? При болезни Паркинсона (БП) то, что ваш врач называет психозом, обычно начинается с легких симптомов, но они могут иметь большое влияние на качество жизни. Медицинские работники обычно называют эти симптомы «психозом, связанным с болезнью Паркинсона». Психоз может варьироваться от сильного замешательства (расстройство мышления) до видения вещей, которых нет (галлюцинации), до веры в то, что не является правдой (заблуждения).
Медицинские работники обычно называют эти симптомы «психозом, связанным с болезнью Паркинсона». Психоз может варьироваться от сильного замешательства (расстройство мышления) до видения вещей, которых нет (галлюцинации), до веры в то, что не является правдой (заблуждения).
Важно сообщать вашей медицинской бригаде о любых галлюцинациях или бредах, даже если они не вызывают беспокойства.
Насколько распространен психоз при болезни Паркинсона?
Примерно 20-40% людей с болезнью Паркинсона сообщают о галлюцинациях или иллюзиях. Если следить за прогрессированием болезни с годами, это число увеличивается. Увеличение не означает, что галлюцинации сохраняются у большинства пациентов. Однако важно отметить, что эти статистические данные иногда включают «делирий», при котором симптомы являются временными из-за лекарств, которые необходимо скорректировать, или инфекции, которую необходимо лечить, и «отдельные незначительные симптомы» или «незначительные галлюцинации», включая иллюзии, когда вместо того, чтобы видеть вещи, которых нет (галлюцинации), люди неверно истолковывают то, что действительно есть. Это наиболее распространенные типы психозов у людей с болезнью Паркинсона, согласно различным исследованиям, встречаемость которых составляет 25-70% людей с болезнью Паркинсона. Как правило, если у человека с БП наблюдаются только эти незначительные галлюцинации, его врач не прописывает антипсихотические препараты, хотя со временем может развиться более серьезный психоз, требующий приема лекарств. В одном исследовании у 10% людей с незначительными галлюцинациями симптомы исчезли в течение нескольких лет, в то время как у 52% симптомы остались прежними, а у 38% симптомы психоза ухудшились.
Это наиболее распространенные типы психозов у людей с болезнью Паркинсона, согласно различным исследованиям, встречаемость которых составляет 25-70% людей с болезнью Паркинсона. Как правило, если у человека с БП наблюдаются только эти незначительные галлюцинации, его врач не прописывает антипсихотические препараты, хотя со временем может развиться более серьезный психоз, требующий приема лекарств. В одном исследовании у 10% людей с незначительными галлюцинациями симптомы исчезли в течение нескольких лет, в то время как у 52% симптомы остались прежними, а у 38% симптомы психоза ухудшились.
Мы рекомендуем людям с болезнью Паркинсона не использовать единый процент для представления распространенности галлюцинаций и PDP. Болезнь Паркинсона — сложное заболевание, и по мере его развития процентное соотношение и риск появления симптомов будут меняться.
Что такое галлюцинации?
Галлюцинации — это когда кто-то видит, слышит или чувствует то, чего на самом деле нет. Их лучше всего описать как обман или уловки мозга, задействующие органы чувств. Галлюцинации — это не сны или кошмары.Они случаются, когда человек бодрствует, и могут происходить в любое время дня и ночи.
Их лучше всего описать как обман или уловки мозга, задействующие органы чувств. Галлюцинации — это не сны или кошмары.Они случаются, когда человек бодрствует, и могут происходить в любое время дня и ночи.
Типы галлюцинаций
- Визуальный: Галлюцинации у людей с БП обычно визуальные. Общие галлюцинации включают видение животных или людей, например, бегущего мимо пушистого существа или умершего влюбленного, сидящего в комнате.
- Слуховая: Слышание ненастоящих голосов или звуков встречается реже, но о них сообщает небольшой процент людей с БП.
- Обонятельный: Обоняние запаха, не связанного с реальным источником, редко встречается при БП.
- Тактильно: Ощущение чего-то воображаемого, например, ползающих по коже жуков, при болезни Паркинсона встречается редко.
- Вкусно: Ощущение горького или ненормального привкуса во рту, не имеющего источника, является редкостью при БП.

Подробнее о галлюцинациях
- Галлюцинации чаще всего являются побочным эффектом лекарств и не обязательно являются признаком снижения когнитивных способностей.Большинство галлюцинаций, которые испытывают люди с БП, мимолетны и не опасны. Однако в некоторых случаях галлюцинации могут стать угрожающими или надоедливыми.
- Хотя галлюцинации могут возникать у любого, кто принимает лекарства для лечения симптомов болезни Паркинсона, они чаще встречаются у людей, у которых есть проблемы с мышлением или памятью, или когда они находятся в состоянии медицинского стресса.
- Визуальные галлюцинации чаще возникают в условиях недостаточной освещенности или плохой видимости. Чтобы снизить риск, увеличьте освещение в особенно темных местах, например в коридорах.
- Галлюцинации могут возникать периферическим зрением (краем глаза) в виде вспышки света, людей или мелких животных, таких как кошки или собаки. Изображения часто исчезают, когда человек присматривается.

- Иногда у людей с БП возникают галлюцинации присутствия — ощущение, что кто-то находится с ними в комнате или стоит позади них.
- Некоторые люди знают, что имеют место галлюцинации. Это называется «сохранением проницательности». Обладая проницательностью, вы могли бы создать механизмы преодоления.Однако некоторые люди находят их невероятно реальными или могут потерять понимание по мере прогрессирования болезни.
Советы для жизни с галлюцинациями
Людям с БП важно говорить о галлюцинациях со своей семьей и командой по уходу, потому что они поддаются лечению и могут быть неприятными, если их не лечить. Обсудите все возможные симптомы со своим врачом, независимо от того, насколько они незначительны, редки или необычны.
- Хорошее освещение и стимулирующие мероприятия по вечерам могут помочь избавиться от галлюцинаций.
- Когда происходит галлюцинация, лица, осуществляющие уход, могут помочь своим близким, заверив их, что они будут в безопасности, и подтверждая опыт своего партнера.
 Например, скажите: «Я выведу кошку на улицу» вместо того, чтобы утверждать, что кошки нет.
Например, скажите: «Я выведу кошку на улицу» вместо того, чтобы утверждать, что кошки нет.
Что такое иллюзии?
Иллюзии — еще одно сенсорное заблуждение. Вместо того чтобы видеть то, чего нет, люди с иллюзиями неверно истолковывают реальные вещи в окружающей среде. Например, одежда в шкафу может выглядеть как группа людей.
Подобно зрительным галлюцинациям, иллюзии возникают в условиях недостаточной освещенности или плохой видимости.
Что такое заблуждения?
Заблуждения — это нелогичные, иррациональные, дисфункциональные взгляды или настойчивые мысли, не основанные на реальности. Они не являются преднамеренными и очень реальны для человека с PD. Люди с заблуждениями, которые чувствуют угрозу, могут становиться спорщиками, агрессивными, взволнованными или небезопасными.
- Бред при БП встречается реже, чем зрительные галлюцинации.Они затрагивают около восьми процентов людей с болезнью Паркинсона.
- По сравнению с галлюцинациями, бред более сложен, представляет больший риск поведенческих расстройств и проблем безопасности, обычно труднее поддается лечению и представляет собой более очевидное ухудшение или ухудшение состояния.

- Бред может начаться ночью как общая спутанность сознания. Со временем замешательство может перерасти в явные заблуждения и поведенческие расстройства в течение дня.
- Все формы бреда можно увидеть при БП, хотя бред ревности и преследования (например, паранойя) встречается наиболее часто и представляет большую проблему для лечения.Эти заблуждения могут привести к агрессии, которая может представлять серьезную угрозу безопасности человека с БП, членов семьи и лиц, осуществляющих уход.
- Паранойя может привести к несоблюдению лекарств — человек отказывается принимать лекарства, считая их ядовитыми или смертельными.
- Бред может быть связан с деменцией. В результате люди с заблуждениями часто сбиты с толку, и с ними чрезвычайно трудно справиться. В этих случаях многим опекунам требуется помощь извне.
Примеры заблуждений в PD
- Ревность
- Убеждение: ваш партнер изменяет.
- Поведение: Паранойя, возбуждение, мнительность, агрессия.

- Преследование
- Убеждение: на вас нападают, преследуют, обманывают или сговаривают.
- Поведение: Паранойя, подозрительность, возбуждение, агрессия, неповиновение, социальная изоляция.
- Соматический
- Убеждение: Ваше тело функционирует ненормально. У вас появляется необычная одержимость своим телом или здоровьем.
- Поведение: Беспокойство, возбуждение, сообщения об аномальных или необычных симптомах, крайняя озабоченность симптомами, частые посещения врача.
Что вызывает галлюцинации и бред?
Медикаменты, деменция и делирий — три основных фактора, способствующих развитию психоза при болезни Паркинсона. Определить причину может быть сложно, потому что эти состояния могут накладываться друг на друга и вызывать схожие симптомы. После определения вероятной причины можно начинать лечение.
Лекарства
Многие лекарства от БП могут вызывать симптомы психоза:
- Классические препараты для лечения БП, такие как карбидопа-леводопа (Синемет) и агонисты дофамина, предназначены для повышения уровня дофамина и улучшения двигательных симптомов.
 Однако, увеличивая выработку дофамина, эти лекарства могут непреднамеренно вызвать серьезные эмоциональные и поведенческие изменения.
Однако, увеличивая выработку дофамина, эти лекарства могут непреднамеренно вызвать серьезные эмоциональные и поведенческие изменения. - Другие лекарства, применяемые для лечения БП, также могут вызывать эти симптомы, снижая уровень ацетилхолина, изменяя его баланс с дофамином. Эти лекарства включают амантадин и холинолитики (артан и когентин). В дополнение к лекарствам, отпускаемым по рецепту, холинолитики обычно являются основным ингредиентом безрецептурных снотворных и многих лекарств от аллергии.
Деменция
Деменция — это термин, используемый для описания группы симптомов, связанных с ухудшением памяти и мышления. Это обычно связано с болезнью Альцгеймера, но у людей с болезнью Паркинсона также может развиться болезнь.
- Галлюцинации и бред могут быть результатом основных химических и физических изменений, происходящих в головном мозге, независимо от других факторов, таких как лекарства от болезни Паркинсона. Это чаще всего наблюдается в случаях БП с деменцией.

- Если психоз и деменция возникают на ранней стадии заболевания, врачи могут рассмотреть диагноз деменции с тельцами Леви (LBD).
Делириум
Делирий — это обратимое изменение уровня внимания и концентрации человека.
- Делирий обычно развивается в течение короткого периода времени (от часов до дней) и проходит после лечения основного заболевания.
- Признаки делирия включают измененное сознание или осознание, неорганизованное мышление, необычное поведение и галлюцинации.
- Поскольку существует очень много симптомов, делирий можно спутать с другими состояниями, такими как слабоумие или психоз, вызванный лекарствами.
- Чтобы диагностировать делирий, необходимо изменить уровень концентрации или внимания человека.
- Люди с болезнью Паркинсона имеют более высокий риск развития делирия при поступлении в больницу из-за новых настроек процедуры или хирургического вмешательства, которые могут быть не связаны с их болезнью Паркинсона.
Общие причины делирия включают:
- Инфекция, например инфекция мочевыводящих путей или пневмония
- Нарушение баланса натрия, калия, кальция или других электролитов
- Ход
- Болезнь сердца
- Болезнь печени
- Лихорадка
- Дефицит витамина B12
- Травма головы
- Сенсорные изменения, такие как потеря слуха и изменения зрения
Помимо заболеваний и изменений, многие часто используемые лекарства и химические вещества также могут вызывать делирий:
- Антихолинергические препараты: гидрохлорид дифенгидрамина (Benadryl ® ), тригексифенидил (Artane ® ), бензтропин (Cogentin ® ), ранитидин (Zantac ® ) и 902 ® дибутинин
- Наркотики, содержащие кодеин или морфин
- Антибиотики
- Нестероидные противовоспалительные препараты (НПВП), включая Aleve ® , Motrin ® и Advil ®
- Инсулин
- Седативные препараты
- Стероиды
- Противосудорожные препараты
- Спирт
- Рекреационные препараты
Факторы риска психоза
Не у всех с болезнью Паркинсона развиваются галлюцинации или бред, но есть несколько вещей, которые могут увеличить ваш риск:
- Деменция или нарушение памяти
- Депрессия: Люди, страдающие депрессией и болезнью Паркинсона, подвергаются большему риску.Кроме того, одна только тяжелая депрессия может вызвать психоз.
- Нарушения сна, например яркие сновидения. Люди обычно сообщают о ярких сновидениях до начала психоза. Другие связанные нарушения сна включают расстройство быстрого сна и общую бессонницу.
- Нарушение зрения
- Пожилой возраст
- Продвинутая или поздняя стадия PD
- Использование препаратов для ПД
Лечение психоза
Лечение психоза при болезни Паркинсона — это многоэтапный процесс, который начинается с разговора с вашим лечащим врачом.Они выполнят ряд шагов, чтобы выяснить, как лучше всего бороться с вашими симптомами.
Шаг 1 . Первым шагом является проведение клинической оценки ваших симптомов с учетом предшествующего анамнеза, стадии заболевания и доступных систем поддержки. Эта оценка поможет определить, если что-то не так с медицинской точки зрения и вам нужно лечение немедленно, или вы можете следить за состоянием и подождать.
Шаг 2 . При необходимости лечение обычно начинается с корректировки лекарств от БП и направления на консультацию.Если у вас все в порядке с медицинской точки зрения, ваш врач может уменьшить или исключить прием лекарств, часто в определенном порядке, чтобы уменьшить симптомы психоза. Это уравновешивающее действие, поскольку дофамин, который используется для стабилизации двигательных симптомов, также может в больших количествах усиливать психологические побочные эффекты.
Шаг 3 . Если необходимо дальнейшее вмешательство, ваш врач может начать антипсихотическую терапию, используя лекарства для восстановления баланса химических веществ в мозге и уменьшения эпизодов галлюцинаций, иллюзий и заблуждений
Лекарства, используемые для лечения психозов
Антипсихотические средства предназначены для уравновешивания аномальных химических уровней в головном мозге.Вплоть до 1990-х годов использование антипсихотических средств при БП было спорным, поскольку применяемые до этого времени препараты снижают избыток дофамина. Это облегчило психоз, но вызвало резкое ухудшение моторных симптомов БП.
К счастью, сейчас доступны лекарства, которые лучше переносятся людьми с БП. Сегодня существует три антипсихотических препарата, которые считаются относительно безопасными для людей с БП: кветиапин (Сероквель ® ), клозапин (Клозарил ® ) и новейший препарат пимавансерин (Нуплазид ® ).Они вызывают ограниченное ухудшение БП при лечении галлюцинаций и бреда.
Пимавансерин
- Пимавансерин был одобрен Управлением по контролю за продуктами и лекарствами США (FDA) в 2016 году специально для лечения психоза, вызванного болезнью Паркинсона.
- В отличие от других нейролептиков, он не блокирует дофамин. Это селективный обратный агонист серотонина, что означает, что он нацелен на рецепторы серотонина.
Клозапин
- Клозапин (Клозарил) был изучен и доказал свою эффективность в улучшении галлюцинаций и бреда при БП.Однако из-за редкого, но серьезного побочного эффекта, известного как агранулоцитоз — уменьшение количества лейкоцитов, которое препятствует способности организма бороться с инфекцией — существует тенденция использовать этот препарат только в том случае, если кветиапин не переносится или не эффективен.
- Любой, кто принимает клозапин, обязан сдавать анализы крови еженедельно в течение первых шести месяцев, а затем каждые две недели для контроля уровня лейкоцитов.
Кветиапин
- Кветиапин (Сероквель) имеет меньше побочных эффектов, но есть ограниченные доказательства его эффективности у людей с болезнью Паркинсона.
- Чаще всего его назначают перед сном, потому что он может иметь легкое седативное действие.
* Важно ознакомиться с антипсихотическими препаратами, поскольку многие из них могут ухудшить двигательные симптомы и не должны назначаться людям с БП. Некоторые из этих лекарств, такие как галоперидол (Haldol), обычно прописываются в больничных условиях пациентам, которые возбуждены или обеспокоены. Лечащие врачи должны знать, что некоторые антипсихотические препараты могут ухудшить состояние человека с БП.
Как поговорить с кем-то с галлюцинациями или бредом
- Обычно бесполезно спорить с тем, кто испытывает галлюцинации или иллюзии. Не пытайтесь рассуждать. Сохраняйте спокойствие и успокаивайте.
- Вы можете сказать, что не видите того, что видит ваш любимый, но некоторые люди находят более успокаивающим осознавать то, что видит человек, чтобы уменьшить стресс. Например, если человек видит в комнате кошку, лучше сказать: «Я вытащу кошку», чем утверждать, что кошки нет.
Страница проверена доктором Чонси Спирс, научным сотрудником по двигательным расстройствам Университета Флориды, Центра передового опыта Фонда Паркинсона.
Как справиться с психозом Паркинсона
Форум AgingCare.com заполнен людьми, которые собираются вместе, чтобы поделиться ценной информацией. Мы собрали лучшие советы и предложения опытных медработников по работе с галлюцинациями и бредом, связанными с лекарствами от PD.
Как справиться с психозом от болезни Паркинсона
«Моя мама имела обыкновение видеть галлюцинации, что повсюду ползают насекомые. Раньше мы пытались убедить ее, что их там нет, но это ее еще больше расстраивало. Ее врач посоветовал нам смириться с этим, притвориться, что мы тоже видим ошибки, и помочь ей избавиться от них с помощью «спрея от насекомых» (который был просто флакончиком Windex). Это сработало. Она сразу успокоилась и сразу почувствовала себя лучше. Больше лекарств не всегда может быть ответом ». –Writervicki
«Вместе с мужем я обнаружила, что малейшее обезвоживание может вызвать спутанность сознания и галлюцинации.Убедитесь, что ваш любимый человек получает достаточно жидкости, и убедитесь, что он сидит прямо во время питья, чтобы избежать аспирации. Использование соломинки может помочь им с приемом пищи, но сначала спросите об этом вашего терапевта ». –Bdeartrm
«Если у близкого человека есть психотические симптомы, вам следует проверить его лекарства. У моего отца были проблемы с галлюцинациями, и врач обнаружил, что причиной был Мирапекс ». –Barkley37
«У моей мамы бывают то, что я называю« эпизодами », когда она говорит всю ночь и весь день галлюцинирует.Так продолжается уже 3 года. Сначала это происходило с разницей в несколько месяцев, а теперь — каждую неделю. Если ее не расстраивает то, что она видит, я просто соглашусь с этим, потому что обычно это проще, чем пытаться убедить ее, что она в ла-ла-стране. В последнее время она спрашивает, как зовут моего мужа, но я в разводе уже несколько лет. Она уверена, что я снова женат и даже видела своего нового мужа по телевизору вчера вечером. Итак, сегодня я сказал ей, что его зовут Саймон. Пока она была довольна этим. Для всех нас, ухаживающих, это всего один день! » –Sulynn49
«Проверьте, есть ли у вашего близкого инфекция мочевого пузыря или инфекция мочевыводящих путей (ИМП).У моей мамы был БП 16 лет, у нее были приступы галлюцинаций. Я бы просто выбрал хорошие. Иногда у нее также были инфекции мочевого пузыря, и это, похоже, усиливало галлюцинации. Никогда не исключайте, что это будет проверено! » –Lovingkid
Просмотрите наши бесплатные
Руководства по уходу за пожилыми людьми
«Я попросила невролог прописать моему мужу нуплазид. Его «приступы» были серьезными и происходили каждую ночь. Он до смерти боялся этих ужасных людей, которые приходили к нему в гости. Препарат подействовал.Он по-прежнему видит людей, но они больше не злые или угрожающие. Какая спасительная жизнь ». –Rosemary44
«Лекарства для пациентов с болезнью Паркинсона — это сложная вещь, которую сложно сбалансировать и контролировать, и может потребоваться частая корректировка. Когда вы добавляете вызов галлюцинациям, все становится еще сложнее. Мой отец много бродил по ночам, часто замечая незваных гостей, которых там не было. Я обнаружил, что ему стало лучше с минимальным количеством лекарств, но все разные ». –Leighbird
Управление психозом при болезни Паркинсона: проблемы и возможности
Раджеш Пахва, MD
Нейропсихиатрические проявления представляют собой ключевой признак болезни Паркинсона (БП) от преддиагностической фазы до терминальной стадии.Психоз при болезни Паркинсона (PDP) считается результатом увеличения количества рецепторов 5-HT2A и дофаминергической гиперактивности. Однако препараты-агонисты дофамина (DA), такие как леводопа (L-допа), которые помогают снизить жесткость мышц и тремор, также могут вызывать психоз, отмеченный галлюцинациями и бредом. Клинический подход к лечению PDP традиционно основан на первоначальном снижении дофаминергического агента и рассмотрении дополнительной терапии для лечения психиатрических симптомов.
Сопутствующие психические расстройства при БП являются обычным явлением, и, несмотря на то, что они оказывают значительное влияние на качество жизни пациентов (КЖ), они остаются недооцененными.В клинических и исследовательских учреждениях были разработаны несколько шкал, которые помогают врачам оценивать такие симптомы, как галлюцинации, делирий и психоз. Появляется все больше доказательств в пользу фармакологических и нефармакологических вариантов лечения депрессии, но доказательства лечения других нейропсихиатрических особенностей гораздо менее надежны. 1 PDP, как сообщается, поражает до 60% пациентов в течение их жизни, и этот риск увеличивается с возрастом и увеличением доз препаратов DA. 2 PDP также ассоциируется с плохим прогнозом и обычно влечет за собой большую нагрузку на обслуживающего персонала, смертность и увеличение числа случаев помещения в дома престарелых.
Установлены определение и формальные критерии PDP как отдельного заболевания. Считается, что симптомы PDP прогрессируют и могут включать галлюцинации, затрагивающие все 5 органов чувств (чаще всего зрение), иллюзии и заблуждения. Прогрессирование таково, что симптомы, которые просто беспокоят на ранней стадии, вероятно, станут более серьезными, разнообразными и доставляющими беспокойство по мере прогрессирования болезни.Сообщается, что PDP и расстройства контроля импульсов связаны с приемом DA 3 и включены в поведенческий спектр немоторных симптомов PD.
«Как только у пациента появляются симптомы психоза, они прогрессируют», — сказал Раджеш Пахва, доктор медицины, профессор неврологии Лаверн и Джойс Райдер в Медицинском центре Канзасского университета. «Клиницисты должны внимательно наблюдать за пациентами и лечить их, когда симптомы начинают вызывать проблемы у пациента или лица, осуществляющего уход».
Фармакологическое лечениеНачало хронической PDP или переход от острого к хроническому состоянию PDP должно побудить к оценке текущих методов лечения и систематическому сокращению этих терапий в следующем порядке: антихолинергические агенты, селегилин, амантадин, DA, ингибиторы катехол-O-метилтрансферазы и леводопа. 4 Если эта стратегия не улучшает симптомы психоза, врачам следует рассмотреть возможность использования ингибиторов холинэстеразы (например, ривастигмина 6-12 мг / 2-3 дня, донепезила 5-10 мг в день или галантамина 4-32 мг / 2-3 дня. дней) или антипсихотических препаратов (клозапин 12,5–62,5 мг в сутки или кветиапин 12,5–75 мг в сутки).
Использование атипичных нейролептиков при БП было связано со статистически значимым риском смерти. 4 В качестве атипичного нейролептика клозапин немного сильнее кветиапина, но связан с повышенным риском агранулоцитоза с предполагаемой распространенностью от 1% до 2%. 4 Кветиапин, производное дибензотиазепина, структурно родственное клозапину, является самым слабым атипичным антипсихотиком и, следовательно, имеет более низкий риск смерти. В исследовании, сравнивающем эффективность клозапина и кветиапина, Merims и его коллеги 5 обнаружили общую тенденцию клозапина по сравнению с кветиапином в борьбе с галлюцинациями и уменьшении бредовых идей, но высокая частота агранулоцитоза с клозапином предполагает ограничение в его использовании.
Другие атипичные нейролептики показали ненадежную эффективность или неприемлемое снижение двигательной функции.Нет данных об эффективности оланзапина при лечении PDP, и это связано с ухудшением двигательной функции. 4 Было также показано, что рисперидон ухудшает двигательную функцию и поэтому не рекомендуется при PDP. 4 Мелперон, атипичный антипсихотик химического класса бутирофенонов, не показал преимуществ по сравнению с плацебо в исследовании Фридмана. 6
Единственным лекарством, одобренным FDA для лечения PDP, является пимавансерин (Nuplazid; Acadia), мощный и высокоселективный обратный агонист 5-HT2A без дофаминергического, адренергического, гистаминергического или мускаринового сродства. 7 Эти атрибуты делают маловероятным блокирование постсинаптического DA и других нецелевых рецепторов. Считается, что механизм действия пимавансерина снижает чрезмерную нейротрансмиссию, разрешенную рецепторами 5-HT2A, тем самым уменьшая зрительные галлюцинации при PDP.
Одобрен FDA в апреле 2016 года, пимавансерин рекомендуется в суточной дозировке 34 мг и показан для лечения бреда и галлюцинаций у пациентов с PDP. В 3-й фазе исследования ACP-103-020 с участием 199 участников было показано, что пимавансерин снижает бред на 41% и галлюцинации на 34% по сравнению с 21% и 18%, соответственно, в группе плацебо. 8 Улучшение галлюцинаций и иллюзий было статистически значимым в глобальных рейтингах Шкалы оценки положительных симптомов. Исследователи также обнаружили, что лечение пимавансерином не ухудшало двигательные симптомы. 8
Пимавансерин не одобрен для лечения пациентов с психозом, связанным с деменцией, который не связан с галлюцинациями и бредом, связанными с PDP, что создает проблемы при лечении пожилых пациентов с PD, которые с большей вероятностью страдают деменцией.Однако результаты недавнего анализа эффективности исследования HARMONY фазы 3 показали, что пимавансерин статистически значимо снижает риск рецидива психоза, связанного с деменцией. 9
Следует избегать назначения препарата пациентам с сердечными аритмиями, симптоматической брадикардией, гипокалиемией, гипомагниемией и удлинением интервала QT в анамнезе или в комбинации с другими лекарствами, которые, как известно, удлиняют интервал QT, включая класс 1A или класс 3. антиаритмические средства. В клинических испытаниях было показано, что пимавансерин хорошо переносится; профиль его побочных эффектов включает инфекции мочевыводящих путей (ИМП), периферические отеки, галлюцинации, спутанность сознания, тошноту и головные боли. 8
«Поскольку симптомы часто начинаются постепенно, и если пациент осматривается в клинике и иногда имеет галлюцинации, и пациент понимает, что они не настоящие, мой подход заключается в наблюдении за пациентами», — сказал Пахва. который также является руководителем отделения болезни Паркинсона и двигательных расстройств и директором Центра передового опыта Фонда Паркинсона при Медицинском центре Канзасского университета. «Если пациент звонит до следующего визита и говорит, что его галлюцинации усиливаются или беспокоят, я проверяю, не добавлены ли новые лекарства, такие как наркотические обезболивающие, и проверяю стандартные лаборатории и [анализ мочи], чтобы убедиться, что они этого не делают. у вас ИМП или обезвоживание.Если у пациента [действительно есть бред, связанный с заболеванием], мы начинаем пимавансерин ».
По сравнению с атипичными нейролептиками для лечения PDP, которые могут вызывать нежелательные явления, такие как ухудшение двигательных симптомов и ортостатическая гипотензия, пимавансерин является предпочтительным вариантом для большинства пациентов на основании его продемонстрированной клинической эффективности и безопасности. 10
«Если возможно, я мог бы уменьшить количество лекарств с антихолинергическими свойствами [если они их принимают], уменьшить или исключить амантадин и уменьшить количество агонистов дофамина», — сказал Пахва.«Если уменьшение количества лекарств не уменьшает галлюцинации, я добавляю пимавансерин».
Недавние результаты, представленные на Ежегодном собрании Американской академии неврологии, состоявшемся 4-10 мая 2019 года в Филадельфии, штат Пенсильвания, показали, что среди людей с PDP или деменцией с тельцами Леви не было значительных различий в эффективности пимавансерина или кветиапина во времени. к прекращению приема лекарств, снижению смертности или улучшению состояния психоза. 11
«Пимавансерин — единственный одобренный препарат для лечения PDP.Поскольку он был одобрен на основании [результатов] 1 исследования, клиницисты часто считают, что данных по его эффективности недостаточно », — сказал Пахва.
Альтернативные варианты леченияУсиление серотонинергической нейротрансмиссии и активации мезокортиколимбического пути посредством электросудорожной терапии (ЭСТ) может иметь антипсихотический и антидепрессивный эффект при БП. 4 Сообщалось о положительных эффектах ЭСТ, при этом Кальдеро & # 769; н-Фахардо и его коллеги отметили улучшение показателей двигательной и немоторной функции по разным шкалам с использованием ЭСТ у 29 пациентов с лекарственно-рефрактерным ПД с психиатрическими симптомами, включая 12 больных психозом и депрессией. 12 О проблемах, связанных с безопасностью и переносимостью ЭСТ, не сообщалось; Важно отметить, что до настоящего времени исследования проводились только с небольшими выборками и не были слепыми, из-за чего возникла необходимость в более крупных, фиктивно контролируемых исследованиях.
Потенциал глубокой стимуляции мозга (DBS) для лечения психических расстройств показал себя многообещающим при таких состояниях, как обсессивно-компульсивное расстройство и большое депрессивное расстройство; однако доказательства влияния DBS на PDP отсутствуют. 4 Исследования выявили переменное положительное и отрицательное влияние на психические симптомы после DBS при БП, при этом некоторые сообщают об ухудшении или появлении новых симптомов, а другие сообщают об улучшениях, а именно в состояниях, связанных с настроением. 13 Эти результаты, хотя и неубедительные для пациентов с PDP, подчеркивают важность отбора пациентов для DBS, поскольку предшествующий анамнез нейропсихиатрических расстройств, по-видимому, влияет на исходы. 13
Результаты доклинических и предварительных исследований также предполагают, что каннабидиол (CBD) обладает терапевтическим потенциалом при немоторных симптомах БП. 14 Многогранный механизм действия в качестве агониста 5-HT1A, частичного агониста рецепторов CB1 и CB2 и антагониста рецептора, связанного с G-белком GPR55, обращает индуцированную железом эпигенетическую модификацию митохондриальной ДНК и восстановление сукцината. дегидрогеназной активности и снижает уровни провоспалительных цитокинов IL-1β, TNF-α, IFN-β, IFN-γ, IL-17 и IL-6 — все это снижает провоспалительные медиаторы, что приводит к нейропротекторному, анксиолитическому , и антипсихотические эффекты. 14
«Несколько экспериментов in vitro продемонстрировали многообещающие нейрозащитные эффекты CBD на моделях БП. В одной из этих моделей с использованием клеток PC12 и SH-SY5Y, обработанных MPP + [1-метил-4-фенилпиридинием], CBD увеличивал жизнеспособность клеток, дифференцировку и экспрессию аксонального [GAP-43] и синаптического [синаптофизина и синапсина I. ] белков », — написали Феррерия-Джуниор и его коллеги, 15 , признавая при этом небольшое количество исследований, посвященных биологическим основам предполагаемого воздействия CBD на БП.«Двойные слепые, плацебо-контролируемые, рандомизированные исследования с более крупными выборками пациентов с БП необходимы для выяснения возможной эффективности и механизмов, задействованных в терапевтическом потенциале КБД при этом двигательном расстройстве. Это также будет включать предполагаемые эффекты CBD в предотвращении тяжелых [побочных] эффектов, вызванных L-допа, и предотвращении прогрессирования болезни Паркинсона ».
Эндоканнабиноидная система служит важным фильтром возбуждающих, тормозных и модулирующих входов, которые действуют в среднем мозге и терминальных областях, чтобы управлять нейротрансмиссией DA, контролируя паттерны возбуждения DA-клеток, терминальное высвобождение и влияние на постсинаптические участки в полосатом теле. 16 Благоприятные эффекты введения CBD наблюдались до или сразу после индукции PD-подобных симптомов в исследованиях на животных, что может указывать на профилактическую роль, а не на терапевтическую. 14 В раннем открытом пилотном исследовании по оценке эффективности CBD в отношении немоторных симптомов PD у 6 пациентов с PDP, психотические симптомы значительно уменьшились при лечении CBD, как было оценено с помощью краткой психиатрической рейтинговой шкалы и опросника психоза Паркинсона. 17
Насущные потребностиПоскольку болезнь Паркинсона и психоз находятся на противоположных концах спектра DA, сложное взаимодействие между ними ставит врачей, пациентов и лиц, осуществляющих уход, перед сложной задачей достижения баланса между физическая и эмоциональная устойчивость.
Несмотря на оценки, согласно которым распространенность БП увеличится более чем вдвое к 2060 году, обучение психиатрической помощи, связанной с ПП, не является стандартом для большинства программ, и потребность в специалистах по психиатрической помощи со временем будет только возрастать с возрастом. Население.Учитывая ограничения на распространение психиатрической помощи в существующие модели интегрированной или многопрофильной помощи, специализированная психиатрическая помощь обычно не доступна, недоступна или интегрирована в большинство неврологических практик. 18
Сопутствующие психиатрические заболевания, преобладающие у большинства пациентов с БП, связаны с большей тяжестью заболевания, ухудшением качества жизни и повышенным использованием ресурсов здравоохранения, при этом более длительное пребывание в больнице и повторные госпитализации увеличивают общую стоимость.Междисциплинарный подход к ведению ПРП имеет решающее значение для улучшения общего результата и связанного со здоровьем качества жизни этих пациентов и лиц, ухаживающих за ними. 19 В будущих исследованиях следует использовать клинические данные и использовать продольные модели для оценки результатов среди пациентов с PDP и коморбидной депрессией и другими психоневрологическими состояниями.
СПИСОК ЛИТЕРАТУРЫ
1. Надь А., Шраг А. Нейропсихиатрические аспекты болезни Паркинсона. Дж. Нейронная передача . 2019; 126 (7): 889-896.DOI: 10.1007 / s00702-019-02019-7.
2. Форсаа Э. Б., Ларсен Дж. П., Вентцель-Ларсен Т. и др. 12-летнее популяционное исследование психоза при болезни Паркинсона. Арка Нейрол . 2010; 67 (8): 996-1001. DOI: 10.1001 / archneurol.2010.166.
3. Вайнтрауб Д., Дэвид А.С., Эванс А.Х., Грант Дж. Э., Стейси М. Клинический спектр нарушений импульсного контроля при болезни Паркинсона. Движение Дисорд . 2015; 30 (2): 121-127. DOI: 10.1002 / mds.26016.
4. Taddei RN, Cankaya S, Dhaliwal S, Chaudhuri KR.Управление психозом при болезни Паркинсона: подчеркивание клинических подтипов и патофизиологических механизмов состояния. Parkinsons Dis. 2017; 2017: 3256542. DOI: 10,1155 / 2017/3256542.
5. Меримс Д., Балас М., Перец С., Шабтай Х., Гилади Н. Перспективное сравнение, слепое по оценке: кветиапин и клозапин при психозе, вызванном болезнью Паркинсона. Clin Neuropharmacol . 2006; 29 (6): 331-337. DOI 10.1097 / 01.WNF.0000236769.31279.19.
6. Friedman JH. Мелперон неэффективен при лечении психоза при болезни Паркинсона. Движение Дисорд . 2012; 27 (6): 803-804. DOI: 10.1002 / mds.24942.
7. Медоукрафт Л.М., Цурутис В., Моррисетт Т. Пимавансерин для лечения галлюцинаций и бреда, связанных с психозом при болезни Паркинсона. Энн Долгосрочная помощь . 2016; 25 (3): 43-48.
8. Исследование безопасности и эффективности пимавансерина у пациентов с психозом при болезни Паркинсона. Clinicaltrials.gov/ct2/show/NCT01174004. Обновлено 26 марта 2014 г. Проверено 26 августа 2019 г.
9.Acadia Pharmaceuticals объявляет о досрочном прекращении ключевой фазы 3 исследования HARMONY из-за положительной эффективности, поскольку пимавансерин соответствует основной конечной точке у пациентов с психозом, связанным с деменцией [пресс-релиз]. Сан-Диего, Калифорния: Acadia Pharmaceuticals Inc; 9 сентября 201 г. biospace.com/article/releases/acadia-pharmaceuticals-announces-pivotal-phase-3-harmony-trial-stopped-early-for-positive-efficacy-as-pimavanserin-meets-the-primary-endpoint- пациенты с психозом, связанным с деменцией /. По состоянию на 10 сентября 2019 г.
10. Lyons KE, Pahwa R, Hermanowicz N, Davis T., Pagan F, Isaacson S. Изменение парадигмы лечения психоза при болезни Паркинсона с помощью пимавансерина. Эксперт Рев Клин Фармакол . 2019; 12 (7): 681-691. DOI: 1080/17512433.2019.1623669.
11. Хорн С., Даходвала Н. Пимавансерин в сравнении с кветиапином для лечения психоза при болезни Паркинсона и деменции с тельцами Леви. Представлено на: Ежегодном собрании Американской академии неврологии, 2019 г .; 4-10 мая 2019 года. Филадельфия, Пенсильвания.n.neurology.org/content/92/15_Supplement/P2.8-037.
12. Кальдерон-Фахардо Х., Сервантес-Арриага А., Льоренс-Аренас Р., Рамирес-Бермудес Дж., Руис-Чоу Б., Родригес-Виоланте М. Электросудорожная терапия при болезни Паркинсона. Arq Neuropsiquiatr . 2015; 73 (10): 856-860. DOI: 10.1590 / 0004-282X20150131.
13. Accolla EA, Pollo C. Эффекты настроения после глубокой стимуляции мозга при болезни Паркинсона: обновленная информация. Front Neurol. 2019; 10: 617. DOI: 10.3389 / fneur.2019.00617.
14. Peres FF, Lima AC, Hallak JEC, Crippa JA, Silva RH, Abílio VC. Каннабидиол как многообещающая стратегия лечения и профилактики двигательных расстройств? Front Pharmacol. 2018; 9: 482. DOI: 10.3389 / fphar.2018.00482.
15. Феррейра-Жуниор NC, Campos AC, Guimarães FS, et al. Биологические основы возможного действия каннабидиола при болезни Паркинсона [опубликовано в Интернете 15 июля 2019 г.]. Браз Дж. Психиатрия . DOI: 10.1590 / 1516-4446-2019-0460.
16.Кови Д.П., Матео Ю., Зульцер Д., Приветствие Дж. Ф., Ловингер Д. Эндоканнабиноидная модуляция нейротрансмиссии дофамина. Нейрофармакология . 2017; 124 (15): 52-61. DOI: 10.1016 / j.neuropharm.2017.04.033.
17. Zuardi AW, Crippa J, Hallak JEC, et al. Каннабидиол для лечения психоза при болезни Паркинсона. J Психофармакол . 2009; 23 (8): 979-983. DOI: 10.1177 / 0269881108096519.
18. Понтоне Г.М., Диссанаяка Н., Добкин Р.Д. и др. Интеграция и расширение специализированных услуг по охране психического здоровья в общественную практику при болезни Паркинсона. Am J Гериатр Психиатрия . 2019; 27 (7): 712-719. DOI: 10.1016 / j.jagp.2019.03.005.
19. Имран С., Пател Р.С., Ониеака Х.К. и др. Коморбидная депрессия и психоз при болезни Паркинсона: отчет о 62 783 госпитализации в США. Cureus . 2019; 11 (7): e5227. DOI: 10.7759 / cureus.5227.
Ведение психоза при болезни Паркинсона
Диагноз болезни Паркинсона (БП) основан на наблюдении за совокупностью двигательных аномалий (брадикинезия, тремор в покое, ригидность зубчатого колеса, постуральная нестабильность) и исключении других вторичных причин паркинсонизм.Заболевание классифицируется как «двигательное расстройство», но для многих пациентов с БП двигательные проблемы являются лишь верхушкой айсберга. Множество психоневрологических расстройств присуще БП или возникают как осложнение дофаминергической терапии (агонисты дофамина, леводопа) или антихолинергических препаратов, используемых для лечения двигательных симптомов (, таблица 1, ). Для некоторых пациентов с БП психоневрологические осложнения являются более серьезным источником заболеваемости, чем двигательная дисфункция. 1,2
Нейропсихиатрические расстройства, связанные с дофаминергической терапией, важно распознавать, потому что они, по крайней мере, частично являются ятрогенными и часто могут быть успешно купированы путем корректировки лекарств для лечения PD пациента.Эта статья посвящена лечению психозов при болезни Паркинсона — проблеме со значительной заболеваемостью. Психоз при БП и расстройствах, связанных с паркинсонизмом (например, деменция с тельцами Леви, деменция при болезни Паркинсона), является независимым предиктором необходимости помещения в лечебное учреждение и повышения смертности.
Восприимчивость к психозу
Основная предрасположенность к психозу во многом зависит от психического состояния пациента. Пациенты с БП без когнитивных нарушений, не получающие лекарств для облегчения двигательных симптомов, редко испытывают бред или галлюцинации.Однако легкие психотические симптомы (например, зрительные иллюзии [искаженное сенсорное восприятие реального стимула], доброкачественные зрительные галлюцинации / ощущение присутствия [ощущение, что кто-то находится поблизости, когда никого нет] или временные галлюцинации [мимолетные визуальные образы на периферии видение]) встречаются примерно у 10-20% недемментированных пациентов с БП, получающих дофаминергические препараты. 3
Галлюцинации чаще появляются в сумерках или вечером (на закате), когда фоновая стимуляция незначительна, или когда пациент находится один в тихой комнате.Агонисты дофамина чаще вызывают галлюцинации, чем карбидопа / леводопа. Психоз с галлюцинациями и бредом был зарегистрирован у 20% пациентов без деменции, получающих лекарства от БП (, таблица 2, ). 4,5
И наоборот, пациенты с паркинсонизмом и деменцией обычно испытывают спонтанные зрительные галлюцинации, бред и паранойю даже при отсутствии лекарств от двигательной дисфункции. Введение дофаминергической терапии часто вызывает или обостряет лежащую в основе склонность к психозу у пациентов с деменцией с тельцами Леви или деменцией при болезни Паркинсона. 6
Пациентов с БП и их опекунов следует регулярно опрашивать на предмет наличия галлюцинаций или ненормальных представлений. Члены семьи часто удивляются, узнав, что их любимый человек испытывает зрительные галлюцинации, потому что многие пациенты с БП не хотят разглашать эту информацию, если их специально не попросят, из страха показаться сумасшедшими. Также важен скрининг пациентов с БП и лиц, ухаживающих за ними, на предмет наличия нарушений контроля над импульсами, таких как чрезмерное увлечение азартными играми, аномальные сексуальные интересы и расточительное поведение, связанное с расходами.Нарушения импульсного контроля обычно остаются невыявленными, если только опытный клиницист специально и усердно не осмотрит их. Психоз и расстройства контроля над импульсами — частые психиатрические осложнения дофаминергической терапии, которые могут иметь серьезные последствия, если их не диагностировать или не лечить.
Хотя доброкачественные галлюцинации / ощущение присутствия не обязательно перерастают в тяжелые галлюцинации или откровенный психоз (галлюцинации, бред), наличие этого феномена у пациентов с БП, которые в остальном чувствуют себя хорошо, должно побуждать врачей проявлять особую осторожность и бдительность при увеличении. дофаминергическая дозировка или добавление новых лекарств.
Галлюцинаторные переживания при БП становятся все более яркими и пугающими по мере того, как симптомы перерастают в психоз. Заблуждения о супружеской неверности, подозрения о вредных заговорах и обвинения в финансовых нарушениях — обычная триада, с которой сталкиваются пациенты с психозами, сопровождающими паркинсонические расстройства. Психотические симптомы могут возникать рано после начала лечения БП, но гораздо реже, чем на более поздних стадиях заболевания. 4,5
Плюсы и минусы медикаментозного лечения
Антихолинергические препараты (например, тригексифенидил, бензтропин) и агонисты дофамина (например, прамипексол, ропинирол, ротиготин) с большей вероятностью вызывают галлюцинации и психоз, чем карбидопатия. леводопа.Риск психоза меняется в зависимости от дозы несколько непредсказуемым образом. Некоторые пациенты (особенно с деменцией) обладают повышенной чувствительностью, и симптомы развиваются при очень низких дозах. Другие хорошо переносят начальное лечение, но психоз развивается по мере увеличения дозировки. Комбинации противопаркинсонических препаратов и одновременный прием других психоактивных препаратов (например, наркотических анальгетиков, миорелаксантов, бензодиазепинов, холинолитиков) значительно повышают риск психоза и делирия.
Карбидопа / леводопа — наиболее эффективный (и наименее дорогой) препарат для лечения моторных симптомов БП. Практически всем пациентам с БП в конечном итоге потребуется терапия карбидопой / леводопой для облегчения двигательных симптомов в течение болезни. Нет веских причин для использования нескольких лекарств, если двигательные симптомы можно успешно лечить с помощью монотерапии карбидопой / леводопой.
Большинству пациентов с БП не нужны агонисты дофамина, антихолинергические агенты, амантадин и другие вспомогательные агенты, такие как ингибиторы моноаминоксидазы типа B (MAO-B) и ингибиторы катехол O -метилтрансферазы (COMT).Эти препараты повышают риск нейропсихиатрических побочных эффектов, и их следует особенно избегать у пациентов с деменцией с тельцами Леви или деменцией при болезни Паркинсона, у которых уже есть предрасположенность к галлюцинациям и психозам. 7
Функция холинергических нейронов головного мозга нарушена в большей степени у пациентов с деменцией с тельцами Леви или деменцией при болезни Паркинсона, чем у пациентов с болезнью Альцгеймера. Антихолинэстеразные препараты ривастигмин и донепезил незначительно улучшают познавательные способности у некоторых пациентов.Полученные данные свидетельствуют о том, что антихолинэстеразные препараты облегчают легкие галлюцинации и могут снизить риск явного психоза. 8,9
Колеблющиеся реакции моторных симптомов
По мере прогрессирования болезни Паркинсона с годами леводопа остается эффективной, но, к сожалению, продолжительность положительного эффекта сокращается. Таким образом, у пациентов, страдающих БП в течение нескольких лет, обычно развиваются двигательные флуктуации, при этом в течение части дня их двигательные симптомы относительно смягчаются; а в других случаях, когда действие лекарства ослабевает или проходит, возникает неприятная неподвижность, скованность и тремор.
Первоначально двигательные колебания отмечаются в конце периода приема карбидопы / леводопы и проходят через 30–60 минут после приема следующей дозы. Однако со временем периоды отсутствия пользы становятся более частыми и менее предсказуемыми. Помимо классических моторных симптомов паркинсонизма, эти периоды «выключения» могут сопровождаться дистонией, сильной болью, тревогой и значительным эмоциональным расстройством.
Определение подходящего интервала времени между дозами карбидопы / леводопы и приемом лекарства натощак (для обеспечения оптимального всасывания и доступности) имеет решающее значение для пациентов с БП с двигательными колебаниями.Тем не менее, многие пациенты с БП с колеблющимися ответами не могут надежно предсказать, когда они будут «включены» или «выключены»; эта неопределенность приводит к значительной инвалидности и отказу от нормального социального взаимодействия.
При ведении пациента с БП с выраженными двигательными колебаниями клиницисты часто используют комбинации (например, карбидопа / леводопа плюс агонисты дофамина, амантадин, ингибиторы СОМТ, ингибиторы МАО-В) и более высокие дозы лекарств. Такой подход часто бывает полезным. Однако повышение доз леводопы в сочетании с дополнительными агентами для контроля двигательных колебаний обычно приводит к побочным эффектам, включая невыносимые дискинезии, синдром дисрегуляции дофамина, нарушения импульсивного контроля или психоз. 1
Ведение психоза при БП с деменцией является сложной задачей (, таблица 3, ). У этих пациентов следует попытаться сократить использование комбинированной терапии с агонистами дофамина, холинолитиками, амантадином, ингибиторами МАО-В и ингибиторами СОМТ. 10
CASE VIGNETTE
Тремор и скованность развиваются в левой ноге 49-летней женщины, которая в анамнезе страдала тревогой и паническими атаками; диагноз — БП.В анамнезе у нее не было нейролептиков, токсинов или других вторичных причин паркинсонизма. Она лечится карбидопой / леводопой, энтакапоном и клоназепамом, и в течение нескольких лет она чувствует себя хорошо. Через пять лет после начала болезни Паркинсона смерть в семье вызывает депрессию. В этот период ее двигательные симптомы ухудшаются, и к ней добавляются агонист дофамина (ропинирол) и селегилин.
В течение следующего года ее личность меняется, она становится все более раздражительной и начинает вести себя странно; она заблуждается, ложно обвиняя мужа в неверности.Она ведет беспорядочную половую жизнь и начинает легкомысленно тратить деньги. Она расстается с мужем. Ее осматривает психиатр и ненадолго госпитализирует. В дополнение к обычным лекарствам от БП она получает пароксетин, клоназепам, литий и рисперидон. Ее дрожь и скованность усиливаются. Лечащий врач увеличивает дозу ропинирола с 6 до 12 мг в день, и в конечном итоге прием рисперидона прекращается. После выписки она переезжает жить к сыну.
Пациент направлен на второе неврологическое заключение; диагноз — психоз и нарушения контроля над импульсами, которые являются следствием дофаминергической терапии, используемой для лечения БП.Энтакапон и селегилин прекращены; ропинирол постепенно снижается и прекращается. Пациент получает лечение карбидопой / леводопой 25 мг / 100 мг перед едой и перед сном, что контролирует двигательные симптомы. Перед сном добавляют кветиапин 25 мг, и она продолжает принимать клоназепам по 0,5 мг 3 раза в день. В течение следующих 9 месяцев галлюцинации и иллюзии прекращаются, а проблемы с контролем над импульсами уменьшаются.
В 1970-х и начале 1980-х годов практика наркологических каникул, когда все противопаркинсонические препараты (включая карбидопу / леводопу) резко прекращались на несколько дней, иногда использовалась для лечения пациентов с БП и витальным психозом.Бред и галлюцинации часто разрешались, но перерыв в лечении трагически приводил к развитию синдрома паркинсона и гиперпирексии (опасное для жизни заболевание, напоминающее злокачественный нейролептический синдром). 11 Резкое прекращение приема леводопы у пациентов с длительной БП опасно. Снижение дозировки леводопы следует проводить медленно — не более чем на 25–30% за раз.
Диапазон доз леводопы широк, и существует значительная разница в восприимчивости к психиатрическим и непсихиатрическим побочным эффектам (таким как сонливость и дискинезия).Задача врача — найти наименьшую дозу карбидопы / леводопы, которая облегчает двигательные симптомы, и назначать эту дозу через соответствующие промежутки времени в течение дня (и в ночное время, если необходимо). Более высокие индивидуальные дозы леводопы имеют больше потенциальных побочных эффектов и не действуют дольше. 7
Перенастройка лечения БП не всегда помогает уменьшить галлюцинации и бред у пациентов, особенно если у пациента скорее деменция с тельцами Леви или деменция, связанная с болезнью Паркинсона, чем БП.В других случаях сокращение приема лекарств может улучшить психическое состояние, но сопровождается невыносимым ухудшением моторных симптомов паркинсонизма. Добавление антипсихотического средства оправдано для контроля явного психоза, который не улучшается при корректировке лекарства, или для предотвращения рецидива психоза, поскольку дозы леводопы осторожно увеличиваются для восстановления двигательной функции.
Нейролептики
Нейролептики первого поколения являются эффективными антипсихотическими средствами, но они имеют значительный риск индукции паркинсонизма или обострения двигательных симптомов у пациентов с БП, деменцией с тельцами Леви или деменцией при болезни Паркинсона.Однако многие психиатры ошибочно полагают, что это не относится к нейролептикам второго поколения. К сожалению, они также несут значительный риск лекарственного паркинсонизма и ухудшения двигательных симптомов. 12,13 Риск побочных эффектов паркинсонизма четко не связан с дозой или продолжительностью терапии нейролептиками. В целом, следует избегать приема нейролептиков у пациентов с психозом с паркинсоническими расстройствами, за исключением клозапина и кветиапина.
Единственными доступными в настоящее время нейролептиками, которые не вызывают паркинсонизм, вызванный наркотиками и не вызывают ухудшения двигательных симптомов, являются кветиапин и клозапин. шизофрения. У пациентов с БП и психозом кветиапин обычно начинают с 12,5 или 25 мг перед сном, и дозу постепенно титруют по мере необходимости (большинству пациентов требуются дозы от 25 до 100 мг / сут).
При БП, деменции с тельцами Леви и деменции при болезни Паркинсона начальная доза клозапина обычно составляет 6,25 или 12,5 мг / сут; Пациентам обычно требуется не более 25–50 мг / сут. 6,12 Основная вегетативная дисфункция, которая сопровождает БП, деменцию с тельцами Леви и деменцию при болезни Паркинсона, увеличивает восприимчивость к значительной ортостатической гипотензии при применении этих препаратов.
Эффективность клозапина без побочных двигательных эффектов у пациентов с БП и психозом была хорошо установлена в двойных слепых контролируемых исследованиях. 15 Несмотря на продемонстрированную пользу при психозах с паркинсоническими расстройствами, использование клозапина ограничено из-за седативного эффекта, ортостатической гипотензии, удлинения интервала QTc и, что наиболее важно, риска агранулоцитоза. В нескольких открытых исследованиях сообщалось, что кветиапин снижает психоз при БП без ухудшения двигательных симптомов, но седативный эффект и гипотензия также ограничивают переносимость. Двойные слепые контролируемые исследования подтвердили, что кветиапин не ухудшает двигательные симптомы у пациентов с БП, но не смогли продемонстрировать эффективность против психоза в этой популяции. 16
Необходимость частого гематологического мониторинга заставила большинство клиницистов неохотно использовать клозапин в качестве терапии первой линии при психозах с паркинсоническими расстройствами. Следовательно, кветиапин обычно используется первоначально, когда требуется нейролептик. Однако пациенты с БП и выраженным психозом, у которых не улучшается состояние кветиапина, должны быть немедленно переведены на клозапин. 12 Еженедельный гематологический мониторинг, безусловно, является разумным компромиссом, если он может предотвратить нарушения социальной сферы пациента или предотвратить необходимость помещения пациента в лечебное учреждение.
CASE VIGNETTE
Левосторонний тремор в покое, брадикинезия, шаркающая походка, микрофотография и гипомимия развиваются у 69-летнего мужчины. Нет данных об использовании нейролептиков или других вторичных причин паркинсонизма. Диагноз — БП, начата монотерапия карбидопой / леводопой 25 мг / 250 мг. Дозу постепенно увеличивают до 3 раз в день, и наблюдается заметное улучшение экстрапирамидных моторных симптомов.
Примерно через 6 лет после начала болезни Паркинсона очевидно, что он становится забывчивым; и хотя он апатичен, он не подавлен.Монотерапия карбидопой / леводопой продолжается для контроля двигательных симптомов или исчезновения между дозами. Он признает, что иногда видит вечером лица или людей, но понимает, что это галлюцинации, и отрицает связанный с этим стресс.
В течение следующих 2 лет его потеря памяти ухудшается, и он часто дезориентируется. Его диагноз — деменция при болезни Паркинсона. Зрительные галлюцинации усиливаются и становятся все более яркими и угрожающими. Он несколько раз звонит в полицию, потому что видит людей в своей спальне, и его поведение становится все более неуправляемым.
Снижают дозу до 2 таблеток карбидопа / леводопа 25 мг / 100 мг 3 раза в сутки, а затем до 1,5 таблеток 3 раза в сутки. Его галлюцинации стали менее тревожными, и он стал намного спокойнее. К сожалению, с уменьшением дозировки у него ухудшаются двигательные симптомы БП, и он несколько раз падает.
Кветиапин начинает уменьшать психотические симптомы, но обладает чрезмерно седативным действием и неэффективен. Кветиапин заменяют клозапином, дозу которого перед сном дозируют до 25 мг.Галлюцинации и бред резко уменьшаются, и он снова может переносить дозу, принимаемую 3 раза в день. Его двигательная функция улучшается, он может встать со стула без посторонней помощи и продолжить ходить с ходунками. К счастью, контроль психоза с помощью клозапина позволяет ему продолжать жить дома с женой и помощницей по совместительству.
Заключение
Сообщения, в которых отмечается повышенная смертность пожилых пациентов с деменцией, получающих антипсихотические препараты, вызывают потенциальные опасения относительно безопасности. 17 Как показано во втором эпизоде, инвалидность и дистресс, вызванные психозом с паркинсоническими расстройствами, перевешивают риск лечения. Необходимы более безопасные и эффективные методы лечения. Общество по борьбе с двигательными расстройствами активно занимается разработкой достоверных критериев оценки результатов клинических испытаний. 18 FDA в настоящее время оценивает исследования нового класса лекарств (селективные обратные агонисты серотонина 5HT-2A), которые могут быть полезными. 19
Раскрытие информации:
Д-р Вайс является директором программы борьбы с болезнью Паркинсона в больнице Синай в Балтиморе и доцентом неврологии Медицинской школы Университета Джона Хопкинса в Балтиморе.Д-р Адлер — заведующий психиатрической больницей Lifebridge Health в Балтиморе. Он не сообщает об отсутствии конфликта интересов относительно предмета этой статьи.
Ссылки:
1. Weiss HD, Marsh L. Расстройства контроля импульсов и компульсивное поведение, связанные с дофаминергической терапией при болезни Паркинсона. Нейрол Клин Практик . 2012; 2: 267-273.
2. Вайнтрауб Д., Burn DJ. Болезнь Паркинсона: типичное психоневрологическое расстройство. Движение Дисорд . 2011; 26: 1022-1031.
3. Мак Дж., Рабинс П., Андерсон К. и др. Распространенность психотических симптомов в выборке из местных сообществ. Am J Гериатр Психиатрия . 2012; 20: 123-132.
4. Морганте Л., Колозимо С., Антонини А. и др .; Исследовательская группа ПРИАМО. Психоз, связанный с болезнью Паркинсона на ранних стадиях: актуальность снижения когнитивных функций и депрессии. J Neurol Neurosurg Psychiatry . 2012; 83: 76-82.
5. Ли А.Х., Вайнтрауб Д. Психоз при болезни Паркинсона без деменции: общие и коморбидные с другими немоторными состояниями. Движение Дисорд . 2012; 27: 858-863.
6. Friedman JH. Болезнь Паркинсона с психозом: обновленная информация. Поведение Neurol . 2012; 27: 469-477.
7. Ahlskog JE. Деменция с тельцами Леви и деменция при болезни Паркинсона . Нью-Йорк: издательство Оксфордского университета; 2014.
8. Савада Х., Оэда Т., Ямамото К. и др. Триггерные механизмы и связанные с пациентом факторы риска психоза при болезни Паркинсона, требующие применения антипсихотических препаратов: ретроспективное когортное исследование. БМС Нейрол . 2013; 13: 145-150.
9. Ридинг П.Дж., Люс А.К., МакКейт И.Г. Ривастигмин в лечении паркинсонических психозов и когнитивных нарушений: открытое испытание. Движение Дисорд . 2001; 16: 1171-1174.
10. Томсен Т.Р., Паниссет М., Суховерски О. и др.Влияние стандарта медицинской помощи при психозе при болезни Паркинсона. J Neurol Neurosurg Psychiatry . 2008; 79: 1413-1415.
11. Ньюман Э.Дж., Гроссет Д.Г., Кеннеди П.Г. Синдром паркинсонизма-гиперпирексии. Нейрокрит Уход . 2009; 10: 136-140.
12. Фридман Дж. А., Фактор С.А. Атипичные нейролептики в лечении лекарственного психоза при болезни Паркинсона. Движение Дисорд . 2000; 15: 201-211.
13. Ричард И. Х., Натт Дж.Ухудшение двигательной функции при болезни Паркинсона: «типичный» ответ на «атипичные» антипсихотические препараты. Неврология . 2000; 55: 748-749.
14. Миясаки Дж. М., Шеннон К., Вун В. и др .; Подкомитет по стандартам качества Американской академии неврологии. Параметр практики: оценка и лечение депрессии, психоза и деменции при болезни Паркинсона: обзор, основанный на фактах. Неврология . 2006; 66: 996-1002.
15. Группа изучения болезни Паркинсона.Клозапин в низких дозах для лечения психоза, вызванного лекарственными препаратами, при болезни Паркинсона. N Engl J Med . 1999; 340: 757-763.
16. Рабей Ю.М., Прохоров Т., Миниовиц А.

 The changing face of Parkinson’s disease-associated psychosis: a cross-sectional study based on the new NINDS-NIMH criteria. Mov Disord 2010;25(6):763-766. https://doi.org/10.1002/mds.22839
The changing face of Parkinson’s disease-associated psychosis: a cross-sectional study based on the new NINDS-NIMH criteria. Mov Disord 2010;25(6):763-766. https://doi.org/10.1002/mds.22839 https://doi.org/10.1038/nrn.2017.91
https://doi.org/10.1038/nrn.2017.91 Park Relat Disord. 2008;14(1):37-42. https://doi.org/10.1016/j.parkreldis.2007.05.009
Park Relat Disord. 2008;14(1):37-42. https://doi.org/10.1016/j.parkreldis.2007.05.009 Psychiatric comorbidities in patients with Parkinson disease and psychosis.
Psychiatric comorbidities in patients with Parkinson disease and psychosis.
 Arch Neurol. 2006;63:713-716.
Arch Neurol. 2006;63:713-716.
 2006;15:339-349.
2006;15:339-349. Retinal involvement in dementia with Lewy bodies: a clue to hallucinations? Ann Neurol. 2003;54:542-547.
Retinal involvement in dementia with Lewy bodies: a clue to hallucinations? Ann Neurol. 2003;54:542-547. 2010;257:1154-1159.
2010;257:1154-1159.
 2000;12:319-334.
2000;12:319-334.
 Reducing clozapine-related morbidity and mortality: 5 years of experience with the Clozaril National Registry. J Clin Psychiatry. 1998;59:3-7.
Reducing clozapine-related morbidity and mortality: 5 years of experience with the Clozaril National Registry. J Clin Psychiatry. 1998;59:3-7. Mov Disord. 2005;20:958-963.
Mov Disord. 2005;20:958-963. Clin Neuropharmacol. 2005;28:185-187.
Clin Neuropharmacol. 2005;28:185-187. 2012;27:803-804.
2012;27:803-804.
 2005;20:203-205.
2005;20:203-205. Cholinesterase inhibition in Parkinson’s disease. J Neurol Neurosurg Psychiatry. 1996;61:324-325.
Cholinesterase inhibition in Parkinson’s disease. J Neurol Neurosurg Psychiatry. 1996;61:324-325.
 Люди с болезнью Паркинсона, как правило, плохо говорят, поэтому логопед необходим для улучшения речи.
Люди с болезнью Паркинсона, как правило, плохо говорят, поэтому логопед необходим для улучшения речи. Агонисты дофамина используется на ранних стадиях болезни Паркинсона, потому что побочные эффекты не такие сильные леводопа. Примеры препаратов-агонистов дофамина: прамипексол, ротиготин, а также ропинироль.
Агонисты дофамина используется на ранних стадиях болезни Паркинсона, потому что побочные эффекты не такие сильные леводопа. Примеры препаратов-агонистов дофамина: прамипексол, ротиготин, а также ропинироль.
 Например, скажите: «Я выведу кошку на улицу» вместо того, чтобы утверждать, что кошки нет.
Например, скажите: «Я выведу кошку на улицу» вместо того, чтобы утверждать, что кошки нет.
 Однако, увеличивая выработку дофамина, эти лекарства могут непреднамеренно вызвать серьезные эмоциональные и поведенческие изменения.
Однако, увеличивая выработку дофамина, эти лекарства могут непреднамеренно вызвать серьезные эмоциональные и поведенческие изменения.