Инфаркт миокарда лечение в стационаре сколько дней: Реабилитация и восстановление после инфаркта
Лечение инфаркта миокарда в Красноярске
Мы часто и по разным поводам слышим фразу «сердечный приступ (heart attack)«, но что на самом деле скрывается за ней? Любой поисковик перенаправит и выдаст суровый диагноз «инфаркт миокарда». Этот действительно страшный недуг с каждым годом лечат всё более и более успешно. Живущим в Красноярске определенно повезло в том, что в нашем городе лечение острого инфаркта миокарда организованно на самом современном уровне с использованием последних достижений высоких технологий в медицине. Вклад в лечение инфаркта миокарда в Красноярске вносят ВСЕ лечебные учреждения — больницы, поликлиники, частные клиники. В чём заключается вклад «Центра Современной Кардиологии» в лечение острого инфаркта миокарда в Красноярске?Отделение кардиотелеметрии позволяет выявить инфаркт с помощью ЭКГ по телефону, отделение кардиореабилитации проводит необходимый комплекс мероприятий по возвращению человека, перенесшего инфаркт миокарда, к обычной жизни, а
 Читайте, коротко — о лечении инфаркта миокарда в Красноярске.
Читайте, коротко — о лечении инфаркта миокарда в Красноярске.Так выглядит инфаркт на ЭКГI.Инфаркт. Что делать?
Что делать если у Вас или Ваших родных и близких появилась жгучая, давящая боль в груди отдающая (иррадиирующая) в челюсть, шею, левую руку, левое плечо, спину; холодный липкий пот; чувство страха смерти? Боль может появиться в покое или при физической нагрузке, сопровождаться одышкой, рвотой, ощущением перебоев в работе сердца.
Первое: обеспечить покой — положить, расстегнуть сдавливающую одежду, обеспечить поступление свежего воздуха.
Второе: дать рассосать одну-две таблетки нитроглицерина, либо брызнуть под язык одну-две дозы нитроспрея.
Третье: если через 7-10 минут после приема нитроглицерина боль не прошла — вызвать «Скорую помощь» и, затем, помочь прибывшим врачам погрузить заболевшего в автомобиль.
Всё это желательно сделать в первые шесть часов от развития первого приступа.
 Чем раньше пациенту будет оказана специализированная помощь —
тем лучше прогноз.
Чем раньше пациенту будет оказана специализированная помощь —
тем лучше прогноз.II. Этапы лечения — «скорая», стационар
Врачи «скорой» записывают кардиограмму, вводят препараты для обезболивания, нитраты, проводят двойную дезагрегантную терапию (при отсутствии противопоказаний!) аспирином и клопидогрелем (или тикагрелором), вводят другие прпараты для нормализации сердечного ритма, артериального давления, пульса и осуществляют транспортировку в стационар.
В больнице пациента с инфарктом миокарда, после осмотра кардиолога, госпитализируют в реанимационное отделение или палату интенсивной терапии, записывают ЭКГ, подтверждают диагноз инфаркта кардиоспецифическими ферментами (МВ-КФК, тропонины) и обеспечивают круглосуточный мониторинг жизненных функций.
При наличии в клинике рентгеноперационной пациенту проводится экстренная коронарография, которая очень часто, заканчивается одномоментной коронарной ангиопластикой.
Нередко состояние пациента оказывается очень тяжелым и это может потребовать проведения искусственной вентиляции легких, назначения инотропных препаратов («кардиотоников»), проведения временной эндокардиальной стимуляции, внутриаортальной баллонной контрпульсации, подключения аппаратуры heart-assistant (например, ЭКМО), а в некоторых случаях — проведения
экстренного кардиохирургического вмешательства.
III. Кардиореабилитация
Через несколько дней, после стабилизации состояния, пациент переводится в специализированное кардиологическое отделение, где лечение и обследования продолжаются. Когда состояние больного позволяет выписать его из стационара, то он направляется для амбулаторного лечения к кардиологу в поликлинику по месту жительства. В связи с дефицитом кардиологов в поликлиниках, на этом этапе лечения, пациент иногда попадает в частные клиники, например в клиники «Центра Современной Кардиологии». Большинство кардиологов нашего Центра имеют опыт работы в крупных стационарах и обеспечивают необходимую преемственность лечения. Восстановление после инфаркта растягивается на несколько месяцев. Реабилитация начинается еще в больнице, где попутно с приемом лекарственных препаратов и прохождением физиотерапевтических процедур постепенно наращивается интенсивность физических упражнений: сначала ходьба по ровной поверхности, затем — по лестницам.
 Лестница — хороший тест на готовность к активной жизни. Если пациент может в среднем темпе подняться на четвертый этаж, не ощущая боль в груди или одышку, значит, восстановление проходит успешно.
Лестница — хороший тест на готовность к активной жизни. Если пациент может в среднем темпе подняться на четвертый этаж, не ощущая боль в груди или одышку, значит, восстановление проходит успешно.По окончанию амбулаторного лечения необходимо провести кардиореабилитацию, чтобы адаптировать человека к повседневной жизни. Такой комплекс лечебно-реабилитационных мероприятий проводится в специализированных кардиологических санаториях или профилакториях. В нашем Центре существует специализированное отделение кардиореабилитации, где на фоне лабораторных и функциональных исследований проводится велотренинг (или тредмил), групповая психотерапия, фитотерапия, ароматерапия и т.п.
Так проходит операция аорто-коронарного шунтирования
В некоторых случаях инфаркт миокарда завершается формированием аневризмы левого желудочка, развитием хронической сердечной недостаточности. В этом случае кардиолог направит такого пациента на консультацию к кардиохирургу для обсуждения возможности проведения операции на открытом сердце в условиях искусственного кровообращения .

На схеме: коронарные артерии и тромб в стволе левой коронарной артерии
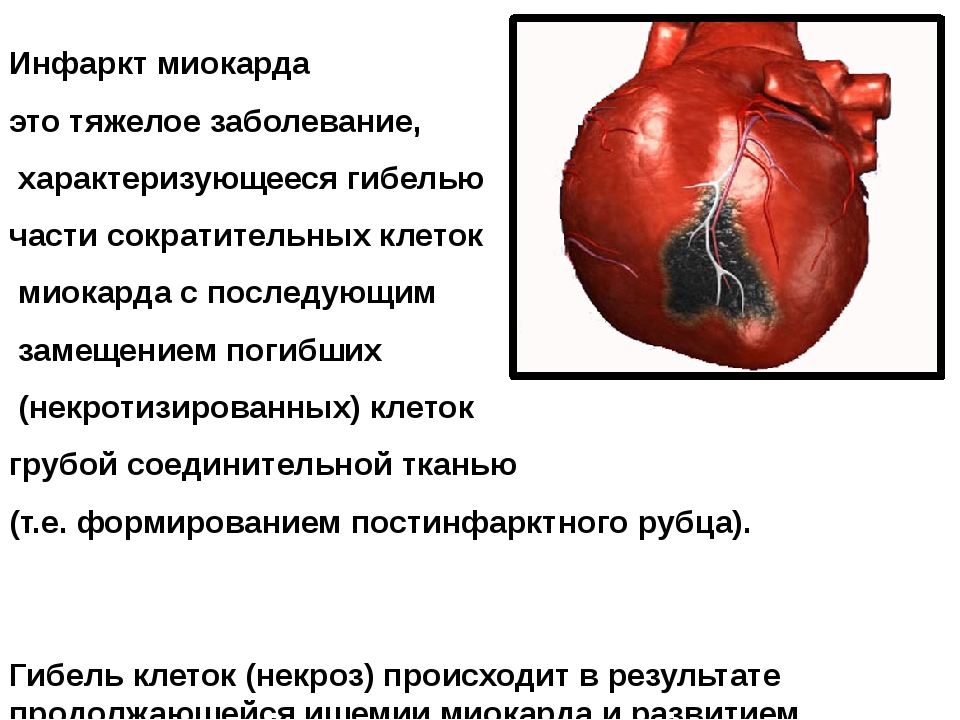
IV. Что такое инфаркт миокарда?
Инфаркт миокарда — это некроз (омертвение) участка сердца, в котором нарушено кровоснабжение. Заболевание очень распространенное (среди мужчин старше 40 лет, инфаркт, в среднем, случается у пяти из каждой тысячи) и очень опасное — смертность до 40-45%, при отсутствии лечения. Очень опасны фатальные осложнения инфаркта — кардиогенный шок, отёк легких, фибрилляция желудочков, разрыв (тампонада) миокарда, атриовентркулярная блокада, тромбоэмболические осложнения — ОНМК, мезентериальный тромбоз и т.п.
 В течение жизни в стенках коронарных артерий откладываются атеросклеротические бляшки.
В течение жизни в стенках коронарных артерий откладываются атеросклеротические бляшки.Этапы формирования атеросклеротической бляшки с развитием тромбоза коронарной артерии
Когда атеросклеротическая бляшка сужает просвет коронарной артерии на 90 и более процентов, этот участок миокарда испытывает дефицит кислорода и развивается его ишемическое повреждение. Если артерию закрывает тромб или если просвет артерии полностью зарастает атеросклеротической бляшкой, то развивается инфаркт (некроз, омертвение) такого участка миокарда. В связи с этим очень важно как можно раньше восстановить кровоток на поврежденном участке. На видео это представлено в коротком ролике:
Инфаркт миокарда различается по локализации (может быть передний, нижний, боковой, задний инфаркт левого желудочка, инфаркт правого желудочка и различные варианты сочетаний), по объему поражения (Q-wave/non-Q-wave — трансмуральный/нетрансмуральный), по анатомии (субэндокардиальный, трансмуральный, субэпикардиальный), по стадиям развития (острейший период, острый, подострый, период рубцевания).
V. Современные технологии лечения инфаркта миокарда
Для консервативного лечения инфаркта используют препараты, влияющие на свертывающую систему крови — ацетилсалициловую кислоту (аспирин), гепарин и его производные. С 80-х годов ХХ века для «растворения» тромбов в коронарных артериях используют тромболитические препараты (стрептазу, стрептокиназу, альтеплазу, метализу и т.д.). Тромболитики снизили смертность при инфаркте миокарда, но их использование ограничено в связи с высокой вероятностью развития кровотечений. С 90-х годов ХХ века для лечения инфаркта миокарда используется экстренная чрескожная транслюминальная баллонная коронарная ангиопластика (ЧТКА), которую чуть позже стали сочетать со стентированием коронарных артерий.
В таких рентгеноперационных проводятся
экстренные коронарографии и стентирование коронарных артерий
В Красноярске такой вид лечения для экстренных пациентов с 1999 года проводится в Краевой клинической больнице .
 Позднее количество клиник, в которых выполняется ЧТКА, увеличилось до пяти (ККБ, 20-я больница, БСМП, СКЦ ФМБА, ФЦ ССХ). На сегодняшний день В КРУГЛОСУТОЧНОМ РЕЖИМЕ ЭКСТРЕННЫЕ КОРОНАРНЫЕ АНГИОПЛАСТИКИ в Красноярске выполняются в Краевой больнице, БСМП и 20-й больнице. По словам министра здравоохранения Красноярского края Вадима Янина в нашем крае «летальность при остром инфаркте миокарда составила 10,4% при среднероссийском показателе 15,8%»
Позднее количество клиник, в которых выполняется ЧТКА, увеличилось до пяти (ККБ, 20-я больница, БСМП, СКЦ ФМБА, ФЦ ССХ). На сегодняшний день В КРУГЛОСУТОЧНОМ РЕЖИМЕ ЭКСТРЕННЫЕ КОРОНАРНЫЕ АНГИОПЛАСТИКИ в Красноярске выполняются в Краевой больнице, БСМП и 20-й больнице. По словам министра здравоохранения Красноярского края Вадима Янина в нашем крае «летальность при остром инфаркте миокарда составила 10,4% при среднероссийском показателе 15,8%»Этапы восстановления коронарного кровотока с помощью стента
В крае с 2016 года высокотехнологичную помощь пациентам с острым коронарным синдромом (инфаркт и связанные с ним состояния) оказывают в Ачинске и Канске .
VI. Какие факторы предрасполагают к развитию острого инфаркта миокарда?
1) Мужской пол
2) Возраст — старше 40 лет
3) Курение (в т.ч. — пассивное)
4) Злоупотребление алкоголем
5) Малоподвижный образ жизни
6) Ожирение
7) Сахарный диабет
8) Нарушение обмена холестерина (избыток «плохого» холестерина ЛПНП, недостаток «хорошего» холестерина ЛПВП, высокий уровент триглицеридов)
9) Гипертоническая болезнь (артериальная гипертензия)
10) Наличие стенокардии напряжения или перенесенного в прошлом инфаркта миокарда
11) Перенесенные стафилококковые и стрептококковые инфекции, ревмокардит (инфекционный фактор)
12) Проживание в условиях загрязненной атмосферы (экологический фактор)VII.
 Что сделать для того чтобы избежать инфаркта миокарда?
Что сделать для того чтобы избежать инфаркта миокарда? Эти рекомендации общеизвестны — вести здоровый образ жизни, соблюдать диету, поддерживать нормальный вес и соответствующий возрасту уровень физической активности, не курить, не злоупотреблять алкоголем. Но если во время физической нагрузки Вы стали отмечать появление жгучей боли за грудиной, проходящей в покое, одышки при обычном уровне физической нагрузки, то Вам необходимо обратиться к кардиологу. Кардиолог во время приема определит тактику Вашего обследования и лечения.
Как правило в обследование входит сбор анализов, запись ЭКГ, эхокардиография (УЗИ сердца), при необходимости — холтеровское мониторирование ЭКГ, суточное мониторирование артериального давления, нагрузочные пробы велоэргометрия или тредмил-тест. Если ситуация вызывает серьезные опасения, то кардиолог направит пациента на инвазивное диагностическое исследование в стационар — коронарографию, по результатам которой может быть определена дальнейшая тактика лечения (консервативная терапия, малоинвазивное вмешательство, АКШ).

Для профилактики инфаркта миокарда кардиолог может назначить некоторые препараты. Например, дезагреганты (ацетилсалициловую кислоту, клопидогрель), бета-адреноблокаторы, ингибиторы АПФ, статины (для снижения риска прогрессирования атеросклероза).
Любую болезнь проще предотвратить, чем лечить. Тем более такую тяжелую, как острый инфаркт миокарда. Не ждите до последнего — запишитесь на приём к кардиологу.
Оригинальный текст — Чупахин С.А.
#рхмдл
Как стентирование спасает при инфаркте миокарда
Инфаркт миокарда – это поражение сердечной мышцы, вызванное внезапным нарушением ее кровоснабжения из-за тромбоза (закупорки) одной из сердечных артерий. Последствия инфаркта можно свести к минимуму, если быстро восстановить кровоток в пораженном сосуде. Наиболее эффективным методом для этого является стентирование.
Из-за чего возникает и как развивается инфаркт миокарда?
В стенках сердечных артерий с возрастом образуются атеросклеротические бляшки. Бляшка уменьшает просвет сосуда, но может никак не проявлять себя до тех пор, пока не случается ее разрыв. На поврежденной бляшке за несколько минут образуется тромб, который перекрывает просвет сосуда. К участку сердечной мышцы прекращается доступ кислорода и питательных веществ. Мышечные клетки на этом участке перестают сокращаться и, если не восстановить кровообращение в течение часа, погибают. Возникает очаг омертвения (некроза). Это и есть инфаркт миокарда.
Бляшка уменьшает просвет сосуда, но может никак не проявлять себя до тех пор, пока не случается ее разрыв. На поврежденной бляшке за несколько минут образуется тромб, который перекрывает просвет сосуда. К участку сердечной мышцы прекращается доступ кислорода и питательных веществ. Мышечные клетки на этом участке перестают сокращаться и, если не восстановить кровообращение в течение часа, погибают. Возникает очаг омертвения (некроза). Это и есть инфаркт миокарда.
Как проявляется инфаркт миокарда?
Главный симптом инфаркта миокарда — сильная боль за грудиной. Она может распространяться на левую руку, плечо, шею, проявляться в спине. Часто боль сопровождается страхом. Вот как описывает свои ощущения один из пациентов: «Представьте себе, что вы разом проглотили половину твердого зеленого яблока. Кусок застрял на полпути — ни туда, ни сюда. И это очень больно, потому что распирает». Иногда инфаркт миокарда проявляется нетипичными симптомами: острой болью в животе, приступом астмы, спутанностью сознания и речи.
Что делать при подозрении на инфаркт миокарда?
Немедленно вызвать cкорую медицинскую помощь. Самый эффективный метод лечения острого инфаркта миокарда — стентирование — можно выполнять только в стационаре с сосудистым отделением, куда больного нужно доставить как можно скорее.
При стентировании к закупоренной сердечной артерии в сжатом виде доставляют сетчатую металлическую трубочку – стент. В месте тромбоза стент расширяют.
В расправленном виде стент восстанавливает нормальный кровоток в сосуде и не дает его стенкам вновь сомкнуться. К пораженному участку сердечной мышцы начинают поступить кислород и питательные вещества — развитие инфаркта останавливается. Всю операцию проводят под местным наркозом, через небольшой прокол в артерии на ноге или руке. Чем раньше сделать стентирование при инфаркте миокарда, тем меньше пострадает сердечная мышца.
Термины, которые часто используют врачи
Распространенное выражение «инфаркт миокарда» знакомо многим, но сейчас врачи при первичной диагностике и выборе лечения чаще используют термин
«острый коронарный синдром» (ОКС). Он включает в себя два диагноза: нестабильная стенокардия и собственно инфаркт миокарда.
Нестабильная стенокардия проявляется внезапной болью в сердце и может быть предвестником инфаркта. Об инфаркте миокарда говорят, когда уже наступило поражение сердечной мышцы.
ОКС проявляется в двух основных формах: ОКС с подъемом сегмента ST на электрокардиограмме, который в большинстве случаев заканчивается инфарктом миокарда, и ОКС без подъема сегмента ST, который может проявляться и как как инфаркт миокарда, и как нестабильная стенокардия.
Об опасности инфаркта и эффективности коронарного стентирования
Что мы знаем об инфаркте? О том, что это тяжелое, смертельно опасное состояние, слышали практически все. В относительно недавнем прошлом спасение жизни человека с обширным инфарктом считалось поистине замечательным итогом лечения, а при самом благоприятном течении заболевания это были долгие месяцы строгого режима, медленное восстановление, потеря трудоспособности.
КОНСТАНТИН АЛЕКСЕНДРОВИЧ КИРЕЕВ, руководитель Центра рентгенэндоваскулярных диагностки и лечения об опасности инфаркта и эффективности коронарного стентирования:
— В первую очередь, необходимо понимать, что представляет собой острый инфаркт миокарда. Это некроз, то есть отмирание участка сердечной мышцы, развивающийся в результате внезапного, остро возникшего нарушения кровотока в системе коронарной (относящейся к сердцу) артерии. Закупорка ветви коронарной артерии может быть вызвана ее тромбозом, реже эмболией или длительным (более получаса) стойким спазмом.
Закупорка ветви коронарной артерии может быть вызвана ее тромбозом, реже эмболией или длительным (более получаса) стойким спазмом.
Наиболее частой причиной инфаркта становится атеросклероз, когда на стенках сосудов происходит образование атеросклеротических бляшек: они сужают просвет коронарных артерий, а также могут способствовать разрушению их стенок, что провоцирует образование тромбов и закупорку.
Острый инфаркт вызывает необратимые изменения в сердечной мышце: гибель части функциональных мышечных клеток сердца (некроз) и последующее их замещение соединительной тканью, то есть формирование постинфарктного рубца. Рубец на миокарде остается на всю жизнь. Рассосаться он не может, и о перенесенном инфаркте сердце помнит всегда. Впоследствии нарушение кровоснабжения миокарда может привести к расстройству сердечной деятельности: развивается сердечная недостаточность, т. е, сердце не выполняет своих функций в полном объеме,
соответственно, для полноценного существования всего организма попросту не хватает «мощности».
Говоря простым языком, из-за острого нарушения кровообращения сердце постепенно начинает «умирать», и чтобы спасти человеку жизнь, как можно скорее необходимо восстановить кровообращение. При несвоевременном оказании медицинской помощи человек с инфарктом может погибнуть в течение первых суток. В целом прогноз исхода инфаркта зависит от величины очага поражения миокарда, тяжести течения, возраста больного, развития осложнений. Но в любом случае на прогноз заболевания влияет своевременность начала лечения и его адекватность.
В Челябинской области ежегодно регистрируется свыше 5000 инфарктов миокарда, и по-прежнему это заболевание остается одной из основных причин преждевременной смерти. Долгое время в лечении острого инфаркта в нашей области действовала далеко не самая передовая стратегия. По показаниям проводилась тромболитическая терапия, то есть введение препаратов, рассасывающих тромб и восстанавливающих проходимость сосуда. Такая помощь оказывалась и бригадами скорой медицинской помощи до госпитализации, и в реанимационных отделениях стационаров. Успех лечения зачастую зависел от правильно выбранного препарата, своевременности начала его применения. Безусловно, о высокой эффективности лекарственной терапии не было и речи: очень высокий процент летальных исходов (около 16−20%), а если человек оставался жив, то становился инвалидом, его сердце не могло работать должным образом.
Успех лечения зачастую зависел от правильно выбранного препарата, своевременности начала его применения. Безусловно, о высокой эффективности лекарственной терапии не было и речи: очень высокий процент летальных исходов (около 16−20%), а если человек оставался жив, то становился инвалидом, его сердце не могло работать должным образом.
Ситуация принципиально изменилась в 2011 году, когда в рамках программы модернизации здравоохранения в Челябинске начали выполнять экстренные операции при острых инфарктах миокарда — чрескожные коронарные вмешательства, в том числе стентирование коронарных артерий. Это был бесспорный прорыв для челябинского здравоохранения.
Коронарное стентирование является самым эффективным способом лечения острого инфаркта миокарда за счет полноценного устранения нарушений кровообращения путем прямого и непосредственного воздействия на инфаркт. Суть метода заключается в том, чтобы в пораженный сосуд через лучевую артерию (на запястье) установить специальный стент с целью восстановления кровотока. Стент — это металлическая сетчатая конструкция, напоминающая полую трубку маленького диаметра. С помощью специального баллона стент в сложенном виде заводится в артерию, под контролем рентген-аппарата доставляется в место сужения сосуда, затем при раздувании баллона под давлением расправляется и имплантируется, расширяя и поддерживая пораженный сосуд в области закупорки или критического сужения и восстанавливая кровоток. Также для того, чтобы сделать вмешательство наиболее эффективным и безопасным, применяется широкий спектр специальных препаратов.
Стент — это металлическая сетчатая конструкция, напоминающая полую трубку маленького диаметра. С помощью специального баллона стент в сложенном виде заводится в артерию, под контролем рентген-аппарата доставляется в место сужения сосуда, затем при раздувании баллона под давлением расправляется и имплантируется, расширяя и поддерживая пораженный сосуд в области закупорки или критического сужения и восстанавливая кровоток. Также для того, чтобы сделать вмешательство наиболее эффективным и безопасным, применяется широкий спектр специальных препаратов.
Преимущества стентирования заключаются еще и в том, что эта операция малотравматична, практически безболезненна, имеет малое количество осложнений, позволяет сократить длительность пребывания в стационаре с 15−17 до 7−11 дней, делает возможной раннюю активность пациента и направление его на реабилитацию в санаторно-курортных условиях.
Благодаря стентированию при острых инфарктах миокарда летальность снизилась почти вдвое, и на сегодняшний день составляет около 6%. Но самое главное, что после инфаркта пациент может вернуться к нормальной, полноценной жизни, к своей работе.
Но самое главное, что после инфаркта пациент может вернуться к нормальной, полноценной жизни, к своей работе.
КОММЕНТАРИЙ ЕВГЕНИЯ МИХАЙЛОВА, главного внештатного кардиолога Южно-Уральской дирекции здравоохранения, кандидата медицинских наук:
— При инфаркте в первые три часа погибает примерно половина толщины сердечной мышцы, в следующие три часа мышца погибает на всю толщину. Поэтому стентирование в остром периоде инфаркта миокарда эффективно, если оно проведено как можно раньше, не позже первых 6 часов от момента развития инфаркта, оптимально — до 2−3 часов. Восстановление кровотока в закупорившейся артерии в этом временном промежутке, до развития необратимых изменений в миокарде, резко уменьшает площадь инфаркта, а иногда позволяет «оборвать» его развитие. Когда же мы вмешиваемся уже по истечении этих 6 часов, мы можем только уменьшить площадь некроза, но не спасти от инфаркта миокарда. Из-за того, что пациенты поступают к нам слишком поздно, половина из них не выживает.
Здесь очень многое зависит от того, как быстро больной или его родственники вызовут бригаду скорой помощи. Люди должны знать клинические проявления инфаркта миокарда. Если внезапно появились сильные, как правило, пугающие боли за грудиной, которые не снимаются приемом нитроглицерина, — медлить нельзя, срочно вызывайте «скорую». Таким образом, первая помощь будет оказана уже на месте: бригада проводит интенсивную терапию для купирования болей и растворения тромба, в максимально сжатые сроки доставит в стационар. Но еще раз повторю, самое главное — вызвать «скорую помощь» вовремя!
О работе рентген-хирургической службы
Четыре дня в неделю мы принимаем пациентов из 4 районов Челябинска и 7 муниципальных образований Челябинской области, это население 700 тысяч человек.
На сегодняшний день для Дорожной клинической больницы чрескожные коронарные вмешательства — одно из приоритетных направлений работы. Нужно отметить, что неотложную помощь мы оказываем всем без исключения, а не только прикрепленным гражданам. Среди больниц сети здравоохранения «РЖД-Медицина» от Калининграда до Хабаровска у нас самый большой объем экстренных операций коронарного стентирования.
Среди больниц сети здравоохранения «РЖД-Медицина» от Калининграда до Хабаровска у нас самый большой объем экстренных операций коронарного стентирования.
Мы заинтересованы в том, чтобы пациент, который к нам приехал больным, вышел от нас относительно здоровым, относительно быстро, чтобы он мог вернуться в строй с минимальной потерей качества жизни. К этому прилагаются все усилия. Очень четко отлажены все действия медицинского персонала для скорейшего определения тактики лечения — от приемного отделения до поступления больного в рентгеноперационную или реанимацию. Мы не просто стремимся к тому, чтобы оказывать эту помощь как можно быстрее, но и имеем для этого все возможности.
Эффективным результатам способствует и то, что практическая работа всегда ведется в тесной связке с наукой. На базе дорожной больницы работают две основные кафедры Южно-Уральского государственного медицинского университета, что означает внедрение современных технологий в лечебный процесс, непрерывное повышение квалификации специалистов, обеспечение консультативной помощью, совместный анализ проводимого лечения, клинических случаев.
Свою работу всегда нужно оценивать в соответствии с мировыми стандартами, чтобы можно было понять, хорошо мы работаем или плохо. Так, считается, что медицинская организация работает хорошо, когда у 70% пациентов с инфарктами выполняются операции коронарного стентирования. У нас в 2017 г. этот показатель равнялся 76%. По моему мнению, сегодня для спасения жизни и сохранения здоровья людей делается все, что нужно.
Как не «дожить до инфаркта»
Существуют основные факторы риска, которые могут привести к развитию инфаркта миокарда. На некоторые из них мы можем воздействовать, на другие — нет. Нельзя повлиять, к примеру, на пол (мужчины более подвержены ишемической болезни сердца), возраст, семейный анамнез, наследственную предрасположенность. Однако мы можем существенно ослабить неблагоприятное действие таких факторов, как артериальная гипертензия, курение, сахарный диабет, повышенный уровень холестерина, избыточный вес, малоподвижный образ жизни. Все эти факторы, как в совокупности, так и каждый самостоятельно провоцируют развитие атеросклероза, который, как я уже говорил, и является основной причиной инфаркта миокарда.
Мы проводили исследование медико-социального статуса, качества жизни, наличия факторов риска атеросклероза в группе пациентов с диагнозом «инфаркт миокарда». В анкетировании принимали участие 200 человек, все жители г. Челябинска, в возрасте до 65 лет (эта возрастная группа — угрожаемая по преждевременной смерти, поколение, которое через 10 лет даст ожидаемый средний показатель продолжительности жизни в стране).
По результатам исследования выяснилось, что образ жизни наших пациентов оставляет желать лучшего. Курит каждый второй пациент, у 90% стаж курения составляет более 20 лет, 2/3 пациентов выкуривают в день пачку сигарет и более. Артериальная гипертензия выявлена у 70% пациентов, при этом антигипертензивные препараты принимают только 20% из них; сахарный диабет — у 40%, повышенный холестерин — у 42%, ожирение — у 55%, то есть у каждого второго исследуемого.
При этом каждый третий из 200 пациентов — с повторным инфарктом, потому что люди пренебрегают вторичной профилактикой, в частности, медикаментозной терапией, отказом от вредных привычек. Многие пациенты, после стентирования чувствуя себя практически здоровыми, хотят поскорее забыть о болезни. Однако забывать о ней нельзя. Чтобы сердце работало качественно, в течение года нужно принимать специальные препараты для разжижения крови, улучшающие сердечный выброс, способствующие минимальному изменению миокарда после инфаркта, статины для снижения уровня холестерина. Также необходимо отказаться от курения, алкоголя, следить за весом, придерживаться определенной диеты и т. д. Итог несоблюдения этих рекомендаций всегда плачевный.
Многие пациенты, после стентирования чувствуя себя практически здоровыми, хотят поскорее забыть о болезни. Однако забывать о ней нельзя. Чтобы сердце работало качественно, в течение года нужно принимать специальные препараты для разжижения крови, улучшающие сердечный выброс, способствующие минимальному изменению миокарда после инфаркта, статины для снижения уровня холестерина. Также необходимо отказаться от курения, алкоголя, следить за весом, придерживаться определенной диеты и т. д. Итог несоблюдения этих рекомендаций всегда плачевный.
Отмечу, что количество пациентов, у которых инфаркт не связан с атеросклерозом, а обусловлен, скорее всего, резким спазмом коронарной артерии на фоне сильного стресса либо большой потерей жидкости и, как следствие, сгущением крови и образованием тромба, в группе исследуемых очень и очень незначительно.
Действительно, люди мало задумываются о своем здоровье, игнорируют тревожные симптомы из-за безответственного к себе отношения либо по незнанию, хотя необходимой информации достаточно и в СМИ, и в интернете, есть очень хорошие ролики социальной рекламы. Но граждане просто не обращают на это внимания.
Сегодня возможности медицины позволяют сохранить жизнь пациентам даже с тяжелым инфарктом. Но настороженность в этом плане должна быть не только у врачей, но и у обычных людей. Без этого никакие технологии не помогут. Атеросклероз — очень злобное заболевание, оно поражает много сосудов, и не только относящихся к сердцу, но и в мозге, конечностях. Поэтому так важно должное внимание к своему здоровью.
Откажитесь от вредных привычек и «быстрого питания», добавьте больше физической активности в свою жизнь, хотя бы 30 минут в день посвящайте физическим упражнениям, пешим прогулкам на свежем воздухе. А еще не пропускайте профосмотры и вовремя обращайтесь к врачу.
Даже если проходить диспансеризацию один раз в три года, это позволит выявить имеющиеся проблемы со здоровьем, скорректировать их, пока не прозвенел колокол. Сейчас есть очень хорошие и доступные лекарства, которые могут не просто улучшить ситуацию, а реально повлиять на прогноз для жизни человека. Инфаркт можно предупредить, и не ценой каких-то невероятных усилий или средств. Надо быть лишь немного внимательнее к себе.
Время госпитализации и исходы острого инфаркта миокарда у пожилых больных в центрально-азиатском регионе | Никишин
1. Avezum A, Makdisse M, Spencer F, et al. Impact of age on management and outcome of acute coronary syndrome: observations from the Global Registry of Acute Coronary Events (GRACE). Am Heart J 2005; 149(1): 67-73.
2. Brieger D, Eagle KA, Goodman SG, et al. GRACE Investigators. Acute coronary syndromes without chest pain, an under diagnosed and under treated high-risk group: Insights from the Global Registry of Acute Coronary Events. Chest 2004; 126: 461-9.
3. George E, Savitha D, Pais P. Pre-hospital issues in acute myocardial infarction. J Assoc Physicians India 2001; 49: 320-3.
4. Gersh BJ, Sliwa C, Mayosi DM, Yusuf S. The epidemic of cardiovascular disease in the developing world: global implications. Eur Heart J 2010; 31: 642-8.
5. Joshi P, Islam S, Pais P, et al. Risk Factors for Early Myocardial Infarction in South Asians Compared With Individuals in Other Countries. JAMA 2007; 297 (3): 286-94.
6. Malhotra S, Gupta M, Chandra KK, et al. Prehospital delay in patients hospitalized with acute myocardial infarction in the emergency unit of a north Indian tertiary care hospital. Indian Heart J 2003; 55: 349-53.
7. Rathore SS, Berger AK, Weinfurt KP, et al. Race, sex, poverty, and the medical treatment of acute myocardial infarction in the elderly. Circulation 2000; 102(6): 642-8.
8. De Servi S, Cavallini C, Dellavalle A, et al.; ROSAI-2 Investigators. Non-ST-elevation acute coronary syndrome in the elderly: treatment strategies and 30-day outcome. Am Heart J 2004; 147(5): 830-6.
9. The future of CVD. In: Mackay J, Mensah G, eds. The Atlas of Heart Disease and Stroke. Geneva, Switzerland: World Health Organization 2004; 74-5.
Инфаркт миокарда
Инфа́ркт миока́рда — одна из клинических форм ишемической болезни сердца, протекающая с развитием ишемического некроза участка миокарда, обусловленного абсолютной или относительной недостаточностью его кровоснабжения.
1 декабря 2012 года Американская коллегия кардиологии и Американская ассоциация сердца опубликовали самые современные клинические рекомендации по ведению инфаркта миокарда со стойкими подъёмами сегмента ST на ЭКГ и его ранних осложнений[1]. Чуть раньше в октябре 2012 года свои рекомендации по данной форме заболевания обновило Европейское общество кардиологии[2]. Последние обновления своих рекомендаций по ведению острого коронарного синдрома без стойких подъёмов сегмента ST на ЭКГ данные общества публиковали в мае[3] и декабре[4] 2011 года соответственно.Классификация
По стадиям развития:
- Острейший период (до 2 часов от начала ИМ)
- Острый период (до 10 дней от начала ИМ)
- Подострый период (с 10 дня до 4-8 недель)
- Период рубцевания (с 4-8 нед до 6 месяцев)
По анатомии поражения:
- Трансмуральный
- Интрамуральный
- Субэндокардиальный
- Субэпикардиальный
По объёму поражения:
- Крупноочаговый (трансмуральный), Q-инфаркт
- Мелкоочаговый, не Q-инфаркт
- Локализация очага некроза.
- Инфаркт миокарда левого желудочка (передний, боковой, нижний, задний).
- Изолированный инфаркт миокарда верхушки сердца.
- Инфаркт миокарда межжелудочковой перегородки (септальный).
- Инфаркт миокарда правого желудочка.
- Сочетанные локализации: задне-нижний, передне-боковой и др.
По течению:
- Моноциклическое
- Затяжное
- Рецидивирующий ИМ (в 1у коронарную артерию подсыпает, новый очаг некроза от 72 часов до 8 дней)
- Повторный ИМ (в др. кор. арт., новый очаг некроза через 28 дней от предыдущего ИМ)
Клиническая классификация, подготовленная объединённой рабочей группой Европейского общества кардиологов, Американского кардиологического колледжа, Американской ассоциации сердца и Всемирной кардиологической федерации (2007)[5]:
- Спонтанный ИМ (тип 1), связанный с ишемией вследствие первичного коронарного события, такого как эрозия бляшки и/или разрушение, растрескивание или расслоение.
- Вторичный ИМ (тип 2), связанный с ишемией, вызванной увеличением недостатка кислорода или его поступления, например, при коронарном спазме, коронарной эмболии, анемии, аритмии, гипер- или гипотензии.
- Внезапная коронарная смерть (тип 3), включая остановку сердца, часто с симптомами предполагаемой ишемии миокарда с ожидаемой новой элевацией ST и новой блокадой левой ножки пучка Гиса, выявлением свежего тромба коронарной артерии при ангиографии и/или аутопсии, наступившей смертью до получения образцов крови или перед повышением концентрации маркеров.
- ЧКВ-ассоциированный ИМ (тип 4а).
- ИМ, связанный с тромбозом стента (тип 4б), который подтверждён ангиографией или аутопсией.
- АКШ-ассоциированный ИМ (тип 5).
Нужно иметь в виду, что иногда у пациентов может возникать несколько типов ИМ одновременно или последовательно. Следует учесть, что термин «инфаркт миокарда» не входит в понятие «некроз кардиомиоцитов» вследствие проведения АКШ (отверстие в желудочке, манипуляции с сердцем) и влияния следующих факторов: почечной и сердечной недостаточности, кардиостимуляции, электрофизиологической абляции, сепсиса, миокардита, действия кардиотропных ядов, инфильтративных заболеваний.
Этиология
Инфаркт миокарда развивается в результате обтурации просвета сосуда кровоснабжающего миокард (коронарная артерия). Причинами могут стать (по частоте встречаемости):
- Атеросклероз коронарных артерий (тромбоз, обтурация бляшкой) 93-98 %
- Хирургическая обтурация (перевязка артерии или диссекция при ангиопластике)
- Эмболизация коронарной артерии (тромбоз при коагулопатии, жировая эмболия т. д.)
- Спазм коронарных артерий
Отдельно выделяют инфаркт при пороках сердца (аномальное отхождение коронарных артерий от аорты).
Факторы риска
Основная статья: Факторы риска ишемической болезни сердцаОсновная статья: Сердечно-сосудистый риск
- Табакокурение и пассивное курение[6]
- Артериальная гипертензия
- Ревмокардит
- Перенесённые стафилококковые и стрептококковые инфекции
- Повышенная концентрация холестерина ЛПНП («плохого» холестерина) в крови
- Низкая концентрация холестерина ЛПВП («хорошего» холестерина) в крови
- Высокий уровень триглицеридов в крови
- Низкий уровень физической активности
- Возраст
- Загрязнение атмосферы[7]
- Пол (Мужчины чаще страдают от инфаркта миокарда, чем женщины)
- Ожирение[8]
- Алкоголизм
- Сахарный диабет
- Инфаркт миокарда в прошлом и манифестация любых других проявлений атеросклероза
Патогенез
Различают стадии:
- Ишемии
- Повреждения (некробиоза)
- Некроза
- Рубцевания
Ишемия может являться предшественником инфаркта и длиться довольно долго. В основе процесса — нарушение гемодинамики миокарда. Обычно клинически значимым считается сужение просвета артерии сердца до такой степени, когда ограничение кровоснабжения миокарда не может быть больше компенсировано. Чаще всего это происходит при сужении артерии на 70% площади её сечения. При исчерпывании компенсаторных механизмов говорят о повреждении, тогда страдают метаболизм и функция миокарда. Изменения могут носить обратимый характер (ишемия). Стадия повреждения длится от 4 до 7 часов. Некроз характеризуется необратимостью повреждения. Через 1-2 недели после инфаркта некротический участок начинает замещаться рубцовой тканью. Окончательное формирование рубца происходит через 1-2 месяца.
Клиническая картина
Основной клинический признак — интенсивная боль за грудиной (ангинозная боль). Однако болевые ощущения могут носить вариабельный характер. Пациент может жаловаться на чувство дискомфорта в груди, боли в животе, горле, руке, лопатке[9]. Нередко заболевание имеет безболевой характер, что характерно для больных сахарным диабетом.
Болевой синдром сохраняется более 15 минут (могут длиться 1 час) и купируется через несколько часов, либо после применения наркотических анальгетиков, нитраты неэффективны. Бывает профузный (липкий) пот [неизвестный термин].
В 20-40 % случаев при крупноочаговых поражениях развиваются признаки сердечной недостаточности. Пациенты отмечают одышку, непродуктивный кашель.
Нередко встречаются аритмии. Как правило это различные формы экстрасистолий или фибрилляция предсердий. Нередко единственным симптомом инфаркта миокарда является внезапная остановка сердца.
Предрасполагающим фактором является физическая нагрузка, психоэмоциональное напряжение, состояние утомления, гипертонический криз.
Атипичные формы инфаркта миокарда
В некоторых случаях симптомы инфаркта миокарда могут носить атипичный характер. Такая клиническая картина затрудняет диагностику инфаркта миокарда. Различают следующие атипичные формы инфаркта миокарда:
- Абдоминальная форма — симптомы инфаркта представлены болями в верхней части живота, икотой, вздутием живота, тошнотой, рвотой. В данном случае симптомы инфаркта могут напоминать симптомы острого панкреатита.
- Астматическая форма — симптомы инфаркта представлены нарастающей одышкой. Симптомы инфаркта напоминают симптомы приступа бронхиальной астмы.
- Безболевая ишемия миокарда наблюдается редко. Возможна слабость. Такое развитие инфаркта наиболее характерно для больных сахарным диабетом, у которых нарушение чувствительности является одним из проявлений болезни (диабета).
- Церебральная форма — симптомы инфаркта представлены головокружениями, нарушениями сознания, неврологическими симптомами; нарушение понимания, происходящего вокруг.
- Коллаптоидная форма — начинается с развития коллапса; в клинике доминируют резкая внезапная артериальная гипотензия, головокружение, появление холодного пота, потемнение в глазах. Расценивается как проявление кардиогенного шока.
- Аритмическая форма — начинается с пароксизма нарушения ритма сердца;
- Периферическая — отличается локализацией боли не в загрудинной или прекардиальной области, а в области горла, в левой руке, конце левого мизинца, в шейно-грудном отделе позвоночника, нижней челюсти.
- Отёчная — у больного появляются одышка, слабость, сравнительно быстро отеки и даже асцит, увеличивается печень — т. е. развивается острая правожелудочковая недостаточность.
- Комбинированная — сочетает различные проявления нескольких атипичных форм.
Диагностика
Болевые зоны при инфаркте миокарда: тёмно-красный = типичная область, светло-красный = другие возможные области.
Вид со спины.
- Ранняя:
- Электрокардиография
- Эхокардиография
- Анализ крови на кардиотропные белки (MB-КФК, АсАТ, ЛДГ1, тропонин[10])
- Отсроченная:
- Коронарография
- Сцинтиграфия миокарда (в настоящее время применяется редко)
Описания ЭКГ при инфаркте миокарда
Стадия развивающегося инфаркта миокарда (0-6 часов)
Стадия развивающегося инфаркта миокарда
- Куполообразный сегмент ST выше изолинии
- Сегмент ST сливается с зубцом T
- Зубец R высокий
- Зубец Q невысокий
Острая стадия инфаркта миокарда (6-7 суток)
Острая стадия инфаркта миокарда
- Отрицательный зубец T
- Уменьшение амплитуды зубца R
- Углубление зубца Q
Заживающий инфаркт миокарда (7-28 суток)
Заживающий инфаркт миокарда
- Отрицательный зубец T
- Сегмент ST приближается к изолинии
Заживший инфаркт миокарда (на 29 сутки — до нескольких лет)
Заживший инфаркт миокарда
- Стойкий зубец Q
- Сниженная амплитуда зубца R
- Положительный зубец T
- Комплекс ST на изолинии[11]
Осложнения
Ранние:
Поздние:
Лечение
Первая помощь
- При подозрении на инфаркт миокарда больного сначала усаживают и успокаивают. Рекомендуется положение сидя, желательно на кресле со спинкой, или полулёжа с согнутыми коленями. Тугую мешающую одежду расстёгивают, ослабляют галстук[15].
- Если больному выписано лекарство от боли в груди, такое как нитроглицерин, и это лекарство под рукой, то больному дают это лекарство[16].
- Если в течение 3 минут после сидения в покое или после принятия нитроглицерина боль не проходит, без промедления вызывают карету скорой помощи. Оказывающим первую помощь нельзя поддаваться на уговоры больного о том, что всё сейчас пройдёт[16]. Если скорая помощь не сможет прибыть быстро, пациента везут в больницу на попутной машине. При этом в машине желательно находиться двум здоровым людям, чтобы один вёл машину, а другой следил за состоянием больного[17].
- Если под рукой оказался аспирин, и у больного нет на аспирин известной ему аллергии, то ему дают разжевать 300 мг аспирина. Если больной постоянно принимает аспирин, принятую этим днём дозу дополняют до 300 мг. Важно разжевать таблетки, иначе аспирин не подействует достаточно быстро[15][17].
- В случае остановки сердца (потеря сознания, отсутствующее или агональное дыхание) немедленно начинают сердечно-лёгочную реанимацию. Её применение многократно увеличивает шансы больного на выживание. Ещё больше увеличивает выживаемость применение портативных дефибрилляторов: будучи в общественном месте (кафе, аэропорт, и т. д.), оказывающим первую помощь необходимо осведомиться у персонала о наличии у них или поблизости дефибриллятора. Определение отсутствия пульса больше не является необходимым условием для начала реанимации, достаточно потери сознания и отсутствия ритмичного дыхания[18].
Врачебная помощь
Лечение на ранних этапах при возможности сводится к устранению боли, восстановлению коронарного кровотока (тромболитическая терапия, ангиопластика коронарных артерий, АКШ). При выраженной сердечной недостаточности в условиях клиники возможна постановка внутриаортальной баллонной контрпульсации.
Устранение боли, одышки и тревоги[править | править вики-текст]
Если боль сохраняется на момент приезда бригады скорой медицинской помощи, врач применяет морфин. Предварительно 10 мг морфина гидрохлорида разводят в 10 мл 0,9 % раствора хлорида натрия или дистиллированной воды. Первую дозу 2-5 мг (то есть 2-5 мл раствора) вводят внутривенно струйно. Затем дополнительно вводят 2-5 мг каждые 5-15 минут до устранения боли или возникновения побочных эффектов.
Введение морфина при инфаркте миокарда без подъёма сегмента ST увеличивает риск смерти[19].
Также с обезболивающей целью возможно применение нейролептанальгезии — сочетание наркотического анальгетика фентанила (0,05-0,1 мг) и нейролептика дроперидола (2,5-10 мг в зависимости от уровня артериального давления). При необходимости нейролептанальгезию повторяют в более низкой дозе.
При наличии у больного артериальной гипоксемии (насыщение артериальной крови кислородом < 90 %), одышки или других признаков сердечной недостаточности дают увлажнённый кислород (через маску или носовой катетер) со скоростью 2-5 л/мин. Артериальную гипоксемию по возможности определяют с помощью пульсоксиметрии.
Несмотря на это, систематические обзоры 2009 и 2010 годов показали, что применение кислорода при инфаркте миокарда увеличивает риск смерти и зону некроза, поэтому на данный момент не рекомендуют использовать кислородотерапию рутинно[20][21].
Больному с выраженным возбуждением, тревогой, страхом (которые не исчезают после введения наркотического анальгетика) можно назначить транквилизатор (например, диазепам внутривенно 2,5-10 мг). Также важно успокоить пациента и его близких.
Антитромбоцитарная терапия
Всем людям с признаками острого коронарного синдрома (инфаркта миокарда или первичной нестабильной стенокардией), не принимающим данное лекарство и без противопоказаний к нему, следует принять ацетилсалициловую кислоту, предварительно разжевав, в первой нагрузочной дозе 162–325 мг[1][3][22][23] (или 150–300 мг согласно европейским рекомендациям[2][4]). Для этих целей не подходит кишечно-растворимая форма, так как начало её действия медленное. При выраженной тошноте, рвоте, сопутствующих заболеваниях желудка возможно внутривенное введение ацетилсалициловой кислоты в дозе 250–500 мг. Далее ацетилсалициловая кислота показана таким больным пожизненно в дозе 75–162 мг/сут[24]. При наличии противопоказаний к ацетилсалициловой кислоте применяют клопидогрел в нагрузочной первой дозе 300 мг и в последующем 75 мг/сут[25][26]. Комбинация клопидогрела с аспирином эффективнее, чем монотерапия аспирином при инфаркте миокарда без подъёма сегмента ST (без статистически значимого влияние на смертность) и экономически оправдана, когда для здравоохранения приемлемы затраты порядка 6078 фунтов стерлингов за каждый дополнительный год полноценной жизни (quality-adjusted life year (QALY))[27]. Рутинное добавление клопидогреля к аспирину при консервативном лечении острого коронарного синдрома без подъёма сегмента ST, а также установке металлического стента без нанесения цитостатика и стента покрытого цитостатиком было рекомендовано Американской коллегией кардиологов в 2007 году[22]. В 2011 году эти рекомендации были немного скорректированы — в частности как аналог клопидогреля (75 мг/сутки) при установке стентов был рекомендован прасугрель по 10 мг в сутки[3].
Антикоагулянты
Применяют нефракционированный гепарин в течение 48 ч. В начале вводят внутривенно струйно 60 МЕ/кг (но не более 4000 МЕ), затем постоянно внутривенно с начальной скоростью 13 МЕ/кг/ч (но не более 100 МЕ/ч) Дальнейшую дозу подбирают, ориентируясь на АЧТВ, который должен в 1,5-2 раза быть больше нормы и контролироваться через 3, 6, 12, 24 ч.
Также возможно применение низкомолекулярного гепарина (эноксапарина), который вводят под кожу живота в дозе 1 мг/кг 2 раза в сутки до 5-7 дней. За 15 мин до первой п/к инъекции необходимо внутривенно струйно ввести 30 мг данного препарата. Доза первых 2 п/к инъекций — не более 100 мг. Преимущества низкомолекулярного гепарина перед нефракционированным: простота введения и нет необходимости в постоянном контроле свёртывания крови.
Иногда применяют фондапаринукс в дозе 2,5 мг под кожу живота 1 раз в сутки. Данный препарат наиболее удобен в применении и в отличие от гепарина вызывает тромбоцитопению в более редких случаях.
Тромболитическая терапия
Тромболитическая терапия показана при инфаркте миокарда с подъёмом сегмента ST на ЭКГ. Эффективность её убедительно доказана, позволяет восстановить коронарный кровоток, ограничить размер инфаркта и снизить смертность. Тромболизис проводят как можно раньше и в пределах 12 ч от начала заболевания. Для этого применяют стрептокиназу в дозе 1,5 млн МЕ внутривенно на 100 мл 0,9 % раствора хлорида натрия в течение 30-60 мин. Также используют альтеплазу на 100—200 мл изотонического раствора по схеме: 15 мг внутривенно струйно, затем 0,75 мг/кг в течение 30 мин (но не более 50 мг) и далее 0,5 мг/кг в течение 60 мин (но не более 35 мг). Альтеплаза имеет преимущества перед стрептокиназой в виде более эффективного восстановления коронарного кровотока за счёт тропности к фибрину тромба, а также отсутствии антигенности.
Бета-адреноблокаторы
При отсутствии противопоказаний применяют метопролол, пропранолол или атенолол. Однако эффективность внутривенного применения бета-адреноблокаторов на ранних этапах не доказана и повышает риск развития кардиогенного шока. Хотя по некоторым данным лечение пациента с сердечным приступом во время перевозки в больницу с помощью метопролола, может значительно уменьшить повреждения сердца при инфаркте миокарда [28]
Лечение инфаркта миокарда стволовыми клетками и экзосомами
В настоящее время терапия инфаркта миокарда стволовыми клетками активно исследуется в экспериментах на животных; клинических испытаний на людях, доказывающих эффективность данной методики, не проводилось. Несмотря на то, что в опытах на животных стволовые клетки оказывают положительный эффект, вопрос лечения ими исследован явно недостаточно для перехода к экспериментам на людях.
В эксперименте на крысах было показано, что мобилизация стволовых клеток под действием колониестимулирующих факторов (англ. Colony-stimulating factor) ускоряет процессы репарации миокарда после инфаркта, при этом рубца почти не остаётся[29].
В систематическом обзоре, опубликованном специалистами Cochrane Collaboration в 2012 году, сообщается, что терапия стволовыми клетками может существенно улучшить прогноз при остром инфаркте миокарда[30].
В экспериментах на животных даже однократное введение экзосом мезенхимальных стволовых клеток уменьшает размер инфаркта и улучшает состояние подопытных. Очевидно, экзосомы восполняют дефицит ферментов, важных для снабжения клетки энергией, а значит, и для скорейшей реабилитации сердечной мышцы [31][32].
Психические изменения и психозы
При инфаркте миокарда возможны психические изменения невротического и неврозоподобного характера. В основе этих изменений лежит реакция личности на тяжёлое, опасное для жизни заболевание. Помимо особенностей личности, психическое состояние больного ИМ определяется также соматогенными и внешними (средовыми) факторами (психологическое влияние медицинского персонала, родственников, других больных и т. д.).
Следует различать адекватные (нормальные) и патологические (невротические) реакции. Реакция на болезнь квалифицируется как адекватная, если: а) поведение больного, его переживания и представления о болезни соответствуют полученной от врача информации о тяжести ИМ и его возможных последствиях; б) больной соблюдает режим, следует предписаниям врача и в) больной в состоянии контролировать свои эмоции.
Среди патологических реакций более чем в 40% случаев наблюдается кардиофобическая реакция, при которой больные испытывают страх перед повторным ИМ и перед внезапной смертью от сердечного приступа. Такие больные чрезмерно осторожны, особенно при попытках расширения режима физической активности. Усиление страха сопровождается дрожью в теле, слабостью, потливостью, сердцебиением, чувством нехватки воздуха.
Также одной из патологических реакций при ИМ возможна депрессивная (тревожно-депрессивная) реакция. Отмечается угнетённое настроение. Больные не верят в возможность благоприятного течения заболевания, испытывают внутреннюю напряжённость, предчувствие надвигающейся беды, опасения за исход заболевания, тревогу за благополучие семьи. Характерны нарушения сна, двигательное беспокойство, потливость, учащённое сердцебиение.
Заметно реже, в основном у пожилых, наблюдается ипохондрическая (депрессивно-ипохондрическая) реакция. При ней отмечаются постоянная и явная переоценка тяжести своего состояния, несоответствие обилия жалоб объективным соматическим изменениям, чрезмерная фиксация внимания на состоянии своего здоровья.
Чревата осложнениями анозогнозическая реакция, при которой отмечается отрицание болезни с игнорированием врачебных рекомендаций и грубыми нарушениями режима.
В отдельных случаях наблюдается истерическая реакция. Для поведения больного характерны эгоцентризм, демонстративность, стремление привлечь к себе внимание окружающих, вызвать сочувствие, эмоциональная лабильность.
Отмеченные выше психические изменения наблюдаются на фоне психической астении: общей слабости, быстрой утомляемости при незначительном физическом или умственном напряжении, ранимости, повышенной возбудимости, нарушениях сна, вегетососудистой неустойчивости.
Психическая астения выражена в большей степени при длительном пребывании на постельном режиме и у больных пожилого возраста.
Если не проводить специальных мероприятий, изменения психики усугубляются, становятся стойкими и в дальнейшем могут значительно препятствовать реабилитации вплоть до инвалидизации по психическому состоянию.
Одно из наиболее грозных осложнений острого периода болезни — психозы, которые наблюдаются примерно в 6—7% случаев. Грубые нарушения поведения, резкие вегетативные сдвиги сопровождаются значительным ухудшением соматического состояния, при психозах чаще наступает летальный исход. В подавляющем большинстве случаев психозы развиваются на 1-й неделе заболевания. Длительность их обычно не превышает 2—5 дней.
Главными причинами психозов при ИМ являются интоксикации продуктами распада из некротического очага в миокарде, ухудшение церебральной гемодинамики и гипоксемия, вызванные нарушением сердечной деятельности. Не случайно психозы наблюдаются чаще всего у больных с обширными поражениями миокарда и острой недостаточностью кровообращения (кардиогенный шок, отёк лёгких).
К возникновению психоза при ИМ предрасполагают поражения головного мозга различной природы (последствия черепно-мозговых травм, хронический алкоголизм, церебральный атеросклероз, гипертоническая болезнь и др.) и пожилой возраст.
Чаще всего психоз возникает в вечерние и ночные часы. Как правило, он протекает в форме делирия. Нарушается сознание с потерей ориентировки в окружающей обстановке и во времени, возникают иллюзии и галлюцинации (чаще зрительные), больной испытывает тревогу и страх, нарастает двигательное беспокойство, приводя к двигательному возбуждению (беспрестанные попытки встать с кровати, выбежать в коридор, вылезти в окно и т. д.). Нередко делирию предшествует состояние эйфории — повышенного настроения с отрицанием болезни и грубой переоценкой своих сил и возможностей.
У больных старческого возраста иногда наблюдаются так называемые просоночные состояния: больной, пробуждаясь ночью, встаёт, несмотря на строгий постельный режим, и начинает бродить по больничному коридору, не осознавая, что он серьёзно болен и находится в больнице.
Профилактика
- Антитромботическая терапия аспирином и/или клопидогрелом снижает риск рецидива инфаркта миокарда. Применение клопидогрела и аспирина снижает риск сердчечно-сосудистых событий, но в то же время повышает риск развития кровотечений[33].
- Бета-блокаторы могут применяться для профилактики инфаркта миокарда у людей, перенёсших инфаркт миокарда в прошлом[34]. Из всех бета-блокаторов бисопролол, метопролола сукцинат и карведилол улучшают прогноз у людей со сниженной фракцией выброса левого желудочка ниже 40 %[35]. Бета-блокаторы после перенесённого инфаркта миокарда снижают смертность и заболеваемость.
- Терапия статинами после инфаркта миокарда снижает смертность[36][37].
- Применение полиненасыщенных длинноцепочечных омега-3 жирных кислот (докозагексаеновой и эйкозапентаеновой) в больших дозах также улучшает прогноз после перенесённого инфаркта миокарда[38][39][40].
- Применение нефракционированного гепарина внутривенно или низкомолекулярного гепарина подкожно у лиц с первичной нестабильной стенокардией снижает риск инфаркта миокарда[41].
- Ингибиторы АПФ также применяют для профилактики инфаркта миокарда у людей со сниженной фракцией выброса левого желудочка ниже 40 %[42].
Прогноз
Прогноз заболевания условно неблагоприятный, после возникновения инфаркта в миокарде развиваются необратимые ишемические изменения, что может привести к осложнениям различной степени тяжести.
Материал из Википедии — свободной энциклопедии
Реабилитация по ОМС
Медицинская реабилитация пациентов после операции на сердце и сосудах
Отделение принимает пациентов Центра,
а также всех регионарных сосудистых центров и кардиологических отделений
города. Для пациентов Центра Мешалкина это уникальная возможность находиться
под наблюдением в одном медицинском учреждении: с первого обращения до
отдаленного постоперационного периода.
1. Пациенты с ишемической болезнью сердца после проведенного оперативного лечения: аортокоронароное шунтирование, маммарокоронарное шунтирование, ангиопластика коронарных артерий. Второй этап реабилитации.
2. Пациенты с ишемической болезнью сердца после перенесенного инфаркта миокарда и стентирования инфаркт связанной артерии, перенесенного инфаркта миокарда в стадии рубцевания (если оперативное лечение было не показано). Второй этап реабилитации.
3. Пациенты, перенесшие протезирование клапанов сердца при приобретенных пороках сердца. Второй этап реабилитации.
4. Пациенты после оперативного лечения сложных нарушений ритма и проводимости сердца. Второй этап реабилитации.
5. Пациенты кардиологического профиля через год после оперативного лечения. Второй этап реабилитации.
6. Пациенты кардиологического профиля — более года после оперативного лечения. Третий этап реабилитации в условиях дневного стационара (при желании пациента во время лечения возможно проживание и питание на платной основе).
Для решения вопроса о госпитализации направляющая медицинская организация (стационар/поликлиника по месту жительства) направляет в Центр пакет документов пациента:
✔выписной эпикриз / заключение о наличии показаний к кардиореабилитации,
✔согласие пациента.
Документы направляются на официальный сайт Центра www.meshalkin.ru (раздел Заочная консультация).Дата госпитализации будет согласована по результату рассмотрения медицинских документов пациента: при наличии показаний/ отсутствии противопоказаний к проведению реабилитационных мероприятий.
К согласованной дате госпитализации, направляющая медицинская организация оформляет для пациента направление по форме 057/у-04.
Направление должно быть оформлено согласно Приложению №11 к приказу Министерства здравоохранения и соц. развития РФ от 22.11.2004 №255.
✔ полное наименование направляющего медицинского учреждения, его адрес или штамп учреждения с указанием кода учреждения по ОГРН
✔ полностью ФИО, дата рождения пациента
✔ код диагноза по МКБ
✔ вид исследования, на которое направляется пациент
✔ учреждение, куда направляется пациент
✔ подпись направившего врача
✔ подпись заведующего отделением
✔ печать направившего мед. учреждения
Условия госпитализацииГоспитализация проводится в согласованный день с 09.00 до 14.00. Точное время прибытия заранее уточнит администратор — при подтверждении даты госпитализации по телефону.
В день госпитализации/обследования по ОМС пациенту при себе обязательно необходимо иметь:
✔ паспорт
✔ действительный полис ОМС
✔ оригинал направления (форма № 057/у-04), действительный на момент госпитализации
✔ выписка из стационарной и/или амбулаторной карты (медицинский эпикриз)
✔ для оформления листка нетрудоспособности Вам понадобится справка с места работы с наименованием учреждения
✔ обязательные для госпитализации анализы и обследования согласно перечню (см. ниже)
Перед госпитализацией обязательно необходимо пройти и иметь при себе указанные ниже обследования.
Обследования сгруппированы по сроку актуальности (до даты госпитализации).
Обследование, обязательное для госпитализации в
отделение медицинской реабилитации пациентов с соматическими заболеваниями |
14 дней | 30 дней | 60 дней |
| Общий анализ крови |
✔ | ||
|
Общий анализ мочи |
✔ | ||
|
Биохимический анализ крови: общий белок, билирубин, АСТ, АЛТ, сахар |
✔ | ||
| Анализ крови на сифилис. При положительном результате анализа обязательна справка из кожно- венерологического диспансера по месту жительства! | ✔ | ||
| Анализ крови на маркеры вирусного гепатита В, C. При положительном результате анализа обязательно заключение инфекциониста по месту жительства! | ✔ | ||
| Анализ крови на ВИЧ-инфекцию. При наличии в анамнезе ВИЧ-инфекции необходимо обязательно иметь заключение из Центра СПИДа по месту жительства, развернутые рекомендации специалиста по ведению пациента в послеоперационном периоде! При наличии АРВ-терапии пациенту необходимо иметь при себе ретровирусные препараты | ✔ | ||
|
Электрокардиограмма (ЭКГ), пленка и заключение |
✔ | ||
|
Уролог (для мужчин), гинеколог (для женщин) |
✔ | ||
|
Флюорография или рентгенография органов грудной клетки (снимки и описание) в двух проекциях (передней, левой боковой) |
Действительно в течение 1 года |
||
✔ Двухместное размещение. В каждой палате: санузел с душем, телевизор, холодильник
✔ Предоставляется постельное белье, полотенце, посуда
✔ Индивидуальное питание в соответствии с профилем заболевания
✔ Возможно одноместное размещение либо размещение в номере одного из близких родственников (лица по уходу): предоставляется при условии оплаты дополнительного койко-места (информация по тел. +7(383)347-60-62)
СТРОГО ЗАПРЕЩЕНО!
✔ Употреблять спиртные напитки
✔ Покидать территорию отделения без согласования с лечащим врачом (оформление пропуска обязательно)
✔ Нарушать лечебно-оздоровительный режим отделения
✔ Курение табака возможно только в специально отведенных местах на улице
ПОСЕЩЕНИЕ ПАЦИЕНТОВ В ОТДЕЛЕНИИ
✔ Посещение родственниками пациентов возможно в свободном режиме ежедневно с 09.00 до 21.00
✔ Посещения могут быть запрещены в случае карантина
Настоящая борьба за жизнь
Пациент К., 47 лет, поступил в отделение кардиореанимации с острым инфарктом миокарда. В момент поступления у пациента развилась фибрилляция желудочков с остановкой кровообращения. Начаты реанимационные мероприятия. Многочисленные попытки дефибрилляции, несмотря на непрямой массаж сердца, искусственную вентиляцию легких, вводимые препараты были неэффективны. По кардиомонитору регистрировался идиовентрикулярный ритм с переходом в асистолию — остановка сердца. На фоне проведения непрямого массажа сердца принято решение начать процедуру экстракорпоральной мембранной оксигенации (ЭКМО), чтобы поддержать гемодинамику и сделать возможным перевод пациента в операционную для реваскуляризации миокарда.
В палате кардиореанимации была выполнена катетеризация бедренной артерии и вены и начата процедура веноартериальной ЭКМО, которая обеспечила кровообращение и позволила выиграть время для перевода в рентгеноперационную. К этому времени непрямой массаж сердца продолжался 40 минут. Аппарат ЭКМО в данном случае выполнял функцию искусственного сердца и позволил прекратить непрямой массаж, несмотря на отсутствие сокращения миокарда.
Экстракорпоральная мембранная оксигенация – это способ временного поддержания функции легких и сердца при их изолированном или сочетанном повреждении. При помощи специального оборудования создается искусственное кровообращение, которое полностью заменяет функции как сердца, так и легких, удаляется углекислый газ, кровь обогащается кислородом. Пока идет процедура, имеется возможность лечить основное заболевание, которое привело к развитию осложнений.
В рентгеноперационной после выполнения коронарографии выявлен тромбоз крупной правой коронарной артерии с полным прекращением кровотока. Рентгенэндоваскулярный хирург произвел реканализацию тромбированного участка с аспирационным удалением тромба и стентированием правой коронарной артерии.
После восстановления кровотока по правой коронарной артерии состояние пациента стабилизировалось. Удалось снизить дозы медикаментозной поддержки. В течение 24 часов с целью профилактики постреанимационного отека головного проводилась искусственная гипотермия до 35оС. Через 50 часов после развития фатального осложнения инфаркта миокарда пациент пришел в сознание, был экстубирован. Производительность контура ЭКМО постепенно снижали, на шестые сутки пациент был отключен от системы ЭКМО, еще через день был переведен в отделение кардиологии и в последующем выписан. Перед выпиской отмечал хорошее самочувствие, сократительная способность сердца практически не пострадала. После реабилитации пациент сможет вернуться к обычной жизни.
Анестезиологи-реаниматологи: Арболишвили Г.Н., Стрельцов Ю.В.
Центр ЭКМО: Кецкало М.В., Кальянова Н.Ю.
Рентгенэндоваскулярный хирург: Молокопой С.Н.
|
Окклюзия правой коронарной артерии |
Восстановление кровотока после стентирования |
Лечение острого инфаркта миокарда, сердечный приступ. Пациент
Ведение пациента с острым инфарктом миокарда (ОИМ) требует неотложной медицинской помощи. Следует соблюдать местные инструкции по ведению инфаркта миокарда там, где они существуют. Пациентам с болью в груди не следует сообщать, что у них был сердечный приступ, до тех пор, пока они не будут соответствовать универсальным критериям инфаркта миокарда. До этого момента рекомендуется использовать терминологию «острый коронарный синдром». Более подробную информацию о диагнозе можно найти в отдельной статье «Острый коронарный синдром».Руководство по стандарту оказания помощи пациентам с острым коронарным синдромом было опубликовано Национальным институтом здравоохранения и передового опыта (NICE) [1] .
Эта статья в основном посвящена лечению ОИМ после подтверждения того, что пациент соответствует требуемым критериям.
Добольничное наблюдение
- При подозрении на ОИМ вызовите скорую помощь. Сделайте ЭКГ как можно скорее, но не откладывайте перевод в больницу, поскольку ЭКГ имеет значение только для догоспитального лечения, если рассматривается вопрос о догоспитальном тромболизисе.
- Посоветуйте любому пациенту с ишемической болезнью сердца вызвать скорую помощь, если боль в груди не реагирует на тринитрат глицерина (GTN) и присутствует более 15 минут или на основании общего клинического состояния — например, тяжелая. одышка или боль.
- Сердечно-легочная реанимация и дефибрилляция в случае остановки сердца.
- Кислород: не вводить кислород в обычном порядке, а контролировать сатурацию кислородом с помощью пульсоксиметрии как можно скорее, в идеале до госпитализации.Предлагайте дополнительный кислород только [2] :
- Людям с сатурацией кислорода менее 94%, которые не подвержены риску гиперкапнической дыхательной недостаточности, стремясь к сатурации 94-98%.
- Людям с хронической обструктивной болезнью легких, которые подвержены риску гиперкапнической дыхательной недостаточности, необходимо достичь целевого насыщения 88-92% до тех пор, пока не будет доступен анализ газов крови.
- Обезболивание с помощью GTN сублингвально / в виде спрея и / или внутривенного опиоида 2,5–5 мг диаморфина или 5–10 мг морфина внутривенно [2] .Избегайте внутримышечных инъекций, так как всасывание ненадежно, а место инъекции может кровоточить, если пациент позже получит тромболитическую терапию.
- Аспирин 300 мг перорально (диспергируемые или жевательные).
- Вставьте канюлю для внутривенного доступа и возьмите анализ крови на FBC, функцию почек и электролиты, глюкозу, липиды, скрининг на свертываемость, C-реактивный белок (CRP) и сердечные ферменты (тропонин I или T).
- Добольничный тромболизис показан, если время от первого звонка до прибытия в больницу составляет более 30 минут.Если первичное чрескожное коронарное вмешательство невозможно провести в течение 120 минут после постановки диагноза ЭКГ, пациенты с острым коронарным синдромом (ОКС) с подъемом сегмента ST должны получить немедленную (до госпитальной или госпитальной) тромболитическую терапию [3] . При лечении людей с фибринолизом одновременно дайте антитромбин [4] .
- NICE рекомендует использовать внутривенный болюс (ретеплаза или тенектеплаза) вместо инфузии для догоспитального тромболизиса [5] .
Лечение начато в больнице
- Если еще не сделано, введите внутривенную канюлю и возьмите анализ крови на сердечные ферменты (тропонин I или T), FBC, функцию почек и электролиты, глюкозу, липиды, CRP и скрининг свертывания. См. Отдельную статью об остром инфаркте миокарда для более подробного обсуждения исследований.
- Продолжайте тщательный клинический мониторинг (включая симптомы, пульс, артериальное давление, сердечный ритм и сатурацию кислорода по данным пульсоксиметрии), кислородную терапию и обезболивание.
- Мониторинг ЭКГ: функции, которые увеличивают вероятность инфаркта: новая элевация сегмента ST; новые зубцы Q; любой подъем сегмента ST; новый дефект проводимости. Другими признаками ишемии являются депрессия сегмента ST и инверсия зубца T.
- Проведите оценку риска будущих сердечно-сосудистых событий, используя стандартную систему баллов, которая прогнозирует шестимесячную смертность — например, оценка риска [6] Глобального реестра острых сердечных событий (GRACE). Используя эту оценку в качестве руководства, наряду с учетом сопутствующих заболеваний и риска кровотечений, определите, следует ли использовать консервативную или инвазивную стратегию.Более подробную информацию см. В отдельной статье «Острый коронарный синдром».
- Рассмотрите возможность консервативного лечения без ранней коронарной ангиографии для людей с нестабильной стенокардией или инфарктом миокарда без подъема сегмента ST (ИМбпST), которые имеют низкий риск неблагоприятных сердечно-сосудистых событий (прогнозируемая шестимесячная смертность 3,0% или менее). В таких случаях предложите прасугрел или тикагрелор с аспирином, если только риск кровотечения высок, и в этом случае используйте клопидогрель и аспирин.
- Пациентам с нестабильной стенокардией или ИМбпST, которым проводится коронарная ангиография, предложите прасугрел или тикагрелор с аспирином после того, как будет определена анатомия коронарных артерий и планируется проведение ЧКВ.Учитывайте риск кровотечения у пациентов старше 75 лет, получавших прасугрел. Если есть отдельное показание для продолжающейся пероральной антикоагуляции, используйте клопидогрель с аспирином.
Реперфузия
[3, 4, 7]Проходимость закупоренной артерии может быть восстановлена чрескожным коронарным вмешательством (ЧКВ) или назначением тромболитического препарата. ЧКВ является предпочтительным методом. По сравнению с консервативной стратегией, инвазивная стратегия (ЧКВ или операция по аортокоронарному шунтированию (АКШ)) связана со снижением частоты рефрактерной стенокардии и повторной госпитализации в краткосрочной перспективе и инфаркта миокарда в долгосрочной перспективе.Однако существует удвоенный риск сердечного приступа, связанного с процедурой, и повышенный риск кровотечения и утечки процедурных биомаркеров [8] .
Первичная ЧКВ
- Первичная ангиопластика позволяет на раннем этапе оценить степень основного заболевания. См. Отдельную статью о чрескожном коронарном вмешательстве.
- Любая задержка первичного ЧКВ после поступления пациента в больницу связана с более высокой смертностью в больнице. Поэтому время до лечения должно быть как можно короче.
- Существует общее мнение о том, что ЧКВ следует рассматривать, если есть ОКС с подъемом сегмента ST, если симптомы появились не позднее, чем за 12 часов до этого. Соответствующий стандарт качества NICE для взрослых рекомендует пациентам с острым инфарктом миокарда с подъемом сегмента ST (ИМпST), которые поступают в течение 12 часов с момента появления симптомов, первичное чрескожное коронарное вмешательство (ЧКВ) в качестве предпочтительной стратегии реперфузии коронарных артерий, как только возможно, но в течение 120 минут после того, как можно было провести фибринолиз [1] .Нет единого мнения о том, полезно ли ЧКВ у пациентов, у которых появились симптомы более чем через 12 часов при отсутствии клинических и / или ЭКГ-свидетельств продолжающейся ишемии.
- Пациенты должны получать ингибитор гликопротеина IIb / IIIa в качестве дополнения к ЧКВ у пациентов со средним и высоким риском для снижения риска немедленной окклюзии сосудов, а также должны получать нефракционированный гепарин или гепарин с низкой молекулярной массой (например, эноксапарин). ) или бивалирудин.
- Прасугрел в комбинации с аспирином рекомендуется в качестве альтернативы для предотвращения атеротромботических событий у взрослых с нестабильной стенокардией, ИМбпST или ИМпST, имеющим первичное или отсроченное ЧКВ.У пациентов с повышенным риском кровотечения в качестве альтернативы можно рассмотреть тикагрелор или клопидогрель.
- Баллонная ангиопластика после инфаркта миокарда снижает риск смерти, нефатального инфаркта миокарда и инсульта по сравнению с тромболитической реперфузией. Однако до 50% пациентов испытывают рестеноз и 3-5% повторных инфарктов миокарда [9] .
- Нет никаких доказательств того, что первичное стентирование снижает смертность по сравнению с баллонной ангиопластикой, но стентирование, по-видимому, связано со снижением риска повторного инфаркта и реваскуляризации целевого сосуда [9] .
- NICE поэтому рекомендует использовать интракоронарную имплантацию стента с лекарственным покрытием у пациентов с ИМпST, ИМбпST и нестабильной стенокардией, которым проводится первичное ЧКВ.
Облегченное ЧКВ
- Облегченное ЧКВ — это использование фармакологической реперфузионной терапии, проводимой до планового ЧКВ.
- Нет доказательств значительного клинического преимущества, поэтому облегченное ЧКВ в настоящее время не рекомендуется.
Rescue PCI
- Rescue PCI определяется как PCI, выполняемая на коронарной артерии, которая остается окклюзированной, несмотря на фибринолитическую терапию.
- Rescue PCI ассоциируется со значительным сокращением сердечной недостаточности и повторного инфаркта, а также со снижением смертности от всех причин, поэтому его следует учитывать при наличии доказательств неудачного фибринолиза на основании клинических признаков и недостаточного разрешения сегмента ST, если имеется клиническое или ЭКГ-свидетельство обширного инфаркта и возможность проведения процедуры менее чем через 12 часов после появления симптомов.
Фибринолитические препараты
Пациентам, которым нельзя предложить ЧКВ в течение 120 минут после того, как должно было быть назначено фибринолиз, следует вводить тромболитический препарат вместе с нефракционированным гепарином (максимум два дня) или низкомолекулярным гепарином. (например, эноксапарин) или фондапаринукс.Тромболитические препараты разрушают тромб, чтобы можно было восстановить приток крови к сердечной мышце, чтобы предотвратить дальнейшее повреждение и способствовать заживлению.
Реперфузия путем тромболизиса часто бывает постепенной, неполной и может быть недостаточной. Существует риск ранней или поздней повторной окклюзии и 1-2% риска внутричерепного кровотечения.
- Фибринолитические препараты действуют как тромболитики, активируя плазминоген с образованием плазмина, который разрушает фибрин и таким образом разрушает тромбы.
- Доказано, что стрептокиназа и альтеплаза снижают смертность.Ретеплаза и тенектеплаза также лицензированы для лечения ОИМ.
- Стрептокиназа и альтеплаза вводятся внутривенно. Ретеплазу и тенектеплазу можно вводить путем быстрой болюсной инъекции.
- Преимущество наиболее велико у пациентов с изменениями ЭКГ, включающими подъем сегмента ST (особенно у пациентов с передним инфарктом), и у пациентов с блокадой ножек пучка Гиса.
- Чем раньше будет проведено лечение, тем больше будет абсолютная польза. Альтеплазу, ретеплазу и стрептокиназу необходимо вводить в течение 12 часов с момента появления симптомов, в идеале — в течение одного часа.Тенектеплазу следует назначать как можно раньше и обычно в течение шести часов после появления симптомов.
- Осложнения, связанные с кровотечением, являются основным риском, связанным с тромболизисом. Противопоказания к тромболизису включают пациентов с нарушениями свертываемости крови или недавнее кровотечение, травму, операцию или острое цереброваскулярное событие в анамнезе.
- Сохранение антител к стрептокиназе может снизить эффективность последующего лечения, поэтому стрептокиназу не следует использовать повторно после первого введения.
Пациенты, которым не проводилась реперфузионная терапия
[4]- Пациентам с ИМпST, поступившим в течение 12 часов после появления симптомов, но реперфузионная терапия не проводилась, или пациентам, поступившим через 12 часов, предложите тикагрелор как часть двойная антитромбоцитарная терапия с аспирином, если только они не имеют высокого риска кровотечения.
- Рассмотрите возможность применения клопидогреля в составе двойной антитромбоцитарной терапии с аспирином или только аспирином для людей с острым ИМпST, не получавших ЧКВ, если у них есть высокий риск кровотечения.
- Пациентам, не получающим реперфузионную терапию, рекомендуется ангиография перед выпиской из стационара (как и пациентам после успешного фибринолиза) при отсутствии противопоказаний.
Операция коронарного шунтирования
- Лишь немногим пациентам в острой фазе требуется АКШ, но может быть показана АКШ:
- После неудачного ЧКВ, коронарной окклюзии, не поддающейся ЧКВ, или наличия рефрактерных симптомов после ЧКВ.
- Кардиогенный шок или механические осложнения, например разрыв желудочка, острая митральная регургитация или дефект межжелудочковой перегородки.
- Многососудистая болезнь.
- Пациентам с неэкстренными показаниями для АКШ (например, при мультисистемном заболевании) рекомендуется лечить инфаркт-зависимое поражение с помощью ЧКВ и, если возможно, выполнить АКШ позже, в более стабильных условиях.
Другое начальное лечение
- Антитромбоцитарный агент:
- Долгосрочный прием низких доз аспирина снижает общую смертность, нефатальный повторный инфаркт, нефатальный инсульт и сосудистую смерть.
- Клопидогрель в комбинации с низкими дозами аспирина рекомендуется при ОИМ с подъемом сегмента ST; комбинация лицензирована на срок не менее четырех недель, но оптимальная продолжительность лечения не установлена.Также было показано, что лечение клопидогрелом и аспирином в течение одного года после ЧКВ является рентабельным [10] .
- Монотерапия клопидогрелом является альтернативой, когда аспирин противопоказан.
- Тикагрелор в сочетании с низкими дозами аспирина рекомендован NICE на срок до 12 месяцев в качестве варианта лечения взрослых с ИМпST, которые кардиологи намереваются лечить с помощью первичного PCI [11] . Эта комбинация также предлагается там, где не предполагается ЧКВ, за исключением случаев высокого риска кровотечения.В таких случаях следует рассмотреть возможность применения клопидогреля с аспирином или только аспирина.
- Бета-адреноблокаторы:
- При применении в течение нескольких часов после инфаркта бета-адреноблокаторы снижают смертность, нефатальную остановку сердца и нефатальный повторный инфаркт.
- Если нет противопоказаний, обычно вводят внутривенно при поступлении, а затем продолжают перорально — увеличивая дозу до максимально переносимой.
- Блокаторы кальциевых каналов дилтиазем или верапамил можно использовать, если нельзя использовать бета-адреноблокаторы, но дилтиазем и верапамил противопоказаны пациентам с дисфункцией левого желудочка.
- Ингибиторы ангиотензинпревращающего фермента (АПФ):
- Они снижают смертность независимо от того, есть ли у пациентов клиническая сердечная недостаточность или дисфункция левого желудочка. Они также снижают риск сердечной недостаточности без летального исхода.
- Увеличьте дозу до максимально переносимой или целевой дозы. Измерьте функцию почек, электролиты и артериальное давление перед началом приема ингибитора АПФ (или антагониста рецепторов ангиотензина-II) и еще раз в течение 1-2 недель.
- Агенты, снижающие холестерин:
- В идеале, если нет противопоказаний, начинать терапию статинами как можно скорее для всех пациентов с признаками сердечно-сосудистых заболеваний (ССЗ).
- Пациенты с фракцией выброса левого желудочка 0,4 или меньше и диабетом или клиническими признаками сердечной недостаточности должны получать эплеренон, антагонист альдостерона (начинать в течение 3-14 дней после инфаркта миокарда и в идеале после терапии ингибиторами АПФ), если только противопоказан почечной недостаточностью или гиперкалиемией (функция левого желудочка должна быть оценена у всех пациентов с ОИМ при первичной госпитализации) [3] .
- Другое лечение:
- Инфузия гепарина используется как дополнительное средство у пациентов, получающих альтеплазу, но не стрептокиназу.Гепарин также показан пациентам, перенесшим первичную ангиопластику.
- Профилактика тромбоэмболии: если гепарин еще не вводится в виде инфузии, пациентам следует регулярно вводить гепарин подкожно, пока они не станут полностью подвижными.
- Инфузия инсулина и глюкозы с последующим интенсивным контролем уровня глюкозы подкожным инсулином для всех людей с диабетом 1 и 2 типа.
- Рутинное использование нитратов, антагонистов кальция, магния и инфузии высоких доз глюкозы, инсулина и калия в настоящее время не рекомендуется во время острой фазы лечения ОИМ.
Оценка сердца и реваскуляризация
Ранняя оценка риска поможет выявить пациентов с высоким риском, которым может потребоваться дальнейшее раннее лечение с помощью ангиографии и коронарной реваскуляризации. Методы кардиологического обследования различаются в зависимости от наличия и опыта в данной местности.
- Регулярное тестирование ЭКГ с физической нагрузкой: субмаксимальное тестирование все чаще проводится перед выпиской из больницы через 4-7 дней. Симптомно-ограниченный тест может быть проведен через 3-6 недель после инфаркта, чтобы оценить прогноз и выявить пациентов с обратимой ишемией (у которых затем должна быть ангиограмма для оценки необходимости АКШ).
- Визуализирующая сцинтиграфия перфузии миокарда с использованием однофотонной эмиссионной компьютерной томографии (ОФЭКТ) может быть выполнена перед выпиской из больницы для оценки степени остаточной ишемии, если пациент еще не прошел катетеризацию сердца и ангиографию. NICE рекомендует, чтобы перфузионная сцинтиграфия миокарда с использованием ОФЭКТ была первым тестом, используемым для [12] :
- Людям, у которых стресс-ЭКГ может не давать точных или четких результатов — например, женщины, люди с определенными необычными паттернами электрической активности их сердце, люди с диабетом или люди, для которых упражнения трудно или невозможно.
- Диагноз для людей, которые с меньшей вероятностью страдают ишемической болезнью сердца и имеют более низкий риск возникновения проблем с сердцем в будущем. Вероятность того, что человек страдает ишемической болезнью сердца, можно оценить, рассматривая ряд факторов — например, возраст, пол, этническое происхождение и семейный анамнез, а также результаты медицинского осмотра и обследований.
- В качестве исследования с участием людей, у которых все еще есть симптомы инфаркта миокарда или несмотря на то, что они прошли курс лечения для улучшения кровотока в коронарной артерии.
- Эхокардиография полезна, если диагноз ставится под сомнение, может определить степень инфаркта и выявить осложнения, такие как острая митральная регургитация, разрыв левого желудочка или выпот в перикард.
- В идеале коронарная ангиография должна выполняться всем пациентам до выписать из больницы.
Дальнейшее ведение пациентов после инфаркта миокарда
[4]См. Отдельную статью об оценке риска сердечно-сосудистых заболеваний.
Вождение после острых коронарных синдромов (включая острый инфаркт миокарда)
[13]- Право группы 1: обычные водительские права на автомобиль или мотоцикл:
- В случае успешного лечения коронарной ангиопластикой вождение можно возобновить через неделю, при условии :
- Никакой другой СРОЧНОЙ реваскуляризации не планируется (в течение четырех недель после острого события).
- Фракция выброса левого желудочка (доля крови, откачиваемой из левого желудочка при каждом сокращении сердца) до выписки из больницы составляет не менее 40%.
- Других дисквалифицирующих условий нет.
- В случае неудачного лечения коронарной ангиопластикой вождение автомобиля может возобновиться через четыре недели при отсутствии других дисквалифицирующих условий.
- Агентство по лицензированию водителей и транспортных средств (DVLA) не нужно уведомлять.
- В случае успешного лечения коронарной ангиопластикой вождение можно возобновить через неделю, при условии :
- Право группы 2: профессиональные водители крупногабаритных грузовых автомобилей или пассажирских транспортных средств:
- Все острые коронарные синдромы лишают владельца водительских прав права на вождение на срок не менее шести недель.
- После этого может быть разрешено повторное лицензирование при условии:
- Требования к упражнениям / другим функциональным тестам могут быть выполнены.
- Других дисквалифицирующих условий нет.
- Фракция выброса левого желудочка ниже 40% считается ограничением для группы 2.
- Необходимо уведомить DVLA.
Работа
- Рекомендации будут зависеть от типа работы, общего состояния здоровья пациента, тяжести инфаркта и осложнений.
- В большинстве случаев возвращение на работу не должно откладываться более чем на три месяца, поскольку с течением времени вероятность успешного возвращения снижается.
- Пациентам, перенесшим остановку сердца или перенесшим АКШ, обычно требуется больше времени для восстановления физического и умственного развития и может потребоваться перерыв на работу до шести месяцев.
Осложнения после инфаркта миокарда
См. Отдельную статью «Осложнения острого инфаркта миокарда».
Сокращение продолжительности пребывания в больнице по поводу острого инфаркта миокарда и исходы после выписки: взгляд в масштабах всего сообщества | Острые коронарные синдромы | JAMA Internal Medicine
Фон Цели этого популяционного исследования заключались в описании тенденций более чем десятилетнего периода (1986-1999 гг.) В отношении продолжительности госпитализации после острого инфаркта миокарда (ОИМ), характеристик пациентов, связанных с различной продолжительностью пребывания в стационаре, и влияния сокращения продолжительности госпитализации. оставайтесь на уровне послеродовой смертности.
Методы Выборка для исследования состояла из 4551 пациента, выписанного после ОИМ из всех больниц в Вустере, штат Массачусетс, за 8 периодов в год в течение периода исследования. Для изучения влияния демографических, клинических и лечебных переменных на продолжительность пребывания в стационаре и связи между сокращением продолжительности пребывания в стационаре и смертностью после выписки использовались регрессионные модели.
Результаты Заметное снижение средней продолжительности пребывания наблюдалось в период с 1986 по 1988 год (11.7 дней) и 1997-1999 гг. (5,9 дней). Факторы, связанные с более длительным пребыванием в больнице, включали пожилой возраст, женский пол, передний ИМ и ИМ с зубцом Q, а также возникновение клинически важных сердечных осложнений. Пациенты, имеющие медицинскую организацию, Medicare, Medicaid или не имеющие страхового покрытия, с меньшей вероятностью будут иметь увеличенный срок пребывания. Повышенная 30- и 90-дневная смертность была связана с продолжительностью пребывания в больнице более 14 дней (отношение шансов 2,08; 95% доверительный интервал 1,18–3.66) по сравнению с пациентами с продолжительностью пребывания от 6 до 8 дней (отношение шансов 2,01; 95% доверительный интервал 1,34–3,01). У пациентов с продолжительностью пребывания менее 6 дней не наблюдалось значительного увеличения смертности после выписки. Аналогичные тенденции наблюдались у пациентов с осложненным ОИМ.
Выводы Мы обнаружили заметное сокращение продолжительности госпитализации пациентов с ОИМ за последнее десятилетие. Однако мы не обнаружили отрицательной связи между сокращением продолжительности пребывания в стационаре и краткосрочной смертностью после выписки из больницы по поводу ОИМ.
Продолжительность госпитализации пациентов с острым инфарктом миокарда (ОИМ) выросла из продолжительного постельного режима и реабилитации более 6 недель в 1950-х годах до нынешней продолжительности пребывания в больнице менее 1 недели. Активное использование подходов к коронарной реваскуляризации и широкое признание психологических и медицинских преимуществ раннего передвижения привели к значительному сокращению продолжительности пребывания в больнице для пациентов с ОИМ.В Соединенных Штатах типичная продолжительность пребывания пациентов с неосложненным ОИМ в настоящее время составляет около 5 дней. Однако существуют значительные различия в продолжительности госпитализации пациентов с ОИМ. На эту изменчивость влияют клинические, медицинские и социально-экономические факторы. В частности, врачи испытывают растущее давление со стороны поставщиков медицинского страхования и своих собственных учреждений с целью выписки пациентов из больницы как можно быстрее.
Хотя четкие тенденции в сокращении сроков пребывания в больнице после ОИМ были очевидны в течение последнего десятилетия, оптимальные сроки выписки были предметом тщательного изучения из-за потенциальных медицинских и экономических последствий ранней или поздней выписки.В пользу политики ранней выписки у пациентов с острой ишемической болезнью сердца свидетельствуют данные клинических испытаний. 1 , 2 Результаты этих исследований позволяют предположить, что выписка из больницы после ОИМ может быть безопасной для надлежащим образом отобранных пациентов уже через 3 дня после острого индексного события. 2 Хотя потенциальная экономия средств, связанная с сокращением продолжительности пребывания, значительна, влияние ранней выписки из больницы после ОИМ на использование и титрование постинфарктной медикаментозной терапии, обеспечение обучения пациентов, а также выявление и лечение ранних и потенциально серьезных клинические осложнения могут быть опасными.
Учитывая масштабы, а также общественное здоровье и клинические последствия ишемической болезни сердца в Соединенных Штатах и других промышленно развитых странах, 3 важно изучить, оказали ли текущие тенденции в политике выписки из больниц пациентов с ОИМ неблагоприятное влияние на их состояние. уровень смертности после выписки. Цель настоящего исследования — описать с многобольничной популяционной точки зрения тенденции более чем десятилетнего опыта (1986-1999 гг.) В продолжительности госпитализации после ОИМ и потенциальное влияние сокращения продолжительности пребывания на смертность после выписки. выживших в больнице.Период нашего исследования включает в себя тромболитическую эру и все более агрессивное лечение ОИМ.
Пациенты, выписанные из всех 16 больниц стандартного столичного статистического района Вустера, штат Массачусетс, за 8 периодов в год в 1986, 1988, 1990, 1991, 1993, 1995, 1997 и 1999 годах после госпитализации по поводу первичной или вторичной выписки с диагнозом ОИМ ( International Классификация болезней, девятая редакция [ ICD-9 ] код 410) составляют исследуемую популяцию настоящего отчета.Эти учебные годы были выбраны на основе наличия финансирования и с целью изучения изменений с течением времени в наших основных конечных точках нашего исследования примерно на ежегодной основе. Медицинские карты всех пациентов с диагнозом ОИМ при выписке из этих больниц были индивидуально рассмотрены и подтверждены в соответствии с заранее установленными диагностическими критериями, которые были подробно описаны ранее. 4 -6 Вкратце, эти критерии включали в себя клинический анамнез длительной боли в груди, не купирующейся отдыхом или использованием нитратов, повышение уровня ферментов сыворотки выше верхнего контрольного предела, установленного лабораторией в каждой больнице, и серийные электрокардиографические записи во время госпитализации, показывающие изменения сегмента ST и / или зубца Q, типичные для ОИМ.Случайная выборка медицинских записей из дополнительных диагностических рубрик, в которых мог быть поставлен диагноз ОИМ (например, МКБ-9 коды 411-414), также выполнялась в течение каждого из исследуемых лет, чтобы охватить всех географически подходящих пациентов, госпитализированных с AMI. Исключались пациенты с периоперационным ОИМ. Клинические осложнения ОИМ оценивались на основании информации из медицинских карт. Эти важные клинические осложнения включали сердечную недостаточность, кардиогенный шок, полную блокаду сердца, рецидивирующую стенокардию, фибрилляцию предсердий и инсульт. 7 -10
Настоящий отчет основан на данных о 4551 жителе столичного региона Вустера, которые соответствовали диагностическим критериям ОИМ в 8 обследованных периодах исследования и были выписаны из всех районных больниц. Пациенты с длительностью пребывания в больнице более 1 месяца, переводы (в или из исследуемых больниц) и пациенты, перенесшие операцию по аортокоронарному шунтированию, были исключены. Чтобы сделать анализ данных более интерпретируемым и совпасть с изменениями в лечении пациентов с ОИМ, эти 8 отдельных лет исследования были объединены в 4 периода для целей анализа.В общей сложности 896 жителей города Вустер с подтвержденным AMI, отвечающим этим критериям, были госпитализированы в период 1986–1988 годов, 1050 — в период 1990–1991 годов, 1275 — в период 1993–1995 годов и 1330 — в период 1997–1999 годов.
Из больничных карт пациентов с подтвержденным ОИМ были извлечены демографические и клинические данные, включая возраст, пол, историю болезни, тип страхового покрытия, осложнения во время госпитализации (например, застойная сердечная недостаточность, кардиогенный шок, полная блокада сердца, рецидив стенокардии, фибрилляция предсердий и инсульт), порядок ОИМ (начальный или предшествующий), тип (зубец Q или не зубец Q) и расположение (передний или нижний / задний).Также были проанализированы истории болезни для выявления использования различных кардиологических препаратов и процедур (например, катетеризация, чрескожное коронарное вмешательство) во время основной госпитализации. 11 Подходы, использованные для определения выживаемости после выписки из каждой из участвовавших в исследовании больниц, включали анализ записей о дополнительных госпитализациях и поиск свидетельств о смерти жителей стандартного столичного статистического района Вустера по всему штату и на национальном уровне.Некоторое дополнительное наблюдение проводилось у большинства выписанных из исследования пациентов (примерно 99%). Последующее наблюдение проводилось до конца 2001 календарного года. Для целей настоящего анализа мы исследовали статус выживаемости через 1 и 3 месяца после выписки из больниц общего профиля. Эти временные точки были выбраны таким образом, чтобы мы могли исследовать периоды в разумной близости от индексной госпитализации, на которые может повлиять преждевременная выписка из больницы после ОИМ. Мы не смогли удовлетворительно провести анализ связи между продолжительностью пребывания в больнице и 7-дневным уровнем смертности после выписки, учитывая небольшое количество смертей, происходящих в этот период.Несмотря на более высокий уровень смертности через 6 и 12 месяцев после выписки из больницы и увеличение количества смертельных исходов для проведения нашего анализа, мы не исследовали взаимосвязь между продолжительностью пребывания в больнице и этими более длительными периодами после выписки. Это произошло из-за потенциально смешивающего влияния других клинических и лечебных факторов, которые могли повлиять на эти показатели смертности, а также из-за трудности интерпретации любых наблюдаемых связей между продолжительностью пребывания в больнице и этими более продолжительными смертями после выписки.
Мы исследовали различия в распределении выбранных характеристик у пациентов с разной продолжительностью пребывания в стационаре в соответствии с критериями статистической значимости χ 2 для тенденций в категориальных переменных и дисперсионного анализа для непрерывных переменных.
Мы использовали логистический многомерный регрессионный анализ, чтобы изучить связь между демографическими, клиническими и лечебными переменными и большей продолжительностью пребывания в стационаре, чем медиана.Переменные, которые контролируются в этом анализе, включали возраст, пол, статус плательщика страховки, историю болезни (например, стенокардию, инсульт, гипертензию, сахарный диабет и сердечную недостаточность), характеристики, связанные с ОИМ (исходные и предыдущие, передние и нижние / задние, Q волна против не зубца Q), больничные клинические осложнения (например, сердечная недостаточность, кардиогенный шок, полная блокада сердца, рецидивирующая стенокардия, фибрилляция предсердий и инсульт), прием любых эффективных сердечных препаратов (определяемых как прием аспирина, β-адреноблокаторов , ингибиторы ангиотензинпревращающего фермента [АПФ], средства для снижения уровня липидов или тромболитики), прием других сердечных препаратов (антагонистов кальция или антиаритмических средств) и проведение кардиологической процедуры (например, катетеризация сердца или чрескожная реваскуляризация) во время индекс госпитализации.
Поскольку продолжительность пребывания в больнице и связанные с ней исходы после выписки связаны с возникновением клинических осложнений во время острой госпитализации, мы также провели анализ подгрупп пациентов с осложненным ОИМ. Для целей этого анализа сложный ОИМ считался присутствующим, когда сердечная недостаточность, кардиогенный шок, полная блокада сердца, рецидивирующая стенокардия, фибрилляция предсердий или инсульт развивались в любое время в течение основной госпитализации.
Мы использовали метод таблицы дожития для изучения различий в выживаемости после выписки в зависимости от продолжительности пребывания в больнице, включая пациентов из разных периодов времени и с разной продолжительностью наблюдения. Логистический многовариантный скорректированный регрессионный анализ использовался для изучения связи между продолжительностью пребывания в больнице и смертностью после выписки через 30 и 90 дней после выписки из больницы. Первоначально анализ проводился с учетом ранее описанных демографических и клинических переменных с объединением нескольких различных переменных (например, истории болезни, эффективных сердечных препаратов и клинических осложнений) в отдельные категориальные переменные, чтобы сделать аналитические модели более надежными.Для каждой из наших конечных точек после выписки мы затем повторили анализ, контролирующий все полученные лекарства (эффективные и другие кардиологические) и все кардиологические процедуры (катетеризация сердца и чрескожные коронарные вмешательства), в дополнение к ранее описанным потенциальным искажающим факторам. Наконец, мы также выполнили серию дополнительных регрессионных анализов, в которых ранее агрегированные демографические, клинические и лечебные факторы были разделены на их индивидуальные переменные.Результаты этих регрессионных анализов соответствовали результатам нашего более раннего анализа, за исключением тех, кто относился к самой высокой категории продолжительности пребывания (≥14 дней), у которых результаты были несколько ослаблены. Отношения шансов (OR), скорректированные с учетом нескольких переменных, с соответствующими 95% доверительными интервалами (CI) были рассчитаны стандартным способом.
Описательные характеристики исследуемой выборки в зависимости от продолжительности пребывания в больнице представлены в таблице 1.Продолжительность госпитализации была разделена на 6 групп на основе распределения наших данных о продолжительности пребывания и на основании того, что можно было бы рассматривать как краткосрочную госпитализацию по сравнению с более продолжительной госпитализацией для пациентов с ОИМ.
Пациенты с более коротким сроком пребывания были моложе, с большей вероятностью были мужчинами, и с большей вероятностью были зарегистрированы в организации по поддержанию здоровья или не имели медицинской страховки. У этих пациентов реже был передний ИМ или ИМ с зубцом Q.Они были значительно реже испытывали каждое из изученных клинических осложнений. Пациенты с более коротким пребыванием в больнице чаще получали аспирин, β-адреноблокаторы, ингибиторы АПФ или средства для снижения уровня липидов, но с меньшей вероятностью получали лечение антагонистами кальция или антиаритмическими средствами. Чрескожная реваскуляризация использовалась больше всего у пациентов с предельной продолжительностью пребывания по сравнению с пациентами с более промежуточным пребыванием.
С середины 80-х годов прошлого века произошли заметные изменения в распределении продолжительности пребывания пациентов с ОИМ (рис. 1).Средняя продолжительность пребывания снизилась с 11,7 дней в период 1986-1988 годов до 5,9 дней в период 1997-1999 годов. В период 1986-1988 годов примерно 60% пациентов были госпитализированы на 10 или более дней по сравнению с примерно 10% пациентов в период 1997-1999 годов. С другой стороны, менее 4% пациентов с ОИМ были выписаны из районных больниц менее чем за 6 дней в период 1986-1988 годов по сравнению с более чем половиной в период 1997-1999 годов.
Факторы, связанные с более длительным пребыванием в больнице
На основе наблюдаемых одномерных ассоциаций связь между определенными демографическими и клиническими переменными с более длительным пребыванием в больнице (продолжительность пребывания в больнице превышает медианное значение для каждого года исследования) была изучена с использованием моделирования логистической регрессии (таблица 2).Демографические факторы, связанные с более длительным пребыванием, включали пожилой возраст и женский пол. Возникновение каждого из исследуемых клинических осложнений, особенно развития инсульта или кардиогенного шока, было тесно связано с увеличением продолжительности пребывания в стационаре. Пациенты с зубцом Q или передним инфарктом миокарда с большей вероятностью будут находиться в больнице в течение длительного времени, равно как и пациенты, получающие другие кардиологические препараты или перенесшие кардиологические процедуры. По сравнению с пациентами со страховкой Blue Cross / Blue Shield, пациенты с медицинскими организациями, Medicaid, Medicare или без покрытия имели значительно меньшую вероятность более длительного пребывания в больнице.Пациенты, получавшие эффективные кардиологические препараты, реже имели длительное пребывание.
Связь между сокращением продолжительности пребывания в больнице и смертностью после выписки
Показатели смертности от всех причин через 1 и 3 месяца после выписки из больницы из-за ОИМ были изучены для оценки связи между продолжительностью пребывания в стационаре в течение последних полутора десятилетий и выживаемостью после выписки.Общие показатели 30- и 90-дневной смертности не претерпели значительных изменений между начальным (1986-1988 гг.) И последним периодом исследования (1997-1999 гг.) (30-дневная смертность, 3,5% против 2,7%, соответственно; 90-дневная смертность. , 7,0% против 5,9%, соответственно), несмотря на сокращение продолжительности пребывания в этот период. Сто сорок девять пациентов (3,3%) умерли в течение первого месяца после выписки из больницы, тогда как 319 пациентов (7,0% от общей выборки исследования) умерли в течение первых 3 месяцев после выписки из больницы.
Мы исследовали связь между продолжительностью пребывания в стационаре и уровнем смертности после выписки в рамках модели регрессии с множеством переменных.После одновременного контроля различных демографических, медицинских и клинических характеристик пациенты с длительностью пребывания в больнице 14 дней и более имели значительно повышенный риск смерти через 30 и 90 дней после выписки из больницы по сравнению с референтной категорией пациентов с продолжительность пребывания от 6 до 7,9 суток (таблица 3). Пациенты с продолжительностью пребывания менее 6-7,9 дней не имели значительных различий в показателях смертности через 30 и 90 дней после выписки из больниц большего Вустера по сравнению с референтной группой.Несмотря на то, что его мощность была недостаточной, из-за сравнительно небольшого количества смертей после выписки, имевших место в первые 7 дней после выписки из больницы, при использовании этой точки отсечения времени после выписки наблюдались тенденции, аналогичные результатам нашего основного исследования. Пациенты, находившиеся в больнице менее 6 дней, имели не большую вероятность умереть в течение первой недели после выписки из больницы, чем пациенты, выписанные после более длительного пребывания в больнице. Многофакторный регрессионный анализ, оценивающий влияние сокращения продолжительности пребывания с течением времени на показатели смертности после выписки с учетом аналогичных демографических, медицинских и клинических переменных, не выявил значительных изменений в вероятности смерти через 30 или 90 дней после выписки из больницы в период с 1986 г. -1988 и 1997-1999 периоды (данные не показаны).
Мы также выполнили дополнительный анализ, изучая связь между продолжительностью пребывания в больнице и 30- и 90-дневными показателями смертности, рассчитанными с момента поступления в больницу (в отличие от выписки из больницы). Были отмечены практически идентичные тенденции с теми, которые ранее наблюдались при использовании выписки из больницы в качестве начальной точки анализа. Например, многовариантные скорректированные шансы смерти в первые 90 дней после поступления в больницу составили 1,03 (95% ДИ, 0,55–1,95), 1.10 (95% ДИ, 0,71–1,72), 1,10 (95% ДИ, 0,72–1,69), 1,34 (95% ДИ, 0,88–2,02) и 2,01 (95% ДИ, 1,33–3,06) для пациентов, которые испытали длительность пребывание в больнице менее 4, от 4 до 5,9, от 8 до 9,9, от 10 до 13,9 и 14 или более дней соответственно.
Острые клинические осложнения и уровень смертности после выписки
Примерно три пятых исследуемых пациентов испытали осложненный ОИМ в период исследования.Частота этих осложнений колебалась от 54% в 1986–1988 гг. До 55% в периоды 1997–1999 гг. Поскольку пациенты с осложненным ОИМ представляют собой группу с особенно высоким риском смертности после выписки, мы исследовали 30- и 90-дневные показатели смертности после выписки отдельно у выживших после осложненного ОИМ в зависимости от продолжительности пребывания в больнице (Таблица 4). По сравнению с пациентами с продолжительностью пребывания в больнице от 6 до 7,9 дней, у этих пациентов с высоким риском не наблюдалось неблагоприятной связи между более коротким пребыванием в больнице и прогнозом после выписки в течение периода до 90 дней после выписки из больницы.Подобные ассоциации наблюдались при использовании более строгих определений осложненного ОИМ или когда эти показатели рассчитывались с момента поступления в больницу, а не с момента выписки из больницы.
Результаты этого популяционного обсервационного исследования предполагают заметные изменения во времени в медиане и распределении продолжительности пребывания в выборке пациентов, госпитализированных с подтвержденным ОИМ в типичном северо-восточном мегаполисе, в масштабах всего сообщества.Средняя продолжительность пребывания снизилась с примерно 12 дней в период 1986–1988 годов до 6 дней в период 1997–1999 годов. Возможно, еще более впечатляющим было более чем 10-кратное увеличение доли пациентов, выписанных из районных больниц менее чем за 6 дней в течение этого периода.
Большая часть наблюдаемого сокращения продолжительности пребывания в больнице может быть связана с улучшением лечения ОИМ, включая более широкое использование методов коронарной реперфузии. Предыдущие результаты Вустерского исследования сердечного приступа документально подтвердили приблизительное удвоение использования тромболитической терапии или чрескожных коронарных вмешательств с середины 1980-х до конца 1990-х годов. 6 Использование эффективных адъювантных методов лечения (аспирин, β-блокаторы и ингибиторы АПФ) за этот период возросло еще более резко. 7 Хотя причинно-следственная связь не может быть выведена из этих данных, прием одного или более эффективных сердечных препаратов защитил от увеличения продолжительности пребывания в настоящем исследовании. Можно ожидать, что использование этих полезных методов лечения повлияет на частоту возникновения большинства клинически значимых осложнений, связанных с ОИМ, которые в нашем исследовании были самыми сильными предикторами увеличения продолжительности пребывания в стационаре.
Мы признаем, что другие доклинические факторы могут играть важную роль в наблюдаемом сокращении продолжительности пребывания в больнице. Ограниченные ресурсы здравоохранения, фиксированные платежи по конкретному диагнозу и сокращение возмещения расходов по программе Medicare наносят финансовый ущерб бюджетам большинства больниц. Неудивительно, что сокращение продолжительности пребывания пациентов с ОИМ стало популярным пунктом бюджетной повестки дня для многих администраторов больниц. Даже после учета других потенциально мешающих факторов вероятность того, что пациенты, имеющие медицинскую организацию или страховку Medicare, будут находиться в больнице на длительный срок, значительно ниже, чем у пациентов со страховкой Blue Cross / Blue Shield.
Снижение продолжительности пребывания в больнице и смертности после выписки
Важнейший вопрос, рассматриваемый в нашем наблюдательном исследовании, заключается в том, связано ли сокращение продолжительности пребывания с течением времени неблагоприятным образом с исходами пациентов после выписки из больницы. Учитывая значительные достижения в терапевтическом лечении ОИМ с течением времени, любой потенциально неблагоприятный эффект преждевременной выписки из больницы трудно изолировать.
Результаты нашего грубого и скорректированного по нескольким параметрам регрессионного анализа не выявили никаких доказательств связи между сокращением продолжительности пребывания в стационаре и выживаемостью после выписки, рассчитанной с момента поступления или выписки из больницы. Грубые и многопараметрические скорректированные 30- и 90-дневные показатели смертности после выписки существенно не изменились с середины 1980-х до конца 1990-х годов. Даже после корректировки на год исследования и различные методы лечения (в дополнение к другим потенциальным прогностическим факторам) мы не смогли наблюдать какой-либо отрицательной связи между сокращением продолжительности пребывания в стационаре и смертностью после выписки.Насколько нам известно, это первое популяционное исследование, описывающее тенденции продолжительности госпитализации пациентов с ОИМ, в котором также изучалась связь между продолжительностью госпитализации и смертностью после выписки из больницы.
В предыдущих исследованиях была предпринята попытка оценить влияние более короткой продолжительности пребывания на исходы, связанные с пациентом, путем сравнения больниц или регионов с разной продолжительностью пребывания в течение одного и того же периода времени. К сожалению, эти исследования были ограничены небольшим размером выборки, ограниченными данными о результатах или отдаленными периодами исследования.При анализе пациентов Medicare, госпитализированных в 1985 г., средняя продолжительность пребывания пациентов с ОИМ в Калифорнии (8,1 дня) была значительно короче, чем у пациентов из Нью-Йорка (12,4 дня). 12 Показатели летальности в больницах были ниже в Калифорнии (21% против 24%), но амбулаторная смертность через 30 дней была значительно выше в Калифорнии (4%) по сравнению с Нью-Йорком (1%), что привело к аналогичным 30-дневным показателям. дневная смертность. Другое исследование 394 пациентов с ОИМ выявило значительные различия в средней продолжительности пребывания (примерно 2 дня) между пациентами, госпитализированными в учебные больницы на Северо-Востоке, по сравнению с пациентами на Западном побережье. 13 Однако никаких существенных различий в связанной с пациентом заболеваемости или функциональном статусе не наблюдалось в период от 3 до 12 месяцев после выписки из больницы. Гораздо более обширный анализ 9600 пациентов с ОИМ из 87 больниц в Онтарио, Канада, выявил еще большую вариабельность продолжительности пребывания в больнице, в среднем от 6,6 до 12,9 дней. 14 Только 12% этой вариации можно отнести к характеристикам пациентов и больниц. Продолжительность госпитализации не была существенно связана со смертностью в больнице после учета других потенциально искажающих переменных.К сожалению, в этом исследовании не анализировались показатели смертности после выписки.
В качестве альтернативы, ряд исследователей попытались выявить подгруппы пациентов с ОИМ, для которых ранняя выписка из больницы могла бы считаться целесообразной. В исследовании 80 пациентов, поступивших в Медицинский центр Мичиганского университета с 1986 по 1987 год с неосложненным ОИМ и без ишемии, спровоцированной тестом с физической нагрузкой, пациенты, рандомизированные для ранней выписки из больницы (день 3), имели аналогичную частоту повторной госпитализации, повторного инфаркта миокарда. или рецидивирующая стенокардия по сравнению с пациентами, выписанными в обычную больницу (7-10 дни). 15 Ни в одной из групп не было смертельных случаев. В 1986 г. 358 пациентов с ОИМ, не получавших тромболитической терапии, прошли скрининг Sanz et al. 16 Из них зубцы Q развились у 105, и они имели неосложненное раннее течение в стационаре. Эти пациенты проходили последующее наблюдение в среднем в течение 12 дней на предмет возникновения любого события, которое могло бы вызвать повторную госпитализацию, если бы была предпринята попытка более ранней выписки. У изучаемых пациентов чуть более четверти (28%) пережили сердечный приступ в течение этого периода, в том числе 4 случая смерти и 1 повторный инфаркт.Эти данные свидетельствуют о необходимости более строгих критериев для выявления пациентов с действительно низким риском ранней выписки из больницы.
Учитывая продолжающееся улучшение методов реперфузии и лечения острых коронарных артерий, исследователи Global Utilization t-PA for Occluded Coronary Arteries Trial (GUSTO) переоценили идентификацию группы пациентов с ОИМ с низким риском, подходящей для ранней выписки из больницы, почти десять лет. позже. 2 Используя более широкое определение неосложненного ИМ, исследователи охарактеризовали примерно 57% из 64 511 пациентов как имеющих неосложненный ИМ.В этом исследовании средняя продолжительность пребывания пациентов с осложненным или неосложненным ОИМ составляла 9 дней (8 дней в США), а 25% пациентов с неосложненным ОИМ оставались в больнице 12 и более дней. Пациенты в группе без осложнений имели значительно более низкие показатели 30-дневной смертности и госпитальных осложнений после 4-го дня. Результаты нашего исследования показывают, что у пациентов с осложненным ОИМ, независимо от используемого рабочего определения, не наблюдалось увеличения показателей смертности после выписки. выписывались из больниц Большого Вустера в более раннее время во время их первичной госпитализации.
Экстраполяция результатов рандомизированных испытаний (или реестров пациентов, включенных в эти испытания) на клиническую практику в условиях сообщества чревата опасностями. Часто практикующие врачи не принимают во внимание ограниченную возможность обобщения опубликованных исследований при обращении к своим пациентам. Исследования, подтверждающие сокращение продолжительности пребывания пациентов с ОИМ, в значительной степени основаны на исследованиях тромболитической терапии, используют строгие определения неосложненного ИМ и обеспечивают правильное использование дополнительных методов лечения.Наш обзор характеристик пациентов с продолжительностью пребывания менее 4 дней в нашем исследовании выявил значительную долю пациентов, которые не соответствуют критериям включения в анализ GUSTO-1. Наши данные свидетельствуют о том, что врачи рано выписывают из больницы пациентов со все более сложными состояниями. Например, 40% пациентов с продолжительностью пребывания менее 4 дней были 75 лет и старше, сердечная недостаточность развилась у 24% во время их госпитализации, а у 12% был 1 или более эпизодов рецидивирующей стенокардии перед выпиской из больницы.Этот вопрос требует дальнейшего изучения, если мы хотим минимизировать потенциальные опасности, связанные с политикой ранней выписки из больницы у пациентов с ОИМ. Многие из этих пациентов с высоким риском являются пожилыми людьми, у них большое бремя сопутствующих заболеваний, они становятся все более слабыми и имеют ограниченные ресурсы, чтобы помочь им в их выздоровлении.
Изучите сильные и слабые стороны
Исследование проводилось на популяции из четко определенной столичной области, социально-демографические и экономические характеристики которой отражают характеристики населения США в целом.Дополнительными сильными сторонами этого исследования являются включение большого числа пациентов с подтвержденным ОИМ, его популяционная перспектива, повышающая обобщаемость результатов исследования, и включение пациентов, госпитализированных во все районные больницы. Однако у этого исследования есть несколько ограничений. Хотя мы смогли описать множество факторов, связанных с ранней или поздней выпиской из больницы, вероятно, существуют другие факторы, связанные с пациентом, поставщиком медицинских услуг и системой здравоохранения, влияние которых на продолжительность пребывания в стационаре мы не смогли оценить.Кроме того, учитывая продолжающееся улучшение лечения пациентов с течением времени, остается трудным изолировать влияние сокращения продолжительности пребывания в стационаре за последнее десятилетие на заболеваемость и смертность. Из-за наших методов сбора данных мы также не смогли выяснить, увеличилась ли повторная госпитализация или риск острых ишемических осложнений по мере сокращения продолжительности пребывания в больнице, что важно для клиницистов и сторонников политики здравоохранения. Наконец, следует проявлять должную осторожность при интерпретации результатов нашего исследования.Это происходит из-за относительно небольшого числа смертей после выписки и отсутствия адекватных статистических данных для более систематического изучения ряда наблюдаемых ассоциаций.
Результаты этого популяционного исследования показывают заметное сокращение продолжительности пребывания в больнице для пациентов с ОИМ за последнее десятилетие. Несмотря на эти тенденции, нет никаких доказательств, подтверждающих отрицательную связь этих изменений в политике больниц с краткосрочной смертностью.Однако очевидно, что врачи выписывают все больше пациентов, прошедших сложный курс лечения в стационаре и подверженных повышенному риску неблагоприятных исходов. Влияние и безопасность ранней выписки у этих разнообразных подгрупп пациентов требуют дальнейшего изучения, равно как и потенциальная экономия затрат и психологическое влияние этих текущих тенденций в предоставлении медицинской помощи.
Автор для корреспонденции и оттиски: Фредерик А. Спенсер, доктор медицины, Отделение сердечно-сосудистой медицины, Медицинский факультет Массачусетского университета, 55 Lake Ave N, Вустер, Массачусетс 01655 (электронная почта: spencerf @ ummhc.org).
Принята к публикации 22 мая 2003 г.
Это исследование было поддержано грантом RO1 HL35434 Национального института сердца, легких и крови, Бетесда, штат Мэриленд,
.Мы благодарим администрацию, медицинские записи и кардиологические отделы участвующих больниц Вустера, Массачусетс, столичного округа, за их сотрудничество.
1. новичок LKCaliff RMGuerci А и другие.Ранняя выписка в тромболитическую эпоху: анализ критериев неосложненного инфаркта из исследования Global Utilization of streptokinase and t-PA for Occluded Coronary Arteries (GUSTO). J Am Coll Cardiol. 1996; 27625-632PubMedGoogle ScholarCrossref 2.Newby Л.К.изенштейн ELCaliff RM и другие. Экономическая эффективность ранней выписки после неосложненного острого инфаркта миокарда. N Engl J Med. 2000; 342749-755PubMedGoogle ScholarCrossref 3.Недоступно, Заболеваемость и смертность: Карточка 2000 по сердечно-сосудистым, легочным и кровяным заболеваниям. Бетесда, Мэриленд, Служба общественного здравоохранения, Национальные институты здравоохранения, 3000; 10
4. Голдберг. RJGore JMAlpert JSDalen JE. Последние изменения в частоте приступов и выживаемости при остром инфаркте миокарда (1975–1981 гг.): Вустерское исследование сердечного приступа. JAMA. 1986; 2552774-2779PubMedGoogle ScholarCrossref 5.Goldberg RJGorak Э. Я. Ярзебский J и другие.Общий взгляд на половые различия и временные тенденции в заболеваемости и выживаемости после острого инфаркта миокарда и внебольничных смертей, вызванных ишемической болезнью сердца. Тираж. 1993; 871947-1953PubMedGoogle ScholarCrossref 6.Goldberg Р.Я. Ярзебский JLessard DGore JM. Два десятилетия (1975–1995) продолжительный опыт в области заболеваемости, госпитальной и долгосрочной летальности от острого инфаркта миокарда: взгляд в масштабах всего сообщества. J Am Coll Cardiol. 1999; 331533-1539PubMedGoogle ScholarCrossref 7.Goldberg RJSamad Н.А.Ярзебский Дж. Гурвиц JBigelow CGore JM. Временные тенденции кардиогенного шока, осложняющего острый инфаркт миокарда. N Engl J Med. 1999; 3401162-1168PubMedGoogle ScholarCrossref 8. Спенсер FAMeyer Т.Е.Гольдберг RJ и другие. Двадцатилетние тенденции (1975–1995 гг.) В заболеваемости, госпитальной и долгосрочной смертности, связанной с сердечной недостаточностью, осложняющей острый инфаркт миокарда: перспектива в масштабах всего сообщества. J Am Coll Cardiol. 1999; 341378-1387PubMedGoogle ScholarCrossref 9. Спенсер FAJabbour SLessard D и другие. Тенденции за два десятилетия (1975–1997) в заболеваемости, госпитальной и долгосрочной смертности, связанной с полной блокадой сердца, осложняющей острый инфаркт миокарда: взгляд в масштабах всего сообщества. Am Heart J. 2003; 145500-507PubMedGoogle ScholarCrossref 10.Goldberg Р.Я. Ярзебский JLessard DWu JGore JM. Последние тенденции в уровне заболеваемости и смертности от фибрилляции предсердий, осложняющей начальный острый инфаркт миокарда: взгляд в масштабах всего сообщества. Am Heart J. 2002; 143519-527PubMedGoogle ScholarCrossref 11. Спенсер FScleparis Г.Гольдберг Р.Я. Ярзебский JLessard DGore JM Десятилетние тенденции (1986–1997) в лечении пациентов с острым инфарктом миокарда: взгляд в масштабах всего сообщества. Am Heart J. 2001; 142594-603PubMedGoogle ScholarCrossref 12.Jencks SFWilliams DKKay TL Оценка смертей, связанных с больницей, по данным выписки: роль продолжительности пребывания и сопутствующих заболеваний. JAMA. 1988; 2602240-2246PubMedGoogle ScholarCrossref 13.Cleary PDGreenfield SMulley AG и другие. Различия в продолжительности пребывания и исходах для шести медицинских и хирургических состояний в Массачусетсе и Калифорнии. JAMA. 1991; 26673-79PubMedGoogle ScholarCrossref 14.Chen Э.Эйлор CD Изменение продолжительности пребывания в больнице по поводу острого инфаркта миокарда в Онтарио, Канада. Med Care. 1994; 32420- 435PubMedGoogle ScholarCrossref 15.Тополь EJBurek Ко’Нил WW и другие. Рандомизированное контролируемое исследование выписки из больницы через три дня после инфаркта миокарда в эпоху реперфузии. N Engl J Med. 1988; 3181083-1088PubMedGoogle ScholarCrossref 16.Sanz GBetriu AOller грамм и другие. Возможность ранней выписки после острого инфаркта миокарда с зубцом Q у пациентов, не получающих тромболитического лечения. J Am Coll Cardiol. 1993; 221795-1801PubMedGoogle ScholarCrossrefОтвет пациентов, лечение и смертность от острого инфаркта миокарда во время пандемии COVID-19 | Европейский кардиологический журнал — Качество помощи и клинические результаты
Аннотация
Цели
COVID-19 мог повлиять на лечение и исходы госпитализированного острого инфаркта миокарда (ОИМ).Мы стремились определить, повлияла ли пандемия COVID-19 на реакцию пациентов, стационарное лечение и смертность от ОИМ.
Методы и результаты
Поступление было классифицировано как инфаркт миокарда без подъема сегмента ST (ИМпST) или ИМпST в 99 больницах Англии в результате кормления живым кормом в рамках Национального проекта аудита ишемии миокарда в период с 1 января 2019 г. по 22 мая 2020 г. Графики временных рядов были оценены с использованием 7-дневного простого скользящего среднего с поправкой на сезонность. С 23 марта 2020 г. (изоляция в Великобритании) среднее количество ежедневных госпитализаций снизилось еще больше для пациентов с ИМбпST [с 69 до 35; коэффициент риска заболеваемости (IRR) 0.51, 95% доверительный интервал (ДИ) 0,47–0,54], чем ИМпST (от 35 до 25; IRR 0,74, 95% ДИ 0,69–0,80) до надира 19 апреля 2020 г. Во время изоляции пациенты были моложе (средний возраст 68,7 vs. 66,9 лет), реже диабетом (24,6% против 28,1%) или цереброваскулярными заболеваниями (7,0% против 8,6%). При инфаркте миокарда с подъемом сегмента ST чаще проводилось первичное чрескожное коронарное вмешательство (81,8% против 78,8%), тромболизис был незначительным (0,5% против 0,3%), средняя продолжительность госпитализации на коронарную ангиографию при ИМбпST снизилась (26.2 против 64,0 ч), средняя продолжительность госпитализации уменьшилась (с 4 до 2 дней), рецепты фармакотерапии вторичной профилактики остались неизменными (каждый> 94,7%). Смертность через 30 дней увеличилась для ИМбпST [с 5,4% до 7,5%; отношение шансов (ОШ) 1,41, 95% ДИ 1,08–1,80], но уменьшилось для ИМпST (с 10,2% до 7,7%; ОШ 0,73, 95% ДИ 0,54–0,97).
Заключение
Во время COVID-19 значительно снизилось количество госпитализаций с ОИМ. Те, кто обратился в больницу, были моложе, имели меньше сопутствующих заболеваний и имели более высокую 30-дневную смертность от ИМбпST.
Введение
Чтобы уменьшить распространение COVID-19, многие страны ввели обязательные меры по социальному сдерживанию (так называемая «изоляция»), что привело к резкому сокращению передвижения местного населения, в том числе скорой помощи в больницах. 1 , 2 В ряде исследований описывается снижение количества пациентов с острым инфарктом миокарда (ОИМ), обращающихся в больницу в этот период, а некоторые предполагают, что люди с симптомами ОИМ могут откладывать или нет. обращение за помощью в службу скорой медицинской помощи. 3–8 Точно так же, готовясь к поступлению большого числа пациентов с вероятным COVID-19 и в ответ на них, больницы провели серьезную реорганизацию своих учреждений неотложной помощи, включая лаборатории катетеризации сердца. В заявлении о консенсусе экспертов Китайского общества кардиологов (CSC) рекомендовано медицинское лечение для большинства пациентов с инфарктом миокарда без подъема сегмента ST (ИМбпST) и тромболизисом у пациентов с ИМпST во время пандемии COVID-19. 9 Напротив, в Северной Америке и Канаде было предложено использовать тромболизис в качестве альтернативы первичному чрескожному коронарному вмешательству (ЧКВ) для пациентов с ИМпST, где существуют ограничения в обычных услугах, а в Великобритании — это первичное ЧКВ. должна оставаться предпочтительной стратегией реперфузии. 10–12
На сегодняшний день данные о представлении, лечении и исходах ОИМ во время пандемии COVID-19 ограничены. Информация была получена из отдельных центров или небольших групп больниц или, в исследованиях, включающих стандартные данные системы здравоохранения, содержала ограниченную информацию о прогностических характеристиках пациентов, включая данные об исходном риске, сопутствующих заболеваниях, времени обращения за помощью, исследованиях и рекомендациях. указанные виды лечения и клинические исходы, особенно с национальной точки зрения. 13 , 14 Понимание того, как изоляция от COVID-19 могла повлиять на обращение за медицинской помощью пациентов с ОИМ, а также на оказание помощи специализированными службами, важно, если предполагается широко распространенные непредвиденные последствия пандемии. сведены к минимуму и сделаны приготовления к потенциальной второй волне. С этой целью главный научный советник правительства Соединенного Королевства поручил Национальному институту исследований сердечно-сосудистых заболеваний подготовить отчет в поддержку ответных мер Министерства здравоохранения на пандемию COVID-19 в Великобритании.В этом исследовании подробно описываются первые национальные идеи, касающиеся реакции пациентов и здравоохранения на ОИМ во время и на этапе восстановления пандемии COVID-9. Он также предоставит обновленные сводные данные временных рядов (при публикации это слово будет иметь гиперссылку на cardiovascularcovid.leeds.ac.uk) для отслеживания динамики характеристик пациентов с ОИМ, ухода и результатов во время текущей пандемии COVID-19 в Англии.
Методы
Данные и пациенты
Национальный аудиторский проект по ишемии миокарда (MINAP) — это обширная клиническая база данных пациентов, госпитализированных с ОИМ, утвержденная Министерством здравоохранения Великобритании для всех больниц в Англии. 15–17 Данные собираются проспективно в каждой больнице, зашифровываются электронным способом и передаются в режиме онлайн в центральную базу данных Национального института исследований сердечно-сосудистых исходов (NICOR). Во время пандемии COVID-19 данные MINAP были получены путем еженедельного прямого кормления на сервер NHS Digital.
Аналитическая когорта была получена из пациентов с ОИМ, поступивших в одну из 180 больниц NHS в Англии в период с 1 января 2017 года по 22 мая 2020 года. Пациенты имели право на участие в исследовании, если им было 18–100 лет и они были госпитализированы в больницу NHS. в Англии с окончательным диагнозом ИМпST или ИМпST.Окончательный диагноз был установлен местными врачами на основании анамнеза, клинического обследования и результатов стационарных исследований в соответствии с согласованным документом Объединенного европейского общества кардиологов и Американского колледжа кардиологов. 18 Рецидивирующие события ОИМ у пациентов, перенесших ОИМ в течение 30 дней после их предыдущего госпитализации, были исключены, поскольку они считались потенциальными осложнениями / неблагоприятными исходами индексного события.
Время появления симптомов определялось как время в течение 10 минут после появления симптомов, а если имел место период перемежающейся боли — время появления тех симптомов, которые побудили пациента обратиться за помощью.Для вывода симптомов по продолжительности обращения за помощью были включены только пациенты, которые были доставлены в больницу на машине скорой помощи. В тех случаях, когда госпитализация следовала за остановкой сердца вне больницы, при отсутствии более подробной информации, время остановки использовалось для появления симптомов. Время поступления в больницу определялось как время прибытия машины скорой помощи в больницу или время регистрации в отделении неотложной помощи и неотложной помощи для пациентов, которые сами явились в отделение.
Статистический анализ
Базовые характеристики были описаны с использованием чисел и процентов [с 95% доверительным интервалом (ДИ) процентов] для категориальных данных и средних значений и стандартных отклонений или медиан и межквартильных диапазонов для нормальных и ненормально распределенных непрерывных переменных.Для NSTEMI вероятность стационарной смертности от всех причин рассчитывалась с использованием шкалы риска GRACE, 19 , и ее разделяли на низкий (1–108), средний (109–140) и высокий риск (141–372). Временные тренды характеристик пациентов и лечения были в основном обобщены путем сравнения данных с начала исследования (1 января 2019–22 марта 2020 г.) с двумя другими периодами: фазой спада с 23 марта («изоляция» в Великобритании) до надира госпитализаций. (19 апреля 2020 г.) и фаза восстановления (с 20 апреля 2020 г. по 22 мая 2020 г.) с использованием тестов χ 2 в квадрате и t в зависимости от распределения данных.Визуальное сравнение также проводилось в другие даты, включая первый подозреваемый случай (31 декабря 2019 г.), изоляцию в Китае (23 января 2020 г.), объявление Всемирной организацией здравоохранения чрезвычайной ситуации в области общественного здравоохранения (30 января 2020 г.) и изоляцию в Италии (2 марта 2020 г.). Подсчет ежедневных случаев был представлен в виде чисел и нескорректированных отношений риска заболеваемости (IRR) с соответствующими 95% доверительными интервалами.
Для графиков временных рядов была оценена 7-дневная простая скользящая средняя (указывающая среднее количество ежедневных госпитализаций в этот день и предшествующие 6 дней) с поправкой на сезонность.Чтобы оценить влияние пандемии COVID-19 на госпитализацию и предоставление услуг, был подобран прерванный временной ряд с использованием обобщенной линейной модели распределения Пуассона и скорректирован с учетом сезонности с помощью гармонического члена. После проверки на наличие избыточной дисперсии была произведена корректировка масштабирования, а автокорреляция исследована с помощью функции частичной автокорреляции.
Данные пациентов были детерминированно связаны с данными регистрации смертей, полученными до 21 июня 2020 года (окончательное наблюдение).Сообщалось о семидневной и 30-дневной нескорректированной смертности от всех причин с сопровождающими 95% доверительными интервалами.
Учитывая реорганизацию NHS, направленную на борьбу с COVID-19, 20 , возможно, произошло сокращение клинического кодирования и представления данных в NICOR, что может имитировать сокращение госпитализаций с ОИМ в течение периода исследования. Это было смягчено и исследовано в несколько этапов. Британское сердечно-сосудистое общество и Британское общество сердечно-сосудистых вмешательств регулярно уведомляли своих членов, а также от NICOR клерку MINAP каждой больницы, подчеркивая важность ввода и представления актуальных данных в NICOR.Было проведено обследование кодирования данных MINAP в каждой больнице NHS для оказания неотложной помощи, а также отслеживание статуса представления, и на основании этого были выявлены 99 больниц, предоставляющих оперативную отчетность, которые еженедельно загружали данные MINAP, и использовались в качестве первичного анализа.
Все тесты были двусторонними, и статистическая значимость принималась как P < 0,05. Статистический анализ проводился в R версии 3.6.3.
Этическое разрешение
Эта работа была одобрена главным научным советником правительства Великобритании для предоставления разведывательных данных о состоянии здоровья Научной консультативной группе по чрезвычайным ситуациям (SAGE), отвечающей за обеспечение своевременных и скоординированных научных рекомендаций для лиц, принимающих решения, для информирования Уход NHS.Государственный секретарь по вопросам здравоохранения и социального обеспечения выпустил NHS Digital с уведомлением в соответствии с правилом 3 (4) NHS (Положения о контроле за информацией о пациентах) 2002 (COPI), чтобы требовать от NHS Digital передавать конфиденциальную информацию о пациентах организациям, имеющим право обрабатывать это в соответствии с COPI для целей COVID-19. NICOR, который включает реестр MINAP (см. NIGB: ECC 1-06 (d) / 2011), в соответствии с разделом 251 Закона о NHS от 2006 г. поддерживает использование информации о пациентах для медицинских исследований без информированного согласия.Для этой быстрой оценки NHS связь данных о здоровье была включена в соответствии с директивами NHS England в области общественного здравоохранения COVID-19 на 2020 год, закрепленными разделом 254 Закона о здравоохранении и социальном обеспечении 2012 года. Исследование соответствует Хельсинкской декларации.
Результаты
Аналитическая когорта была составлена из 117 327 пациентов, госпитализированных с ОИМ в Англии в течение периода исследования (дополнительный материал онлайн, , рисунок S1 ). После исключения к 22 мая 2020 года в 99 больниц Англии поступило 50 689 пациентов с ОИМ.Данные включали 17 246 ИМпST и 33 443 ИМпST.
Больные острым инфарктом миокарда
С 23 марта 2020 г. число госпитализаций с ОИМ снизилось на 42,3% до минимума 19 апреля, что представляет собой снижение среднего числа госпитализаций в день со 104 до 60 (IRR 0,59, 95% ДИ 0,56–0,61). ). С надира до 22 мая 2020 года среднее число госпитализаций увеличилось до 72 (1,19, 95% ДИ 1,12–1,26) и качественно стабилизировалось после первоначального выздоровления ( Рисунок 1 ).
Рисунок 1
Временные ряды ежедневных госпитализаций по поводу острого инфаркта миокарда в период с 1 января 2019 года по 22 мая 2020 года в результате инфаркта миокарда с подъемом сегмента ST и инфаркта миокарда без подъема сегмента ST. Данные 99 больниц Национальной службы здравоохранения Англии. Линии представляют собой 7-дневную простую скользящую среднюю (обозначающую среднее количество ежедневных посещений за этот день и предшествующие 6 дней) с поправкой на сезонность. Даты изоляции COVID, включая первый подозреваемый случай (31 декабря 2019 г.), изоляцию в Китае (23 января 2020 г.), объявление Всемирной организацией здравоохранения чрезвычайной ситуации в области общественного здравоохранения (30 января 2020 г.) и изоляцию в Великобритании (23 марта 2020 г.), показаны с помощью жирная вертикальная линия.Обновления всех цифр доступны на сайте cardiovascularcovid.leeds.ac.uk. ОИМ, острый инфаркт миокарда; ИМбпST, инфаркт миокарда без подъема сегмента ST; ИМпST, инфаркт миокарда с подъемом сегмента ST.
Рисунок 1
Временной ряд ежедневных госпитализаций по поводу острого инфаркта миокарда в период с 1 января 2019 года по 22 мая 2020 года в результате инфаркта миокарда с подъемом сегмента ST и инфаркта миокарда без подъема сегмента ST. Данные 99 больниц Национальной службы здравоохранения Англии. Линии представляют собой 7-дневную простую скользящую среднюю (обозначающую среднее количество ежедневных посещений за этот день и предшествующие 6 дней) с поправкой на сезонность.Даты изоляции COVID, включая первый подозреваемый случай (31 декабря 2019 г.), изоляцию в Китае (23 января 2020 г.), объявление Всемирной организацией здравоохранения чрезвычайной ситуации в области общественного здравоохранения (30 января 2020 г.) и изоляцию в Великобритании (23 марта 2020 г.), показаны с помощью жирная вертикальная линия. Обновления всех цифр доступны на сайте cardiovascularcovid.leeds.ac.uk. ОИМ, острый инфаркт миокарда; ИМбпST, инфаркт миокарда без подъема сегмента ST; ИМпST, инфаркт миокарда с подъемом сегмента ST.
Пациенты, госпитализированные с ОИМ во время фазы спада, были моложе (66.87 против 68,69 лет), чаще мужчины (69,6% против 67,9%, Таблица 1 ) и реже страдали диабетом (24,5% против 28,1%) и цереброваскулярными заболеваниями (7,1% против 8,6%, Рисунок 2 ). У них была более низкая медианная концентрация креатинина, реже они сами обращались в больницу без обращения в службу скорой помощи (11,4% против 20,6%) и реже страдали отеком легких (2,5% против 4,4%, Таблица 2 и Рисунок 3 ). Средняя продолжительность появления симптомов до обращения за помощью и средняя продолжительность обращения за помощью в больницу для тех, кто прибывает на машине скорой помощи, оставались стабильными (, таблица 2, ).Доля пациентов, находящихся под наблюдением кардиолога, получивших стационарную эхокардиографию и направленных на кардиологическую реабилитацию, оставалась очень высокой, как и назначение фармакотерапии вторичной профилактики при выписке из больницы ( Рисунок 3 ). Средняя продолжительность пребывания в больнице снизилась с 4 до 2 дней (, таблица 2, ), а смертность от всех причин через 30 дней осталась стабильной (, рисунок 4, ).
Рисунок 2
График временных рядов ежедневных госпитализаций с острым инфарктом миокарда в период с 1 января 2019 года по 22 мая 2020 года для исходных характеристик пациентов, инфаркта миокарда с подъемом сегмента ST и инфаркта миокарда без подъема сегмента ST.Данные 99 больниц Национальной службы здравоохранения Англии. Линии представляют собой 7-дневную простую скользящую среднюю (обозначающую среднее количество ежедневных посещений за этот день и предшествующие 6 дней) с поправкой на сезонность. Дата блокировки COVID (23 марта 2020 г.) выделена жирной вертикальной линией. Обновления всех цифр доступны на сайте cardiovascularcovid.leeds.ac.uk. ИМбпST, инфаркт миокарда без подъема сегмента ST; ИМпST, инфаркт миокарда с подъемом сегмента ST.
Рисунок 2
График временных рядов ежедневных госпитализаций с острым инфарктом миокарда в период с 1 января 2019 года по 22 мая 2020 года для исходных характеристик пациентов, инфаркта миокарда с подъемом сегмента ST и инфаркта миокарда без подъема сегмента ST.Данные 99 больниц Национальной службы здравоохранения Англии. Линии представляют собой 7-дневную простую скользящую среднюю (обозначающую среднее количество ежедневных посещений за этот день и предшествующие 6 дней) с поправкой на сезонность. Дата блокировки COVID (23 марта 2020 г.) выделена жирной вертикальной линией. Обновления всех цифр доступны на сайте cardiovascularcovid.leeds.ac.uk. ИМбпST, инфаркт миокарда без подъема сегмента ST; ИМпST, инфаркт миокарда с подъемом сегмента ST.
Рисунок 3
График временных рядов ежедневных госпитализаций с острым инфарктом миокарда в период с 1 января 2019 г. по 22 мая 2020 г. для ответа пациента и оказания стационарной помощи, инфаркта миокарда с подъемом сегмента ST и инфаркта миокарда без подъема сегмента ST.Данные 99 больниц Национальной службы здравоохранения Англии. Линии представляют собой 7-дневную простую скользящую среднюю (обозначающую среднее количество ежедневных посещений за этот день и предшествующие 6 дней) с поправкой на сезонность. Дата блокировки COVID (23 марта 2020 г.) выделена жирной вертикальной линией. Данные о симптомах, требующих обращения за помощью, относятся только к пациентам, доставленным в больницу на машине скорой помощи. Скорость перевода относится к доле пациентов, госпитализированных с инфарктом миокарда без подъема сегмента ST, которых переводили из одной больницы в другую для проведения инвазивной коронарной терапии.Обновления всех цифр доступны на сайте cardiovascularcovid.leeds.ac.uk. ИМбпST: инфаркт миокарда без подъема сегмента ST; ИМпST, инфаркт миокарда с подъемом сегмента ST.
Рисунок 3
График временных рядов ежедневных госпитализаций с острым инфарктом миокарда в период с 1 января 2019 г. по 22 мая 2020 г. для ответа пациента и оказания стационарной помощи, инфаркта миокарда с подъемом сегмента ST и инфаркта миокарда без подъема сегмента ST. Данные 99 больниц Национальной службы здравоохранения Англии. Линии представляют собой 7-дневную простую скользящую среднюю (обозначающую среднее количество ежедневных посещений за этот день и предшествующие 6 дней) с поправкой на сезонность.Дата блокировки COVID (23 марта 2020 г.) выделена жирной вертикальной линией. Данные о симптомах, требующих обращения за помощью, относятся только к пациентам, доставленным в больницу на машине скорой помощи. Скорость перевода относится к доле пациентов, госпитализированных с инфарктом миокарда без подъема сегмента ST, которых переводили из одной больницы в другую для проведения инвазивной коронарной терапии. Обновления всех цифр доступны на сайте cardiovascularcovid.leeds.ac.uk. ИМбпST: инфаркт миокарда без подъема сегмента ST; ИМпST, инфаркт миокарда с подъемом сегмента ST.
Рисунок 4
Нескорректированные коэффициенты смертности от всех причин через 30 дней после госпитализации с инфарктом миокарда с подъемом сегмента ST и инфарктом миокарда без подъема сегмента ST, по фазам до блокировки, снижения и восстановления. Показатели смертности были представлены с доверительным интервалом 95%. Обновления всех цифр доступны на сайте cardiovascularcovid.leeds.ac.uk. ОИМ, острый инфаркт миокарда; ИМбпST, инфаркт миокарда без подъема сегмента ST; ИМпST, инфаркт миокарда с подъемом сегмента ST.
Рисунок 4
Не скорректированные коэффициенты смертности от всех причин через 30 дней после госпитализации с инфарктом миокарда с подъемом сегмента ST и инфарктом миокарда без подъема сегмента ST, по фазам до блокировки, снижения и восстановления. Показатели смертности были представлены с доверительным интервалом 95%. Обновления всех цифр доступны на сайте cardiovascularcovid.leeds.ac.uk. ОИМ, острый инфаркт миокарда; ИМбпST, инфаркт миокарда без подъема сегмента ST; ИМпST, инфаркт миокарда с подъемом сегмента ST.
Таблица 1Исходные характеристики пациентов, госпитализированных с острым инфарктом миокарда в Англии до и после карантина в Великобритании от COVID-19
| . | AMI до блокировки Великобритании . | AMI с 23 марта 2020 г. по 19 апреля 2020 г. . | AMI после 20 апреля 2020 г. . | P -тренд . |
|---|---|---|---|---|
| . | n = 46555 . | n = 1708 . | n = 2426 . | . |
| Возраст (лет), среднее (стандартное отклонение) | 68.69 (13,55) | 66,87 (13,46) | 67,60 (13,33) | <0,001 |
| Мужской | 31580 (67,9%, 67,4–68,3) | 1186 (69,6%, 67,368 | ) 906,8 (70,3%, 68,4–72,1) | 0,017 |
| Текущий курильщик | 10863 (25,2%, 24,8–25,6) | 424 (27,7%, 25,5–30,1) | 583 (26,3%, 24,5–28,2) | 0,051 |
| История болезни | ||||
| АКШ | 3030 (7.3%, 7,1–7,6) | 98 (6,7%, 5,5–8,1) | 161 (7,6%, 6,5–8,8) | 0,587 |
| Цереброваскулярные заболевания | 3584 (8,6%, 8,3–8,9) | 104 (7,0%, 5,8–8,5) | 168 (7,8%, 6,8–9,1) | 0,056 |
| Хроническая почечная недостаточность | 3241 (7,7%, 7,5–8,0) | 117 (7,9%, 6,6 –9,4) | 152 (7,0%, 6,0–8,2) | 0,484 |
| Застойная сердечная недостаточность | 3174 (7.6%, 7,3–7,8) | 101 (6,8%, 5,6–8,2) | 146 (6,8%, 5,8–8,0) | 0,244 |
| ХОБЛ или астма | 7358 (17,6%, 17,2–18,0) | 258 (17,5%, 15,6–19,5) | 371 (17,3%, 15,7–19,0) | 0,931 |
| Сахарный диабет | 12597 (28,1%, 27,7–28,5) | 396 (24,6%, 24,6%, 24,6%, 24,6%, –26,8) | 611 (26,5%, 24,7–28,3) | 0,002 |
| Гиперлипидемия | 12935 (30.9%, 30,5–31,3) | 453 (30,5%, 28,2–33,0) | 702 (32,7%, 30,7–34,7) | 0,216 |
| Гипертония | 22813 (53,6%, 53,1–54,1) | 797 (52,8%, 50,2–55,3) | 1172 (53,8%, 51,7–55,9) | 0,805 |
| Заболевание периферических сосудов | 1838 (4,4%, 4,2–4,6) | 62 (4,2%, 3,3–4,6) 5,4) | 93 (4,4%, 3,6–5,3) | 0,922 |
| Предыдущий MI | 10187 (24.1%, 23,7–24,5) | 350 (23,4%, 21,3–25,7) | 482 (22,4%, 20,6–24,2) | 0,169 |
| Предыдущее PCI | 6679 (16,2%, 15,8–16,5) | 237 (16,2%, 14,3–18,2) | 340 (16,1%, 14,5–17,7) | 0,993 |
| . | AMI до блокировки Великобритании . | AMI с 23 марта 2020 г. по 19 апреля 2020 г. . | AMI после 20 апреля 2020 г. . | P -тренд . | |
|---|---|---|---|---|---|
| . | n = 46555 . | n = 1708 . | n = 2426 . | . | |
| Возраст (лет), среднее значение (стандартное отклонение) | 68,69 (13,55) | 66,87 (13,46) | 67,60 (13,33) | <0,001 | |
| 31580 ( | ) Мужской | ,9%, 67,4–68,3) | 1186 (69,6%, 67,3–71,8) | 1703 (70,3%, 68,4–72,1) | 0,017 |
| Текущий курильщик | 10863 (25,2%, 24,8–25,6) | 424 (27,7%, 25,5–30,1) | 583 (26,3%, 24,5–28,2) | 0,051 | |
| История болезни | |||||
| 98 (6,7%, 5,5–8.1) | 161 (7,6%, 6,5–8,8) | 0,587 | |||
| Цереброваскулярные заболевания | 3584 (8,6%, 8,3–8,9) | 104 (7,0%, 5,8–8,5) | 168 (7,8% , 6,8–9,1) | 0,056 | |
| Хроническая почечная недостаточность | 3241 (7,7%, 7,5–8,0) | 117 (7,9%, 6,6–9,4) | 152 (7,0%, 6,0–8,2) | 0,484 | |
| Застойная сердечная недостаточность | 3174 (7,6%, 7,3–7,8) | 101 (6.8%, 5,6–8,2) | 146 (6,8%, 5,8–8,0) | 0,244 | |
| ХОБЛ или астма | 7358 (17,6%, 17,2–18,0) | 258 (17,5%, 15,6–19,5) | 371 (17,3%, 15,7–19,0) | 0,931 | |
| Сахарный диабет | 12597 (28,1%, 27,7–28,5) | 396 (24,6%, 22,5–26,8) | 611 (26,5%, 26,5%, 26,5%, 26,5%, –28,3) | 0,002 | |
| Гиперлипидемия | 12935 (30,9%, 30,5–31.3) | 453 (30,5%, 28,2–33,0) | 702 (32,7%, 30,7–34,7) | 0,216 | |
| Гипертония | 22813 (53,6%, 53,1–54,1) | 797 (52,8%, 50,2–55,3) | 1172 (53,8%, 51,7–55,9) | 0,805 | |
| Заболевание периферических сосудов | 1838 (4,4%, 4,2–4,6) | 62 (4,2%, 3,3–5,4) | 93 (4,4%, 3,6–5,3) | 0,922 | |
| Предыдущий MI | 10187 (24.1%, 23,7–24,5) | 350 (23,4%, 21,3–25,7) | 482 (22,4%, 20,6–24,2) | 0,169 | |
| Предыдущее PCI | 6679 (16,2%, 15,8–16,5) | 237 (16,2%, 14,3–18,2) | 340 (16,1%, 14,5–17,7) | 0,993 |
Исходные характеристики пациентов, госпитализированных с острым инфарктом миокарда в Англии до и после COVID-19 в Великобритании блокировка
| . | AMI до блокировки Великобритании . | AMI с 23 марта 2020 г. по 19 апреля 2020 г. . | AMI после 20 апреля 2020 г. . | P -тренд . |
|---|---|---|---|---|
| . | n = 46555 . | n = 1708 . | n = 2426 . | . |
| Возраст (лет), среднее (стандартное отклонение) | 68.69 (13,55) | 66,87 (13,46) | 67,60 (13,33) | <0,001 |
| Мужской | 31580 (67,9%, 67,4–68,3) | 1186 (69,6%, 67,368 | ) 906,8 (70,3%, 68,4–72,1) | 0,017 |
| Текущий курильщик | 10863 (25,2%, 24,8–25,6) | 424 (27,7%, 25,5–30,1) | 583 (26,3%, 24,5–28,2) | 0,051 |
| История болезни | ||||
| АКШ | 3030 (7.3%, 7,1–7,6) | 98 (6,7%, 5,5–8,1) | 161 (7,6%, 6,5–8,8) | 0,587 |
| Цереброваскулярные заболевания | 3584 (8,6%, 8,3–8,9) | 104 (7,0%, 5,8–8,5) | 168 (7,8%, 6,8–9,1) | 0,056 |
| Хроническая почечная недостаточность | 3241 (7,7%, 7,5–8,0) | 117 (7,9%, 6,6 –9,4) | 152 (7,0%, 6,0–8,2) | 0,484 |
| Застойная сердечная недостаточность | 3174 (7.6%, 7,3–7,8) | 101 (6,8%, 5,6–8,2) | 146 (6,8%, 5,8–8,0) | 0,244 |
| ХОБЛ или астма | 7358 (17,6%, 17,2–18,0) | 258 (17,5%, 15,6–19,5) | 371 (17,3%, 15,7–19,0) | 0,931 |
| Сахарный диабет | 12597 (28,1%, 27,7–28,5) | 396 (24,6%, 24,6%, 24,6%, 24,6%, –26,8) | 611 (26,5%, 24,7–28,3) | 0,002 |
| Гиперлипидемия | 12935 (30.9%, 30,5–31,3) | 453 (30,5%, 28,2–33,0) | 702 (32,7%, 30,7–34,7) | 0,216 |
| Гипертония | 22813 (53,6%, 53,1–54,1) | 797 (52,8%, 50,2–55,3) | 1172 (53,8%, 51,7–55,9) | 0,805 |
| Заболевание периферических сосудов | 1838 (4,4%, 4,2–4,6) | 62 (4,2%, 3,3–4,6) 5,4) | 93 (4,4%, 3,6–5,3) | 0,922 |
| Предыдущий MI | 10187 (24.1%, 23,7–24,5) | 350 (23,4%, 21,3–25,7) | 482 (22,4%, 20,6–24,2) | 0,169 |
| Предыдущее PCI | 6679 (16,2%, 15,8–16,5) | 237 (16,2%, 14,3–18,2) | 340 (16,1%, 14,5–17,7) | 0,993 |
| . | AMI до блокировки Великобритании . | AMI с 23 марта 2020 г. по 19 апреля 2020 г. . | AMI после 20 апреля 2020 г. . | P -тренд . | |
|---|---|---|---|---|---|
| . | n = 46555 . | n = 1708 . | n = 2426 . | . | |
| Возраст (лет), среднее значение (стандартное отклонение) | 68,69 (13,55) | 66,87 (13,46) | 67,60 (13,33) | <0,001 | |
| 31580 ( | ) Мужской | ,9%, 67,4–68,3) | 1186 (69,6%, 67,3–71,8) | 1703 (70,3%, 68,4–72,1) | 0,017 |
| Текущий курильщик | 10863 (25,2%, 24,8–25,6) | 424 (27,7%, 25,5–30,1) | 583 (26,3%, 24,5–28,2) | 0,051 | |
| История болезни | |||||
| 98 (6,7%, 5,5–8.1) | 161 (7,6%, 6,5–8,8) | 0,587 | |||
| Цереброваскулярные заболевания | 3584 (8,6%, 8,3–8,9) | 104 (7,0%, 5,8–8,5) | 168 (7,8% , 6,8–9,1) | 0,056 | |
| Хроническая почечная недостаточность | 3241 (7,7%, 7,5–8,0) | 117 (7,9%, 6,6–9,4) | 152 (7,0%, 6,0–8,2) | 0,484 | |
| Застойная сердечная недостаточность | 3174 (7,6%, 7,3–7,8) | 101 (6.8%, 5,6–8,2) | 146 (6,8%, 5,8–8,0) | 0,244 | |
| ХОБЛ или астма | 7358 (17,6%, 17,2–18,0) | 258 (17,5%, 15,6–19,5) | 371 (17,3%, 15,7–19,0) | 0,931 | |
| Сахарный диабет | 12597 (28,1%, 27,7–28,5) | 396 (24,6%, 22,5–26,8) | 611 (26,5%, 26,5%, 26,5%, 26,5%, –28,3) | 0,002 | |
| Гиперлипидемия | 12935 (30,9%, 30,5–31.3) | 453 (30,5%, 28,2–33,0) | 702 (32,7%, 30,7–34,7) | 0,216 | |
| Гипертония | 22813 (53,6%, 53,1–54,1) | 797 (52,8%, 50,2–55,3) | 1172 (53,8%, 51,7–55,9) | 0,805 | |
| Заболевание периферических сосудов | 1838 (4,4%, 4,2–4,6) | 62 (4,2%, 3,3–5,4) | 93 (4,4%, 3,6–5,3) | 0,922 | |
| Предыдущий MI | 10187 (24.1%, 23,7–24,5) | 350 (23,4%, 21,3–25,7) | 482 (22,4%, 20,6–24,2) | 0,169 | |
| Предыдущее PCI | 6679 (16,2%, 15,8–16,5) | 237 (16,2%, 14,3–18,2) | 340 (16,1%, 14,5–17,7) | 0,993 |
Клиническая картина, лечение и исходы пациентов, госпитализированных с острым инфарктом миокарда в Англии до и после изоляции от COVID-19 в Великобритании
| . | AMI до блокировки . | AMI с 23 марта 2020 г. по 19 апреля 2020 г. . | AMI после 20 апреля 2020 г. . | P -тренд . | |
|---|---|---|---|---|---|
| . | n = 46555 . | n = 1708 . | n = 2426 . | . | |
| Клиническая картина | |||||
| Самостоятельное обращение в больницу | 9608 (20.6%, 20,3–21,0) | 195 (11,4%, 10,0–13,0) | 406 (16,7%, 15,3–18,3) | <0,001 | |
| Систолическое артериальное давление (мм рт. Ст.), Среднее (SD) | 139,48 (28,05) | 141,07 (28,13) | 141,81 (28,61) | <0,001 | |
| Частота сердечных сокращений (уд / мин), медиана (IQR) | 77,00 (66,00–90,00) | 78,00 (67,00) | 79,00 (67,00–91,00) | <0,001 | |
| Креатинин (мкмоль / л), медиана (IQR) | 84.00 (71,00–104,00) | 83,00 (69,00–101,00) | 84,00 (70,00–102,00) | 0,005 | |
| догоспитальная остановка сердца | 1731 (3,8%, 3,7–4,0) | 67 (4,1 %, 3,2–5,2) | 73 (3,1%, 2,5–3,9) | 0,173 | |
| При догоспитальной остановке сердца: нет восстановления сердечного ритма или возврата, но умер в больнице | 532 (30,7%, 28,6–33,0 ) | 15 (22,4%, 13,5–34,5) | 24 (32,9%, 22,6–45,0) | 0.314 | |
| Электрокардиографическая элевация сегмента ST | 15380 (33,3%, 32,8–33,7) | 706 (41,8%, 39,4–44,1) | 841 (35,2%, 33,3–37,1) | <0,001 | |
| Отек легких | 1879 (4,4%, 4,2–4,6) | 39 (2,5%, 1,8–3,4) | 82 (3,7%, 3,0–4,6) | <0,001 | |
| Кардиогенный шок | 674 ( 1,6%, 1,5–1,7) | 24 (1,5%, 1,0–2,3) | 34 (1.5%, 1,1–2,2) | 0,987 | |
| Время реакции пациента и здравоохранения | |||||
| Продолжительность звонка от симптома (мин), медиана (IQR) | 30,00 79 ) | 76,50 (27,00–299,75) | 90,00 (30,00–316,00) | 0,115 | |
| Продолжительность госпитализации (мин), медиана (IQR) | 79,00 (60,00–104,00) | 80,00 (63668 | 80,00 .00–103,75) | 76,00 (59,00–95,00) | <0,001 |
| Лекарственные препараты во время выписки | |||||
| ACEi / ARB 3028668 | ,5 94,74,8 ) | 1160 (95,1%, 93,7–96,2) | 1686 (94,8%, 93,6–95,7) | 0,557 | |
| Бета-блокатор | 32248 (96,2%, 96,0–96,4) | 1232 (96,9% , 95,8–97,8) | 1731 (96.9%, 96,0–97,7) | 0,121 | |
| Аспирин | 34516 (97,9%, 97,8–98,1) | 1314 (98,4%, 97,6–99,0) | 1852 (98,4%, 97,7–98,9) | 0,193 | |
| Статин | 34858 (97,6%, 97,4–97,7) | 1322 (97,9%, 97,0–98,6) | 1875 (97,6%, 96,8–98,2) | 0,730 | |
| клопрас тикагрелор | 34280 (97,5%, 97,4–97,7) | 1321 (99.2%, 98,6–99,6) | 1857 (99,0%, 98,4–99,4) | <0,001 | |
| Внутрибольничные исходы | |||||
| Направление на реабилитацию 906 89,3%, 88,9–89,6) | 1220 (89,7%, 87,9–91,2) | 1684 (89,6%, 88,1–90,9) | 0,798 | ||
| Стационарная эхокардиография | 31406 (77,3%, 76,9–77,7 ) | 1118 (76.6%, 74,3–78,7) | 1637 (78,5%, 76,6–80,2) | 0,361 | |
| Плановое наблюдение кардиолога | 30816 (85,4%, 85,0–85,8) | 1119 (87,1%, 85,1–88,8) | 1604 (87,6%, 85,9–89,0) | 0,011 | |
| Средняя продолжительность пребывания в стационаре (IQR) | 4,00 (2,00–7,00) | 2,00 (2,00–4,00) | 3,00 (2,00–5,00) | <0,001 | |
| Семидневная смертность | 2035 (4.4%, 4,2–4,6) | 81 (4,7%, 3,8–5,9) | 100 (4,1%, 3,4–5,0) | 0,630 | |
| Тридцатидневная смертность | 3268 (7,0%, 6,8–7,3 ) | 129 (7,6%, 6,4–8,9) | 149 (6,1%, 5,2–7,2) | 0,167 |
| . | AMI до блокировки . | AMI с 23 марта 2020 г. по 19 апреля 2020 г. . | AMI после 20 апреля 2020 г. . | P -тренд . | |
|---|---|---|---|---|---|
| . | n = 46555 . | n = 1708 . | n = 2426 . | . | |
| Клиническая картина | |||||
| Самостоятельное обращение в больницу | 9608 (20.6%, 20,3–21,0) | 195 (11,4%, 10,0–13,0) | 406 (16,7%, 15,3–18,3) | <0,001 | |
| Систолическое артериальное давление (мм рт. Ст.), Среднее (SD) | 139,48 (28,05) | 141,07 (28,13) | 141,81 (28,61) | <0,001 | |
| Частота сердечных сокращений (уд / мин), медиана (IQR) | 77,00 (66,00–90,00) | 78,00 (67,00) | 79,00 (67,00–91,00) | <0,001 | |
| Креатинин (мкмоль / л), медиана (IQR) | 84.00 (71,00–104,00) | 83,00 (69,00–101,00) | 84,00 (70,00–102,00) | 0,005 | |
| догоспитальная остановка сердца | 1731 (3,8%, 3,7–4,0) | 67 (4,1 %, 3,2–5,2) | 73 (3,1%, 2,5–3,9) | 0,173 | |
| При догоспитальной остановке сердца: нет восстановления сердечного ритма или возврата, но умер в больнице | 532 (30,7%, 28,6–33,0 ) | 15 (22,4%, 13,5–34,5) | 24 (32,9%, 22,6–45,0) | 0.314 | |
| Электрокардиографическая элевация сегмента ST | 15380 (33,3%, 32,8–33,7) | 706 (41,8%, 39,4–44,1) | 841 (35,2%, 33,3–37,1) | <0,001 | |
| Отек легких | 1879 (4,4%, 4,2–4,6) | 39 (2,5%, 1,8–3,4) | 82 (3,7%, 3,0–4,6) | <0,001 | |
| Кардиогенный шок | 674 ( 1,6%, 1,5–1,7) | 24 (1,5%, 1,0–2,3) | 34 (1.5%, 1,1–2,2) | 0,987 | |
| Время реакции пациента и здравоохранения | |||||
| Продолжительность звонка от симптома (мин), медиана (IQR) | 30,00 79 ) | 76,50 (27,00–299,75) | 90,00 (30,00–316,00) | 0,115 | |
| Продолжительность госпитализации (мин), медиана (IQR) | 79,00 (60,00–104,00) | 80,00 (63668 | 80,00 .00–103,75) | 76,00 (59,00–95,00) | <0,001 |
| Лекарственные препараты во время выписки | |||||
| ACEi / ARB 3028668 | ,5 94,74,8 ) | 1160 (95,1%, 93,7–96,2) | 1686 (94,8%, 93,6–95,7) | 0,557 | |
| Бета-блокатор | 32248 (96,2%, 96,0–96,4) | 1232 (96,9% , 95,8–97,8) | 1731 (96.9%, 96,0–97,7) | 0,121 | |
| Аспирин | 34516 (97,9%, 97,8–98,1) | 1314 (98,4%, 97,6–99,0) | 1852 (98,4%, 97,7–98,9) | 0,193 | |
| Статин | 34858 (97,6%, 97,4–97,7) | 1322 (97,9%, 97,0–98,6) | 1875 (97,6%, 96,8–98,2) | 0,730 | |
| клопрас тикагрелор | 34280 (97,5%, 97,4–97,7) | 1321 (99.2%, 98,6–99,6) | 1857 (99,0%, 98,4–99,4) | <0,001 | |
| Внутрибольничные исходы | |||||
| Направление на реабилитацию 906 89,3%, 88,9–89,6) | 1220 (89,7%, 87,9–91,2) | 1684 (89,6%, 88,1–90,9) | 0,798 | ||
| Стационарная эхокардиография | 31406 (77,3%, 76,9–77,7 ) | 1118 (76.6%, 74,3–78,7) | 1637 (78,5%, 76,6–80,2) | 0,361 | |
| Плановое наблюдение кардиолога | 30816 (85,4%, 85,0–85,8) | 1119 (87,1%, 85,1–88,8) | 1604 (87,6%, 85,9–89,0) | 0,011 | |
| Средняя продолжительность пребывания в стационаре (IQR) | 4,00 (2,00–7,00) | 2,00 (2,00–4,00) | 3,00 (2,00–5,00) | <0,001 | |
| Семидневная смертность | 2035 (4.4%, 4,2–4,6) | 81 (4,7%, 3,8–5,9) | 100 (4,1%, 3,4–5,0) | 0,630 | |
| Тридцатидневная смертность | 3268 (7,0%, 6,8–7,3 ) | 129 (7,6%, 6,4–8,9) | 149 (6,1%, 5,2–7,2) | 0,167 |
Клиническая картина, лечение и исходы пациентов, госпитализированных с острым инфарктом миокарда в Англии до и после изоляции от COVID-19 в Великобритании
| . | AMI до блокировки . | AMI с 23 марта 2020 г. по 19 апреля 2020 г. . | AMI после 20 апреля 2020 г. . | P -тренд . | |
|---|---|---|---|---|---|
| . | n = 46555 . | n = 1708 . | n = 2426 . | . | |
| Клиническая картина | |||||
| Самостоятельное обращение в больницу | 9608 (20.6%, 20,3–21,0) | 195 (11,4%, 10,0–13,0) | 406 (16,7%, 15,3–18,3) | <0,001 | |
| Систолическое артериальное давление (мм рт. Ст.), Среднее (SD) | 139,48 (28,05) | 141,07 (28,13) | 141,81 (28,61) | <0,001 | |
| Частота сердечных сокращений (уд / мин), медиана (IQR) | 77,00 (66,00–90,00) | 78,00 (67,00) | 79,00 (67,00–91,00) | <0,001 | |
| Креатинин (мкмоль / л), медиана (IQR) | 84.00 (71,00–104,00) | 83,00 (69,00–101,00) | 84,00 (70,00–102,00) | 0,005 | |
| догоспитальная остановка сердца | 1731 (3,8%, 3,7–4,0) | 67 (4,1 %, 3,2–5,2) | 73 (3,1%, 2,5–3,9) | 0,173 | |
| При догоспитальной остановке сердца: нет восстановления сердечного ритма или возврата, но умер в больнице | 532 (30,7%, 28,6–33,0 ) | 15 (22,4%, 13,5–34,5) | 24 (32,9%, 22,6–45,0) | 0.314 | |
| Электрокардиографическая элевация сегмента ST | 15380 (33,3%, 32,8–33,7) | 706 (41,8%, 39,4–44,1) | 841 (35,2%, 33,3–37,1) | <0,001 | |
| Отек легких | 1879 (4,4%, 4,2–4,6) | 39 (2,5%, 1,8–3,4) | 82 (3,7%, 3,0–4,6) | <0,001 | |
| Кардиогенный шок | 674 ( 1,6%, 1,5–1,7) | 24 (1,5%, 1,0–2,3) | 34 (1.5%, 1,1–2,2) | 0,987 | |
| Время реакции пациента и здравоохранения | |||||
| Продолжительность звонка от симптома (мин), медиана (IQR) | 30,00 79 ) | 76,50 (27,00–299,75) | 90,00 (30,00–316,00) | 0,115 | |
| Продолжительность госпитализации (мин), медиана (IQR) | 79,00 (60,00–104,00) | 80,00 (63668 | 80,00 .00–103,75) | 76,00 (59,00–95,00) | <0,001 |
| Лекарственные препараты во время выписки | |||||
| ACEi / ARB 3028668 | ,5 94,74,8 ) | 1160 (95,1%, 93,7–96,2) | 1686 (94,8%, 93,6–95,7) | 0,557 | |
| Бета-блокатор | 32248 (96,2%, 96,0–96,4) | 1232 (96,9% , 95,8–97,8) | 1731 (96.9%, 96,0–97,7) | 0,121 | |
| Аспирин | 34516 (97,9%, 97,8–98,1) | 1314 (98,4%, 97,6–99,0) | 1852 (98,4%, 97,7–98,9) | 0,193 | |
| Статин | 34858 (97,6%, 97,4–97,7) | 1322 (97,9%, 97,0–98,6) | 1875 (97,6%, 96,8–98,2) | 0,730 | |
| клопрас тикагрелор | 34280 (97,5%, 97,4–97,7) | 1321 (99.2%, 98,6–99,6) | 1857 (99,0%, 98,4–99,4) | <0,001 | |
| Внутрибольничные исходы | |||||
| Направление на реабилитацию 906 89,3%, 88,9–89,6) | 1220 (89,7%, 87,9–91,2) | 1684 (89,6%, 88,1–90,9) | 0,798 | ||
| Стационарная эхокардиография | 31406 (77,3%, 76,9–77,7 ) | 1118 (76.6%, 74,3–78,7) | 1637 (78,5%, 76,6–80,2) | 0,361 | |
| Плановое наблюдение кардиолога | 30816 (85,4%, 85,0–85,8) | 1119 (87,1%, 85,1–88,8) | 1604 (87,6%, 85,9–89,0) | 0,011 | |
| Средняя продолжительность пребывания в стационаре (IQR) | 4,00 (2,00–7,00) | 2,00 (2,00–4,00) | 3,00 (2,00–5,00) | <0,001 | |
| Семидневная смертность | 2035 (4.4%, 4,2–4,6) | 81 (4,7%, 3,8–5,9) | 100 (4,1%, 3,4–5,0) | 0,630 | |
| Тридцатидневная смертность | 3268 (7,0%, 6,8–7,3 ) | 129 (7,6%, 6,4–8,9) | 149 (6,1%, 5,2–7,2) | 0,167 |
| . | AMI до блокировки . | AMI с 23 марта 2020 г. по 19 апреля 2020 г. . | AMI после 20 апреля 2020 г. . | P -тренд . | |
|---|---|---|---|---|---|
| . | n = 46555 . | n = 1708 . | n = 2426 . | . | |
| Клиническая картина | |||||
| Самостоятельное обращение в больницу | 9608 (20.6%, 20,3–21,0) | 195 (11,4%, 10,0–13,0) | 406 (16,7%, 15,3–18,3) | <0,001 | |
| Систолическое артериальное давление (мм рт. Ст.), Среднее (SD) | 139,48 (28,05) | 141,07 (28,13) | 141,81 (28,61) | <0,001 | |
| Частота сердечных сокращений (уд / мин), медиана (IQR) | 77,00 (66,00–90,00) | 78,00 (67,00) | 79,00 (67,00–91,00) | <0,001 | |
| Креатинин (мкмоль / л), медиана (IQR) | 84.00 (71,00–104,00) | 83,00 (69,00–101,00) | 84,00 (70,00–102,00) | 0,005 | |
| догоспитальная остановка сердца | 1731 (3,8%, 3,7–4,0) | 67 (4,1 %, 3,2–5,2) | 73 (3,1%, 2,5–3,9) | 0,173 | |
| При догоспитальной остановке сердца: нет восстановления сердечного ритма или возврата, но умер в больнице | 532 (30,7%, 28,6–33,0 ) | 15 (22,4%, 13,5–34,5) | 24 (32,9%, 22,6–45,0) | 0.314 | |
| Электрокардиографическая элевация сегмента ST | 15380 (33,3%, 32,8–33,7) | 706 (41,8%, 39,4–44,1) | 841 (35,2%, 33,3–37,1) | <0,001 | |
| Отек легких | 1879 (4,4%, 4,2–4,6) | 39 (2,5%, 1,8–3,4) | 82 (3,7%, 3,0–4,6) | <0,001 | |
| Кардиогенный шок | 674 ( 1,6%, 1,5–1,7) | 24 (1,5%, 1,0–2,3) | 34 (1.5%, 1,1–2,2) | 0,987 | |
| Время реакции пациента и здравоохранения | |||||
| Продолжительность звонка от симптома (мин), медиана (IQR) | 30,00 79 ) | 76,50 (27,00–299,75) | 90,00 (30,00–316,00) | 0,115 | |
| Продолжительность госпитализации (мин), медиана (IQR) | 79,00 (60,00–104,00) | 80,00 (63668 | 80,00 .00–103,75) | 76,00 (59,00–95,00) | <0,001 |
| Лекарственные препараты во время выписки | |||||
| ACEi / ARB 3028668 | ,5 94,74,8 ) | 1160 (95,1%, 93,7–96,2) | 1686 (94,8%, 93,6–95,7) | 0,557 | |
| Бета-блокатор | 32248 (96,2%, 96,0–96,4) | 1232 (96,9% , 95,8–97,8) | 1731 (96.9%, 96,0–97,7) | 0,121 | |
| Аспирин | 34516 (97,9%, 97,8–98,1) | 1314 (98,4%, 97,6–99,0) | 1852 (98,4%, 97,7–98,9) | 0,193 | |
| Статин | 34858 (97,6%, 97,4–97,7) | 1322 (97,9%, 97,0–98,6) | 1875 (97,6%, 96,8–98,2) | 0,730 | |
| клопрас тикагрелор | 34280 (97,5%, 97,4–97,7) | 1321 (99.2%, 98,6–99,6) | 1857 (99,0%, 98,4–99,4) | <0,001 | |
| Внутрибольничные исходы | |||||
| Направление на реабилитацию 906 89,3%, 88,9–89,6) | 1220 (89,7%, 87,9–91,2) | 1684 (89,6%, 88,1–90,9) | 0,798 | ||
| Стационарная эхокардиография | 31406 (77,3%, 76,9–77,7 ) | 1118 (76.6%, 74,3–78,7) | 1637 (78,5%, 76,6–80,2) | 0,361 | |
| Плановое наблюдение кардиолога | 30816 (85,4%, 85,0–85,8) | 1119 (87,1%, 85,1–88,8) | 1604 (87,6%, 85,9–89,0) | 0,011 | |
| Средняя продолжительность пребывания в стационаре (IQR) | 4,00 (2,00–7,00) | 2,00 (2,00–4,00) | 3,00 (2,00–5,00) | <0,001 | |
| Семидневная смертность | 2035 (4.4%, 4,2–4,6) | 81 (4,7%, 3,8–5,9) | 100 (4,1%, 3,4–5,0) | 0,630 | |
| Тридцатидневная смертность | 3268 (7,0%, 6,8–7,3 ) | 129 (7,6%, 6,4–8,9) | 149 (6,1%, 5,2–7,2) | 0,167 |
Во время фазы выздоровления (с 20 апреля по 22 мая 2020 г.) характеристики пациента при поступлении с ОИМ был аналогичен таковому у пациентов в фазе спада (, таблица 1, и , рисунок 2, ).Тем не менее, наблюдалось частичное возвращение к показателям самопрезентаций с ОИМ в больницах (16,7% против 20,6%) и пациентов с отеком легких (3,7% против 4,4%, Таблица 2 ). В то время как средняя продолжительность появления симптомов до обращения за помощью не отличалась от предыдущих фаз, средняя продолжительность обращения за помощью в больницу для тех, кто прибыл на машине скорой помощи, была короче на 4 минуты (, таблица 2, ). Доля пациентов, осмотренных кардиологом, получивших стационарную эхокардиографию, направленных на кардиологическую реабилитацию и использующих методы вторичной профилактики, оставалась очень высокой ( Таблица 2 и Рисунок 3 ).Средняя продолжительность пребывания в больнице увеличилась до 3 дней ( Рисунок 3 ), а смертность от всех причин через 30 дней осталась стабильной ( Рисунок 4 ).
Пациенты с инфарктом миокарда с подъемом сегмента ST
19 апреля число госпитализаций с ИМпST снизилось на 28,6% до минимума, что представляет собой снижение среднего числа госпитализаций в день с 35 до 25 (ВНД 0,74, 95% ДИ 0,69–0,80) и остается стабильным при выздоровлении. фаза.
Профили ухода и исходы пациентов, госпитализированных с ИМпST не отличались от ИМпST, поступивших до изоляции (дополнительный материал онлайн, Таблица S1 и Рисунок 3 ).Тем не менее, количество людей, самостоятельно обращающихся в больницу в фазе спада, сократилось на 50% (8,2% против 4,0%), что увеличилось после минимума госпитализаций (5,8%). Во время фазы восстановления средняя продолжительность обращения за помощью в больницу уменьшилась на 3 минуты по сравнению с периодом до блокировки, а среднее время пребывания в больнице до реперфузии увеличилось на 4 минуты. Использование первичного ЧКВ было очень высоким на протяжении всего периода исследования, и небольшое количество пациентов с ИМпST подверглись тромболизису (0.3%). За три периода времени средняя продолжительность пребывания в больнице изменилась с 3 до 2 до 3 дней, а общая смертность от всех причин через 30 дней снизилась с 10,2% до блокировки до 7,7% в фазе снижения и увеличилась до 8,3% в этап восстановления (дополнительный материал в Интернете, Таблица S1, и Рисунок 4, ).
Пациенты с инфарктом миокарда без подъема сегмента ST
Число госпитализаций с ИМбпST снизилось на 49,3% до минимума 19 апреля, что представляет собой снижение среднего числа госпитализаций в день с 69 до 35 (IRR 0.51, 95% ДИ 0,47–0,54). С надира до 31 мая 2020 года среднее число госпитализаций увеличилось до 46 (1,32, 95% ДИ 1,22–1,42) (, рисунок 1, ).
После изоляции пациенты, госпитализированные с ИМбпST, были моложе (68,5 против 70,2 лет) и реже страдали сахарным диабетом (26,7% против 31,5%) и отеком легких (2,2% против 4,7%, дополнительные материалы онлайн, Таблица S2 ). В фазе спада наблюдалось снижение на 3% доли пациентов с ИМбпST, получивших инвазивную коронарную стратегию, и меньшее количество переводов между больницами при таком подходе.Однако для тех, кто получил инвазивную стратегию, среднее время до инвазивной коронарной ангиографии было сокращено с 64 до 26 до 38 часов в течение трех последовательных фаз (дополнительный материал онлайн, , таблица S2 ). Задержки в получении инвазивной коронарной стратегии при ИМбпST с меньшей вероятностью были связаны с лабораторными проблемами с катетером и с большей вероятностью были связаны с сопутствующими заболеваниями пациента. Во время фазы восстановления средняя продолжительность обращения в больницу уменьшилась на 5 минут. После изоляции доля обследованных кардиологом, количество выписываемых препаратов для вторичной профилактики и направление на кардиологическую реабилитацию оставались на высоком уровне, но использование стационарной эхокардиографии было ниже в фазе спада.За три периода времени средняя продолжительность пребывания в больнице изменилась с 5 до 2–3 дней. Смертность от всех причин через 30 дней увеличилась с 5,4% до блокировки до 7,5% в фазе снижения и снизилась до 5,0% в фазе восстановления ( Рисунок 4 ).
Обсуждение
Начало социальной изоляции — состояние изоляции — для уменьшения распространения инфекции COVID-19 было связано с почти 50% снижением количества госпитализаций с ОИМ и значительно более высокой ранней смертностью от ИМбпST до самого низшего уровня госпитализаций, несмотря на высокие уровни стационарного лечения.Хотя вначале наблюдалось восстановление числа госпитализаций, это продолжалось, и до конца исследования период оставался на уровне двух третей от показателя до блокировки. Учитывая количество пациентов с ОИМ, которые не обращаются в больницу (и задержки в обращении среди госпитализированных), в ближайшем будущем вероятно увеличение смертности от ОИМ среди населения и увеличение количества госпитализаций по поводу сердечной недостаточности. В то время как снижение числа госпитализаций подтверждают выводы из других источников данных, 3–8 , 14 , это исследование выявляет низший уровень и, что вызывает озабоченность, прекращение траектории восстановления госпитализаций.Поэтому важно, чтобы общественность постоянно сообщала об обращении за неотложной медицинской помощью при ОИМ.
Число госпитализаций с ИМбпST значительно снизилось. Вероятно, пациенты с ИМбпST не обращались за медицинской помощью, потому что они чувствовали, что их симптомы, которые с меньшей вероятностью будут болью в груди или дискомфортом в груди, 21 не подтверждают риск потенциального контакта с инфекцией COVID-19 в больнице. . Хотя мы решили стратифицировать анализ по дате карантина в Великобритании, очевидно, что снижение числа госпитализаций началось ранее в 2020 году, а также освещение в международных средствах массовой информации смертей, переполненных больниц, строгих ограничений в отдельных странах, а также заявления Всемирного здравоохранения. Организация чрезвычайной ситуации в области общественного здравоохранения заставила многих пациентов с ОИМ не обращаться в больницы из-за опасений заразиться инфекцией COVID-19, быть изолированными в палате без посетителей и из-за желания защитить больницы.Кроме того, в начале пандемии была широко освещена связь между возрастом или ранее существовавшими заболеваниями и худшими исходами после заражения COVID-19, и многие пациенты с ИМбпST считали себя подверженными значительному риску из-за своей болезни. возраст и сопутствующие заболевания.
Ранняя смертность увеличилась при ИМбпST, но не от ИМпST. В Великобритании лечение ИМпST осуществляется институционально, 22 , о чем свидетельствует поддержание очень высокого уровня помощи.Защита общенациональной первичной службы ЧКВ в Великобритании контрастирует с другими международными рекомендациями, взятыми из предварительной информации о чрезмерно загруженных услугах из-за дополнительной рабочей нагрузки, связанной с пациентами с COVID-19, и мерами больниц, введенными для уменьшения распространения инфекции. 8 Показатели смертности от ИМбпST повышались в фазе снижения, когда меньше пациентов посещало больницу. Возможно, что здесь играли роль и другие факторы, включая более высокое бремя сопутствующих заболеваний, более частую ишемию миокарда и, возможно, влияние инфекции COVID-19.Более того, наблюдалось снижение ИМбпST с отеком легких, что позволяет предположить, что пациенты с ишемией миокарда на больших площадях могли умереть в сообществе. Хотя стандарты внутрибольничного ухода поддерживались на высоком уровне, мы наблюдали несколько меньшее использование инвазивной коронарной стратегии и более низкие показатели межбольничного перевода для этой стратегии во время фазы снижения, что позволяет предположить, что, возможно, большее количество пациентов лечилось с медицинской точки зрения. в противном случае получил бы инвазивное лечение.
В отличие от других стран, где были изменены рекомендации по ведению пациентов с ОИМ, Великобритания сохранила свои процессы лечения ОИМ. Это было подтверждено на всех трех этапах периода этого исследования, когда использование доказательной помощи было очень высоким и несколько увеличивалось для антиагрегантной фармакотерапии. Более того, пандемия COVID-19 позволила провести естественный эксперимент со службами NHS AMI в Англии, что указывает на то, что для NSTEMI продолжительность инвазивной коронарной стратегии может быть значительно сокращена, когда соотношение персонала и медицинских учреждений к пациентам выросла.
Запрос этих данных в реальном времени из национального реестра AMI дает возможность подготовиться к будущим серьезным кризисам в области здравоохранения. Во-первых, очевидно, что до директив правительства о социальном дистанцировании общественность, казалось, реагировала на международный кризис, разворачивающийся через СМИ. Во-вторых, в то время как социальная изоляция была рекомендована для пациентов с более высоким риском, такие пациенты также подвержены более высокому риску ОИМ. Важно напоминать населению на этапе восстановления, что они должны посещать больницу в случае возникновения неотложной медицинской помощи — это сообщение было направлено как правительством, так и представителями здравоохранения в начале периода изоляции в Великобритании.В-третьих, хотя это исследование не смогло количественно оценить все неблагоприятные последствия, связанные со снижением и изменением представлений об ОИМ, в литературе есть убедительные доказательства более высоких показателей смертности, инсульта и сердечной недостаточности, когда пациенты с ОИМ не получают обращение или присутствие поздно. 23 Наконец, следует ожидать скрытого превышения смертности и заболеваемости, связанных с ОИМ, и заранее подготовить медицинские услуги. 23
Хотя сильные стороны этого связанного реестра очевидны, мы признаем ограничения исследования.MINAP не собирает данные по всем случаям ОИМ в Англии 24 , а по некоторым больницам загрузка данных задерживается. Это могло переоценить снижение показателей госпитализации. Тем не менее, мы обследовали все больницы неотложной помощи в Англии и призвали к быстрой отчетности. Связь с национальным регистром смертей позволила установить точные даты цензуры, но, учитывая короткое время наблюдения, возможно, что полное влияние пандемии COVID-19 на прогноз пациентов, госпитализированных с ОИМ, не очевидно.
Заключение
Общенациональные данные из Англии, связанные с регистрацией смертей, показывают, что после блокировки в Великобритании из-за пандемии COVID-19 число госпитализаций с ОИМ до минимума сократилось примерно на один месяц, что свидетельствует о том, что многие пациенты откладывали обращение за помощью в службы экстренной помощи. Несмотря на свидетельства сохранения высокого уровня специализированной стационарной помощи и увеличения числа ранних смертей от ИМбпST. Учитывая, что ОИМ является распространенным явлением и что отсроченное лечение ОИМ или его отсутствие связано с серьезными сердечно-сосудистыми и цереброваскулярными событиями, правительствам и системам здравоохранения во всем мире следует подготовиться к увеличению смертности и заболеваемости, связанных с ОИМ, в ближайшем будущем.
Дополнительные материалы
Дополнительные материалы доступны в European Heart Journal — Quality of Care and Clinical Outcomes онлайн.
Благодарности
J.W. имел полный доступ ко всем данным в исследовании и берет на себя ответственность за точность анализа данных. Национальный институт сердечно-сосудистых исходов, NICOR, предоставил NHS Digital Национальному проекту аудита ишемии миокарда, данные MINAP за 2017–2020 годы и взял на себя ответственность за целостность данных MINAP.Управление национальной статистики предоставило NSH Digital данные о смертности и берет на себя ответственность за достоверность этих данных. Авторы выражают признательность Крису Робаку и Тому Денвуду из NHS digital за предоставление и создание безопасной среды для размещения данных и аналитическую поддержку. Авторы выражают признательность Британскому фонду сердца / Национальному институту исследований в области здравоохранения за сотрудничество, которое уделяет приоритетное внимание исследовательским проектам COVID в Великобритании.
Финансирование
Дж.W. и C.P.G. финансируются Университетом Лидса. M.A.M. финансировался Университетом Кила. M.R. финансировался Национальным институтом исследований в области здравоохранения. Национальный проект аудита ишемии миокарда проводится по заказу Партнерства по улучшению качества здравоохранения в рамках Национальной программы клинического аудита и оценки результатов пациентов.
Конфликт интересов: Не объявлен.
Доступность данных
У авторов нет разрешения на передачу данных, но доступ к данным можно получить через NHS Digital после утверждения.
Список литературы
1Jia
JS
Лю
X
юаней
юаней
Сюй
Г
Джиа
Дж
Christakis
NA.
Поток населения определяет пространственно-временное распространение COVID-19 в Китае
.Природа
2020
;582
:389
—394
,3Mafham
MM
Spata
E
Голдакр
R
Gair
D
Curnow
P
Брей
М
и другие.Пандемия COVID-19, частота госпитализаций и лечения острых коронарных синдромов в Англии
.Ланцет
2020
. DOI: 10.1016 / S0140-6736 (20) 31356-8.4Metzler
B
Сиострзонек
П
Папка
RK
Бауэр
А
Reinstadler
SJ.
Снижение числа госпитализаций с острым коронарным синдромом в Австрии после вспышки COVID-19: пандемический ответ вызывает побочное повреждение сердца
.Eur Heart J
2020
; 41 :1852
—1853
.5De Filippo
O
D’Ascenzo
F
Анджелини
Ф
Боккино
PP
Conrotto
F
Saglietto
A
и другие.Снижение количества госпитализаций по поводу ОКС во время вспышки COVID-19 в Северной Италии
.N Engl J Med
2020
;383
:88
—89
.6Гарсия
Ю
Альбахдади
MS
Meraj
PM
Шмидт
С
Гарберих
Р
Джаффер
FA
и другие.Снижение числа активизаций лабораторий катетеризации сердца с подъемом сегмента ST в США во время пандемии COVID-19
.J Am Coll Cardiol
2020
; 75. дой: 10.1016 / j.jacc.2020.04.011.7Махмуд
E
Дауэрман
HL
Welt
FG
Посланник
JC
Rao
SV
Шлифовка
C
и другие.Ведение острого инфаркта миокарда во время пандемии COVID-19
.Катетер Cardiovasc Interv
2020
,8Tam
CF
Cheung
KS
Лам
S
Вонг
A
Юнг
A
Sze
M
и другие.Влияние вспышки коронавирусного заболевания 2019 г. (COVID-19) на лечение инфаркта миокарда с подъемом сегмента ST в Гонконге, Китай
.Circ Cardiovasc Qual Outcomes
2020
;13
:e006631
.9Han
Y
Цзэн
H
Цзян
H
Ян
Y
Юань
Z
Cheng
X
и другие.Консенсус экспертов CSC по принципам клинического ведения пациентов с тяжелыми сердечно-сосудистыми заболеваниями во время эпидемии COVID-19
.Тираж
2020
;141
: e810 – e816.10Дерево
DA
Сатанантан
Дж
Джин
К
Мансур
S
Ly
HQ
Quraishi
AU
Лавуа
A
и другие.Меры предосторожности и процедуры при коронарных и структурных вмешательствах на сердце во время пандемии COVID-19: руководство Канадской ассоциации интервенционной кардиологии
.Банка J Cardiol
2020
. doi: 10.1016 / j.cjca.2020.03.027.11Миссия Американской кардиологической ассоциации: «Мост жизни» и «Руководствуйтесь рекомендациями» Консультативная рабочая группа по ишемической болезни сердца и Комитеты Совета по клинической кардиологии по неотложной кардиологической помощи и общей кардиологии и интервенционной сердечно-сосудистой помощи.Временное руководство для систем оказания медицинской помощи при ИМпST во время пандемии COVID-19: миссия AHA: линия жизни. Тираж
2020
; 142 :199
—202
.12Daniels
MJ
Коэн
MG
Баври
AA
Кумбхани
DJ.
Реперфузия ИМпST в эпоху COVID-19 — все как обычно?
Тираж
2020
;141
:1948
—1950
.15Wilkinson
C
Вестон
С
Тиммис
A
Quinn
T
Ключи
A
Gale
CP.
Национальный аудиторский проект по ишемии миокарда (MINAP)
.Eur Heart J Qual Care Clin Outcomes
2020
;6
:19
—22
.16Рашид
M
Kontopantelis
E
Kinnaird
T
Curzen
N
Гейл
CP
Мохамед
MO
и другие.Связь между лабораторным статусом госпитального сердечного катетера, использованием инвазивной стратегии и исходами после NSTEMI
.Банка J Cardiol
2020
;36
:868
—877
.17Рашид
M
Curzen
N
Kinnaird
T
Lawson
CA
Myint
PK
Kontopantelis
E
и другие.Базовый риск, сроки инвазивной стратегии и соответствие руководящим принципам при ИМбпST: общенациональный анализ из MINAP
.Int J Cardiol
2020
;301
:7
—13
.18Антман
E
Басанд
J-P
Кляйн
Вт
Оман
М
Сендон
JLL
Rydén
L
и другие.Новое определение инфаркта миокарда — согласованный документ Объединенного комитета Европейского общества кардиологов / Американского колледжа кардиологов по новому определению инфаркта миокарда: Объединенный комитет Европейского общества кардиологов / Американского колледжа кардиологов
.JACC
2000
;36
:959
—969
,19Грейнджер
CB
Голдберг
RJ
Даббоус
О
Пипер
KS
Орел
KA
Пушка
CP
и другие.;Глобальный регистр исследователей острых коронарных событий
.Предикторы госпитальной смертности в глобальном регистре острых коронарных событий
.Arch Intern Med
2003
;163
:2345
—2353
,21Песнь
JG
Роджерс
WJ
Голдберг
RJ
Петерсон
ED
Венгер
NK
Vaccarino
В
Kiefe
CI
и другие.Связь возраста и пола с проявлением симптомов инфаркта миокарда и внутрибольничной смертностью
.JAMA
2012
;307
:813
—822
.22Холл
M
Лаут
К
Dondo
ТБ
Алабас
ОА
Броган
RA
Gutacker
N
и другие. ;Национальный институт исследований сердечно-сосудистых заболеваний
.Детерминанты первичного чрескожного коронарного вмешательства у пациентов и больниц в Англии, 2003-2013 гг.
.Сердце
2016
;102
:313
—319
., 23Шиоми
H
Накагава
Y
Моримото
T
Фурукава
Y
Накано
A
Шираи
Ю
и другие. ;Следователи CREDO-Kyoto AMI
.Связь времени начала баллона и времени от двери до баллона с долгосрочным клиническим исходом у пациентов с острым инфарктом миокарда с подъемом сегмента ST, перенесших первичное чрескожное коронарное вмешательство: обсервационное исследование
.BMJ
2012
;344
:e3257
.24Herrett
E
Шах
н.э.
Боггон
R
Denaxas
S
Смит
л
фургон Staa
T
и другие.Полнота и диагностическая достоверность регистрации случаев острого инфаркта миокарда в системе первичной медико-санитарной помощи, стационарной помощи, регистрах болезней и национальных регистрационных записях о смертности: когортное исследование
.BMJ
2013
;346
:f2350
.Опубликовано от имени Европейского общества кардиологов. Все права защищены. © Автор (ы) 2020. Для получения разрешений обращайтесь по электронной почте: [email protected].
Национальные тенденции в продолжительности пребывания в больницах по поводу острого инфаркта миокарда в Китае | BMC Cardiovascular Disorders
Yang G, Wang Y, Zeng Y, Gao GF, Liang X, Zhou M, Wan X, Yu S, Jiang Y, Naghavi M, Vos T, Wang H, Lopez AD, Murray CJ: Быстрый переход к здоровью в Китае, 1990–2010: результаты исследования глобального бремени болезней 2010. Lancet 2013, 381: 1987–2015. 10.1016 / S0140-6736 (13) 61097-1
Артикул PubMed Google Scholar
Moran A, Gu D, Zhao D, Coxson P, Wang YC, Chen CS, Liu J, Cheng J, Bibbins-Domingo K, Shen YM, He J, Goldman L: Будущие сердечно-сосудистые заболевания в Китае : модель Маркова и прогнозы сценариев факторов риска на основе модели политики в отношении ишемической болезни сердца — Китай. Circ Cardiovasc Qual Outcomes 2010, 3: 243–52. 10.1161 / CIRCOUTCOMES.109.
Статья PubMed PubMed Central Google Scholar
Kociol RD, Lopes RD, Clare R, Thomas L, Mehta RH, Kaul P, Pieper KS, Hochman JS, Weaver WD, Armstrong PW, Granger CB, Patel MR: Международные вариации и факторы, связанные с повторная госпитализация после инфаркта миокарда. JAMA 2012, 307: 66–74.10.1001 / jama.2011.1926
CAS Статья PubMed Google Scholar
Kaul P, Newby LK, Fu Y, Mark DB, Califf RM, Topol EJ, Aylward P, Granger CB, Van de Werf F, Armstrong PW: Международные различия в развитии ранних выделений после острого инфаркта миокарда . Lancet 2004, 363: 511–7. 10.1016 / S0140-6736 (04) 15536-0
Артикул PubMed Google Scholar
Wang L, Zhang M, Guo L, Qi J, Luo H, He H, Wang X, Yang H, Wu Y, Miu C, Chen X, Wu J: Клинические методы, основанные на интегративной медицине в китайских больницах, улучшают результаты лечения для пациентов с острым инфарктом миокарда: многоцентровое нерандомизированное исторически контролируемое исследование. Evid Based Complement Alternat Med 2012, 2012: 821641.
PubMed PubMed Central Google Scholar
Zhang Q, Zhang RY, Qiu JP, Zhang JF, Wang XL, Jiang L, Liao ML, Zhang JS, Hu J, Yang ZK, Shen WF: Проспективное многоцентровое рандомизированное исследование, сравнивающее перевод врача и пациента для первичного чрескожного коронарного вмешательства в острый инфаркт миокарда с подъемом сегмента ST. Chin Med J (Engl) 2008, 121: 485–91.
Google Scholar
Салех С.С., Каллан М., Террио М., Ландор N: Влияние на стоимость условий, приобретенных в больнице, среди пациентов, оказывающих интенсивную терапию. Med Care 2010, 48: 518–26. 10.1097 / MLR.0b013e3181dbd7ef
Статья PubMed Google Scholar
Mark DB, Newby LK: Ранняя выписка из больницы после неосложненного инфаркта миокарда: возможны ли дальнейшие улучшения? Eur Heart J 2003, 24: 1613–5. 10.1016 / S0195-668X (03) 00434-2
Артикул PubMed Google Scholar
Polverejan E, Gardiner JC, Bradley CJ, Holmes-Rovner M, Rovner D: Оценка средней стоимости больницы в зависимости от продолжительности пребывания и характеристик пациента. Health Econ 2003, 12: 935–47. 10.1002 / hec.774
Артикул PubMed Google Scholar
Soekhlal RR, Burgers LT, Redekop WK, Tan SS: Стоимость лечения острого инфаркта миокарда в Нидерландах. Neth Heart J 2013, 21: 230–5.10.1007 / s12471-013-0386-y
CAS Статья PubMed PubMed Central Google Scholar
Китайское кардиологическое общество: Рекомендации по диагностике и лечению нестабильной стенокардии / инфаркта миокарда без подъема сегмента ST. Чин Дж. Кардиол 2007, 35 (4) : 295–304.
Google Scholar
Китайское кардиологическое общество: Рекомендации по диагностике и лечению инфаркта миокарда с подъемом сегмента ST. Chin J Cardiol 2010, 38 (8) : 675–90.
Google Scholar
Hamm CW, Bassand JP, Agewall S, Bax J, Boersma E, Bueno H, Caso P, Dudek D, Gielen S, Huber K, Ohman M, Petrie MC, Sonntag F, Uva MS, Storey RF , Wijns W, Zahger D, ESC Комитет по практическим рекомендациям: ESC Рекомендации по лечению острых коронарных синдромов у пациентов без стойкого подъема сегмента ST: Целевая группа по лечению острых коронарных синдромов (ACS) у пациентов без стойкое повышение сегмента ST по оценке Европейского общества кардиологов (ESC). Eur Heart J 2011, 32: 2999–3054.
Артикул PubMed Google Scholar
Van de Werf F, Bax J, Betriu A, Blomstrom-Lundqvist C, Crea F, Falk V, Filippatos G, Fox K, Huber K, Kastrati A, Rosengren A, Steg PG, Tubaro M, Verheugt F, Weidinger F, Weis M, Комитет по практическим рекомендациям ESC (CPG): Ведение острого инфаркта миокарда у пациентов со стойким подъемом сегмента ST: Целевая группа по лечению острого инфаркта миокарда в Европе с подъемом сегмента ST Общество кардиологов. Eur Heart J 2008, 29: 2909–45.
CAS Статья PubMed Google Scholar
O’Gara PT, Kushner FG, Ascheim DD, Casey DE Jr, Chung MK, de Lemos JA, Ettinger SM, Fang JC, Fesmire FM, Franklin BA, Granger CB, Krumholz HM, Linderbaum JA, Morrow Д.А., Ньюби Л.К., Орнато Дж. П., Оу Н, Рэдфорд М.Дж., Тамис-Холланд Дж. Э., Томмазо К.Л., Трейси С.М., Ву Ю.Дж., Чжао Д.X., Андерсон Дж.Л., Джейкобс А.К., Гальперин Дж.Л., Альберт Н.М., Бриндис Р.Г., Крегер М.А., Деметс D, Фонд Американского колледжа кардиологов / Целевая группа Американской кардиологической ассоциации по практическим рекомендациям, и др. .: Руководство ACCF / AHA по лечению инфаркта миокарда с подъемом сегмента ST, 2013: отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации по практическим рекомендациям. Обращение 2013, 127 (4) : e362–425.
Артикул PubMed Google Scholar
Джнейд Х., Андерсон Дж. Л., Райт Р.С., Адамс К.Д., Бриджес С.Р., Кейси Д.Е.-младший, Эттингер С.М., Фесмир Ф.М., Ганиатс Т.Г., Линкофф А.М., Петерсон Э.Д., Филиппидес Дж. Дж., Теру П., Венгер Н. JP, Андерсон Дж. Л., Авторский комитет 2012 Члены: 2012 ACCF / AHA Обновление Руководства по ведению пациентов с нестабильной стенокардией / инфарктом миокарда без подъема сегмента ST (Обновление Руководства 2007 года и замена целевого обновления 2011 года): a отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации о практических рекомендациях. Тираж 2012 г., 126: 875–910.
Артикул PubMed Google Scholar
Berger AK, Duval S, Jacobs DR Jr, Barber C, Vazquez G, Lee S, Luepker RV: Отношение продолжительности пребывания в больнице при остром инфаркте миокарда к смертности после выписки. Am J Cardiol 2008, 101: 428–34. 10.1016 / j.amjcard.2007.09.090
Статья PubMed PubMed Central Google Scholar
Baker DW, Einstadter D, Husak SS, Cebul RD: Тенденции смертности после выписки и повторной госпитализации: не слишком ли сильно сократилась продолжительность пребывания? Arch Intern Med 2004, 164: 538–44. 10.1001 / archinte.164.5.538
Артикул PubMed Google Scholar
Saczynski JS, Lessard D, Spencer FA, Gurwitz JH, Gore JM, Yarzebski J, Goldberg RJ: Сокращение продолжительности пребывания пациентов, госпитализированных с ОИМ: влияние на смертность и повторные госпитализации. Am J Med 2010, 123: 1007–15. 10.1016 / j.amjmed.2010.05.018
Статья PubMed PubMed Central Google Scholar
Kaboli PJ, Go JT, Hockenberry J, Glasgow JM, Johnson SR, Rosenthal GE, Jones MP, Vaughan-Sarrazin M: Связи между сокращением продолжительности пребывания в больнице и 30-дневным коэффициентом повторной госпитализации и смертностью: 14 -летний опыт работы в 129 больницах по делам ветеранов. Ann Intern Med 2012, 157: 837–45.10.7326 / 0003-4819-157-12-201212180-00003
Артикул PubMed Google Scholar
Kotowycz MA, Cosman TL, Tartaglia C, Afzal R, Syal RP, Natarajan MK: Безопасность и возможность ранней выписки из больницы при инфаркте миокарда с подъемом сегмента ST — проспективное и рандомизированное исследование в группах низкого риска пациенты с первичным чрескожным коронарным вмешательством (исследование Safe-Depart). Am Heart J 2010, 159: 117 e1–6.
Артикул Google Scholar
Yip HK, Wu CJ, Chang HW, Hang CL, Wang CP, Yang CH, Hung WC, Yu TH, Yeh KH, Chua S, Fu M, Chen MC: Возможность и безопасность ранней выписки для пациентов низкого риска с острым инфарктом миокарда после успешного прямого чрескожного коронарного вмешательства. Jpn Heart J 2003, 44: 41–9. 10.1536 / jhj.44.41
Артикул PubMed Google Scholar
Smith EJ, Rothman MT, Timmis AD: Длительное пребывание в больнице после острого инфаркта миокарда: оценка доказательств. Ланцет 2004, 363: 502–3. 10.1016 / S0140-6736 (04) 15574-8
Артикул PubMed Google Scholar
Topol EJ, Burek K, O’Neill WW, Kewman DG, Kander NH, Shea MJ, Schork MA, Kirscht J, Juni JE, Pitt B: Рандомизированное контролируемое испытание выписки из больницы через три дня после миокарда инфаркт в эпоху реперфузии. N Engl J Med 1988, 318: 1083–8. 10.1056 / NEJM198804283181702
CAS Статья PubMed Google Scholar
Дхармараджан К., Ли Дж., Ли Х, Лин З, Крумхольц Х.М., Цзян Л: Китайское ретроспективное исследование острого инфаркта миокарда по оценке сердечных событий, ориентированное на пациента (China PEACE): дизайн исследования. Circ Cardiovasc Qual Outcomes 2013, 6: 732–40.10.1161 / CIRCOUTCOMES.113.000441
Артикул PubMed PubMed Central Google Scholar
Li J, Li X, Wang Q, Hu S, Wang Y, Masoudi FA, Spertus JA, Krumholz HM, Jiang L, для China PEACE Collaborative Group: Тенденции в характеристиках, лечении и результатах среди пациенты с инфарктом миокарда с подъемом сегмента ST в Китае с 2001 по 2011 г .: Китайское ретроспективное исследование ОИМ PEACE. Ланцет 2014.DOI: 10.1016 / S0140–6736 (14) 60921–1
Google Scholar
Khouw N, Wasim M, Aziz A, Uppal H, Chandran S, Potluri R: У южноазиатских пациентов с инфарктом миокарда продолжительность пребывания в больнице короче. Int J Cardiol 2014, 171: e54–5. 10.1016 / j.ijcard.2013.11.111
Статья PubMed Google Scholar
Choi JS, Kim YA, Kang YU, Kim CS, Bae EH, Ma SK, Ahn YK, Jeong MH, Kim SW: Клинические последствия внутрибольничной анемии в сочетании с острым повреждением почек и хронической почкой заболевание у больных острым инфарктом миокарда. PLoS One 2013, 8: e75583. 10.1371 / journal.pone.0075583
CAS Статья PubMed PubMed Central Google Scholar
Hamada H, Sekimoto M, Imanaka Y: Влияние системы предполагаемой суточной оплаты с системой группировки, подобной DRG (DPC / PDPS), на использование ресурсов и качество здравоохранения в Японии. Политика здравоохранения 2012, 107: 194–201. 10.1016 / j.healthpol.2012.01.002
Артикул PubMed Google Scholar
Джонс К., Саксон Л., Каннингем В., Адамс П.: Вторичная профилактика для пациентов после инфаркта миокарда: краткое изложение обновленных рекомендаций NICE. BMJ 2013, 347: f6544. 10.1136 / bmj.f6544
Артикул PubMed Google Scholar
Ades PA: Кардиологическая реабилитация и вторичная профилактика ишемической болезни сердца. N Engl J Med 2001, 345 (12) : 892–902. 10.1056 / NEJMra001529
CAS Статья PubMed Google Scholar
Wang W, председатель SY, Thompson DR, Twinn SF: Восприятие медицинскими работниками больничной кардиологической реабилитации в материковом Китае: предварительное исследование. J Clin Nurs 2009, 18 (24) : 3401–8. 10.1111 / j.1365-2702.2009.02876.x
Артикул PubMed Google Scholar
Лю CY, Wang XY, Hua J: Какое будущее у врачей в Китае? Ланцет 2013, 382: 937.
Артикул PubMed Google Scholar
Прекращение насилия в отношении врачей в Китае Lancet 2012, 379: 1764.
Инь Дж., Лурас Х., Хаген Т.П., Даль Ф.А.: Влияние финансирования на основе видов деятельности на продолжительность пребывания в больнице пожилых пациентов, страдающих сердечными заболеваниями, в Норвегии. BMC Health Serv Res 2013, 13: 172. 10.1186 / 1472-6963-13-172
Статья PubMed PubMed Central Google Scholar
Гао Ц., Сюй Ф., Лю GG: Платежная реформа и изменения в здравоохранении в Китае. Soc Sci Med 2014, 111: 10–6.
Артикул PubMed Google Scholar
Подробная информация о внедрении базового медицинского страхования для городских жителей в Пекине [http://www.bjld.gov.cn/cardbiz/BulletinChild/122/201151673430/news.htm]
Пилотные схемы базового медицинского страхования для городских жителей в Шанхае http://www.shanghai.gov.cn/shanghai/node2314/node3124/node3125/node3131/userobject6ai1841.html
Santolucito PA, Tighe DA, McManus DD, Yarzebski J, Lessard D, Gore JM, Goldberg RJ: Лечение и исходы заболевания почек и острого инфаркта миокарда. Am J Med 2010, 123: 847–55. 10.1016 / j.amjmed.2010.04.025
Статья PubMed PubMed Central Google Scholar
Куо Ю.Ф., Гудвин JS: Влияние госпиталистов на продолжительность пребывания в популяции медперсонала: вариации в зависимости от характеристик больницы и пациента. J Am Geriatr Soc 2010, 58: 1649–57. 10.1111 / j.1532-5415.2010.03007.x
Артикул PubMed PubMed Central Google Scholar
Министерство здравоохранения Китая: Руководство по управлению клиническими путями (экспериментальная основа). http://www.nhfpc.gov.cn/yzygj/s3589/200910/479af260b55a4fc3b4b978321b56b465.shtml
Drye EE, Normand SL, Wang Y, Rossapp JS, Schreiner R GC, Han L HM: Сравнение стандартизированных по больничному риску показателей смертности, рассчитанных с использованием внутрибольничных и 30-дневных моделей: обсервационное исследование с последствиями для составления профилей в больницах. Ann Intern Med 2012, 156: 19–26. 10.7326 / 0003-4819-156-1-201201030-00004
Артикул PubMed PubMed Central Google Scholar
Hakkinen U, Chiarello P, Cots F, Peltola M, Ratto H: Классификация пациентов и больничные расходы на лечение острого инфаркта миокарда в девяти европейских странах. Health Econ 2012, 21 (Дополнение 2) : 19–29.
Артикул PubMed Google Scholar
Vavalle JP, Lopes RD, Chen AY, Newby LK, Wang TY, Shah BR, Ho PM, Wiviott SD, Peterson ED, Roe MT, Granger CB: Продолжительность пребывания в больнице пациентов с не-ST инфаркт миокарда с подъемом сегмента. Am J Med 2012, 125: 1085–94. 10.1016 / j.amjmed.2012.04.038
Статья PubMed Google Scholar
Chen E, Naylor CD: Различия в продолжительности пребывания в больнице по поводу острого инфаркта миокарда в Онтарио, Канада. Med Care 1994, 32: 420–35. 10.1097 / 00005650-19
00-00002CAS Статья PubMed Google Scholar
Pearson SD, Kleefield SF, Soukop JR, Cook EF, Lee TH: Критические меры вмешательства для сокращения продолжительности пребывания в больнице. Am J Med 2001, 110: 175–80.10.1016 / S0002-9343 (00) 00705-1
CAS Статья PubMed Google Scholar
Huerta S, Heber D, Sawicki MP, Liu CD, Arthur D, Alexander P, Yip I, Li ZP, Livingston EH: Сокращение продолжительности пребывания за счет внедрения клинической схемы бариатрической хирургии в академической среде. центр здравоохранения. Am Surg 2001, 67: 1128–35.
CAS PubMed Google Scholar
Стивен А.Е., Бергер DL: Сокращение продолжительности пребывания в больнице и снижение затрат в больнице с внедрением ускоренного пути оказания клинической помощи после плановой резекции толстой кишки. Хирургия 2003, 133: 277–82. 10.1067 / мсы.2003.19
Статья PubMed Google Scholar
Powell-Jackson T, Yip WC, Han W: Изменение стимулов со стороны спроса и предложения для улучшения обращения за первичной медико-санитарной помощью в сельских районах Китая. Health Econ 2014. doi: 10.1002 / hec.3060
Google Scholar
Рейнхольд Т., Тирфельдер К., Мюллер-Рименшнайдер Ф., Виллих С.Н.: Экономические последствия для здоровья после внедрения DRG — систематический обзор. Gesundheitswesen 2009, 71 (5) : 306–12. 10.1055 / с-0028-1119399
CAS Статья PubMed Google Scholar
Kominski GF, Witsberger C: Тенденции в отношении продолжительности пребывания пациентов в программе Medicare: 1979–87. Health Care Financ Rev 1993, 15 (2) : 121–35.
CAS PubMed PubMed Central Google Scholar
Ван З., Лю Р., Ли П, Цзян C: Изучение перехода на КРГ в развивающихся странах: тематическое исследование в Шанхае, Китай. Pak J Med Sci 2014, 30 (2) : 250–5.
CAS PubMed PubMed Central Google Scholar
Спенсер Ф.А., Лессард Д., Гор Дж. М., Ярзебски Дж., Голдберг Р. Дж.: Уменьшение продолжительности пребывания в больнице по поводу острого инфаркта миокарда и исходов после выписки: взгляд в масштабах всего сообщества. Arch Intern Med 2004, 164: 733–40. 10.1001 / archinte.164.7.733
Артикул PubMed Google Scholar
Paul SD, Eagle KA, Guidry U, DiSalvo TG, Villarreal-Levy G, Smith AJ, O’Donnell CJ, Mahjoub ZA, Muluk V, Newell JB, O’Gara PT: Есть ли гендерные различия в представлении и управлении влияют на предикторы стоимости госпитализации и продолжительности пребывания после острого инфаркта миокарда? Am J Cardiol 1995, 76: 1122–5. 10.1016 / S0002-9149 (99) 80318-X
CAS Статья PubMed Google Scholar
Schellings DA, Ottervanger JP, Hof AW V ‘t, de Boer MJ, Dambrink JH, Hoorntje JC, Gosselink And M, Suryapranata H, Zwolle Исследовательская группа инфаркта миокарда: Предикторы и важность длительного пребывания в больнице после первичного ЧКВ для элевации ST инфаркт миокарда. Дис. Коронарной артерии 2011, 22: 458–62. 10.1097 / MCA.0b013e3283495d5f
Статья PubMed Google Scholar
Долговременная выживаемость пациентов с острым инфарктом миокарда и внебольничной остановкой сердца: проспективное когортное исследование
Резюме
Цель
Сравнить краткосрочную и долгосрочную выживаемость пациентов, госпитализированных после острого приступа инфаркт миокарда (ОИМ) с остановкой сердца вне больницы (ВГОК) и без нее.
Методы
Проспективное когортное исследование всех пациентов с ОИМ, поступивших в университетскую больницу Осло Уллеваль с 1 сентября 2005 г. по 31 декабря 2011 г. Смертность от всех причин была получена из Норвежского регистра причин смерти с датой цензуры 31 декабря 2013 г. Кумулятивная выживаемость оценивалась с помощью метода Каплана-Мейера и таблицы выживаемости. Для сравнения рисков использовались логистическая регрессия и регрессия Кокса.
Результаты
Мы идентифицировали 404 пациента с ОИМ с ВГОК и 9425 пациентов без него.Пациенты с ОИМ без ВГОК были классифицированы как инфаркт миокарда с подъемом сегмента ST (ИМпST, n = 4522) или без ИМпST (ИМбпST, n = 4903). Средний возраст составил 63,6 ± стандартное отклонение (SD) 12,5, 63,8 ± 13,1 и 69,7 ± 13,6 лет для пациентов с ВГОК, ИМпST и ИМбпST, соответственно. Коронарная ангиография с последующим чрескожным коронарным вмешательством по показаниям была проведена у 87% пациентов с ВГК, 97% пациентов с ИМпST и 80% пациентов с ИМбпST. Тридцатидневная выживаемость составила 63%, 94% и 94%, а 8-летняя выживаемость — 49%, 74% и 57% соответственно.Среди пациентов, выживших в первые 30 дней, не было обнаружено существенной разницы в риске в течение длительного периода наблюдения (скорректированный коэффициент риска (aHR) OHCAvsSTEMI 1,15 [95% CI 0,82–1,60], aHR OHCAvsNSTEMI 0,89 [95% ДИ 0,64–1,24]).
Выводы
Долгосрочная выживаемость после ВГОК, вызванного ОИМ, была хорошей: 49% госпитализированных пациентов остались живы через восемь лет. Хотя краткосрочная смертность оставалась высокой, пациенты с ВГОК, живущие через 30 дней, имели такой же долгосрочный риск, что и пациенты с ОИМ без ВГОК.
Ключевые слова
Остановка сердца вне больницы
Острый инфаркт миокарда
Долговременная выживаемость
Рекомендуемые статьиЦитирующие статьи (0)
Просмотреть аннотацию© 2017 Автор (ы). Опубликовано Elsevier Ireland Ltd.
Рекомендуемые статьи
Цитирующие статьи
Остановка сердца после инфаркта миокарда вне больницы
Quick Takes
- В современном общенациональном шведском регистре частота внебольничной остановки сердца (ВГОК) в течение 90 дней после инфаркта миокарда равна 0.3% у пациентов, перенесших коронарную ангиографию в стационаре и выписанных без ИКД.
- Помимо ФВЛЖ, предикторы ВГОК включали мужской пол, диабет, почечную недостаточность, сердечную недостаточность и недавно выявленную фибрилляцию предсердий или трепетание предсердий.
Учебных вопросов:
Какова частота внезапной сердечной смерти (ВСС) и ее предикторы на раннем этапе после инфаркта миокарда (ИМ) в современной Швеции?
Методы:
Авторы использовали данные SWEDEHEART, Шведского реестра сердечно-легочной реанимации и Шведского реестра кардиостимуляторов и имплантируемых кардиовертеров-дефибрилляторов (ICD).Пациенты с инфарктом миокарда, перенесшие коронарную ангиографию и выписанные живыми в период с 2009 по 2017 год без предварительной ИКБ, наблюдались в течение 90 дней. Для оценки связи между клиническими параметрами и остановкой сердца вне больницы использовались модели регрессии Кокса. (OHCA).
Результатов:
Из 121 379 случаев ВГКА произошла у 349 (0,29%), а смерть без ВГКА — у 2194 (1,8%). Всего шесть переменных (мужской пол, диабет, расчетная скорость клубочковой фильтрации 2, класс Киллипа ≥II, впервые возникшая фибрилляция / трепетание предсердий и нарушение фракции выброса левого желудочка [LVEF], классифицированных как 40-49%, 30-39% , а также
Выводы:
В этом общенациональном исследовании частота ВГОК в течение 90 дней после ИМ была
Перспектива:
Текущий анализ показывает, что частота ВСС в течение 90 дней после инфаркта миокарда и ангиографии составляет около 0.3%, что ниже, чем показали предыдущие исследования и исторические данные. Частично это может быть связано с улучшением показателей реваскуляризации и лечения в соответствии с рекомендациями. Помимо ФВЛЖ, предикторы ВГОК включали мужской пол, диабет, почечную недостаточность, сердечную недостаточность и недавно выявленную фибрилляцию предсердий или трепетание предсердий. Необходимы дальнейшие исследования, чтобы оценить полезность включения критериев отбора помимо ФВЛЖ для выявления пациентов, которым полезны стратегии профилактики ВГОК на раннем этапе после ИМ.
Клинические темы: Острые коронарные синдромы, аритмии и клинические EP, сердечная недостаточность и кардиомиопатии, инвазивная сердечно-сосудистая ангиография и вмешательство, неинвазивная визуализация, профилактика, имплантируемые устройства, SCD / желудочковые аритмии, аритмия / аритмия предсердий, аритмия предсердий и ACS, Вмешательства и визуализация, Ангиография, Ядерная визуализация
Ключевые слова: Острый коронарный синдром, Аритмия, Сердечный, Фибрилляция предсердий, Трепетание предсердий, Коронарная ангиография, Смерть, Внезапная, Сердечная ангиография, Дефибрилляторы Смерть Скорость клубочковой фильтрации, Сердечная недостаточность, Инфаркт миокарда, Остановка сердца вне больницы, Выписка пациента, Почечная недостаточность, Вторичная профилактика Инсультная функция , Левый
<Вернуться к спискам
Взаимосвязь между ранним наблюдением врача и 30-дневной повторной госпитализацией после острого инфаркта миокарда и сердечной недостаточности
Аннотация
Фон
Тридцатидневная частота повторных госпитализаций после острого инфаркта миокарда (ОИМ) и сердечной недостаточности являются важными показателями результатов лечения пациентов.Раннее наблюдение врача после выписки из больницы пропагандируется как метод снижения частоты повторной госпитализации в течение 30 дней. Однако связь s между ранним наблюдением после выписки и 30-дневной повторной госпитализацией по поводу ОИМ и сердечной недостаточности неубедительна. Мы использовали общенациональные популяционные данные для изучения взаимосвязи между 7-дневным наблюдением врача и 30-дневной повторной госпитализацией, а также дальнейшими ассоциациями 7-дневного врача (во время основной госпитализации и при последующем наблюдении) и последующего наблюдения кардиолога с 30-дневная повторная госпитализация по поводу инфаркта миокарда без подъема сегмента ST (ИМбпST) или сердечной недостаточности.
Методы
Мы проанализировали всех пациентов 18 лет и старше с ИМбпST и сердечной недостаточностью, выписанных из больниц в 2010 году на Тайване с помощью Тайваньской национальной исследовательской базы данных по медицинскому страхованию. Модели пропорциональных рисков Кокса с надежными оценками дисперсии сэндвича и взвешиванием баллов склонности были выполнены после корректировки характеристик пациента и больницы для проверки связи между 7-дневным периодом наблюдения врача и 30-дневным повторным посещением.
Результаты
Популяция исследования ИМбпST и сердечной недостаточности включала 5008 и 13 577 пациентов, соответственно.Раннее наблюдение врача было связано с более низким коэффициентом риска повторной госпитализации по сравнению с отсутствием раннего наблюдения врача для пациентов с ИМбпST (отношение рисков [HR], 0,47; 95% доверительный интервал [CI], 0,39–0,57), и для пациенты с сердечной недостаточностью (ОР 0,54; 95% ДИ 0,48–0,60). Последующее наблюдение у одного и того же врача было связано с меньшим коэффициентом риска повторной госпитализации по сравнению с наблюдением другого врача для пациентов с ИМбпST (ОР 0,56; 95% ДИ 0,48–0,65) и для пациентов с сердечной недостаточностью (ОР 0.69; 95% ДИ, 0,62–0,76).
Выводы
Для каждого состояния пациенты, которые обращаются к врачу амбулаторно в течение 7 дней после выписки, имеют более низкий риск 30-дневной повторной госпитализации. Более того, пациенты, которые амбулаторно посещают того же врача в течение 7 дней после выписки, имеют гораздо меньший риск 30-дневной повторной госпитализации.
Образец цитирования: Tung Y-C, Chang G-M, Chang H-Y, Yu T-H (2017) Взаимосвязь между ранним наблюдением врача и 30-дневной повторной госпитализацией после острого инфаркта миокарда и сердечной недостаточности.PLoS ONE 12 (1): e0170061. https://doi.org/10.1371/journal.pone.0170061
Редактор: Джузеппе Андо, Мессинский университет, ИТАЛИЯ
Поступила: 15 июня 2016 г .; Принята к печати: 28 декабря 2016 г .; Опубликован: 27 января 2017 г.
Авторские права: © 2017 Tung et al. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Набор данных, используемый в этом исследовании, принадлежит Министерству здравоохранения и социального обеспечения Тайваня (MOHW). Министерство здравоохранения и социального обеспечения должно одобрить наше приложение для доступа к этим данным. Любой исследователь, заинтересованный в доступе к этому набору данных, может подать заявку в Министерство здравоохранения и социального обеспечения с просьбой о доступе. Пожалуйста, свяжитесь с сотрудниками MOHW (электронная почта: [email protected]) для получения дополнительной помощи. Адрес Министерства здравоохранения и социального обеспечения Тайваня: No.488, п. 6, Zhongxiao E. Rd., Nangang District, Taipei City 115, Тайвань (R.O.C.). Телефон: + 886-2-8590-6848.
Финансирование: Министерство науки и технологий Тайваня предоставляет финансовую поддержку (MOST 103-2410-H-002-209-MY2 и MOST 105-2410-H-002-220-MY2). Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Авторы заявили об отсутствии конкурирующих интересов.
Введение
Политики, клиницисты и плательщики, которые стремятся улучшить результаты в области здравоохранения, сосредоточивают внимание на 30-дневных показателях повторной госпитализации пациентов с острым инфарктом миокарда и пациентов с сердечной недостаточностью [1]. Раннее наблюдение врача после выписки из больницы пропагандируется как метод снижения частоты повторных госпитализаций [2]. Однако исследования взаимосвязи между ранним наблюдением после выписки и исходами пациентов по поводу острого инфаркта миокарда и сердечной недостаточности не только редки, но и неубедительны.Из всего двух известных нам исследований по этой теме одно показало, что выписка из больниц с более высокими показателями раннего последующего наблюдения связана с сокращением 30-дневной повторной госпитализации по поводу сердечной недостаточности [3], но другое не установило такой взаимосвязи. для острого инфаркта миокарда. [4] Более того, насколько нам известно, ни одно исследование не изучало, связано ли раннее наблюдение с одним и тем же врачом или кардиологом с более низкой 30-дневной повторной госпитализацией пациентов с острым инфарктом миокарда и пациентов с сердечной недостаточностью.
Предполагается, что раннее или своевременное амбулаторное наблюдение у врача для дальнейшей оценки или лечения влияет на снижение количества повторных госпитализаций среди выписанных пациентов с сердечной недостаточностью и пациентов с острым инфарктом миокарда. [3–7] Переход из больницы в дом. это период особенно высокого риска. Своевременное наблюдение после выписки было предложено в качестве важного компонента усилий по оптимизации ухода за больными в переходный период во время периода высокого риска после выписки.[8, 9] При физиологическом стрессе и аллостатической нагрузке, вызванных госпитализацией, могут существовать риски в критический 30-дневный период после выписки. [10] Что еще более важно, ближайшие дни после выписки также являются уязвимым периодом из-за дополнительных методов лечения или изменений в существующей медицинской терапии, которые могут ухудшить результаты лечения пациентов. [3, 11] Семидневное наблюдение у врачей может иметь преимущество в виде улучшение результатов лечения пациентов за счет предоставления клинических вмешательств в отношении нестабильности заболевания (например, диагностических тестов и смены лекарств) [12] и 7-дневного наблюдения у одного и того же врача (из-за преемственности врачей) или у специалиста (из-за специальности врача) может быть связан с лучшими результатами, чем наблюдение у других врачей.[3, 4] Однако в нескольких исследованиях изучалась взаимосвязь между 7-дневным наблюдением врача и результатами лечения пациентов.
На Тайване Национальное управление медицинского страхования является единственным страховщиком и внедряет национальное медицинское страхование с 1 марта 1995 года. Уровень покрытия национального медицинского страхования достиг 99,9%, и почти все медицинские учреждения являются поставщиками услуг национального медицинского страхования. Каждый участник может бесплатно посещать любую больницу или клинику и пользуется комплексными преимуществами с политикой низкого распределения затрат (совместное страхование 10% для стационарного лечения с годовым лимитом около 1700 долларов США и 1 долларом США.7–12,0 доплата за амбулаторный прием). Национальная администрация медицинского страхования возмещала поставщикам в основном на основе платы за услуги с начала реализации национальной программы медицинского страхования. Программа сокращения реадмиссии в больницы, которая в соответствии с Законом о доступном медицинском обслуживании требует, чтобы центры услуг Medicare и Medicaid сокращали выплаты больницам с чрезмерным процентом повторной госпитализации в связи с острым инфарктом миокарда и сердечной недостаточностью [13], еще не введена на Тайване.Таким образом, система здравоохранения Тайваня предоставляет прекрасную возможность проверить, улучшает ли раннее наблюдение после выписки результаты лечения пациентов с острым инфарктом миокарда и пациентов с сердечной недостаточностью.
Чтобы лучше понять взаимосвязь между ранним наблюдением после выписки и исходами пациентов, мы использовали общенациональные популяционные данные из Тайваня, чтобы изучить, было ли наблюдение врача в течение 7 дней после выписки связано с сокращением 30-дневной повторной госпитализации для пациенты с острым инфарктом миокарда и с сердечной недостаточностью.Мы также определили, было ли раннее наблюдение у того же врача или кардиолога связано с гораздо лучшими результатами для пациентов.
Методы
База данных
В этом исследовании мы использовали Национальную базу данных исследований в области медицинского страхования, предоставленную Национальным управлением медицинского страхования и управляемую Национальными научно-исследовательскими институтами здравоохранения Тайваня. База данных, которая выпускается ежегодно, состоит из следующих параметров: заявки на получение стационарной медицинской помощи, заявки на получение медицинской помощи при амбулаторном лечении, заявки на получение фармацевтической помощи, медицинские учреждения, работающие по контракту, специалисты здравоохранения в учреждениях медицинского обслуживания, работающие по контракту, и получатели помощи.Таким образом, база данных дает возможность изучить взаимосвязь между ранним наблюдением после выписки и результатами лечения пациентов.
Этическое заявление
Протокол этого исследования был одобрен Экспертным советом больницы Национального Тайваньского университета (протокол № 201601056RINB). Набор данных, который мы использовали в этом исследовании, был вторичными данными; вся информация была обезличена владельцами данных.
Популяция исследования
В это исследование были включены все пациенты в возрасте 18 лет и старше, которые были выписаны из больниц неотложной помощи в 2010 г. с основным диагнозом острого инфаркта миокарда без подъема сегмента ST (Международная классификация болезней, 9-й пересмотр, клиническая модификация [МКБ-9 -CM] код 410.7) [4, 14–16] и сердечная недостаточность с сохраненной фракцией выброса или без нее (код 428 МКБ-9-CM) соответственно [17–20]. [3, 4] Мы исключили пациентов, которые были госпитализированы с таким же заболеванием в течение последних 6 лет, умерли в больнице, были переведены, выписаны из больницы вопреки рекомендациям врача или были выписаны вопреки врачебной рекомендации в крайне критическом состоянии. состояние. [4, 21]
Меры переменных
Раннее наблюдение.
Раннее наблюдение определялось тем, имели ли выписанные пациенты амбулаторный визит к врачу в течение 7 дней после выписки. [3, 4] Продолжительность семи дней была выбрана в соответствии с текущими усилиями по улучшению ухода за переходным периодом. [22] ] Раннее наблюдение у одного и того же врача определялось тем, посещали ли выписанные пациенты того же врача во время госпитализации и во время раннего наблюдения [3]. Считается, что пациенты, которые посещают одного и того же врача во время госпитализации и при последующем наблюдении, имеют лучшую непрерывность лечения.[3, 19] Раннее наблюдение кардиолога определялось тем, посещали ли выписанные пациенты кардиолога в течение 7 дней после выписки. [3, 4] Чтобы изучить, является ли комбинированный эффект наблюдения одним и тем же врачом и последующего наблюдения кардиолога. также учитывались исходы пациентов, время взаимодействия между наблюдением одного и того же врача и наблюдением кардиолога.
Характеристики пациентов и больниц.
Ковариаты включали характеристики пациента и больницы. Ковариаты пациента включали пол, возраст, сопутствующие заболевания, историю болезни, лечение в стационаре (чрескожное коронарное вмешательство, использование отделения интенсивной терапии, проведение хирургической операции), продолжительность пребывания, исходные лекарства (аспирин, β-адреноблокаторы, статины, ингибитор ангиотензинпревращающего фермента / блокатор рецепторов ангиотензина), лекарства в течение 7 дней после выписки, низкий доход, сельское проживание, количество госпитализаций за последний год и количество посещений кабинета за последний год.[3, 4, 9, 19, 23–26].
Индекс Чарлсона-Дейо использовался для количественной оценки сопутствующих заболеваний у пациентов. [27] Этот индекс представляет собой сумму взвешенных баллов, основанных на наличии или отсутствии 17 различных заболеваний в течение прошлого года и индекса госпитализации. Оценка 0 означает отсутствие индекса коморбидности, а более высокие баллы указывают на большее бремя коморбидности. Кроме того, мы также измерили историю болезни пациентов, особенно связанную с сердечно-сосудистыми заболеваниями за последний год, и индексную госпитализацию, которая включала факторы сердечного риска (артериальная гипертензия, сахарный диабет), предшествующие сердечные заболевания (инфаркт миокарда, сердечная недостаточность, фибрилляция или трепетание предсердий). ) и сопутствующие соматические заболевания (заболевание периферических сосудов, почечная недостаточность).[28] Использование исходных лекарств измерялось в зависимости от того, были ли они назначены во время пребывания в больнице и при выписке. Низкий доход измерялся тем, был ли пациент зачислен как получатель помощи с низким доходом. Проживание в сельской местности определялось, проживает ли пациент в сельской местности, на основании предыдущих исследований с использованием базы данных национальных исследований в области медицинского страхования. [29–32]
Ковариаты больницы включали объем больницы (низкий, средний, высокий), уровень больницы (академический медицинский центр, региональный, районный), статус преподавателя (да / нет) и географическое положение (Тайбэй, север, центральный, южный, Као-Пин). , восточная).Мы определили объем пациентов, прошедших лечение в больницах, с использованием годового объема по конкретному состоянию, а затем разделили эти «годовые» объемы на тертили.
Показатели результата.
Нашим первичным результатом была 30-дневная повторная госпитализация по всем причинам, которая определялась как любая повторная госпитализация в любую больницу неотложной помощи в течение 30 дней после выписки. [3, 4] Повторная госпитализация рассматривается как потенциальные индикаторы плохой помощи или упущенные возможности лучше координировать уход.[33, 34] Кроме того, повторная госпитализация обходится системе здравоохранения дорого и обычно представляет собой предотвратимое нежелательное явление для пациентов. [24] Вторичными интересными исходами были повторная госпитализация в течение 30 дней после выписки по сердечно-сосудистой причине (первичный и вторичный коды МКБ-9-CM 390–459) [17, 35] и повторная госпитализация в течение 30 дней после выписки по той же причине, что и первичная госпитализация.
Статистический анализ
Мы использовали модели пропорциональных рисков Кокса с надежными оценками дисперсии «сэндвич» и взвешиванием по шкале склонностей, скорректированными для всех характеристик пациента и больницы, чтобы изучить связь между 7-дневным наблюдением врача и 30-дневным повторным посещением по поводу острого инфаркта миокарда и сердечной недостаточности.[28, 36] Модели пропорциональных рисков Кокса позволяют нам учитывать продолжительность выживания после выписки, чтобы избежать проблемы, заключающейся в том, что пациенты с ранним посещением являются наиболее тяжелыми, а затем они с меньшей вероятностью будут повторно госпитализированы, потому что они больше умирают. довольно часто. В моделях основное внимание уделялось времени от выписки до даты первой повторной госпитализации в течение 30 дней наблюдения. Пациенты подвергались цензуре в день смерти или через 30 дней после выписки, в зависимости от того, что наступило раньше. Все анализы были скорректированы для кластеризации на уровне больницы с использованием надежных оценок дисперсии сэндвича.Мы смоделировали 30-дневную реадмиссию в зависимости от 7-дневного наблюдения врача, пола, возраста, сопутствующих заболеваний, истории болезни, стационарного лечения, продолжительности пребывания, исходных лекарств, низкого дохода, проживания в сельской местности, количества госпитализаций в течение в прошлом году, количество посещений кабинета за последний год, объем больниц, уровень больниц, статус преподавателя и географическое положение.
Кроме того, мы использовали анализ предрасположенности, чтобы уменьшить систематическую ошибку отбора и потенциальные исходные различия между группами раннего наблюдения и группами без раннего наблюдения.[9, 28] Показатели предрасположенности были рассчитаны путем моделирования модели логистической регрессии, в которой зависимой переменной являлось наличие у выписанного пациента амбулаторного визита к врачу в течение 7 дней после выписки. Независимыми переменными были пол пациента, возраст, сопутствующие заболевания, история болезни, стационарное лечение, продолжительность пребывания, исходные лекарства, низкий доход, проживание в сельской местности, количество госпитализаций в течение прошлого года, количество посещений офиса в течение прошлого года, объем больниц, уровень больниц, статус преподавания и географическое положение.Затем каждый пациент был взвешен по шкале обратной склонности при выполнении моделей пропорциональных рисков Кокса с надежными оценками дисперсии сэндвича, чтобы уменьшить систематическую ошибку отбора [25, 37-40]
Наконец, мы далее использовали модели пропорциональных рисков Кокса с надежными оценками дисперсии сэндвича, скорректированными для всех пациентов (включая лекарства после выписки) и характеристик больниц, чтобы изучить индивидуальные и комбинированные ассоциации раннего наблюдения одного и того же врача и раннего кардиолога с 30-ю пациентами. дневная реадмиссия среди группы раннего наблюдения.При анализе чувствительности мы изменили определение раннего наблюдения врача, разрешив раннее наблюдение в течение 14 дней после выписки [3]. Статистическая значимость была обозначена двусторонним значением P <0,05. Все анализы были выполнены с использованием SAS версии 9.3 (SAS Institute Inc, Кэри, Северная Каролина).
Результаты
Базовые характеристики и результаты
Что касается инфаркта миокарда без подъема сегмента ST (ИМбпST), мы выявили 6596 пациентов, выписанных из больницы в 2010 году.Мы исключили пациентов в возрасте до 18 лет (N = 0) и пациентов, которые впоследствии были госпитализированы с NSTEMI (N = 397) или ранее госпитализировались с NSTEMI в течение последних 6 лет (N = 249). После исключения (рис. 1) окончательная популяция ИМбпST включала 5008 пациентов. Окончательная популяция с сердечной недостаточностью составила 13577 пациентов.
В таблице 1 представлены эти характеристики пациентов. Среди пациентов с ИМбпST частота раннего наблюдения у врача, у того же врача и у кардиолога составила 76.7%, 56,1% и 44,8% соответственно. Среди пациентов с сердечной недостаточностью частота раннего наблюдения у врача, у того же врача и у кардиолога составила 74,9%, 52,9% и 37,6% соответственно. Тридцатидневная частота повторных госпитализаций по всем причинам для пациентов с ИМбпST и пациентов с сердечной недостаточностью составила 19,9% и 23,3% соответственно.
Связь раннего наблюдения с характеристиками пациента и больницы
В таблице 2 показано сравнение выписок после амбулаторных посещений врача в течение 7 дней с выписками без них.Для NSTEMI исходными характеристиками, которые различались между группами наблюдения и группами без последующего наблюдения, были анамнез (сердечная недостаточность, фибрилляция или трепетание предсердий), использование ЧКВ, продолжительность сати, использование статинов, количество амбулаторных посещений за последний год. , объем, уровень и расположение больницы. В отношении сердечной недостаточности исходными характеристиками, которые различались между группами наблюдения и группами без наблюдения, были анамнез (артериальная гипертензия, сердечная недостаточность), использование ЧКВ, продолжительность пребывания, количество госпитализаций в течение последнего года, количество амбулаторных посещений в течение прошлый год, количество больниц, уровень, статус преподавателя и местоположение.После взвешивания баллов предрасположенности две группы ИМбпST и сердечной недостаточности были хорошо сбалансированы по исходным характеристикам.
Связь между ранним наблюдением и 30-дневной реадмиссией
В таблице 3 показаны нескорректированные связи между ранним врачебным наблюдением и характеристиками пациентов и больниц с 30-дневной повторной госпитализацией. Для каждого состояния раннее наблюдение у врача, раннее наблюдение у того же врача и раннее наблюдение у кардиолога были связаны с сокращением 30-дневной повторной госпитализации.Для двух состояний характеристиками пациента и больницы, связанными с 30-дневной повторной госпитализацией, были пол пациента, возраст, сопутствующие заболевания, история болезни, стационарное лечение, продолжительность пребывания, исходные лекарства, лекарства в течение 7 дней после выписки, низкий доход, количество количество госпитализаций за последний год, количество амбулаторных посещений за последний год, количество больниц, уровень и преподавательский статус.
Результаты серии моделей пропорциональных рисков Кокса с надежными оценками дисперсии сэндвича и взвешиванием по шкале склонности, как показано в таблице 4, демонстрируют связь между ранним последующим наблюдением и 30-дневной повторной госпитализацией после поправки на характеристики пациента и больницы.В модели 1 раннее наблюдение врача было связано с более низким коэффициентом риска повторной госпитализации по всем причинам по сравнению с отсутствием раннего наблюдения врача для пациентов с ИМбпST (отношение рисков [HR], 0,47; 95% доверительный интервал [CI], 0,39–0,57), а также для пациентов с сердечной недостаточностью (ОР 0,54; 95% ДИ 0,48–0,60). Раннее наблюдение врача также было связано с более низким 30-дневным периодом повторной госпитализации по сердечно-сосудистой причине и по той же причине.
Для дальнейшего определения индивидуальных и комбинированных ассоциаций наблюдения одного и того же врача и кардиолога с 30-дневной повторной госпитализацией среди пациентов с ранним наблюдением мы не обнаружили синергетических ассоциаций между эффектами наблюдения одного и того же врача и кардиолога.Таким образом, термин взаимодействия между одним и тем же врачом и последующим наблюдением кардиолога был удален в модели 2. Последующее наблюдение за одним и тем же врачом было связано с более низким коэффициентом риска повторной госпитализации по всем причинам по сравнению с наблюдением другого врача для пациентов с ИМбпST (HR, 0,56; 95% ДИ 0,48–0,65) и для пациентов с сердечной недостаточностью (ОР 0,69; 95% ДИ 0,62–0,76). Последующее наблюдение у врача также было связано с более низким 30-дневным периодом повторной госпитализации по сердечно-сосудистой причине и по той же причине. Надежность наших первичных результатов оценивалась анализом чувствительности.Результаты были аналогичными, когда мы изменили переходный период с 7 дней на 14 дней.
Обсуждение
Это исследование было первым исследованием, в котором использовались общенациональные популяционные данные для изучения связи между ранним наблюдением врача и 30-дневной повторной госпитализацией, а также относительной связи раннего наблюдения у одного врача и раннего кардиолога с 30-дневным периодом наблюдения. повторная госпитализация по поводу ИМбпST и сердечной недостаточности. Для каждого состояния мы обнаружили, что раннее наблюдение врача было связано с уменьшением 30-дневного повторного госпитализации по сравнению с отсутствием раннего наблюдения врача.Более того, раннее наблюдение у одного и того же врача было связано с более низкой 30-дневной повторной госпитализацией по сравнению с ранним наблюдением у другого врача.
На Тайване около 75% госпитализированных пациентов с ИМбпST и сердечной недостаточностью были амбулаторно посещены в течение 7 дней после выписки. Наиболее раннее последующее наблюдение осуществлялось тем же врачом, который лечил пациента во время основной госпитализации, и обычно кардиологами. Показатели раннего наблюдения врачом, одним и тем же врачом и ранним кардиологом на Тайване были выше, чем в Соединенных Штатах (38.3%, 18,1% и 7,5% соответственно для сердечной недостаточности) [3]. Эти результаты объясняются тем, что все больницы на Тайване являются закрытыми системами и оплачиваются как стационарные, так и амбулаторные услуги на платной основе Национальным управлением медицинского страхования (NHIA). Таким образом, врачам, работающим только в больницах, может быть разрешено лечить пациентов в стационаре, и больницы также используют переменную заработную плату, чтобы побудить штатных врачей оказывать стационарные и амбулаторные услуги. Более того, клинические руководства рекомендуют раннее наблюдение врача.Поэтому большинство больничных врачей не только назначают недельный запас лекарств при выписке, но также назначают контрольный визит в течение 7 дней после выписки.
Это исследование сделало два основных вывода о связи между ранним наблюдением врача и 30-дневной повторной госпитализацией по поводу ИМбпST и сердечной недостаточности. Во-первых, мы обнаружили, что раннее наблюдение у любого врача было связано с более низкой 30-дневной повторной госпитализацией для каждого состояния. Этот результат согласуется с выводом Hernandez et al.[3] Эрнандес и др. Подтвердили связь между ранним врачебным осмотром на уровне больницы и 30-дневной повторной госпитализацией среди получателей льгот Medicare, госпитализированных по поводу сердечной недостаточности. Однако агрегированная переменная на уровне группы (на уровне больницы) может использоваться в другой конструкции, нежели ее тезка на индивидуальном уровне (на уровне пациента). [41–43] Таким образом, ограничения использования агрегированного показателя в качестве косвенного показателя для его тезки на индивидуальном уровне относятся не только к ошибкам измерения, но и к построению достоверности, то есть к тому, действительно ли это один и тот же конструкт, который измеряется обеими переменными.[41, 43, 44]
Также необходимо отметить, что на уровне пациента связь между временем от выписки из больницы до амбулаторного наблюдения у врача и риском повторной госпитализации искажается тяжестью заболевания. Пациенты, перенесшие более тяжелый острый инфаркт миокарда или сердечную недостаточность или менее стабильные с медицинской точки зрения, не только обычно наблюдаются раньше после выписки из больницы, но и имеют более высокий риск повторной госпитализации. [3, 4] Поэтому мы использовали подход, основанный на оценке предрасположенности. исправьте ошибку выбора.Использование метода оценки склонности может помочь уменьшить систематическую ошибку выбора и обеспечить более достоверные результаты анализа. Это исследование может поддержать текущие клинические рекомендации, рекомендующие пациентам с сердечной недостаточностью или ИМбпST, выписанным из больницы, получить раннее или своевременное амбулаторное наблюдение у врача для дальнейшей оценки или лечения. [5, 7]
Еще одним примечательным открытием было то, что раннее наблюдение у одного и того же врача (преемственность врача) было связано с дальнейшим сокращением 30-дневной повторной госпитализации.Этот вывод согласуется с выводом ван Валравена и др. [23] и Макалистера и др. [19] В Онтарио, Канада, Walraven et al. Обнаружили, что 30-дневное наблюдение у одного и того же врача, а не у другого врача, было связано со снижением 30-дневной смертности после выписки или невыборной повторной госпитализацией в случае невыборной медицинской или хирургической операции. условия. В Альберте, Канада, McAlister et al. Обнаружили, что 30-дневное наблюдение у знакомого врача было связано с более низкой трехмесячной смертностью после выписки или срочной повторной госпитализацией по поводу сердечной недостаточности по сравнению с отсутствием последующего наблюдения.Хотя при выписке прогрессирование заболевания улучшается, ремиссии не достигается. Из-за раннего наблюдения у другого врача, если врач не знает прогрессирования заболевания у конкретного пациента, его прогрессирование может быть интерпретировано как ухудшение, требующее повторной госпитализации. [23] Более того, раннее наблюдение у того же врача с большей вероятностью позволит на раннем этапе определить терапевтическую эффективность и раннее выявить осложнения госпитальной терапии или процедур из-за знакомства с курсом лечения в больнице.Раннее обследование и лечение могут помочь избежать более серьезных последующих проблем, ведущих к повторной госпитализации.
В этом исследовании существовали некоторые ограничения. Во-первых, пациенты не распределялись случайным образом. Это наблюдательное и ретроспективное исследование; следовательно, мы не можем назначать исследуемых предметов случайным образом. Для уменьшения систематической ошибки отбора была принята оценка предрасположенности [25, 37-40]. Более того, хотя, как и в других исследованиях с использованием административных баз данных, информация о серьезности заболевания не была доступна для корректировки риска, мы скорректировали ее с учетом возраста пациента, сопутствующих заболеваний, интенсивной терапии. использование стационара и хирургическая операция, которые также важны для корректировки сложности заболевания.[9, 19, 23–26] Однако мы не можем полностью исключить возможность наличия неизмеримых искажающих факторов, таких как поведенческие факторы риска. Различия в результатах между группами последующего наблюдения и группами без наблюдения могут быть сбиты с толку неизмеренными поведенческими факторами риска, которые могут повлиять на доступ к медицинской помощи. Во-вторых, в этом исследовании раннее наблюдение определялось как амбулаторный визит в течение 7 дней после выписки. 7-дневное окно уже обсуждалось и было выбрано в соответствии с историческим прецедентом и клинической достоверностью.[3, 4] Однако мы также провели анализ чувствительности, изучающий связь между 14-дневным периодом наблюдения и 30-дневным повторным посещением.
Наконец, на Тайване до сих пор нечасто наблюдалось наблюдение у обученной и специализированной медсестры (менеджера по уходу). Это может быть связано с тем, что NHIA не возмещает эту услугу. Основываясь на двух связанных исследованиях, одно исследование выписанного пациента с сердечной недостаточностью в Северной Калифорнии, США, обнаружило, что раннее амбулаторное наблюдение у врача связано с более низким шансом 30-дневной повторной госпитализации, но последующее наблюдение по телефону с обученным врачом. а специализированная медсестра или фармацевт — нет.[45] Другое исследование, посвященное амбулаторным пациентам с сердечной недостаточностью в регионе Апулия в Италии, показало, что введение менеджеров по уходу в систему первичной медико-санитарной помощи имеет потенциал для сокращения повторных госпитализаций благодаря тесному партнерству между менеджером по уходу и пациентом сотрудничество между врачом и менеджером по уходу. [46] В будущих исследованиях необходимо выяснить, будет ли эффект раннего последующего визита к медицинскому работнику таким же, как у врача, у выписанных пациентов с сердечной недостаточностью или острым инфарктом миокарда.
Заключение
Наше национальное популяционное исследование показало, что 7-дневное наблюдение у врача было связано с меньшим 30-дневным повторным обращением, а непрерывность лечения у врача (7-дневное наблюдение у одного и того же врача) было связано с гораздо меньшим 30-дневным повторным обращением. для пациентов с ИМбпST и сердечной недостаточностью. Это исследование может предоставить доказательства в поддержку руководящих принципов, рекомендующих назначить ранний контрольный визит после выписки, и может предоставить основанный на доказательствах подход для улучшения 30-дневной повторной госпитализации после ИМбпST и сердечной недостаточности.
Благодарности
Исследование было поддержано грантами Министерства науки и технологий (MOST 103-2410-H-002-209-MY2 и MOST 105-2410-H-002-220-MY2) в Тайване и частично основано на данные из Национальной базы данных исследований в области медицинского страхования, предоставленные Национальным управлением медицинского страхования, Министерство здравоохранения и социального обеспечения и управляемые Национальными научно-исследовательскими институтами здравоохранения. Интерпретация и выводы, содержащиеся в данном документе, не отражают мнения Национального управления медицинского страхования, Министерства здравоохранения и социального обеспечения и Национальных научно-исследовательских институтов здравоохранения.
Вклад авторов
- Концептуализация: YCT.
- Обработка данных: YCT GMC THY.
- Формальный анализ: YCT GMC HYC THY.
- Получение финансирования: YCT.
- Исследование: YCT GMC HYC THY.
- Методология: YCT GMC HYC THY.
- Администрация проекта: YCT THY.
- Ресурсы: YCT THY.
- Программное обеспечение: YCT.
- Надзор: THY.
- Подтверждение: YCT GMC HYC THY.
- Визуализация: YCT.
- Написание — оригинальная черновик: YCT.
- Написание — просмотр и редактирование: YCT GMC HYC THY.
Ссылки
- 1. Центры услуг Medicare и Medicaid. Итоги 2015 г. [10 декабря 2015 г.]. http://www.cms.gov/Medicare/Quality-Initiatives-Patient-Assessment-Instruments/HospitalQualityInits/OutcomeMeasures.html.
- 2. Дженкс С.Ф., Уильямс М.В., Коулман Е.А. Повторные госпитализации среди пациентов, участвующих в программе оплаты медицинских услуг Medicare. N Engl J Med. 2009. 360 (14): 1418–28. pmid: 121
- 3. Hernandez AF, Greiner MA, Fonarow GC, Hammill BG, Heidenreich PA, Yancy CW и др. Взаимосвязь между ранним врачебным осмотром и 30-дневной повторной госпитализацией участников программы Medicare, госпитализированных по поводу сердечной недостаточности. ДЖАМА. 2010. 303 (17): 1716–22. pmid: 20442387
- 4.
Хесс К.Н., Шах Б.Р., Пэн С.А., Томас Л., Роу М.Т., Петерсон Э.Д.Связь раннего наблюдения врача и 30-дневного повторного госпитализации после инфаркта миокарда без подъема сегмента ST среди пожилых пациентов. Тираж. 2013. 128 (11): 1206–13. pmid: 23
5
- 5. Янси К.В., Джессап М., Бозкурт Б., Батлер Дж., Кейси Д.Е., Дразнер М.Х. и др. Руководство ACCF / AHA по лечению сердечной недостаточности, 2013: отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации по практическим рекомендациям. Тираж. 2013; 128 (16): e240 – e327.pmid: 23741058
- 6. О’Гара П.Т., Кушнер Ф.Г., Ашейм Д.Д., Кейси Д.Е., Чанг М.К., де Лемос Дж. А. и др. Рекомендации ACCF / AHA по ведению инфаркта миокарда с подъемом сегмента ST, 2013: краткое содержание: отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации по практическим рекомендациям. Тираж. 2013; 127 (4): 529–55. pmid: 23247303
- 7. Амстердам Э.А., Венгер Н.К., Бриндис Р.Г., Кейси ДжейДЭ, Ганиатс Т.Г., Холмс Дж.Д.Р. и др. Руководство AHA / ACC от 2014 г. по ведению пациентов с острыми коронарными синдромами без подъема сегмента ST: отчет Целевой группы Американского колледжа кардиологов / Американской кардиологической ассоциации по практическим рекомендациям.J Am Coll Cardiol. 2014; 64 (24): e139 – e228. pmid: 25260718
- 8.
Коулман Э.А., Уильямс М.В. Выполнение качественных переходов по уходу: призыв делать все правильно. J Hosp Med. 2007. 2 (5): 287–90. pmid: 17
2
- 9. Полевой Т.С., Огарек Дж., Гарбер Л., Рид Дж., Гурвиц Дж. Х. Связь раннего наблюдения после выписки врачом первичной медико-санитарной помощи и 30-дневной повторной госпитализации пожилых людей. J Gen Intern Med. 2015; 30 (5): 565–71. pmid: 25451987
- 10. Krumholz HM.Постбольничный синдром — приобретенное преходящее состояние генерализованного риска. N Engl J Med. 2013. 368 (2): 100–2. pmid: 23301730
- 11. Леендертсе А.Дж., Эгбертс А.С., Стокер Л.Дж., Ван ден Бемт П.М., Группа HS. Частота и факторы риска госпитализаций в связи с предотвратимыми приемами лекарств в Нидерландах. Arch Intern Med. 2008. 168 (17): 1890–6. pmid: 18809816
- 12. Ryan J, Kang S, Dolacky S, Ingrassia J, Ganeshan R. Изменение количества повторных госпитализаций и последующих посещений в рамках инициативы по повышению качества повторной госпитализации при сердечной недостаточности.Am J Med. 2013; 126 (11): 989–94 e1. pmid: 24054174
- 13. Центры услуг Medicare и Medicaid. Программа сокращения реадмиссии 2012 [15 августа 2014 г.]. http://www.cms.gov/Medicare/Medicare-Fee-for-Service-Payment/AcuteInpatientPPS/Readmissions-Reduction-Program.html.
- 14. Glickman SW, Shofer FS, Wu MC, Scholer MJ, Ndubuizu A, Peterson ED, et al. Разработка и проверка правила приоритезации для немедленного получения электрокардиограммы в 12 отведениях в отделении неотложной помощи для выявления инфаркта миокарда с подъемом сегмента ST.Am Heart J. 2012; 163 (3): 372–82. Epub 2012/03/20. pmid: 22424007
- 15. Андерссон С., Шилан Д., Го А.С., Чанг Т.И., Кази Д., Соломон М.Д. и др. бета-адреноблокаторы и сердечные приступы у пациентов с впервые диагностированной ишемической болезнью сердца. J Am Coll Cardiol. 2014; 64 (3): 247–52. Epub 2014/07/19. pmid: 25034059
- 16. Тунг Ю.К., Чанг Г.М., Чиен К.Л., Ту Ю.К. Взаимосвязь между врачом и объемом больницы, процессами и результатами лечения острого инфаркта миокарда.Med Care. 2014. 52 (6): 519–27. pmid: 24783991
- 17. Ezekowitz JA, van Walraven C, McAlister FA, Armstrong PW, Kaul P. Влияние специализированного наблюдения за амбулаторными пациентами с застойной сердечной недостаточностью. CMAJ. 2005. 172 (2): 189–94. pmid: 15655239
- 18. Юнг Д.Ф., Бум Н.К., Го Х., Ли Д.С., Шульц С.Е., Ту СП. Тенденции заболеваемости и исходов сердечной недостаточности в Онтарио, Канада: с 1997 по 2007 год. CMAJ. 2012; 184 (14): E765–73. pmid: 223
- 19. Макалистер Ф.А., Янгсон Э., Бакал Дж. А., Каул П., Эзековиц Дж., Ван Вальравен К.Влияние преемственности врача на смерть или неотложную повторную госпитализацию после выписки у пациентов с сердечной недостаточностью. CMAJ. 2013; 185 (14): E681–9. pmid: 23959284
- 20. Chiu HY, Cheng SH, Tung YC. Связь преемственности и уровня с результатами и расходами после выписки пациентов с сердечной недостаточностью. Тайвань. Общественное здравоохранение. 2016; 35 (1): 66–79.
- 21. Krumholz HM, Lin Z, Keenan PS, Chen J, Ross JS, Drye EE, et al. Связь между повторной госпитализацией и уровнем смертности пациентов, госпитализированных с острым инфарктом миокарда, сердечной недостаточностью или пневмонией.ДЖАМА. 2013. 309 (6): 587–93. pmid: 23403683
- 22. Американский колледж кардиологии. От больницы к дому (h3H): Американский колледж кардиологии; 2007 [8 июля 2015 г.]. http://h3hquality.org/.
- 23. ван Валравен С., Мамдани М., Фанг Дж., Остин П.С. Непрерывность лечения и результаты пациента после выписки из больницы. J Gen Intern Med. 2004. 19 (6): 624–31. Epub 2004/06/24. pmid: 15209600
- 24. Krumholz HM, Merrill AR, Schone EM, Schreiner GC, Chen J, Bradley EH, et al.Особенности работы больницы при остром инфаркте миокарда и сердечной недостаточности. 30-дневная смертность и повторная госпитализация. Результаты Circ Cardiovasc Qual. 2009. 2 (5): 407–13. Epub 2009/12/25. pmid: 20031870
- 25. Тунг Ю.К., Чанг Г.М., Чен Ю.Х. Связь количества врачей и посещений в выходные дни с исходом ишемического инсульта на Тайване: общенациональное популяционное исследование. Med Care. 2009. 47 (9): 1018–25. pmid: 19648828
- 26.
Тунг Ю.К., Чанг Г.М., Ченг Ш. Долгосрочное влияние сокращения возмещения на основе платы за услуги на процессы и результаты оказания помощи при инсульте: исследование прерванных временных рядов, Тайвань.Результаты Circ Cardiovasc Qual. 2015; 8 (1): 30–7. pmid: 254
- 27. Дейо Р.А., Черкин Д.С., Чиол М.А. Адаптация индекса клинической коморбидности для использования с административными базами данных МКБ-9-CM. J Clin Epidemiol. 1992. 45 (6): 613–9. pmid: 1607900
- 28. Чарнецкий А., Чонг А., Ли Д.С., Шулл М.Дж., Ту СП, Лау С. и др. Связь между наблюдением врача и результатами лечения после оценки боли в груди у пациентов из группы высокого риска. Тираж. 2013; 127 (13): 1386–94. pmid: 23547178
- 29.Лю CY, Hung YT, Chuang YL, Chen YJ, Weng WS, Liu JS и др. Стратификационное исследование урбанизации Тайваня. Журнал управления здоровьем. 2006; 4 (1): 1–22.
- 30. Lin YH, Chen YC, Tseng YH, Lin MH, Hwang SJ, Chen TJ и др. Тенденция неравенства между городом и деревней в использовании хосписов на Тайване. PLoS One. 2013; 8 (4): e62492. Epub 2013/05/10. pmid: 23658633
- 31. Чанг HY, Bodycombe DP, Huang WF, Weiner JP. Распределение ресурсов с поправкой на риски: на примере Тайваньского государственного медицинского страхования.Азия Пак Дж. Общественное здравоохранение. 2015; 27 (2): Np958–71. Epub 2013/01/25. pmid: 23343643
- 32. Ю ТХ, Хоу Ю.С., Тунг Ю.К., Чунг КП. Почему результаты лечения АКШ различаются в городских и сельских районах Тайваня? Взгляд с точки зрения качества обслуживания. Int J Qual Health Care. 2015; 27 (5): 361–8. Epub 2015/08/05. pmid: 26239475
- 33. Институт медицины. Вознаграждение поставщика услуг: согласование стимулов в программе Medicare. Вашингтон, округ Колумбия: Национальная академия прессы; 2007.
- 34.Консультативная комиссия по оплате Medicare. Содействие повышению эффективности Medicare, отчет для Конгресса Нью-Джерси (NW): MEDPAC; 2007 [цитируется 17 июля 2013 года]. http://www.medpac.gov/documents/Jun07_EntireReport.pdf.
- 35. Чжан Ю., Каплан К.М., Байк С.Х., Чанг С.К., Лаве-младший. Приверженность к лечению и повторная госпитализация после инфаркта миокарда в популяции Medicare. Am J Manag Care. 2014; 20 (11): e498–505. pmid: 25651604
- 36. Чарнецкий А., Ван Дж. Т., Ту СП, Ли Д. С., Шулл М. Дж., Лау С. и др.Роль врача первичной медико-санитарной помощи и последующего наблюдения кардиолога за пациентами из группы низкого риска с болью в груди после оценки отделения неотложной помощи. Am Heart J. 2014; 168 (3): 289–95. pmid: 25173539
- 37. Hirano K, Imbens GW, Ridder G. Эффективная оценка средних эффектов лечения с использованием оценочной оценки предрасположенности. Econometrica. 2003. 71 (4): 1161–89.
- 38. Хуанг И.К., Франгакис С., Доминичи Ф., Дитте, Великобритания, Ву А.В. Применение метода оценки предрасположенности для корректировки риска при составлении профилей нескольких групп врачей, оказывающих помощь при астме.Health Serv Res. 2005. 40 (1): 253–78. pmid: 15663712
- 39. Ян Г., Стемковски С., Сондерс В. Б.. Обзор применения оценки предрасположенности к результатам здравоохранения и эпидемиологии Denver 2007 [18 февраля 2015 г.]. http://www.lexjansen.com/pharmasug/2007/pr/pr02.pdf.
- 40. Chang HY, Zhou M, Tang W, Alexander GC, Singh S. Риск желудочно-кишечного кровотечения, связанный с пероральными антикоагулянтами: популяционное ретроспективное когортное исследование. Bmj. 2015; 350: h2585. pmid: 25
6 - 41.Шварц С. Ошибка экологической ошибки: возможное неправильное использование концепции и последствия. Am J Public Health. 1994. 84 (5): 819–24. pmid: 8179055
- 42. Сассер М. Логика в экологическом: I. Логика анализа. Am J Public Health. 1994. 84 (5): 825–9. pmid: 8179056
- 43. Diez Roux AV. Изучение факторов на уровне группы в эпидемиологии: переосмысление переменных, дизайн исследований и аналитические подходы. Epidemiol Rev.2004; 26 (1): 104–11.
- 44. Geronimus AT, Bound J, Neidert LJ. О правомерности использования геокодированных характеристик переписи для проксимации индивидуальных социально-экономических характеристик. J Am Stat Assoc. 1996. 91 (434): 529–37.
- 45. Ли К.К., Ян Дж., Эрнандес А.Ф., Штаймле А.Е., Go AS. Характеристики последующего наблюдения после выписки, связанные с 30-дневной повторной госпитализацией после сердечной недостаточности. Med Care.
