Болезнь паркинсона 3 стадия по хен яру: Болезнь Паркинсона – причины возникновения, признаки и симптомы, лечение болезни Паркинсона
Глубокая стимуляция мозга при болезни Паркинсона
- Главная
- Услуги
- Методы лечения
- Глубокая стимуляция мозга при болезни Паркинсона
Методы лечения
Глубокая стимуляция мозга или DBS — это хирургический метод лечения некоторых заболеваний, сопровождающихся расстройством движений. В ее основе высокочастотная стимуляция глубинных структур головного мозга посредством имплантированных электродов.
Глубокая стимуляция головного мозга применяется уже более 40 лет во всем мире и считается высокоэффективным методом лечения развернутых и поздних стадий болезни Паркинсона.
Метод также так же успешно применяется в лечении генерализованной и сегментарной форм дистонии, эссенциальном треморе при неэффективности консервативных методах терапии, в т.ч. ботулинотерапии.
Когда стоит задуматься об операции?
К сожалению, болезнь Паркинсона является хроническим заболеванием, которое со временем прогрессирует.
ОСНОВНЫЕ ПОКАЗАНИЯ К ОПЕРАЦИИ:
— наличие инвалидизирующего тремора, резистентного к медикаментозному лечению;
— наличие инвалидизирующих лекарственных дискинезий, не поддающихся медикаментозной коррекции;
— наличие инвалидизирующих моторных флуктуаций, не поддающихся медикаментозной коррекции;
КРИТЕРИИ ОТБОРА НА ОПЕРАЦИЮ:
1. Истинная болезнь Паркинсона при длительности заболевания не менее 5 лет
 и выше по Хен-Яру)
и выше по Хен-Яру)3. Снижение качества жизни вследствие гипокинетических флуктуаций и/или медикаментозных дискинезийпри невозможности адекватного медикаментозного контроля
4. Возраст до 70 лет (относительное ограничение, возможно и в более позднем взрасте)
5. Высокая эффективность терапии леводопой (снижение тяжести двигательных нарушений на фоне приема тестовой дозы леводопы не менее чем на 50% по III части шкалы UPDRS)
6. Двигательная активность на фоне действия леводопы (ON-состояние) по шкале Schwab and England 70% и выше
Чего ожидать от операции?
При соблюдении критериев отбора пациентов и технически правильной выполненной операции все пациенты испытывают облегчение симптомов заболевания сразу после операции (даже до включения нейростимулятора).
ОСНОВНЫЕ ЭФФЕКТЫ DBS:
— уменьшение количества применяемых препаратов;
— снижение выраженности ригидности, тремора, гипокинезии;
— устранение тяжелых эпизодов «включения», «выключения»;
— уменьшение застываний в выключенном состоянии;
— уменьшение выраженности лекарственных дискинезий.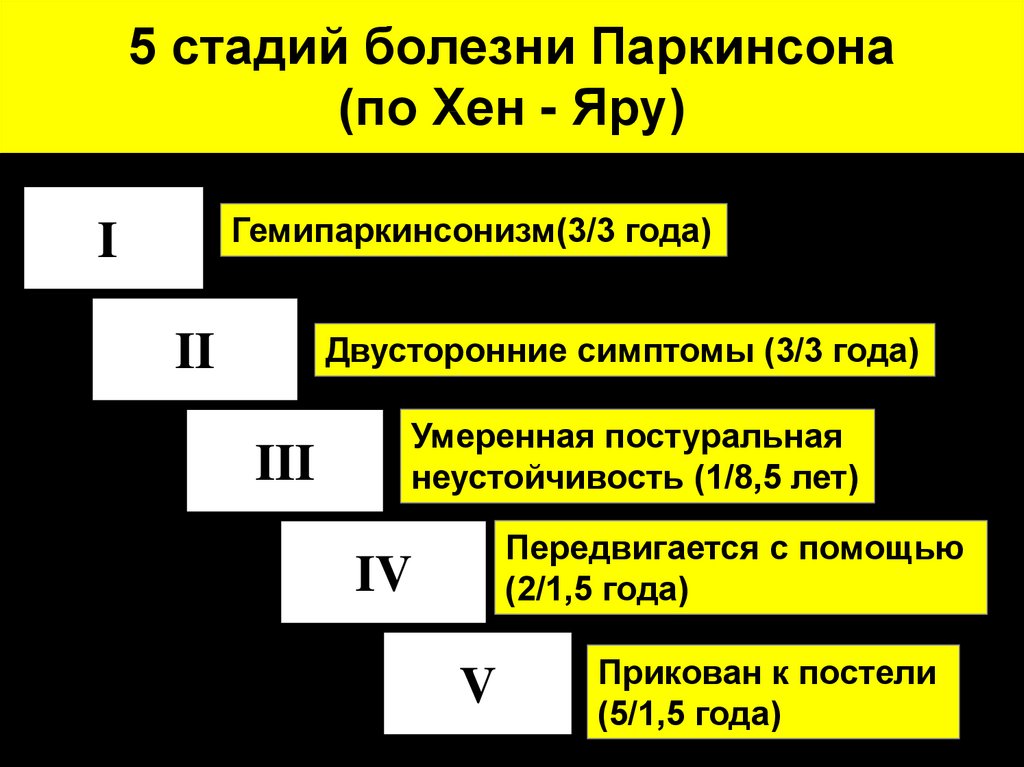
Недавно опубликованы исследования, в которых сообщается положительное влияние операции на настроение и поведение пациентов после операции.
Около 30-40% пациентов испытывают завышенные ожидания относительного возможностей оперативного лечения. К сожалению, операция не вылечивает заболевание, которое со временем прогрессирует. Но способна значимо улучшить качество жизни, в первую очередь двигательную функцию.
DBS никак не влияет на нарушение речи, памяти, поддержании равновесия и некоторые другие симптомы.
Операция является дорогостоящей и достаточно сложной в техническом выполнении. В России глубокая стимуляция мозга при болезни Паркинсона выполняется в ведущих нейрохирургических центрах страны (Москва, Санкт-Петербург, Новосибирск, Тюмень) высококвалифицированными нейрохирургами.
Имплантируются системы стимуляции Американского производства, которые используются в Израиле, США и странах Европы. Гражданам Российской Федерации операции доступны по квотам высокотехнологичной медицинской помощи (ВМП) и на платной основе.
На базе нашей Smart Clinic проводится отбор пациентов на глубокую стимуляцию мозга (DBS) в соответствии с международными критериями, осуществляется вся необходимая предоперационная подготовка и оформление документов. После выполнения операции пациенты наблюдаются в нашей клиники, где им проводится подбор параметров стимуляции и коррекция лекарственной терапии.
Статья подготовлена врачом неврологом-паркинсонологом Смирновым П.В.
Записаться на Глубокая стимуляция мозга при болезни Паркинсона
Ваше имя: *
Ваш телефон: *
Болезнь Паркинсона
БОЛЕЗНЬ ПАРКИНСОНА — нейродегенеративное заболевание, характеризующееся прогрессирующей утратой дофаминергических нейронов, что клинически проявляется в утере контроля над произвольными движениями.
Эпидемиология
Болезнь Паркинсона (далее — БП) является одной из наиболее распространенных форм расстройств движений человека и одной из самых частых патологий среди первичных хронических нейродегенеративных заболеваний. Распространенность БП в общей популяции составляет до 140 случаев на 100 000 населения. Около 5-7% случаев имеют прямую наследственную основу. Семейный характер заболевания по данным разных авторов и проспективных исследований встречается у 15%-23% больных. Спорадическая БП ассоциируется: с возможными генетическими мутациями, экзогенными факторами риска (воздействие пестицидов — чаще развивается у сельских жителей, прием нейролептиков и др.). Риск развития заболевания повышается с возрастом. Возраст, в котором, как правило, начинается заболевание — старше 50 лет.
1. Двигательные нарушения: брадикинезия, мышечная ригидность, тремор покоя, нарушение походки и снижение постуральных рефлексов.

2. Вегетативные симптомы (дисфункция кишечника и желчевыводящих путей, мочевого пузыря, сексуальная дисфункция, ортостатическая гипотензия).
3. Сенсорные расстройства.
4. Когнитивные симптомы (деменция).
5.Нейропсихические симптомы (депрессия).
Постуральная неустойчивость и связанные с ней падения остаются наименее изученными элементами симптомокомплекса БП. Постуральные нарушения присоединяются к другим симптомам БП на развернутых стадиях болезни и являются одними из наиболее инвалидизирующих клинических синдромов БП, приводят к выраженным ограничениям повседневной активности больных.
Патогенез
- прогрессирующая дегенерация специфических дофаминергических систем головного мозга,
- нарушение взаимодействия между неспецифическими системами головного мозга отвечающих за двигательную активность и организацию движений,
- функциональные нарушения на уровне сегментарного аппарата спинного мозга, альфа-гамма дисбаланс, нарушение взаимоотношений между мышцами агонистами и антагонистами.

Клинические формы болезни
Форма синдрома паркинсонизма определяется в зависимости от преобладания в клинических проявлениях болезни одного из компонентов классической триады симптомов — дрожания, ригидности или гипокинезии. Выделяют дрожательные, ригидные, смешанные и акинетические клинические формы паркинсонизма.
Стадии болезни Паркинсона по шкале Хена и Яра
Стадия 0.0 — нет признаков паркинсонизма
Стадия 1.0 — унилатеральный тремор, ригидность, брадикинезия
Стадия 1.5 — односторонние проявления с вовлечение аксиальной мускулатуры
Стадия 2.0 — билатеральный тремор, ригидность, акинезия без нарушения функции равновесия
Стадия 2.5 мягкие двухсторонние проявления. Сохранена способность преодалевать вызванную ретропульсию
Стадия 3.0 — умеренные или средней тяжести двухсторонние проявления. Небольшая постуральная неустойчивость. Больной не нуждается в посторонней помощи
Стадия 4.
 0 — тяжелая обездвиженность. Однако больной еще может ходить или стоять без поддержки
0 — тяжелая обездвиженность. Однако больной еще может ходить или стоять без поддержкиСтадия 5.0 — без посторонней помощи больной прикован к постели
Лечение болезни Паркисона
— медикаментозная терапия
— хирургическое лечение
— физические методы лечения
— психотерапия
Считается, что наиболее эффективна комплексная терапия БП, основанная на принципах этиопатогенетического и симптоматического лечения, которая должна учитывать полисистемный характер его проявлений. К дополнительным методам лечения при БП относят физические методы лечения, которым отводят важную роль в сохранении двигательной активности больных, поддержании подвижности в суставах, предотвращении нарушений позы и ходьбы, предотвращении инвалидизации.
Медикаментозная терапия — применение лекарственных препаратов, компенсирующих недостаток дофамина в организме и ослабляющих клинические проявления болезни.
Другие материалы в этой категории: « Продукты в жару Вакцинация — За или против? За! »
Церебральная амилоидная нагрузка и оценка стадии 3 по Хену и Яру при болезни Паркинсона
1.
2. Evans JR, Mason SL, Williams-Gray CH, Foltynie T, Brayne C, Robbins TW, Barker RA. Естественная история лечения болезни Паркинсона в когорте инцидентов, основанной на сообществе. J Neurol Нейрохирург Психиатрия. 2011;82:1112–1118. [PubMed] [Google Scholar]
3. Goetz CG, Stebbins GT, Blasucci LM. Дифференциальное прогрессирование двигательных нарушений при лечении леводопой болезни Паркинсона. Мов Беспорядок. 2000;15:479–484. [PubMed] [Google Scholar]
4. Roos RA, Jongen JC, van der Velde EA. Клиническое течение больных идиопатической болезнью Паркинсона. Мов Беспорядок. 1996; 11: 236–242. [PubMed] [Google Scholar]
5. де ла Фуэнте-Фернандес Р., Шульцер М., Курамото Л., Крэгг Дж., Рамачандиран Н., Ау В.Л., Мак Э., Маккензи Дж., Маккормик С., Сосси В., Рут Т.Дж., Ли К.С. , Калн Д.Б., Штёссл А.Дж. Возрастное прогрессирование нигростриарной дисфункции при болезни Паркинсона. Энн Нейрол. 2011;69:803–810. [PubMed] [Академия Google]
Энн Нейрол. 2011;69:803–810. [PubMed] [Академия Google]
6. Staffen W, Mair A, Unterrainer J, Trinka E, Ladurner G. Измерение прогрессирования идиопатической болезни Паркинсона с помощью [123I] бета-CIT SPECT. J Neural Transm (Вена) 2000; 107: 543–552. [PubMed] [Google Scholar]
7. Maetzler W, Reimold M, Liepelt I, Solbach C, Leyhe T, Schweitzer K, Eschweiler GW, Mittelbronn M, Gaenslen A, Uebele M, Reischl G, Gasser T, Machulla HJ, Барс Р., Берг Д. Связывание [11C]PIB при деменции при болезни Паркинсона. Нейроизображение. 2008; 39: 1027–1033. [PubMed] [Академия Google]
8. Muller ML, Frey KA, Petrou M, Kotagal V, Koeppe RA, Albin RL, Bohnen NI. бета-амилоид и постуральная нестабильность и затруднение походки при болезни Паркинсона с риском деменции. Мов Беспорядок. 2013; 28: 296–301. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Петру М., Двамена Б.А., Фёрстер Б.Р., Макихерн М.П., Бонен Н.И., Мюллер М.Л., Альбин Р.Л., Фрей К.А. Отложение амилоида при болезни Паркинсона и когнитивных нарушениях: систематический обзор. Мов Беспорядок. 2015;30:928–935. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Мов Беспорядок. 2015;30:928–935. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Лю Э., Шмидт М.Е., Марголин Р., Сперлинг Р., Кеппе Р., Мейсон Н.С., Кланк В.Е., Матис К.А., Саллоуэй С., Фокс Н.С., Хилл Д.Л., Лес А.С., Коллинз П., Грегг К.М., Ди Дж., Лу Y, Tudor IC, Wyman BT, Booth K, Broome S, Yuen E, Grundman M, Brashear HR. Амилоид-бета 11C-PiB-ПЭТ — результат 2 рандомизированных исследований 3 фазы бапинеузумаба при БА. Неврология. 2015; 85: 692–700. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Шах Н., Фрей К.А., Мюллер М.Л., Петру М., Котагал В., Кеппе Р.А., Скотт П.Дж., Альбин Р.Л., Бонен Н.И. Полосатая и корковая бета-амилоидопатия и познание при болезни Паркинсона. Мов Беспорядок. 2016; 31:111–117. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Хьюз А.Дж., Дэниел С.Е., Килфорд Л., Лис А.Дж. Точность клинической диагностики идиопатической болезни Паркинсона: клинико-патологическое исследование 100 случаев. J Neurol Нейрохирург Психиатрия. 1992; 55: 181–184. [Бесплатная статья PMC] [PubMed] [Google Scholar]
1992; 55: 181–184. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Goetz CG, Fahn S, Martinez-Martin P, Poewe W, Sampaio C, Stebbins GT, Stern MB, Tilley BC, Dodel R, Dubois B, Holloway R , Jankovic J, Kulisevsky J, Lang AE, Lees A, Leurgans S, LeWitt PA, Nyenhuis D, Olanow CW, Rascol O, Schrag A, Teresi JA, Van Hilten JJ, LaPelle N. Пересмотр Объединенного Шкала оценки болезни Паркинсона (MDS-UPDRS): план процесса, формата и клиниметрического тестирования. Мов Беспорядок. 2007; 22:41–47. [PubMed] [Академия Google]
14. Goetz CG, Poewe W, Rascol O, Sampaio C, Stebbins GT, Counsell C, Giladi N, Holloway RG, Moore CG, Wenning GK, Yahr MD, Seidl L. Отчет Целевой группы Общества двигательных расстройств о Hoehn и Промежуточная шкала Yahr: состояние и рекомендации. Мов Беспорядок. 2004;19:1020–1028. [PubMed] [Google Scholar]
15. Hoehn MM, Yahr MD. Паркинсонизм: начало, прогрессирование и смертность. Неврология. 1967; 17: 427–442. [PubMed] [Google Scholar]
16. Williams-Gray CH, Mason SL, Evans JR, Foltynie T, Brayne C, Robbins TW, Barker RA. Исследование болезни Паркинсона CampPaIGN: 10-летний прогноз в когорте заболевших. J Neurol Нейрохирург Психиатрия. 2013; 84: 1258–1264. [PubMed] [Академия Google]
Williams-Gray CH, Mason SL, Evans JR, Foltynie T, Brayne C, Robbins TW, Barker RA. Исследование болезни Паркинсона CampPaIGN: 10-летний прогноз в когорте заболевших. J Neurol Нейрохирург Психиатрия. 2013; 84: 1258–1264. [PubMed] [Академия Google]
17. Малек Н., Лоутон М.А., Ласточка Д.М., Гроссет К.А., Марринан С.Л., Баджадж Н., Баркер Р.А., Берн Д.Дж., Харди Дж., Моррис Х.Р., Уильямс Н.М., Вуд Н., Бен-Шломо Ю., Гроссет Д.Г. Сосудистое заболевание и сосудистые факторы риска в отношении двигательных функций и когнитивных функций при ранней болезни Паркинсона. Mov Disord 2016 [бесплатная статья PMC] [PubMed] [Google Scholar]
18. Reed BR, Marchant NL, Jagust WJ, DeCarli CC, Mack W, Chui HC. Коронарный риск коррелирует с церебральным отложением амилоида. Нейробиол Старение. 2012;33:1979–1987. [PMC free article] [PubMed] [Google Scholar]
19. Virmani T, Moskowitz CB, Vonsattel JP, Fahn S. Клинико-патологические характеристики замирания походки при вскрытии подтвержденной болезни Паркинсона.

