Симптом белоглазова время появления: Признак Белоглазова
снижение температуры тела, симптом Белоглазова (кошачий глаз), трупные пятна :: BusinessMan.ru
Смерть — явление, однажды настигающее каждого человека. В медицине ее описывают как необратимую потерю функций дыхательной, сердечно-сосудистой и центральной нервной системы. Различные признаки указывают на момент ее наступления.
Проявления данного состояния могут быть изучены по нескольким направлениям:
- признаки биологической смерти — ранние и поздние;
- непосредственные симптомы.
Что такое смерть?
Гипотезы о том, что представляет собой смерть, различны в разных культурах и исторических периодах.
В условиях современности она констатируется, когда имеет место остановка сердца, дыхания и кровообращения.
Соображения общества относительно гибели человека представляют не только теоретический интерес. Прогресс в медицине позволяет быстро и правильно установить причину этого процесса и предотвратить его, если возможно.
В настоящее время существует ряд вопросов, обсуждаемых врачами и исследователями касательно смерти:
- Можно ли отключить человека от аппарата искусственного поддержания жизнедеятельности без согласия родственников?
- Может ли человек умереть по собственной воле, если лично просит не принимать никаких мер, направленных на сохранность его жизни?
- Могут ли родственники или законные представители принимать решения касательно смерти, если человек без сознания, а лечение не помогает?
Люди верят, что смерть — это уничтожение сознания, а за ее порогом душа умершего переходит в иной мир.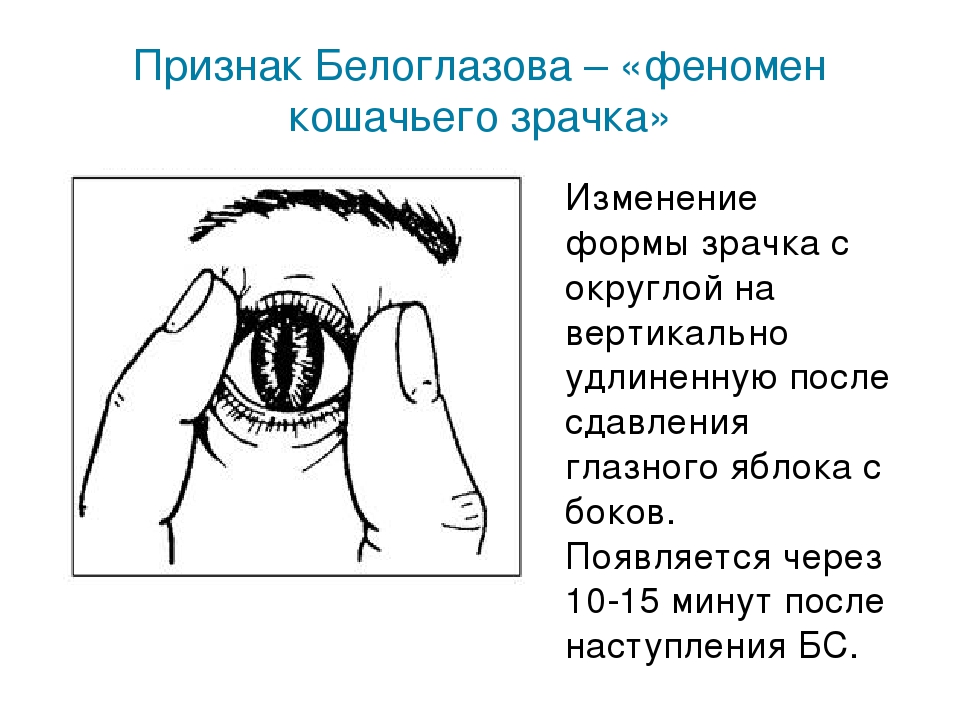 Но то, что происходит на самом деле, по сей день является загадкой для общества. Поэтому сегодня, как уже говорилось, остановимся на следующих вопросах:
Но то, что происходит на самом деле, по сей день является загадкой для общества. Поэтому сегодня, как уже говорилось, остановимся на следующих вопросах:
- признаки биологической смерти: ранние и поздние;
- психологические аспекты;
- причины.
Когда сердечно-сосудистая система перестает действовать, нарушая транспортировку крови, то прекращает функционировать мозг, сердце, печень, почки и остальные органы. Это не происходит одновременно.
Мозг является первым органом, который теряет свои функции из-за отсутствия кровоснабжения. Через несколько секунд после того, как подача кислорода прекращается, человек теряет сознание. Далее заканчивает свою деятельность механизм обмена веществ. После 10 минут кислородного голодания клетки мозга погибают.
Выживание различных органов и клеток, исчисляемое в минутах:
- Мозг: 8–10.
- Сердце: 15–30.
- Печень: 30–35.
- Мышцы: от 2 до 8 часов.
- Сперма: от 10 до 83 часов.

Статистические данные и причины
Основным фактором гибели человека в развивающихся странах являются инфекционные заболевания, в развитых — атеросклероз (болезнь сердца, инфаркт и инсульт), раковые патологии и другие.
Из 150 тыс. людей, умирающих по всему миру, примерно ⅔ погибают от старения. В развитых странах эта доля гораздо выше и составляет 90 %.
Причины биологической смерти:
- Курение. В 1910 году от него умерло более 100 миллионов человек.
- В развивающихся странах плохие санитарные условия и отсутствие доступа к современным медицинским технологиям повышают процент смертности от инфекционных заболеваний. Чаще всего люди умирают от туберкулеза, малярии, СПИДа.
- Эволюционная причина старения.
- Самоубийство.
- Автокатастрофа.
Как видите, причины смерти могут быть различными. И это далеко не весь перечень причин того, из-за чего умирают люди.
В странах с высоким уровнем дохода большинство населения доживает до 70-летнего возраста, преимущественно умирая из-за хронических заболеваний.
Признаки биологической смерти (ранние и поздние) проявляются после наступления клинической смерти. Они наступают сразу же после момента прекращения мозговой активности.
Симптомы-предвестники
Непосредственные признаки, указывающие на смерть:
- Нечувствительность (потеря движений и рефлексов).
- Потеря ритма ЭЭГ.
- Остановка дыхания.
- Остановка сердца.
Но такие признаки, как потеря чувствительности, движений, остановка дыхания, отсутствие пульса и т. д. могут появиться из-за обморока, торможения блуждающего нерва, эпилепсии, наркоза, электрошока. Другими словами, они могут означать смерть лишь тогда, когда связаны с полной потерей ритма ЭЭГ в течение длительного периода времени (более 5 минут).
Большинство людей часто задают себе сакраментальный вопрос: «Как это произойдет и почувствую ли я приближение смерти?». Сегодня на этот вопрос однозначного ответа не существуют, поскольку у каждого симптомы различны, в зависимости от имеющегося заболевания.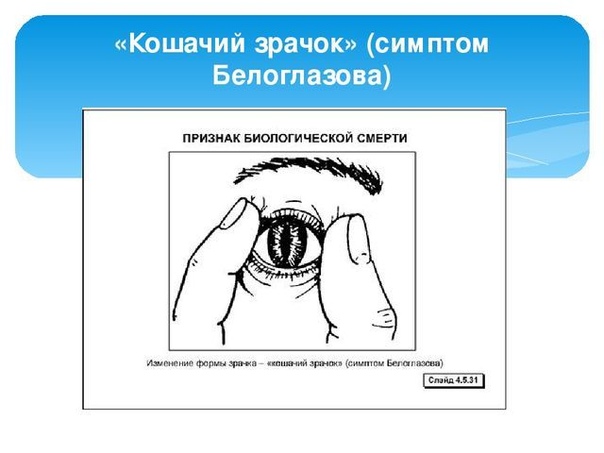
Симптомы, проявляющиеся при приближении смерти:
- белый кончик носа;
- холодный пот;
- бледные руки;
- неприятный запах изо рта;
- прерывистое дыхание;
- нерегулярный пульс;
- снижение температуры тела;
- сонливость.
Общие сведения о начальных симптомах
Точную грань между жизнью и смертью трудно определить. Чем дальше от рубежа, тем яснее разница между ними. То есть чем ближе смерть, тем визуально заметнее она будет.
Ранние признаки обозначают молекулярную или клеточную смерть, они длятся на протяжении 12–24 часов.
Физические изменения характеризуются следующими ранними симптомами:
- Высыхание роговицы глаз.
- Когда наступает биологическая смерть, то обменные процессы прекращаются. Следовательно, все тепло, находящееся в теле человека, выходит в окружающую среду, и наступает охлаждение трупа.
 Медицинские работники утверждают, что время остывания зависит от температуры в помещении, где находится тело.
Медицинские работники утверждают, что время остывания зависит от температуры в помещении, где находится тело. - Синюшность кожных покровов начинается в течение 30 минут. Она появляется из-за недостаточного насыщения крови кислородом.
- Трупные пятна. Их локализация зависит от положения человека и от заболевания, которым он был болен. Они возникают из-за перераспределения крови в организме. Проявляются в среднем спустя 30 минут.
- Трупное окоченение. Оно начинается примерно через два часа после смерти, идет от верхних конечностей, медленно перемещаясь на нижние. Полностью выраженное трупное окоченение достигается во временном промежутке от 6 до 8 часов.
Сужение зрачка — один из первоначальных симптомов
Симптом Белоглазова — один из самых первых и достоверных проявлений у умершего человека. Именно благодаря этому признаку можно без лишних обследований определить биологическую смерть.
Почему его еще называют кошачий глаз? Потому что в результате сдавливания глазного яблока, зрачок из круглого превращается в овальный, как у кошек.
Этот признак является очень достоверным и появляется из-за любых причин, итогом которых оказалась смерть. У здорового человека присутствие такого явления невозможно. Симптом Белоглазова появляется по причине прекращения кровообращения и внутриглазного давления, а также из-за дисфункции мышечных волокон вследствие смерти.
Поздние проявления
Поздние признаки представляют собой разложение тканей, или гниение тела. Оно ознаменовано появлением зеленовато-обесцвеченного окраса кожных покровов, которые появляются спустя 12-24 часа после смерти.
Другие проявления поздних признаков:
- Мраморность — это сеть отметин на коже, наступающая после 12 часов, которая становится заметной по прошествии от 36 до 48 часов.
- Черви – начинают появляться в результате гнилостных процессов.
- Так называемые трупные пятна становятся видны примерно через 2–3 часа после остановки сердца.
 Они возникают, потому что кровь обездвижена, и поэтому собирается под действием силы тяжести в определенных точках тела. Образование таких пятен может характеризовать признаки биологической смерти (ранние и поздние).
Они возникают, потому что кровь обездвижена, и поэтому собирается под действием силы тяжести в определенных точках тела. Образование таких пятен может характеризовать признаки биологической смерти (ранние и поздние). - Мышцы расслаблены на первых порах, процесс затвердения мышц занимает от трех до четырех часов.
Когда именно будет достигнута стадия биологической смерти, на практике определить невозможно.
Основные стадии
Существует три стадии, через которые проходит человек в процессе умирания.
Общество по паллиативной медицине делит заключительные этапы смерти следующим образом:
- Предагональная фаза. Несмотря на прогрессирование болезни, пациенту необходима независимость и самостоятельная жизнь, но он не может себе этого позволить из-за того, что находится между жизнью и смертью. Ему необходим хороший уход. Эта фаза относится к последним нескольким месяцам. Именно в этот момент больной чувствует некоторое облегчение.
- Терминальная фаза.
 Ограничения, вызванные болезнью, не остановить, симптомы накапливаются, пациент становится слабее, и его активность снижается. Данный этап может наступить за несколько недель до смерти.
Ограничения, вызванные болезнью, не остановить, симптомы накапливаются, пациент становится слабее, и его активность снижается. Данный этап может наступить за несколько недель до смерти. - Завершающая фаза описывает процесс умирания. Она протекает короткий промежуток времени (человек либо слишком хорошо себя чувствует, либо очень плохо). Спустя несколько дней больной умирает.
Процесс терминальной фазы
Она различна для каждого человека. У многих умерших незадолго до смерти определяются физические изменения и признаки, которые говорят о ее приближении. У других эти симптомы могут отсутствовать.
Многие умирающие люди хотят съесть что-нибудь вкусное в последние несколько дней. У других, наоборот, плохой аппетит. И то и другое является нормальным явлением. Но необходимо знать, что потребление калорий и жидкости усложняет процесс умирания. Считается, что организм менее чувствительно реагирует на изменения, если никакие питательные вещества некоторое время не поставляются.
Очень важно следить за слизистой оболочкой рта, обеспечить хороший и регулярный уход, чтобы не было сухости. Поэтому умирающему нужно давать понемногу пить воду, но часто. В противном случае могут возникнуть такие проблемы, как воспаление, затруднения при глотании, боли и грибковые инфекции.
Многие умирающие незадолго до смерти становятся беспокойными. Другие – никак не воспринимают наступающую смерть, поскольку понимают, что уже ничего не исправить. Часто люди находятся в полусонном состоянии, взгляд тускнеет.
Возможна частая остановка дыхания, либо оно может быть быстрым. Иногда дыхание очень неравномерно, постоянно меняется.
И наконец, изменения кровотока: пульс слабый или быстрый, температура тела падает, руки и ноги холодеют. Незадолго до наступления смерти сердце бьется слабо, дыхание затрудненное, активность мозга снижается. Через несколько минут после угасания работы сердечно-сосудистой системы мозг перестает функционировать, наступает биологическая смерть.
Как проводится осмотр умирающего?
Осмотр должен проводиться быстро, чтобы, в случае если человек жив, успеть направить пациента в больницу и провести соответствующие мероприятия. Вначале необходимо прощупать пульс на руке. Если он не прощупывается, то можно попробовать почувствовать пульс на сонной артерии, слегка на нее нажав. Затем при помощи стетоскопа прослушать дыхание. Опять никаких признаков жизни не обнаружилось? Тогда врачу потребуется сделать искусственное дыхание и массаж сердца.
Если после проделанных манипуляций у пациента нет пульса, значит, необходимо подтвердить факт смерти. Для этого открывают веки и двигают головой умершего в стороны. Если глазное яблоко фиксируется и движется вместе с головой, значит, наступила смерть.
По глазам можно несколькими способами наверняка определить, умер человек или нет. Например, взять клинический фонарик и проверить глаза на сужение зрачков. Когда человек умирает, зрачки становятся узкими, появляется помутнение роговицы. Она теряет глянцевый вид, но не всегда такой процесс происходит сразу. Особенно у тех пациентов, которым диагностировали сахарный диабет или имеются заболевания, связанные со зрением.
Она теряет глянцевый вид, но не всегда такой процесс происходит сразу. Особенно у тех пациентов, которым диагностировали сахарный диабет или имеются заболевания, связанные со зрением.
В случае сомнений можно сделать ЭКГ и ЭЭГ-мониторинг. ЭКГ в течение 5 минут покажет, жив человек или мертв. Отсутствие волн на ЭЭГ подтверждает смерть (асистолия).
Поставить диагноз «смерть» нелегко. В некоторых случаях возникают трудности из-за анабиоза, чрезмерного употребления седативных и снотворных средств, переохлаждения, алкогольного опьянения и др.
Психологические аспекты
Танатология — междисциплинарная область исследования, занимающаяся изучением вопросов смерти. Это относительно новая дисциплина в научном мире. В 50–60-е годы ХХ века исследования открыли путь к психологическому аспекту данной проблемы, начали разрабатываться программы для оказания помощи в преодолении глубоко эмоциональных проблем.
Ученые выделили несколько этапов, через которые проходит умирающий человек:
- Отрицание.

- Страх.
- Депрессия.
- Принятие.
По мнению большинства специалистов, эти стадии не всегда возникают в таком порядке, как указано выше. Они могут быть смешаны и дополнены чувством надежды либо ужаса. Страх —сжатие, притеснение от ощущения надвигающейся опасности. Особенность страха — интенсивный психический дискомфорт от того, что умирающий не может исправить грядущих событий. Реакцией на страх могут быть: нервное или диспепсическое расстройство, головокружение, нарушение сна, дрожь, внезапная потеря контроля над выделительными функциями.
Не только умирающий человек, но и его родственники и друзья проходят через стадии отрицания и принятия. Следующий этап — горе, наступающее после смерти. Как правило, оно переносится тяжелее, если человек не знал о состоянии родственника. В этой фазе присутствует нарушение сна и потеря аппетита. Иногда посещает чувство страха и гнева из-за того, что уже ничего не изменить. Позже грусть переходит в депрессию и одиночество. В какой-то момент боль утихает, жизненная энергия возвращается, но психологическая травма может сопровождать человека длительный период.
В какой-то момент боль утихает, жизненная энергия возвращается, но психологическая травма может сопровождать человека длительный период.
Уход человека из жизни может осуществляться на дому, но в большинстве случаев таких людей помещают в больницу в надежде оказать помощь и спасти.
Биологическая смерть
Биологическая смерть (или истинная смерть) представляет собой необратимое прекращение физиологических процессов в клетках и тканях (см. смерть). Со временем меняются возможности медицины по реанимации умерших пациентов. Поэтому признаки биологической смерти на каждом этапе развития медицины уточняются.
К ранним признакам биологической смерти относятся:

К поздним признакам биологической смерти относятся:
Биологическая смерть субъекта не означает одномоментную биологическую смерть тканей и органов, составляющих его организм. Время до смерти тканей, составляющих тело человека, в основном определяется их способностью выживать в условиях гипоксии и аноксии. У разных тканей и органов эта способность различна. Наиболее короткое время жизни в условиях аноксии наблюдается у ткани головного мозга, если более точно, у коры головного мозга и подкорковых структур. Стволовые отделы и спинной мозг имеют большую устойчивость к аноксии. Другие ткани тела человека обладают этим свойством в более выраженной степени. Так, сердце сохраняет свою жизнеспособность в течение 1,5—2 часов после наступления биологической смерти. Почки, печень и некоторые другие органы сохраняют жизнеспособность до 3—4 часов. Мышечная ткань, кожа и некоторые другие ткани вполне могут быть жизнеспособными в сроки до 5—6 часов после наступления биологической смерти. Костная ткань, являясь самой инертной тканью организма человека, сохраняет свои жизненные силы до нескольких суток. С явлением переживаемости органов и тканей тела человека связана возможность трансплантации их и чем в более ранние сроки после наступления биологической смерти изымаются органы для трансплантации, чем более жизнеспособными они являются, тем больше вероятность их успешного дальнейшего функционирования в другом организме.
Мышечная ткань, кожа и некоторые другие ткани вполне могут быть жизнеспособными в сроки до 5—6 часов после наступления биологической смерти. Костная ткань, являясь самой инертной тканью организма человека, сохраняет свои жизненные силы до нескольких суток. С явлением переживаемости органов и тканей тела человека связана возможность трансплантации их и чем в более ранние сроки после наступления биологической смерти изымаются органы для трансплантации, чем более жизнеспособными они являются, тем больше вероятность их успешного дальнейшего функционирования в другом организме.
Вторичная облитерация слезоотводящих путей после терапии радиоактивным йодом | Ярцев
Лечение заболеваний щитовидной железы при помощи радиоактивного йода стало возможным в 40-х годах XX века после получения E. Fermi изотопов йода и осуществления экспериментальных исследований, доказавших, что щитовидная железа активно захватывает йод [1]. Известно, что у первого в истории пациента, который получал лечение радиоактивным йодом по поводу дифференцированного рака щитовидной железы на протяжении 6 лет, был отмечен значительный регресс опухоли, однако по прошествии 9 лет после начала лечения пациент умер. При вскрытии был установлен анапластический рак [1, 2]. По-видимому, с этого момента проблемы, связанные с потенциальными осложнениями терапии радиоактивным йодом, стали объектом активных исследований. Несмотря на то что на сегодняшний день такая терапия проводится часто, а число осложнений невысоко, до сих пор абсолютная безопасность терапии изотопами йода не достигнута, а разработка профилактических мероприятий и способов коррекции индуцированных изменений остается актуальной задачей [3, 4].
При вскрытии был установлен анапластический рак [1, 2]. По-видимому, с этого момента проблемы, связанные с потенциальными осложнениями терапии радиоактивным йодом, стали объектом активных исследований. Несмотря на то что на сегодняшний день такая терапия проводится часто, а число осложнений невысоко, до сих пор абсолютная безопасность терапии изотопами йода не достигнута, а разработка профилактических мероприятий и способов коррекции индуцированных изменений остается актуальной задачей [3, 4].
Среди прочих известны и офтальмологические осложнения терапии радиоактивным йодом, которые требуют специального наблюдения или активного вмешательства офтальмолога.
Наиболее частым офтальмологическим осложнением такой терапии является развитие сухого кератоконъюнктивита, связанного с поражением слезных желез. Так, R. Solans и соавт. [5] показали, что это состояние формируется у четверти всех пациентов, перенесших терапию радиоактивным йодом. Сухой кератоконъюнктивит чаще всего манифестирует в ранние сроки после лечения и, как правило, является транзиторным состоянием, однако в ряде случаев выраженность его значительна, и необходимо проводить интенсивное местное лечение. Авторами также описаны случаи развития сухого кератоконъюнктивита и в более поздние сроки. C. Alexander и соавт. [6] исследовали офтальмологические осложнения в средние и поздние сроки у пациентов, получавших терапию радиоактивным йодом по поводу рака щитовидной железы, и показали, что в 23% случаев у пациентов развивался конъюнктивит; в ряде случаев пациентам было выполнено оперативное лечение, направленное на улучшение дренажной функции слезоотводящих путей.
Авторами также описаны случаи развития сухого кератоконъюнктивита и в более поздние сроки. C. Alexander и соавт. [6] исследовали офтальмологические осложнения в средние и поздние сроки у пациентов, получавших терапию радиоактивным йодом по поводу рака щитовидной железы, и показали, что в 23% случаев у пациентов развивался конъюнктивит; в ряде случаев пациентам было выполнено оперативное лечение, направленное на улучшение дренажной функции слезоотводящих путей.
Слезная жидкость, которую секретируют слезные железы, омывает глазную поверхность, собирается в медиальном углу глазной щели и при моргании через расположенные в верхнем и нижнем веке слезные точки и канальцы перемещается в носослезный проток, открывающийся в нижнем носовом ходе. Постоянная секреция слезной жидкости и ее непрерывное перемещение позволяют осуществлять ряд важных функций, среди которых — защитная и трофическая. Посредством слезной жидкости происходит питание роговицы, а защитная функция обеспечивается механическим удалением поллютантов с глазной поверхности, действием лизоцима и факторов специфической иммунной защиты [7]. При нарушении слезоотведения возникает застой слезной жидкости, что провоцирует вначале развитие слезотечения, а затем — хронического воспалительного процесса на глазной поверхности.
При нарушении слезоотведения возникает застой слезной жидкости, что провоцирует вначале развитие слезотечения, а затем — хронического воспалительного процесса на глазной поверхности.
Известно, что активный захват йода осуществляется при непосредственном действии мембранного белка-котранспортера Na+/I– (SLC5A5). Этот белок обнаруживают не только в щитовидной железе, но и в других тканях. Фундаментальное исследование O. Leder [8] подтвердило, что при введении радиоактивного йода он определяется, в том числе, в слизистой оболочке носа и носослезного протока. Указанный белок, ответственный за активный трансмембранный транспорт ионов I–, обнаруживается в тканях слезного мешка и носослезного протока [9]. Наибольшая экспрессия этого белка отмечается именно в тех областях, которые чаще других подвергаются фиброплазии после терапии радиоактивным йодом. H. Sakahara и соавт., S. Yuoness и соавт. и M. Ali и cоавт. [10–12] с помощью однофотонной эмиссионной компьютерной томографии (ОФЭКТ) выявили накопление радиоактивного йода в тканях носослезного протока у пациентов после терапии радиоактивным йодом. Эти данные позволяют считать поражение слезоотводящих путей специфическим осложнением терапии радиоактивным йодом.
Эти данные позволяют считать поражение слезоотводящих путей специфическим осложнением терапии радиоактивным йодом.
Первыми на проблему вторичного сужения слезоотводящих путей у пациентов после терапии радио активным йодом обратили внимание R. Kloos и соавт. [13]. Авторы описали развитие сужения и облитерации слезоотводящих путей у 10 пациентов, таким образом, обнаружив развитие этого состояния в 3% случаев после терапии радиоактивным йодом. У 6 пациентов для коррекции этого состояния потребовалось оперативное вмешательство, в 2 случаях повторное. У 7 пациентов нарушение слезоотведения имело двусторонний характер. Симптомами нарушения дренажной функции слезоотводящих путей, описанными авторами, были слезотечение, наличие отделяемого на веках, постоянный конъюнктивит, дакриоцистит и появление плотного образования в области слезного мешка. Эти симптомы фиксировались у пациентов в течение 6,5 мес после окончания терапии радиоактивным йодом. Минимальная доза, ассоциированная с поражением слезоотводящих путей, составила 150 мКи.
Позднее T. Shepler и соавт. [14] описали случай дакриоцистита у пациентки после терапии радиоактивным йодом. Авторы выполнили дакриоцисториностомию, проведя в дальнейшем гистологическое исследование удаленной ткани слизистой оболочки полости носа и стенки слезного мешка, которое подтвердило воспалительный характер поражения и выявило участки фиброплазии.
По данным разных авторов [13, 15–20], симптомы нарушения слезоотведения у пациентов развивались через 3—20 мес после терапии радиоактивным йодом, однако наиболее часто — через 6 мес. При двустороннем поражении вначале появлялись клинически значимые симптомы только с одной стороны [20].
Ограничения ряда исследований объясняют относительно широкий диапазон частоты встречаемости вторичной облитерации слезоотводящих путей. Так, J. Burns и соавт. [17] сообщили о развитии этого состояния у 4,6% пациентов после терапии радио активным йодом. В другой работе [21] нарушение слезоотведения обнаружено у 18% пациентов. Однако в первом исследовании показатель мог быть занижен (поскольку функция слезоотведения оценивалась только у пациентов, активно предъявлявших жалобы на слезотечение), а во втором исследовании он мог быть несколько завышен (поскольку для оценки дренажной функции слезоотводящих путей использовался метод лакримальной сцинтиграфии, не исключающий получение ложноположительных результатов) [22]. K. Al-Qahtani и соавт. [15] фиксировали случаи обращения с жалобами на слезотечение у пациентов, перенесших терапию радиоактивный йодом по поводу дифференцированного рака щитовидной железы. Недостаточность слезоотведения у таких пациентов была обнаружена в 2,2% случаев. F. da Fonseca и соавт. [23] сравнили частоту нарушений слезоотведения у пациентов с раком щитовидной железы, получавших и не получавших терапию радиоактивным йодом, и показали, что у пациентов после такого лечения частота сужений слезоотводящих путей составила 6,8% случаев, тогда как у пациентов контрольной группы такого осложнения отмечено не было.
K. Al-Qahtani и соавт. [15] фиксировали случаи обращения с жалобами на слезотечение у пациентов, перенесших терапию радиоактивный йодом по поводу дифференцированного рака щитовидной железы. Недостаточность слезоотведения у таких пациентов была обнаружена в 2,2% случаев. F. da Fonseca и соавт. [23] сравнили частоту нарушений слезоотведения у пациентов с раком щитовидной железы, получавших и не получавших терапию радиоактивным йодом, и показали, что у пациентов после такого лечения частота сужений слезоотводящих путей составила 6,8% случаев, тогда как у пациентов контрольной группы такого осложнения отмечено не было.
M. Ali и соавт. [12] показали, что нарушения слезоотведения зависят от дозы радиоактивного йода. С помощью ОФЭКТ накопление радиоактивного йода в области носовой полости и носослезного протока было выявлено у пациентов, получавших терапию радиоактивным йодом в дозе 100 мКи (50 наблюдений) и более 150 мКи (50 наблюдений). У пациентов, получавших радиоактивный йод в большей дозе, его накопление было более выраженным, что позволило предположить и более высокий риск развития осложнений у этих пациентов. A. Fard-Esfahani и соавт. обнаружили, что у пациентов, получавших терапию радиоактивным йодом в дозе менее 300 мКи, частота развития недостаточности слезоотведения составила 7,7%, тогда как у пациентов, получавших терапию в дозе более 300 мКи, — 27,4%. При этом выраженность сужения (от развития частичной непроходимости до полной облитерации) также возрастала пропорционально дозе излучения. Сообщений о развитии клинически значимой облитерации слезоотводящих путей у пациентов, получавших терапию радиоактивным йодом в дозе ниже 150 мКи, нами не найдено.
A. Fard-Esfahani и соавт. обнаружили, что у пациентов, получавших терапию радиоактивным йодом в дозе менее 300 мКи, частота развития недостаточности слезоотведения составила 7,7%, тогда как у пациентов, получавших терапию в дозе более 300 мКи, — 27,4%. При этом выраженность сужения (от развития частичной непроходимости до полной облитерации) также возрастала пропорционально дозе излучения. Сообщений о развитии клинически значимой облитерации слезоотводящих путей у пациентов, получавших терапию радиоактивным йодом в дозе ниже 150 мКи, нами не найдено.
Чаще всего для обнаружения нарушений слезоотведения достаточно клинического обследования, при котором находят увеличение размера слезного мениска, замедление теста с исчезновением красителя, регургитацию жидкости при попытке промывания слезоотводящих путей и препятствия при их зондировании [6, 13–15, 17, 20, 21, 23]. Отдельные авторы [21] пользовались лакримальной сцинтиграфией для верификации состояния дренажной функции слезоотводящих путей. Кроме того, имеются сообщения о применении визуализирующих технологий на основе рентгеновского излучения для точной локализации патологического процесса [15, 24].
Кроме того, имеются сообщения о применении визуализирующих технологий на основе рентгеновского излучения для точной локализации патологического процесса [15, 24].
При начальных стадиях сужения слезоотводящих путей возможна местная противовоспалительная терапия [13, 17]. Клинически эффективно назначение местных увлажняющих препаратов, глюкокортикостероидов, антибиотиков, противоаллергических препаратов, а также интраназальных сосудосуживающих средств. По мнению M. Ali [20], такое лечение результативно на ранних стадиях развития процесса, поскольку облитерация слезоотводящих путей формируется не одномоментно, а является исходом прогрессирования воспалительного процесса. Подробных указаний на тактику консервативного лечения пациентов с вторичными сужениями слезоотводящих путей в литературе нами не обнаружено. Можно предположить, что при коррекции таких состояний целесообразно использовать те же подходы, которые применимы у пациентов с первичными сужениями слезоотводящих путей (в частности, промывание слезоотводящих путей растворами ферментных препаратов, антибиотиками, кортикостероидами, антимикотическими препаратами, антиметаболитами и иммуномодуляторами) [25—27]. Наиболее эффективным лечением, по данным литературы [13, 14, 17, 20, 21, 23, 28–31] является хирургическая реконструкция путей слезоотведения, заключающая ся в их реканализации (баллонная дакриопластика, интубация слезоотводящих путей) и создании дакриостомы между полостью слезного мешка и полостью носа (дакриоцисториностомия или между конъюнктивальной полостью и полостью носа (лакориностомия). Эффективность оперативного лечения у таких пациентов несколько ниже, чем при первичной облитерации слезоотводящих путей.
Наиболее эффективным лечением, по данным литературы [13, 14, 17, 20, 21, 23, 28–31] является хирургическая реконструкция путей слезоотведения, заключающая ся в их реканализации (баллонная дакриопластика, интубация слезоотводящих путей) и создании дакриостомы между полостью слезного мешка и полостью носа (дакриоцисториностомия или между конъюнктивальной полостью и полостью носа (лакориностомия). Эффективность оперативного лечения у таких пациентов несколько ниже, чем при первичной облитерации слезоотводящих путей.
На сегодняшний день клинических рекомендаций по профилактике осложнений, связанных с сужением слезоотводящих путей, индуцированным радиоактивным йодом, не существует. В то же время есть отдельные исследования, указывающие на то, что превентивное назначение увлажняющих глазных капель позволяет снизить риск развития этого осложнения [19]. V. Juniat и соавт. [32] рекомендуют профилактически интубировать слезоотводящие пути перед терапией радиоактивным йодом, однако число наблюдений в указанном исследовании и его дизайн не позволяют сделать обоснованных с позиций доказательной медицины выводов. M. Ali и соавт. [20] полагают, что целесообразно сосредоточиться на создании медикаментозных средств, блокирующих активность белка-котранспортера Na+/I– в тканях носослезного протока, что теоретически может снизить влияние радиоактивного йода.
M. Ali и соавт. [20] полагают, что целесообразно сосредоточиться на создании медикаментозных средств, блокирующих активность белка-котранспортера Na+/I– в тканях носослезного протока, что теоретически может снизить влияние радиоактивного йода.
Заключение
По данным литературы, вторичное поражение слезоотводящих путей после терапии радиоактивным йодом является редким осложнением, которое вместе с тем в ряде случаев требует интенсивного консервативного или оперативного лечения. Известно, что само по себе слезотечение значительно снижает качество жизни. При наиболее раннем обнаружении признаков поражения слезоотводящих путей возможно проведение малоинвазивных вмешательств с высокой клинической эффективностью. Целесообразно рекомендовать пациентам консультацию офтальмолога сразу же после появления симптомов нарушения слезоотведения. Нарушение проходимости слезоотводящих путей в ряде случаев приводит к хроническому дакриоциститу, развитию флегмон слезного мешка и осложнениям со стороны глазного яблока, в том числе к формированию гнойной язвы роговицы. На сегодняшний день около 70% пациентов получают некорректное лечение по поводу слезотечения, возникшего после терапии радиоактивным йодом, тогда как установление диагноза происходит через 12 мес после возникновения заболевания [13], а в ряде случаев и в более поздние сроки [15].
На сегодняшний день около 70% пациентов получают некорректное лечение по поводу слезотечения, возникшего после терапии радиоактивным йодом, тогда как установление диагноза происходит через 12 мес после возникновения заболевания [13], а в ряде случаев и в более поздние сроки [15].
Дополнительная информация
Источник финансирования. Поисково-аналитическая работа проведена в рамках утвержденной научно-исследовательской работы 0511-2014-0025.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Участие авторов. Оба автора внесли равный вклад в проведение поисково-аналитической работы и подготовку статьи, прочли и одобрили финальную версию перед публикацией.
1. Румянцев П.О., Коренев С.В. История появления терапии радиоактивным йодом. // Клиническая и экспериментальная тиреоидология. — 2015. — Т. 11. — № 4. — С. 51-55. [Rumiantsev PO, Korenev SV. The history of radioiodine therapy beginnings. Clinical and Experimental Thyroidology. 2015;11(4):51-55. (In Russ.)]. doi: https://doi.org/10.14341/ket2015451-55
// Клиническая и экспериментальная тиреоидология. — 2015. — Т. 11. — № 4. — С. 51-55. [Rumiantsev PO, Korenev SV. The history of radioiodine therapy beginnings. Clinical and Experimental Thyroidology. 2015;11(4):51-55. (In Russ.)]. doi: https://doi.org/10.14341/ket2015451-55
2. Seidlin SM, Rossman I, et al. Radioiodine therapy of metastases from carcinoma of the thyroid; a 6-year progress report. J Clin Endocrinol Metab. 1949;9(11):1122-1137, Il lust. doi: https://doi.org/10.1210/jcem-9-11-1122
3. Lee SL. Complications of radioactive iodine treatment of thyroid carcinoma. J Natl Compr Canc Netw. 2010;8(11):1277-1287. doi: https://doi.org/10.6004/jnccn.2010.0094
4. Van nostrand D. The benefits and risks of i-131 therapy in patients with well-differentiated thyroid cancer. Thyroid. 2009;19(12):1381-1391. doi: https://doi.org/10.1089/thy.2009.1611
Thyroid. 2009;19(12):1381-1391. doi: https://doi.org/10.1089/thy.2009.1611
5. Solans R, Bosch JA, Galofre P, et al. Salivary and lacrimal Gland dysfunction (Sicca Syndrome) after radioiodine therapy. J Nucl Med. 2001;42(5):738-743.
6. Alexander C, Bader JB, Schaefer A, et al. Intermediate and long-term side effects of high-dose radioiodine therapy for thyroid carcinoma. J Nucl Med. 1998;39(9):1551-1554.
7. Garreis F, Gottschalt M, Paulsen FP. Antimicrobial peptides as a major part of the innate immune defense at the ocular surface. Dev Ophthalmol. 2010;45:16-22. doi: https://doi.org/10.1159/000315016
8. Leder O. The significance of extrathyroidal radioactive iodine accumulation and secretion in clinical pathology. Histochemistry. 1982;74(4):585-588. doi: https://doi.org/10.1007/bf00496673
Histochemistry. 1982;74(4):585-588. doi: https://doi.org/10.1007/bf00496673
9. Morgenstern KE, Vadysirisack DD, Zhang Z, et al. Expression of sodium iodide symporter in the lacrimal drainage system: implication for the mechanism underlying nasolacrimal duct obstruction in I131-treated patients. Ophthalmic Plast Reconstr Surg. 2005;21(5):337-344. doi: https://doi.org/10.1097/01.iop.0000179369.75569.a8
10. Sakahara H, Yamashita S, Suzuki K, et al. Visualization of nasolacrimal drainage system after radioiodine therapy in patients with thyroid cancer. Ann Nucl Med. 2007;21(9):525-527. doi: https://doi.org/10.1007/s12149-007-0056-5
11. Yuoness S, Rachinsky I, Driedger AA, Belhocine TZ. Differentiated thyroid cancer with epiphora: detection of nasolacrimal duct obstruction on I-131 Spect/Ct. Clin Nucl Med. 2011;36(12):1149-1152. Doi: Https://doi.org/10.1097/Rlu.0b013e3182336016
Clin Nucl Med. 2011;36(12):1149-1152. Doi: Https://doi.org/10.1097/Rlu.0b013e3182336016
12. Ali MJ, Vyakaranam AR, Rao JE, et al. Iodine-131 therapy and lacrimal drainage system toxicity: nasal localization studies using whole body nuclear scintigraphy and SPECT-CT. Ophthalmic Plast Reconstr Surg. 2017;33(1):13-16. doi: https://doi.org/10.1097/IOP.0000000000000603
13. Kloos RT, Duvuuri V, Jhiang SM, et al. Nasolacrimal drainage system obstruction from radioactive iodine therapy for thyroid carcinoma. J Clin Endocrinol Metab. 2002;87(12):5817-5820. doi: https://doi.org/10.1210/jc.2002-020210
14. Shepler TR, Sherman SI, Faustina MM, et al. Nasolacrimal duct obstruction associated with radioactive iodine therapy for thyroid carcinoma. Ophthalmic Plast Reconstr Surg. 2003;19(6):479-481. doi: https://doi.org/10.1097/01.IOP.0000092802.75899.F8
Ophthalmic Plast Reconstr Surg. 2003;19(6):479-481. doi: https://doi.org/10.1097/01.IOP.0000092802.75899.F8
15. Al-Qahtani KH, Al Asiri M, Tunio MA, et al. Nasolacrimal duct obstruction following radioactive iodine 131 therapy in differentiated thyroid cancers: review of 19 cases. Clin Ophthalmol. 2014;8:2479-2484. doi: https://doi.org/10.2147/OPTH.S71708
16. Brockmann H, Wilhelm K, Joe A, et al. Nasolacrimal drainage obstruction after radioiodine therapy: case report and a review of the literature. Clin Nucl Med. 2005;30(8):543-545. doi: https://doi.org/10.1097/01.rlu.0000170013.84378.2a
17. Burns JA, Morgenstern KE, Cahill KV, et al. Nasolacrimal obstruction secondary to I131 therapy. Ophthalmic Plast Reconstr Surg. 2004;20(2):126-129. doi: https://doi.org/10.1097/01.iop.0000117340.41849.81
doi: https://doi.org/10.1097/01.iop.0000117340.41849.81
18. Fonseca FL, Lunardelli P, Matayoshi S. Lacrimal drainage system obstruction associated to radioactive iodine therapy for thyroid carcinoma. Arq Bras Oftalmol. 2012;75(2):97-100.
19. Sun GE, Hatipoglu B. Epiphora after radioactive iodine ablation for thyroid cancer. Thyroid. 2013;23(2):243-245. doi: https://doi.org/10.1089/thy.2011.0186
20. Ali MJ. Iodine-131 therapy and nasolacrimal duct obstructions: what we know and what we need to know. Ophthalmic Plast Reconstr Surg. 2016;32(4):243-248. doi: https://doi.org/10.1097/IOP.0000000000000647
21. Fard-Esfahani A, Farzanefar S, Fallahi B, et al. Nasolacrimal duct obstruction as a complication of iodine-131 therapy in patients with thyroid cancer. Nucl Med Commun. 2012;33(10):1077-1080. doi: https://doi.org/10.1097/MNM.0b013e3283570fb8
Nasolacrimal duct obstruction as a complication of iodine-131 therapy in patients with thyroid cancer. Nucl Med Commun. 2012;33(10):1077-1080. doi: https://doi.org/10.1097/MNM.0b013e3283570fb8
22. Sagili S, Selva D, Malhotra R. Lacrimal scintigraphy: interpretation more art than science. Orbit. 2012;31(2):77-85. doi: https://doi.org/10.3109/01676830.2011.648797
23. da Fonseca FL, Yamanaka PK, Kato JM, Matayoshi S. Lacrimal system obstruction after radioiodine therapy in differentiated thyroid carcinomas: a prospective comparative study. Thyroid. 2016;26(12):1761-1767. doi: https://doi.org/10.1089/thy.2015.0657
24. Song H, Jeong J, Ju Koh M. Epiphora after radioactive iodine therapy in a low-risk patient. Clin Nucl Med. 2015;40(6):536-537. doi: https://doi.org/10.1097/RLU.0000000000000717
doi: https://doi.org/10.1097/RLU.0000000000000717
25. Атькова Е.Л., Федоров А.А., Резникова Л.В., и др. Пятилетний опыт использования цитологического метода в дакриологии. // Вестник офтальмологии. — 2013. — Т. 129. — № 5. — С. 104-113. [At’kova EL, Fedorov AA, Reznikova LV, et al. Five-year application experience of cytological method in dacryological practice. Annals of ophtalmology. 2013;129(5):104-113. (In Russ.)].
26. Choontanom R. Probing and syringing with 3% solution of NaCl and/or 0.2 mg/ml mitomycin-C in nasolacrimal duct obstruction patients. J Med Assoc Thai. 2010;93(Suppl 6):S197-S202.
27. Rumelt S. Primary treatment of nasolacrimal duct obstruction. J AAPOS. 2009;13(4):426; author reply 426-427. doi: https://doi. org/10.1016/j.jaapos.2009.04.003
org/10.1016/j.jaapos.2009.04.003
28. Атькова Е.Л., Федоров А.А., Ярцев В.Д., Роот А.О. Разработка оптимального способа проведения баллонной дакрио пластики. // Вестник офтальмологии. — 2015. — Т. 131. — № 2. — С. 99-104. [At’kova EL, Fedorov AA, Yartsev VD, Root AO. Developing the optimal protocol for balloon dacryoplasty. Annals of ophtalmology. 2015;131(2):99-104. (In Russ.)]. doi: https://doi.org/10.17116/oftalma2015131299-104
29. Атькова Е.Л., Ярцев В.Д., Краховецкий Н.Н., Роот А.О. Малоинвазивные вмешательства при дакриостенозе: современные тенденции. // Вестник офтальмологии. — 2014. — Т. 130. — № 6. — С. 89-97. [At’kova EL, Iartsev VD, Krakhovetskii NN, Root AO. Minimally invasive surgery for dacryostenosis: modern trends. Annals of ophtalmology. 2014;130(6):89-97. (In Russ.)].
30. Белоглазов В.Г. Альтернативные варианты восстановления проходимости слезоотводящих путей. // Вестник офтальмологии. — 2006. — Т. 122. — № 1. — С. 8-12. [Beloglazov VG. Alternatives to recovery of lacrimal duct patency. Annals of ophtalmology. 2006;122(1):8-12. (In Russ.)].
Белоглазов В.Г. Альтернативные варианты восстановления проходимости слезоотводящих путей. // Вестник офтальмологии. — 2006. — Т. 122. — № 1. — С. 8-12. [Beloglazov VG. Alternatives to recovery of lacrimal duct patency. Annals of ophtalmology. 2006;122(1):8-12. (In Russ.)].
31. Sweeney AR, Davis GE, Chang SH, Amadi AJ. Outcomes of endoscopic dacryocystorhinostomy in secondary acquired nasolacrimal duct obstruction: a case-control study. Ophthalmic Plast Reconstr Surg. 2018;34(1):20-25. doi: https://doi.org/10.1097/IOP.0000000000000841
32. Juniat VAR, Rajak S. The use of prophylactic Nunchaku stents to reduce the risk of nasolacrimal duct obstruction in patients with midfacial tumours undergoing radiotherapy. Orbit. 2017;36(5):298-300. doi: https://doi.org/10.1080/01676830.2017.1337182
Uterine bleeding in menopause, cancer risks | Kovalyova
All women with postmenopausal bleeding should be referred urgently. Еndometrial cancer is mostly diagnosed after menopause and often becomes apparent with atypical uterine bleeding.
Еndometrial cancer is mostly diagnosed after menopause and often becomes apparent with atypical uterine bleeding.
Климактерический период (климакс, климактерий) – это физиологический переходный период в жизни женщины или своеобразная ступень жизни, занимающая период времени между репродуктивной фазой и старостью. Согласно статистике, более 1/3 своей жизни женщина находится в периоде пери- и постменопаузы. По мнению ряда авторов, менопауза является сигналом для реализации профилактической медицины, когда формируются болезни старости, включая сердечно-сосудистые, неврологические и костно-мышечные заболевания [1]. В последние годы отмечается прогрессирующее увеличение средней продолжительности жизни женщин. Число пожилых женщин значительно превышает число пожилых мужчин. Согласно данным Всемирной организации здравоохранения, к 2015 г. 46% женского населения мира будет состоять из женщин старше 45 лет, при этом 8,3% будут страдать климактерическим синдромом. Исходя из этого актуален вопрос сохранения здоровья женской популяции и адекватного лечения климактерических проблем, возникающих более чем у 70% женщин в указанный период жизни. На фоне общего биологического старения организма инволютивные изменения происходят в половых органах и прежде всего в яичниках. Возрастное снижение пула примордиальных фолликулов и прекращение функционирования яичников генетически детерминированы и зависят главным образом от величины первоначального овариального резерва. Маточные кровотечения в пери- и постменопаузе – кровянистые выделения из половых путей циклического или чаще ациклического характера, возникающие в период пери- и постменопаузы. Дисфункциональные маточные кровотечения обусловлены изменениями в эндометрии на фоне нарушения гормональной функции яичников при отсутствии органической патологии органов малого таза. Маточные кровотечения являются наиболее частыми клиническими симптомами климактерия и самой распространенной причиной госпитализации в гинекологические стационары (10–35%).
46% женского населения мира будет состоять из женщин старше 45 лет, при этом 8,3% будут страдать климактерическим синдромом. Исходя из этого актуален вопрос сохранения здоровья женской популяции и адекватного лечения климактерических проблем, возникающих более чем у 70% женщин в указанный период жизни. На фоне общего биологического старения организма инволютивные изменения происходят в половых органах и прежде всего в яичниках. Возрастное снижение пула примордиальных фолликулов и прекращение функционирования яичников генетически детерминированы и зависят главным образом от величины первоначального овариального резерва. Маточные кровотечения в пери- и постменопаузе – кровянистые выделения из половых путей циклического или чаще ациклического характера, возникающие в период пери- и постменопаузы. Дисфункциональные маточные кровотечения обусловлены изменениями в эндометрии на фоне нарушения гормональной функции яичников при отсутствии органической патологии органов малого таза. Маточные кровотечения являются наиболее частыми клиническими симптомами климактерия и самой распространенной причиной госпитализации в гинекологические стационары (10–35%). Чрезмерная кровопотеря создает опасность возникновения железодефицитной анемии и служит причиной нарушений сексуальной жизни женщины, снижает качество жизни. Маточные кровотечения являются показанием для проведения около 60% гистерэктомий и большей части эндоскопических деструктивных хирургических вмешательств. Многообразие причин маточных кровотечений в пери- и постменопаузе создает большие возможности для проведения дифференциального диагноза, тем не менее условно можно выделить следующие виды: • органические, обусловленные патологией эндо- и миометрия, шейки матки, влагалища и яичников, в том числе онкогинекологическая патология; • неорганические, связанные с ановуляцией в пременопаузе и атрофией эндометрия в постменопаузе; • ятрогенные, связанные с влиянием гормональных (заместительная гормонотерапия) и негормональных препаратов (антикоагулянты, стероиды, барбитураты и др.), химио-, рентгено- и лучевая терапия; • обусловленные экстрагенитальными заболеваниями (коагулопатии, цирроз печени, заболевания эндокринных желез – щитовидной, поджелудочной, надпочечников, нарушения системы гемостаза и др.). При проведении дифференциальной диагностики у женщин с сохраненным менструальным циклом следует исключить беременность. Необходимо отметить, что аномальными кровотечениями на фоне циклического режима заместительной гормонотерапии считают появление обильных или длительных кровотечений в ожидаемые дни закономерных менструальноподобных реакций или любые ациклические кровяные выделения из половых путей. На фоне непрерывной комбинированной гормонотерапии – появление кровотечения после длительного периода аменореи или кровотечения, продолжающееся более 6 мес после начала терапии. Несмотря на то что основным индуктором кровотечения на фоне комбинированного режима гормонотерапии служит прогестаген, доказана доминирующая роль эстрогенов в его генезе. Причинами кровотечений прорыва могут быть атрофия слизистой оболочки (без патологических изменений) и снижение биоактивности половых гормонов. Вероятность появления кровотечения прорыва на фоне комбинированного непрерывного режима гормонотерапии повышается при уровне эстрадиола в плазме крови более 40 пг/мл [2]. Согласно современным представлениям наиболее часто в климактерии маточные кровотечения вызваны развитием гиперпластических состояний эндометрия, которые в этот возрастной период жизни женщины имеют высокий риск малигнизации. Показано, что некоторые формы рака являются гормональнозависимыми, кроме того, возраст обеспечивает активизацию проонкологических факторов, предрасполагающих к повышению риска развития онкологических заболеваний. В пре- и постменопаузе наиболее частой причиной маточных кровотечений служат полипы эндометрия, которые в зависимости от соотношения железистого и стромального компонентов, а также пролиферативной активности могут быть железистыми, железистофиброзными, фиброзными и аденоматозными. Частота полипов эндометрия встречается в 1,1–3,2% случаев, достигая 9–54% у женщин с маточными кровотечениями. В постменопаузе полипы эндометрия занимают ведущую роль среди внутриматочной патологии и достигают 52,2% случаев. Этиология роста полипа из ткани эндометрия и факторы, играющие в этом процессе ключевую роль, остаются до конца неизвестными. Считают, что пусковым фактором развития полипов эндометрия является пролонгированное пролиферативное действие эстрогенов, ведущее к повышению количества митозов в эндометрии. В постменопаузе трофическая стимуляция циркулирующих в кровотоке эстрогенов снижается, в то время как возрастает эффект от локального синтеза эстрогенов в эндометрии. Одним из ключевых факторов, определяющих уровень циркуляции эстрогенов у женщин в постменопаузе, является ароматаза, при помощи которой происходит синтез эстрогенов из андрогенов. Повышение активности ароматазы ведет к проявлению эстрогензависимых пролиферативных процессов, включая рак молочной железы, рак эндометрия, эндометриоз, аденомиоз и миому матки [3]. Участие жировой ткани как эндокринного органа в формировании внутриматочной патологии не вызывает сомнений. Показано повышение активности ароматазы P-450 в жировой ткани у женщин с возрастом. В тканях полипов эндометрия выявлено нарушение соотношения процессов пролиферации и апоптоза. Так, у женщин в пре- и постменопаузе отмечено повышение уровня Bcl-2 в железистой ткани полипов эндометрия, что свидетельствует о снижении активности апоптоза. На сегодняшний день нет консенсуса по вопросам ведения пациенток с рецидивирующими полипами эндометрия. В исследовании A.Domingues (2009 г.) отмечено, что фактором риска онкогенной трансформации полипов эндометрия является кровотечение. Недавно опубликованы результаты систематического обзора и метаанализа данных литературы, касающихся прогноза заболевания (риска малигнизации) при маточных кровотечениях, обусловленных полипами эндометрия, в зависимости от менопаузального статуса женщин (уровень доказательности III) [4]. Показано двукратное повышение частоты внутриматочной неоплазии на фоне полипов у женщин с симптоматическими кровотечениями по сравнению с женщинами без кровотечений. Отмечено, что у женщин в постменопаузе частота образования предраковых/злокачественных полипов в 3 раза выше по сравнению с женщинами репродуктивного возраста. Несмотря на большое количество публикаций, данные относительно размера полипа и риска его злокачественного перерождения были противоречивыми. Авторы подтверждают необходимость исключения злокачественного заболевания эндометрия при наличии любого маточного кровотечения у женщин в постменопаузе. Одна из ведущих причин кровотечений в климактерии – гиперплазия эндометрия, наиболее часто возникающая в возрасте 45–55 лет. В зависимости от структурных и цитологических изменений слизистой оболочки матки ее подразделяют на гиперплазию без атипии (простую и сложную) и атипическую гиперплазию (простую и сложную). Повышение частоты гиперплазии эндометрия связано не только с возрастными изменениями функции яичников, но и с большой частотой ожирения, а также нарушениями клеточного иммунитета, увеличивающими риск развития злокачественных процессов. В своих работах T.Perri и соавт. (2010 г.) факторами риска рака эндометрия у женщин в постменопаузе называют маточные кровотечения и возраст женщин старше 55 лет (р<0,05). Авторы подчеркивают, что особенности патогенеза пролиферативных процессов в эндометрии повышают их онкогенный потенциал, так как являются результатом пролиферации генетически измененных стволовых клеток базального слоя эндометрия. Маточные кровотечения могут возникать не только при доброкачественных изменениях слизистой оболочки матки, но и на фоне рака эндометрия. Показано, что разная экспрессия эстрогеновых рецепторов a в стволовых/прогениторных клетках может играть определенную роль в развитии гинекологических заболеваний, связанных с патологической пролиферацией эндометрия, включая рак эндометрия. В генезе гиперплазии и неоплазии эндометрия возникает нарушение соотношения механизмов пролиферации и апоптоза, что подтверждается изменением уровней специфических маркеров (Ki-67, PTEN, K-ras, p-53, 16, 21, 27, HER2/neu, IMP 3) [5]. Органическими причинами маточных кровотечений могут стать миома матки, внутренний эндометриоз, гормонально активные новообразования яичников, патология шейки матки и слизистой оболочки влагалища. В пременопаузальном возрасте ациклический характер кровотечений может быть обусловлен возрастной ановуляцией, приводящей к дефициту прогестерона и относительной гиперэстрогении. В постменопаузе кровотечение может появиться при отсутствии органической патологии на фоне атрофии эндометрия вследствие нарушения ангиогенеза, увеличения плотности сосудов эндометрия, проницаемости эндотелия и его разрывов, повышения локального фибринолиза и нарушения экспрессии матриксных металлопротеиназ. Клинические проявления маточных кровотечений: • менометроррагии – нерегулярные длительные маточные кровотечения, как правило, на фоне задержки менструации; • меноррагии – регулярные, длительные, обильные маточные кровотечения; • метроррагии – ациклические (межменструальные) кровянистые выделения из половых путей; • полименореи – регулярные маточные кровотечения (менструации) с интервалом менее 21 дня. В пременопаузе чаще возникают менометроррагии, нередко служащие одной из ведущих причин возникновения железодефицитной анемии, в постменопаузе – метроррагии на фоне отсутствия менструаций или применения заместительной гормонотерапии. Диагностика и терапия маточных кровотечений является актуальной проблемой, обусловленной не только высокой частотой патологии и ее рецидивирующим течением, но и патогенетической неоднородностью морфологических изменений эндометрия. Комплексное клинико-лабораторное обследование включает оценку кровопотери, характера менструаций, определение b-хорионического гонадотропина человека (в пременопаузе), клинический и биохимический анализ крови, исследование свертывающей системы крови, гормональное обследование (при образованиях в яичниках – СА-125, СА-19-9), трансвагинальное УЗИ органов малого таза, мазок на онкоцитологию из шейки матки. При наличии показаний проводят цветовое допплеровское картирование, магнитно-резонансную томографию органов малого таза, биопсию эндометрия, а также гистероскопию и раздельное диагностическое выскабливание эндометрия и эндоцервикса с морфологическим исследованием. Необходимо отметить, что на основании систематического обзора и метаанализа данных по определению толщины эндометрия как предиктора рака у женщин с маточными кровотечениями в постменопаузе показано, что пороговое значение этого показателя – 3 мм. Толщина эндометрия определялась при трансвагинальном УЗИ [6]. Терапия маточных кровотечений зависит от их генеза и интенсивности, направлена на выяснение причины, остановку кровотечения и профилактику рецидива. При наличии внутриматочной патологии проводят гистероскопию с раздельным диагностическим выскабливанием, резектоскопию, аблацию эндометрия, в ряде случаев – экстирпацию матки. Лечение органической патологии, манифестирующей маточными кровотечениями (полипы, гиперплазия и рак эндометрия, миома матки, аденомиоз, заболевания шейки матки и влагалища, аденомиоз, новообразования в яичниках) проводят в соответствии со стандартами лечения и характером выявленного заболевания. Для лечения маточных кровотечений в пременопаузальном возрасте, а точнее для профилактики их рецидивов после выскабливания проводят медикаментозную терапию. Показаниями к консервативной терапии служат гиперпластические процессы эндометрия при отсутствии другой гинекологической и экстрагенитальной патологии или в сочетании с небольшими интрамуральными-субсерозными узлами миомы и диффузной формы аденомиоза 1-й степени [7]. Основным компонентом медикаментозной терапии являются гормональные препараты разных групп, позволяющие регулировать состояние эндометрия. При отсутствии противопоказаний возможно применение препаратов циклической заместительной гормонотерапии, прогестагенных препаратов, агонистов гонадотропин-рилизинг-гормона, гестринона, левоноргестрелсодержащей внутриматочной системы Мирена. В связи с выраженными андрогенобусловленными побочными эффектами антигонадотропные препараты используются реже. Назначение комбинированных оральных контрацептивов у женщин в перименопаузе, по мнению ряда авторов, спорно ввиду высокого риска развития побочных эффектов. Учитывая большую частоту формирования латентного недостатка железа или развития железодефицитной анемии у больных с маточными кровотечениями необходимо проведение антианемической терапии c использованием препаратов железа. Например, препарат Актиферрин® содержит комбинацию сульфата железа (железо II) и D, L-серина. Входящая в состав Актиферрина a-аминокислота серин способствует более эффективному всасыванию железа и его поступлению в системный кровоток, что приводит к восстановлению его нормального содержания в организме, а также позволяет уменьшить дозу этого элемента, обеспечивая лучшую переносимость препарата. Актиферрин® выпускается в виде капель для приема внутрь, капсул и сиропа. Режим дозирования для взрослых: по 1 капсуле 1–2 раза в сутки под контролем уровня гемоглобина и сывороточного железа. При наличии экстрагенитальной патологии наряду с гемостатической терапией проводят лечение основного заболевания. Таким образом, тактика лечения женщин с маточными кровотечениями в климактерическом периоде определяется причиной кровотечения, степенью кровопотери, сопутствующей соматической и обменно-эндокринной патологией. Учитывая высокую частоту онкологической трансформации пролиферативных процессов эндометрия у пациенток с кровотечениями, проблема профилактики и повышения эффективности терапии представляется актуальной и требует пристального изучения.
Чрезмерная кровопотеря создает опасность возникновения железодефицитной анемии и служит причиной нарушений сексуальной жизни женщины, снижает качество жизни. Маточные кровотечения являются показанием для проведения около 60% гистерэктомий и большей части эндоскопических деструктивных хирургических вмешательств. Многообразие причин маточных кровотечений в пери- и постменопаузе создает большие возможности для проведения дифференциального диагноза, тем не менее условно можно выделить следующие виды: • органические, обусловленные патологией эндо- и миометрия, шейки матки, влагалища и яичников, в том числе онкогинекологическая патология; • неорганические, связанные с ановуляцией в пременопаузе и атрофией эндометрия в постменопаузе; • ятрогенные, связанные с влиянием гормональных (заместительная гормонотерапия) и негормональных препаратов (антикоагулянты, стероиды, барбитураты и др.), химио-, рентгено- и лучевая терапия; • обусловленные экстрагенитальными заболеваниями (коагулопатии, цирроз печени, заболевания эндокринных желез – щитовидной, поджелудочной, надпочечников, нарушения системы гемостаза и др.). При проведении дифференциальной диагностики у женщин с сохраненным менструальным циклом следует исключить беременность. Необходимо отметить, что аномальными кровотечениями на фоне циклического режима заместительной гормонотерапии считают появление обильных или длительных кровотечений в ожидаемые дни закономерных менструальноподобных реакций или любые ациклические кровяные выделения из половых путей. На фоне непрерывной комбинированной гормонотерапии – появление кровотечения после длительного периода аменореи или кровотечения, продолжающееся более 6 мес после начала терапии. Несмотря на то что основным индуктором кровотечения на фоне комбинированного режима гормонотерапии служит прогестаген, доказана доминирующая роль эстрогенов в его генезе. Причинами кровотечений прорыва могут быть атрофия слизистой оболочки (без патологических изменений) и снижение биоактивности половых гормонов. Вероятность появления кровотечения прорыва на фоне комбинированного непрерывного режима гормонотерапии повышается при уровне эстрадиола в плазме крови более 40 пг/мл [2]. Согласно современным представлениям наиболее часто в климактерии маточные кровотечения вызваны развитием гиперпластических состояний эндометрия, которые в этот возрастной период жизни женщины имеют высокий риск малигнизации. Показано, что некоторые формы рака являются гормональнозависимыми, кроме того, возраст обеспечивает активизацию проонкологических факторов, предрасполагающих к повышению риска развития онкологических заболеваний. В пре- и постменопаузе наиболее частой причиной маточных кровотечений служат полипы эндометрия, которые в зависимости от соотношения железистого и стромального компонентов, а также пролиферативной активности могут быть железистыми, железистофиброзными, фиброзными и аденоматозными. Частота полипов эндометрия встречается в 1,1–3,2% случаев, достигая 9–54% у женщин с маточными кровотечениями. В постменопаузе полипы эндометрия занимают ведущую роль среди внутриматочной патологии и достигают 52,2% случаев. Этиология роста полипа из ткани эндометрия и факторы, играющие в этом процессе ключевую роль, остаются до конца неизвестными. Считают, что пусковым фактором развития полипов эндометрия является пролонгированное пролиферативное действие эстрогенов, ведущее к повышению количества митозов в эндометрии. В постменопаузе трофическая стимуляция циркулирующих в кровотоке эстрогенов снижается, в то время как возрастает эффект от локального синтеза эстрогенов в эндометрии. Одним из ключевых факторов, определяющих уровень циркуляции эстрогенов у женщин в постменопаузе, является ароматаза, при помощи которой происходит синтез эстрогенов из андрогенов. Повышение активности ароматазы ведет к проявлению эстрогензависимых пролиферативных процессов, включая рак молочной железы, рак эндометрия, эндометриоз, аденомиоз и миому матки [3]. Участие жировой ткани как эндокринного органа в формировании внутриматочной патологии не вызывает сомнений. Показано повышение активности ароматазы P-450 в жировой ткани у женщин с возрастом. В тканях полипов эндометрия выявлено нарушение соотношения процессов пролиферации и апоптоза. Так, у женщин в пре- и постменопаузе отмечено повышение уровня Bcl-2 в железистой ткани полипов эндометрия, что свидетельствует о снижении активности апоптоза. На сегодняшний день нет консенсуса по вопросам ведения пациенток с рецидивирующими полипами эндометрия. В исследовании A.Domingues (2009 г.) отмечено, что фактором риска онкогенной трансформации полипов эндометрия является кровотечение. Недавно опубликованы результаты систематического обзора и метаанализа данных литературы, касающихся прогноза заболевания (риска малигнизации) при маточных кровотечениях, обусловленных полипами эндометрия, в зависимости от менопаузального статуса женщин (уровень доказательности III) [4]. Показано двукратное повышение частоты внутриматочной неоплазии на фоне полипов у женщин с симптоматическими кровотечениями по сравнению с женщинами без кровотечений. Отмечено, что у женщин в постменопаузе частота образования предраковых/злокачественных полипов в 3 раза выше по сравнению с женщинами репродуктивного возраста. Несмотря на большое количество публикаций, данные относительно размера полипа и риска его злокачественного перерождения были противоречивыми. Авторы подтверждают необходимость исключения злокачественного заболевания эндометрия при наличии любого маточного кровотечения у женщин в постменопаузе. Одна из ведущих причин кровотечений в климактерии – гиперплазия эндометрия, наиболее часто возникающая в возрасте 45–55 лет. В зависимости от структурных и цитологических изменений слизистой оболочки матки ее подразделяют на гиперплазию без атипии (простую и сложную) и атипическую гиперплазию (простую и сложную). Повышение частоты гиперплазии эндометрия связано не только с возрастными изменениями функции яичников, но и с большой частотой ожирения, а также нарушениями клеточного иммунитета, увеличивающими риск развития злокачественных процессов. В своих работах T.Perri и соавт. (2010 г.) факторами риска рака эндометрия у женщин в постменопаузе называют маточные кровотечения и возраст женщин старше 55 лет (р<0,05). Авторы подчеркивают, что особенности патогенеза пролиферативных процессов в эндометрии повышают их онкогенный потенциал, так как являются результатом пролиферации генетически измененных стволовых клеток базального слоя эндометрия. Маточные кровотечения могут возникать не только при доброкачественных изменениях слизистой оболочки матки, но и на фоне рака эндометрия. Показано, что разная экспрессия эстрогеновых рецепторов a в стволовых/прогениторных клетках может играть определенную роль в развитии гинекологических заболеваний, связанных с патологической пролиферацией эндометрия, включая рак эндометрия. В генезе гиперплазии и неоплазии эндометрия возникает нарушение соотношения механизмов пролиферации и апоптоза, что подтверждается изменением уровней специфических маркеров (Ki-67, PTEN, K-ras, p-53, 16, 21, 27, HER2/neu, IMP 3) [5]. Органическими причинами маточных кровотечений могут стать миома матки, внутренний эндометриоз, гормонально активные новообразования яичников, патология шейки матки и слизистой оболочки влагалища. В пременопаузальном возрасте ациклический характер кровотечений может быть обусловлен возрастной ановуляцией, приводящей к дефициту прогестерона и относительной гиперэстрогении. В постменопаузе кровотечение может появиться при отсутствии органической патологии на фоне атрофии эндометрия вследствие нарушения ангиогенеза, увеличения плотности сосудов эндометрия, проницаемости эндотелия и его разрывов, повышения локального фибринолиза и нарушения экспрессии матриксных металлопротеиназ. Клинические проявления маточных кровотечений: • менометроррагии – нерегулярные длительные маточные кровотечения, как правило, на фоне задержки менструации; • меноррагии – регулярные, длительные, обильные маточные кровотечения; • метроррагии – ациклические (межменструальные) кровянистые выделения из половых путей; • полименореи – регулярные маточные кровотечения (менструации) с интервалом менее 21 дня. В пременопаузе чаще возникают менометроррагии, нередко служащие одной из ведущих причин возникновения железодефицитной анемии, в постменопаузе – метроррагии на фоне отсутствия менструаций или применения заместительной гормонотерапии. Диагностика и терапия маточных кровотечений является актуальной проблемой, обусловленной не только высокой частотой патологии и ее рецидивирующим течением, но и патогенетической неоднородностью морфологических изменений эндометрия. Комплексное клинико-лабораторное обследование включает оценку кровопотери, характера менструаций, определение b-хорионического гонадотропина человека (в пременопаузе), клинический и биохимический анализ крови, исследование свертывающей системы крови, гормональное обследование (при образованиях в яичниках – СА-125, СА-19-9), трансвагинальное УЗИ органов малого таза, мазок на онкоцитологию из шейки матки. При наличии показаний проводят цветовое допплеровское картирование, магнитно-резонансную томографию органов малого таза, биопсию эндометрия, а также гистероскопию и раздельное диагностическое выскабливание эндометрия и эндоцервикса с морфологическим исследованием. Необходимо отметить, что на основании систематического обзора и метаанализа данных по определению толщины эндометрия как предиктора рака у женщин с маточными кровотечениями в постменопаузе показано, что пороговое значение этого показателя – 3 мм. Толщина эндометрия определялась при трансвагинальном УЗИ [6]. Терапия маточных кровотечений зависит от их генеза и интенсивности, направлена на выяснение причины, остановку кровотечения и профилактику рецидива. При наличии внутриматочной патологии проводят гистероскопию с раздельным диагностическим выскабливанием, резектоскопию, аблацию эндометрия, в ряде случаев – экстирпацию матки. Лечение органической патологии, манифестирующей маточными кровотечениями (полипы, гиперплазия и рак эндометрия, миома матки, аденомиоз, заболевания шейки матки и влагалища, аденомиоз, новообразования в яичниках) проводят в соответствии со стандартами лечения и характером выявленного заболевания. Для лечения маточных кровотечений в пременопаузальном возрасте, а точнее для профилактики их рецидивов после выскабливания проводят медикаментозную терапию. Показаниями к консервативной терапии служат гиперпластические процессы эндометрия при отсутствии другой гинекологической и экстрагенитальной патологии или в сочетании с небольшими интрамуральными-субсерозными узлами миомы и диффузной формы аденомиоза 1-й степени [7]. Основным компонентом медикаментозной терапии являются гормональные препараты разных групп, позволяющие регулировать состояние эндометрия. При отсутствии противопоказаний возможно применение препаратов циклической заместительной гормонотерапии, прогестагенных препаратов, агонистов гонадотропин-рилизинг-гормона, гестринона, левоноргестрелсодержащей внутриматочной системы Мирена. В связи с выраженными андрогенобусловленными побочными эффектами антигонадотропные препараты используются реже. Назначение комбинированных оральных контрацептивов у женщин в перименопаузе, по мнению ряда авторов, спорно ввиду высокого риска развития побочных эффектов. Учитывая большую частоту формирования латентного недостатка железа или развития железодефицитной анемии у больных с маточными кровотечениями необходимо проведение антианемической терапии c использованием препаратов железа. Например, препарат Актиферрин® содержит комбинацию сульфата железа (железо II) и D, L-серина. Входящая в состав Актиферрина a-аминокислота серин способствует более эффективному всасыванию железа и его поступлению в системный кровоток, что приводит к восстановлению его нормального содержания в организме, а также позволяет уменьшить дозу этого элемента, обеспечивая лучшую переносимость препарата. Актиферрин® выпускается в виде капель для приема внутрь, капсул и сиропа. Режим дозирования для взрослых: по 1 капсуле 1–2 раза в сутки под контролем уровня гемоглобина и сывороточного железа. При наличии экстрагенитальной патологии наряду с гемостатической терапией проводят лечение основного заболевания. Таким образом, тактика лечения женщин с маточными кровотечениями в климактерическом периоде определяется причиной кровотечения, степенью кровопотери, сопутствующей соматической и обменно-эндокринной патологией. Учитывая высокую частоту онкологической трансформации пролиферативных процессов эндометрия у пациенток с кровотечениями, проблема профилактики и повышения эффективности терапии представляется актуальной и требует пристального изучения.
- Медицина климактерия. Под ред. В.П.Сметник. М.: Литера, 2006; с. 15–32, 187–217.
- Ведение женщин в пери — и постменопаузе. Практические рекомендации. Ярославль: Литера, 2010; с. 92–119.
- Lee S.C, Kaunitz A.M, Sanchez-Ramos L et al. Heterogeneity in endometrial expression of aromatase in polyp — bearing uteri. Hum Reprod 2008;23 (1): 80–4.
- Rhatigan R.M. The oncogenic potential of endometrial polyps: a systematic review and meta — analysis. Obstet Gynecol 2010; 116: 1197–205.
- Yasue A, Hasegawa K, Udagawa Y. Effects of tamoxifen on the endometrium and its mechanism of carcinogenicity. Hum Cell 2011; 24 (2): 65–73.
- Timmermans B, Opmeer K, Khan S et al. Endometrial thickness measurement for detecting endometrial cancer in women with postmenopausal bleeding: A systematic review and meta — analysis. Obstet Gynecol 2010; 116 (1): 160–7.
- Кулаков В.И., Селезнева Н.Д., Белоглазова С.Е. Руководство по оперативной гинекологии. М.: Медицинское информационное агентство, 2006.
Cited-By
Article Metrics
Refbacks
- There are currently no refbacks.
Что такое холодовая аллергия и надо ли ее лечить?
Отличить обычное шелушение кожи от заболевания не так сложно: холодовая аллергия проявляется через какое-то время после нахождения на холоде и долго не проходит. В то время как с шелушением легко справляются смягчающие и увлажняющие кремы.
Интересно, что организм может так отреагировать не только на мороз, но и на холодные напитки или еду — получается, что заболеть можно даже летом. Чаще всего холодовой аллергии подвержены дети. У взрослых она, конечно, тоже встречается, но реже и переносится гораздо легче. В группу риска попадают те, кто имеет наследственную предрасположенность или страдает другими видами аллергии.
Воздействуя на слизистую оболочку глаза, холодовая аллергия способна вызвать обильное слезотечение. Также она может отражаться на дыхательной системе — в виде бронхоспастического рефлекса, который в тяжелых случаях может привести к образованию астматического статуса (тяжелого, угрожающего жизни осложнения бронхиальной астмы). В этом случае необходима экстренная интенсивная терапия.
Обычно негативная реакция организма на холод возникает спонтанно и может исчезнуть самостоятельно без применения медикаментов. Однако если аллергия проявляется часто, сохраняется надолго и достаточно выражена, заниматься самолечением не стоит. Для скорейшего выздоровления необходимо обратиться к врачу общей практики или к аллергологу, которые, возможно, попросят сдать анализ крови на такие маркеры, как эозинофилы и иммуноглобулин E. Если аллергия протекает в легкой форме, эти показатели могут не измениться вовсе.
Холодовая аллергия лечится так же, как и любая другая, антигистаминными препаратами. Курс может длиться от нескольких дней до нескольких месяцев. Если холодовую аллергию не лечить, то последствия могут быть такими же, как и после запущенной формы аллергии: острая крапивница, развитие бронхиальной астмы. Однако аллергия на холод, как правило, редко перетекает в серьезное заболевание.
Чтобы обезопасить себя от холодовой аллергии, необходимо тепло одеваться, стараться не дышать холодным воздухом и мазать открытые участки тела специальным кремом, защищающим от холода (или обычным жирным кремом). Для профилактики рекомендуется принимать витамины А, Е, С и PP.
Ведение пациентов с подтвержденным 2019-nCoV
Сводка последних изменений
- Новая информация о возможности недооценки скрытой гипоксемии с помощью пульсоксиметрии, особенно среди лиц с темной кожей
- Новая информация о дерматологических проявлениях, связанных с COVID-19
- Новая информация о длительном выделении репликационно-компетентного SARS-CoV-2 у лиц с тяжелым иммунодефицитом
- Новая информация об отчетах о повторном заражении вариантными вирусами
Просмотреть предыдущие обновления
В этом документе содержится руководство по уходу за пациентами, инфицированными SARS-CoV-2, вирусом, вызывающим COVID-19.Национальные институты здравоохранения (NIH) опубликовали рекомендации по клиническому лечению COVID-19 external icon, подготовленные Группой рекомендаций по лечению COVID-19. Рекомендации основаны на научных данных и мнениях экспертов и регулярно обновляются по мере появления новых данных.
Инструкции, касающиеся детей с COVID-19, см. В разделе «Педиатрические аспекты» ниже.
Клиническая презентация
Инкубационный период
Считается, что инкубационный период COVID-19 продлится до 14 дней, при этом среднее время от контакта до появления симптомов составляет 4-5 дней. (1-3) Одно исследование показало, что 97,5% людей с COVID-19, у которых есть симптомы, заболевают в течение 11,5 дней после заражения SARS-CoV-2. (3)
Презентация
Признаки и симптомы COVID-19, присутствующие в начале болезни, различаются, но в течение болезни многие люди с COVID-19 будут испытывать следующее: (1,4-9)
- Лихорадка или озноб
- Кашель
- Одышка или затрудненное дыхание
- Усталость
- Боли в мышцах или теле
- Головная боль
- Новая потеря вкуса или запаха
- Боль в горле
- Заложенность или насморк
- Тошнота или рвота
- Диарея
Симптомы могут различаться в зависимости от тяжести заболевания.Например, одышка чаще встречается среди людей, госпитализированных с COVID-19, чем среди людей с более легкими формами заболевания (не госпитализированные пациенты). (10, 11) Атипичные проявления COVID-19 возникают часто, и пожилые люди и люди с сопутствующими заболеваниями могут испытывать лихорадку и респираторные симптомы позже во время болезни, чем люди моложе или не имеющие сопутствующих заболеваний. (12, 13) В одном исследовании с участием 1099 госпитализированных пациентов лихорадка присутствовала только у 44% при поступлении в больницу, но в конечном итоге у 89% пациентов поднялась температура во время госпитализации. (1) Усталость, головная боль и боли в мышцах (миалгия) являются одними из наиболее часто встречающихся симптомов у людей, которые не госпитализированы, а боль в горле и заложенность носа или насморк (ринорея) также могут быть заметными симптомами. Многие люди с COVID-19 испытывают желудочно-кишечные симптомы, такие как тошнота, рвота или диарея, иногда до появления лихорадки и признаков и симптомов со стороны нижних дыхательных путей. (9) Потеря обоняния (аносмия) или вкуса (агевзия) часто отмечалась у трети пациентов в одном исследовании, особенно среди женщин и пациентов младшего и среднего возраста. (14)
Дерматологические проявления
Дерматологические проявления могут быть связаны с COVID-19. (99-102) Хотя частота остается неизвестной, сообщения варьируются от 0,2% в начале пандемии до 20,4%. (1,103-105) Связь с серьезностью заболевания и временем появления кожных симптомов у пациентов с COVID-19 неясна. (106-108) Клинические проявления разнообразны, хотя при исследовании 171 человека с лабораторно подтвержденным COVID-19 (от легкой до тяжелой степени) наиболее частыми кожными проявлениями были: макулопапулезная сыпь (22%). ), обесцвеченные поражения пальцев рук и ног (18%) и крапивница (16%).Среди всех участников исследования с COVID-19 и любыми кожными проявлениями примерно 60% сообщили о лихорадке и / или кашле. (109) Оценка кожных проявлений у пациентов с COVID-19 остается сложной задачей, поскольку симптомы могут напоминать множество других болезненных состояний. Кроме того, лечение COVID-19 также может вызывать определенные побочные эффекты на коже. (110) Изображения кожных находок доступны в Американской академии дерматологии, внешний значок.
Бессимптомная и предсимптомная инфекция
В нескольких исследованиях задокументировано инфицирование SARS-CoV-2, вирусом, вызывающим COVID-19, у пациентов, у которых никогда не было симптомов (бессимптомных), и у пациентов, у которых еще не было симптомов (бессимптомных). (15-29) Поскольку бессимптомные люди не всегда проходят обследование, распространенность бессимптомной инфекции и выявление пресимптомной инфекции еще недостаточно изучены. Текущие данные, основанные на тестировании полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР) для SARS-CoV-2 и серологических исследованиях, предполагают, что бессимптомные инфекции могут быть обычным явлением и что общее количество инфекций, вероятно, больше, чем количество зарегистрированных случаев . (15,22-24,30,31) У пациентов могут быть отклонения на визуализации грудной клетки до появления симптомов. (16)
Бессимптомная и предсимптомная передача
Растущее количество эпидемиологических исследований документально подтвердило передачу SARS-CoV-2 в течение пресимптоматического инкубационного периода. (19,28,29,32) В исследованиях с использованием обнаружения ОТ-ПЦР сообщалось о низких порогах цикла, что указывает на большее количество вирусной РНК среди людей с бессимптомной и пресимптомной инфекцией SARS-CoV-2. Аналогичным образом в вирусной культуре рост вируса наблюдался в образцах, полученных от пациентов с бессимптомной и пресимптомной инфекцией. (22,24,27,33) Доля передачи SARS-CoV-2 из-за бессимптомной или пресимптомной инфекции по сравнению с симптоматической инфекцией не совсем ясна; однако недавние исследования действительно предполагают, что люди, у которых нет симптомов, могут передавать вирус. (22,24,34)
Клинический курс
Степень тяжести заболевания
Большая когорта, в которую вошли более 44000 человек с COVID-19 из Китая, показала, что степень тяжести заболевания может варьироваться от легкой до критической: (35)
- От легкой до умеренной (от легких симптомов до легкой пневмонии): 81%
- Тяжелая (одышка, гипоксия или поражение легких более чем на 50% при визуализации): 14%
- Критическое состояние (дыхательная недостаточность, шок или дисфункция полиорганной системы): 5%
В этом исследовании все смертельные случаи произошли среди пациентов с тяжелым заболеванием, а общий коэффициент летальности (CFR) составил 2.3%. (35) CFR среди пациентов с критическим заболеванием составлял 49%. (35) Среди детей в Китае тяжесть заболевания была ниже, чем у взрослых, при этом 94% пораженных детей имели бессимптомное, легкое или умеренное заболевание; 5% страдают тяжелым заболеванием; и менее 1% страдают критическим заболеванием. (13) Среди случаев COVID-19 в США, зарегистрированных с 22 января по 30 мая 2020 г., в целом доля госпитализированных составила 14%, в том числе 2% поступили в отделение интенсивной терапии (ОИТ).Всего умерло 5% пациентов. (36)
Клиническая прогрессия
Среди пациентов, участвовавших в нескольких ранних исследованиях из Ухани, Китай, у которых было тяжелое заболевание COVID-19, среднее время от начала заболевания до появления одышки составляло 5–8 дней; среднее время от начала заболевания до острого респираторного дистресс-синдрома (ОРДС) составляло 8–12 дней; а среднее время от начала заболевания до поступления в ОИТ составляло 9,5–12 дней. (5,6,37,38) Клиницисты должны знать о возможности быстрого ухудшения состояния некоторых пациентов с COVID-19 примерно через неделю после начала заболевания.Среди всех госпитализированных пациентов 26–32% пациентов были госпитализированы в отделение интенсивной терапии. (6,8,38) Среди всех пациентов 3–17% имели ОРДС по сравнению с 20–42% для госпитализированных пациентов и 67–85% для пациентов, поступивших в ОИТ. (1,4-6,8,38) Смертность среди пациентов, поступивших в ОИТ, колебалась от 39% до 72% в зависимости от исследования и характеристик популяции пациентов. (5,8,37,38) Средняя продолжительность госпитализации выживших составила 10–13 дней. (1,6,8)
Факторы риска тяжелых заболеваний
Возраст — серьезный фактор риска тяжелых заболеваний, осложнений и смерти. (1,6,8,13,34,35,39-42) Среди когорты из более чем 44 000 подтвержденных случаев COVID-19 в Китае показатель летальности возрастал с возрастом и был самым высоким среди самой старшей когорты. Смертность среди людей 80 лет и старше составила 14,8%; 70–79 лет — 8,0%; 60–69 лет — 3,6%; 50–59 лет — 1,3%; 40–49 лет — 0,4%; а для лиц моложе 40 лет — 0,2%. (35) Согласно эпидемиологическим данным США на 16 марта 2020 г., CFR был самым высоким у людей в возрасте 85 лет и старше (диапазон 10–27%), за которыми следовали люди в возрасте 65–84 лет (3–11%). , в возрасте 55–64 лет (1–3%) и была ниже у людей моложе 55 лет (<1%). (39)
CFRв большой когорте в Китае был повышен для пациентов с сопутствующими заболеваниями: 10,5% пациентов с сердечно-сосудистыми заболеваниями, 7,3% пациентов с диабетом, 6,3% пациентов с хроническими респираторными заболеваниями и 5,6% пациентов с раком умирают от Заболевание, связанное с COVID. (35) Перенесенный ранее инсульт, диабет, хроническое заболевание легких и хроническое заболевание почек — все это связано с повышением тяжести заболевания и неблагоприятными исходами из-за COVID-19. Сердечные заболевания, включая сердечную недостаточность, ишемическую болезнь сердца, кардиомиопатии и легочную гипертензию, повышают риск тяжелого заболевания COVID-19.Люди с гипертонией могут подвергаться повышенному риску тяжелого заболевания, вызванного COVID-19, и должны продолжать принимать свои лекарства в соответствии с предписаниями. (43)
С учетом различий в возрасте и распространенности основных заболеваний смертность, связанная с COVID-19, о которой сообщалось в Соединенных Штатах, похоже, аналогична отчетам из Китая. (36, 39) См. Раздел «Люди, подверженные повышенному риску тяжелого заболевания», чтобы узнать больше о тех, кто подвержен повышенному риску.
Повторное заражение
На сегодняшний день существуют ограниченные данные о повторном заражении SARS-CoV-2 после выздоровления от COVID-19. (44-46) Опубликованные отчеты о случаях заболевания показали, что повторное заражение возможно, но все еще неясно, как долго люди, выздоровевшие от COVID-19, защищены от повторного заражения SARS-CoV-2, какая концентрация антител необходима для дают защиту и как часто может произойти повторное заражение. (44-46) COVID-19 коррелировал с обнаружением антител IgM и IgG к SARS-CoV-2. (48-51) COVID-19 коррелировал с обнаружением антител IgM и IgG к SARS-CoV-2. (48-51) О реинфекции вирусом варианта SARS-CoV-2 сообщалось в Бразилии, (116-118) в Великобритании, ( 119) и в Южной Африке. ( 120) Риск повторного заражения может возрасти в будущем из-за воздействия штаммов вируса варианта SARS-CoV-2, которые не нейтрализуются иммунными антисыворотками, например, недавно описанной в Южной Африке. ( 121)
Длительное обнаружение SARS-CoV-2
В то время как выделение вирусной РНК снижается с исчезновением симптомов, выделение РНК SARS-CoV-2 может продолжаться от нескольких дней до недель. (37,47,48) Таким образом, обнаружение вирусной РНК во время выздоровления не обязательно указывает на репликационно-компетентный вирус (инфекционность) или наличие нового инфекционного вируса. Некоторые выздоровевшие люди могут иметь детектируемую РНК SARS-CoV-2 в образцах верхних дыхательных путей в течение до 3 месяцев после начала заболевания, хотя и в концентрациях, значительно более низких, чем во время болезни, в диапазонах, где репликационно-компетентный вирус не был надежно восстановлен и заразность маловероятно.Некоторые люди с тяжелым заболеванием могут продуцировать репликационно-способный вирус более 10 дней, что может потребовать увеличения продолжительности изоляции и мер предосторожности до 20 дней после появления симптомов. Ограниченные данные свидетельствуют о том, что некоторые пациенты с тяжелым иммунодефицитом (например, пациенты с лимфомой, гипогаммаглобулинемией, реципиенты гемопоэтических стволовых клеток, пациенты со СПИДом, пациенты, получающие иммуносупрессию с помощью химиотерапии, системных кортикостероидов и биопрепаратов) могут продуцировать репликационно-компетентный вирус после 20 дней и требуют дополнительного тестирования и консультации со специалистами-инфекционистами и специалистами по инфекционному контролю. (111-115 ) Для получения дополнительной информации о продолжительности выделения вируса среди людей с инфекцией SARS-CoV-2 см. Продолжительность изоляции и меры предосторожности для взрослых с COVID-19. Также см. Критерии расследования предполагаемых случаев атипичной пневмонии CDC. Реинфекция CoV-2, а также Общий протокол расследования предполагаемой реинфекции SARS-CoV-2.
Результаты лабораторных и радиографических исследований
Тест на инфекцию
Диагностика COVID-19 требует обнаружения РНК или антигена SARS-CoV-2 в образцах из дыхательных путей.Обнаружение вирусной РНК SARS-CoV-2 лучше в образцах носоглотки по сравнению с образцами из горла. (32,47,52) Образцы нижних дыхательных путей могут иметь более высокий выход вируса, чем образцы верхних дыхательных путей. (53) Тесты на антиген SARS-CoV-2 также можно использовать в различных стратегиях тестирования . См. «Временное руководство по быстрому тестированию на антигены для SARS-CoV-2» для получения дополнительной информации об эффективном использовании тестов на антигены в различных ситуациях тестирования. РНК SARS-CoV-2 также была обнаружена в кале и крови. (51,54) Обнаружение РНК SARS-CoV-2 в крови может быть маркером тяжелого заболевания. (55)
Инфекция как SARS-CoV-2, так и другими респираторными вирусами (например, гриппом) или бактериями хорошо задокументирована, и обнаружение другого респираторного патогена не исключает COVID-19. (56) Клиницистам рекомендуется рассмотреть возможность тестирования на другие вирусные причины респираторных заболеваний, например гриппа, в дополнение к тестированию на SARS-CoV-2 в зависимости от возраста пациента, сезона или клинических условий.Клиницисты также должны учитывать бактериальные и грибковые причины пневмонии (например, болезнь легионеров у пациентов, контактировавших с водой из ранее закрытых зданий или ночных путешествий, пневмококковая пневмония и кокцидиоидомикоз) у пациентов, у которых ПЦР-отрицательный результат на SARS CoV-2, по клиническим показаниям. . См. Рекомендации IDSA / ATS: внешний значок.
Для получения дополнительной информации о тестировании на COVID-19 и сборе, обработке и хранении образцов посетите Обзор тестирования на SARS-CoV-2 (COVID-19) и Часто задаваемые вопросы о COVID-19 для лабораторий.
Другие результаты лабораторных исследований
Лимфопения — наиболее частая лабораторная находка среди людей с COVID-19, которая обнаруживается у 83% госпитализированных пациентов. (1,5) Лимфопения, нейтрофилия, повышенный уровень аланинаминотрансферазы и аспартатаминотрансферазы в сыворотке, повышенный уровень лактатдегидрогеназы, высокий уровень С-реактивного белка (СРБ) и высокий уровень ферритина могут быть связаны с большей тяжестью заболевания. (1,5,6,8) Повышенный уровень D-димера и лимфопения были связаны со смертностью. (8,37,57,58) Прокальцитонин обычно нормален при поступлении, но может повышаться у пациентов, поступивших в отделение интенсивной терапии. (4-6) Пациенты с критическим заболеванием имели высокий уровень воспалительных факторов в плазме, что указывает на потенциальную иммунную дисрегуляцию. (5,59)
Результаты рентгенографии
Рентгенограммы грудной клетки пациентов с COVID-19 обычно демонстрируют двустороннюю консолидацию воздушного пространства, хотя у некоторых пациентов рентгенограммы грудной клетки не примечательны на ранней стадии заболевания. (1,47) Изображения компьютерной томографии (КТ) грудной клетки пациентов с COVID-19 обычно демонстрируют двустороннее периферическое помутнение матового стекла. (60-71) Поскольку эта картина КТ грудной клетки неспецифична и может быть обнаружена при пневмониях, вызванных другими инфекциями, диагностическая ценность КТ грудной клетки для COVID-19 может быть низкой и зависеть от рентгенологической интерпретации. (70) Одно исследование показало, что 56% пациентов, поступивших в течение двух дней после постановки диагноза, имели нормальную компьютерную томографию. (62) Напротив, другие исследования выявили аномалии компьютерной томографии грудной клетки у пациентов до обнаружения РНК SARS-CoV-2 при ОТ-ПЦР проб из носоглотки. (71) Учитывая вариабельность результатов визуализации грудной клетки, только рентгенография или КТ не рекомендуются для диагностики COVID-19. Американский колледж радиологии также не рекомендует КТ для скрининга или в качестве теста первой линии для диагностики COVID-19. (См. Значок рекомендаций Американского колледжа радиологии).
Клиническое ведение и лечение
Национальные институты здравоохранения (NIH) опубликовали рекомендации по профилактике, тестированию и ведению пациентов с COVID-19. Для получения дополнительной информации посетите Руководство NIH Coronavirus Disease 2019 (COVID-19). Внешний значок рекомендации основан на научных данных и мнениях экспертов и регулярно обновляется по мере появления новых данных. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило ремдесивир (Veklury) для лечения COVID-19 в определенных ситуациях.Клиническое лечение COVID-19 включает меры профилактики и контроля инфекций, а также поддерживающую терапию, включая дополнительный кислород и искусственную вентиляцию легких по показаниям.
Болезнь легкой и средней степени тяжести
Пациенты с легкой клинической картиной (отсутствие вирусной пневмонии и гипоксии) могут изначально не нуждаться в госпитализации, и большинство пациентов смогут лечить свое заболевание дома. Решение о наблюдении за пациентом в стационаре или амбулаторно следует принимать в индивидуальном порядке.Это решение будет зависеть от клинической картины, потребности в поддерживающей терапии, потенциальных факторов риска тяжелого заболевания и способности пациента к самоизоляции дома. Пациенты с факторами риска тяжелого заболевания (см. «Люди с повышенным риском тяжелого заболевания») должны находиться под тщательным наблюдением, учитывая возможный риск развития тяжелого заболевания, особенно на второй неделе после появления симптомов. (5,6,35)
В некоторых клинических условиях пульсоксиметрия используется для оценки и мониторинга состояния оксигенации пациента.Клиницисты должны знать, что пульсоксиметры могут показывать неоптимальную точность в определенных группах населения. (92,93) Ограниченные данные исследований с небольшим количеством участников предполагают, что пигментация кожи может влиять на точность пульсоксиметра. (94-97) В одном исследовании, опубликованном в декабре 2020 года, использовались данные о гонках, о которых сообщали сами участники, и сравнивали пульсоксиметрию с измерением сатурации артериальной крови кислородом в двух группах взрослых пациентов, которые получали дополнительный кислород. Эти когорты включали 1333 белых пациента и 276 чернокожих пациентов в одной университетской больнице в период с января по июль 2020 года, а также 7342 белых пациента и 1050 чернокожих пациентов в отделениях интенсивной терапии в 178 больницах в течение 2014-2015 годов.Авторы сообщили, что скрытая гипоксемия (определяемая в исследовании как «насыщение артериальной крови кислородом <88% газами артериальной крови, несмотря на насыщение кислородом от 92 до 96% по данным пульсоксиметрии») не выявлялась пульсоксиметрией почти в три раза чаще в Black пациенты, чем белые пациенты. (98) Это исследование подчеркивает важность оценки других факторов (например, состояний высокого риска, наблюдаемых признаков и симптомов) вместо того, чтобы полагаться только на измерения пульсоксиметрии при оценке, сортировке и ведении пациентов с подозрением или лабораторно подтвержденным COVID. -19.
Для получения информации о рекомендациях по профилактике инфекций и борьбе с ними см. Руководство по инфекционному контролю для медицинских работников в отношении коронавируса (COVID-19).
Тяжелая болезнь
У некоторых пациентов с COVID-19 будет тяжелое заболевание, требующее госпитализации для лечения. Стационарное ведение пациентов включает поддерживающее лечение наиболее распространенных осложнений тяжелой формы COVID-19: пневмонии, гипоксемической дыхательной недостаточности / ОРДС, сепсиса и септического шока, кардиомиопатии и аритмии, острого повреждения почек и осложнений от длительной госпитализации, включая вторичные бактериальные и грибковые инфекции, тромбоэмболия, желудочно-кишечные кровотечения и полинейропатия / миопатия в критических состояниях. (1,4-6,13,35,40,72-74)
Дополнительную информацию можно найти в разделе «Клинические вопросы о COVID-19: вопросы и ответы». Дополнительные ресурсы и руководящие документы по лечению и ведению COVID-19, включая стационарное ведение пациентов в критическом состоянии, представлены ниже.
Гиперкоагуляция и COVID-19
Некоторые пациенты с COVID-19 могут иметь признаки состояния гиперкоагуляции и иметь повышенный риск венозного и артериального тромбоза крупных и мелких сосудов. (57,58,75-80) Лабораторные отклонения, обычно наблюдаемые среди госпитализированных пациентов с коагулопатией, связанной с COVID-19, включают:
- Легкая тромбоцитопения
- Повышение уровня D-димера
- Продукты повышенного разложения фибрина
- Длительное протромбиновое время
Повышенные уровни D-димера тесно связаны с повышенным риском смерти. (8,37,57,58)
Имеется несколько сообщений о госпитализированных пациентах с тромботическими осложнениями, наиболее часто с тромбозом глубоких вен и тромбоэмболией легочной артерии. (58,75-77) Другие зарегистрированные проявления включают:
- Микроваскулярный тромбоз пальцев стопы («COVID toes»)
- Свертывание внутрисосудистых катетеров
- Травма миокарда с подъемом сегмента ST
- Ход крупных сосудов (78,79)
Патогенез гиперкоагуляции, связанной с COVID-19, изучен не полностью. Однако гипоксия и системное воспаление, вторичные по отношению к COVID-19, могут привести к высокому уровню воспалительных цитокинов и активации пути коагуляции. (81)
Доступные данные для информирования клинического руководства о профилактике или лечении венозной тромбоэмболии у пациентов с COVID-19 все еще развиваются, и новая информация часто публикуется. Несколько национальных профессиональных ассоциаций предоставляют ресурсы для получения последней информации о гиперкоагуляции, связанной с COVID-19, включая лечение антикоагулянтами. Дополнительную информацию о гиперкоагуляции и COVID-19 можно получить на внешнем значке Американского общества гематологии и на внешнем значке Национальных институтов здравоохранения.
Педиатрические рекомендации
Все чаще данные указывают на то, что клинические симптомы, которые испытывают дети с COVID-19, похожи на симптомы взрослых, но болезнь обычно протекает легче, чем у взрослых, и тяжесть симптомов зависит от возраста ребенка. Многие дети, инфицированные SARS-CoV-2, остаются бессимптомными или имеют легкое заболевание. (82,83) Симптомы, о которых обычно сообщают у детей с COVID-19, включают кашель или лихорадку, и многие дети также испытывают желудочно-кишечные или другие симптомы. (84-88) Несмотря на то, что у большинства детей с COVID-19 заболевание протекает бессимптомно или в легкой форме, у детей были зарегистрированы тяжелые исходы, включая летальный исход. (89) Дети любого возраста с определенными сопутствующими заболеваниями могут подвергаться повышенному риску тяжелого заболевания; также младенцы (младше 12 месяцев) могут подвергаться повышенному риску тяжелого заболевания COVID-19. (89, 90)
CDC и партнеры исследуют мультисистемный воспалительный синдром у детей (MIS-C), связанный с COVID-19.Пациенты с MIS-C обычно жалуются на стойкую лихорадку, боль в животе, рвоту, диарею, кожную сыпь, кожно-слизистые поражения и, в тяжелых случаях, гипотензию и шок. У больных детей повышены лабораторные маркеры воспаления (например, CRP, ферритин), и у большинства пациентов наблюдаются лабораторные маркеры повреждения сердца (например, тропонин; натрийуретический пептид B-типа (BNP) или proBNP). У некоторых пациентов наблюдается миокардит, сердечная дисфункция и острое повреждение почек. Не все дети с MIS-C испытывают одни и те же признаки и симптомы, а у некоторых детей могут быть симптомы, не перечисленные здесь.MIS-C может начаться через несколько недель после заражения ребенка SARS-CoV-2. Ребенок мог заразиться в результате бессимптомного контакта, и в некоторых случаях ребенок и его опекуны могли не осознавать, что ребенок был инфицирован.
Подробные сведения об уходе за детьми с подтвержденным или подозреваемым COVID-19 и связанными с ним осложнениями см. По адресу:
Исследовательская терапия
Национальные институты здравоохранения опубликовали рекомендации по медицинскому лечению внешнего заражения COVID-19, подготовленные Группой рекомендаций по лечению COVID-19.Это руководство содержит информацию о терапевтических средствах и будет обновляться по мере появления новой информации и одобрения FDA для использования лекарств и других терапевтических вмешательств. Лица, которым нужна информация о зарегистрированных клинических испытаниях COVID-19 в США, могут найти такую информацию здесь: ClinicalTrials.govexternal icon.
Прекращение применения мер предосторожности при передаче или изоляция дома
Пациенты, которые клинически выздоровели и могут выписаться из больницы, но которые не были освобождены от мер предосторожности, связанных с передачей инфекции, могут продолжать изоляцию по месту жительства до тех пор, пока не будут освобождены.Рекомендации по отмене мер предосторожности, связанных с передачей инфекции, или изоляции в домашних условиях для пациентов, выздоровевших от COVID-19, см .:
Предыдущие обновления
По состоянию на 3 ноября 2020 г.
- Новая информация для лабораторных и радиографических результатов
- Новая информация для педиатрии
- Изменения для ясности и существенные обновления сносок в
- Блок оповещения о гриппе
- Информация об одобрении FDA ремдесивира
По состоянию на 27 октября 2020 г.
- Содержимое обновлено до Reinfection
По состоянию на 10 сентября 2020 г.
- Содержимое обновлено до Reinfection
По состоянию на 20 июня 2020 г., чтобы отразить следующее:
По состоянию на 29 мая 2020 г.
По состоянию на 25 мая 2020 г.
По состоянию на 20 мая 2020 г.
По состоянию на 12 мая 2020 г.
- Новая информация о гиперкоагуляции, связанной с COVID-19
- Обновленное содержание и ресурсы, включая новые рекомендации NIH по лечению
- Незначительные изменения для ясности
- Guan WJ, Ni ZY, Hu Y и др.Клиническая характеристика коронавирусной болезни 2019 в Китае. N Engl J Med . 2020 30 апреля; 382: 1708–1720. doi: 10.1056 / NEJMoa2002032 внешний значок.
- Li Q, Guan X, Wu P и др. Динамика ранней передачи новой пневмонии, инфицированной коронавирусом, в Ухане, Китай. N Engl J Med . 2020 26 марта; 382: 1199–207. doi: 10.1056 / nejmoa2001316 внешний значок.
- Лауэр С.А., Грантц К.Х., Би К. и др. Инкубационный период коронавирусной болезни 2019 (COVID-19) из официально зарегистрированных подтвержденных случаев: оценка и применение. Энн Интерн Мед. . 2020 5 мая; 172 (9): 577–82. doi: 10.7326 / M20-0504 внешний значок.
- Чен Н., Чжоу М., Дун Х и др. Эпидемиологические и клинические характеристики 99 случаев новой коронавирусной пневмонии 2019 г. в Ухане, Китай: описательное исследование. Ланцет . 2020 февраль; 395: 507–13. DOI: 10.1016 / S0140-6736 (20) 30211-7 внешний значок.
- Хуанг Ц., Ван И, Ли Х и др. Клинические особенности пациентов, инфицированных новым коронавирусом 2019 г., в Ухане, Китай. Ланцет .2020 февраль; 395: 497–506. DOI: 10.1016 / S0140-6736 (20) 30183-5 внешний значок.
- Ван Д., Ху Б., Ху С. и др. Клинические характеристики 138 госпитализированных пациентов с новой коронавирусной пневмонией 2019 г. в Ухане, Китай. ЯМА . 2020 7 февраля; 323 (11): 1061–9. doi: 10.1001 / jama.2020.1585 внешний значок.
- Xu XW, Wu XX, Jiang XG и др. Клинические данные в группе пациентов, инфицированных новым коронавирусом 2019 года (SARS-Cov-2), за пределами Ухани, Китай: ретроспективная серия случаев. BMJ . 2020 19 февраля; 368: m606. doi: 10.1136 / bmj.m606 внешний значок.
- Wu C, Chen X, Cai Y и др. Факторы риска, связанные с синдромом острого респираторного дистресса и смертью пациентов с коронавирусной болезнью 2019 Пневмония в Ухане, Китай. JAMA Intern Med . 2020 марта 13; 180 (7): 934–43. doi: 10.1001 / jamainternmed.2020.0994 внешний значок.
- Pan L, Mu M, Yang P, et al. Клинические характеристики пациентов с COVID-19 с пищеварительными симптомами в провинции Хубэй, Китай: описательное, кросс-секционное, многоцентровое исследование. Ам Дж. Гастроэнтерол . 2020 Май; 115 (5): 766–73. doi: 10.14309 / ajg.0000000000000620 внешний значок.
- Killerby ME, Link-Gelles R, Haight SC, et al. Характеристики, связанные с госпитализацией пациентов с COVID-19 — Метрополитен Атланта, Джорджия, март – апрель 2020 г. MMWR . 2020 июн 26; 69: 790–794. doi: 10.15585 / mmwr.mm6925e1 внешний значок.
- Tenforde MW, Rose EB, Lindsell CJ и др. Характеристики взрослых амбулаторных и стационарных пациентов с COVID-19 —– 11 академических медицинских центров, США, март –– май 2020 г. MMWR . 2020 3 июля; 69: 841-846. doi: 10.15585 / mmwr.mm6926e3 внешний значок.
- Цай Дж., Сюй Дж., Линь Д. и др. Серия клинических случаев у детей с новой коронавирусной инфекцией 2019 г .: клинико-эпидемиологические особенности. Clin Infect Dis 2020; 71 (6): 1547–-1551. DOI: 10.1093 / cid / ciaa198 внешний значок.
- Dong Y, Mo X, Hu Y и др. Эпидемиология COVID-19 среди детей в Китае. Педиатрия . 2020 июн; 145 (6): e20200702. doi: 10.1542 / peds.2020-0702 внешний значок.
- Джакомелли А., Пеццати Л., Конти Ф и др. Самостоятельно сообщаемые обонятельные и вкусовые расстройства у пациентов с SARS-CoV-2: перекрестное исследование. Клин Инфекция Дис . 2020 август; 71 (15): 889–890. DOI: 10.1093 / cid / ciaa330 внешний значок.
- Лу Х, Чжан Л., Ду Х и др. Инфекция SARS-CoV-2 у детей. N Engl J Med . 2020 23 апреля; 382: 1663-5. doi: 10.1056 / NEJMc2005073 внешний значок.
- Чан Дж. Ф., Юань С., Кок К. Х. и др. Семейный кластер пневмонии, связанный с новым коронавирусом 2019 года, указывающий на передачу от человека к человеку: исследование семейного кластера. Ланцет . 2020 февраль; 395: 514–23. DOI: 10.1016 / S0140-6736 (20) 30154-9 внешний значок.
- Hu Z, Song C, Xu C и др. Клинические характеристики 24 бессимптомных инфекций COVID-19, проверенных среди близких людей в Нанкине, Китай. Наука, Китай, Жизнь, Наука . 2020 4 марта; 63: 706–11. doi: 10.1007 / s11427-020-1661-4 внешний значок.
- Wang Y, Liu Y, Liu L, Wang X, Luo N, Ling L. Клинический исход 55 бессимптомных случаев заражения SARS-Coronavirus-2 на момент госпитализации в Шэньчжэне, Китай. J Заразить Dis . 2020 июн 1. doi: 10.1093 / infdis / jiaa119external icon.
- Pan X, Chen D, Xia Y, et al. Бессимптомные случаи в семейном кластере с инфекцией SARS-CoV-2. Ланцет Infect Dis . 2020 Апрель; 20: 410-1. DOI: 10.1016 / S1473-3099 (20) 30114-6 внешний значок.
- Бай Й, Яо Л., Вэй Т. и др. Предполагаемая бессимптомная передача COVID-19 носителем. ЯМА . 2020 21 февраля; 323 (14): 1406-1407. doi: 10.1001 / jama.2020.2565 внешний значок.
- Kam KQ, Yung CF, Cui L, et al.Здоровый младенец с коронавирусной болезнью 2019 (COVID-19) с высокой вирусной нагрузкой. Клин Инфекция Дис . 2020 1 августа; 71 (15): 847–9. DOI: 10.1093 / cid / ciaa201 внешний значок.
- Кимбалл А., Хатфилд К.М., Аронс М. и др. Бессимптомные и предсимптомные инфекции SARS-CoV-2 у жителей учреждения длительного ухода с квалифицированным медицинским уходом — округ Кинг, Вашингтон, март 2020 г. MMWR . 2020 27 марта; 69: 377-81. doi: 10.15585 / mmwr.mm6913e1 внешний значок.
- Roxby AC, Greninger AL, Hatfield KM и др.Выявление SARS-CoV-2 среди жителей и сотрудников сообщества для пожилых людей, проживающих с уходом, — Сиэтл, Вашингтон, 2020 г. MMWR . 2020 3 апреля; 69: 416–8. doi: 10.15585 / mmwr.mm6914e2 внешний значок.
- Мизумото К., Кагая К., Заребски А., Чоуэлл Г. Оценка бессимптомной доли случаев заболевания коронавирусом 2019 (COVID-19) на борту круизного лайнера Diamond Princess, Иокогама, Япония, 2020 г. Euro Surveill . 2020 5 февраля; 25. DOI: 10,2807% 2F1560-7917.ES.2020.25.10.2000180 внешний значок.
- Hoehl S, Rabenau H, Berger A, et al. Свидетельства инфекции SARS-CoV-2 у возвращающихся путешественников из Ухани, Китай. N Engl J Med . 2020 26 марта; 382: 1278–80. doi: 10.1056 / NEJMc2001899 внешний значок.
- Wei WE, Li Z, Chiew CJ, Yong SE, Toh MP, Lee VJ. Пресимптомная передача SARS-CoV-2 — Сингапур, 23 января — 16 марта 2020 г. MMWR . 2020 1 апреля; 69: 411-5. doi: 10.15585 / mmwr.mm6914e1 внешний значок.
- Тонг З.Д., Тан А., Ли К.Ф. и др.Возможная предсимптомная передача SARS-CoV-2, провинция Чжэцзян, Китай, 2020 г. Emerg Infect Dis . 2020 Май; 26: 1052–4. DOI: 10.3201 / eid2605.200198.
- Qian G, Yang N, Ma AHY, et al. Передача COVID-19 внутри семейного кластера через несимптомные инфекционные заболевания в Китае. Клин Инфекция Дис . 2020 23 марта; 71 (15): 861–2. org: 10.1093 / cid / ciaa316external icon.
- Роте С., Шунк М., Сотманн П. и др. Передача инфекции 2019-nCoV от бессимптомного контакта в Германии. N Engl J Med . 2020 5 марта; 382: 970–1. doi: 10.1056 / NEJMc2001468 внешний значок.
- Хейверс, Ф. П., Рид, К., Лим, Т., Монтгомери, Дж. М., Клена, Д. Д., Холл, А. Дж., Фрай, А. М., Кэннон, Д. Л., Чианг, К. Ф., Гиббонс, А. и Крапюная, И. антитела к SARS-CoV-2 в 10 центрах США, 23 марта — 12 мая 2020 г. JAMA Internal Medicine . 2020 21 июля. Doi: 10.1001 / jamainternmed.2020.4130external icon.
- Rosenberg ES, Tesoriero JM, Rosenthal EM, et al.Совокупная заболеваемость и диагностика инфекции SARS-CoV-2 в Нью-Йорке. Энн Эпидемиол . 2020 август; 48: 23–9. DOI: 10.1016 / j.annepidem.2020.06.004 внешний значок.
- Цзоу Л., Руан Ф., Хуанг М. и др. Вирусная нагрузка SARS-CoV-2 в образцах верхних дыхательных путей инфицированных пациентов. N Engl J Med . 2020 марта 19; 382: 1177–9. org: 10.1056 / NEJMc2001737 внешний значок.
- Аронс М.М., Хэтфилд К.М., Редди С.С., Кимбалл А., Джеймс А., Джейкобс Дж.Р. Пресимптомные инфекции SARS-CoV-2 и передача в учреждении квалифицированного сестринского ухода. N Engl J Med . 2020 28 мая; 382: 2081–90. doi: 10.1056 / NEJMoa2008457 внешний значок.
- Ли Р., Пей С., Чен Б. и др. Существенная недокументированная инфекция способствует быстрому распространению нового коронавируса (SARS-CoV-2). Наука . 2020 1 мая; 368 (6490): 489–93. http://www.doi.org/10.1126/science.abb3221внешний значок.
- Wu Z, McGoogan JM. Характеристики и важные уроки вспышки коронавирусного заболевания 2019 г. (COVID-19) в Китае: сводка отчета о 72314 случаях, предоставленного Китайским центром по контролю и профилактике заболеваний. ЯМА . 2020 24 февраля; 323 (13): 1239–42. doi: 10.1001 / jama.2020.2648 внешний значок.
- Стокс Е.К., Самбрано Л.Д., Андерсон К.Н. и др. Эпиднадзор за случаями коронавируса в 2019 г. — США, 22 января — 30 мая 2020 г. MMWR . 2020 июня 19; 69: 759–765. doi: 10.15585 / mmwr.mm6924e2 внешний значок.
- Zhou F, Yu T, Du R, et al. Клиническое течение и факторы риска смертности взрослых пациентов с COVID-19 в Ухане, Китай: ретроспективное когортное исследование. 2020 июн; 395: 1054–62.doi.org/10.1016/S0140-6736(20)30566-3 внешний значок.
- Ян Х, Ю Й, Сюй Дж и др. Клиническое течение и исходы тяжелобольных пациентов с пневмонией SARS-CoV-2 в Ухане, Китай: одноцентровое ретроспективное наблюдательное исследование. Ланцет Респир Мед . 2020 Apr; 8 (5): 475–81. http://www.doi.org/10.1016/S2213-2600(20)30079-5 Внешний значок.
- Биалек С., Баунди Э, Боуэн В. и др. Тяжелые исходы среди пациентов с коронавирусной болезнью 2019 (COVID-19) — США, 12 февраля — 16 марта 2020 г. MMWR . 2020 18 марта; 69: 343-6. doi: 10.15585 / mmwr.mm6912e2 внешний значок.
- Арентц М., Йим Э., Клафф Л. и др. Характеристики и исходы 21 тяжелобольного пациента с COVID-19 в штате Вашингтон. ЯМА . 2020 марта 19; 323 (16) 1612–4. doi: 10.1001 / jama.2020.4326 внешний значок.
- Ливингстон Э., Бухер К. Коронавирусная болезнь 2019 (COVID-19) в Италии. ЯМА . 2020 17 марта; 323 (14): 1335. doi: 10.1001 / jama.2020.4344 внешний значок.
- Джексон BR et al., Предикторы при поступлении ИВЛ и смерти в наблюдательной когорте взрослых, госпитализированных с COVID-19. Клинические инфекционные болезни . 2020 сен 24; ciaa1459. DOI: 10.1093 / cid / ciaa1459 внешний значок.
- Чоу Н., Флеминг-Дутра К., Гирке Р. и др. Предварительные оценки распространенности отдельных основных состояний здоровья среди пациентов с коронавирусным заболеванием, 2019 г. — США, 12 февраля — 28 марта 2020 г. MMWR . 2020 31 марта; 69: 382–6.doi: 10.15585 / mmwr.mm6913e2 внешний значок.
- To KK, Hung IF, Ip JD и др. Повторное заражение COVID-19 филогенетически отличным штаммом SARS-коронавируса-2 подтверждено секвенированием всего генома. Клин Инфекция Дис . 2020 Aug 25; ciaa1275. DOI: 10.1093 / cid / ciaa1275 внешний значок.
- Тиллетт Р., Севинский Дж., Хартли П. и др. Геномные доказательства в случае повторного заражения SARS-CoV-2. ССРН . 2020 31 августа. Доступно по адресу: https://ssrn.com/abstract=3680955. DOI: 10.2139 / ssrn.3680955 внешний значок.
- Van Elslande JV, Vermeersch P, Vandervoort K, et al. Симптоматическая реинфекция SARS-CoV-2 филогенетически отличным штаммом. Клинические инфекционные болезни . 2020 сен 5; ciaa1330. DOI: 10.1093 / cid / ciaa1330 внешний значок.
- Young BE, Ong SWX, Kalimuddin S, et al. Эпидемиологические особенности и клиническое течение пациентов, инфицированных SARS-CoV-2 в Сингапуре. ЯМА . 2020 3 марта; 323 (15): 1488–94. doi: 10.1001 / jama.2020.3204 внешний значок.
- Чжао Дж., Юань Ц., Ван Х. и др. Ответы антител на SARS-CoV-2 у пациентов с новым коронавирусным заболеванием 2019 г. Clin Infect Dis . 2020 28 мая. Doi: 10.1093 / cid / ciaa344external icon.
- Чжан В., Ду РХ, Ли Б. и др. Молекулярное и серологическое исследование пациентов, инфицированных 2019-nCoV: наличие нескольких путей выделения. Emerg Microbes Infect . 2020 7 февраля; 9: 386–9. DOI: 10.1080 / 22221751.2020.1729071 внешний значок.
- Го Л., Рен Л., Ян С. и др.Профилирование раннего гуморального ответа для диагностики нового коронавирусного заболевания (COVID-19). Клин Инфекция Дис . 2020 август; 71 (15): 778–85. DOI: 10.1093 / cid / ciaa310 внешний значок.
- Ван В., Сюй И, Гао Р. и др. Обнаружение SARS-CoV-2 в различных типах клинических образцов. ЯМА . 2020 11 марта; 323 (18): 1843-33. doi: 10.1001 / jama.2020.3786 внешний значок.
- То К.К., Цанг О.Т., Леунг В.С. и др. Временные профили вирусной нагрузки в образцах слюны задней части ротоглотки и ответы сывороточных антител во время инфекции SARS-CoV-2: наблюдательное когортное исследование. Ланцет Infect Dis . 2020 Май; 20 (5): 565–74. DOI: 10.1016 / S1473-3099 (20) 30196-1 внешний значок.
- Мохаммади А., Эсмаилзаде Э., Ли Й., Бош Р. Дж., Ли Дж. Обнаружение SARS-CoV-2 в различных респираторных участках: систематический обзор и метаанализ. EBioMedicine . 2020 Сен; 59 (102903). doi: 10.1016 / j.ebiom.2020.102903 внешний значок.
- Чжан Ц., Ши Л., Ван Ф.С. Травма печени при COVID-19: управление и проблемы. Ланцет Гастроэнтерол Гепатол . 2020 Май; 5: 428–30.DOI: 10.1016 / S2468-1253 (20) 30057-1 внешний значок.
- Чен В., Лан И, Юань Х и др. Обнаруживаемая вирусная РНК 2019-nCoV в крови является убедительным показателем дальнейшей клинической тяжести. Emerg Microbes Infect. 2020 25 февраля; 9: 469–73. DOI: 10.1080 / 22221751.2020.1732837 внешний значок.
- Ding Q, Lu P, Fan Y, Xia Y, Liu M. Клинические характеристики пациентов с пневмонией, коинфицированных новым коронавирусом 2019 года и вирусом гриппа, в Ухане, Китай. J Med Virol . 2020 20 марта; 92 (9): 1549-1555.doi: 10.1002 / jmv.25781 внешний значок.
- Tang N, Li D, Wang X, Sun Z. Аномальные параметры коагуляции связаны с плохим прогнозом у пациентов с новой коронавирусной пневмонией. J Thromb Haemost. 2020 19 февраля; 18 (4). doi: 10.1111 / jth.14768 внешний значок.
- Американский венозный форум. Рекомендации по профилактике и лечению ВТЭ у пациентов с COVID-19. 2020. По состоянию на апрель 2020 г. по адресу https://www.veinforum.org/covid-19external icon.
- Цинь Ц., Чжоу Л., Ху З. и др.Нарушение регуляции иммунного ответа у пациентов с COVID-19 в Ухане, Китай. Клин Инфекция Дис . 2020 марта 12; 71 (15): 762–8). DOI: 10.1093 / cid / ciaa248 внешний значок.
- Ши Х, Хан Х, Цзян Н. и др. Радиологические данные 81 пациента с пневмонией COVID-19 в Ухане, Китай: описательное исследование. Ланцет Infect Dis . 2020 апр; 20: 425–34. DOI: 10.1016 / S1473-3099 (20) 30086-4 внешний значок.
- Ай Т, Ян З, Хоу Х и др. Корреляция КТ грудной клетки и ОТ-ПЦР при коронавирусной болезни 2019 (COVID-19) в Китае: отчет о 1014 случаях. Радиология . 2020 26 февраля; 296 (2): E32 – E40. doi: 10.1148 / radiol.2020200642 внешний значок.
- Bernheim A, Mei X, Huang M и др. Результаты компьютерной томографии грудной клетки при коронавирусной болезни-19 (COVID-19): зависимость от продолжительности заражения. Радиология . 2020 20 февраля; 295 (3): 685–91. doi: 10.1148 / radiol.2020200463 внешний значок.
- Lei J, Li J, Li X, Qi X. КТ-изображение нового коронавируса 2019 г. (2019-nCoV) пневмонии 90 415. Радиология . 2020 31 января; 295 (1): 18. DOI: 10.1148 / радиол.2020200236 внешний значок.
- Ши Х, Хан Х, Чжэн С. Эволюция проявлений КТ у пациента, перенесшего пневмонию, вызванную новым коронавирусом (2019-nCoV) 2019 г., в Ухане, Китай. Радиология . 2020 7 февраля; 295 (1): 20. doi: 10.1148 / radiol.2020200269 внешний значок.
- Wang Y, Dong C, Hu Y, et al. Временные изменения результатов КТ у 90 пациентов с пневмонией COVID-19: продольное исследование. Радиология . 2020 марта 19; 296 (2): E55 –- E64. doi: 10.1148 / radiol.2020200843 внешний значок.
- Xu X, Yu C, Qu J, et al. Визуализация и клинические особенности пациентов с новым коронавирусом 2019 года SARS-CoV-2. Eur J Nucl Med Mol Imaging . 2020 28 февраля; 47: 1275–80. doi: 10.1007 / s00259-020-04735-9 внешний значок.
- Ян В., Цао Ц., Цинь Л. и др. Клинические характеристики и визуальные проявления новой коронавирусной болезни 2019 года (COVID-19): многоцентровое исследование в городе Вэньчжоу, Чжэцзян, Китай. J Заражение . 2020 Апрель; 80 (4): 388–93. DOI: 10.1016 / j.jinf.2020.02.016 внешний значок.
- Чжао В., Чжун З., Се Х, Ю Ку, Лю Дж. Связь между результатами компьютерной томографии грудной клетки и клиническими условиями коронавирусной болезни (COVID-19). Пневмония: многоцентровое исследование. Ам Дж. Рентгенол . 2020 Май; 214 (5): 1072–7. doi: 10.2214 / AJR.20.22976 внешний значок.
- Пан Ф, Йе Т, Сан П. и др. Динамика изменений легких на КТ грудной клетки во время выздоровления от пневмонии, вызванной новым коронавирусом (COVID-19) 2019 г. Радиология . 2020 13 февраля; 295 (3): 715–21. DOI: 10.1148 / радиол.2020200370 внешний значок.
- Bai HX, Hsieh B, Xiong Z и др. Работа радиологов по дифференциации COVID-19 от вирусной пневмонии на КТ грудной клетки. Радиология . 10 марта 2020 г .; 296 (2): E46 – E54. doi: 10.1148 / radiol.2020200823 внешний значок.
- Xie X, Zhong Z, Zhao W, Zheng C, Wang F, Liu J. КТ грудной клетки при типичной пневмонии 2019-nCoV: связь с отрицательным тестом RT-PCR. Радиология . 12 февраля 2020 г .; 296 (2): E41 – E45. doi: 10.1148 / radiol.2020200343 внешний значок.
- Го Т., Фан И., Чен М. и др. Сердечно-сосудистые последствия летальных исходов пациентов с коронавирусной болезнью 2019 (COVID-19). Джама Кардиол . 2020 27 марта; 5 (7): 811–818. DOI: 10.1001 / jamacardio.2020.1017 внешний значок.
- Inciardi RM, Lupi L, Zaccone G и др. Вовлечение сердца у пациента с коронавирусной болезнью 2019 (COVID-19). Джама Кардиол . 2020 марта 27; 5 (7): 811–8. DOI: 10.1001 / jamacardio.2020.1017 внешний значок.
- Ши С., Цинь М., Шен Б. и др.Ассоциация сердечной травмы со смертностью у госпитализированных пациентов с COVID-19 в Ухане, Китай. Джама Кардиол . 2020 25 марта; 5 (7): 802–10. DOI: 10.1001 / jamacardio.2020.0950 внешний значок.
- Клок, ФА; Круип, MJHA; ван дер Меер NJM et al. Частота тромботических осложнений у тяжелобольных пациентов интенсивной терапии с COVID-19. Исследование тромбоза . 2020 июл; 191: 145–7. doi: 10.1016 / j.thromres.2020.04.013 внешний значок.
- Хелмс, Дж; Таккард, C; Северак, Ф. и др.Высокий риск тромбоза у пациентов с тяжелой инфекцией SARS-CoV-2: многоцентровое проспективное когортное исследование. Медицина интенсивной терапии . 2020 4 мая; 46 (6): 1089–8. DOI: 10.1007 / s00134-020-06062-x внешний значок.
- Grillet, F; Бер, Дж; Calame, H et al. Острая легочная эмболия, связанная с пневмонией COVID-19, обнаруженная с помощью легочной КТ-ангиографии. Радиология 2020 . 23 апреля; 296 (3): E186 – E188. doi: 10.1148 / radiol.2020201544 внешний значок.
- Оксли, Т; Мокко, Дж; Маджиди, С. и др.Инсульт крупных сосудов как признак Covid-19 у молодых. N Engl J Med . 2020 28 апреля; 382: e60. doi: 10.1056 / NEJMc2009787 внешний значок.
- Li, Y; Ван, М; Zhou, Y et al. Острое цереброваскулярное заболевание после COVID-19: единый центр, ретроспективное, обсервационное исследование. Инсульт Vasc Neurol . 2020 2 июля; 5 (3): e000431. doi: 10.1136 / svn-2020-000431 внешний значок.
- Margo, C; Mulvey, J; Берлин, Д. и др. Связанное с комплементом микрососудистое повреждение и тромбоз в патогенезе тяжелой инфекции COVID-19: отчет о пяти случаях. Трансляционные исследования . 2020 июн; 220: 1–13. doi: 10.1016 / j.trsl.2020.04.007 внешний значок.
- Мерад, М., Мартин, Дж. К. Патологическое воспаление у пациентов с COVID-19: ключевая роль моноцитов и макрофагов. Нат Рев Иммунол . 2020 6 мая; 20: 355–62. doi: 10.1038 / s41577-020-0331-4 внешний значок.
- Ассакер, Рита и др. Симптомы COVID-19 у детей: метаанализ опубликованных исследований. Британский журнал анестезии . 2020 Сен; 125 (3): E330 – E332.doi: 10.1016 / j.bja.2020.05.026 внешний значок.
- Poline et al. Систематический скрининг на SARS-CoV-2 у детей при госпитализации: проспективное многоцентровое исследование во Франции. Клиническая инфекционная болезнь . 25 июля 2020 г .: ciaa1044. DOI: 10.1093 / cid / ciaa1044 внешний значок.
- Dong Y, Mo X, Hu Y и др. Эпидемиология COVID-19 среди детей в Китае. Педиатрия .2020 июнь doi: 10.1542 / peds.2020-0702external icon.
- Foster CE, Moulton EA, Munoz FM, et al.Коронавирусная болезнь 2019 у детей, находящихся на попечении в детской больнице Техаса: начальные клинические характеристики и результаты. Журнал Общества детских инфекционных болезней .2020 6 июня; 9 (3): 373–7. doi: 10.1093 / jpids / piaa072 внешний значок.
- Xu H, Liu E, Xie J, et al. Последующее исследование детей, инфицированных SARS-CoV-2, из Западного Китая. Анналы трансляционной медицины . 2020 Май; 8 (10): 623. doi: 10.21037 / atm-20-3192 внешний значок.
- Шекердемиан Л.С., Махмуд Н.Р., Вулф К.К. и др.Характеристики и исходы у детей с инфекцией коронавируса 2019 (COVID-19), поступивших в отделения детской интенсивной терапии США и Канады. JAMA Педиатрия . 2020 11 мая; 174 (9): 868–73. DOI: 10.1001 / jamapediatrics.2020.1948 внешний значок.
- Mannheim J, Gretsch S, Layden JE, Fricchione MJ. Характеристики госпитализированных случаев заболевания COVID-19 у детей — Чикаго, Иллинойс, март – апрель 2020 г. J Pediatric Infect Dis Soc . 2020 июн 1; piaa070. doi: 10.1093 / jpids / piaa070 внешний значок.
- Ким Л., Уитакер М., О’Халлоран А. и др. Частота госпитализаций и характеристики детей в возрасте <18 лет, госпитализированных с лабораторно подтвержденным COVID-19 - COVID-NET, 14 штатов, 1 марта - 25 июля 2020 г. MMWR . 2020 14 августа; 69 (32): 1081–88. doi: 10.15585 / mmwr.mm6932e3 внешний значок.
- Bellino S, et al. Факторы риска серьезности заболевания COVID-19 для педиатрических пациентов в Италии. Педиатрия . 2020 Октябрь; 146 (4): e2020009399. doi: 10.1542 / peds.2020-009399 внешний значок.
- Хорби, Питер и др. Дексаметазон у госпитализированных пациентов с Covid-19 — предварительный отчет. N Engl J Med . 2020 17 июля. Doi: 10.1056 / NEJMoa2021436внешняя иконка.
- Люкс AM, Свенсон ER. Пульсоксиметрия для мониторинга пациентов с COVID-19 в домашних условиях. Возможные подводные камни и практическое руководство. Ann Am Thorac Soc. 2020 Сен; 17 (9): 1040-1046. DOI: 10.1513 / AnnalsATS.202005-418FR Внешний значок
- Филип Кейдж, Беннетт Б., Фуллер С. и др. Точность пульсоксиметрии у пациентов с COVID-19, покидающих отделение интенсивной терапии: клиническая оценка.BMJ Open Respir Res. 2020 Декабрь; 7 (1): e000778. DOI: 101136 / bmjresp-2020-000778 внешний значок
- Джубран А., Тобин М.Дж. Надежность пульсовой оксиметрии при титровании дополнительной кислородной терапии у пациентов, зависимых от искусственной вентиляции легких. Грудь. 1990 июн; 97 (6): 1420-5.doi: 10.1378 / сундук.97.6.1420 внешний значок
- Cahan C, Decker MJ, Hoekje PL, Strohl KP. Соглашение между неинвазивными оксиметрическими показателями насыщения кислородом. Грудь. 1990 апр; 97 (4): 814-9.doi: 10.1378 / сундук.97.4.814 внешний значок
- Bickler PE, Feiner JR, Severinghaus JW.Влияние пигментации кожи на точность пульсоксиметра при низкой насыщенности. Анестезиология. 2005 апр; 102 (4): 715-9. Doi: 10.1097 / 00000542-200504000-00004 внешний значок
- Feiner JR, Severinghaus JW, Bickler PE. Темная кожа снижает точность пульсоксиметров при низком насыщении кислородом: влияние типа датчика оксиметра и пола. Anesth Analg. 2007 декабрь; 105 (6 доп.): S18-23. DOI: 10.1213 / 01.ane.0000285988.35174.d9 Внешний значок
- Сджодинг М.В., Диксон Р.П., Ивашина Т.Дж. и др. Расовые предубеждения в измерениях пульсовой оксиметрии. N Engl J Med. 2020 17 декабря; 383 (25): 2477-2478. doi: 10.1056 / NEJMc2029240 внешний значок
- Гальван Касас С., Катала А, Карретеро Эрнандес Дж. И др. Классификация кожных проявлений COVID-19: быстрое проспективное общенациональное консенсусное исследование в Испании с 375 случаями. Br J Dermatol. 2020 июл; 183 (1): 71-77.doi: 10.1111 / bjd.19163external icon
- Фахми Д.Х., Эль-Амави Х.С., Эль-Самонги Массачусетс и др. COVID-19 и дерматология: подробное руководство для дерматологов. J Eur Acad Dermatol Venereol.2020 июл; 34 (7): 1388-1394.doi: 10.1111 / jdv.16545external icon
- Freeman EE, McMahon DE, Lipoff JB и др. Пернио-подобные поражения кожи, связанные с COVID-19: серия случаев с участием 318 пациентов из 8 стран. J Am Acad Dermatol. 2020; 83 (2): 486-492.doi: 10.1016 / j.jaad.2020.05.109 внешний значок
- Сушонванит П., Леерунякул К., Коситкулйорн С. Кожные проявления при COVID-19: уроки, извлеченные из текущих данных. J Am Acad Dermatol. 2020; 83 (1): e57-e60.doi: 10.1016 / j.jaad.2020.04.094 внешний значок
- De Giorgi V, Recalcati S, Jia Z и др. Кожные проявления, связанные с коронавирусной болезнью 2019 (COVID-19): проспективное исследование из Китая и Италии. J Am Acad Dermatol. 2020; 83 (2): 674-675. DOI: 10.1016 / j.jaad.2020.05.073 внешний значок
- Цзя Дж. Л., Камцева М., Рао С. А., Линос Э. Кожные проявления COVID-19: предварительный обзор. J Am Acad Dermatol. 2020 авг; 83 (2): 687-690.doi: 10.1016 / j.jaad.2020.05.059внешняя иконка
- Рекалкати С. Кожные проявления COVID-19: первая перспектива.J Eur Acad Dermatol Venereol. 2020 Май; 34 (5): e212-e213.doi: 10.1111 / jdv.16387external icon
- Данешгаран Г., Дубин Д.П., Гулд DJ. Кожные проявления COVID-19: обзор, основанный на фактах. Am J Clin Dermatol. 2020; 21 (5): 627-639. doi: 10.1007 / s40257-020-00558-4. doi: 10.1007 / s40257-020-00558-4 внешний значок
- де Массон А., Буазиз Дж. Д., Сулимович Л. и др. Обморожения — частая находка на коже во время пандемии COVID-19: ретроспективное общенациональное исследование, проведенное во Франции. J Am Acad Dermatol.2020; 83 (2): 667-670.doi: 10.1016 / j.jaad.2020.04.161 внешний значок
- Сачдева М., Джанотти Р., Шах М. и др. Кожные проявления COVID-19: отчет о трех случаях и обзор литературы. J Dermatol Sci. 2020; 98 (2): 75-81.doi: 10.1016 / j.jdermsci.2020.04.011 внешний значок
- Freeman EE, McMahon DE, Lipoff JB и др. Спектр дерматологических проявлений, связанных с COVID-19: международный регистр 716 пациентов из 31 страны. J Am Acad Dermatol. 2020 Октябрь; 83 (4): 1118-1129.DOI: 10.1016 / j.jaad.2020.06.1016 внешний значок
- Türsen Ü, Türsen B, Lotti T. Кожные побочные эффекты потенциальных препаратов COVID-19. Dermatol Ther. 2020 июл; 33 (4): e13476. DOI: 10.1111 / dth.13476. Epub 2020 22 мая. Doi: 10.1111 / dth.13476 внешний значок
- Avanzato AA, Matson MJ, Seifert SN, et al. Пример из практики: длительное инфекционное выделение SARS-CoV-2 у бессимптомного пациента с ослабленным иммунитетом и раком. Cell 2020 23 декабря; 183 (1–12) .doi: 10.1016 / j.cell.2020.10.049 внешний значок
- Aydillo T, Gonzalez-Reiche AS, Aslam S, et al.Выделение жизнеспособного SARS-CoV-2 после иммуносупрессивной терапии рака. N Engl J Med. 2020 24 декабря; 383 (26): 2586-2588.doi: 10.1056 / NEJMc2031670 внешний значок
- Баанг Дж. Х., Смит С., Мирабелли С. и др. Длительная репликация коронавируса 2 тяжелого острого респираторного синдрома у пациента с ослабленным иммунитетом. J Infect Dis. 2021, 4 января; 223 (1): 23-27. DOI: 10.1093 / infdis / jiaa666 внешний значок
- Чой Б., Чоудхари М.К., Реган Дж. И др. Стойкость и эволюция SARS-CoV-2 у хозяина с ослабленным иммунитетом.N Engl J Med. 2020 3 декабря; 383 (23): 2291-2293.doi: 10.1056 / NEJMc2031364 внешний значок
- Tarhini H, Recoing A, Bridier-Nahmias A, et al. Длительная инфекционность SARS-CoV-2 среди трех пациентов с ослабленным иммунитетом: от длительного выделения вируса до суперинфекции SARS-CoV-2. J Infect Dis. 2021, 8 февраля: jiab075. doi: 10.1093 / infdis / jiab075 внешний значок. Онлайн до печати.
- Nonaka CKV, Франко М.М., Граф Т. и др. Геномные доказательства случая повторного заражения SARS-CoV-2 спайковой мутацией E484K в Бразилии.Препринты 2021, 2021010132. doi: 10.20944 / preprints202101.0132.v1 внешний значок
- Naveca F, da Costa C, Nascimento V, et al. Повторное заражение SARS-CoV-2 новым вызывающим беспокойство вариантом (VOC) P.1 в Амазонасе, Бразилия. Препринт. Опубликовано 18 января 2021 г. https://virological.org/t/sars-cov-2-reinfection-by-the-new-variant-of-concern-voc-p-1-in-amazonas-brazil/596external icon
- Resende PC, Bezerra JF, de Vasconcelos RHT и др. Мутация Spike E484K в первом случае повторного заражения подтверждена в Бразилии, 2020.Препринт. Опубликовано 10 января 2021 г. https://virological.org/t/spike-e484k-mutation-in-the-first-sars-cov-2-reinfection-case-confirmed-in-brazil-2020/584external icon
- Харрингтон Д., Келе Б., Перейра С. и др. Подтверждено повторное заражение SARS-CoV-2, вариант VOC-202012/01. Clin Infect Dis. 2021, 9 января: ciab014. DOI: 10.1093 / cid / ciab014 внешний значок. Онлайн до печати.
- Zucman N, Uhel F, Descamps D, Roux D, Ricard JD. Тяжелая реинфекция южноафриканским вариантом 501Y SARS-CoV-2.V2: Отчет о случае. Clin Infect Dis. 2021, 10 февраля: ciab129. DOI: 10.1093 / cid / ciab129 внешний значок. Онлайн до печати.
- Вибмер СК, Эйрес Ф., Херманус Т. и др. SARS-CoV-2 501Y.V2 ускользает от нейтрализации южноафриканской донорской плазмой COVID-19. Препринт. bioRxiv. 2021; 2021.01.18.427166. Опубликовано 19 января 2021 г. doi: 10.1101 / 2021.01.18.427166 внешний значок
Клинических вопросов о COVID-19: вопросы и ответы
1. Если медицинские работники вылечились от инфекции SARS-CoV-2, но подверглись высокому риску заражения в течение 3 месяцев после первоначального заражения пациенту с SARS-CoV- 2, следует ли ограничивать их работу в течение 14 дней после заражения?
CDC опубликовал временное руководство по оценке рисков и ограничениям работы для медицинских работников с потенциальным воздействием SARS-CoV-2.Из-за их часто обширного и тесного контакта с людьми, которые подвержены высокому риску тяжелого заболевания, в этом руководстве рекомендуется консервативный подход к мониторингу медицинских работников и применению ограничений на работе для предотвращения передачи инфекции от потенциально заразных медицинских работников пациентам, другим медицинским работникам и посетителям. Обзор имеющихся в настоящее время данных показывает, что большинство людей не заражаются повторно в течение 3 месяцев после заражения SARS-CoV-2. Тестирование бессимптомных людей в течение этого 3-месячного периода осложняется тем фактом, что у некоторых людей в этот период обнаруживается вирус от их предшествующей инфекции; положительный результат теста в этот период может быть более вероятным результатом предыдущей инфекции, чем новой инфекции, которая представляет риск передачи.
В свете этого, зараженные медицинские работники, которые находятся в течение 3 месяцев с момента их первоначального заражения, могут продолжать работать, отслеживая симптомы, соответствующие COVID-19, и соблюдая все рекомендуемые методы профилактики и контроля инфекций (например, универсальное использование подходящих управления источником). Если симптомы развиваются, необходимо обследовать подвергшихся воздействию медработников и, возможно, протестировать их на SARS-CoV-2, если не установлена альтернативная этиология. Некоторые учреждения могут по-прежнему принять решение ввести ограничения на работу для бессимптомных медицинских работников после повышенного риска, особенно если есть неуверенность в отношении предшествующей инфекции или устойчивости иммунного ответа человека.Примеры могут включать:
- Медицинские работники с базовыми иммунодефицитными состояниями (например, после трансплантации органов) или с ослабленным иммунитетом (например, получают химиотерапию) в течение 3 месяцев после заражения SARS-Cov-2, которые могут подвергаться повышенному риску повторного заражения. Однако данные о том, какие конкретные условия могут привести к более высокому риску, и масштабы риска отсутствуют.
- HCP, у которых есть опасения, что их первоначальный диагноз инфекции SARS-CoV-2 мог быть основан на ложноположительном результате теста (например,g. у пациента не было симптомов, положительный тест на антиген и подтверждающий тест амплификации нуклеиновых кислот (NAAT) не проводился).
- HCP, у которых есть доказательства того, что они подверглись воздействию нового варианта SARS-CoV-2, для которого риск повторного заражения может быть выше (например, контакт с человеком, который, как известно, инфицирован новым вариантом).
CDC продолжает активно исследовать частоту повторного заражения и обстоятельства, связанные с этими эпизодами, включая роль, которую новые варианты могут играть в повторном заражении, и при необходимости скорректирует рекомендации по мере поступления дополнительной информации.
2. Если у медицинского работника в течение 3 месяцев после первоначального заражения появятся симптомы, соответствующие COVID-19, следует ли отстранить их от работы и пройти повторное обследование?
Медицинский работникв течение 3 месяцев после подтвержденной инфекции SARS-CoV-2, у которого развиваются симптомы, соответствующие COVID-19, следует обследовать, чтобы определить потенциальную альтернативную этиологию их симптомов. Если не удается определить альтернативную этиологию симптомов, может потребоваться повторное тестирование на инфекцию SARS-CoV-2 с пониманием того, что положительный вирусный тест может представлять собой остаточные вирусные частицы от предыдущей инфекции, а не новую инфекцию.Решения о необходимости и продолжительности отстранения от работы должны основываться на предполагаемом диагнозе (например, грипп, инфекция SARS-CoV-2).
3. Должны ли медицинские работники в течение 3 месяцев после первоначального заражения носить все рекомендованные средства индивидуальной защиты (СИЗ) при уходе за пациентами с подозрением или подтвержденной инфекцией SARS-CoV-2? Например, если количество респираторов ограничено, следует ли отдавать предпочтение респираторам медицинским работникам, которые ранее не были инфицированы?
Независимо от подозреваемого или подтвержденного иммунитета, медицинский персонал должен всегда носить все рекомендованные СИЗ при уходе за пациентами.В ситуациях нехватки СИЗ предприятиям следует обращаться к стратегиям CDC по оптимизации поставок СИЗ. Однако, как и в случае с другими инфекционными заболеваниями (например, корью), распределение доступных СИЗ не должно основываться на том, были ли медицинские работники ранее инфицированы или есть доказательства иммунитета.
4. Следует ли в течение 3 месяцев после первоначального заражения назначать медицинский работник для оказания помощи пациентам с подозрением или подтвержденной инфекцией SARS-CoV-2?
Хотя у людей, выздоровевших от инфекции SARS-CoV-2, может развиться некоторый защитный иммунитет, продолжительность и степень такого иммунитета неизвестны.Кадровые решения должны основываться на обычной практике учреждения. Любой медицинский работник, назначенный для лечения пациентов с подозрением или подтвержденной инфекцией SARS-CoV-2, независимо от истории инфекции, должен соблюдать все рекомендуемые методы профилактики и контроля инфекций при оказании помощи. Также доступно руководство по сокращению нехватки персонала.
Критерии расследования предполагаемых случаев повторного инфицирования SARS-CoV-2 (ICR)
CDC осведомлены о недавних сообщениях о предполагаемых случаях повторного заражения SARS-CoV-2 среди лиц, у которых ранее был диагностирован COVID-19 [1–3] .В настоящее время нет общепринятого определения того, что представляет собой повторное заражение SARS-CoV-2, и в отчетах используются различные методы тестирования, что затрудняет диагностику повторного заражения. Для выработки общего понимания того, что представляет собой повторное инфицирование SARS-CoV-2, CDC предлагает использовать оба
1) критерии исследования для выявления случаев с более высоким индексом подозрения на повторное заражение и
2) геномное тестирование парных образцов .
изучил соответствующие периоды времени после первоначального заражения или заболевания SARS-CoV-2 для расследования повторного заражения.С августа 2020 года CDC рекомендовал против необходимости повторного тестирования людей с бессимптомной инфекцией в течение 90 дней после первой инфекции или заболевания SARS-CoV-2, поскольку данные на сегодняшний день предполагают, что повторное инфицирование не происходит в течение этого временного окна (Руководство CDC о продолжительности изоляции и мерах предосторожности для взрослых с COVID-19).
В настоящее время мы предлагаем два временных окна для расследования, как указано ниже:
- Для людей с COVID-19 или без него — подобных симптомов ≥90 дней после первоначального заражения / заболевания; и
- Для людей с COVID-19 — подобных симптомов 45–89 дней после первоначального заражения / заболевания.
Для лиц с обнаружением РНК SARS-CoV-2 в образце респираторных органов через ≥90 дней после их первой лабораторно подтвержденной инфекции / заболевания SARS-CoV-2 мы применяем стандартный набор критериев, подробно описанных ниже. Также важно расследование очень подозрительных случаев, похожих на COVID-19, в течение 45–89-дневного периода. Однако мы предлагаем более строгие критерии для отбора случаев в этот более ранний период времени, используя более высокий индекс подозрения на повторное заражение. Если будут обнаружены доказательства повторного заражения в течение этого временного окна, это послужит дополнительной информацией для будущих профилактических мероприятий и разработки рекомендаций.
CDC отмечает, что повторное заражение SARS-CoV-2 является быстро развивающейся областью исследований. Этот первоначальный набор предложенных критериев может не охватить всех случаев повторного заражения; мы предлагаем эти начальные критерии исследования, чтобы лучше понять возможность повторного заражения. Этот первоначальный набор предложенных критериев будет уточнен, если новые доказательства предложат другие способы расследования с целью создания стандартизированного определения случая повторного заражения SARS-CoV-2.
- Расследование дел, соответствующих критерию A или B
- Для лиц с обнаружением РНК SARS-CoV-2 ≥90 дней с момента первого заражения SARS-CoV-2
Лица с обнаружением РНК SARS-CoV-2 * ≥90 дней после первого обнаружения SARS-CoV- 2 РНК, независимо от наличия симптомов
И
Доступны парные респираторные образцы (по одному от каждого эпизода инфекции)
* Если обнаружено с помощью ОТ-ПЦР, включать, только если значение Ct <33 или если значение Ct недоступно - Для людей с симптомами, подобными COVID-19 и обнаружением РНК SARS-CoV-2 45–89 дней с момента первой инфекции SARS-CoV-2
Лица с обнаружением РНК SARS-CoV-2 * ≥45 дней после первое обнаружение РНК SARS-CoV-2
И
С симптоматическим вторым эпизодом и без очевидной альтернативной этиологии для COVID-19-подобных симптомов OR тесный контакт с человеком, у которого лабораторно подтвержден COVID-19
AND
Доступны парные респираторные образцы (по одному от каждого эпизода инфекции) * Если обнаружено с помощью ОТ-ПЦР, включать только в том случае, если значение Ct <33 или значение Ct недоступно.
В условиях ограниченных возможностей геномного тестирования CDC предлагает уделять первоочередное внимание обследованию людей в временном окне ≥90 дней, поскольку более длительный интервал времени между первым и вторым заражением может иметь более высокое подозрение на повторное заражение.
- Для лиц с обнаружением РНК SARS-CoV-2 ≥90 дней с момента первого заражения SARS-CoV-2
- Выбор лабораторных тестов для проведения
Геномное секвенирование парных образцов, отвечающих приведенным ниже критериям качества, необходимо для исследования реинфекции. Один только анализ однонуклеотидного полиморфизма может быть или не может быть достаточным, чтобы отличить реинфекцию от длительного шеддинга, поскольку вариации скорости мутации SARS-CoV-2 внутри хозяина плохо изучены.Однако идентификация парных образцов из разных линий (как определено в Nextstrain или GISAID) служит доказательством более высокого качества для повторного заражения SARS-CoV-2. Критерии качества тестирования и уровни доказательств более подробно описаны ниже. Геномное тестирование должно соответствовать всем следующим критериям качества для расследования повторного заражения SARS-CoV-2:
- Для достижения консенсуса рекомендуется охват генома> 100 / на базовую позицию
- Оценка Q консенсуса> 30 при покрытии 99% генома
- Для анализа малых вариаций рекомендуется 1000-кратное среднее покрытие генома
- Удаление загрязнения праймера ампликона из сборки
Дополнительно:
- Использование платформ высокоточного секвенирования (оценка Q на чтение> 30) предпочтительно для достижения консенсуса
- Если используются платформы секвенирования с низкой точностью (оценка Q на чтение <30), рекомендуется проверка SNP с помощью альтернативного метода секвенирования.
Уровень доказательности реинфекций с использованием геномных данных следующий:
Лучшее свидетельство
Различные группы SARS-CoV-2, определенные в Nextstrain и GISAID, между первой и второй инфекцией, в идеале в сочетании с другими доказательствами фактического заражения (например,g., высокие титры вируса в каждом образце, положительный результат на sgmRNA или культуру)
Умеренные доказательства
> 2 нуклеотидных различий в месяц * в консенсусе между последовательностями, которые соответствуют показателям качества, указанным выше, в идеале в сочетании с другими доказательствами фактической инфекции (например, высокие титры вируса в каждом образце, положительный результат на sgmRNA или культуру)
Слабые доказательства, но возможны
≤2 нуклеотидных различий в месяц * консенсуса между последовательностями, которые соответствуют указанным выше показателям качества, или> 2 нуклеотидных различий в месяц * консенсуса между последовательностями, которые не соответствуют указанным выше показателям качества, в идеале в сочетании с другими доказательствами фактического заражения ( е.g., высокие титры вируса в каждом образце, положительный результат на sgmRNA или культуру)
* Скорость мутации SARS-CoV-2 оценивается в 2 нуклеотидных различия в месяц; таким образом, если подозрение на повторное инфицирование происходит через 90 дней после первоначального инфицирования, для умеренных доказательств потребуется> 6 нуклеотидных различий.
В настоящее время тестируются только парные образцы для определения повторного заражения, поскольку протоколов для определения повторного заражения от одного образца еще не существует .
Другая информация может предоставить подтверждающие, но не окончательные доказательства реинфекции, такие как посевы или анализ субгеномной мРНК (для выявления наличия репликационно-компетентного вируса) или серологические исследования, которые могут быть полезны для документирования серологического ответа на SARS-CoV- 2. Помимо лабораторных данных, другие подтверждающие доказательства реинфекции могут включать клиническое течение (симптомы, похожие на COVID-19) и эпидемиологические связи с подтвержденным случаем.
Доказательства передачи COVID-19 до появления симптомов
Существенные изменения:
1) SI должен сокращаться по мере того, как меры контроля становятся более строгими (более быстрое обнаружение контактов), но это не обсуждается, только немного странное удлинение инкубационного периода. Например, такое сокращение было заметно у Lipsitch et al., 2003 для SARS. Прокомментируйте пожалуйста.
Мы добавили цифры в стиле Кливленда и сравнили последовательные интервалы между ранней и поздней фазами (рис. 6), а также добавили обсуждение точки зрения рецензента в текст (раздел «Последовательные интервалы» в результатах). Необработанные серийные интервалы действительно сокращаются примерно на день в обоих местах в более поздних и ранних подмножествах данных. Мы также добавили анализ выживаемости, чтобы выяснить, может ли этот результат быть результатом усечения справа.При этом не было обнаружено существенной разницы между ранней и поздней стадиями, хотя это не исключает, что произошло укорочение. Мы процитировали статью Science.
Отчет № 42) Ferguson et al. (Отчет 4 Имперского колледжа о COVID) отметили ранее недооцененную предвзятость в ретроспективном отслеживании контактов, которая может увеличить количество коротких серийных интервалов или инкубационного периода. Актуальность этого исследования для меня неясна, но к нему следует обратиться.
представляет собой анализ показателя летальности, поэтому мы не уверены, что такое ранее недооцененная систематическая ошибка.Мы согласны с тем, что отслеживание контактов может быть предвзятым по ряду причин, в том числе в отношении близких контактов, которых люди, вероятно, смогут назвать, вспомнил воздействия, которые, скорее всего, были недавними, и правильное усечение — тот факт, что люди с более ранним проявлением симптомов наблюдается раньше (хотя это повлияет как на серийные интервалы, так и на инкубационные периоды). Мы подтверждаем в Приложении 1, что мы не учли эти эффекты, и прокомментировали это в Обсуждении. Мы также скорректировали усечение вправо в нашем новом анализе с учетом промежуточных случаев в оценках инкубационного периода (см. Ниже).
3) Похоже, что данные действительно в значительной степени поддерживают пресимптоматическую передачу. Могут ли авторы уточнить границы этого? Например, если последовательные интервалы и инкубационные периоды не коррелированы или положительно коррелированы, или если для каждого случая оценивается вероятность того, что передача была до появления симптомов, каков был бы результат с точки зрения фактической доли передачи до симптомов?
Это сложный и интересный вопрос.Фактически, одна из причин, по которой мы не выделяли наши предсимптоматические фракции больше в первой версии, заключалась в том, что мы знали, что вычитание независимых выборок из двух распределений не дает хорошей оценки распределения различий (только разница в значит, по линейности). Мы значительно разработали этот аспект работы, и теперь мы учитываем корреляции. Для этого мы оценили ковариацию (и корреляцию) серийного интервала и распределения инкубационного периода с использованием «прямых» выборок, т.е.е. как можно более прямо из данных. Затем мы совместно провели повторную выборку из наших оценочных распределений, учитывая этот уровень ковариации. Удивительно, но это не повлияло на часть отрицательных образцов (серийный интервал минус инкубационный период), как мы могли предположить. Они остаются высокими, и в Тяньцзине они выше, чем в Сингапуре. Анализ находится в конце раздела «Материалы и методы» и «Результаты», а метод выборки (на основе многомерных распределений с предельной гамма-плотностью) приведен в Приложении 1, подраздел «Предсимптоматическая передача: подробные сведения о методах».
4) Если предположить, что ответ на 3 — «много», как я подозреваю, здесь возникает парадокс — что Сингапур держал эпидемию под контролем в течение нескольких месяцев с помощью вмешательств в основном на основе случая, прежде чем она потерпела неудачу, ситуация, которая не могла произойти (I думаю), если большая часть передачи была бессимптомной. Эти два факта (анализ и контроль, продлившийся до начала апреля) кажутся противоречащими друг другу. Пожалуйста, обсудите.
Ответ на 3 действительно кажется «довольно много» — около половины или даже больше в новой Таблице 1.Мы согласны с тем, что это хороший момент, и добавили подробности в Обсуждение. По сути, мы не думаем, что предсимптоматическая передача обязательно делает вмешательства на основе случая неэффективными, если отслеживание контактов осуществляется тщательно и дополняется надежным выявлением случаев. В Сингапуре бессимптомные близкие контакты были помещены в превентивный карантин — мы подозреваем, что эта досимптомная передача в сообществе сводится к минимуму после выявления кластера. Мы цитируем Lee, Chiew and Khong, 2020, за усилия по сдерживанию.
Кроме того, если эффективное выявление случаев ограничивает количество симптоматической передачи, имеет смысл, что доля досимптомного распространения, которую мы обнаруживаем, будет выше, поскольку это представляет собой оставшуюся передачу, которая не была предотвращена.
5) Мы хотели бы немного подробнее обсудить удлинение инкубационного периода — может ли это просто означать, что до введения ограничений взаимодействие, определяемое как передающее, не было ответственным, но на самом деле передача произошла несколькими днями ранее, возможно, в более раннее взаимодействие двух людей? Было бы неплохо, если бы авторы могли прокомментировать, почему мы можем или не можем исключить такую возможность.
Да, мы подозреваем, что это должно быть связано с взаимодействиями, которые, как предполагается, ответственны за воздействие, неправильно распределенное для Тяньцзиня. Мы обновили данные и некоторые предположения, касающиеся воздействия, и теперь обнаруживаем, что разница между ранним и поздним сроком значительна только в Тяньцзине. Фактически это соответствует пре- или бессимптомной передаче; если люди контактировали с кем-то с симптомами, а затем подвергались контакту с человеком без симптомов (например, в условиях группового карантина), воздействие, вероятно, было бы связано с контактом до карантина, и временной интервал в данных не был бы образец инкубационного периода.Вместо этого это будет выборка из одного или нескольких поколений плюс инкубационный период — см. Ниже. Мы добавили обсуждение этого в раздел «Результаты инкубационного периода».
6) Основная проблема заключается в том, что, в отличие от метода, используемого для оценки серийного интервала, подход, используемый для оценки инкубационного периода, предполагает, что все случаи (и потенциальные инфекторы) были идентифицированы и подтверждены, и не допускает передачи от бессимптомных случаи. Это кажется особенно проблематичным для сингапурского набора данных, в котором все данные, по-видимому, относятся к госпитализированным случаям; таким образом, менее тяжелые случаи могли быть пропущены (если только все пациенты не были госпитализированы в качестве формы изоляции).В Тяньцзине неясно, были ли госпитализированы подтвержденные случаи, но кажется вероятным, что бессимптомные или легкие инфекции могли быть пропущены. Значительное увеличение предполагаемого инкубационного периода для «ранних» и «поздних» случаев предполагает, что контакт с бессимптомными / необнаруженными случаями, вероятно, искажает результаты, поскольку можно было бы ожидать большей распространенности и, следовательно, более высокого риска контакта с бессимптомными случаями случаи позже. Если бы между подтвержденным и предполагаемым индексным случаем был нераспознанный случай, предположительно, предполагаемый инкубационный период сократился бы примерно на 50% (по крайней мере).
Это хороший момент. См. Ответ на соответствующий вопрос:
7) Метод оценки серийного интервала, с другой стороны, действительно учитывает множественные (необнаруженные) поколения передачи между подтвержденными случаями в смешанной модели. Таким образом, эти два подхода делают разные предположения о потенциальном наличии / роли бессимптомных случаев. Кроме того, здесь нет реальной разработки методики. Авторы применяют к своим данным два различных установленных метода вместо того, чтобы представлять единую структуру для оценки инкубационного периода и серийного интервала (что было бы новым и значительно усилило бы анализ).
Мы представили еще один анализ, который, как нам кажется, является новым методом. Как отмечалось выше, если бы были неизвестные промежуточные продукты, то выбранный «инкубационный период» вместо этого был бы выборкой из суммы интервалов между поколениями: A заражает B, B заражает C,…, за которым следует инкубационный период: время C от воздействия до симптома начало. Предполагая, что инкубационный период и время генерации могут быть смоделированы как гамма-распределение, можно записать вероятность для времени от воздействия A (например, при событии или массовом скоплении) и появления симптомов C. Плотность — это свертка гамма-плотностей.Мы разработали новый анализ в этом направлении и действительно обнаружили более короткие инкубационные периоды, чем без промежуточных продуктов. Мы также обнаружили, что инкубационный период длиннее, чем время генерации, что дает альтернативный аргумент в пользу вывода о предсимптоматической передаче. Насколько нам известно, это в сочетании с описанным выше ковариационным анализом представляет собой новый методологический вклад.
8) Наконец, оценки R0, представленные в аннотации и основном тексте, не основаны на фактических данных из Сингапура и Тяньцзиня.Вместо этого они используют свои оценки серийного среднего интервала и стандартного отклонения для каждого параметра и точечную оценку скорости роста (без неопределенности) из другого исследования, основанного на данных для всего материкового Китая. Таким образом, ошибочно предполагать, что это оценки R0 специально для Сингапура и Тяньцзиня.
Мы согласны и изменили формулировку. Оценка R0 (в любом смысле, не говоря уже о конкретных популяциях) никогда не была основным направлением работы, и этот раздел предназначен только для того, чтобы отметить, что модели, использующие последовательные интервалы типа SARS (7.5 дней), можно было бы сделать вывод, что R0 был выше, чем у моделей, использующих наши серийные интервальные оценки 4+ дней. Мы исправили это.
https://doi.org/10.7554/eLife.57149.sa2 .

 Медицинские работники утверждают, что время остывания зависит от температуры в помещении, где находится тело.
Медицинские работники утверждают, что время остывания зависит от температуры в помещении, где находится тело. Они возникают, потому что кровь обездвижена, и поэтому собирается под действием силы тяжести в определенных точках тела. Образование таких пятен может характеризовать признаки биологической смерти (ранние и поздние).
Они возникают, потому что кровь обездвижена, и поэтому собирается под действием силы тяжести в определенных точках тела. Образование таких пятен может характеризовать признаки биологической смерти (ранние и поздние). Ограничения, вызванные болезнью, не остановить, симптомы накапливаются, пациент становится слабее, и его активность снижается. Данный этап может наступить за несколько недель до смерти.
Ограничения, вызванные болезнью, не остановить, симптомы накапливаются, пациент становится слабее, и его активность снижается. Данный этап может наступить за несколько недель до смерти.