Осложнения ишемического инсульта: Ишемический инсульт: прогнозы, последствия и реабилитация
факторы риска и методы профилактики
Ишемические осложнения хирургического лечения пациентов с болезнью мойя-мойя: факторы риска и методы профилактики
Сайт издательства «Медиа Сфера»
содержит материалы, предназначенные исключительно для работников здравоохранения. Закрывая это сообщение, Вы подтверждаете, что являетесь дипломированным медицинским работником или студентом медицинского образовательного учреждения.
Лукшин В.А.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Шульгина А.А.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Усачев Д.Ю.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Коршунов А.Е.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Белоусова О.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Лубнин А.Ю.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии имени академика Н.Н. Бурденко» Минздрава России
Ишемические осложнения хирургического лечения пациентов с болезнью мойя-мойя: факторы риска и методы профилактики
Журнал: Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2021;85(6): 26‑35
DOI 10.17116/neiro20218506126
Как цитировать
Лукшин В.А., Шульгина А.А., Усачев Д.Ю., Коршунов А.Е., Белоусова О.Б., Лубнин А.Ю.
Ишемические осложнения хирургического лечения пациентов с болезнью мойя-мойя: факторы риска и методы профилактики.
Lukshin VA, Shulgina AA, Usachev DYu, Korshunov AE, Belousova OB, Lubnin AYu. Ischemic complications following surgical treatment of moyamoya disease: risk factors and prevention. Zhurnal Voprosy Neirokhirurgii Imeni N.N. Burdenko. 2021;85(6):26‑35. (In Russ., In Engl.).
https://doi.org/10.17116/neiro20218506126
Авторы:
Лукшин В.А.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Все авторы (6)
Закрыть метаданные
Одной из самых сложных проблем хирургического лечения пациентов с болезнью мойя-мойя является предотвращение ишемических периоперационных осложнений, риск которых значительно выше, чем при другой цереброваскулярной патологии, и может достигать 30%.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Установить неблагоприятные прогностические факторы развития церебральных ишемических осложнений, связанных с хирургическими вмешательствами, у пациентов с болезнью мойя-мойя для определения группы больных повышенного риска и разработки рекомендаций по периоперационному ведению пациентов данной категории.
МАТЕРИАЛ И МЕТОДЫ
Проанализированы клинические, инструментальные данные и результаты хирургического лечения 80 пациентов с различными формами ангиопатии мойя-мойя, которым выполнено 134 оперативных реваскуляризирующих вмешательства. Этапная реваскуляризация обоих полушарий (80 операций) выполнена 40 пациентам. Большинству пациентов (n=55) проведена комбинированная реваскуляризация головного мозга (79 операций).
РЕЗУЛЬТАТЫ
Стойкие осложнения хирургического лечения в виде ишемического инсульта развились в 7 (5,3%) случаях, эпизоды обратимого нарастания неврологического дефицита — в 36 (27%). В результате статистического анализа выявлены факторы риска развития периоперационных осложнений: критический стеноз/окклюзия задней мозговой артерии (OR 9,704), грубый перфузионный дефицит 2—3-й степени (OR 5,393) и транзиторная ишемическая атака или ишемический инсульт в анамнезе в течение 3 мес до операции (OR 6,433). При наличии не менее двух из этих признаков чувствительность и специфичность в отношении прогноза развития послеоперационных осложнений составляют 80,7 и 88,6% соответственно.
При наличии не менее двух из этих признаков чувствительность и специфичность в отношении прогноза развития послеоперационных осложнений составляют 80,7 и 88,6% соответственно.
ВЫВОДЫ
Пациенты с болезнью мойя-мойя подвержены высокому риску развития периоперационных осложнений по причине сложной перестройки коллатерального мозгового кровообращения и высокой чувствительности головного мозга к изменениям локальной и системной гемодинамики. Этим обусловлена необходимость особо тщательного периоперационного ведения для исключения патогенетических факторов, провоцирующих ишемию. Хирургическое лечение целесообразно выполнять в ранние сроки развития заболевания для снижения риска как ишемических и геморрагических поражений вследствие естественного течения заболевания, так и тяжелых периоперационных осложнений.
Ключевые слова:
Болезнь мойя-мойя
ишемический инсульт
хирургическая реваскуляризация
комбинированная реваскуляризация
экстраинтракраниальный микроанастомоз
осложнения хирургического лечения
Авторы:
Лукшин В. А.
А.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Шульгина А.А.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Усачев Д.Ю.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Коршунов А.Е.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Белоусова О.Б.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России
Лубнин А.Ю.
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии имени академика Н.Н. Бурденко» Минздрава России
- РИНЦ AuthorID: 370609
- Scopus AuthorID: 57192157123
- ORCID: 0000-0003-2595-5877
Список литературы:
- Guzman R, Lee M, Achrol A, Bell-Stephens T, Kelly M, Do HM, Marks MP, Steinberg GK.
 Clinical outcome after 450 revascularization procedures for moyamoya disease. Journal of Neurosurgery. 2009;111(5):927-935. https://doi.org/10.3171/2009.4.JNS081649
Clinical outcome after 450 revascularization procedures for moyamoya disease. Journal of Neurosurgery. 2009;111(5):927-935. https://doi.org/10.3171/2009.4.JNS081649 - Iwama T, Hashimoto N, Tsukahara T, Murai B. Peri-operative complications in adult moyamoya disease. Acta Neurochirurgica. 1995;132(1-3):26-31. https://doi.org/10.1007/BF01404844
- Sakamoto T, Kawaguchi M, Kurehara K, Kitaguchi K, Furuya H, Karasawa J. Risk factors for neurologic deterioration after revascularization surgery in patients with moyamoya disease. Anesthesia and Analgesia. 1997;85(5):1060-1065. https://doi.org/10.1097/00000539-199711000-00018
- Starke RM, Komotar RJ, Connolly ES. Optimal surgical treatment for moyamoya disease in adults: direct versus indirect bypass. Neurosurgical Focus. 2009;26(4):E8. https://doi.org/10.3171/2009.01.FOCUS08309
- Jung YJ, Ahn JS, Kwon DH, Kwun BD. Ischemic complications occurring in the contralateral hemisphere after surgical treatment of adults with moyamoya disease.

- Шульгина А.А., Лукшин В.А., Усачев Д.Ю., Коршунов А.Е., Белоусова О.Б., Пронин И.Н. Комбинированная реваскуляризация головного мозга в лечении болезни мойя-мойя. Вопросы нейрохирургии им. Н.Н. Бурденко. 2021;85(2):47-59. https://doi.org/10.17116/neiro20218502147
- Houkin K, Nakayama N, Kuroda S, Nonaka T, Shonai T, Yoshimoto T. Novel Magnetic Resonance Angiography Stage Grading for Moyamoya Disease. Cerebrovascular Diseases. 2005;20(5):347-354. https://doi.org/10.1159/000087935
- Suzuki J, Takaku A. Cerebrovascular «moyamoya» disease. Disease showing abnormal net-like vessels in base of brain. Archives of Neurology. 1969;20(3):288-299. https://doi.org/10.1001/archneur.1969.00480090076012
- Togao O, Mihara F, Yoshiura T, Tanaka A, Noguchi T, Kuwabara Y, Kaneko K, Matsushima T, Honda H. Cerebral hemodynamics in Moyamoya disease: correlation between perfusion-weighted MR imaging and cerebral angiography.
 AJNR. American Journal of Neuroradiology. 2006;27(2):391-397.
AJNR. American Journal of Neuroradiology. 2006;27(2):391-397. - Baltsavias G, Khan N, Valavanis A. The collateral circulation in pediatric moyamoya disease. Child’s Nervous System: ChNS. 2015;31(3):389-398. https://doi.org/10.1007/s00381-014-2582-5
- Шульгина А.А., Лукшин В.А., Шульц Е.И., Баталов А.И., Пронин И.Н., Усачев Д.Ю. Методика оценки цереброваскулярной недостаточности у пациентов с ангиопатией мойя-мойя методом МР-ASL перфузии. Медицинская визуализация. 2021;25(2):102-115. https://doi.org/10.24835/1607-0763-883
- Grubb RL, Powers WJ, Derdeyn CP, Adams HP, Clarke WR. The Carotid Occlusion Surgery Study. Neurosurgical Focus. 2003;14(3):1-7. https://doi.org/10.3171/foc.2003.14.3.10
- Choi JW, Chong S, Phi JH, Lee JY, Kim H-S, Chae JH, Lee J, Kim SK. Postoperative symptomatic cerebral infarction in pediatric moyamoya disease: risk factors and clinical outcome. World Neurosurgery. 2020;136:158-164. https://doi.org/10.1016/j.wneu.2019.12.072
- Kazumata K, Ito M, Tokairin K, Ito Y, Houkin K, Nakayama N, Kuroda S, Ishikawa T, Kamiyama H.
 The frequency of postoperative stroke in moyamoya disease following combined revascularization: a single-university series and systematic review. Journal of Neurosurgery. 2014;121(2):432-440. https://doi.org/10.3171/2014.1.JNS13946
The frequency of postoperative stroke in moyamoya disease following combined revascularization: a single-university series and systematic review. Journal of Neurosurgery. 2014;121(2):432-440. https://doi.org/10.3171/2014.1.JNS13946 - Uchino H, Nakayama N, Kazumata K, Kuroda S, Houkin K. Edaravone reduces hyperperfusion-related neurological deficits in adult moyamoya disease: historical control study. Stroke. 2016;47(7):1930-1932. https://doi.org/10.1161/STROKEAHA.116.013304
- Funaki T, Takahashi JC, Takagi Y, Kikuchi T, Yoshida K, Mitsuhara T, Kataoka H, Okada T, Fushimi Y, Miyamoto S. Unstable moyamoya disease: clinical features and impact on perioperative ischemic complications. Journal of Neurosurgery. 2015;122(2):400-407. https://doi.org/10.3171/2014.10.JNS14231
- Wei W, Chen X, Yu J, Li XQ. Risk factors for postoperative stroke in adults patients with moyamoya disease: a systematic review with meta-analysis. BMC Neurology. 2019;19(1):1-8. https://doi.org/10.
 1186/s12883-019-1327-1
1186/s12883-019-1327-1 - Huang APH, Liu HM, Lai DM, Yang CC, Tsai YH, Wang KC, Yang SH, Kuo MF, Tu YK. Clinical significance of posterior circulation changes after revascularization in patients with moyamoya disease. Cerebrovascular Diseases. 2009;28(3):247-257. https://doi.org/10.1159/000228254
- Czabanka M, Boschi A, Acker G, Pena-Tapia P, Schubert GA, Schmiedek P, Vajkoczy P. Grading of moyamoya disease allows stratification for postoperative ischemia in bilateral revascularization surgery. Acta Neurochirurgica. 2016;158(10):1895-1900. https://doi.org/10.1007/s00701-016-2941-y
- Kim SH, Choi JU, Yang KH, Kim TG, Kim DS. Risk factors for postoperative ischemic complications in patients with moyamoya disease. Journal of Neurosurgery. 2005;103(5):433-438. https://doi.org/10.3171/ped.2005.103.5.0433
- Iwama T, Hashimoto N, Yonekawa Y. The relevance of hemodynamic factors to perioperative ischemic complications in childhood moyamoya disease. Neurosurgery. 1996;38(6):1120-1125; discussion 1125-11256.
 https://doi.org/10.1097/00006123-199606000-00011
https://doi.org/10.1097/00006123-199606000-00011 - Yusa T, Yamashiro K. Local cortical cerebral blood flow and response to carbon dioxide during anesthesia in patients with moyamoya disease. Journal of Anesthesiah. 1999;13(3):131-135. https://doi.org/10.1007/s005400050043
- Nomura S, Kashiwagi S, Uetsuka S, Uchida T, Kubota H, Ito H. Perioperative management protocols for children with moyamoya disease. Child’s Nervous System: ChNS. 2001;17(4-5):270-274. https://doi.org/10.1007/s003810000407
- Sun H, Wilson C, Ozpinar A, Safavi-Abbasi S, Zhao Y, Nakaji P, Wanebo JE, Spetzler RF. Perioperative Complications and Long-Term Outcomes After Bypasses in Adults with Moyamoya Disease: A Systematic Review and Meta-Analysis. World Neurosurgery. 2016;92:179-188. https://doi.org/10.1016/j.wneu.2016.04.083
Закрыть метаданные
COVID-ассоциированный ишемический инсульт
Пандемия коронавирусной инфекции 2019-2020 продемонстрировала не только высокую агрессивность нового инфекционного агента, но и его способность вызывать тяжелые сердечно-сосудистые осложнения. Ишемический инсульт (ИИ) в последние десятилетия является одной из ведущих причин смерти в старших возрастных группах [1]. Обобщение первых результатов лечения пострадавших от коронавирусной инфекции показало, что развитие ИИ у таких больных весьма вероятно. Высокая летальность больных пожилого возраста, зараженных COVID-19, отчасти связана с развитием фатальных сердечно-сосудистых осложнений, наиболее тяжелым из которых является инсульт.
Ишемический инсульт (ИИ) в последние десятилетия является одной из ведущих причин смерти в старших возрастных группах [1]. Обобщение первых результатов лечения пострадавших от коронавирусной инфекции показало, что развитие ИИ у таких больных весьма вероятно. Высокая летальность больных пожилого возраста, зараженных COVID-19, отчасти связана с развитием фатальных сердечно-сосудистых осложнений, наиболее тяжелым из которых является инсульт.
Анализ немногочисленных доступных публикаций в которых упоминается проблема COVID-ассоциированного ишемического инсульта может показать не только значимость проблемы, но и раскрыть механизмы острой церебральной ишемии. Предупреждение острых нарушений мозгового кровообращения (ОНМК) у инфицированных COVID-19 представляется одной из важных клинических задач, которые необходимо решать в условиях высокой загруженности специализированных стационаров и дефицита специалистов.
Новый патогенетический подтип ишемического инсульта?
По данным первых публикаций, в которых были проанализированы неврологические осложнения коронавирусной инфекции острые нарушения мозгового кровообращения (ОНМК) обнаруживались у 6% больных [2].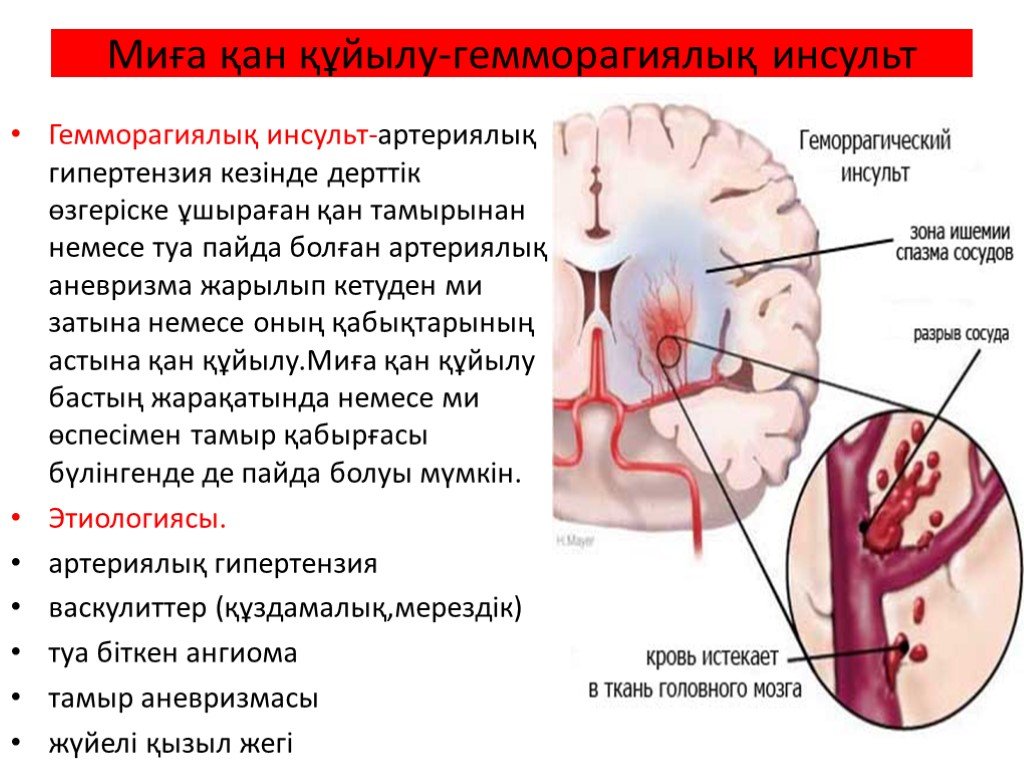 Первые обобщения клинических наблюдений показывают, что в структуре патогенетических подтипов ишемического инсульта (ИИ) преобладают синдромы тромботической окклюзии крупных артерий [3]. Кроме того, высокая частота нарушений сознания (более 15% по данным Mao L. 2020) может свидетельствовать о возможности диффузных повреждений мозга по типу острой (токсической, гипоксемической, ишемической) энцефалопатии.
Первые обобщения клинических наблюдений показывают, что в структуре патогенетических подтипов ишемического инсульта (ИИ) преобладают синдромы тромботической окклюзии крупных артерий [3]. Кроме того, высокая частота нарушений сознания (более 15% по данным Mao L. 2020) может свидетельствовать о возможности диффузных повреждений мозга по типу острой (токсической, гипоксемической, ишемической) энцефалопатии.
Для уточнения патогенеза острой церебральной ишемии в настоящее время принято выделять патогенетические подтипы ИИ в соответствии с этиологической классификацией TOAST. Согласно этой классификации, около 80% всех ИИ распределяются между основными подтипами – атеротромботический (атеросклеротическая болезнь крупных артерий), кардиоэмболический (основная причина – фибрилляция предсердий), лакунарный (микроангиопатия – болезнь мелких артерий). Формально, ОНМК на фоне коронавирусной инфекции можно отнести в категорию «другие установленные причины». Однако существуют несколько важных аргументов «против» такого формального распределения. Эти аргументы требуют более детального анализа причин и механизмов COVID-ассоциированного ишемического инсульта. Первый аргумент исходит из предположения, что эта форма ОНМК не ассоциирована с атеросклерозом, а следовательно, имеет оригинальный патогенез и совершенно другую этиологию. Второй аргумент основывается на фактах, свидетельствующих об участии активного воспалительного процесса в патогенезе COVID-ассоциированного ишемического инсульта. Наконец, третий аргумент исходит из сложившейся практики лечения таких больных. В отличии от стандартных методов лечения, основанных на применении антитромбоцитарной и гиполипидемической терапии с целью предупреждения атеротромбоза, у больных с коронавирусной инфекцией лучшие результаты демонстрируют антикоагулянты (не соответствует действующим клиническим рекомендациям) [4].
Эти аргументы требуют более детального анализа причин и механизмов COVID-ассоциированного ишемического инсульта. Первый аргумент исходит из предположения, что эта форма ОНМК не ассоциирована с атеросклерозом, а следовательно, имеет оригинальный патогенез и совершенно другую этиологию. Второй аргумент основывается на фактах, свидетельствующих об участии активного воспалительного процесса в патогенезе COVID-ассоциированного ишемического инсульта. Наконец, третий аргумент исходит из сложившейся практики лечения таких больных. В отличии от стандартных методов лечения, основанных на применении антитромбоцитарной и гиполипидемической терапии с целью предупреждения атеротромбоза, у больных с коронавирусной инфекцией лучшие результаты демонстрируют антикоагулянты (не соответствует действующим клиническим рекомендациям) [4].
Анализ клинических данных показывает, что больные переносят инсульт в острый период коронавирусной инфекции на фоне гипертермии и часто пневмонии. Для инсульта характерно крупноочаговое повреждение в каротидном сосудистом бассейне, больше похожее на синдром тромботической окклюзии крупной артерии. Существенным отличием COVID-зависимого от атеротромботического ИИ является отсутствие связи тромба с атеросклеротической бляшкой и наличие признаков воспаления сосудистой стенки. D.McNamara (2020) обращает внимание воспаление и отёк артерий сосудистого бассейна в котором развивается инфаркт мозга, что можно расценивать как острый васкулит. Воспаление и отёк сосудистой стенки прямо или косвенно связанный с воздействием вируса или аутоиммунной реакцией представляется возможным, но не облигатным признаком развития и генерализации инфекционного процесса. Более того, неврологический синдром, ассоциированный с воспалением крупных артерий – это скорее редкость, чем закономерность. Анализ первых данных, содержащих сопоставление клинической картины ОНМК и результатов лабораторных тестов может в некоторой степени объяснить факт и частоту развития синдрома поражения крупных артерий. L. Mao c соавт. (2020) представляют анализ лабораторных данных 124 больных, находившихся на стационарном лечении с коронавирусной инфекцией.
Существенным отличием COVID-зависимого от атеротромботического ИИ является отсутствие связи тромба с атеросклеротической бляшкой и наличие признаков воспаления сосудистой стенки. D.McNamara (2020) обращает внимание воспаление и отёк артерий сосудистого бассейна в котором развивается инфаркт мозга, что можно расценивать как острый васкулит. Воспаление и отёк сосудистой стенки прямо или косвенно связанный с воздействием вируса или аутоиммунной реакцией представляется возможным, но не облигатным признаком развития и генерализации инфекционного процесса. Более того, неврологический синдром, ассоциированный с воспалением крупных артерий – это скорее редкость, чем закономерность. Анализ первых данных, содержащих сопоставление клинической картины ОНМК и результатов лабораторных тестов может в некоторой степени объяснить факт и частоту развития синдрома поражения крупных артерий. L. Mao c соавт. (2020) представляют анализ лабораторных данных 124 больных, находившихся на стационарном лечении с коронавирусной инфекцией. Средний возраст больных — 54 года, тяжелое течение заболевания отмечалось у 59%. Цереброваскулярные синдромы выявлены у 6% больных, все в группе тяжелого течения. Авторы сравнили результаты лабораторных тестов в группе тяжелого и легкого течения коронавирусной инфекции. Достоверные различия отмечены в отношении содержания лимфоцитов (0,9 (01,-2,6) и 1,3 (0,4-2,6) соответственно), С-реактивного белка (мг/л) – 37,1 (0,1-212,1) и 9,4 (0,4-112) соответственно, D-димер (мг/л) – 0,9 (0,1-20,0) и 0,4 (0,2-8,7) соответственно. Даже поверхностный взгляд на результаты лабораторных тестов показывает, что активные воспалительные и тромбогенные реакции развиваются только у тяжелых больных. Однако и в группе тяжелых отмечается очень высокая дисперсность лабораторных показателей – от нормы до выраженных превышений обычных значений. Это, вероятно, значит, что гипервоспаление и гиперкоагуляция отмечается не у всех, а только у некоторых больных с иммунным ответом, который определяется индивидуальными особенностями больного.
Средний возраст больных — 54 года, тяжелое течение заболевания отмечалось у 59%. Цереброваскулярные синдромы выявлены у 6% больных, все в группе тяжелого течения. Авторы сравнили результаты лабораторных тестов в группе тяжелого и легкого течения коронавирусной инфекции. Достоверные различия отмечены в отношении содержания лимфоцитов (0,9 (01,-2,6) и 1,3 (0,4-2,6) соответственно), С-реактивного белка (мг/л) – 37,1 (0,1-212,1) и 9,4 (0,4-112) соответственно, D-димер (мг/л) – 0,9 (0,1-20,0) и 0,4 (0,2-8,7) соответственно. Даже поверхностный взгляд на результаты лабораторных тестов показывает, что активные воспалительные и тромбогенные реакции развиваются только у тяжелых больных. Однако и в группе тяжелых отмечается очень высокая дисперсность лабораторных показателей – от нормы до выраженных превышений обычных значений. Это, вероятно, значит, что гипервоспаление и гиперкоагуляция отмечается не у всех, а только у некоторых больных с иммунным ответом, который определяется индивидуальными особенностями больного. Такая гиперреактивность может быть обусловлена генетическими особенностями больного или состоянием иммунитета. Вероятно, определение предикторов и биомаркеров агрессивного течения болезни является важной научной и практической задачей, решение которой позволит избежать таких тяжелых осложнений как инсульт. Однако возможность такой гиперреактивности наводит на мысль о применении активной иммуносупрессии при появлении признаков васкулита.
Такая гиперреактивность может быть обусловлена генетическими особенностями больного или состоянием иммунитета. Вероятно, определение предикторов и биомаркеров агрессивного течения болезни является важной научной и практической задачей, решение которой позволит избежать таких тяжелых осложнений как инсульт. Однако возможность такой гиперреактивности наводит на мысль о применении активной иммуносупрессии при появлении признаков васкулита.
Итак, следует ли считать, что существует особый патогенетический подтип ишемического инсульта – COVID-зависимый инсульт? Да. COVID-зависимый ИИ – это острое нарушение мозгового кровообращения, обусловленное острой воспалительной васкулопатией и тромбозом крупных артерий головного мозга. Признание нового подтипа ИИ не исключает развития у больных с коронавирусной инфекцией и других вариантов ОНМК, если речь идет о пациентах, демонстрирующих соответствующие ассоциированные с атеросклерозом заболевания и синдромы (артериальная гипертония, фибрилляция предсердий, атеросклероз). Сам факт заболевания COVID-19, госпитализация с неясными перспективами представляют из себя фактор дестабилизации заболевания сердечно-сосудистой системы, протекавшего ранее относительно стабильно. Гиперкоагуляционный статус больных с коронавирусной инфекцией – это другой важный фактор изменения стабильного течения заболеваний, ассоциированных с атеросклерозом.
Сам факт заболевания COVID-19, госпитализация с неясными перспективами представляют из себя фактор дестабилизации заболевания сердечно-сосудистой системы, протекавшего ранее относительно стабильно. Гиперкоагуляционный статус больных с коронавирусной инфекцией – это другой важный фактор изменения стабильного течения заболеваний, ассоциированных с атеросклерозом.
Коагулопатия – как причина сосудистых событий и цель лечения
Показательна эволюция представлений врачей о наиболее значимых звеньях патогенеза коронавирусной инфекции. В первых публикациях китайских специалистов основное внимание уделялось респираторному дистресс-синдрому, гипертермии и интоксикации. С распространением эпидемии на страны Европы и американский континент, накоплением клинических наблюдений и лабораторных данных, специалисты больше внимание стали уделять системным нарушениям гемостаза у больных в остром и подостром периоде заболевания. Наряду с общеинфекционным синдромом, внутрисосудистое тромбообразование во многих случаях достигающее степени диссеминированного внутрисосудистого свертывания крови является ключевым фактором, определяющим исход заболевания. Коагулопатия, развивающаяся при коронавирусной инфекции имеет сложный патогенез, который выходит за пределы триады Вирхова и приводит к образованию венозных и артериальных тромбозов. Действие мощных прокоагулянтых факторов таких как повреждение эндотелия сосудов, системное воспаление с формированием нейтрофильных внеклеточных ловушек и выбросом гистонов, ферментов и пептидов приводит к формированию множественных внутрисосудистых тромбов [5-8]. Наряду с обтурирующими тромбами вен и крупных артерий, микротромбы блокируют микроциркуляцию, создавая условия для ишемии органов и тканей. Создаются условия для тромбоэмболизма как в венозной, так и в артериальной системе, включая механизм парадоксальной эмболии для реализации которого без коагулопатии не было необходимых условий. Особенностью коагулопатии при коронавирусной инфекции является высокая скорость развития патологических процессов, которые протекают с быстрым истощением системы физиологических антикоагулянтов, в том числе протеинов С и S, снижением фибринолитического потенциала крови.
Коагулопатия, развивающаяся при коронавирусной инфекции имеет сложный патогенез, который выходит за пределы триады Вирхова и приводит к образованию венозных и артериальных тромбозов. Действие мощных прокоагулянтых факторов таких как повреждение эндотелия сосудов, системное воспаление с формированием нейтрофильных внеклеточных ловушек и выбросом гистонов, ферментов и пептидов приводит к формированию множественных внутрисосудистых тромбов [5-8]. Наряду с обтурирующими тромбами вен и крупных артерий, микротромбы блокируют микроциркуляцию, создавая условия для ишемии органов и тканей. Создаются условия для тромбоэмболизма как в венозной, так и в артериальной системе, включая механизм парадоксальной эмболии для реализации которого без коагулопатии не было необходимых условий. Особенностью коагулопатии при коронавирусной инфекции является высокая скорость развития патологических процессов, которые протекают с быстрым истощением системы физиологических антикоагулянтов, в том числе протеинов С и S, снижением фибринолитического потенциала крови. Скрининговая коагулограмма демонстрирует увеличение концентрации фибриногена, снижение антитромбона III, протеинов S и C, время свертывания крови укорачивается. Установлено, что уровень D-димера коррелирует с тяжестью заболевания и его увеличение часто свидетельствует о развитии коагулопатии. На сегодняшний день уровень D-димера считается наиболее надёжным биомаркером гиперкоагуляции у больных с коронавирусной инфекцией.
Скрининговая коагулограмма демонстрирует увеличение концентрации фибриногена, снижение антитромбона III, протеинов S и C, время свертывания крови укорачивается. Установлено, что уровень D-димера коррелирует с тяжестью заболевания и его увеличение часто свидетельствует о развитии коагулопатии. На сегодняшний день уровень D-димера считается наиболее надёжным биомаркером гиперкоагуляции у больных с коронавирусной инфекцией.
Понимание одного из ключевых механизмов системных повреждений органов и тканей при коронавирусной инфекции привело к изменению лечебной стратегии [6,7]. Тромбопрофилактика является одним из главных направлений терапии больных, которые находятся в отделении интенсивной терапии. Особенности коагулопатии при коронавирусной инфекции привели к признанию низкомолекулярных гепаринов в качестве основного антитромботического средства, которое используется на протяжении всего острого периода заболевания. В качестве поддерживающего лечения, которое может проводится до 40 дней, а при необходимости и дольше, рассматриваются такие антикоагулянты как ривароксабан (10 мг в сутки). Вопрос о применении глюкокортикоидов для подавления острого воспаления остается открытым до накопления и обобщения результатов клинической практики и специальных исследований.
Вопрос о применении глюкокортикоидов для подавления острого воспаления остается открытым до накопления и обобщения результатов клинической практики и специальных исследований.
Выводы
Особенности коагулопатии при коронавирусной инфекции создают условия для ОНМК в основе которых лежит тромботическая окклюзия крупной артерии, не связанная с атеротромбозом – COVID-зависимый ИИ. Опасное инфекционное заболевание способствует развитию и других вариантов ИИ: атеротромботического, кардиоэмболического и парадоксальной эмболии. Однако в целом, вероятность ишемического инсульта при острой коронавирусной инфекции не очень велика (примерно 6%). Профилактика COVID-зависимого ИИ основывается на применении антикоагулянтов, целесообразность назначения которых определяется тяжестью заболевания и биомаркерами тромбообразования, наиболее надёжным из которых является D-димер.
Д.м.н., профессор Евгений Алексеевич Широков
Библиография
1. Mozaffarian D., Benjamin E., Go A. et al. Heart Disease and Stroke Statistics—2016 Update. Circulation. 2016; 133(4):e38-e360.
et al. Heart Disease and Stroke Statistics—2016 Update. Circulation. 2016; 133(4):e38-e360.
2. Mao L., Jin H., Wang M. et.al. Neurologic Manifestations of Hospitalized Patients With Coronavirus Disease 2019 in Wuhan, China/
3. McNamara D. COVID-19 Linked to Large Vessel Stroke in Young Adults/ April 24, 2020/ https://www.medscape.com/viewarticle/929345?src=wnl_edit_tpal&uac=296430PX&impID=2359734&faf=1
JAMANeurol.doi:10.1001/jamaneurol.2020.1127 PublishedonlineApril10,2020.
4. Powers W., Rabinstein A., Ackerson T. et al. 2018 Guidelines for the Early Management of Patients With Acute Ischemic Stroke. A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke. 2018;49:eXXX– eXXX. doi: 10.1161/STR.0000000000000158.
5. Tang N, Li D, Wang X, Sun Z. Abnormal coagulation parameters are associated with poor prognosis in patients with novel coronavirus pneumonia. J Thromb Haemost 2020; 18: 844–47.
6. Zucker D., Zucker B. Hospital-based use of thromboprophylaxis in patients with COVID-19 / Published online April 21, 2020 https://doi.org/10.1016/S0140-6736(20)30926-0
7. Cuker A.,Peyvandi L.Coronavirus disease 2019 (COVID-19): Hypercoagulability/ This topic last updated: Apr 29, 2020. https://www.uptodate.com/contents/coronavirus-disease-2019-covid-19-hypercoagulability?fbclid=IwAR0swwtIFghGPtI-p7Hjwse58R67p6NmY36PUerS7IZ4k0nEqgFPHmMO2xI
8. Fuchs N.A., Brill A.,, Wagner D.D. Neutrophil Extracellular Trap (NET) Impact on Deep Vein Thrombosis. Arterioscler. Thromb. Vasc. Biol. 2012;32(: 1777–1783.
Ишемический инсульт: профилактика осложнений и вторичная профилактика
1. Лангхорн П., Стотт Д.Дж., Робертсон Л., Макдональд Дж., Джонс Л., Макалпайн С., Дик Ф., Тейлор Г.С., Мюррей Г. Медицинские осложнения после инсульта: многоцентровое исследование. Инсульт. 2000;31(6):1223–1229. [PubMed] [Google Scholar]
2. Индредавик Б., Роведер Г., Наалсунд Э. , Лидерсен С. Медицинские осложнения в комплексном инсультном отделении и услуга ранней выписки. Инсульт. 2008;39(2):414–420. [PubMed] [Академия Google]
, Лидерсен С. Медицинские осложнения в комплексном инсультном отделении и услуга ранней выписки. Инсульт. 2008;39(2):414–420. [PubMed] [Академия Google]
3. Хилкер Р., Поэттер С., Финдейзен Н., Собески Дж., Джейкобс А., Невелинг М., Хейсс В.Д. Внутрибольничная пневмония после острого инсульта: значение для неврологической интенсивной терапии. Инсульт. 2003;34(4):975–981. [PubMed] [Google Scholar]
4. Хинчи Дж. А., Шепард Т., Фьюри К., Смит Д., Ван Д., Тонн С. Формальные протоколы скрининга дисфагии предотвращают пневмонию. Инсульт. 2005;36(9):1972–1976. [PubMed] [Google Scholar]
5. Galvan TJ. Дисфагия: опускаться и оставаться внизу. Ам Дж Нурс. 2001;101(1):37–42. викторина 43. [PubMed] [Google Scholar]
6. Чаморро А., Хоркахада Дж. П., Обач В., Варгас М., Ревилла М., Торрес Ф., Сервера А., Планас А. М., Менса Дж. Исследование ранней системной профилактики инфекции после инсульта: рандомизированное клиническое исследование. Инсульт. 2005;36(7):1495–1500. [PubMed] [Google Scholar]
7. Adams HP, Jr, del Zoppo G, Alberts MJ, Bhatt DL, Brass L, Furlan A, Grubb RL, Higashida RT, Jauch EC, Kidwell C, Lyden PD, Morgenstern LB, Куреши А.И., Розенвассер Р.Х., Скотт П.А., Вийдикс Э.Ф. Рекомендации по раннему лечению взрослых с ишемическим инсультом: рекомендации Совета по инсульту Американской кардиологической ассоциации/Американской ассоциации инсульта, Совета по клинической кардиологии, Совета по сердечно-сосудистой радиологии и интервенционным вмешательствам, а также Атеросклеротических заболеваний периферических сосудов и результатов качества медицинской помощи в междисциплинарных исследованиях. Группы: Американская академия неврологии подтверждает ценность этого руководства как учебного пособия для неврологов. Инсульт. 2007;38(5):1655–1711. [PubMed] [Академия Google]
Adams HP, Jr, del Zoppo G, Alberts MJ, Bhatt DL, Brass L, Furlan A, Grubb RL, Higashida RT, Jauch EC, Kidwell C, Lyden PD, Morgenstern LB, Куреши А.И., Розенвассер Р.Х., Скотт П.А., Вийдикс Э.Ф. Рекомендации по раннему лечению взрослых с ишемическим инсультом: рекомендации Совета по инсульту Американской кардиологической ассоциации/Американской ассоциации инсульта, Совета по клинической кардиологии, Совета по сердечно-сосудистой радиологии и интервенционным вмешательствам, а также Атеросклеротических заболеваний периферических сосудов и результатов качества медицинской помощи в междисциплинарных исследованиях. Группы: Американская академия неврологии подтверждает ценность этого руководства как учебного пособия для неврологов. Инсульт. 2007;38(5):1655–1711. [PubMed] [Академия Google]
8. Гелбер Д.А., Гуд Д.К., Лавен Л.Дж., Ферхулст С.Дж. Причины недержания мочи после острого полушарного инсульта. Инсульт. 1993;24(3):378–382. [PubMed] [Google Scholar]
9. Patel M, Coshall C, Rudd AG, Wolfe CD. Естественное течение и влияние на 2-летние исходы недержания мочи после инсульта. Инсульт. 2001;32(1):122–127. [PubMed] [Google Scholar]
Естественное течение и влияние на 2-летние исходы недержания мочи после инсульта. Инсульт. 2001;32(1):122–127. [PubMed] [Google Scholar]
10. Чан Х. Управление мочевым пузырем при неотложной помощи пациентам с инсультом: проект повышения качества. J Neurosci Нурс. 1997;29(3): 187–190. [PubMed] [Google Scholar]
11. Bernhardt J, Dewey H, Thrift A, Donnan G. Неактивный и одинокий: физическая активность в течение первых 14 дней пребывания в отделении острого инсульта. Инсульт. 2004;35(4):1005–1009. [PubMed] [Google Scholar]
12. Hilker R, Poetter C, Findeisen N, Sobesky J, Jacobs A, Neveling M, Heiss WD, Bernhardt J, Dewey H, Thrift A, Collier J, Donan G. A очень ранний реабилитационное исследование при инсульте (AVERT): безопасность и осуществимость фазы II. Инсульт. 2008 фев; 39 (2): 390–6. Epub 2008 Jan 3. [PubMed] [Google Scholar]
13. Wijdicks EF. Легочная эмболия, связанная с острым инсультом. Материалы клиники Мэйо. 1997;72(4):297. [PubMed] [Google Scholar]
14. Шерман Д.Г., Альберс Г.В., Бладин С., Фиески С., Габбай А.А., Касе С.С., О’Риордан В., Пинео Г.Ф. Эффективность и безопасность эноксапарина по сравнению с нефракционированным гепарином для профилактики венозной тромбоэмболии после острого ишемического инсульта (исследование PREVAIL): открытое рандомизированное сравнение. Ланцет. 2007;369(9570): 1347–1355. [PubMed] [Google Scholar]
Шерман Д.Г., Альберс Г.В., Бладин С., Фиески С., Габбай А.А., Касе С.С., О’Риордан В., Пинео Г.Ф. Эффективность и безопасность эноксапарина по сравнению с нефракционированным гепарином для профилактики венозной тромбоэмболии после острого ишемического инсульта (исследование PREVAIL): открытое рандомизированное сравнение. Ланцет. 2007;369(9570): 1347–1355. [PubMed] [Google Scholar]
15. Йоргенсен Л., Энгстад Т., Якобсен Б.К. Более высокая частота падений среди лиц, перенесших инсульт в течение длительного времени, чем в контрольной популяции: депрессивные симптомы предсказывают падения после инсульта. Инсульт. 2002;33(2):542–547. [PubMed] [Google Scholar]
16. Келли-Хейс М. Показатели исхода инсульта. J Cardiovasc Nurs. 2004;19(5):301–307. [PubMed] [Google Scholar]
17. Пул К.Е., Рив Дж., Уорбертон Э.А. Падения, переломы и остеопороз после инсульта: пора подумать о защите? Инсульт. 2002;33(5):1432–1436. [PubMed] [Академия Google]
18. Смит Дж., Форстер А. , Хаус А., Кнапп П., Уайт Дж., Янг Дж. Информационное обеспечение пациентов, перенесших инсульт, и тех, кто за ними ухаживает. Cochrane Database Syst Rev. 2008;(2):CDOO1919. [Google Scholar]
, Хаус А., Кнапп П., Уайт Дж., Янг Дж. Информационное обеспечение пациентов, перенесших инсульт, и тех, кто за ними ухаживает. Cochrane Database Syst Rev. 2008;(2):CDOO1919. [Google Scholar]
19. Сакко Р.Л., Адамс Р., Альберс Г., Альбертс М.Дж., Бенавенте О., Фьюри К., Гольдштейн Л.Б., Горелик П., Гальперин Дж., Харбо Р., Джонстон С.К., Катзан И., Келли-Хейс М., Кентон EJ, Marks M, Schwamm LH, Tomsick T. Рекомендации по профилактике инсульта у пациентов с ишемическим инсультом или транзиторной ишемической атакой: Заявление для медицинских работников Совета Американской кардиологической ассоциации/Американской ассоциации инсульта по инсульту: при поддержке Совета по сердечно-сосудистой радиологии и вмешательствам: Американская академия неврологии подтверждает ценность этого руководства. Инсульт. 2006;37(2):577–617. [PubMed] [Академия Google]
Распространенные осложнения после инсульта: что это такое и что делать?
Генри Хоффман
Вторник, 16 октября 2018 г.
Последнее изменение от 26 августа 2022 г.
Инсульт возникает, когда приток крови к мозгу внезапно прерывается, что препятствует поступлению кислорода в мозг и вызывает быструю гибель клеток мозга. По данным Центров по контролю и профилактике заболеваний (CDC), инсульты являются одной из основных причин смерти и инвалидности. Различают три основных типа инсульта:
- Геморрагический инсульт является наименее распространенным типом инсульта, на его долю приходится всего 15% всех инсультов, но они являются причиной более 40% всех смертей, связанных с инсультом. Геморрагический инсульт — это либо разрыв аневризмы головного мозга, либо ослабление кровеносного сосуда. Кровь проливается в мозг или вокруг него и создает отек и давление, повреждая клетки и ткани в мозге.
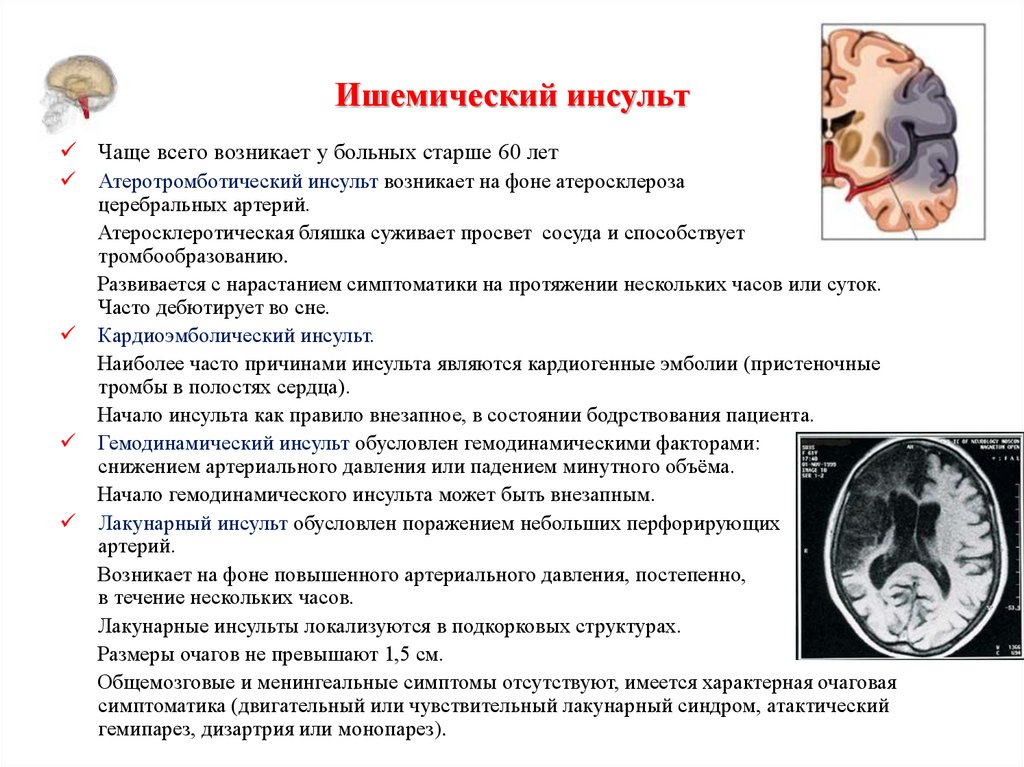
- Ишемический инсульт возникает, когда кровеносный сосуд, несущий кровь к мозгу, закупоривается тромбом, в результате чего кровь не достигает мозга. Повышенное кровяное давление является частой причиной ишемического инсульта.
 Ишемические инсульты составляют 87% всех инсультов. Различают два типа ишемического инсульта: эмболический и тромботический. Эмболический инсульт — это когда фрагмент тромба или бляшки образуется где-то в организме и перемещается в мозг. Попав в мозг, сгусток перемещается в кровеносный сосуд, достаточно маленький, чтобы сгусток блокировал проход крови. Тромботический инсульт вызывается тромбом, который образуется внутри одной из артерий, снабжающих кровью головной мозг.
Ишемические инсульты составляют 87% всех инсультов. Различают два типа ишемического инсульта: эмболический и тромботический. Эмболический инсульт — это когда фрагмент тромба или бляшки образуется где-то в организме и перемещается в мозг. Попав в мозг, сгусток перемещается в кровеносный сосуд, достаточно маленький, чтобы сгусток блокировал проход крови. Тромботический инсульт вызывается тромбом, который образуется внутри одной из артерий, снабжающих кровью головной мозг. - Транзиторная ишемическая атака (ТИА). Также известная как «мини-инсульт», в случае ТИА приток крови к мозгу блокируется на короткий период времени, обычно не более пяти минут. ТИА может проявлять симптомы, подобные инсульту, которые длятся менее 24 часов, прежде чем исчезнут. Хотя ТИА, как правило, не вызывают необратимого повреждения головного мозга, они являются серьезным предупредительным признаком того, что в будущем может произойти инсульт, и их нельзя игнорировать.
Осложнения после инсульта — это медицинские, эмоциональные и неврологические проблемы, которые могут возникнуть у выжившего после инсульта. В одном исследовании у 85% пациентов, госпитализированных по поводу инсульта, возникло по крайней мере одно осложнение после инсульта. У выжившего могут возникнуть серьезные или незначительные осложнения, в зависимости от тяжести инсульта и других факторов. Осложнения не всегда постоянны. Во многих случаях с ними можно справиться при своевременном и соответствующем лечении.
В одном исследовании у 85% пациентов, госпитализированных по поводу инсульта, возникло по крайней мере одно осложнение после инсульта. У выжившего могут возникнуть серьезные или незначительные осложнения, в зависимости от тяжести инсульта и других факторов. Осложнения не всегда постоянны. Во многих случаях с ними можно справиться при своевременном и соответствующем лечении.
Если кровь течет по венам слишком медленно, это может привести к образованию тромба или закупорке кровеносных сосудов. Когда тромб образуется в вене, это вызывает тромбоз глубоких вен. ТГВ чаще всего возникает в голени или бедре, но может возникать и в других частях тела. Случай ТГВ может стать опасным для жизни, если сгусток крови сместится и попадет в жизненно важный орган. Лекарства и ранняя мобилизационная терапия после инсульта могут предотвратить ТГВ и помочь человеку быстрее вернуться к ходьбе и другим видам деятельности.
Инсульт вызывает повреждение головного мозга, что приводит к образованию рубцовой ткани. Эта рубцовая ткань прерывает электрическую активность в головном мозге. Нарушение электрической активности может вызвать судороги. Судороги являются одним из наиболее частых осложнений ишемического инсульта, которым страдают 22% выживших.
ПневмонияПневмония является основной причиной заболеваемости и смертности после инсульта. По данным Медицинской школы Университета Индианы, пневмония является наиболее частой причиной повторной госпитализации после инсульта. В случае инсульта проблемы с глотанием могут вызвать аспирацию или попадание пищи или жидкостей в дыхательные пути, что может привести к инфекции грудной клетки или пневмонии.
Отек головного мозга Отек или воспаление являются частью естественной реакции организма на травму. Отек относится к набуханию из-за захваченной жидкости. Однако если отек возникает в головном мозге, это может вызвать серьезные осложнения. Отек головного мозга может ограничивать кровоснабжение головного мозга, что приводит к гибели мозговой ткани. Воспаление головного мозга является одним из основных осложнений ишемического инсульта. Получение медицинской помощи, как только наблюдаются симптомы инсульта, может помочь снизить вероятность развития тяжелого отека мозга.
Отек головного мозга может ограничивать кровоснабжение головного мозга, что приводит к гибели мозговой ткани. Воспаление головного мозга является одним из основных осложнений ишемического инсульта. Получение медицинской помощи, как только наблюдаются симптомы инсульта, может помочь снизить вероятность развития тяжелого отека мозга.
Существует множество проблем с мочевым пузырем, которые могут возникнуть в результате инсульта. Часто у выживших после инсульта возникают сильные позывы или потребность в частом мочеиспускании. Когда человек, перенесший инсульт, не может справить нужду должным образом, потому что он не может добраться до ванной или снять одежду, это называется функциональным недержанием мочи. Другие выжившие после инсульта будут иметь недержание мочи и будут мочиться, не осознавая, что они это сделали, что известно как рефлекторное недержание мочи. Следовательно, когда человек, перенесший инсульт, не может полностью опорожнить мочевой пузырь самостоятельно, это называется задержкой мочи. Если это произойдет, вполне вероятно, что человеку потребуется катетер, чтобы обеспечить полное опорожнение мочевого пузыря.
Если это произойдет, вполне вероятно, что человеку потребуется катетер, чтобы обеспечить полное опорожнение мочевого пузыря.
Клиническая депрессия часто возникает после серьезного кризиса со здоровьем. Каждый четвертый человек, переживший инсульт, страдает серьезной депрессией. Депрессия может вызывать грусть, раздражительность, трудности с концентрацией внимания, безнадежность, апатию, изменения аппетита и режима сна, а иногда даже мысли о самоубийстве. Важно лечить депрессию с помощью специалистов в области психического здоровья.
Пролежни Когда мягкие ткани прижимаются к более твердой поверхности, такой как стул или кровать, в течение длительного периода времени кровоснабжение этой области снижается. Это может привести к повреждению или отмиранию кожной ткани. Когда это происходит, может образоваться пролежень. Профилактика является ключом к пролежням: правильное положение и соответствующее оборудование необходимы, чтобы избежать их. Перенесший инсульт должен обсудить со своим врачом или терапевтом соответствующее оборудование, такое как надувные матрасы и подушки для инвалидных колясок.
Перенесший инсульт должен обсудить со своим врачом или терапевтом соответствующее оборудование, такое как надувные матрасы и подушки для инвалидных колясок.
Контрактуры — это потеря подвижности с течением времени из-за аномального укорочения структур мягких тканей, охватывающих один или несколько суставов. К ним относятся кожа, связки, сухожилия, мышцы и суставные капсулы. Потеря подвижности в любой из этих структур ограничивает подвижность сустава, что приводит к боли, тугоподвижности и, в конечном итоге, к контрактуре. Длительное растяжение с низкой нагрузкой является предпочтительным методом устранения контрактуры. В одном из таких продуктов, SaeboStretch, используется революционная технология растяжения, которая помогает поддерживать или улучшать подвижность, сводя к минимуму повреждение суставов и боль.
Боль в плече Боль в плече возникает у 80 % пациентов, перенесших инсульт, у которых практически отсутствуют произвольные движения пораженной конечности. Подвывих или частичный вывих плеча; спастичность плеча; тендинит; и разрывы вращательной манжеты плеча — все возможные причины боли в плече. Боль в плече можно лечить с помощью правильного позиционирования, включая поддержку сустава с помощью ортопедических стелек, а также раннего вмешательства по труду и / или физиотерапии. В некоторых случаях, если боль становится хронической, врач может назначить пероральные кортикостероиды.
Подвывих или частичный вывих плеча; спастичность плеча; тендинит; и разрывы вращательной манжеты плеча — все возможные причины боли в плече. Боль в плече можно лечить с помощью правильного позиционирования, включая поддержку сустава с помощью ортопедических стелек, а также раннего вмешательства по труду и / или физиотерапии. В некоторых случаях, если боль становится хронической, врач может назначить пероральные кортикостероиды.
Общие нарушения после инсульта, такие как дисбаланс, сенсорные нарушения, слабость, проблемы со зрением и отсутствие координации, естественным образом повышают риск падений и несчастных случаев. Физическая и трудотерапия может помочь снизить этот риск и восстановить стабильность и утраченную функцию. Можно приобрести модификации для дома и вспомогательные устройства, которые помогут предотвратить падения и несчастные случаи при выполнении обычных повседневных действий.
Чувство социальной изоляции Инсульт часто может повлиять на чувство социального места пострадавшего. Их роль в семье может существенно измениться после инсульта: возможно, они были кормильцами, а сейчас находятся в длительном отпуске. Внезапная потеря дохода или резкая смена потребностей и ожиданий в отношении ухода могут усилить стресс. Группы поддержки доступны для переживших инсульт и их близких и являются отличным ресурсом для решения этих проблем.
Их роль в семье может существенно измениться после инсульта: возможно, они были кормильцами, а сейчас находятся в длительном отпуске. Внезапная потеря дохода или резкая смена потребностей и ожиданий в отношении ухода могут усилить стресс. Группы поддержки доступны для переживших инсульт и их близких и являются отличным ресурсом для решения этих проблем.
Осложнения инсульта являются обычным явлением, и специалисты по реабилитации после инсульта знают, как структурировать раннее лечение для оптимального восстановления.
ФизиотерапияРанняя мобилизация является ключом к предотвращению осложнений от паралича в результате инсульта. Физиотерапия помогает выжившим после инсульта улучшить равновесие, силу и подвижность. Физиотерапевт предложит упражнения , которые помогут пациенту стать более подвижным и укрепить мышцы для стояния, ходьбы, наклонов и других повседневных действий.
Трудотерапия Трудотерапия для лиц, переживших инсульт, направлена на облегчение участия в приобретении жизненных навыков путем устранения продолжающегося дефицита, такого как слабость, потеря чувствительности, а также когнитивные или зрительные нарушения, которые ограничивают участие в функциональной деятельности.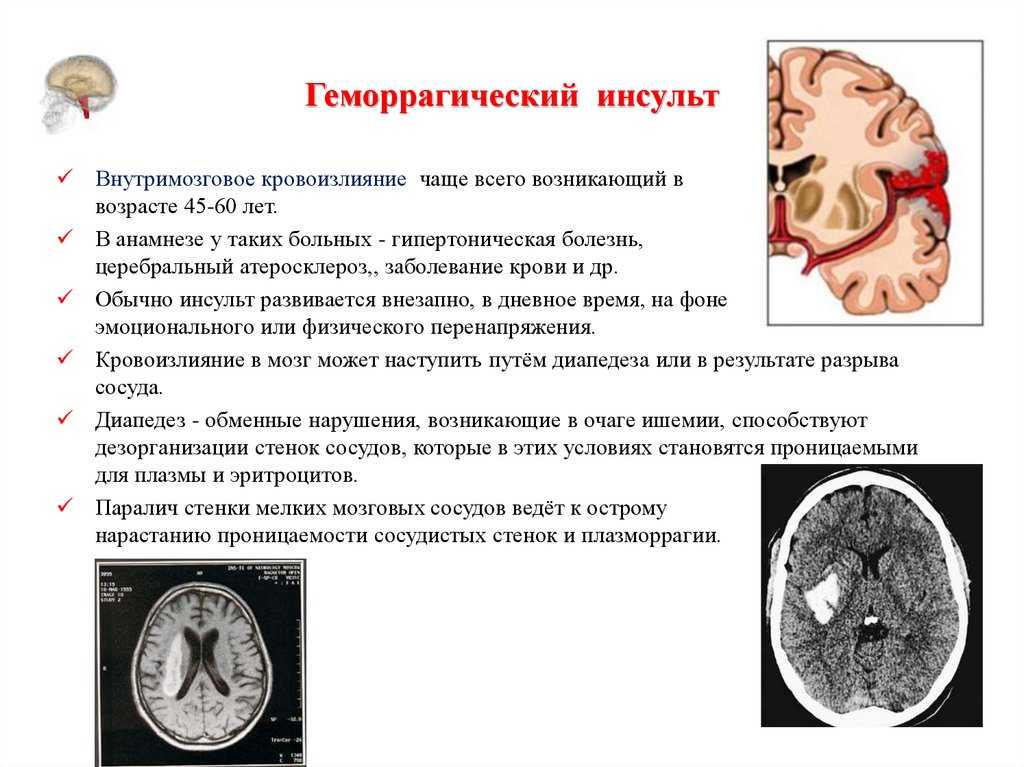 Эрготерапевты также помогают пострадавшим, определяя способы сделать дом более безопасным или более доступным для пострадавшего и, среди прочего, обучая стратегиям восстановления независимости после инсульта.
Эрготерапевты также помогают пострадавшим, определяя способы сделать дом более безопасным или более доступным для пострадавшего и, среди прочего, обучая стратегиям восстановления независимости после инсульта.
Логопеды оценивают и лечат нарушения общения, познания и глотания у выживших после инсульта.
Другие специалисты в реабилитационном центре после инсульта Восстановление после инсульта и устранение осложнений в результате инсульта будет различным процессом для каждого выжившего. В команде много разных участников, которые способствуют восстановлению человека, перенесшего инсульт. Некоторые из членов команды могут включать лечащего врача (PCP), невролога, физиотерапевта (доктор физиотерапии), диетолога, медсестру или социального работника. Некоторым выжившим, возможно, придется обратиться за помощью к разным членам команды, в зависимости от того, какой была их жизнь до инсульта и как инсульт повлиял на них. Выжившим придется полагаться на свою команду по восстановлению после инсульта, поэтому важно иметь профессионалов, квалифицированных в вопросах, которые их затрагивают.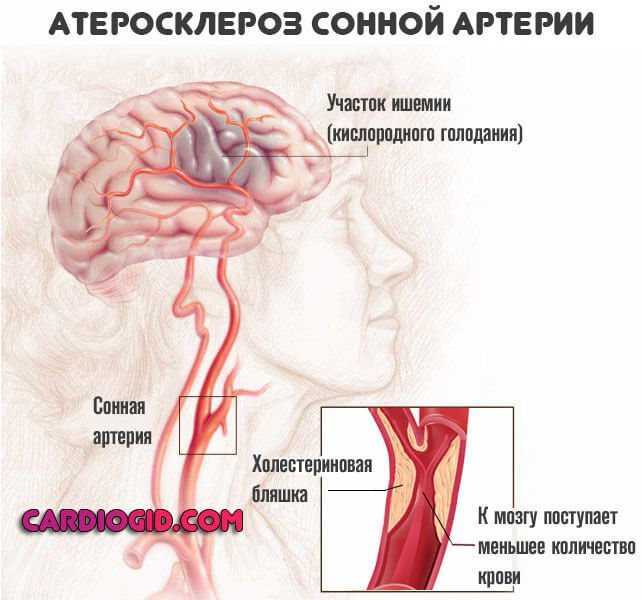

 Clinical outcome after 450 revascularization procedures for moyamoya disease. Journal of Neurosurgery. 2009;111(5):927-935. https://doi.org/10.3171/2009.4.JNS081649
Clinical outcome after 450 revascularization procedures for moyamoya disease. Journal of Neurosurgery. 2009;111(5):927-935. https://doi.org/10.3171/2009.4.JNS081649
 AJNR. American Journal of Neuroradiology. 2006;27(2):391-397.
AJNR. American Journal of Neuroradiology. 2006;27(2):391-397.  The frequency of postoperative stroke in moyamoya disease following combined revascularization: a single-university series and systematic review. Journal of Neurosurgery. 2014;121(2):432-440. https://doi.org/10.3171/2014.1.JNS13946
The frequency of postoperative stroke in moyamoya disease following combined revascularization: a single-university series and systematic review. Journal of Neurosurgery. 2014;121(2):432-440. https://doi.org/10.3171/2014.1.JNS13946 1186/s12883-019-1327-1
1186/s12883-019-1327-1 https://doi.org/10.1097/00006123-199606000-00011
https://doi.org/10.1097/00006123-199606000-00011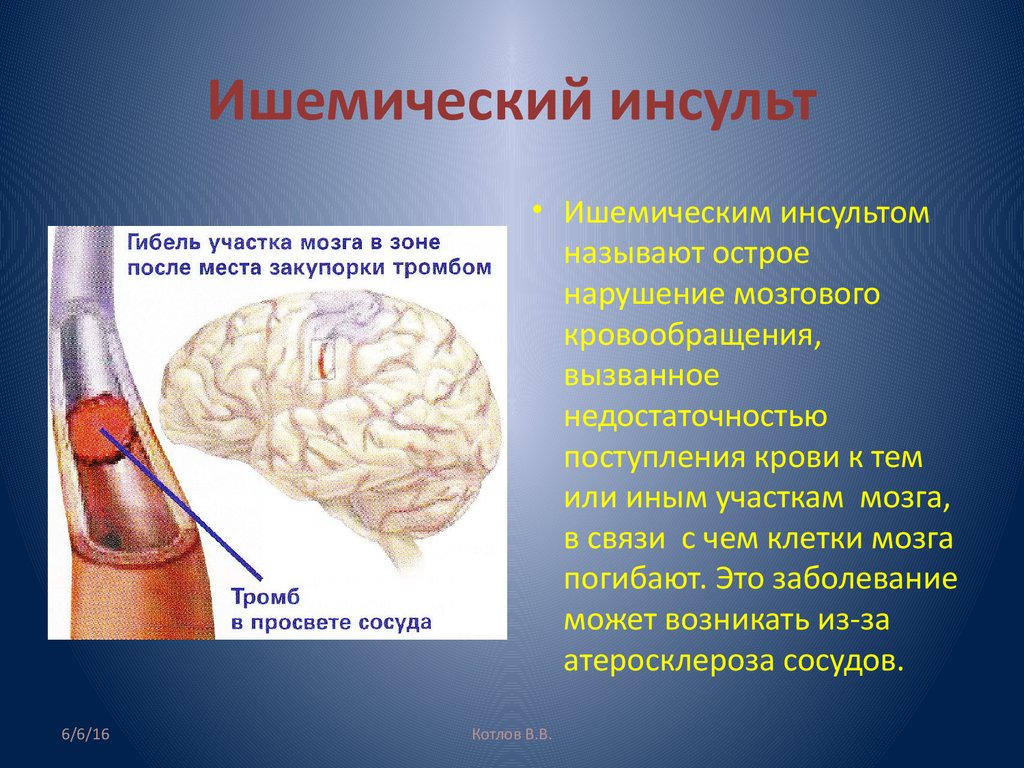 Ишемические инсульты составляют 87% всех инсультов. Различают два типа ишемического инсульта: эмболический и тромботический. Эмболический инсульт — это когда фрагмент тромба или бляшки образуется где-то в организме и перемещается в мозг. Попав в мозг, сгусток перемещается в кровеносный сосуд, достаточно маленький, чтобы сгусток блокировал проход крови. Тромботический инсульт вызывается тромбом, который образуется внутри одной из артерий, снабжающих кровью головной мозг.
Ишемические инсульты составляют 87% всех инсультов. Различают два типа ишемического инсульта: эмболический и тромботический. Эмболический инсульт — это когда фрагмент тромба или бляшки образуется где-то в организме и перемещается в мозг. Попав в мозг, сгусток перемещается в кровеносный сосуд, достаточно маленький, чтобы сгусток блокировал проход крови. Тромботический инсульт вызывается тромбом, который образуется внутри одной из артерий, снабжающих кровью головной мозг.