Онкобольные перед смертью признаки: На исходе жизни: чего ожидать вам и вашим родным
Экспериментальный метод борьбы с реакцией отторжения после трансплантации почти вдвое увеличил выживаемость онкопациентов
Применение стероидов (и кортикостероидов в частности) — главный метод борьбы с отторжением донорского костного мозга у пациентов с онкологическими заболеваниями, однако он чреват множеством осложнений, и четверть пациентов к нему невосприимчива. Петербургские ученые предложили альтернативный подход — подавление белка, активирующего слишком агрессивные Т-лимфоциты. Такая терапия позволила спасти практически всех испытуемых, — хотя обычно выживаемость немногим превышает 50%, — а также оставила в их организме достаточно «бойцов» для противостояния микробам и вирусам. С результатами работы, поддержанной грантом Российского научного фонда (РНФ), можно ознакомиться на страницах журнала Bone Marrow Transplantation.
Примерно у половины онкобольных после пересадки стволовых клеток костного мозга развивается так называемая реакция «трансплантат против хозяина» (РТПХ). Это результат того, что иммунные клетки — Т-лимфоциты — донора начинают атаковать ткани пациента: в первые 100 дней (острая стадия) это проявляется поражениями кожи, пищеварительной системы и печени, а после, когда синдром уже переходит в хроническую стадию, страдают практически все системы органов. Подобное осложнение — одна из главных причин смерти людей, перенесших трансплантацию костного мозга.
Это результат того, что иммунные клетки — Т-лимфоциты — донора начинают атаковать ткани пациента: в первые 100 дней (острая стадия) это проявляется поражениями кожи, пищеварительной системы и печени, а после, когда синдром уже переходит в хроническую стадию, страдают практически все системы органов. Подобное осложнение — одна из главных причин смерти людей, перенесших трансплантацию костного мозга.
Основной подход к лечению РТПХ (так называемая «первая линия терапии») — применение гормонов кортикостероидов, подавляющих сразу несколько механизмов защиты. Однако при этом высоки риски серьезных осложнений, среди которых диабет и катаракта, а из-за практически полного отсутствия иммунитета возможны рецидивы рака; кроме того, около 25% пациентов не реагируют на такое лечение.
Сотрудники Научно-исследовательского института детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета имени И. П. Павлова (Санкт-Петербург) проверили эффективность замены стероидных препаратов на ингибиторы кальциневрина. Эти вещества подавляют активность фермента, опосредованно запускающего синтез воспалительных молекул Т-лимфоцитами. Такой подход медики проверили на пациентах от 18 до 67 лет, которым пересадили костный мозг, в том числе и с уменьшенным количеством Т-клеток, а затем лечили противоопухолевым циклофосфамидом (он также подавляет отторжение донорского материала) — это обычное назначение после процедуры. Однако у людей проявились признаки иммунологического конфликта, и авторы начали лечение ингибиторами кальциневрина. Среди испытуемых оказались 34 человека с острой РТПХ и 40 — с хронической РТПХ средней или тяжелой степени.
Эти вещества подавляют активность фермента, опосредованно запускающего синтез воспалительных молекул Т-лимфоцитами. Такой подход медики проверили на пациентах от 18 до 67 лет, которым пересадили костный мозг, в том числе и с уменьшенным количеством Т-клеток, а затем лечили противоопухолевым циклофосфамидом (он также подавляет отторжение донорского материала) — это обычное назначение после процедуры. Однако у людей проявились признаки иммунологического конфликта, и авторы начали лечение ингибиторами кальциневрина. Среди испытуемых оказались 34 человека с острой РТПХ и 40 — с хронической РТПХ средней или тяжелой степени.
Результаты показали эффективность терапии для 80% пациентов с хроническим синдромом (практически все со средней степенью и чуть больше половины с тяжелой) и лишь для 47% с острым (причем состояние улучшалось лишь при относительно слабых кожных повреждениях). Авторы продолжили наблюдать за больными, чтобы оценить долгосрочные эффекты. Так, спустя два года выжили 95% и 76% пациентов из первой и второй группы соответственно. Это хороший результат, поскольку обычно выживаемость составляет порядка 50–60%. Интересно, что лечение оказалось эффективнее для пациентов, которым пересаживали донорский материал с обычным, а не искусственно сниженным количеством Т-лимфоцитов. Это объясняется тем, что терапия без стероидов приводила к подавлению более «агрессивных» по отношению к тканям больного Т-клеток, тогда как регуляторные, подавляющие чрезмерный иммунный ответ, работали нормально. Также примечательно, что испытуемые, не принимавшие кортикостероиды, реже нуждались в антибиотиках и противовирусных препаратах — это значит, что предложенная авторами схема не затрагивала системы защиты организма, необходимые для противостояния патогенам.
Это хороший результат, поскольку обычно выживаемость составляет порядка 50–60%. Интересно, что лечение оказалось эффективнее для пациентов, которым пересаживали донорский материал с обычным, а не искусственно сниженным количеством Т-лимфоцитов. Это объясняется тем, что терапия без стероидов приводила к подавлению более «агрессивных» по отношению к тканям больного Т-клеток, тогда как регуляторные, подавляющие чрезмерный иммунный ответ, работали нормально. Также примечательно, что испытуемые, не принимавшие кортикостероиды, реже нуждались в антибиотиках и противовирусных препаратах — это значит, что предложенная авторами схема не затрагивала системы защиты организма, необходимые для противостояния патогенам.
«Мы продемонстрировали высокую выживаемость пациентов, при этом бесстероидная терапия не влияет так сильно и так глубоко на иммунитет больного, как традиционная. Пока результаты получены на небольшой группе пациентов, но мы надеемся, что в дальнейшем в эксперименте поучаствует еще больше людей», — говорит руководитель проекта, поддержанного грантом РНФ, Иван Моисеев, доктор медицинских наук, заместитель директора по научной работе НИИ ДОГиТ ПСПбГМУ.
Управление симптомами конца жизни — American Nurse
По мере приближения смерти многие пациенты с хроническими заболеваниями испытывают неприятные признаки и симптомы. Например, у людей с сердечной недостаточностью одышка из-за задержки жидкости может вызвать агонию. У онкологических больных может преобладать боль. Другие распространенные симптомы конца жизни (EOL) включают возбуждение и делирий, тревогу, утомляемость, слабость, запор, тошноту и рвоту.
Для пациентов, находящихся в конце жизни, паллиативная помощь, как и уход в хосписе, означает прекращение лечения, за исключением тех, которые облегчают симптомы (например, паллиативная химиотерапия). Раннее вмешательство в паллиативную помощь может привести к улучшению качества жизни, улучшению сна, снижению утомляемости и уменьшению боли, что, в свою очередь, улучшает самочувствие пациента. В исследовании 151 пациента с раком легкого, рандомизированного для получения стандартной или паллиативной помощи, паллиативная помощь улучшила качество жизни и увеличила выживаемость, хотя пациенты получали менее агрессивную помощь.
Однако слишком часто паллиативная помощь не применяется до тех пор, пока пациент не окажется на грани смерти. Многие пациенты и медицинские работники не знают, что паллиативная помощь может облегчить симптомы; они ошибочно предполагают, что это то же самое, что терминальная помощь или уход в хосписе. Более того, не все пациенты могут получить доступ к специалистам по паллиативной помощи на ранних стадиях хронического заболевания. Хотя паллиативная помощь была признана специальностью в 2006 г., специально обученных практикующих врачей по-прежнему относительно мало. (См. Сколько времени осталось у пациента? , щелкнув PDF-файл выше)
От лечения к комфорту
Когда пациент близок к смерти, цель лечения меняется с лечения на комфорт, и облегчение симптомов является одним из самых ценных вкладов, которые могут предложить медицинские работники. Практики паллиативной помощи также могут помочь семьям принять трудные решения по таким вопросам, как кодовый статус пациента или использование зонда для кормления.
Управление симптомами EOL может быть очень сложным. Многие пациенты имеют множественные сопутствующие заболевания. Коморбидные заболевания и метастатический рак могут иметь многогранные проявления; их необходимо упростить и рассмотреть каждый пункт. Некоторые симптомы EOL могут стать рефрактерными; примеры включают задержку жидкости у пациентов с сердечно-сосудистыми заболеваниями, которая может усугубить респираторный дистресс, а также боль и анорексию у больных раком. Эти симптомы требуют более продвинутых методов, таких как паллиативная седация или имплантированные помпы для обезболивания.
Симптомы EOL требуют агрессивного подхода к лечению. У медицинских работников нет времени, чтобы опробовать длительные графики титрования опиоидов или экспериментировать с методами, которые могут принести или не принести облегчение.
Кластеры симптомов
У многих пациентов с EOL симптомы проявляются вместе в кластере, что создает большую проблему для лечения. Такой кластер усугубляет дистресс пациента и его труднее лечить, поскольку симптомы могут иметь синергетический эффект друг на друга и увеличивать общее бремя симптомов. Усталость является наиболее распространенным симптомом, возникающим группами; это особенно заметно у больных раком. Другие симптомы, которые могут группироваться вместе, включают бессонницу, боль, затрудненное дыхание, тошноту, слабость, рвоту, изменения аппетита и изменение вкуса.
Усталость является наиболее распространенным симптомом, возникающим группами; это особенно заметно у больных раком. Другие симптомы, которые могут группироваться вместе, включают бессонницу, боль, затрудненное дыхание, тошноту, слабость, рвоту, изменения аппетита и изменение вкуса.
Когда пациент начинает сообщать о множественных симптомах, необходимо тщательно оценить план лечения. После выбора вмешательства необходимо отслеживать его влияние на другие симптомы. Например, круглосуточное предоставление противорвотных средств при тошноте может усилить седативный эффект, что требует корректировки других седативных препаратов, таких как анальгетики, седативные средства и снотворные. Распознавание кластера симптомов и предоставление соответствующих вмешательств может улучшить контроль над всеми симптомами.
Боль
Боль является наиболее распространенным симптомом EOL и наиболее опасным. Боль может быть вызвана многими причинами, включая хронические состояния, такие методы лечения, как невропатии, связанные с химиотерапией, и прогрессирование заболевания. Приблизительно 75% пациентов с запущенным раком испытывают боль. Независимо от причины, облегчение боли является главным приоритетом, поскольку оно может улучшить качество жизни и снять стресс. Сильная боль требует агрессивного обезболивания, включая как фармакологические, так и немедикаментозные варианты по мере необходимости.
Приблизительно 75% пациентов с запущенным раком испытывают боль. Независимо от причины, облегчение боли является главным приоритетом, поскольку оно может улучшить качество жизни и снять стресс. Сильная боль требует агрессивного обезболивания, включая как фармакологические, так и немедикаментозные варианты по мере необходимости.
Оцените боль пациента по самоотчету, используя числовую шкалу интенсивности боли (NPI), где 0 означает отсутствие боли, а 10 — максимально сильную боль. Важным применением NPI является определение эффективности вмешательства; уменьшение боли на 2 балла считается клинически значимым. Если пациент не может самостоятельно сообщить о боли, используйте поведенческую шкалу боли; такие шкалы основаны на поведении, определяемом как указание на боль. Повторно оцените уровень боли после вмешательства, чтобы убедиться, что лекарство или другое средство уменьшило боль в ожидаемой степени.
Когда фармакологическая анальгезия является вариантом, поставщики медицинских услуг должны выбрать режим лечения, который будет адекватно контролировать боль, но у них нет времени, чтобы менять, титровать или комбинировать анальгетики по мере необходимости. Многие умирающие пациенты испытывают боль в течение длительного времени, даже не достигнув EOL. Простым инструментом для определения того, какой тип лекарств помогает при различных уровнях боли, является шкала Всемирной организации здравоохранения:
Многие умирающие пациенты испытывают боль в течение длительного времени, даже не достигнув EOL. Простым инструментом для определения того, какой тип лекарств помогает при различных уровнях боли, является шкала Всемирной организации здравоохранения:
- Шаг 1. Легкая боль (интенсивность NPI от 1 до 3): ацетаминофен; нестероидные противовоспалительные препараты; адъювантные препараты, такие как трициклические антидепрессанты и миорелаксанты
- Этап 2. Умеренная боль (интенсивность от 4 до 6): комбинация опиоидов, таких как гидрокодон и ацетаминофен или оксикодон и ацетаминофен, плюс продолжительная адъювантная терапия
- Этап 3. Сильная боль (интенсивность от 7 до 10): опиоиды, такие как морфин и гидроморфон, а также продолжительная адъювантная терапия.
Морфин (золотой стандарт обезболивания при раке) и гидроморфон обычно используются для облегчения боли при EOL. Если пациент все еще может принимать пероральные препараты, может потребоваться быстрое повышение дозы, при этом либеральные дозы назначаются при прорывной боли (например, при возникшей боли или при неэффективности приема дозы).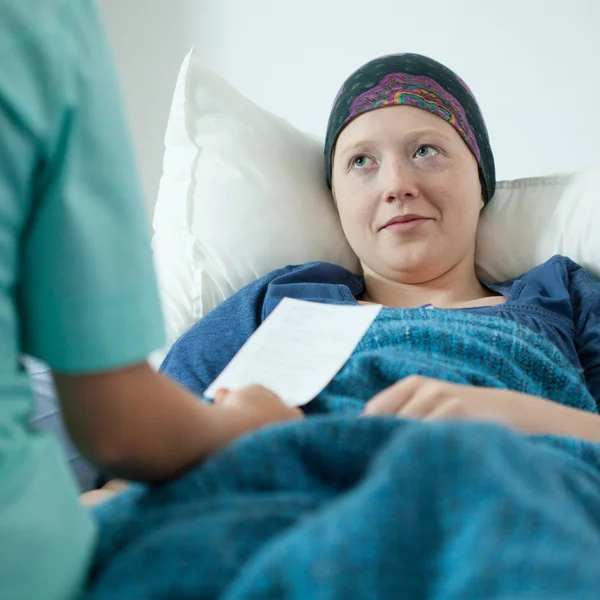
Опиоиды обычно вводят в виде непрерывных инфузий (внутривенно или подкожно) для облегчения боли или респираторного дистресса. Чтобы эффективно начать инфузию опиоидов, вводите болюсную дозу, примерно вдвое превышающую обычную болюсную дозу, до тех пор, пока не будет достигнут комфорт или контроль дыхания. Например, если непрерывная инфузия начинается со скорости 1 мг/ч, начальная болюсная доза должна составлять 2 мг. Начальная доза для непрерывной инфузии составляет
1 мг/час для морфина или 0,2 мг/час для гидроморфона, титруется до уровня комфорта пациента. Чтобы обеспечить доставку адекватных количеств для контроля боли, должны быть доступны дополнительные болюсные дозы для введения при повышенной интенсивности боли или дыхательной недостаточности.
Усовершенствованные методы обезболивания
Усовершенствованные методы обезболивания доступны для лечения пациентов с ЭОЛ. Если пациент может активировать помпу для контролируемой пациентом анальгезии (PCA) с непрерывной инфузией и активируемыми пациентом болюсами, портативная помпа может быть предоставлена как для домашнего, так и для стационарного использования. Опиоиды, обычно используемые в помпах АКП, включают морфин, гидроморфон и цитрат фентанила.
Эпидуральный катетер может обеспечить отличное обезболивание при использовании раствора местного анестетика и опиоида. Катетер может быть проложен от его точки входа на спине пациента до бокового расположения для большей стабильности катетера и более легкого управления. Используемые лекарства, такие как морфин без консервантов и бупивакаин, можно вводить в виде непрерывной инфузии болюсными дозами, активируемыми пациентом, почти так же, как и при АПК.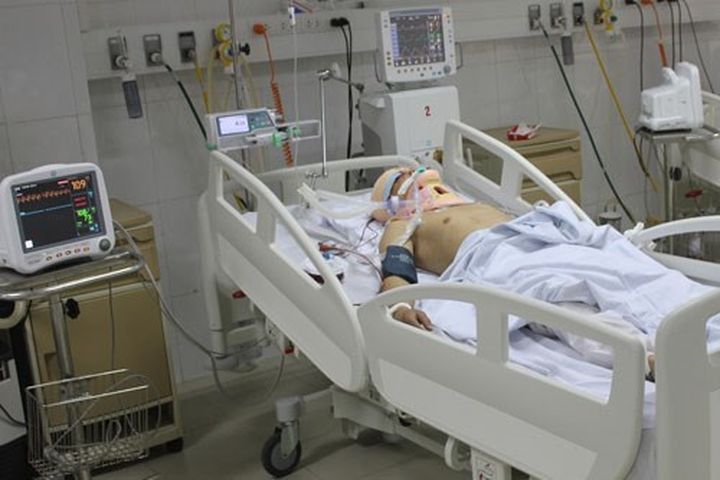 Эпидуральный катетер можно использовать до 30 дней; при необходимости его заменяют еще на 30 дней.
Эпидуральный катетер можно использовать до 30 дней; при необходимости его заменяют еще на 30 дней.
Специалисты по анестезиологии и обезболиванию могут предоставить широкий спектр регионарных методик для первичного обезболивания или дополнительного контроля боли. Методы регионарной анестезии, такие как блокада чревного сплетения у пациентов с раком поджелудочной железы, могут обеспечить эффективное обезболивание и имеют преимущество в экономии опиоидов.
При непреодолимой боли местный анестетик В.В. инфузии также могут обеспечить отличное облегчение с опиоид-сберегающим эффектом. И.В. лидокаин вводят в виде болюса от 1 до 3 мг/кг в течение 20-30 минут с непрерывной инфузией, начинающейся после завершения болюсного введения. Анестетик кетамин также можно использовать для дополнительного обезболивания; непрерывную инфузию начинают со скорости 0,04 мг/кг/час с максимальной дозой 0,3 мг/кг/час. Хотя кетамин может вызывать галлюцинации или диссоциативное состояние, он может облегчить боль, когда одних опиоидов недостаточно. Если пациент принимает опиоиды, когда начинается инфузия кетамина, уменьшите дозировку опиоидов на 25%. Этот тип инфузии обычно контролируется практикующим врачом со специальными навыками, например специалистом по боли или врачом паллиативной помощи, и может использоваться как часть протокола терминальной седации.
Если пациент принимает опиоиды, когда начинается инфузия кетамина, уменьшите дозировку опиоидов на 25%. Этот тип инфузии обычно контролируется практикующим врачом со специальными навыками, например специалистом по боли или врачом паллиативной помощи, и может использоваться как часть протокола терминальной седации.
Делирий и возбуждение
Многие пациенты с EOL впадают в бред или возбуждение, что может вызвать дистресс как у пациента, так и у его семьи. Делирий и возбуждение трудно поддаются лечению. Когнитивное расстройство острого начала, бред бывает нескольких типов — гипоактивный, гиперактивный и смешанный. Раннее выявление пациентов из группы риска способствует раннему распознаванию и быстрому лечению. После выявления делирия или возбуждения необходима всесторонняя постоянная оценка. Частота делирия у неизлечимых пациентов колеблется от 20 до 88%, при этом у 32-45% пациентов делирий развивается в течение недели до смерти. Больные с делирием могут часто пытаться встать с постели, несмотря на то, что они очень слабы или не могут поддерживать свой вес.
Имейте в виду, что делирий значительно отличается от слабоумия, которое оказывает более медленное и прогрессирующее изнурительное воздействие на память и функции. Делирий влияет на когнитивные функции, внимание, цикл сна и бодрствования, настроение и речь. Члены семьи могут заявить, что пациент «просто сегодня не в себе» или «в обычных условиях никогда бы не сказал таких вещей». Распространенными причинами делирия являются опиоиды, обезвоживание, инфекции, гипоксия, дефицит питательных веществ, почечная недостаточность, метастазы в головной мозг и эндокринные нарушения. Присутствие знакомых людей может помочь переориентировать и расслабить пациента.
Для обеспечения безопасности пациента в периоды бреда или возбуждения может потребоваться физическое сдерживание. Но по возможности избегайте использования средств сдерживания, потому что это может усугубить возбуждение. Галоперидол является наиболее эффективным средством для лечения ажитации. Этот препарат обладает меньшим седативным действием, чем лоразепам; кроме того, лоразепам оказался неэффективным при лечении делирия. Когда пациент достигает EOL, бензодиазепины и седативные нейролептики считаются одинаково эффективными в контроле возбуждения.
Когда пациент достигает EOL, бензодиазепины и седативные нейролептики считаются одинаково эффективными в контроле возбуждения.
Одышка, также называемая одышкой, одышкой или кислородным голоданием, является распространенным симптомом EOL. Это может произойти в начале процесса умирания с заболеванием легких или без него и может серьезно ухудшить качество жизни. Оценка пациента помогает определить основную причину одышки и определить соответствующее лечение, оценку и реакцию на лечение. Пациенты с сердечной недостаточностью могут испытывать одышку, поскольку жидкость накапливается и сдавливает легочную ткань. У онкологических больных с плевральным выпотом может возникать одышка из-за скопления жидкости в плевральной полости.
В EOL одышка возникает примерно у 75% пациентов с сердечной недостаточностью, от 20% до 70% больных раком и от 56% до 94% пациентов с респираторными заболеваниями. Кислород может не облегчить одышку, за исключением случаев, когда она вызвана гипоксией. Опиоиды обычно используются для облегчения одышки, особенно у больных раком; текущие рекомендации призывают к пероральному, внутривенному или подкожному введению опиоидов. При необходимости можно начать непрерывную инфузию после того, как болюсная доза обеспечит достаточное облегчение одышки. Чаще всего используется морфин; начальная доза составляет от 1 до 2 мг/час, титруется вверх по мере необходимости. Имейте в виду, что распыление морфина не дало достаточных положительных результатов и не рекомендуется.
Опиоиды обычно используются для облегчения одышки, особенно у больных раком; текущие рекомендации призывают к пероральному, внутривенному или подкожному введению опиоидов. При необходимости можно начать непрерывную инфузию после того, как болюсная доза обеспечит достаточное облегчение одышки. Чаще всего используется морфин; начальная доза составляет от 1 до 2 мг/час, титруется вверх по мере необходимости. Имейте в виду, что распыление морфина не дало достаточных положительных результатов и не рекомендуется.
Обязательно обсудите с пациентом и его семьей использование опиоидов для лечения боли, одышки или того и другого до начала такой терапии. Опишите опиоидную терапию как способ управления симптомами; некоторые семьи могут подумать, что это делается для того, чтобы ускорить смерть пациента. Рассказывая об использовании и преимуществах этих лекарств, вы можете помочь членам семьи привыкнуть к ним. (См. Понимание принципа двойного эффекта , щелкнув значок PDF выше.)
Слабость и усталость
Наиболее распространенные хронические симптомы, связанные с раком и другими хроническими заболеваниями, слабость и утомляемость могут быть следствием заболевания, его лечения, повышенной активности или других факторов (например, нарушений сна). Примерно 99% больных раком испытывают усталость. Исследования показывают, что L-карнитин, микронутриент, который превращает жировые отложения в энергию, оказывает положительное влияние на пациентов на ранних стадиях усталости, связанной с болезнью, но литературных данных слишком мало, чтобы рекомендовать его для общей практики.
Примерно 99% больных раком испытывают усталость. Исследования показывают, что L-карнитин, микронутриент, который превращает жировые отложения в энергию, оказывает положительное влияние на пациентов на ранних стадиях усталости, связанной с болезнью, но литературных данных слишком мало, чтобы рекомендовать его для общей практики.
Хотя усталость может ухудшать качество жизни неизлечимых пациентов, она также может выполнять защитную функцию и помогать пациентам справляться со страданиями. По этой причине поставщики медицинских услуг должны позволить пациентам решать, насколько активными они предпочитают быть или какие виды деятельности они могут терпеть.
Запор
Запор может быть одним из самых неприятных симптомов, с которым нужно справиться, и тяжелым состоянием для пациентов, которые не могут регулярно опорожнять кишечник. Поскольку многие пациенты с EOL регулярно получают опиоиды, можно ожидать запор, а также боль в животе, тошноту и рвоту и постоянные позывы к дефекации (с плохими результатами). Плохое пероральное потребление и непереносимость жидкости могут привести к обезвоживанию и усугубить действие лекарств и отсутствие активности.
Плохое пероральное потребление и непереносимость жидкости могут привести к обезвоживанию и усугубить действие лекарств и отсутствие активности.
Таким образом, режим лечения кишечника всегда должен сопровождать опиоидную терапию. Если пациент может принимать пероральные слабительные и размягчители стула, давайте их на регулярной основе. Если пациент не может принимать достаточное количество жидкости, избегайте давать слабительные средства, образующие объем, такие как Миралакс, поскольку пациент может быть не в состоянии потреблять достаточное количество жидкости, чтобы слабительное подействовало. Если запор тяжелый, в соответствии с указаниями назначают пероральные слабительные и ректальные клизмы или суппозитории. При запорах, вызванных опиоидами, метилналтрексон, вводимый подкожно в дозе 0,15 мг/кг, может обеспечить послабление через 4 часа. Конфеты торговой марки Sorbee, содержащие сорбит (который способствует послаблению), можно использовать при более легких запорах.
Тошнота и рвота
Тошнота и рвота чаще встречаются на ранних стадиях хронического заболевания; кроме того, они могут быть результатом такого лечения, как химиотерапия. Противорвотные средства могут контролировать эти симптомы, и их, возможно, потребуется давать круглосуточно.
Противорвотные средства могут контролировать эти симптомы, и их, возможно, потребуется давать круглосуточно.
Плохой контроль секреции
В EOL контроль секреции может быть проблемой. Так называемый «предсмертный хрип» — шумное, хриплое дыхание — возникает в результате движения секрета, скопившегося в горле. Это часто происходит, когда у пациента отсутствует способность очищать выделения. Отсасывание в это время может вызывать дискомфорт и дистресс, приводя к возбуждению и усилению секреции. Вместо этого поместите пластырь со скополамином за ухом пациента, как указано в инструкции, чтобы высушить выделения. Также рассмотрите возможность введения И.В. или подкожный гликопирролат (Robinul). Имейте в виду, что И.В. Администрация обеспечивает более быстрое начало.
Проблемы с питанием
У большинства пациентов с ЭОЛ плохой аппетит, и они не могут потреблять достаточное количество пищи, чтобы удовлетворить свои потребности в калориях. Уровни общего белка и альбумина указывают на уровень дефицита питания. По мере приближения смерти организм начинает отключаться, и потребности в питании резко снижаются. В это время подумайте о том, чтобы предложить пациенту любимую пищу, если он еще может глотать.
По мере приближения смерти организм начинает отключаться, и потребности в питании резко снижаются. В это время подумайте о том, чтобы предложить пациенту любимую пищу, если он еще может глотать.
Многие семьи опасаются, что пациент EOL умрет от голода. (На самом деле организм больше не нуждается в питании, и голод подавляется.) Некоторые семьи настолько обеспокоены, что рассматривают возможность установки гастростомической трубки для обеспечения жидкого питания. Некоторым пациентам может быть полезен зонд для кормления, например, пациенту, перенесшему острый инсульт, от которого ожидается некоторое значимое выздоровление, но не восстановление глотательного рефлекса. Однако большинству неизлечимых пациентов через зонд для кормления подается только жидкость, которую организм больше не может использовать, что приводит к отеку, который может вызвать болезненный отек конечностей.
При обсуждении питания обязательно предлагайте информацию и поддержку пациенту и его семье. Поддержка семей, которые принимают решение о кормлении через зонд, может занять много времени и быть труднодоступной. Но многие семьи сообщают, что они ценили поддержку, которую они получили от профессионалов, которые заботились о близком человеке, который не мог принимать пищу.
Но многие семьи сообщают, что они ценили поддержку, которую они получили от профессионалов, которые заботились о близком человеке, который не мог принимать пищу.
Паллиативная седация — спорный метод, используемый в первую очередь для пациентов с трудноизлечимыми симптомами, которые не ответили на более распространенные методы лечения. При неконтролируемой одышке, тошноте, делирии или боли паллиативная седация может принести облегчение как пациенту, так и членам его семьи, которые должны наблюдать за страданиями пациента. Цель этой техники — облегчить страдания, а не ускорить смерть. Не путайте паллиативную седацию с эвтаназией, предполагающей целенаправленное прекращение жизни пациента.
Лекарства, которые можно использовать для паллиативной седации, включают внутривенное введение или подкожно мидазолам и барбитураты, отдельно или в комбинации. Клиника Майо также одобряет использование пропофола и кетамина.
Решение об использовании паллиативной седации должно приниматься после того, как клиницисты и члены семьи согласятся с тем, что симптомы пациента не реагируют на терапию, и паллиативная седация является единственным вариантом, который потенциально может облегчить симптомы. В исследовании 78 умирающих пациентов с рефрактерными симптомами средняя продолжительность паллиативной седации составила 22 часа. Смерть пациентов не была ускорена; на самом деле у них была более длительная выживаемость, чем у аналогичных пациентов, которым не вводили седативные средства, и семьи считали, что результаты были удовлетворительными. (В систематическом обзоре 10 исследований паллиативной седации средняя продолжительность паллиативной седации составила 2,8 дня.)
В исследовании 78 умирающих пациентов с рефрактерными симптомами средняя продолжительность паллиативной седации составила 22 часа. Смерть пациентов не была ускорена; на самом деле у них была более длительная выживаемость, чем у аналогичных пациентов, которым не вводили седативные средства, и семьи считали, что результаты были удовлетворительными. (В систематическом обзоре 10 исследований паллиативной седации средняя продолжительность паллиативной седации составила 2,8 дня.)
Паллиативная седация должна проводиться под наблюдением или проводиться специалистом по паллиативной помощи или другим специалистом в области паллиативной седации. Семьи должны быть осведомлены об этой технике и о том, чего ожидать. Прежде всего, научите семью тому, что паллиативная седация предназначена для облегчения страданий от рефрактерных симптомов, а не для ускорения смерти.
Обучение и поддержка пациентов и их семей
Предоставление информации о процессе умирания и постановка целей ухода помогает обеспечить участие членов семьи в уходе за своим близким. Чаще всего семьи выбирают в качестве цели комфорт, обычно выражаемый словами «Мы не хотим, чтобы ей было больно» или «Мы просто хотим, чтобы ему было комфортно». Если у пациента есть предварительная инструкция, призывающая к использованию обезболивающего, даже если это может ускорить смерть, обсуждение становится немного проще.
Чаще всего семьи выбирают в качестве цели комфорт, обычно выражаемый словами «Мы не хотим, чтобы ей было больно» или «Мы просто хотим, чтобы ему было комфортно». Если у пациента есть предварительная инструкция, призывающая к использованию обезболивающего, даже если это может ускорить смерть, обсуждение становится немного проще.
Обсуждение целей ухода дает поставщикам медицинских услуг представление о том, что семья думает о конкретных методах лечения (например, опиоидах), и проясняет вопросы или неправильные представления. Имейте в виду, что члены семьи могут быть незнакомы с решениями, которые необходимо принять, поэтому убедитесь, что они полностью понимают варианты. Некоторые семьи выступают против постоянного приема морфина, считая, что он ускоряет смерть; Сообщите им, что он может облегчить одышку и облегчить боль даже в низких дозах. Если вы потратите время на то, чтобы рассказать им о преимуществах обезболивания, это поможет им чувствовать себя более комфортно при лечении.
Также знайте, что, рассматривая вариант «сделать все возможное» для любимого человека, члены семьи могут не понимать, что это значит — какие вмешательства будут предприняты и каковы их последствия. Скажем, например, семья выбирает интубацию и искусственную вентиляцию легких для пациента с тяжелым респираторным заболеванием. Они могут не осознавать, что однажды начав эти вмешательства, может потребоваться их продолжение, иначе пациент умрет. Интубация и вентиляция легких требуют седации, что означает, что пациент не сможет принимать решения. Таким образом, трудное решение о прекращении респираторной поддержки может лечь на семью. (Даже если у пациента есть предварительное распоряжение, пожелания семьи иногда могут преобладать над этим документом.) Обязательно поддерживайте их, когда они принимают эти душераздирающие решения. Например, при обсуждении значения и последствий сердечной реанимации и вентиляции предоставьте членам семьи все необходимые им факты, чтобы они могли принять обоснованные решения, подходящие для пациента.
Обсуждение процесса умирания также может быть полезным. Для многих членов семьи это может быть первый раз, когда они видят, как человек умирает. Попробуйте начать обсуждение с описания того, что происходит, когда кто-то умирает. Например, объясните, как начинается апноэ, упомянув, что пациент будет делать более поверхностные вдохи и периоды апноэ будут более частыми по мере приближения смерти. Это может успокоить семью и облегчить им пребывание у постели больного.
Когда вы ухаживаете за умирающим пациентом, вы оказываете особый вид помощи. День смерти человека должен быть таким же важным, как и день рождения. Каждый пациент уникален и заслуживает уважения. Контроль симптомов EOL, обеспечение поддержки семьи и распознавание уникальных качеств пациента могут сделать эту область сестринской практики столь же полезной, сколь и сложной.
Ивонн Д’Арси — практикующая медсестра отделения боли и паллиативной помощи в больнице Suburban в Бетесде, штат Мэриленд.
На что обратить внимание во время Covid-19 · Страх Нижнего мыса LifeCare
Нижний мыс Страх LifeCare Стареющие родители, Умирающие дома, Хоспис, Lifecare Respons, Паллиативная помощь, Неизлечимый рак
Все мы беспокоимся и переживаем, когда у близкого человека диагностируют серьезное заболевание. По мере прогрессирования заболевания мы замечаем признаки того, что может потребоваться специализированная помощь, такая как хоспис или паллиативная помощь. Мы ненавидим думать, что нашему любимому человеку становится хуже, поэтому мы можем продолжать говорить себе, что это всего лишь временная неудача и что наш любимый человек поправится.
По мере прогрессирования заболевания мы замечаем признаки того, что может потребоваться специализированная помощь, такая как хоспис или паллиативная помощь. Мы ненавидим думать, что нашему любимому человеку становится хуже, поэтому мы можем продолжать говорить себе, что это всего лишь временная неудача и что наш любимый человек поправится.
Часто мы даже не хотим рассматривать эти виды помощи, если только врач не скажет нам, что это необходимо. Но в эпоху COVID-19 люди реже посещают своих врачей, чтобы избежать заражения, а врачи посещают меньше пациентов, чтобы уменьшить распространение вируса. Таким образом, ожидание того, что ваш врач порекомендует лечение, может лишить вашего близкого и вашу семью улучшенного качества жизни, которое обеспечивают хоспис и паллиативная помощь.
Важно знать, что любой человек может направить кого-то в хоспис или паллиативную помощь, чтобы улучшить качество жизни для себя или своих знакомых.
Паллиативная помощь предназначена для людей любого возраста и на любой стадии заболевания, в то время как лечебное лечение продолжается и может начинаться во время постановки диагноза. Этот тип специализированной медицинской помощи помогает контролировать боль, управлять симптомами и снижать стресс, пока кто-то получает лечение, необходимое для лечения его болезни. Лучше всего он работает, когда его добавляют в план ухода за пациентом как можно раньше в процессе заболевания.
Этот тип специализированной медицинской помощи помогает контролировать боль, управлять симптомами и снижать стресс, пока кто-то получает лечение, необходимое для лечения его болезни. Лучше всего он работает, когда его добавляют в план ухода за пациентом как можно раньше в процессе заболевания.
Хосписная помощь предназначена для тех, кто живет с серьезным заболеванием, чей текущий прогноз указывает на то, что ожидаемая продолжительность жизни составляет шесть месяцев или меньше. В основе лежит междисциплинарная команда, которая разрабатывает индивидуальный план ухода, исходя из того, что наиболее важно для пациента и его близкого человека. Важно пройти обследование и начать лечение в хосписе как можно раньше, поскольку исследования доказывают, что уход в хосписе также может увеличить продолжительность жизни. К сожалению, большинство людей ждут, пока не станет слишком поздно, чтобы воспользоваться многими преимуществами, которые предлагает хосписная помощь.
Признаки, которые могут указывать на то, что пора выяснить, подходит ли хоспис или паллиативная помощь вам или близкому вам человеку:
- Необъяснимая потеря веса
- Проведение большего количества времени в постели или кресле — снижение бдительности и увеличение времени сна
- Более частые падения
- Повышенная потребность в лекарствах из-за неконтролируемой боли или симптомов
- Одышка
- Трудности при выполнении повседневных задач: купание, вставание с постели, одевание, ходьба, приготовление и прием пищи
- Увеличение количества обращений в отделение неотложной помощи и множественных госпитализаций
Если вы замечаете эти признаки у себя или у близкого человека, вам следует подумать о том, чтобы поговорить с одним из наших специалистов, позвонив нам по телефону 800-733-1476.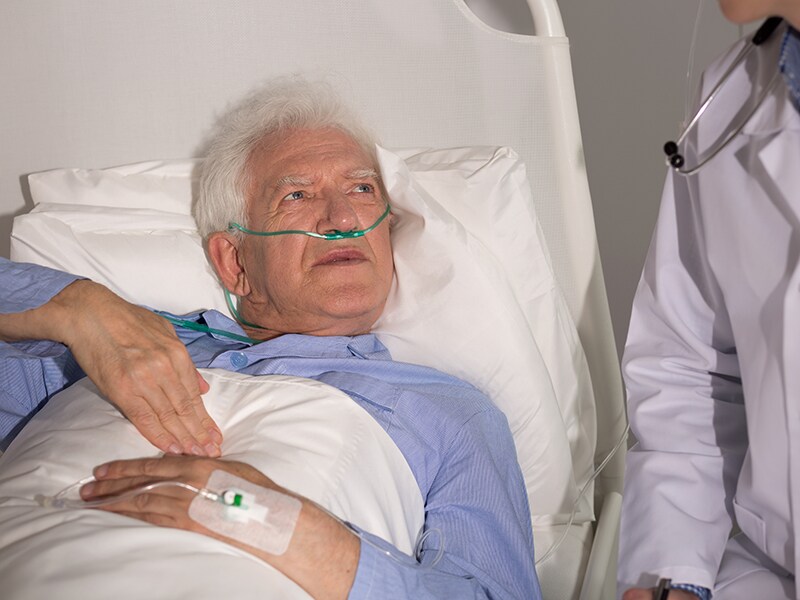 Мы можем запланировать оценку, чтобы определить, может ли какой-либо из этих видов помощи принести пользу вам или вашему близкому человеку.
Мы можем запланировать оценку, чтобы определить, может ли какой-либо из этих видов помощи принести пользу вам или вашему близкому человеку.
Или вы можете пройти наш короткий тест «Какой уход правильный». Это может помочь вам определить, подходит ли вам или вашему близкому хоспис или паллиативная помощь.
Не позволяйте страху перед COVID-19 помешать вам или близкому вам человеку получить необходимую помощь.
Несмотря на обоснованные опасения по поводу инфекции во время этой пандемии, наша команда имеет опыт предотвращения распространения инфекционных заболеваний и проходит рекомендованные CDC процедуры скрининга, чтобы снизить вероятность распространения коронавируса. Уход и поддержка могут быть предоставлены, пока принимаются меры предосторожности, чтобы обеспечить максимальную безопасность пациентов, членов семьи и членов нашей команды.
Если показано лечение в хосписе, мы можем обеспечить необходимый уход и поддержку на дому у пациента. Из-за вируса у пациентов паллиативной помощи есть возможность воспользоваться услугой TeleCare, где регулярные виртуальные визиты используются для снятия боли и симптомов.
