Мозговой инсульт: причины, симптомы и лечение всех видов заболеваний в ФНКЦ ФМБА
Инсульт — общие понятия и описания
Главная » Неврология » Инсульт — общие понятия и описания
Инсульт — это острое нарушение кровообращения в головном мозге, которое появляется в результате образования разрыва (геморрагия) или закупорки (ишемия) одного из сосудов головного мозга или нескольких, питающих ту или иную часть мозга, а также кровоизлияние в оболочки. Таким образом, относительно патогенеза различают геморрагический и ишемический тип инсульта.
Инсульт — это целая группа заболеваний, которая обусловленная сосудистой острой патологией мозга и приводящие к внезапному исчезновению или нарушению мозговой функции, длящихся более суток или даже приводящие к летальному (смертельному) исходу. К инсультам относят субарахноидальное кровоизлияние, кровоизлияние непосредственно в мозг и инфаркт мозга.
Классификация инсульта
Различают основных два вида инсульта:
Ишемический инсульт
Его ещё называют инфаркт мозга. Как правило, данному виду инфаркта подвержены пожилые люди, старше 60-ти лет. Обычно у них в анамнезе отмечаются перенесённые такие заболевания, как инфаркт миокарда, сахарный диабет, нарушение проводимости и/или ритма сердца. Особую роль в развитии инфаркта мозга играют врождённые или приобретённые патологии магистральных артерий или нарушение реологических свойств крови.
Как правило, данному виду инфаркта подвержены пожилые люди, старше 60-ти лет. Обычно у них в анамнезе отмечаются перенесённые такие заболевания, как инфаркт миокарда, сахарный диабет, нарушение проводимости и/или ритма сердца. Особую роль в развитии инфаркта мозга играют врождённые или приобретённые патологии магистральных артерий или нарушение реологических свойств крови.
По этиологии, ишемический инсульт может быть:
- атеротромботический,
- гемодинамический,
- лакунарный,
- по типу микроокклюзии гемореологической.
Геморрагический инсульт
К данному виду инсульта относится внутримозговое нетравматическое кровоизлияние или же субарахноидальное нетравматическое кровоизлияние. Иногда последний вид геморрагического инсульта рассматривают, как отдельный вид.
Относительно времени учёта регрессии неврологического дефицита, различают:
- Преходящие мозгового нарушения кровообращения, когда в течении суток регрессирует неврологический дефицит, относительно непосредственно с инсультом.

- Малый инсульт, когда регрессия неврологического дефицита длится на протяжении 3-х недель с момента начала заболевания.
Этиология инсульта
Этиология инсульта зависит от его типа. Ишемический инсульт, как правило, развивается на фоне тромбирования (закупорки) или сужения сосудов, обычно это артерии, которые питают клетки мозга, что в итоге приводит к гибели последних.
К кровоизлиянию в головной мозг чаще всего, в 80-85% случаев, приводит гипертоническая болезнь. Намного реже причиной могут стать: интоксикация, изменения сосудов мозга, чаще воспалительные, заболевания крови, авитаминоз, атеросклероз и прочие болезни. Кровь из сосудов в мозг поступает или в результате разрыва сосудов или путём диапедеза. В том и другом случае всегда в основе выхода за пределы сосудистого русла крови, лежит ангиодистонические функционально-динамические расстройства не только общей мозговой циркуляции, но и регионарной. При чём, последнее имеет наибольшее значение.
Субарахноидальное кровоизлияние, как правило происходит внезапно в результате разрыва артериальной аневризмы. К травматическим причинам относят черепно-мозговой травмы. Кроме того, субарахноидальное кровоизлияние (САК) может развиться в результате употребления кокоина, артериовенозных мальформаций, опухолевых кровоизлияний (имеет ввиду опухоли мозга или оболочек мозга), серповидно-клеточной анемии, заболеваний или патологий сосудов спинного мозга, при приёме антикоагулянтов, гипофизарном инсульте или нарушении свёртывающей кровяной системы.
Инсульт имеет довольно много вариантов клинического проявления, всё зависит от того какая артерия повреждена или в какую часть мозга было кровоизлияние. Лечение инсульта всего проводится в стационаре под контролем врача.
Другие статьи по неврологии:- Болезнь Хантингтона дифференциальная диагностика и лечение
- Болезнь Хантингтона диагностика
- Хорея Хантингтона симптомы
- Болезнь Хантингтона
- Гепатоцеребральная дистрофия
- Болезнь Вильсона-Коновалова
- Диагностика и лечение инсульта
- Остеохондроз
Качество лекарственной терапии больных, перенесших мозговой инсульт, в зависимости от наличия или отсутствия сахарного диабета, на амбулаторном этапе регистра РЕГИОН-М | Марцевич
Введение
Мозговой инсульт (МИ) — преобладающая причина инвалидизации населения [1][2].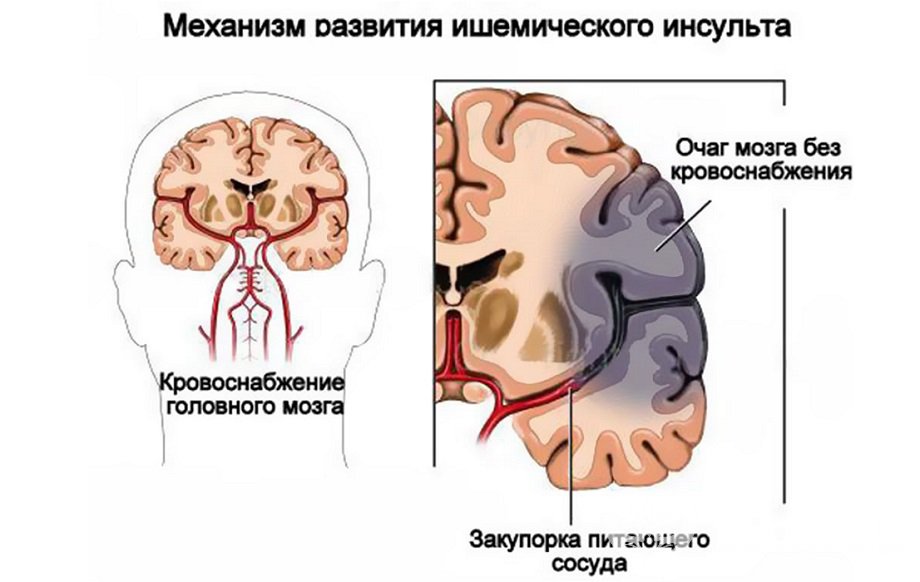 Выжившие после острого нарушения мозгового кровообращения (ОНМК) больные имеют неблагоприятный прогноз жизни, в первую очередь, из-за высокого риска развития сердечно-сосудистых осложнений (ССО) и повторных ОНМК. Так, риск МИ увеличивается в ~10 раз у лиц, перенесших ишемический МИ и транзиторную ишемическую атаку (ТИА), при этом он максимален в ранние сроки с момента заболевания. Вторичная профилактика ССО должна начинаться как можно раньше после развития ОНМК и проводить ее следует в течение всей оставшейся жизни [3][4][5] согласно международным рекомендациям по вторичной профилактике ишемического инсульта [5][6].
Выжившие после острого нарушения мозгового кровообращения (ОНМК) больные имеют неблагоприятный прогноз жизни, в первую очередь, из-за высокого риска развития сердечно-сосудистых осложнений (ССО) и повторных ОНМК. Так, риск МИ увеличивается в ~10 раз у лиц, перенесших ишемический МИ и транзиторную ишемическую атаку (ТИА), при этом он максимален в ранние сроки с момента заболевания. Вторичная профилактика ССО должна начинаться как можно раньше после развития ОНМК и проводить ее следует в течение всей оставшейся жизни [3][4][5] согласно международным рекомендациям по вторичной профилактике ишемического инсульта [5][6].
Одним из значимых факторов риска развития ОНМК и его неблагоприятного исхода является сахарный диабет (СД) [1][7][8]. По данным исследований последних лет >10% больных СД 2 типа погибают в результате ОНМК [9], причем существенная часть этих пациентов умирает в острой стадии болезни. У пациентов, страдающих СД, риск ССО чрезвычайно высок, и профилактика ССО также должна проводиться на постоянной основе [7][8]. Особенности лечения пациентов, перенесших ОНМК, имеющих и не имеющих СД, на амбулаторном этапе остаются недостаточно изученными. В настоящей публикации впервые представлен анализ качества лекарственной терапии (ЛТ), назначенной в поликлинике пациентам, перенесшим ОНМК, в течение 12 мес. до его развития и в период двухлетнего наблюдения, в поликлинической части регистра РЕГИОН-М (РЕГИстр больных, перенесших Острое Нарушение мозгового кровообращения и госпитализированных в московский стационар).
Особенности лечения пациентов, перенесших ОНМК, имеющих и не имеющих СД, на амбулаторном этапе остаются недостаточно изученными. В настоящей публикации впервые представлен анализ качества лекарственной терапии (ЛТ), назначенной в поликлинике пациентам, перенесшим ОНМК, в течение 12 мес. до его развития и в период двухлетнего наблюдения, в поликлинической части регистра РЕГИОН-М (РЕГИстр больных, перенесших Острое Нарушение мозгового кровообращения и госпитализированных в московский стационар).
Данные доказательной медицины свидетельствуют о том, что раннее начало комплекса мер по вторичной профилактике ССО у лиц, перенесших ОНМК, способно значительно снизить риск развития повторного МИ [4][5][6][7][8][9]. Учитывая высокую социальную значимость ОНМК, представляется важным изучить качество медикаментозного лечения в реальной амбулаторно-поликлинической практике пациентов, перенесших ОНМК, в зависимости от наличия и отсутствия СД.
Цель — оценить качество рекомендуемого в поликлинике медикаментозного лечения больных, перенесших острое нарушение мозгового кровообращения (ОНМК), до его развития и в течение 2 лет после выписки, в зависимости от наличия или отсутствия сахарного диабета (СД).
Материал и методы
Подробно протокол всего госпитально-поликлинического регистра РЕГИОН и отдельных его частей был опубликован ранее [10][11][12]. В настоящем фрагменте исследования использованы данные амбулаторной части регистра РЕГИОН-М, в которую были включены все пациенты, прикрепленные к Городской поликлинике № 64 ДЗМ г. Москвы, выписанные из “ГКБ им. Ф.И. Иноземцева г. Москвы” в период с 01.01.2012 по 30.04.2017гг с подтвержденным диагнозом ОНМК: мозговой инсульт или ТИА. Факт прикрепления к поликлинике № 64 устанавливался по адресу регистрации, указанному пациентом или его родственниками при поступлении в стационар.
На основании электронной базы данных поликлиники № 64 были выделены 684 прикрепленных пациента, выписанных за указанный период из стационара с диагнозом “ОНМК/ТИА”. Среди них было 122 пациента с диагнозом СД и 562 без СД. Диагноз СД без указания типа в поликлинической части регистра устанавливался на основании наличия его в амбулаторной карте пациента. В карту индивидуального наблюдения пациента из амбулаторных карт вносились социально-демографические признаки, клинико-анамнестические данные, тип перенесенного ОНМК, факторы риска (ФР), сердечно-сосудистые (ССЗ) и сопутствующие заболевания, результаты по обращениям к врачам поликлиники и назначенных лекарственных препаратов (ЛП) за последние 12 мес. до референсного ОНМК за первые 6 мес. после него и при последнем состоявшемся визите до окончания наблюдения. Проведен анализ информации, внесенной в карту индивидуального наблюдения. Медиана длительности наблюдения составила 22 (интерквартильный размах 13,0-37,75) мес. Качество лекарственной терапии оценивалось на основании ее соответствия современным клиническим рекомендациям по лечению и профилактике ССО у пациентов с ОНМК и СД, явившихся на визит в поликлинику [6][7].
В карту индивидуального наблюдения пациента из амбулаторных карт вносились социально-демографические признаки, клинико-анамнестические данные, тип перенесенного ОНМК, факторы риска (ФР), сердечно-сосудистые (ССЗ) и сопутствующие заболевания, результаты по обращениям к врачам поликлиники и назначенных лекарственных препаратов (ЛП) за последние 12 мес. до референсного ОНМК за первые 6 мес. после него и при последнем состоявшемся визите до окончания наблюдения. Проведен анализ информации, внесенной в карту индивидуального наблюдения. Медиана длительности наблюдения составила 22 (интерквартильный размах 13,0-37,75) мес. Качество лекарственной терапии оценивалось на основании ее соответствия современным клиническим рекомендациям по лечению и профилактике ССО у пациентов с ОНМК и СД, явившихся на визит в поликлинику [6][7].
Статистический анализ был выполнен с помощью пакета программ SPSS Statistics version 23.0, IBM, США. Переменные представлены в виде абсолютного количества и % от общего числа.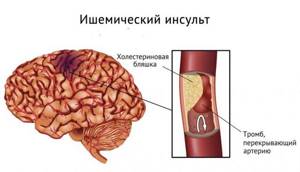 Различия между группами пациентов определялись при помощи критерия χ2 Пирсона, с поправкой Йетса. Уровень статистической значимости был установлен при р<0,05.
Различия между группами пациентов определялись при помощи критерия χ2 Пирсона, с поправкой Йетса. Уровень статистической значимости был установлен при р<0,05.
Результаты
В когорте больных с ОНМК и СД средний возраст пациентов (М±SD) и доля женщин были достоверно выше, по сравнению с пациентами, имеющими ОНМК без СД: 71,5±10,9 vs 68,0±14,7 лет (р<0,05) и 72,1 vs 55,2% (р<0,05), соответственно. По структуре типа перенесенного референсного ОНМК пациенты с СД и без него достоверно не различались. Доля ТИА составила 10,7 vs 18,7%, ишемического инсульта 82,0 vs 73,7%, геморрагического 6,9 vs 7,4% (p>0,05), остальные 0,6 и 0,2% приходились на смешанный ишемический и геморрагический инсульт. На рисунке 1 представлены данные о наличии ССЗ, а также ряда сопутствующих заболеваний у больных, включенных в амбулаторно-поликлиническую часть регистра РЕГИОН-М с наличием и отсутствием СД. Лица с сопутствующим СД по сравнению с пациентами без СД достоверно чаще имели в анамнезе ишемическую болезнь сердца (ИБС) (р<0,001), перенесенный инфаркт миокарда (ИМ) (р<0,001), МИ (р<0,05), хроническую болезнь почек (ХБП) (р<0,001) и хроническую сердечную недостаточность (ХСН) (р<0,001).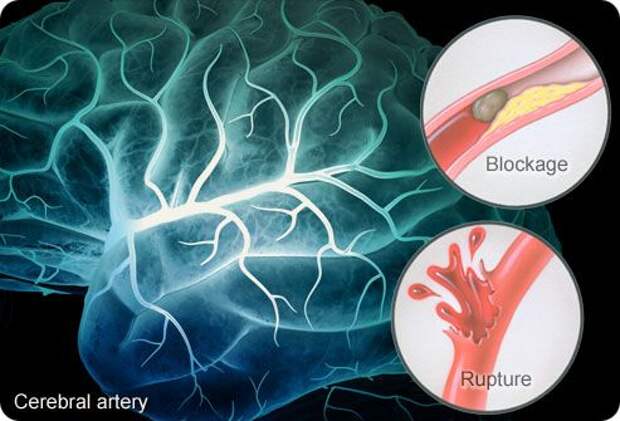 Артериальная гипертония (АГ) имела место у большинства больных с ОНМК, однако у больных СД она выявлялась достоверно чаще — в 95,9 vs 81,3%, соответственно (р<0,001).
Артериальная гипертония (АГ) имела место у большинства больных с ОНМК, однако у больных СД она выявлялась достоверно чаще — в 95,9 vs 81,3%, соответственно (р<0,001).
Рис. 1 Наличие ССЗ и сопутствующих заболеваний у больных, перенесших ОНМК, имеющих и не имеющих СД.
Примечание: ОНМК в ан. — ОНМК в анамнезе, ИБС в ан. — ИБС в анамнезе, ХБЛ — хроническая болезнь легких.
Данные о таких ФР, как курение, ожирение, гиперлипидемия, гиподинамия, отягощенная наследственность по ранним ССЗ, злоупотребление алкоголем отсутствовали в подавляющем большинстве амбулаторных карт больных, сравнение частоты наличия ФР в группах пациентов с СД и без него не проводилось.
Поскольку качество ЛТ оценивали по данным амбулаторных карт пациентов, был проведен сравнительный анализ основных клинико-анамнестических и демографических характеристик пациентов, посещавших и не посещавших поликлинику на различных этапах наблюдения. Пациенты с СД находились под наблюдением врачей чаще, чем без СД: 90,2 vs 81,7% (р<0,05) до референсного ОНМК, 74,6 и 61,7% (р<0,001) до 6 мес. , а в период после 6 мес. и до завершения периода наблюдения — 85,2 и 76,9%, соответственно (р<0,01). Посещали поликлинику до референсного ОНМК преимущественно коморбидные пациенты, имеющие СД — 19 vs 10%, не страдающие СД (р<0,05), или инвалидность — 38,5 vs 11,3% (р<0,001), ОНМК в анамнезе — 20,2 vs 5,2% (р<0,001), ИБС — 69 vs 26% (р<0,001), ХСН — 17 vs 6% (р<0,01), фибрилляцию предсердий (ФП) — 18 vs 8,7% (р<0,05), АГ — 92 vs 45% (р<0,001), ХБП — 16,5 vs 2,6% (р<0,001), онкологические заболевания — 10,4 vs 4,3% (р<0,01). Пациенты, посещавшие поликлинику после ОНМК, также чаще имели инвалидность, СД и сопутствующие заболевания.
, а в период после 6 мес. и до завершения периода наблюдения — 85,2 и 76,9%, соответственно (р<0,01). Посещали поликлинику до референсного ОНМК преимущественно коморбидные пациенты, имеющие СД — 19 vs 10%, не страдающие СД (р<0,05), или инвалидность — 38,5 vs 11,3% (р<0,001), ОНМК в анамнезе — 20,2 vs 5,2% (р<0,001), ИБС — 69 vs 26% (р<0,001), ХСН — 17 vs 6% (р<0,01), фибрилляцию предсердий (ФП) — 18 vs 8,7% (р<0,05), АГ — 92 vs 45% (р<0,001), ХБП — 16,5 vs 2,6% (р<0,001), онкологические заболевания — 10,4 vs 4,3% (р<0,01). Пациенты, посещавшие поликлинику после ОНМК, также чаще имели инвалидность, СД и сопутствующие заболевания.
Далее была проанализирована частота назначения врачами поликлиники ЛТ пациентам, перенесшим ОНМК, на различных этапах наблюдения и ее соответствие современным клиническим рекомендациям [6][7][8]. Поскольку ноотропные, антиоксидантные и иные нейротропные препараты не имеют убедительной доказательной базы в отношении способности улучшать прогноз пациентов, перенесших ОНМК, они в проведенный анализ не включались.
В таблице 1 приведена частота назначения ЛП различных групп до развития референсного ОНМК у больных СД (n=110) и без него (n=459), посещавших поликлинику в течение 12 мес. до развития ОНМК. Достоверных различий в частоте назначения различных групп ЛП у лиц с СД и без него не выявлено, за исключением гипогликемических. До референсной госпитализации ЛП в поликлинике были рекомендованы 67,3% больным СД и 54,7% пациентам без СД (p<0,01), хотя первые посещали поликлинику достоверно чаще — 90,2 vs 81,7% (p<0,05). Статины были назначены лишь 15,5% пациентам с СД и 14,4% без него, дезагреганты 32,7 и 25,5%, ингибиторы ангиотензинпревращающего фермента (иАПФ)/блокаторы рецепторов ангиотензина II (БРА) — 41,4 и 37,9%, бета-адреноблокаторы (β-АБ) — 9,1 и 7,8%, соответственно.
Учитывая тот факт, что большинство пациентов имели высокий риск развития ССО даже до референсного ОНМК, частота назначения основных групп ЛП, способных снизить риск ССО, была крайне низка. Так, из 112 пациентов с ФП только 19 (17%) получали оральные антикоагулянты (варфарин или новые оральные антикоагулянты — НОАК) до референсного ОНМК. При наличии у 61,8% пациентов ИБС, у 92% — АГ, у 17,8% — СД, статины получали 17% до референсного ОНМК, хотя должны были получать большинство. С дезагрегантами (препараты аспирина и клопидогрел) ситуация была не лучше, их получали 18% пациентов, хотя должны были получать не <62%. При наличии АГ у 92% пациентов только 40% получали иАПФ/ БРА, 15% − β-АБ до референсного ОНМК.
При наличии у 61,8% пациентов ИБС, у 92% — АГ, у 17,8% — СД, статины получали 17% до референсного ОНМК, хотя должны были получать большинство. С дезагрегантами (препараты аспирина и клопидогрел) ситуация была не лучше, их получали 18% пациентов, хотя должны были получать не <62%. При наличии АГ у 92% пациентов только 40% получали иАПФ/ БРА, 15% − β-АБ до референсного ОНМК.
В таблице 2 представлена частота назначения врачами поликлиники ЛП различных групп на постгоспитальном этапе у 438 больных (с СД n=91 и без него n=347), явившихся в поликлинику в течение первых 6 мес. после развития референсного ОНМК. Пациентам с СД достоверно чаще, чем лицам без сопутствующего СД, назначались гипогликемические препараты, клопидогрел, β-АБ и антагонисты кальция (АК). В отношении других классов ЛП достоверных различий выявлено не было. Как и на догоспитальном этапе, частота назначения основных групп ЛП, показанных для вторичной профилактики ССО, была недостаточна. Так, частота назначения дезагрегантов/антикогулянтов и статинов не превышала 60-70 и 40% в обеих группах, соответственно.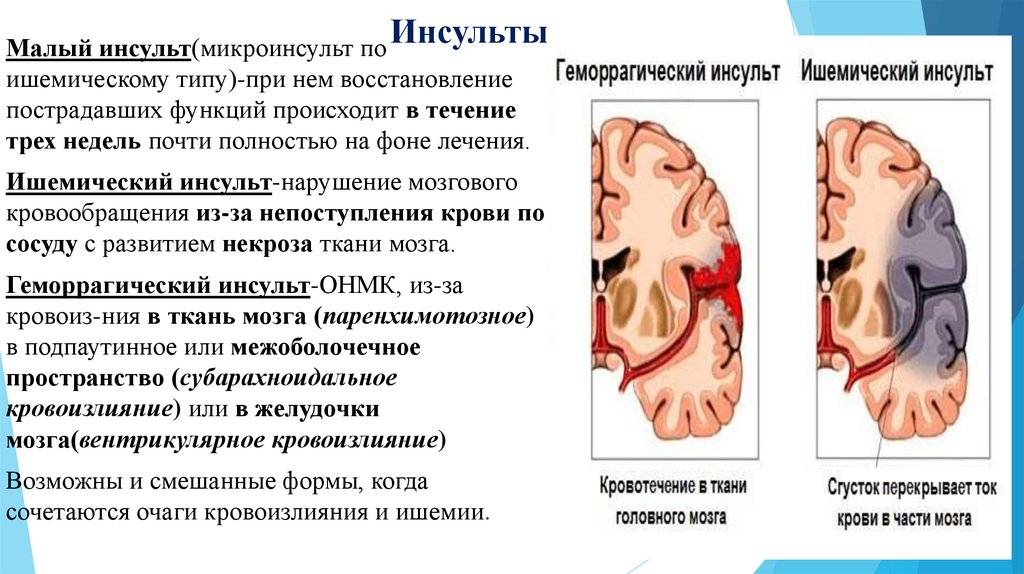
В таблице 3 представлена частота назначения в поликлинике ЛП различных групп у 536 больных: с СД (n=104) и без него (n=432) через ≥6 мес. после развития референсного ОНМК до окончания периода наблюдения. Достоверных различий в частоте назначения ЛП в подгруппах пациентов с СД и без него не выявлено. При этом наблюдалось снижение частоты назначения дезагрегантов и статинов через 6 мес. после перенесенного ОНМК по сравнению с первыми 6 мес. наблюдения после ОНМК. Препараты аспирина были назначены 56% пациентов с СД и 50,7% без СД в первые 6 мес. и только 26,9% пациентов с СД и 33% без СД позднее 6 мес. (p<0,05 для обеих групп), а статины — 39,6% пациентов с СД и 39,2% без СД в первые 6 мес. и 28,8% пациентов с СД и 27% пациентов без СД позднее 6 мес. (p<0,05 для обеих групп).
Таблица 1
Частота назначения ЛП различных групп на достгоспитальном этапе (в течение 12 мес. до развития референсного ОНМК) у больных СД и без СД (n=569)
Примечание: нд — недостоверно.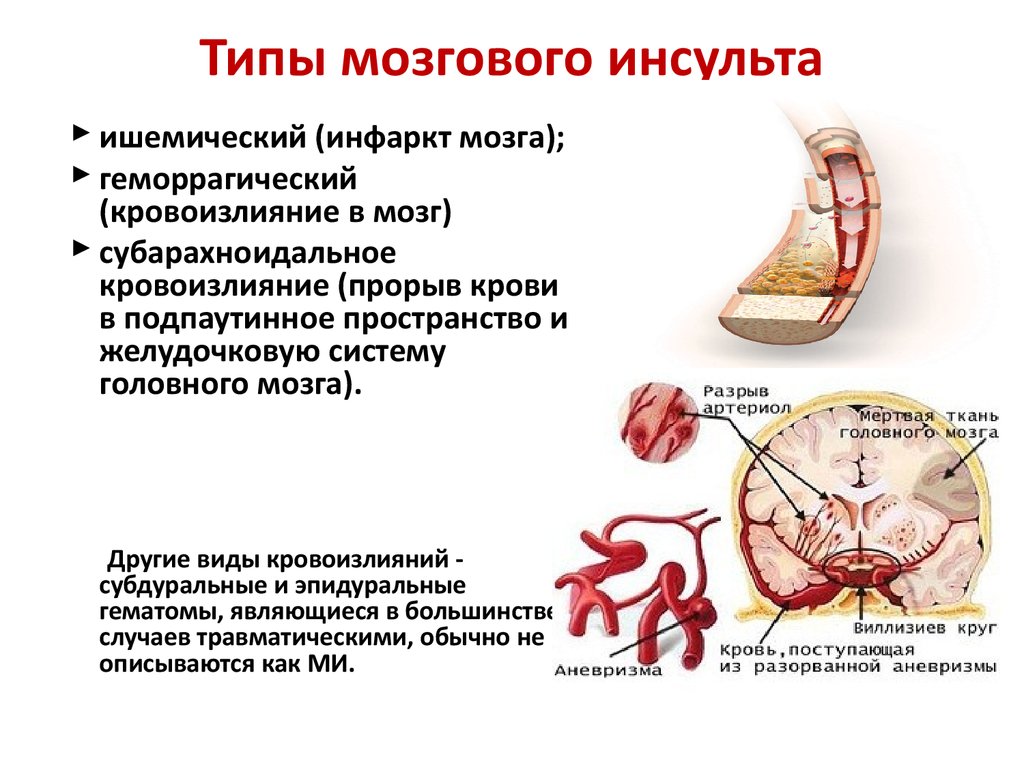
Таблица 2
Частота назначения ЛП различных групп на постгоспитальном этапе (в первые 6 мес. после ОНМК) у больных СД и без СД (n=438)
Примечание: нд — недостоверно.
Таблица 3
Частота назначения ЛП различных групп на отдаленном этапе (позже 6 мес. после развития ОНМК) у больных СД и без СД (n=536)
Примечание: нд — недостоверно.
Обсуждение
Поскольку оценка качества терапии, назначенной врачами поликлиники на разных этапах наблюдения, проводилась на основании данных амбулаторных карт пациентов, посещавших поликлинику до и/или после референсного ОНМК, был проведен анализ обращаемости пациентов в поликлинику по месту регистрации. Установлено, что посещали поликлинику в течение последних 12 мес. до референсного события и после него примерно равное количество пациентов — 90% больных с СД и 83% без него. Углубленный анализ показал, что посещали поликлинику преимущественно пациенты, имеющие СД или инвалидность, а также имеющие иные хронические заболевания, т. е. наиболее тяжелые пациенты.
е. наиболее тяжелые пациенты.
Тот факт, что более половины пациентов, имевших высокий риск ССО до развития референсного ОНМК в связи с наличием СД, ССЗ, таких как ИБС, ФП, ХСН, АГ и перенесенного ранее ИМ, не получали адекватной ЛТ, а данные о наличии ФР и вредных привычек в подавляющем большинстве амбулаторных карт больных отсутствовали, свидетельствует о недостаточном внимании врачей поликлиники к первичной и вторичной профилактике ССО. Такие пациенты должны были получать, как минимум, статины, дезагреганты или антикоагулянты, иАПФ/БРА и β-АБ. Так, на момент развития ОНМК лишь ~17% пациентов получали статины, ~18% — дезагреганты, 40% — иАПФ/БРА, 15% — β-АБ, что явно недостаточно. Схожая ситуация была выявлена в регистре ЛИС-2 (Люберецкое исследование смертности больных, перенесших острый инфаркт миокарда-2), где до развития референсного ОНМК лечение в поликлинике получала лишь малая часть пациентов [13]. Наличие СД практически не влияло на качество первичной и вторичной профилактики ССЗ на догоспитальном этапе, хотя у лиц с СД коррекцию ФР следует проводить особенно агрессивно [7][8].
После референсного ОНМК частота назначения ЛП в поликлинике за первые 6 мес. после перенесенного ОНМК достоверно увеличилась как в группе больных с СД, так без него, для статинов, дезагрегантов, иАПФ/БРА и β-АБ, однако все еще оставалась недостаточной. Спустя 6 мес. после выписки частота назначения ЛП в группах с СД и без СД, снизилась на 50 и 33%, соответственно, для статинов, на 30 и 35% для дезагрегантов, на 40 и 31% для иАПФ/БРА (p<0,05), и осталась прежней для β-АБ.
Достоверных различий в частоте назначения большинства групп ЛП пациентам с СД и без него как до, так и после референсного ОНМК, не было, за исключением гипогликемических на всех этапах, и более частого назначения β-АБ, АК и клопидогрела пациентам с СД за первые 6 мес. после выписки.
Таким образом, значительная часть пациентов с очень высоким риском ССО не получала весь необходимый для вторичной профилактики ССО набор ЛП. В доступной литературе мы не встретили публикаций, в которых бы приводили данные об амбулаторном лечении пациентов, перенесших ОНМК, направленном на вторичную профилактику МИ и других ССО. Схожие тенденции были выявлены в регистре ПРОГНОЗ ИБС (Факторы, определяющие ПРОГНОЗ жизни больных стабильно протекающей Ишемической Болезнью Сердца), где наблюдалось увеличение частоты применения дезагрегантов, статинов, β-АБ, иАПФ/БРА у пациентов со стабильной ИБС, выписанных из стационара после проведения коронароангиографии, и последующее ее снижение через 4 и 7 лет наблюдения [14].
Схожие тенденции были выявлены в регистре ПРОГНОЗ ИБС (Факторы, определяющие ПРОГНОЗ жизни больных стабильно протекающей Ишемической Болезнью Сердца), где наблюдалось увеличение частоты применения дезагрегантов, статинов, β-АБ, иАПФ/БРА у пациентов со стабильной ИБС, выписанных из стационара после проведения коронароангиографии, и последующее ее снижение через 4 и 7 лет наблюдения [14].
Важность вторичной профилактики у пациентов, перенесших ОНМК, иллюстрируют результаты российского клинического исследования [15], проведенного неврологами, занимающимися реабилитацией пациентов после перенесенного ОНМК на амбулаторном этапе. Авторами была выявлена значительная разница в уровне смертности среди пациентов, получавших эффективную вторичную профилактику ССО, как немедикаментозную (отказ от вредных привычек, повышение физической активности, снижение веса), так и медикаментозную. Большинство (n=281) больных проводили эффективную профилактику повторного МИ. И только небольшая часть (45 из 326) больных отказывались от регулярного приема ЛП, несмотря на наличие рекомендаций врача. Смерть от МИ, ИМ или острая сосудистая смерть развилась у 5% больных, которые принимали регулярное лечение, и у 47% больных, которые постоянно не принимали ни антигипертензивные препараты, ни антитромбоцитарные средства после перенесенного ОНМК. От регулярного приема лекарственных средств достоверно чаще отказывались мужчины, курильщики, злоупотребляющие алкоголем пациенты. В группе больных, перенесших ишемический МИ и регулярно принимающих лечение, значительно реже, чем у пациентов с отказом от регулярного лечения, возникали повторный МИ (3 и 16%, соответственно), ИМ (1 и 7%), смерть от ССЗ (1 и 13,8%).
Смерть от МИ, ИМ или острая сосудистая смерть развилась у 5% больных, которые принимали регулярное лечение, и у 47% больных, которые постоянно не принимали ни антигипертензивные препараты, ни антитромбоцитарные средства после перенесенного ОНМК. От регулярного приема лекарственных средств достоверно чаще отказывались мужчины, курильщики, злоупотребляющие алкоголем пациенты. В группе больных, перенесших ишемический МИ и регулярно принимающих лечение, значительно реже, чем у пациентов с отказом от регулярного лечения, возникали повторный МИ (3 и 16%, соответственно), ИМ (1 и 7%), смерть от ССЗ (1 и 13,8%).
Заключение
Лекарственная терапия пациентов с перенесенным ОНМК, как при наличии СД, так и без него, рекомендуемая в поликлинике по месту жительства, характеризуется недостаточной частотой назначения основных групп препаратов, необходимых для вторичной профилактики ССО на всех этапах наблюдения.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Симптомы, причины и лечение церебрального инсульта или приступа
Симптомы, причины и лечение церебрального инсульта или приступа | MedantaЧто такое церебральный инсульт?
Прерывание или уменьшение кровоснабжения головного мозга вызывает мозговой инсульт. Нехватка снабжения приводит к недостатку кислорода или питательных веществ в мозге и приводит к смерти головного мозга.0014
Симптомы
Следующие симптомы указывают на мозговой инсульт:
- Ощущение онемения или паралича лица, ноги или руки.
- Проблемы со зрением одним или обоими глазами.
- Постоянная головная боль.
- Проблемы с ходьбой, речью или пониманием.
- Головокружение или нарушение координации.
- Трудности с контролем мочевого пузыря или дефекации.
- Депрессия.
- Паралич или слабость с одной или обеих сторон тела.
Показать больше Скрыть
Причины
Основными причинами мозгового инсульта являются:
- Малоподвижный образ жизни.

- Ожирение или избыточный вес.
- Чрезмерное употребление алкоголя.
- Незаконное употребление наркотиков.
- Высокое кровяное давление.
- Потребление табака.
- Высокий уровень холестерина.
- Диабет.
- Обструктивное апноэ сна.
- Сердечно-сосудистые заболевания.
- Семейный анамнез и возраст также являются факторами риска.
Показать больше Скрыть
Риски
К основным факторам риска этого заболевания относятся:
- Высокое кровяное давление.
- Диабет.
- Курение.
- Ожирение.
Показать больше Скрыть
Профилактика
Чтобы предотвратить возникновение этого заболевания, необходимо позаботиться о следующем:
- Не курить.
- Соблюдайте сбалансированную диету.
- Регулярно проверяйте артериальное давление
Показать больше Скрыть
Как это диагностируется?
В Medanta первым этапом диагностики является физикальное обследование для изучения истории болезни и семейного анамнеза пациента. Дополнительные диагностические тесты включают:
Дополнительные диагностические тесты включают:
…
В Medanta первым этапом диагностики является физикальное обследование для изучения истории болезни пациента и его семьи. Дополнительные диагностические тесты включают:
Анализы крови
КТ (компьютерная томография)
МРТ (магнитно-резонансная томография)
УЗИ сонных артерий.
Cerebral angiogram
Echocardiogram
Use of drugs
Carotid endarterectomy
Angioplasty
Surgical treatment
Consult with experienced doctors
Д -р Арун Гарг
Директор
Институт нейронаузинтов
Профиль профиль
Доктор Гаурав Гоэль
Директор и глава — Нейро вмешательство. Председатель — Эндоскопический портал малоинвазивной нейрохирургии
Институт неврологии
Просмотр профиля
Имя:
Мобильный номер:
Код проверки:
Пользователь соглашается и признает, что он прочитал, понял и принимает положения и условия, содержащиеся в брошюре, прилагаемой к Устройству (« .
.
Настоящим Пользователь соглашается и признает, что Устройство (аппаратное и программное обеспечение), используемое при предоставлении
услуг Medanta предоставляется на условиях «как есть» и «по мере доступности» через Alivecor India Private.
Ограничено. Меданта никоим образом не поддерживает и не продвигает Устройство, а также не несет ответственности.
за любые претензии, заверения или гарантии, явные или подразумеваемые, в отношении безопасности, надежности,
долговечность и производительность устройства.
Когда-то использованные услуги не могут быть отменены, за исключением случаев, когда Пользователь просит отменить
услугу в день покупки, в этом случае полная сумма платы за услугу возвращается Пользователю.
при условии, что Устройство не распаковывалось.
 medanta.org. Расширенная программа, которой воспользовался Пользователь, активируется автоматически по истечении срока действия существующей программы услуг.
medanta.org. Расширенная программа, которой воспользовался Пользователь, активируется автоматически по истечении срока действия существующей программы услуг.В случаях, когда Пользователь решил воспользоваться Услугами через арендованное Устройство, возвращается возвращаемый залог. Сумма в размере 5 000 фунтов стерлингов (« Сумма депозита ») применяется и оплачивается Пользователем. Возврат депозита Сумма подлежит возврату Устройства в рабочем и неповрежденном состоянии. Возврат депозита Сумма должна быть внесена тем же способом оплаты, что и при покупке, в случаях, когда Пользователь лично посещает Меданту для возврата Устройства. Если Пользователь решит вернуть Устройство по почте, Сумма депозита будет возвращена в электронном виде через НЕФТЬ или банковским переводом через Medanta в течение семь (7) рабочих дней с момента получения Устройства и получения отсканированного изображения/копии Аннулированного Чек банковского счета Пользователя.
По истечении срока действия услуг (либо по количеству ЭКГ, либо по продолжительности программы), предоставленных
Пользователь, Устройство должно быть возвращено в течение десяти (10) дней, в противном случае Сумма Депозита будет
конфискован.
Обратите внимание, что комплект ЭКГ или возвращаемый депозит за устройство не подлежат передаче от одного пациента к другому.
еще один.
Спасибо за отзыв.
Восстановление кишечника сохраняет функцию мозга после инсульта
Резюме: Трансплантация кишечных эпителиальных стволовых клеток от здоровых доноров снизила смертность от инсульта, уменьшила объем мертвой мозговой ткани и кишечную проницаемость, а также предотвратила вызванное инсультом снижение когнитивных функций.
Источник: Texas A&M
Инсульт является основной причиной смерти, деменции и серьезной длительной инвалидности. По данным Американской кардиологической ассоциации, у пациентов, перенесших инсульт, также повышен риск депрессии, что негативно влияет на функциональное и когнитивное восстановление.
Единственный одобренный Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) препарат для лечения инсульта, который представляет собой тип рекомбинантного тканевого активатора плазминогена, должен вводиться в течение определенного периода времени после начала инсульта и имеет ограниченный успех.
Чтобы улучшить исходы инсульта, ученые из Медицинской школы Техасского университета A&M проводят новаторские исследования связи между вызванной инсультом проницаемостью кишечника или негерметичностью и когнитивными нарушениями.
Команда Texas A&M исследовала новую идею о том, может ли трансплантация кишечных эпителиальных стволовых клеток (IESCs) от здоровых доноров восстановить кишечный барьер после инсульта и улучшить исходы инсульта.
Результаты их доклинического исследования, опубликованные в журнале Brain, Behavior, and Immunity , показывают, что трансплантация IESC снижает смертность от инсульта, уменьшает объем мертвых тканей и негерметичность кишечника, а также предотвращает вызванные инсультом когнитивные нарушения.
Согласно недавним исследованиям, у двух третей пациентов с инсультом разовьются когнитивные нарушения, а у одной трети всех пациентов с инсультом разовьется деменция, поэтому существует острая необходимость в более эффективных методах лечения инсульта, которые сохраняют когнитивные функции после острого инсульт, и которые остаются защитными в последующие недели.
Хотя традиционные исследования в области лечения инсульта сосредоточены на головном мозге, кишечник рано и быстро реагирует на инсульт изменениями, которые могут предшествовать многим воспалительным явлениям, связанным с заболеванием, вызванным инсультом. Эти изменения в кишечнике, такие как повышенная проницаемость, вероятно, приводят к перемещению продуктов, которые синтезируются в кишечнике, в кровоток.
Многие из этих продуктов являются токсичными и, следовательно, могут усиливать воспаление и усугублять повреждение головного мозга, вызванное инсультом.
Данные различных исследований показывают, что IESC восстанавливают кишечник и снижают его проницаемость. После инсульта эти восстановительные процессы могут иметь решающее значение для сохранения когнитивной функции.
«Очевидно, что ось кишечник-мозг участвует в травмах после инсульта», — сказала Фарида Сохрабджи, доктор философии, профессор Риджентс, руководитель отдела неврологии и экспериментальной терапии и старший автор исследования.
«Учет влияния здоровья кишечника на мозг после инсульта может позволить нам более эффективно продвигать методы лечения инсульта».
Имея это в виду, Сохрабджи и ее команда трансплантировали первичные IESC от здоровых доноров после инсульта в доклинической модели. IESC от молодых доноров восстанавливали структуру кишечника и снижали проницаемость кишечника и, следовательно, снижали уровень в крови белков и других молекул, токсичных для клеток головного мозга.
Трансплантация IESC также предотвращала депрессивное поведение и когнитивные нарушения в течение нескольких недель после инсульта. Трансплантация IESC от пожилых доноров не улучшала исходы инсульта, что указывает на то, что успешная трансплантация зависит от возраста донора.
Хотя традиционные исследования в области лечения инсульта сосредоточены на головном мозге, кишечник рано и быстро реагирует на инсульт изменениями, которые могут предшествовать многим воспалительным явлениям, связанным с заболеванием, вызванным инсультом. Изображение находится в открытом доступе
Изображение находится в открытом доступеВсе еще находящееся на доклинической стадии, это исследование подчеркивает важность раннего терапевтического вмешательства после инсульта и определяет будущие направления работы.
«В будущих исследованиях будет изучено уточнение дозировки и сроков применения протокола», — сказал Сохрабджи. «Систематическое изучение стареющих стволовых клеток также важно для объяснения того, почему пожилые пациенты переносят более тяжелые инсульты».
Сохрабджи, нейробиолог, внесший значительный вклад в литературу по патогенезу инсульта, объяснила, что это доклиническое исследование было инициировано Катиреш Кумар Мани, доктором философии, младшим научным сотрудником в ее лаборатории.
Мани, изучающая биологию кишечника, получила грант от Американской кардиологической ассоциации для поддержки этого проекта. Объединение их опыта позволило им вывести исследования в области терапии инсульта на новую территорию с впечатляющими результатами.
Они также получили щедрый грант от WoodNext Foundation , который способствует их инновационным исследованиям.
«В конечном счете, это исследование, как ожидается, продвинет разработку новых методов лечения, которые воздействуют на эпителий кишечника и восстанавливают его, чтобы помочь смягчить инвалидность после инсульта, — сказал Сохрабджи, — но предпосылка — что стволовые клетки кишечника могут быть терапевтически ценными за пределами кишечника — может быть рассмотрен для лечения гораздо большего числа неврологических заболеваний».
См. также
Автор: Лесли Хентон
Источник: Texas A&M
Контакт: Лесли Хентон – Texas A&M
Изображение: Изображение находится в открытом доступе
«Трансплантация кишечных эпителиальных стволовых клеток как новая терапия цереброваскулярного инсульта» Farida Sohrabj et al. Мозг, поведение и иммунитет.0195
Почти у 2/3 rds выживших после инсульта наблюдаются сосудистые когнитивные нарушения, а у трети пациентов с инсультом через 1–3 года после инсульта развивается деменция. Эти ужасные последствия подчеркивают необходимость эффективных методов лечения инсульта.
Эти ужасные последствия подчеркивают необходимость эффективных методов лечения инсульта.
Помимо повреждающего воздействия на головной мозг, инсульт быстро нарушает регуляцию кишечного эпителия, что приводит к повышению уровня в крови воспалительных цитокинов и токсичных кишечных метаболитов из-за «дырявого» кишечника.
Мы проверили, улучшит ли восстановление кишечника с помощью трансплантации кишечных эпителиальных стволовых клеток (IESC) восстановление после инсульта.
Органоиды, содержащие IESC, полученные от молодых крыс, трансплантированных взрослым крысам после инсульта, вводились в кишечник, восстанавливали вызванную инсультом дисморфологию кишечника и снижали проницаемость кишечника, а также снижали циркулирующие уровни эндотоксина LPS и воспалительного цитокина IL-17A.
Примечательно, что трансплантаты IESC также улучшили вызванную инсультом острую (4 дня) сенсорно-моторную инвалидность и хроническую (30 дней) когнитивно-аффективную функцию. Более того, IESC от старых животных демонстрировали признаки старения и не оказывали терапевтического воздействия на инсульт.


