Лечение тотальной деменции при паркинсонизме: Подходы к оптимизации лечения депрессии у пациентов с болезнью Паркинсона
Подходы к оптимизации лечения депрессии у пациентов с болезнью Паркинсона
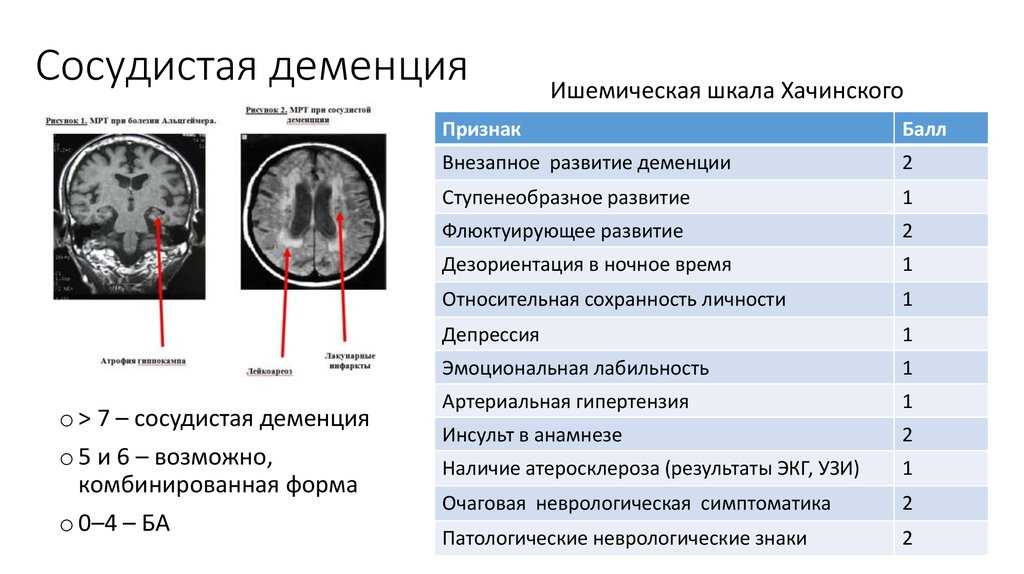
Патологическое старение в своей основе часто имеет атрофию клеток определенных отделов головного мозга. Психические расстройства, сопровождающие подобные атрофические процессы, выделяют в отдельную группу психических заболеваний позднего возраста. Данное обобщение основывается на ряде сходных для этих форм характеристик [4]: медленное малозаметное начало и хроническое неуклонно прогредиентное течение; неблагоприятный прогноз вследствие необратимости болезненного процесса; постепенное развитие слабоумия вплоть до «тотальной» деменции; доминирование эндогенного патологического процесса; атрофия паренхимы головного мозга и заместительная гидроцефалия.
К группе дегенеративных заболеваний относится болезнь Паркинсона (БП).
БП, или дрожательный паралич, был описан в 1817 г. Это заболевание относят к развивающимся в позднем возрасте дегенеративно-атрофическим заболеваниям экстрапирамидной системы головного мозга. Средний возраст больных к периоду начала болезни составляет 50- 60 лет. Течение болезни обычно хронически-прогредиентное [4, 9, 10].
Средний возраст больных к периоду начала болезни составляет 50- 60 лет. Течение болезни обычно хронически-прогредиентное [4, 9, 10].
Этой патологии подвержены в среднем от 100 до 300 человек на 100 000 населения во всем мире. В России больные с БП составляют от 8 до 10% популяции. Качество жизни пациентов с БП резко снижено. Такие больные, постепенно по мере течения заболевания инвалидизируясь и нуждаясь в социальной реабилитации и длительном уходе [1, 2], создают значительное бремя для общества. В связи с увеличением продолжительности жизни и постарением населения число больных паркинсонизмом постоянно увеличивается, что повышает актуальность рассматриваемой проблемы [24, 32].
Цель данной публикации — обсуждение возможностей проведения адекватной антидепрессивной терапии у пациентов с БП и оценка влияния этой терапии на клиническую выраженность моторных нарушений и симптомы депрессии при паркинсонизме.
Депрессию относят к немоторным симптомам БП, которые также представлены вегетативными нарушениями, тревожностью и психотическими расстройствами (ночные кошмары, галлюцинации, иллюзии и психомоторное возбуждение во сне).
Депрессия при БП может носить эндогенный и экзогенный характер. Эндогенная депрессия связана с дефицитом моноаминов, характерным для данного заболевания; экзогенная депрессия связана с реакцией больного на внешние факторы, в данном случае речь идет о реакции на прогрессирующее хроническое заболевание, его неблагоприятные социально-экономические перспективы и изменения во взаимоотношениях с коллегами и родственниками [6].
Наличие депрессии при БП коррелирует с более быстрым прогрессированием когнитивых (регуляторных) нарушений, появлением психотических симптомов (малых зрительных галлюцинаций, иллюзий). Вместе с тем показано, что коррекция депрессии оказывает положительное воздействие как на двигательные, так и недвигательные проявления БП — когнитивные функции, нарушения сна и боль [8, 10, 22].
Вместе с тем показано, что коррекция депрессии оказывает положительное воздействие как на двигательные, так и недвигательные проявления БП — когнитивные функции, нарушения сна и боль [8, 10, 22].
Существенную роль в формировании депрессии при БП играют психологические факторы. Наблюдения показывают, что наиболее выраженный стресс у пациентов обычно вызывают начало болезни и установление диагноза, а затем тяжелые осложнения на поздних этапах болезни. С этим согласуется преимущественное выявление депрессивных расстройств на самых ранних и поздних стадиях заболевания. Дефицит дофамина в головном мозге при БП, возможно, дополнительно способствует снижению адаптации к стрессогенным факторам, которыми являются болезнь и связанные с ней изменения качества жизни. В основе данного предположения лежат данные о повышении утилизации дофамина в условиях экспериментального стресса [9, 23].
Одну из главных ролей в генезе депрессии при БП играют такие изменения физиологического метаболизма мозга, как недостаток выработки дофамина, а также нарушение выработки норадреналина и серотонина. Полагают, что дисфункция серотонинергической системы ответственна за возникновение у больных БП тревоги и агрессии [28, 29].
Полагают, что дисфункция серотонинергической системы ответственна за возникновение у больных БП тревоги и агрессии [28, 29].
Одним из возможных предрасполагающих факторов развития депрессии при БП является наличие наследственной отягощенности депрессивными расстройствами. У близких родственников пациентов с БП отмечена большая частота депрессии. Обсуждалась связь частоты депрессии с латерализацией симптомов БП, а именно с преобладанием тяжести двигательных нарушений справа, что косвенно свидетельствует о большей значимости левого полушария в формировании депрессивных расстройств [1, 10].
Для диагностики большой депрессии необходимо наличие депрессивного настроения и/или ангедонии в течение не менее 2 нед и более в сочетании с 5 или более из нижеприведенных критериев, вызывающих значительный дистресс или нарушение повседневной активности. Малая депрессия диагностируется при сочетании с 2-5 критериями. Если депрессивное настроение сочетается с 2 другими симптомами и наблюдается в течение большинства дней за последние 2 года, диагностируется дистимия [3, 29].
Согласно DSM-IV, существуют следующие критерии депрессии: подавленное настроение; снижение интересов и способности испытывать удовольствие; значительное снижение или повышение аппетита и массы тела; нарушения сна; психомоторное возбуждение или заторможенность; повышенная утомляемость, упадок сил; ощущение собственной бесполезности, идеи виновности; снижение способности к концентрации внимания, принятию решений; повторяющиеся мысли о смерти, суицидальные попытки.
Частыми признаками депрессии у больных БП служат стойкое угнетение настроения, ангедония (неспособность испытывать удовольствие), дисфория, снижение аппетита, изменение массы тела, быстрая утомляемость, нарушение сна, низкая самооценка, повышенная тревожность, раздражительность, суицидальные мысли, пессимистические мысли о будущем. В то же время такие характерные для эндогенной депрессии симптомы, как чувство вины, ощущение жизненного краха или самобичевание, встречаются при БП существенно реже [30].
Депрессия может появиться на любом этапе течения БП, но нередко (в 30% случаев) предшествует его первым клиническим двигательным проявлениям (гипокинезия, ригидность, тремор покоя) [13].
Важно отметить возможную связь депрессии и степени тяжести двигательных симптомов заболевания. В ходе некоторых работ были выявлены позитивные корреляции между частотой депрессии и тяжестью брадикинезии. Наряду с этим было отмечено, что депрессия отмечается реже и выражена в меньшей степени у пациентов с преимущественно дрожательной формой БП. В частности, у пациентов с акинетико-ригидной формой БП депрессия выявлена у 38% пациентов против 15% с преимущественно дрожательной формой заболевания. Наличие взаимосвязи депрессии и брадикинезии, вероятно, свидетельствует о наличии общих патофизиологических механизмов формирования этих нарушений.
В ряде случаев появление симптомов депрессии тесно связано с колебаниями эффективности использующихся для лечения БП препаратов в течение суток. При этом депрессия возникает на фоне окончания действия разовой дозы препаратов (в периоде «выключения») и исчезает с наступлением эффекта очередной дозы (в фазу «включения») [2]. Наличие клинических особенностей депрессии, проявления которой четко «привязаны» к флюктуациям симптомов БП, позволило выделить подтипы депрессивных расстройств по принципу наличия или отсутствия связи с флюктуациями симптомов. Так, для депрессии, связанной с периодами «выключения», характерна ассоциация с выраженностью основных двигательных и недвигательных симптомов (болью, вегетативными нарушениями), зависимость появления от времени приема и дозы дофаминергических препаратов. В противоположность этому депрессия, не связанная с периодами «выключения», не имеет четкой связи с выраженностью двигательных симптомов и стадией БП, режимом дофаминергической терапии; может появляться за несколько лет до диагностики основных симптомов БП. Наличие депрессии, выраженность которой находится в тесной зависимости от эффективности доз леводопы, подтверждает значимую роль в ее формировании центральной дофаминергической дисфункции.
При этом депрессия возникает на фоне окончания действия разовой дозы препаратов (в периоде «выключения») и исчезает с наступлением эффекта очередной дозы (в фазу «включения») [2]. Наличие клинических особенностей депрессии, проявления которой четко «привязаны» к флюктуациям симптомов БП, позволило выделить подтипы депрессивных расстройств по принципу наличия или отсутствия связи с флюктуациями симптомов. Так, для депрессии, связанной с периодами «выключения», характерна ассоциация с выраженностью основных двигательных и недвигательных симптомов (болью, вегетативными нарушениями), зависимость появления от времени приема и дозы дофаминергических препаратов. В противоположность этому депрессия, не связанная с периодами «выключения», не имеет четкой связи с выраженностью двигательных симптомов и стадией БП, режимом дофаминергической терапии; может появляться за несколько лет до диагностики основных симптомов БП. Наличие депрессии, выраженность которой находится в тесной зависимости от эффективности доз леводопы, подтверждает значимую роль в ее формировании центральной дофаминергической дисфункции.
Депрессия при БП часто может не диагностироваться, или, напротив, гипердиагностироваться. Это объясняется некоторыми общими чертами, характерными для депрессии и БП. Такими общими затрудняющими правильную диагностику симптомами являются: уменьшение психомоторной активности, повышенная утомляемость, снижение аппетита, снижение либидо, гипомимия, гипофония, нарушение внимания, расстройство сна [5, 8].
В клинической и исследовательской практике для скрининговой диагностики депрессии, определения ее тяжести, оценки динамики на фоне терапии используются количественные шкалы и опросники: шкала депрессии Гамильтона (НАМ-D), опросник депрессии Бека (ВДI), госпитальная шкала тревоги и депрессии (HADS), шкала депрессии Монтгомери-Асберг (MADRS). Для оценки тяжести депрессивных симптомов рекомендуется использовать НАМ-D, ВДI, MADRS.
Для оценки тяжести депрессивных симптомов рекомендуется использовать НАМ-D, ВДI, MADRS.
Наличие выраженных когнитивных нарушений затрудняет диагностику депрессии и требует информативной помощи близких пациента. Для оценки депрессии у пациентов с деменцией применяется Корнельская шкала депрессии при деменции [3, 26].
При постановке диагноза депрессии проявления ангедонии следует дифференцировать от апатии. Апатия рассматривается как нарушение мотивации и характеризуется снижением целенаправленного поведения, эмоциональной и когнитивной активности, сужением круга интересов. Данное нарушение может являться как проявлением депрессии, так и самостоятельным симптомом БП у пациентов без депрессивных расстройств. По данным наблюдательных исследований, апатия отмечается у 17- 42% пациентов с БП, при этом ее коморбидность с депрессией составляет 12-30%. Помимо связи с депрессией проявления апатии при БП коррелируют с наличием когнитивных нарушений (брадифренией, регуляторными лобными расстройствами), в меньшей степени — с тяжестью двигательных симптомов заболевания [12, 16].
Определенное сходство с проявлениями депрессии и апатии имеет феномен повышенной утомляемости. Утомляемость определяется как ощущение физической усталости и отсутствия энергии, нарушающее повседневную жизнь, не связанное с умственным переутомлением, сонливостью, нарушением двигательных функций вследствие БП. Данный феномен выявляется у 40- 56% пациентов с БП, при этом, как и апатия, он может быть проявлением депрессии, либо феноменологически самостоятельным симптомом заболевания [15].
По данным разных авторов, депрессивный синдром при БП ухудшает показатели качества жизни в большей степени, чем выраженность двигательных нарушений. Депрессия при БП ухудшает повседневную активность, качество жизни больных, снижает комплаентность (готовность выполнять назначения врача), отягощает течение основного заболевания, часто является фактором риска развития деменции при БП. Кроме того, депрессия у больных БП значительно ухудшает качество жизни родственников, живущих вместе с пациентом или ухаживающих за ним [5].
Пациенты с БП, которые испытывают длительную депрессию, несмотря на адекватную антипаркинсоническую терапию, нуждаются в психотерапии, назначении антидепрессантов, в крайних случаях — электросудорожной терапии [10].
Лечение депрессии при БП прежде всего должно предусматривать адекватную противопаркинсоническую терапию для оптимального контроля основных двигательных нарушений. Некоторые противопаркинсонические препараты обладают антидепрессивным эффектом (агонисты дофаминовых рецепторов, ингибиторы МАО типа В) [5, 8, 11, 20, 21].
Пациентам с депрессией необходимо проводить психотерапию (рациональную и поведенческую). Очень важно доведение до них информации о природе заболевания, методах лечения БП, приемах и приспособлениях в повседневной жизни, улучшающих активность. Эта информация должна предоставляться лечащим врачом во время приема пациента, а также в виде популярных пособий для больных и их родственников [2].
В случае, если улучшение двигательной активности на фоне адекватной терапии БП не сопровождается уменьшением депрессивных симптомов, больному назначают антидепрессанты.
К основным свойствам идеального антидепрессанта относятся быстрота наступления терапевтического эффекта, безопасность при передозировке, минимальное влияние на соматические функции, минимальное взаимодействие с противопаркинсоническими препаратами. Кроме того, важны простота схем лечения и титрования терапевтической дозы, что является важным у больных БП с нарушением когнитивных функций и, прежде всего, памяти.
Обычно для лечения депрессии при БП применяют селективные ингибиторы обратного захвата серотонина (СИОЗС), трициклические и тетрациклические антидепрессанты, реже — ингибиторы МАО [20, 21].
До сих пор при БП с наличием депрессивного синдрома на практике наиболее часто используются СИОЗС. Однако эти препараты нельзя сочетать с приемом ингибиторов МАО типа В (селегилином) [25, 29, 30]. При отсутствии эффекта в течение первых 3 нед дозу антидепрессанта увеличивают, а при неэффективности — заменяют другим препаратом с иным механизмом действия (например, трициклическим антидепрессантом).
Трициклические антидепрессанты менее предпочтительны при БП, так как они обладают побочными холинолитическими эффектами — вызывают повышение внутриглазного давления, задержку мочеиспускания, запоры, нарушение аккомодации, артериальную гипотензию и нарушение сердечного ритма. Кроме того, у больных БП они часто вызывают зрительные галлюцинации, дезориентацию, приводят к нарастанию когнитивных расстройств, свойственных этому заболеванию [21].
К группе риска по применению трициклических антидепрессантов относятся больные в возрасте старше 60 лет, с гипертрофией предстательной железы, глаукомой, ортостатической гипотензией, инфарктом миокарда, нарушением сердечного ритма.
В случаях возникновения депрессии в периоды «выключения» коррекция флуктуаций при помощи изменения схемы приема препаратов леводопы и/или комбинирование их с агонистами дофаминовых рецепторов, ингибиторами КОМТ и МАО достаточно эффективна без дополнительного назначения антидепрессантов [4, 9].
Частым симптомом при БП является тревога. Она наблюдается в среднем в 40% случаев. Тревожные расстройства при БП могут проявляться общей тревожностью, паническими атаками, социофобией, обсессивно-компульсивными расстройствами. Согласно DSM-IV, критериями тревоги являются беспокойство и 3 дополнительных симптома из следующих: усталость, быстрая утомляемость, нарушение концентрации внимания, повышенная раздражительность, мышечное напряжение, нарушения сна, отмечаемые в течение последних 6 мес [9, 30].
Панические атаки встречаются у 24% больных БП. Они проявляются различными пароксизмальными психическими, вегетативными и соматическими симптомами. Наиболее часто наблюдаются приступообразные тахикардия, тремор, затруднения дыхания, гипервентиляция, боль в грудной клетке, учащенное мочеиспускание, гипергидроз, ощущение дурноты, головокружение. Как правило (в 90% случаев), панические атаки возникают в период «выключения», когда заканчивается действие противопаркинсонических средств и возникает нарастание двигательных нарушений [31].
Лечение больных БП с проявлениями тревоги прежде всего должно предусматривать оптимизацию противопаркинсонической терапии с уменьшением эпизодов «выключения». При недостаточном эффекте назначают небольшие дозы короткодействующих бензодиазепинов. При наличии когнитивных нарушениий у больных БП доза бензодиазепинов должна быть меньшей, курс лечения не должен превышать 1,5 мес во избежание появления привыкания [30, 31].
Учитывая связь патогенеза БП с уменьшением числа дофаминергических нейронов в различных отделах головного мозга и снижением функционирования соответствующих синаптических связей, этим пациентам нельзя назначать препараты, усугубляющие нарушения обмена моноаминов.
К сожалению, многие антипсихотические препараты, применение которых обсуждается для лечения сопутствующих паркинсонизму депрессии, тревоги, диссомнии и т.д., а также осложнений леводопатерапии (таких, как галлюцинации), дают именно отрицательные корреляции с основными проявлениями БП, увеличивая ригидность, брадикинезию (сбалансированные антагонисты серотониновых и дофаминовых рецепторов), усиливая когнитивный дефект (атипичные нейролептики, антихолинергические средства). Имеющий большое сродство к серотониновым рецепторам нейролептик сероквель почти не влияет на двигательную и когнитивную функции, но часто вызывает сонливость и тревогу.
Имеющий большое сродство к серотониновым рецепторам нейролептик сероквель почти не влияет на двигательную и когнитивную функции, но часто вызывает сонливость и тревогу.
Что касается препаратов антидепрессивного действия, то здесь ситуация еще сложнее. Первые представители этой группы — трициклические антидепрессанты (амитриптилин) подавляют обратный захват моноаминов [17, 22, 25]; ингибиторы моноаминоксидазы (фенелзин) блокируют катаболизм моноаминов. Эти группы, достаточно эффективные при лечении депрессии, но имеют существенные недостатки в плане переносимости и безопасности. Разработанные позднее СИОЗС, ингибиторы обратного захвата норадреналина (ИОЗН) и ингибиторы обратного захвата серотонина и норадреналина (ИОЗСН) обладают более благоприятным профилем безопасности и эффективнее устраняют коморбидную тревогу, которая часто сопровождает стрессовые ситуации при острой соматической патологии, но не превосходят своих предшественников по эффективности в отношении депрессии при хронических заболеваниях [18, 20]. Это становится еще более актуальным при выборе лечения, когда речь идет о нейродегенеративной патологии, которая длится пожизненно.
Это становится еще более актуальным при выборе лечения, когда речь идет о нейродегенеративной патологии, которая длится пожизненно.
Кроме того, все эти препараты имеют моноаминергические механизмы действия, которые могут в разной степени, но негативно повлиять на дофаминергическую систему, вызывая либо ухудшение основных клинических проявлений паркинсонизма, либо потенцирование осложнений леводопатерапии.
Как альтернативу пытались использовать антагонисты NMDA- (N-метил-D-аспартат) рецепторов, которые вызывают достаточно быстрое развитие антидепрессивного эффекта, однако оказывают выраженные нежелательные психомиметические эффекты [23].
В качестве инновационного подхода для лечения депрессии при БП можно рассматривать применение вальдоксана (агомелатин), который является агонистом MT1-, МТ2-мелатонинергических и антагонистом 5-НТ2с-серотонинергических рецепторов. Мелатонин является важным регулятором циркадианных ритмов, определяющих структуру сна и имеющих непосредственное отношение к процессу старения организма в связи с ослаблением реактивности циркадианных часов на стимулы окружающей среды [13, 14, 27].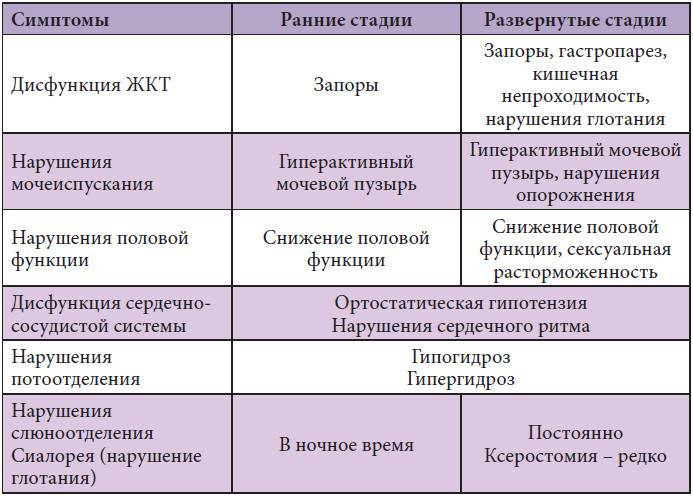 При исследовании терапевтического профиля вальдоксана было установлено повышение выброса дофамина и норадреналина в синаптических структурах лобной коры. Препарат, являясь агонистом мелатонина, проявляет выраженный антагонизм к 5-НТ2с-рецепторам. Полисинаптический путь действия вальдоксана, пролегающий из супрахиазмального ядра (СХЯ) в вентротегментальное, происходит из мезокортикальных и мезолимбических дофаминергических путей. Таким образом, опосредуется влияние 5-НТ2с-рецепторов, расположенных в СХЯ, на восходящую дофаминергическую трансмиссию. Блокада этих рецепторов приводит к высвобождению дофамина в области лобной коры и повышению трансмиссии, активность которой ослаблена при депрессии [18, 21]. Особенности действия вальдоксана послужили обоснованием его выбора для лечения депрессии при БП. У авторов статьи имеются собственные предварительные наблюдения.
При исследовании терапевтического профиля вальдоксана было установлено повышение выброса дофамина и норадреналина в синаптических структурах лобной коры. Препарат, являясь агонистом мелатонина, проявляет выраженный антагонизм к 5-НТ2с-рецепторам. Полисинаптический путь действия вальдоксана, пролегающий из супрахиазмального ядра (СХЯ) в вентротегментальное, происходит из мезокортикальных и мезолимбических дофаминергических путей. Таким образом, опосредуется влияние 5-НТ2с-рецепторов, расположенных в СХЯ, на восходящую дофаминергическую трансмиссию. Блокада этих рецепторов приводит к высвобождению дофамина в области лобной коры и повышению трансмиссии, активность которой ослаблена при депрессии [18, 21]. Особенности действия вальдоксана послужили обоснованием его выбора для лечения депрессии при БП. У авторов статьи имеются собственные предварительные наблюдения.
Вальдоксаном лечили 7 больных, 2 мужчин и 5 женщин, средний возраст которых был 64 года, а средняя продолжительность болезни — 14 лет. Препарат был назначен в дозе 25 мг в сутки в течение 6 мес, после чего больных продолжали наблюдать с целью установления стабильности терапевтического эффекта. Основная противопаркинсоническая терапия не изменялась на протяжении всего периода исследования. При обследовании пациентов использовали унифицированную шкалу оценки БП (UPDRS), опросник качества сна (LSEQ) и шкалу Гамильтона для оценки депрессии (НАМ-D).
Препарат был назначен в дозе 25 мг в сутки в течение 6 мес, после чего больных продолжали наблюдать с целью установления стабильности терапевтического эффекта. Основная противопаркинсоническая терапия не изменялась на протяжении всего периода исследования. При обследовании пациентов использовали унифицированную шкалу оценки БП (UPDRS), опросник качества сна (LSEQ) и шкалу Гамильтона для оценки депрессии (НАМ-D).
Полученные данные позволяют говорить не только о возможности коррекции тревожно-депрессивных расстройств, но и качества сна и бодрствования, а также положительных сдвигах в отношении симптомов паркинсонизма (вследствие усиления дофаминергической трансмиссии). Важно отметить, что это улучшение было стабильным в течение 3-4 мес после окончания лечения вальдоксаном.
Малое число пациентов пока не позволяет сделать обобщающие выводы по поводу эффективности вальдоксана. Но приведенное наблюдение может послужить стимулом к новым исследованиям терапевтического спектра вальдоксана, в том числе при дегенеративных заболеваниях ЦНС.
В заключение следует отметить, что БП несомненно требует комплексного терапевтического подхода. Это касается в первую очередь БП с депрессией.
Выявление деменции при болезни Паркинсона. Современная диагностика и лечение в Москве
Болезнь Паркинсона – известное во всем мире и достаточно распространенное заболевание нервной системы. Деменция, возникающая при этом заболевании, заслуживает отдельного внимания, поскольку она проявляется всего у половины пациентов с таким диагнозом, и не всегда удается заподозрить ее развитие на ранних этапах.
Диагностика самой болезни Паркинсона обычно не вызывает особых затруднений. Наличие тремора, а также ригидности мышц, ограничение темпа и ритма движений, затруднение в походке и стоянии на месте сразу наталкивает на мысль о синдроме Паркинсона. Единственное, стоит разобраться, не связано ли это состояние с приемом каких-либо лекарственных средств, особенно психиатрических, что может вызывать лекарственный паркинсонизм.
Однако, деменция, которая может быть следствием многих нервных болезней, при данной патологии не будет иметь характерных черт, что обычно вызывает диагностические сложности. К тому же, варианты развития слабоумия могут быть абсолютно противоположными по симптоматике, например, у некоторых пациентов развивается эйфория, истерия и даже психомоторное возбуждение, а у других – признаки апатии, депрессии и даже суицидальных попыток. Единственное, что будет общим – это нарастание мнестических нарушений, то есть забывчивость и трудности в приобретении новых знаний и навыков. Пациенты могут помнить, что было в далекие времена их молодости, однако забывают события прожитого сегодня дня. К тому же, они с трудом могут построить логические взаимосвязи, что часто приводит к странным поступкам и действиям. Все интеллектуально-психологические симптомы оценивают специалисты с помощью доказательных методов, специальных тестов и ряда других мероприятий.
В настоящее время заболевание считается неизлечимым, поэтому весь комплекс лечебных мероприятий направлен на компенсацию и коррекцию симптомов болезни. Так, например, симптоматику нарушений со стороны двигательной системы, улучшает препарат «леводопа», а также агонисты дофаминовых рецепторов, ингибиторы моноаминоксидазы. Холиноблокаторы, или антихолинергические препараты, благоприятно воздействуют на симптомы дрожания, или тремора, мышц. Хирургическое лечение считается «методом отчаяния», то есть рекомендовано только в случае невозможности скорректировать симптомы консервативным путем, и всегда тщательно оценивается риск не проведения операции и ее осложнений. К таким методам относится таламотомия и паллидотомия, которые являются деструктивными вариантами вмешательства. При этом разрушается очаг патологического возбуждения нейронов. Также существует, наоборот, нейростимуляция других структур головного мозга, ответственных за контроль двигательной активности тела человека. В стадии исследования находится генная терапия и лечение с помощью стволовых клеток.
Так, например, симптоматику нарушений со стороны двигательной системы, улучшает препарат «леводопа», а также агонисты дофаминовых рецепторов, ингибиторы моноаминоксидазы. Холиноблокаторы, или антихолинергические препараты, благоприятно воздействуют на симптомы дрожания, или тремора, мышц. Хирургическое лечение считается «методом отчаяния», то есть рекомендовано только в случае невозможности скорректировать симптомы консервативным путем, и всегда тщательно оценивается риск не проведения операции и ее осложнений. К таким методам относится таламотомия и паллидотомия, которые являются деструктивными вариантами вмешательства. При этом разрушается очаг патологического возбуждения нейронов. Также существует, наоборот, нейростимуляция других структур головного мозга, ответственных за контроль двигательной активности тела человека. В стадии исследования находится генная терапия и лечение с помощью стволовых клеток.
В любом случае, на сегодняшний день, к сожалению, полностью избавиться от болезни невозможно, и она прогрессирует, несмотря на проводимые мероприятия. Прогноз зависит от степени тяжести заболевания, его формы, а также личностных и физиологических особенностей пациента.
Прогноз зависит от степени тяжести заболевания, его формы, а также личностных и физиологических особенностей пациента.
Деменция | Фонд Паркинсона
Болезнь Паркинсона (БП) больше всего известна связанными с ней двигательными (или моторными) симптомами, такими как тремор и замедление движений, но когнитивные изменения также могут быть среди распространенных симптомов БП, не связанных с движением.
Около половины людей с болезнью Паркинсона будут иметь умеренных когнитивных нарушений — изменений в памяти и мышлении, которые заметны, но не настолько, чтобы повлиять на повседневную деятельность.
По мере прогрессирования заболевания у людей, живущих с болезнью Паркинсона, могут развиться более значительные или серьезные проблемы с памятью и мышлением, иногда называемые деменция . Термин «деменция» означает, что у человека наблюдаются постоянные когнитивные изменения, которые достаточно значительны, чтобы влиять на повседневную жизнь. Сочетание двигательных и когнитивных нарушений может быть особенно сложным, даже ограничивая способность человека с болезнью Паркинсона участвовать в социальной среде и выполнять основные действия.
Сочетание двигательных и когнитивных нарушений может быть особенно сложным, даже ограничивая способность человека с болезнью Паркинсона участвовать в социальной среде и выполнять основные действия.
Деменция или значительное снижение когнитивных функций также могут серьезно повлиять на партнеров по уходу и связаны со стрессом у партнера по уходу. Чтобы лучше заботиться о тех, кто живет с этим заболеванием, партнеры по уходу за людьми с деменцией, связанной с болезнью Паркинсона, также должны уделять первоочередное внимание уходу за собой.
Проблемы и симптомы болезни Паркинсона, связанные с настроением, сном, лекарствами или другими медицинскими проблемами, могут выглядеть как слабоумие. Поскольку многие другие факторы могут влиять на когнитивные способности при болезни Паркинсона, точный диагноз имеет важное значение.
Типы слабоумия
Изменения в структуре и химическом составе мозга могут вызывать проблемы с памятью и мышлением при болезни Паркинсона.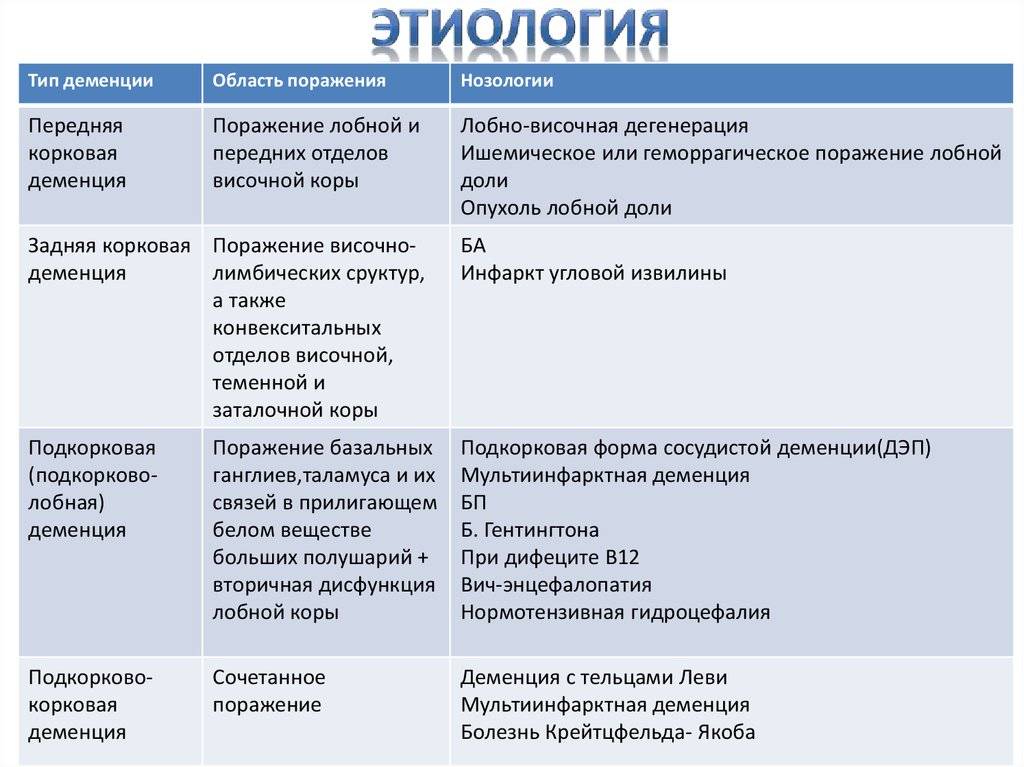 Альфа-синуклеин, белок, играющий ключевую роль в развитии болезни Паркинсона, образует липкие скопления, называемые тельцами Леви, которые могут нарушать нормальное функционирование мозга и приводить к слабоумию. Из-за этого иногда может использоваться термин «деменция с тельцами Леви (ДТЛ)».
Альфа-синуклеин, белок, играющий ключевую роль в развитии болезни Паркинсона, образует липкие скопления, называемые тельцами Леви, которые могут нарушать нормальное функционирование мозга и приводить к слабоумию. Из-за этого иногда может использоваться термин «деменция с тельцами Леви (ДТЛ)».
Деменция с тельцами Леви включает два различных типа связанных деменций, отличающихся тем, какие симптомы начинаются, когда:
- Деменция при болезни Паркинсона (PDD) – диагностируется, когда у человека, живущего с БП, наблюдается значительное снижение когнитивных функций после года или более двигательных симптомов (чаще всего после многих лет двигательных симптомов).
- Деменция с тельцами Леви (DLB) – диагностируется, когда снижение когнитивных функций является самым ранним симптомом или когда снижение когнитивных функций и моторные симптомы начинаются и прогрессируют одновременно.

Глубокое погружение с нашей книгой
Познание: Путеводитель по болезни Паркинсона объясняет, что влияет на ваше мышление и какие когнитивные изменения могут произойти при болезни Паркинсона. Не пропустите наши советы и истории, рассказывающие о том, как люди, страдающие болезнью Паркинсона, справляются с деменцией.
ПРОЧИТАТЬ
Симптомы деменции
Возможные изменения мышления, памяти и поведения у людей с деменцией при болезни Паркинсона могут быть самыми разнообразными.
Изменения памяти и путаница
Признаки могут варьироваться от забывания о том, как выполнять простые задачи, такие как приготовление кофе, до трудностей с концентрацией внимания, обучением, запоминанием или решением проблем:
- Люди с ПРД могут быть дезориентированы и сбиты с толку.
- У людей с ПРД могут наблюдаться нарушения кратковременной и долговременной памяти.

Изменения настроения, галлюцинации и паранойя
Люди с ПРД могут стать возбужденными, раздражительными или даже агрессивными. Другие проявления деменции при болезни Паркинсона могут включать:
- Галлюцинации – видение, слух или ощущение нереальных вещей.
- Бредовые идеи – странные или нереалистичные убеждения, включая параноидальное мышление, подозрительность или недоверие.
Проблемы зрительного восприятия
PDD может вызвать тонкие зрительно-перцептивные проблемы. Эти проблемы могут способствовать зрительному неправильному восприятию или иллюзиям. Это может включать в себя трудности с поиском объектов в людном месте или проблемы с навигацией по знакомым или незнакомым местам. Ночное слабое освещение или дегенерация желтого пятна могут усугубить эти проблемы.
Языковые проблемы
Люди с деменцией при болезни Паркинсона могут испытывать трудности в общении:
- По мере развития PDD у пользователей могут возникать проблемы с присвоением имен объектам или они могут называть их неправильно.

- Трудности с пониманием сложных предложений, таких как вопрос или информация, без более подробного описания.
- Проблемы с речью, такие как проблемы с произношением слов, даже когда они могут думать о слове, которое хотят сказать. Двигательные симптомы могут вызывать замедленную или невнятную речь.
Лечение деменции
Поговорите со своим участковым врачом, предпочтительно с неврологом или специалистом по двигательным расстройствам, о деменции. Хотя нет никакого способа остановить прогрессирование болезни, врач может помочь справиться с симптомами.
Исследования показали, что лекарства, отпускаемые по рецепту, разработанные для лечения болезни Альцгеймера, имеют преимущества при деменции при БП, включая ривастигмин (единственное лекарство от БП, одобренное FDA), донепезил и галантамин.

Ваш врач может порекомендовать вам работу со специально обученным нейропсихологом или логопедом, который может предложить когнитивную восстановительную терапию. Этот метод учит людей с когнитивными нарушениями способам компенсации проблем с памятью или мышлением с помощью:
- Тестирования, которое определяет сильные когнитивные способности для преодоления более слабых областей мышления.
- Выделение конкретных стратегий, помогающих в повседневной жизни.
Люди на ранних стадиях PDD могут самостоятельно использовать навыки когнитивной коррекции. Партнеры по уходу и члены семьи могут помочь применять стратегии по мере прогрессирования деменции.
Этот тип лечения включает изменения в окружающей среде, чтобы свести к минимуму проблемы с памятью, зрением и восприятием или ориентацией.
 Стратегии включают в себя расхламление и упрощение жилых помещений, чтобы уменьшить путаницу, и использование слабого ночного освещения, чтобы уменьшить визуальное неправильное восприятие и путаницу.
Стратегии включают в себя расхламление и упрощение жилых помещений, чтобы уменьшить путаницу, и использование слабого ночного освещения, чтобы уменьшить визуальное неправильное восприятие и путаницу.Структурированный, регулярный распорядок дня также может помочь людям с деменцией, связанной с болезнью Паркинсона, чувствовать себя более комфортно.
Различия между деменцией Паркинсона и болезнью Альцгеймера
Прогрессивные когнитивные изменения, влияющие на повседневную жизнь при болезни Альцгеймера и Паркинсона, являются типами деменции.
Деменция при болезни Паркинсона (PDD) может возникать как прогрессирование болезни Паркинсона после нескольких лет двигательных симптомов. Деменция с тельцами Леви (DLB) диагностируется, когда сначала происходит снижение когнитивных функций, или когда двигательные симптомы болезни Паркинсона и снижение когнитивных функций возникают и прогрессируют близко друг к другу.
Болезнь Альцгеймера, смертельное заболевание головного мозга, вызывает снижение памяти, мышления и навыков рассуждения. Врачи (часто с помощью таких специалистов, как неврологи, нейропсихологи, гериатры и гериатрические психиатры) могут диагностировать болезнь Альцгеймера. Посетите Ассоциацию Альцгеймера, чтобы узнать о 10 признаках болезни Альцгеймера.
Врачи (часто с помощью таких специалистов, как неврологи, нейропсихологи, гериатры и гериатрические психиатры) могут диагностировать болезнь Альцгеймера. Посетите Ассоциацию Альцгеймера, чтобы узнать о 10 признаках болезни Альцгеймера.
Деменция при болезни Паркинсона имеет тенденцию быть менее инвалидизирующей, чем болезнь Альцгеймера. У людей с болезнью Альцгеймера трудности с речью возникают раньше, чем у людей с болезнью Паркинсона, и они не могут формировать новые воспоминания, в отличие от людей с болезнью Паркинсона.
часто задаваемых вопросов: деменция и болезнь Паркинсона
Да. Болезнь Альцгеймера и болезнь Паркинсона влияют на разные белки в головном мозге, что позволяет человеку с болезнью Паркинсона также иметь болезнь Альцгеймера.
В редких случаях у человека с болезнью Паркинсона может быть диагностирована деменция при болезни Паркинсона и болезнь Альцгеймера.
 Невролог, который лечит болезнь Паркинсона вместе с нейропсихологом, гериатром или гериатрическим психиатром, может помочь диагностировать болезнь Альцгеймера.
Невролог, который лечит болезнь Паркинсона вместе с нейропсихологом, гериатром или гериатрическим психиатром, может помочь диагностировать болезнь Альцгеймера.Согласно последним исследованиям, до 70 процентов людей с болезнью Паркинсона разовьют слабоумие как часть прогрессирования заболевания.
Единого теста для PDD не существует. Диагноз ставится клинически. Если вы или кто-то, с кем вы проводите время, замечаете когнитивные изменения, важно обсудить их со своей командой по уходу. Если у вас нет команды по уходу, важно найти специалиста или врача, знакомого с деменцией или гериатрической медициной. Позвоните в службу поддержки Фонда Паркинсона по номеру 1-800-4PD-INFO (1-800-473-4636), чтобы получить направление.
Люди с деменцией, связанной с болезнью Паркинсона, часто хотят знать, как болезнь может повлиять на продолжительность их жизни.
 В то время как люди с болезнью Паркинсона могут рассчитывать на такую же продолжительность жизни, как и население в целом, исследования показывают, что как деменция при болезни Паркинсона, так и деменция с тельцами Леви могут сократить продолжительность жизни, как правило, из-за медицинских осложнений болезни, а не из-за самой болезни.
В то время как люди с болезнью Паркинсона могут рассчитывать на такую же продолжительность жизни, как и население в целом, исследования показывают, что как деменция при болезни Паркинсона, так и деменция с тельцами Леви могут сократить продолжительность жизни, как правило, из-за медицинских осложнений болезни, а не из-за самой болезни.
PD Деменция и вопросы безопасности
Вопросы безопасности следует учитывать и контролировать с момента постановки диагноза. По мере продвижения PDD следите за тем, чтобы ваш любимый человек не оставался один, и попытайтесь:
- Прежде чем беспокоиться о безопасности, оцените свои права на вождение. Ваш врач может выдать направление на оценку вождения.
- Решайте юридические и финансовые вопросы и защищайте финансы. Люди с деменцией подвергаются большему риску стать жертвой мошенничества и мошенничества.

- Минимизируйте риски, связанные с назначением рецепта. Согласуйте с врачом названия лекарств и дозы для человека с болезнью Паркинсона. Если человек находится на ранних стадиях деменции и дееспособен, вместе наполняйте его еженедельную коробочку с таблетками и контролируйте их использование.
- Загляните в системы медицинского оповещения. Эти системы могут иметь решающее значение в случае падения или если ваш любимый человек вышел за пределы дома. Доступны многие типы систем, от браслетов и подвесок до смарт-часов с функцией обнаружения падения и подключения одной кнопкой к 911.
- Оценить безопасность оружия. Если у вашего близкого есть огнестрельное оружие или оно есть дома, подумайте о том, чтобы обсудить это с врачом и принять дополнительные меры предосторожности.
Советы по общению с человеком с ПРД
Настроение и двигательные изменения, связанные с БП, могут повлиять на общение; когнитивные изменения и деменция при болезни Паркинсона могут усугубить эти трудности.
- Сохраняйте спокойствие и запаситесь терпением. Обычно бесполезно пытаться рассуждать или спорить с человеком, страдающим галлюцинацией или бредом. Если человек напуган галлюцинацией или бредом, постарайтесь перенаправить его внимание на что-то другое.
- Признание того, что человек видит, даже если вы этого не видите, может уменьшить стресс.
- Говорите медленно и на уровне глаз. Общайтесь простыми предложениями.
- Задавайте по одному вопросу и ждите ответа.
- Ограничьте отвлекающие факторы. Выключите телевизор или радио, прежде чем просить человека с ПРД что-либо сделать.
- Рассмотрите причины деструктивного поведения. Может ли ваш любимый человек быть голодным, испытывать жажду, усталость, боль, разочарование, одиночество или скуку?
- Если человек застрял на идее, попробуйте с ним согласиться, а затем сменить тему.
- Можно использовать юмор для разрядки стрессовых ситуаций, но избегайте негативного юмора или сарказма — их могут неправильно понять.

Страница проверена доктором Чонси Спирсом, клиническим ассистентом профессора, и доктором Сиднеем М. Спанья, клиническим научным сотрудником Мичиганского университета.
Связанные записи в блоге
Уголок сиделки
Переезд вашего близкого человека в центр долгосрочного ухода
ПРОЧИТАТЬ
Уголок сиделки
Уголок сиделки: Леви Что? Объяснение деменции с тельцами Леви
ПРОЧИТАТЬ
Новости науки
Насколько распространен когнитивный спад при болезни Паркинсона?
ПРОЧИТАТЬ
Болезни Альцгеймера и Паркинсона: сходства и различия
Узнайте о сходствах и различиях между двумя распространенными дегенеративными заболеваниями головного мозга.
Рон приводит свою 78-летнюю жену Сару в клинику памяти с неотложной проблемой. Сара стала все чаще забывать, несмотря на то, что ее симптомы болезни Паркинсона, по-видимому, хорошо контролируются стандартными лекарствами, здоровой диетой и большой физической активностью. Она теряет ход мыслей на полуслове и очень запуталась в том, где находится, пока ехала по наезженному маршруту к дому своей дочери. У нее развивается слабоумие? Это часть болезни Паркинсона? Или у нее развивается болезнь Альцгеймера? И в чем разница между болезнью Альцгеймера и болезнью Паркинсона?
Она теряет ход мыслей на полуслове и очень запуталась в том, где находится, пока ехала по наезженному маршруту к дому своей дочери. У нее развивается слабоумие? Это часть болезни Паркинсона? Или у нее развивается болезнь Альцгеймера? И в чем разница между болезнью Альцгеймера и болезнью Паркинсона?
Что такое деменция?
Деменция — это синдром, а не конкретное заболевание. Это означает, что клинические признаки деменции могут быть результатом любой из большой группы травм, инфекций или заболеваний. Симптомы деменции могут включать один или несколько из списка, включающего нарушение памяти, снижение способности удерживать в уме несколько задач одновременно и распределять внимание между ними, проблемы с пониманием языка или выражением, проблемы с пониманием пространственной ориентации, нарушение исполнительной функции и неточность. декодирование чужих невербальных сигналов.
Что такое болезнь Альцгеймера?
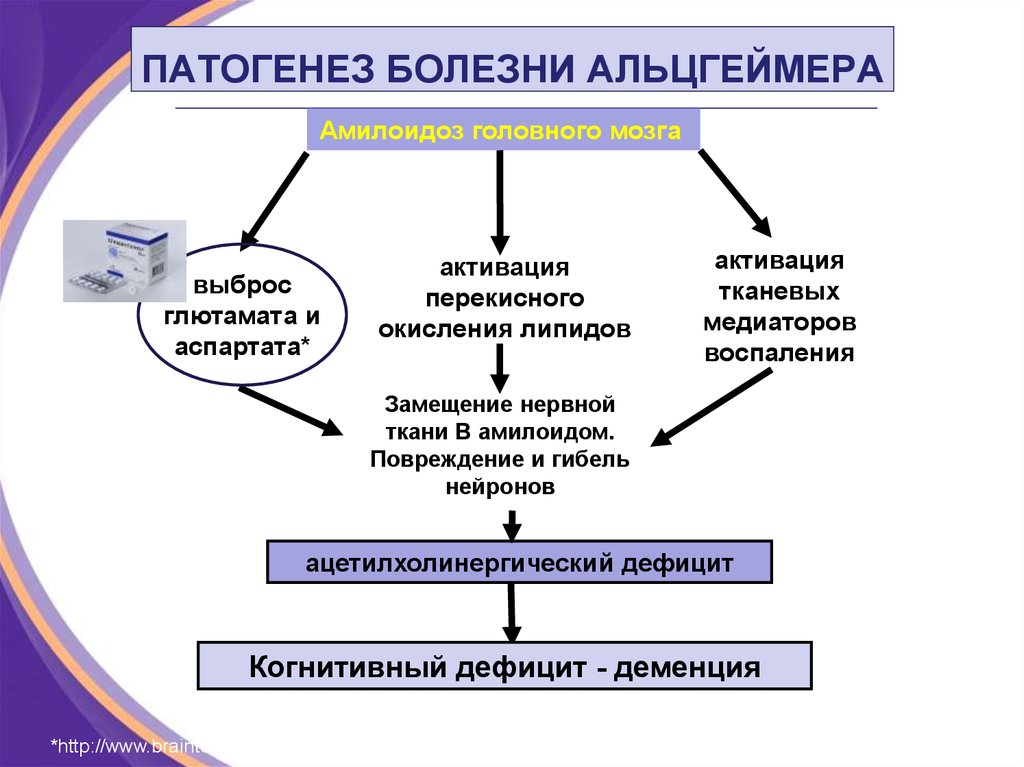
Болезнь Альцгеймера (БА), наиболее распространенная форма деменции среди пожилых людей, представляет собой необратимую дегенерацию головного мозга, которая вызывает нарушения памяти, познания, личности и других функций, что в конечном итоге приводит к смерти от полной мозговой недостаточности. Генетические факторы и факторы окружающей среды, включая диету, активность, курение, черепно-мозговую травму, диабет и другие медицинские заболевания, повышают риск развития этой формы заболевания. Отличительными признаками болезни Альцгеймера являются накопление бета-амилоидных бляшек между нервными клетками (нейронами) в головном мозге и нейрофибриллярные клубки, представляющие собой скрученные волокна, обнаруживаемые внутри клеток головного мозга). Эти клубки состоят в основном из белка, называемого тау.
Генетические факторы и факторы окружающей среды, включая диету, активность, курение, черепно-мозговую травму, диабет и другие медицинские заболевания, повышают риск развития этой формы заболевания. Отличительными признаками болезни Альцгеймера являются накопление бета-амилоидных бляшек между нервными клетками (нейронами) в головном мозге и нейрофибриллярные клубки, представляющие собой скрученные волокна, обнаруживаемые внутри клеток головного мозга). Эти клубки состоят в основном из белка, называемого тау.
Болезнь Паркинсона (БП) была описана Джеймсом Паркинсоном почти за 100 лет до д-ра Алоиса Альцгеймера , который описал деменцию, позже названную болезнью Альцгеймера (БА). Названный Паркинсоном «дрожательным параличом», болезнь Паркинсона диагностируется, когда у человека проявляются по крайней мере два из этих трех симптомов: замедление движений (брадикинезия), мышечная ригидность и тремор (в покое). Мы распознаем многие другие сопутствующие признаки болезни Паркинсона, в том числе невыразительное лицо, тихую речь, судорожный почерк, шаркающую походку, проблемы с вставанием со стула и затрудненное глотание. Многие симптомы идиопатической болезни Паркинсона возникают, когда определенные нервные клетки, вырабатывающие дофамин в мозге, начинают работать со сбоями и умирают.
Многие симптомы идиопатической болезни Паркинсона возникают, когда определенные нервные клетки, вырабатывающие дофамин в мозге, начинают работать со сбоями и умирают.
Большинство случаев называют «идиопатическими», что означает, что причина остается неизвестной, хотя небольшое число случаев связано с отравлением (некоторыми пестицидами, марганцем, окисью углерода), травмой головы, более сложными БП-подобными неврологическими расстройствами (такими как сосудистые паркинсонизм, прогрессирующий надъядерный паралич и множественная системная атрофия) или обратимые токсические эффекты лекарственных препаратов (нейролептики и некоторые противорвотные препараты),
Возраст начала симптомы впервые появляются после середины 60-х годов. БП начинается раньше, чем БА, обычно в возрасте от 50 до 65 лет, со средним возрастом начала около 62 лет, и лишь несколько случаев начинаются до 40 лет. При распространенности около 3 случаев на 1000 человек БП встречается реже, чем AD, но все еще важная причина неврологических заболеваний среди пожилых людей.
Небольшой процент людей с БА и БП имеют «раннее начало» заболевания. При БП симптомы могут проявиться в возрасте до 50 лет. Формы БП с ранним началом часто, но не всегда, наследуются. При БА форма с ранним началом начинается в возрасте до 60 лет. Многие люди с ранним началом БА, хотя и не все, унаследовали специфические генные мутации.
Как и симптомы болезни Альцгеймера, симптомы болезни Паркинсона вызваны разрушением клеток головного мозга. В отличие от болезни Альцгеймера, при которой обнаруживаются бляшки и клубки, при микроскопическом исследовании головного мозга при болезни Паркинсона обнаруживают потерю клеток, вырабатывающих дофамин, важное химическое вещество мозга, участвующее в коммуникации нервных клеток, в связанной с движением части мозга, называемой черной субстанцией. Можно увидеть, что клетки черной субстанции включают аномальные скопления белка, называемые «тельцами Леви».
Снижение когнитивных функций Снижение когнитивных функций часто встречается как при БА, так и при БП, хотя при БП встречается значительно реже.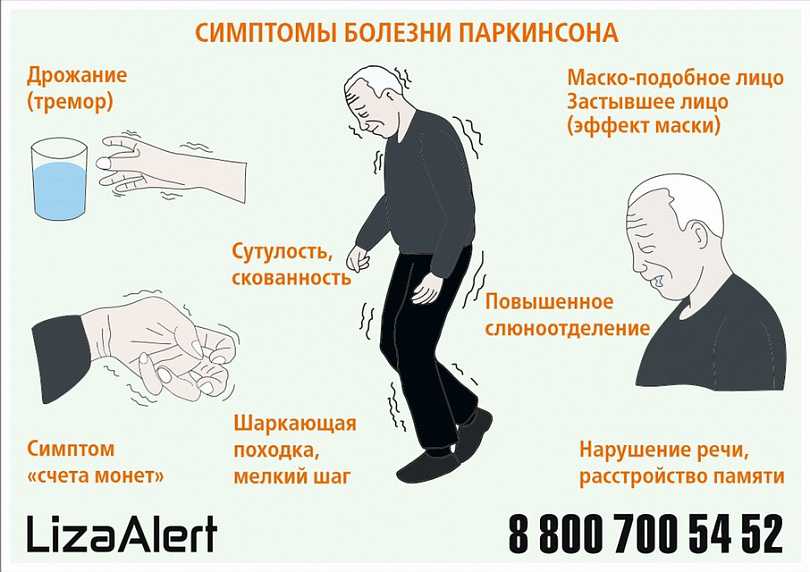 У половины людей с болезнью Паркинсона развиваются когнитивные трудности, которые могут варьироваться от легкой забывчивости до выраженной деменции. Деменция при БП называется «подкорковой» из-за расположения пораженных областей головного мозга, а клинические симптомы подкорковой деменции несколько отличаются от «кортикальной» деменции, такой как БА. При БП деменция замедленная физическая активность может сопровождаться замедленным мышлением и проблемами с памятью, которые более чувствительны к напоминаниям, чем при БА, потому что трудности связаны с извлечением памяти, а не с хранением новых знаний, как при БА.
У половины людей с болезнью Паркинсона развиваются когнитивные трудности, которые могут варьироваться от легкой забывчивости до выраженной деменции. Деменция при БП называется «подкорковой» из-за расположения пораженных областей головного мозга, а клинические симптомы подкорковой деменции несколько отличаются от «кортикальной» деменции, такой как БА. При БП деменция замедленная физическая активность может сопровождаться замедленным мышлением и проблемами с памятью, которые более чувствительны к напоминаниям, чем при БА, потому что трудности связаны с извлечением памяти, а не с хранением новых знаний, как при БА.
Как и у людей с БА, у людей с БП могут возникать поведенческие проблемы. Апатия является общим развитием обоих заболеваний, как и депрессия. Иногда бывает трудно отличить эти синдромы друг от друга, но важно попробовать, потому что они лечатся по-разному. Депрессия при БП часто поддается лечению антидепрессантами, возможно, в большей степени, чем при БА, и нельзя упускать из виду возможность уменьшения симптомов лечения БП.
Тревога характерна как для БП, так и для БА и может потребовать поведенческого лечения, снижения уровня БА или лекарств от БП, или добавления антидепрессантов или противотревожных препаратов, учитывая, что оба состояния делают пациентов уязвимыми для побочных эффектов лекарств. .
Психотические симптомыПсихотические симптомы, такие как бред и галлюцинации, также могут возникать как при БА, так и при БП. При обоих расстройствах эти симптомы могут указывать на делирий, вызванный инфекцией или другими заболеваниями. У пациентов с болезнью Паркинсона дополнительный риск психотических симптомов добавляется лекарствами, которые лечат симптомы двигательных расстройств. В более высоких дозах эти полезные лекарства могут вызывать галлюцинации и параноидальные идеи.
Нарушения сна Наконец, качество сна ухудшается как при БА, так и при БП. Пациенты с БА часто имеют фрагментарный сон, в то время как пациенты с БП испытывают другую проблему, называемую расстройством поведения с быстрым движением глаз, при котором физическая активность возникает во время обычно неподвижного периода быстрого сна. Расстройство поведения в фазе быстрого сна может поддаваться лечению клоназепамом, лекарством, которого обычно избегают при БА из-за беспокойства о влиянии на память и бдительность.
Расстройство поведения в фазе быстрого сна может поддаваться лечению клоназепамом, лекарством, которого обычно избегают при БА из-за беспокойства о влиянии на память и бдительность.
У некоторых пожилых людей двигательные симптомы, сходные с симптомами БП, появляются после или незадолго до развития когнитивных трудностей, похожих на БА. Эта комбинация двигательных и когнитивных изменений характерна для болезни, которую некоторые считают второй наиболее распространенной деменцией: деменция с тельцами Леви (ДТЛ). Как следует из названия, LBD — это состояние, при котором снижение когнитивных функций очень заметно, иногда гораздо более заметно, чем двигательные симптомы, однако микроскопические изменения в мозге сходны с таковыми при болезни Паркинсона.
Вопрос о том, действительно ли ДТЛ отличается от болезни Паркинсона с деменцией или является вариантом того же расстройства, остается предметом дискуссий, хотя обнаружение увеличенных отложений бета-амилоида (амилоидных бляшек) в головном мозге людей с ДТЛ позволяет предположить разницу между этими условиями. Симптомы LBD могут включать резкие колебания когнитивных функций, а также падения и психотические симптомы. Как и у пациентов с БП, и даже в большей степени, чем у пациентов с БА, стандартная антипсихотическая терапия часто осложняется тяжелыми токсическими реакциями. Однако когнитивные усилители, используемые при БА, могут играть полезную роль в лечении ДТЛ.
Симптомы LBD могут включать резкие колебания когнитивных функций, а также падения и психотические симптомы. Как и у пациентов с БП, и даже в большей степени, чем у пациентов с БА, стандартная антипсихотическая терапия часто осложняется тяжелыми токсическими реакциями. Однако когнитивные усилители, используемые при БА, могут играть полезную роль в лечении ДТЛ.
Важно различать различные типы нейродегенеративных состояний: это помогает определить наилучший подход к лечению. Лекарства, подходящие для одного из этих состояний, например, могут создавать проблемы при назначении пациенту с другим заболеванием. Дальнейшее тестирование Сары выявило легкие симптомы когнитивных нарушений, которые, вероятно, связаны с ее болезнью Паркинсона, но усугубляются одним из лекарств, которые она принимала. Ясность ее ума немного улучшилась после корректировки этого лекарства. Хотя когнитивные изменения, связанные с болезнью Паркинсона, со временем могут ухудшиться, нет никаких признаков того, что у нее развивается БА, и фактически на данный момент у нее нет диагноза деменции.
В таблице ниже представлены сходства и различия между болезнями Альцгеймера и Паркинсона. На мобильных устройствах проведите влево, чтобы увидеть все столбцы таблицы.
Сравнение болезни Альцгеймера и болезни Паркинсона
| Болезнь Альцгеймера | Болезнь Паркинсона | |
|---|---|---|
| Типичный возраст начала заболевания | После 60 лет (поздняя форма) До 60 лет (ранняя форма) | 50–65 лет (поздняя форма) До 50 лет (ранняя форма) |
| Ключевые белки, связанные с заболеванием | Бета-амилоид и тау | Альфа-синуклеин |
| Движение и координация | Снижение координации | Будет проявляться как минимум два из этих трех симптомов: мышечная ригидность, замедление движений или тремор |
| Нарушения памяти, познания, личности и других функций | Обычно присутствует | Часто присутствует |
| Память | Трудности с изучением новых воспоминаний | Проблемы с извлечением воспоминаний |
| Апатия и депрессия | Общий | Общий |
| Психотические симптомы (бред, паранойя и галлюцинации) | Может произойти | Может возникать как часть болезненного процесса или как побочный эффект дофаминергических препаратов |
| Нарушения сна | Непрерывность сна нарушается и фрагментируется на ранних стадиях заболевания, что приводит к дневному сну и эпизодам бодрствования ночью | Расстройство поведения в фазе быстрого сна (активные движения тела во сне) часто встречается Качество сна в целом ухудшается |
Aarsland D, Larsen JP, Lim NG, et al.
 Спектр нервно-психических расстройств у больных болезнью Паркинсона. J Neurol Нейрохирург Психиатрия 1999;67:492-6.
Спектр нервно-психических расстройств у больных болезнью Паркинсона. J Neurol Нейрохирург Психиатрия 1999;67:492-6.Аарсланд Д., Каммингс Дж.Л., Ларсен Дж.П. Нейропсихиатрические различия между болезнью Паркинсона с деменцией и болезнью Альцгеймера. Int J Geriatric Psychiatry 2001; 16:184-91.
Борек Л.Л., Амик М.М., Фридман Дж.Х. Немоторные аспекты болезни Паркинсона. CNS Spectr 2006;11(7):541-54.
Ferreri F, Agbokou C, Gauthier S. Распознавание и лечение нейропсихиатрических осложнений при болезни Паркинсона. CMAJ 2006; 175:1545-52.
Кирш-Дарроу Л., Фернандес Х.Ф., Марсиске М. и др. Диссоциирующая апатия и депрессия при болезни Паркинсона. Неврология 2006;67:33-8.
McDonald WM, Richard IH, DeLong MR. Распространенность, этиология и лечение депрессии при болезни Паркинсона. Биологическая психиатрия 2003;54:363-75.
Менза М., Марш Л. (ред.). Психиатрические проблемы при болезни Паркинсона. Практическое руководство. New York, Taylor & Francis, 2006.





 Стратегии включают в себя расхламление и упрощение жилых помещений, чтобы уменьшить путаницу, и использование слабого ночного освещения, чтобы уменьшить визуальное неправильное восприятие и путаницу.
Стратегии включают в себя расхламление и упрощение жилых помещений, чтобы уменьшить путаницу, и использование слабого ночного освещения, чтобы уменьшить визуальное неправильное восприятие и путаницу.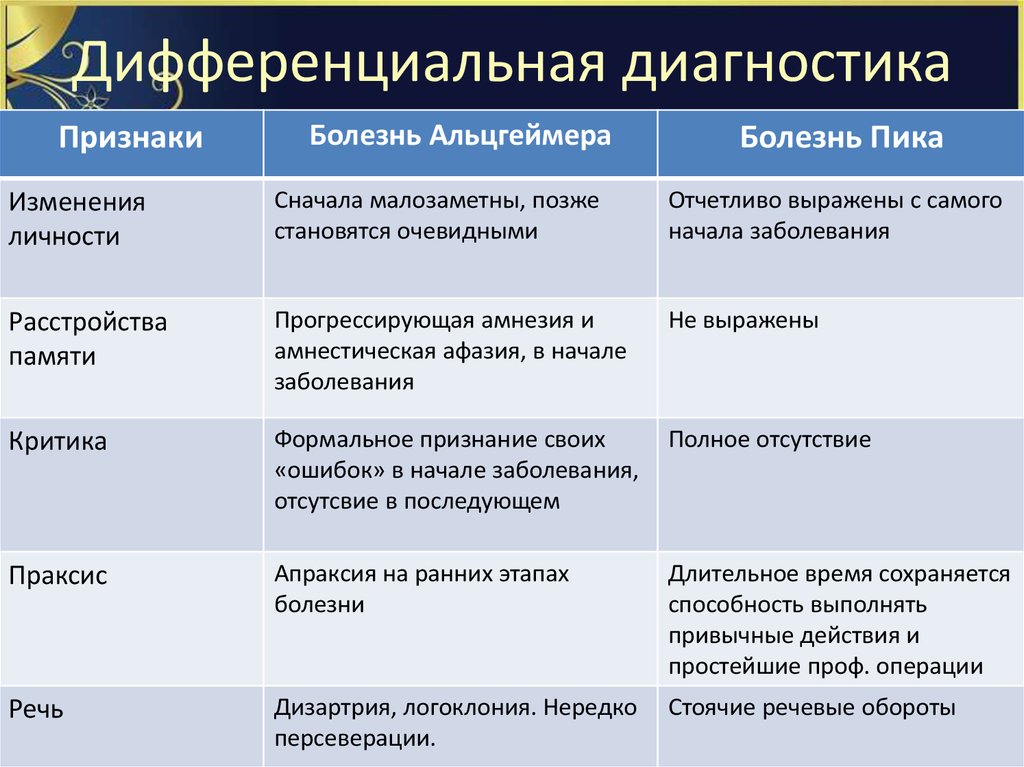 Невролог, который лечит болезнь Паркинсона вместе с нейропсихологом, гериатром или гериатрическим психиатром, может помочь диагностировать болезнь Альцгеймера.
Невролог, который лечит болезнь Паркинсона вместе с нейропсихологом, гериатром или гериатрическим психиатром, может помочь диагностировать болезнь Альцгеймера. В то время как люди с болезнью Паркинсона могут рассчитывать на такую же продолжительность жизни, как и население в целом, исследования показывают, что как деменция при болезни Паркинсона, так и деменция с тельцами Леви могут сократить продолжительность жизни, как правило, из-за медицинских осложнений болезни, а не из-за самой болезни.
В то время как люди с болезнью Паркинсона могут рассчитывать на такую же продолжительность жизни, как и население в целом, исследования показывают, что как деменция при болезни Паркинсона, так и деменция с тельцами Леви могут сократить продолжительность жизни, как правило, из-за медицинских осложнений болезни, а не из-за самой болезни.

 Спектр нервно-психических расстройств у больных болезнью Паркинсона. J Neurol Нейрохирург Психиатрия 1999;67:492-6.
Спектр нервно-психических расстройств у больных болезнью Паркинсона. J Neurol Нейрохирург Психиатрия 1999;67:492-6.