Лечение болезни паркинсона в россии: Лечение болезни Паркинсона в Москве – МЕДСИ
Болезнь Паркинсона. Центр экстрапирамидных заболеваний
Уважаемые пациенты,
амбулаторный прием по системе ОМС (при наличии направления) осуществляется для пациентов со следующими нозологиями:
—
цервикальная дистония (спастическая кривошея), оромандибулярная дистониея, блефароспазм, а также другие формы фокальных / сегментарных дистоний— генерализованная (торсионная дистония)
— болезнь Паркинсона — по ОМС только пациенты с перенесенной операцией по установке электростимулятора
Осуществляется
введение ботулинического токсина под контролем ЭМГ, УЗИ по системе ОМС при наличии препарата у пациента
Центр экстрапирамидных заболеваний
структурное подразделение отдела клинической неврологии и медицины сна Всероссийского центра экстренной и радиационной медицины им.
В ЦЕНТРЕ ЭКСТРАПИРАМИДНЫХ ЗАБОЛЕВАНИЙ ОСУЩЕСТВЛЯЕТСЯ АМБУЛАТОРНАЯ И СТАЦИОНАРНАЯ ПОМОЩЬ ПАЦИЕНТАМ С ЗАБОЛЕВАНИЯМИ:
— болезнь Паркинсона
— эссенциальный тремор
— мультисистемная атрофия (оливопонтоцеребеллярная дегенерация — тип С, стриатонигральная дегенерация — тип Р)
— прогрессирующий надъядерный паралич
— кортико-базальная дегенерация
— болезнь диффузных телец Леви (деменция с тельцами Леви)
— сосудистый паркинсонизм
— нормотензивная гидроцефалия
— токсический паркинсонизм
— болезни накопления (гепато-лентикулярная дегенерация, нейродегенерация связанная с накоплением железа)
— фокальная, сегментарная, мультифокальная дистония
— генерализованная дистония
— болезнь Гентингтона (хорея Гентигтона)
Телефон для связи
8 (812) 923-58-82
(по будням с 10:00 до 16:00)
Лечение болезни Паркинсона в Санкт-Петербурге
Болезнь Паркинсона — одно из самых частых неврологических заболеваний и одна из основных причин инвалидизации, связанной с поражением нервной системы. В нашей стране в настоящее время насчитывается не менее 200 тыс. пациентов с болезнью Паркинсона, причем ежегодно появляются от 15 до 20 тыс. новых случаев заболевания. Хотя болезнь может проявиться в широком возрастном диапазоне, заболеваемость особенно велика у пожилых, среди которых 1-2% страдают данным заболеванием. Если нынешние тенденции к увеличению доли пожилых в обществе сохранятся, то в ближайшие десятилетия число пациентов с
В нашей стране в настоящее время насчитывается не менее 200 тыс. пациентов с болезнью Паркинсона, причем ежегодно появляются от 15 до 20 тыс. новых случаев заболевания. Хотя болезнь может проявиться в широком возрастном диапазоне, заболеваемость особенно велика у пожилых, среди которых 1-2% страдают данным заболеванием. Если нынешние тенденции к увеличению доли пожилых в обществе сохранятся, то в ближайшие десятилетия число пациентов с
Первый пациент с болезнью Паркинсона получил новые нейроны
* By submitting the completed data in the registration form, I confirm that I am a healthcare worker of the Russian Federation and give specific, informed and conscious consent to the processing of personal data to the Personal Data Operator Pfizer Innovations LLC (hereinafter referred to as the “Operator”) registered at the address: St. Moscow, Presnenskaya embankment, house 10, 22nd floor.
Moscow, Presnenskaya embankment, house 10, 22nd floor.
I grant the Operator the right to carry out the following actions with my personal data, as well as information about my hobbies and interests (including by analyzing my profiles on social networks): collecting, recording, systematizing, accumulating, storing, updating (updating, changing) , extraction, use, transfer (access, provision), deletion and destruction, by automated and (or) partially automated (mixed) processing of personal data.
Consent is granted with the right to transfer personal data to affiliated persons of Pfizer Innovations LLC, including Pfizer LLC (Moscow, Presnenskaya naberezhnaya, 10, 22nd floor), and with the right to order the processing of personal data, incl. h. LLC «Redox» (Moscow, Volgogradskiy prospect, house 42, building 42A, floor 3, room 3) and LLC «Supernova» (Moscow, Varshavskoe shosse, house 132), which processes and stores personal data.
The processing of my personal data is carried out for the purpose of registering on the Operator’s website www. pfizerprofi.ru to provide me with access to information resources of the Pfizer company, as well as to interact with me by providing information through any communication channels, including mail, SMS, e-mail, telephone and other communication channels.
pfizerprofi.ru to provide me with access to information resources of the Pfizer company, as well as to interact with me by providing information through any communication channels, including mail, SMS, e-mail, telephone and other communication channels.
This consent is valid for 10 (ten) years.
I have been informed about the right to receive information regarding the processing of my personal data, in accordance with the Federal Law of July 27, 2006 No. 152-FZ «On Personal Data».
This consent can be revoked by me at any time by contacting the address of the Operator-Pfizer Innovations LLC or by phone. 8 495 287 5000.
*Отправляя заполненные данные в регистрационной форме, я подтверждаю, что являюсь работником здравоохранения Российской Федерации и даю конкретное, информированное и сознательное согласие на обработку персональных данных Оператору персональных данных ООО «Пфайзер Инновации» (далее «Оператор»), зарегистрированному по адресу: г. Москва, Пресненская набережная, дом 10, 22 этаж.
Я предоставляю Оператору право осуществлять с моими персональными данными, а также сведениями о моих хобби и увлечениях (в том числе с помощью анализа моих профилей в социальных сетях) следующие действия: сбор, запись, систематизация, накопление, хранение, уточнение (обновление, изменение), извлечение, использование, передача (доступ, предоставление), удаление и уничтожение, путем автоматизированной и (или) частично автоматизированной (смешанной) обработки персональных данных.
Согласие предоставляется с правом передачи персональных данных аффилированным лицам ООО «Пфайзер Инновации», в т. ч. ООО «Пфайзер» (г. Москва, Пресненская набережная, дом 10, 22 этаж), и с правом поручения обработки персональных данных, в т.ч. ООО «Редокс», (г. Москва, Волгоградский проспект, дом 42, корпус 42А, этаж 3, ком. 3) и ООО «Супернова» (г. Москва, Варшавское шоссе, дом 132), осуществляющим обработку и хранение персональных данных.
Обработка моих персональных данных осуществляется с целью регистрации на сайте Оператора www. pfizerprofi.ru для предоставления мне доступа к информационным ресурсам компании Пфайзер, а также для взаимодействия со мной путем предоставления информации через любые каналы коммуникации, включая почту, SMS, электронную почту, телефон и иные каналы коммуникации.
pfizerprofi.ru для предоставления мне доступа к информационным ресурсам компании Пфайзер, а также для взаимодействия со мной путем предоставления информации через любые каналы коммуникации, включая почту, SMS, электронную почту, телефон и иные каналы коммуникации.
Срок действия данного согласия — 10 (десять)лет.
Я проинформирован (-а) о праве на получение информации, касающейся обработки моих персональных данных, в соответствии с Федеральным законом от 27.07.2006 г. №152-ФЗ «О персональных данных».
Данное согласие может быть отозвано мною в любой момент посредством обращения по адресу нахождения Оператора-ООО «Пфайзер Инновации» или по тел. 8 495 287 5000.
Хирургическое лечение болезни Паркинсона Текст научной статьи по специальности «Клиническая медицина»
ОРИГИНАЛЬНЫЕ СТАТЬИ
3ОРИГИНАЛЬНЫЕ СТАТЬИ
УДК 616. 858-089
858-089
С.К. Акшулаков (д.м.н.), Ч.С. Шашкин (к.м.н.), Е.Т. Махамбетов (к.м.н.), А.С. Шпеков, Ж.И. Комаров АО «Национальный центр нейрохирургии», Астана, Казахстан
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ БОЛЕЗНИ ПАРКИНСОНА
Введение. Болезнь Паркинсона это хроническое прогрессирующее дегенеративное заболевание центральной нервной системы. Распространенность (общее количество больных, страдающих данным заболеванием в определенный момент времени) болезни Паркинсона в среднем по миру колеблется от 72 до 258,8 на 100 тысяч населения.
В 47 случаях в качестве цели было выбрано субталамическое ядро (STN), в одном случае — внутренний членик бледного шара (GPi). Мужчин было 23, женщин — 25. Средний возраст составил 57 лет. Средняя длительность заболевания -10 лет. Выраженные дискинезии и флюктуации были у 75% пациентов.
Мужчин было 23, женщин — 25. Средний возраст составил 57 лет. Средняя длительность заболевания -10 лет. Выраженные дискинезии и флюктуации были у 75% пациентов.
Имплантировались система глубинной стимуляции головного мозга Activa PC производства компании Medtronic (США), состоящая из двух электродов, удлинительных кабелей и постоянного генератора импульсов. Результаты исследования. Улучшение двигательных функций составило до 80%. Постуральная неустойчивость, нарушения походки и автономные симптомы регрессировали в меньшей степени. Всем пациентам уменьшена доза допаминергических препаратов на 30% и больше, что привело к полному регрессу лекарственных дискинезий во всех случаях. Осложнения наблюдались у 5 пациентов.
Обсуждение полученных данных. Глубинная стимуляция головного мозга позволяет максимально купировать основные симптомы болезни Паркинсона, такие как ригидность, тремор и брадикинезия, а в ряде случаев и постуральную неустойчивость и нарушения походки. Правильный отбор на хирургическое лечение является залогом успешного результата.
Правильный отбор на хирургическое лечение является залогом успешного результата.
Ключевые слова: болезнь Паркинсона, глубинная стимуляция головного мозга
Введение
Болезнь Паркинсона (БП) является второй самой распространенной нейродегенеративной болезнью, которая поражает от 1% до 3% взрослого населения старше 65 лет [1]. Распространенность (общее количество больных, страдающих данным заболеванием в определенный момент времени) болезни Паркинсона в среднем по миру колеблется от 72 до 258,8 на 100 тысяч населения [2, 3]. Болезнь распространена больше у женщин в соотношении 1,0 на 1,9. Заболеваемость составляет от 4,5 до 19 на 100 тысяч населения в год. Экстраполируя мировые данные эпидемиологии болезни Паркинсона можно предположить, что в настоящее время в Казахстане имеется от 16 до 23 тысяч больных БП, а ежегодно их количество становится на 1200 больше.
Болезнь распространена больше у женщин в соотношении 1,0 на 1,9. Заболеваемость составляет от 4,5 до 19 на 100 тысяч населения в год. Экстраполируя мировые данные эпидемиологии болезни Паркинсона можно предположить, что в настоящее время в Казахстане имеется от 16 до 23 тысяч больных БП, а ежегодно их количество становится на 1200 больше.
Учитывая высокую частоту инвализизации больных с БП, значительное снижение качества жизни у данных пациентов, возникает острая
необходимость улучшения медицинской помощи данной категории больных. В 1990-х годах развился и стал применяться в лечении двигательных расстройств метод глубинной стимуляции головного мозга. Метод заключается в высокочастотной электрической стимуляции глубинных ядер, таких как субталамическе ядро, бледный шар и таламус [4, 5].
Материалы и методы
В 2013-2014 годах в Национальном центре нейрохирургии было прооперировано 48 пациентов с болезнью Паркинсона. Для отбора пациентов использовали международные критерии отбора на хирургическое лечение, при БП:
Для отбора пациентов использовали международные критерии отбора на хирургическое лечение, при БП:
1. Болезнь Паркинсона
2. Возраст до 70 лет
3. Хоен-Яр 3-5 ст.
4. Длительность заболевания более 5 лет.
5. Хороший ответ на лечение леводопой -положительный допаминовый тест — улучшение моторных функций не менее чем на 30%.
6. Моторные флюктуации.
7. Дискинезии.
Использовались критерии исключения на хирургическое лечение при БП:
1. Психические нарушения — когнитивный дефицит, деменция, галлюцинации, расстройства поведения.
2. Выраженная депрессия.
3. Тяжелые соматические заболевания.
4. Органические поражения базальных ганглиев.
5. Синдром паркинсонизма и Паркинсон-плюс.
Всем пациентам проведено клиническое
тестирование, используя UPDRS-тест, общеклинические исследования, МРТ головного мозга для исключения сопутствующей патологии. МРТ 3 Тесла проведена в 17 случаях для проведения таргетирования.
В день операции пациентам проводилась фиксация стереотаксической рамы, затем МРТ со стереотаксической рамой и МРТ-индикатором в режимах Т2 SE и Т1 с внутривенным контрастированием. В 5 случаях проведена КТ головного мозга. Планирование цели и траектории проводилось на программном обеспечении Sur-giPlan (Elekta, Sweden). Как правило, применялся прямой метод таргетирования по Danish et al., используя T2 Axial МРТ. В 47 случаях в качестве цели было выбрано субталамическое ядро (STN), в одном случае — внутренний членик бледного шара (GPi). Мужчин было 23, женщин — 25. Средний возраст составил 57 лет. Средняя длительность заболевания — 10 лет. Выраженные дискинезии и флюктуации были у 75% пациентов.
Как правило, применялся прямой метод таргетирования по Danish et al., используя T2 Axial МРТ. В 47 случаях в качестве цели было выбрано субталамическое ядро (STN), в одном случае — внутренний членик бледного шара (GPi). Мужчин было 23, женщин — 25. Средний возраст составил 57 лет. Средняя длительность заболевания — 10 лет. Выраженные дискинезии и флюктуации были у 75% пациентов.
Во время операции использовался микроэлектродрекординг для определения цели, а затем тестовая стимуляция с клиническими пробами. Имплантировались система глубинной стимуляции головного мозга Activa PC производства компании Medtronic (США), состоящая из двух электродов, удлинительных кабелей и постоянного генератора импульсов. Постоянный генератор импульсов имплантировался в левую подключичную область.
Первичная нейростимуляция проводилась в большинстве случаев на второй день после имплантации. Параметры стимуляции: частота
130 Hz, длина волны 60 pS, амплитуда и контакт выставлялась по наилучшему результату. Наблюдение проводилось в сроки до месяца, 3 и 6 месяцев после хирургического лечения.
Наблюдение проводилось в сроки до месяца, 3 и 6 месяцев после хирургического лечения.
Результаты исследования
Стимуляция STN довольно хорошо изучена. Улучшение на 50% по UPDRS двигательной шкале после стимуляции STN поддерживалось на протяжении 5 лет [6]. Тремор и ригидность особенно поддается лечению стимуляцией STN,
а также брадикинезия, нарушения походки и постуральная неустойчивость. Стимуляция STN позволяет в 50-60% случаев снизить дозу допаминергических средств, дискинезии вследствие леводопы также уменьшаются в 94% случаев через 12 месяцев после лечения [7, 8]. В наших наблюдениях улучшение моторных функций в виде значительного регресса ригидности, тремора и брадикинезии составило до 80%. Постуральная неустойчивость, нарушения походки и автономные симптомы регрессировали в меньшей степени и в случаях, когда они регрессировали после приема леводопы. Всем пациентам уменьшена доза допаминергических препаратов на 30% и больше, что привело к полному регрессу лекарственных дискинезий во всех случаях, а в 7 случаях удалось отойти от препаратов совсем. осложнения наблюдались у 5 пациентов. У одного пациента произошло кровоизлияние в месте имплантации электрода, что привело к удалению системы, проведению экстренного оперативного вмешательства по удалению гематомы и декомпрессии мозга. После курсов реабилитации и проведения плановой краниопластики, пациенту была проведена повторное оперативное лечение с положительным результатом. У одного пациента развился ишемический инсульт в послеоперационном периоде. У двух пациентов наблюдалось инфекционное осложнение, в связи с чем система была полностью удалена. У двух пациентов в раннем послеоперационном периоде развилась тромбоэмболия легочной артерии. Из них один случай завершился летальным исходом.
Всем пациентам уменьшена доза допаминергических препаратов на 30% и больше, что привело к полному регрессу лекарственных дискинезий во всех случаях, а в 7 случаях удалось отойти от препаратов совсем. осложнения наблюдались у 5 пациентов. У одного пациента произошло кровоизлияние в месте имплантации электрода, что привело к удалению системы, проведению экстренного оперативного вмешательства по удалению гематомы и декомпрессии мозга. После курсов реабилитации и проведения плановой краниопластики, пациенту была проведена повторное оперативное лечение с положительным результатом. У одного пациента развился ишемический инсульт в послеоперационном периоде. У двух пациентов наблюдалось инфекционное осложнение, в связи с чем система была полностью удалена. У двух пациентов в раннем послеоперационном периоде развилась тромбоэмболия легочной артерии. Из них один случай завершился летальным исходом.
Обсуждение полученных данных
Глубинная стимуляция головного мозга стала важной частью лечения двигательных расстройств, проводимого в Национальном центре нейрохирургии в городе Астане. Для пациентов, у которых симптомы заболевания не поддаются медикаментозной терапии, стимуляция является эффективным методом лечения, позволяющий максимально купировать основные симптомы болезни Паркинсона, такие как ригидность, тремор и брадикинезия, а в ряде случаев и постуральную неустойчивость и нарушения походки. Правильный отбор на хирургическое лечение является залогом успешного результата.
Для пациентов, у которых симптомы заболевания не поддаются медикаментозной терапии, стимуляция является эффективным методом лечения, позволяющий максимально купировать основные симптомы болезни Паркинсона, такие как ригидность, тремор и брадикинезия, а в ряде случаев и постуральную неустойчивость и нарушения походки. Правильный отбор на хирургическое лечение является залогом успешного результата.
список литературы
1. Twelves, D., Perkins, K.S.M., Counsell, C., 2003. Systematic review of incidence studies of Parkinson’s disease. Mov. Disord. 18, 19-31.
2. Катунина У.А. и др. Эпидемилогия
паркинсонизма. Журнал неврологии и психиатрии, 11, 2009, стр. 76-80.
3. E.R. Dorsey et al. Projected number of people with Parkinson disease in the most populous nations, 2005 through 2030.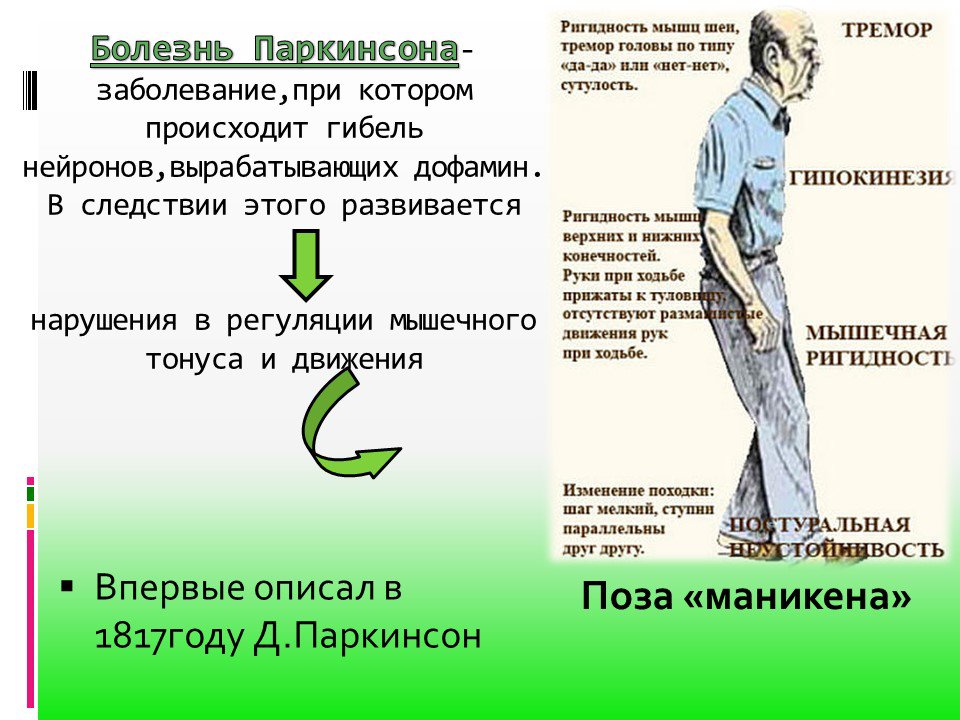 Neurology 2007. 68, 384-386.
Neurology 2007. 68, 384-386.
4. Kumar, R., et al., 2003. Long-term follow-up of thalamic deep brain stimulation for essential and parkinsonian tremor. Neurology 61, 1601-1604.
5. Obeso, J., et al., 2001. Deep-brain stimulation of the subthalamic nucleus or the pars interna of the globus pallidus in Parkinson’s disease. N. Engl. J. Med. 345, 956-963.
6. Hamani, C., et al., 2005. Bilateral subthalamic nucleus stimulation for Parkinson’s disease: a systematic review the clinical literature. Neurosurgery 56, 1313-1321.
7. Krack, P., et al., 2003. Five-year follow-up of bilateral stimulation of the subthalamic nucleus in advanced Parkinson’s disease. N. Engl. J. Med. 349, 1925-1934.
ОРИГИНАЛЬНЫЕ СТАТЬИ
5
4
8. Kleiner-Fisman, G., et al., 2006. Subthalamic nu- 10. cleus deep brain stimulation: summary and metaanalysis of outcomes. Mov. Disord. 21, S290-S304.
Kleiner-Fisman, G., et al., 2006. Subthalamic nu- 10. cleus deep brain stimulation: summary and metaanalysis of outcomes. Mov. Disord. 21, S290-S304.
9. Deuschl, G., et al., 2006. A randomized trial of deep-brain stimulation for Parkinson’s disease. N. 11. Engl. J. Med. 355, 896-908.
Weaver, F., et al., 2009. Bilateral deep brain stimulation vs best medical therapy for patients with advanced Parkinson disease: a randomized controlled trial. JAMA 301, 63-73.
Anderson, VC., et al., 2005. Pallidal vs subthalamic nucleus deep brain stimulation in Parkinson disease. Arch. Neurol. 62, 554-560.
ТУЙІНДЕМЕ
С.К. Акшулаков (m.fA), Е.Т. Махамбетов (m.f.k.),
Ч. ы» АК„ Астана, К,азак,стан
ы» АК„ Астана, К,азак,стан
ПАРКИНСОН АУРУЫНЬЩ ХИРУРГИЯЛЫК ЕМІ
Кіріспе. Паркинсон ауруы бул орталык жYЙке жYЙесініц созылмалы ершімелі дегенерациялык сыркаты. Оныц таралуы 100 мыц халыкка шакканда 72-ден 258,8-ге дейін.
Материалдар мен адістер. 2013-2014 жылдары ¥лттык нейрохирургия орталыFында Паркинсон ауруымен 48 наукаска ота жасалды. Пациенттерді хирургиялык емге іріктеуде халыкаралык критерийлер колданылды.
47 жаFдайда нысана ретінде субталамустык ядро, ал бір жаFдайда бозFылт шардыц ішкі белімі тацдалды (GPi). Ер адамдар саны 23, эйелдер 25 болды. Орта жас 57-ді курады. Сыркаттыц орташа узактыFы — 10 жыл. Айкын дискинезиялар мен флюктуациялар 75% пациентте болды.
Medtronic (АК.Ш) компаниясымен ендірілген мидыц терец стимуляциясы жYЙесі Activa PC имплантацияланды. Ол екі электрод, узарту кабелдері мен туракты генератордан турады.
Ол екі электрод, узарту кабелдері мен туракты генератордан турады.
Зерттеу натижелері. КозFалыс кызметтерініц жаксаруы 80% дейін жетті. Туру тураксыздыFы, жYріс бузылуы мен автономды симптомдардыц кері кайтуы темендеу дэрежеде болды. Барлык пациенттерге допаминергиялык дэрілердіц дозасы 30%-Fа жэне одан кеп темендетілді, ал бул дэртк дискинезиялардыц регресіне алып келді, екі жаFдайда дэрілерден толык бас тартуFа кол жеткізілді. Аскыныстар 5 пациентте байкалды.
Талк,ылау. Мидыц терец стимуляциясы, курысу, тремор жэне брадикинезия (кейбір жаFдайда туру тураксыздыFы мен жYріс бузылуы) сиякты Паркинсон сыркатыныц негізгі симптомдарын барынша басуFа мYмкіндік беретін, нэтижелі эдіс болып табылады. Хирургиялык емге дурыс іріктеуді жYргізу табысты нэтиженіц кепілі болып табылады.
Негізгі сездер: Паркинсон ауруы, мидыц
терец стимуляциясы
SUMMARY
S.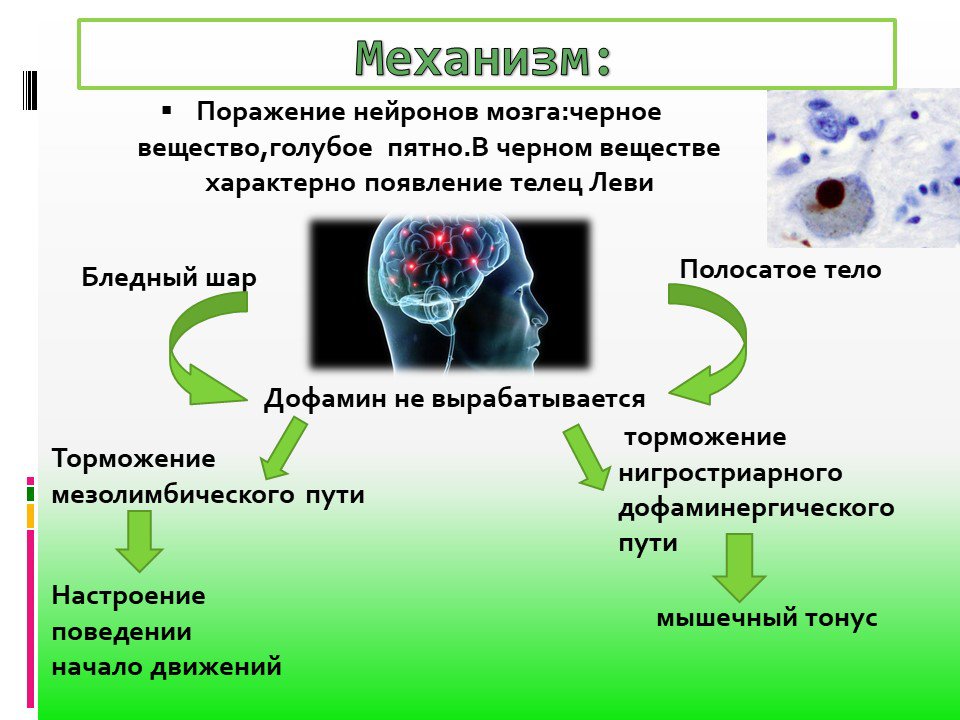 Akshulakov (D.Med.Sci.), Ye. Makhambetov (Ph.D),
Akshulakov (D.Med.Sci.), Ye. Makhambetov (Ph.D),
Ch. Shashkin (Ph.D), A. Shpekov, Zh. Komarov
«National centre for neurosurgery» JSC, Astana, Kazakhstan
SURGICAL TREATMENT OF PARKINSON’S DISEASE
Background. Parkinson disease (PD) is chronic progressive degenerative disease of the central nervous system with prevalence 72 to 258,8 for 100 thousand people.
Materials and methods. 50 PD patients were operated in the National center for neurosurgery in period 2013-2014. We used international selection criteria.
We stimulated subthalamic nucleus in 48 cases and globus pallidus interna in 1 case. There were 23 male and 25 female. The average age of the patients was 57 y.o. The average duration of disease was 10 years. Severe fluctuations and dyskinesias were in 75% of cases.
Severe fluctuations and dyskinesias were in 75% of cases.
We implanted DBS therapy Activa PC system from Medtronic (USA), which were consisted from two leads, extension cables and IPG.
Results. Improvement of motor functions was in 80% of cases. Postural instability, gait problems and autonomic symptoms less regressed. We decrease the dosage of dopaminergic drugs for 30% and more thereafter the drug induced dyskinesia regressed in all cases moreover in two cases we postponed medication completely. We had complications in 5 cases.
Discussion. Deep brain stimulation is effective treatment of PD and can decrease main symptoms of the disease: rigidity, tremor and bradykinesia and sometimespostural instability and gait problems. The right patient selection is a key for good result of this procedure.
Key Words: Parkinson’s disease deep brain stimulation
В Красноярском крае провели первую операцию по лечению болезни Паркинсона
«Даже не раздумывал, соглашаться на операцию или нет, сразу принял решение. Очень благодарен врачам, чувствую, словно стал моложе», — делится Юрий, первый пациент в крае, которому провели уникальную операцию. Врачи установили ему в глубинные отделы мозга специальный электростимулятор для DBS-терапии – электроимпульсы блокируют патологические эффекты, благодаря чему удается убрать тремор и скованность движений.
Очень благодарен врачам, чувствую, словно стал моложе», — делится Юрий, первый пациент в крае, которому провели уникальную операцию. Врачи установили ему в глубинные отделы мозга специальный электростимулятор для DBS-терапии – электроимпульсы блокируют патологические эффекты, благодаря чему удается убрать тремор и скованность движений.
Ввели стимулятор с помощью специального навигационного оборудования, которое по сотым долям миллиметра продвигается по заранее запланированной траектории. При этом невролог постоянно отслеживал состояние пациента, его неврологические функции – оперируемый должен находиться в сознании, чтобы была возможность определить эффективность вживляемого прибора. Операция длилась около 6 часов. Хирургическое вмешательство провели накануне, и уже спустя сутки после операции Юрий может принимать пищу и необходимые препараты, самостоятельно вставать и передвигаться. А спустя 1-3 месяца специалисты проведут программирование стимулятора, после этого он начнет полноценно работать.
В Красноярскую краевую клиническую больницу мужчина прилетел из заполярного Норильска. Диагноз «болезнь Паркинсона» Юрию поставили 12 лет назад, когда ему было 40 – практически перестала работать правая рука, затем начались проблемы с ногой, а потом и вовсе болезнь сказалась на всей правой части тела. И только после этого Юрий обратился к врачам.
«Сейчас планов у меня на жизнь полно, дети растут – старший с армии скоро вернется, младший школу заканчивает, их надо поднимать. Я 7 лет на пенсии, работу с таким диагнозом было сложно найти, но сейчас дела с этим явно пойдут лучше», — рассказывает Юрий.
Главный внештатный специалист-невролог Красноярского края, профессор, доцент кафедры нервных болезней КрасГМУ Наталья Исаева поясняет, что зачастую болезнь Паркинсона развивается с 55 лет, но есть и доля пациентов, которым на момент заболевания нет и 40 лет.
«Социальную значимость болезни Паркинсона трудно переоценить, это одно из наиболее распространенных нейродегенеративных заболеваний нервной системы, и по мере прогрессирования оно неуклонно приводит к ограничению повседневной активности и инвалидицаии пациентов», — отмечает она. Самый характерный симптом болезни Паркинсона, вопреки распространенному мнению, не тремор, а замедленность и скованность движений, в первую очередь страдает мелкая моторика – становится трудно нажимать на кнопки пульта, набирать текст на телефоне, застегивать пуговицы. Пациент также может жаловаться на неустойчивость при ходьбе, боли в спине, шее, суставах, на общую слабость, нарушение сна и обоняния, повышенную сонливость днем и перепады давления. А тремор и согбенная поза являются дополнительными симптомами, которые свидетельствуют о достаточно серьезной степени развития болезни Паркинсона.
Самый характерный симптом болезни Паркинсона, вопреки распространенному мнению, не тремор, а замедленность и скованность движений, в первую очередь страдает мелкая моторика – становится трудно нажимать на кнопки пульта, набирать текст на телефоне, застегивать пуговицы. Пациент также может жаловаться на неустойчивость при ходьбе, боли в спине, шее, суставах, на общую слабость, нарушение сна и обоняния, повышенную сонливость днем и перепады давления. А тремор и согбенная поза являются дополнительными симптомами, которые свидетельствуют о достаточно серьезной степени развития болезни Паркинсона.
Специалисты также отметили, что на зарождение болезни Паркинсона влияет генетический фактор, поэтому стоит обращать вниманием на своё здоровье, если у вас есть родственники, страдающие этим заболеванием. На сегодняшний день не существует мер профилактики этой болезни, однако адекватные ежедневные физические нагрузки позволяют замедлить не только развитие болезни Паркинсона, но и многих других заболеваний.
«Не все пациенты подходят для хирургического лечения, и не все в нем нуждаются, многим достаточно медикаментозной терапии. Вместе с докторами профессорской клиники мы вели очень жесткий отбор для DBS-терапии, учитывали возраст, сопутствующие патологии, когнитивные нарушения. За 3 года нашей работы мы отобрали 9 подходящих человек, однако 3-м в итоге были вынуждены отказать. Болезнь Паркинсона невозможно вылечить, но благодаря хирургическому вмешательству можно существенно улучшить качество жизни больных», — рассказывает врач-невролог Татьяна Дунайцева, ведущая прием в кабинете экстрапирамидной патологии.
Первым 3-м пациентам проведет операцию заведующий функциональным нейрохирургическим отделением новосибирского ФГБУ «Федеральный центр нейрохирургии» Минздрава России Александр Дмитриев, который обучит красноярских специалистов технологии, а после врачи краевой больницы будут выполнять операции самостоятельно. Общая потребность Красноярского края в таких операциях при более чем 5 тыс. людей, страдающих болезнью Паркинсона, – около 20-ти в год.
людей, страдающих болезнью Паркинсона, – около 20-ти в год.
Как правило, одной операции хватает на всю жизнь, однако необходима перезарядка электростимулятора, ее проводят раз в 7-15 лет. Это уже более простая операции, длится всего лишь около часа, в течение которого заменяют стимулятор, находящийся под грудной мышцей.
В Красноярском крае пациенты с 2018 года наблюдаются в двух клинических кабинетах – жители края в краевой клинической больницы на базе консультативно-диагностической поликлиники и жители Красноярска на базе профессорской клиники. По словам заведующего нейрохирургическим отделением № 2 КГБУЗ «Краевая клиническая больница» Антона Ботова, идея внедрения DBS-терапии вынашивалась долго: «Это стало неким апогеем деятельности большого числа неравнодушных людей, которые в этом участвовали, включая краевой Минздрав, который выделил квоты, федеральное правительство, администрацию больницы и кабинет экстрапирамидной недостаточности».
Вещество для лечения болезни Паркинсона обнаружили новосибирские ученые
Новосибирск. 18 марта. ИНТЕРФАКС — Ученые Новосибирского института органической химии им.Н.Н.Ворожцова (НИОХ) подобрали вещество, восстанавливающее нейроны, поврежденные болезнью Паркинсона.
18 марта. ИНТЕРФАКС — Ученые Новосибирского института органической химии им.Н.Н.Ворожцова (НИОХ) подобрали вещество, восстанавливающее нейроны, поврежденные болезнью Паркинсона.
«Нами обнаружен новый класс веществ, которые не только устраняют симптомы болезни Паркинсона, но и способствуют регенерации нейронов», — сообщил главный научный сотрудник НИОХ Константин Волчо на симпозиуме «Генные и клеточные технологии в моделировании и терапии заболеваний человека».
Он отметил, что ранее в НИОХ было синтезировано вещество, восстанавливающее двигательную активность у животных, у которых была искусственно вызвана болезнь Паркинсона особым нейротоксином.
В настоящее время доклинические исследования успешно завершены, однако этот препарат воздействует на симптомы, не восстанавливая поврежденную нервную ткань.
В дальнейшем были синтезированы производные этого вещества, причем некоторые из них существенно превосходят исходный препарат.
«По сути, мы нашли целый класс антипаркинсонических агентов», — сказал ученый.
Одно из производных, как установлено в ходе экспериментов, поддерживало выживаемость нейронов, не влияя при этом на рост других тканей, что снимает проблему онкологии.
Пока что результат подтвержден на клетках и на мышах. «Оказалось, что нами достигнут полный успех, нейроны, которые поражаются токсином, практически полностью восстановились. Это означает, что появляется надежда не только на симптоматическую, но и реальную терапию болезни Паркинсона с восстановлением нейронов», — отметил К.Волчо.
По его словам, продолжение экспериментов на обезьянах сталкивается с финансовыми и этическими ограничениями. При этом не факт, что соединение, эффективное для мышей, подействует на приматов, подчеркнул специалист.
Выходом могли бы стать испытания на клеточных линиях людей, страдающих паркинсонизмом, и создание «библиотеки» соединений, эффективных против заболевания, считает К.Волчо.
ИСТОЧНИКИ
Вещество для лечения болезни Паркинсона обнаружили новосибирские ученые
Интерfакс Образование (academia.interfax.ru), 18/03/2019
Новосибирские ученые подобрали вещество для лечения болезни Паркинсона
Новости сибирской науки (www.sib-science.info), 19/03/2019
Новосибирские ученые обнаружили новое вещество, восстанавливающее поврежденные болезнью Паркинсона нейроны
— Общественное телевидение России, 18/03/2019
Вещество для лечения болезни Паркинсона нашли ученые из Новосибирска
— ИА Политика сегодня (polit.info), 18/03/2019
Российские ученые нашли средство от болезни Паркинсона
— ИА Амител (amic.ru), 18/03/2019
Российские ученые нашли средство от болезни Паркинсона
— Gorodskoyportal.ru/barnaul, 18/03/2019
Российские ученые нашли средство от болезни Паркинсона
— Mirtesen.sputnik.ru, 18/03/2019
В России нашли средство от болезни Паркинсона
— Ura.ru (ura.news), 18/03/2019
В России нашли средство от болезни Паркинсона
— Gorodskoyportal.ru/ekaterinburg, 18/03/2019
Новосибирские ученые нашли вещество против болезни Паркинсона
— The world news (theworldnews.net), 18/03/2019
Новосибирские ученые получили вещество для лечения болезни ПаркинсонаRusBase (rb.ru), 18/03/2019
Новосибирские ученые подобрали вещество для лечения болезни Паркинсона
— Новосибирские новости (nscn.ru), 18/03/2019
Новосибирские ученые нашли вещество против болезни Паркинсона
— Российская газета (rg.ru), 18/03/2019
В России нашли средство от болезни Паркинсона
— Между строк (mstrok.ru), 19/03/2019
Новосибирские ученые нашли вещество против болезни Паркинсона
— Красноярский медицинский портал (krasgmu.net), 19/03/2019
Новосибирские ученые нашли вещество против болезни Паркинсона- Здоровая Чувашия (med.cap.ru), 19/03/2019
Современные методы лечения нарушений сна при болезни Паркинсона у пациентов, ранее подвергшихся радиационному воздействию | Слизкова
1. 30 лет после Чернобыля: патогенетические механизмы формирования соматической патологии, опыт медицинского сопровождения участников ликвидации последствий аварии на Чернобыльской электростанции : монография / под ред. С.С. Алексанина. СПб. : Политехника-принт, 2016. 506 с.
30 лет после Чернобыля: патогенетические механизмы формирования соматической патологии, опыт медицинского сопровождения участников ликвидации последствий аварии на Чернобыльской электростанции : монография / под ред. С.С. Алексанина. СПб. : Политехника-принт, 2016. 506 с.
2. Гундарова О.П., Федоров В.П., Афанасьев Р.В. Оценка психоневрологического статуса ликвидаторов радиационных аварий. Воронеж : Науч. книга, 2012. 232 с.
3. Ковров Г.В., Агальцов М.В., Сукмарова З.Н. Эффективность мелатонина пролонгированного высвобождения при первичных нарушениях сна у пациентов старше 55 лет // Неврология, нейропсихиатрия, психосоматика. 2016. Т. 8, № 2. С. 24–30.
4. Левашкина И.М. Дисциркуляторные изменения головного мозга у ликвидаторов последствий аварии на Чернобыльской АЭС по данным диффузионно-тензорной магнитно-резонансной томографии : автореф. дис. … канд. мед. наук. СПб., 2019. 24 с.
дис. … канд. мед. наук. СПб., 2019. 24 с.
5. Левин О.С. Сосудистый паркинсонизм: 20 лет спустя // РМЖ. 2017. № 21. С. 1500–1506.
6. Нодель М.Р., Шевцова К.В. Гиперсомния при болезни Паркинсона: диагностика, патофизиология, подходы к терапии // Неврологический журнал. 2017. № 2. С. 57–63.
7. Слизкова Ю.Б., Брюзгин В.А. Коррекция расстройств сна у сотрудников МЧС: результаты применения мелатонина пролонгированного действия // Неврология, нейропсихиатрия, психосоматика. 2017. Т. 9, № 1. С. 67–70.
8. Ушаков И.Б., Федоров В.П. Нейроморфологические корреляты пролонгированных радиационных воздействий // Мед.-биол. и соц.-психол. пробл. безопасности в чрезв. ситуациях. 2018. № 3. С. 86–97.
С. 86–97.
9. Федоров В.П. Церебральные структурно-функциональные паттерны фракционированного гамма-облучения // Строение организма человека и животных в норме, патологии и эксперименте: сб. работ, посвящ. 85-летию со дня рождения проф. А.С. Леонтюка / под ред. Т.М. Студеникиной, И.А. Мельникова, В.С. Гайдука ; Белорус. гос. мед. ун-т. Минск : БГМУ, 2017. С. 184–188.
10. Brodsky M.A., Godbold J., Roth T. Oanow C.W. Sleeping in Parkinson’s disease: a controlled study // Mov. Disord. 2003. Vol. 18, N 6. P. 668–672. DOI: 10.1002/mds.10429.
11. Gallagher D.A., Lees A.J., Schrag A. What are most important nonmotor symptoms in patients with Parkinson’s disease and we missing them? // Mov. Disord. 2010. Vol. 25, N 15. P. 2493–2500. DOI: 10.1002/mds.23394.
12. Sobreira-Neto M.A., Pena-Pereira M.A., Sobreira E.S.T. [et al.]. High Frequency of Sleep Disorder in Parkinson’s Disease and Its Relationship with Quality of Life // Eur. Neurol. 2017. Vol. 78, N 5/6. P. 330–337. DOI: 10.1159/000481939.
Sobreira-Neto M.A., Pena-Pereira M.A., Sobreira E.S.T. [et al.]. High Frequency of Sleep Disorder in Parkinson’s Disease and Its Relationship with Quality of Life // Eur. Neurol. 2017. Vol. 78, N 5/6. P. 330–337. DOI: 10.1159/000481939.
13. Suziki К., Okuma Y., Uchiyama T. [et al.]. Impact of sleep-related symptoms on clinical motor subtypes and disability in Parkinson’s disease: a multicenter cross-sectional study // J. Neurol. Neurosurg. Psychiatry. 2017. Vol. 88, N 11. P. 953–959. DOI: 10.1136/jnnp-2017-316136.
14. Tandberg Е., Larson J.P., Karlsen K. Excessive daytime sleeping benefi in Parkinson’s disease: a community-based study // Mov. Disord. 1999. Vol. 14, N 6. P. 922–927.
15. The report of the Committee without its annexes appears as Official Records of the General Assembly, Sixty-third Session, Supplement N 46. 2011. 220 р.
2011. 220 р.
Всемирный день борьбы с болезнью Паркинсона | Новости
Более 6 миллионов человек в мире и 280 тысяч пациентов в России страдают болезнью Паркинсона, вторым по распространенности нейродегенеративным заболеванием после болезни Альцгеймера. Это хроническое прогрессирующее заболевание головного мозга чаще диагностируется в возрасте старше 50 лет. Однако болезнь «молодеет», кроме того, от первых симптомов до постановки диагноза может пройти более 10 лет. О ключевых проблемах, с которыми сталкиваются пациенты, и путях их решения рассказывали эксперты на пресс-конференции, посвященной Всемирному дню борьбы с болезнью Паркинсона, который ежегодно отмечается 11 апреля.
Болезнь Паркинсона приобретает все большую социальную значимость. В том числе потому, что начало болезни все чаще приходится на более молодой возраст: в нашем центре по лечению паркинсонизма около трети пациентов в возрасте 45–60 лет. Кроме того, болезнь постоянно прогрессирует, постепенно лишая человека важных двигательных навыков, необходимых для повседневной жизни. Это приводит к инвалидизации пациентов на развернутой стадии болезни.
Кроме того, болезнь постоянно прогрессирует, постепенно лишая человека важных двигательных навыков, необходимых для повседневной жизни. Это приводит к инвалидизации пациентов на развернутой стадии болезни.
Среди основных симптомов заболевания: замедленность движений и скованность мышц, замедленная и шаркающая походка, семенение, потеря равновесия, дрожание конечностей, застывшее лицо, замедленность мышления и нарушение концентрации внимания, несмотря на сохранность интеллекта. Специалисты отмечают, что задолго до основных симптомов могут наблюдаться снижение обоняния, нарушения сна, частые запоры, депрессии.
«Двигательные нарушения при болезни Паркинсона возникают вследствие нарушения работы экстрапирамидной системы головного мозга, которая обеспечивает согласованность работы различных мышц, выполнение автоматизированных движений, — подчеркнула Алла Аркадьевна Тимофеева, доцент, к.м.н., кафедры неврологии Первого СПбГМУ им. Павлова. — И именно эти движения страдают при данном заболевании: нарушаются ходьба, бег, повороты, способность сесть, встать, страдают письмо, навыки одевания, нарезания еды и прочие привычные движения. При этом сила каждой отдельной мышцы не страдает, но рассогласованность их работы не дает человеку нормально двигаться».
При этом сила каждой отдельной мышцы не страдает, но рассогласованность их работы не дает человеку нормально двигаться».
Тремор (дрожание) в конечностях, который многие считают обязательным симптомом болезни Паркинсона, встречается лишь в половине случаев. А вот замедленность, скованность мышц — это обязательные симптомы болезни. В ряде случаев они могут сопровождаться болями в мышцах, что порой становится причиной постановки неправильного диагноза.
Возникновение заболевания связано с дегенерацией дофаминергических нейронов головного мозга . Почему это происходит, достоверно не известно. К факторам риска причисляют как генетическую предрасположенность, так и влияние внешних факторов, таких как плохая экологическая обстановка, воздействие пестицидов, травмы головы.
В настоящее время болезнь Паркинсона неизлечима, хотя активно ведутся разработки препаратов, способных приостановить ее развитие, изучаются возможности генной терапии, использования антител и других инновационных подходов.
Медикаментозная терапия способна уменьшать выраженность симптомов, давая возможность пациентам с болезнью Паркинсона жить и работать на протяжении долгого времени — 10–15 и более лет. Существует несколько групп препаратов для лечения болезни Паркинсона. Одна из групп — препараты, содержащие леводопу, они уже более полувека являются самыми эффективными и хорошо переносимыми препаратами. Лечение болезни, особенно у пациентов более молодого возраста, как правило, начинают с препаратов других групп. Однако в определенный период леводопа должна быть назначена всем пациентам с болезнью Паркинсона, иначе проходят драгоценные месяцы и годы нормальной либо приближенной к нормальной двигательной активности. В большинстве случаев пациентам назначается комплексная медикаментозная терапия, включающая в себя несколько таблетированных препаратов. Со временем у пациентов возникают колебания в проявлении симптомов в течение суток. Весь день делится на периоды уменьшения выраженности симптомов после приема препаратов и периоды резкого нарастания проявления болезни после окончания действия лекарств. Колебание выраженности симптомов в течение дня — это не результат привыкания к препаратам, а проявление прогрессирования нейродегенеративного процесса, лежащего в основе болезни. На развернутых стадиях заболевания, когда таблетки становятся недостаточно эффективными для помощи пациентам, используется метод внутрикишечной доставки препаратов леводопы с помощью помпы, нейрохирургическое лечение с внедрением электродов в глубинные структуры головного мозга. Эти методы помогают обеспечить пациенту стабильную компенсацию симптомов в течение дня.
Колебание выраженности симптомов в течение дня — это не результат привыкания к препаратам, а проявление прогрессирования нейродегенеративного процесса, лежащего в основе болезни. На развернутых стадиях заболевания, когда таблетки становятся недостаточно эффективными для помощи пациентам, используется метод внутрикишечной доставки препаратов леводопы с помощью помпы, нейрохирургическое лечение с внедрением электродов в глубинные структуры головного мозга. Эти методы помогают обеспечить пациенту стабильную компенсацию симптомов в течение дня.
Важную роль для сохранения активного образа жизни пациента играют реабилитационные мероприятия, включающие двигательные упражнения, творческие занятия, психологическую поддержку. В школе пациентов в Санкт-Петербурге есть все эти компоненты. Это не только залог успеха в лечении двигательных нарушений, но и возможность сделать жизнь пациента более активной, раскрасить ее в позитивные тона, дать возможность снова обрести свое место в обществе. Об этом подробно рассказали специалисты, которые принимают участие в школах пациентов.
Об этом подробно рассказали специалисты, которые принимают участие в школах пациентов.
Надежда Николаевна Хахулина, координатор проекта «Школы для пациентов с болезнью Паркинсона»: «Английская фамилия Паркинсон заставляет вспомнить о грозном недуге, постепенно отбирающем у больного способность двигаться, говорить, мыслить… Но иногда случаются чудеса: пациент, которого вчера ничего не радовало, сегодня надевает красивую одежду и идет на реабилитацию. Танцевальная терапия — один из эффективных методов лечения этой болезни, где таблетки часто оказываются бессильными. Людям, которые сейчас танцуют, еще недавно было трудно сделать несколько шагов. Еще несколько лет назад многие из них выглядели неухоженными, грустными, потерявшими интерес к жизни. Сейчас это красивые, общительные люди, которые живут, а не существуют. Их пример заражает других. Занятия в атмосфере добра, красоты, взаимопомощи творят чудеса. И я счастлива быть неотъемлемой частичкой этого проекта, который, как и каждый его участник, стал частью моей жизни. Уже невозможно представить себя без наших танцевальных пятниц, без теплого общения за праздничным столом, без нашего волшебного зала, где совсем не похожие на пациентов люди кружатся в вихре жизни».
Уже невозможно представить себя без наших танцевальных пятниц, без теплого общения за праздничным столом, без нашего волшебного зала, где совсем не похожие на пациентов люди кружатся в вихре жизни».
Елена Аркадьевна Хвостикова, руководитель «Центра помощи пациентам «Геном»»: «Там, где еще не всегда справляются лекарства, срабатывают воля к жизни и любовь к близким. Именно эту любовь и стремление к жизни мы стараемся привить с помощью дансинг-терапии. И каждую нашу встречу мы наблюдаем за волшебством преображения и чудесами пробуждения к жизни. Лично для меня этот проект — это счастье объединения. Взаимодействие, интеграция, общность: вместе мы по-настоящему становимся единым целым. И каждый из нас: и те, кто помогает пациентам, и те, кто страдает от болезни Паркинсона, — дополняет друг друга, несмотря на свой уникальный жизненный путь, сферу интересов и область деятельности. Порой слезы счастья на глазах оттого, что клуб стал родным местом для наших пациентов, точкой, в которой все друг друга дополняют. Пазл сложился. Именно объединение — это ключ к сердцу каждого пациента, который раскрывает потенциал максимальных возможностей по преодолению трудностей, связанных с болезнью Паркинсона».
Пазл сложился. Именно объединение — это ключ к сердцу каждого пациента, который раскрывает потенциал максимальных возможностей по преодолению трудностей, связанных с болезнью Паркинсона».
Пресс-конференция организована «Центром помощи пациентам «Геном»» при спонсорской поддержке компании AbbVie.
Новое средство от болезни Паркинсона
Работает в сфере медицинского копирайтинга 2 года. Она учится в аспирантуре психологического факультета. Автор ряда научных публикаций в области клинической психологии. Кроме того, она изучает физиологию центральной нервной системы, нейропсихологию и психиатрию. В свободное время изучает практики внимательности и проводит психологические консультации.
Что объединяет художника Сальвадора Дали , актера Майкла Дж. Фокса, боксера Мохаммеда Али , музыканта Оззи Осборна и Папы Иоанна Павла II ? Медицинский диагноз.Все они, а также еще 10 миллионов человек во всем мире страдают болезнью Паркинсона. Кратко о заболевании и подробностях его комплексного лечения — читайте прямо сейчас в статье MediGlobus .
ПРОЧИТАЙТЕ:
Причины болезни Паркинсона
Первые симптомы болезни Паркинсона
Признаки болезни Паркинсона
Лечение болезни Паркинсона RANC
Медицинское лечение болезни Паркинсона
Хирургическое лечение болезни Паркинсона
Шансы на выздоровление от болезни Паркинсона
БОЛЕЗНЬ ПАРКИНСОНА: ПРИЧИНЫ, ПРИЗНАКИ И СИМПТОМЫ
Болезнь Паркинсона — хроническое, медленно прогрессирующее дегенеративное заболевание нервной системы , влияющее на двигательные функции, приводящее к замедлению движений и затруднениям при ходьбе.
Первое упоминание об этой болезни упоминается в 175 AD . Древнеримский врач Клавдий Гален посвятил свою работу «О дрожании, пульсации, судорогах и треморе», в которой он описал симптомы болезни и предлагаемое лечение. Первое исследование болезни было проведено английским врачом Джеймсом Паркинсоном в 1817 году. Оно легло в основу его «Очерка о трепетном параличе», позже болезнь была названа по имени доктора.
В настоящее время — болезнь Паркинсона является вторым по распространенности возрастным неврологическим заболеванием после болезни Альцгеймера и одной из самых загадочных патологий . Причины болезни Паркинсона все еще изучаются, методы лечения усовершенствованы .
ПРИЧИНЫ БОЛЕЗНИ ПАРКИНСОНА: ЧТО НОВОЕ ИССЛЕДОВАНИЕ ПОКАЗЫВАЕТ США
Согласно американскому порталу http://www.parkinson.org, современные исследования сосредоточены на попытках идентифицировать и найти генов (или комбинация генов), что приводит к болезни Паркинсона.На сегодняшний день мутации обнаружены в 4 генах, которые имеют прямое отношение к заболеванию. Исследователи обнаружили, что эти мутации приводят к гибели дофамина нейронов .
Дофамин — это не только гормон счастья. Это также нейротрансмиттер и отвечает за двигательную активность человека. Потеря 70-80% нейронов, выделяющих дофамин, приводит к нарушению движений и тремору в конечностях.
Согласно новостной сайт https: // parkinsonsnewstoday.com от 2 мая 2018 г., журнал Neurology опубликовал описание последнего исследования болезни «Легкая ЧМТ и риск болезни Паркинсона» / A Chronic Effects of Neurotrauma Consortium Study. Его результаты говорят, что черепно-мозговая травма , в частности сотрясение мозга , может увеличить риск болезни Паркинсона у мужчин на 50% .
СИМПТОМЫ БОЛЕЗНИ ПАРКИНСОНА
Первым признаком болезни является дрожание одной руки в покое.Люди часто не обращают внимания на легкий тремор, списывая его на усталость, личные переживания, чрезмерное эмоциональное напряжение и т. Д.
Болезнь Паркинсона развивается медленно , со временем начинают дрожать обе руки и голова. Когда человека что-то беспокоит, тремор становится сильнее, тогда как в обычных случаях он может полностью уйти в покой.
Получить бесплатную консультацию
ПРИЗНАКИ БОЛЕЗНИ ПАРКИНСОНА
Заболевание чаще всего диагностируется у мужчин старше 60 лет лет.Женщины болеют болезнью Паркинсона в 1,5 раза реже чаще. Вначале болезнь протекает почти бессимптомно . По мере развития заболевания начинают появляться его явные признаки.
основных признаков болезни Паркинсона:
- медлительность и ограниченность движений: пациент может надолго замерзнуть в неудобной позе;
- шаркающая походка ;
- лицо становится застывшим, лишенным эмоций;
- речь становится тихой , монотонной;
- мышечный тонус повышается: слегка согнутые руки и ноги, сутулость, голова вперед;
- трудность передвижения : человеку трудно начать движение и трудно остановиться; трудно удерживать равновесие;
- кожа становится жирной; повышается слюноотделение;
- усиливает потоотделение ; снижение обоняния;
- возникает запор; проблемы с мочеиспусканием;
- происходит постепенная полная потеря контроля над телом.
СПОСОБЫ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА
ЛЕЧЕНИЕ БОЛЕЗНИ ПАРКИНСОНА НОВЫМ МЕТОДОМ RANC
Одним из современных методов лечения этого неврологического заболевания является RANCVeRation Of 9000 Centers. ) метод. Его основная цель — восстановить деятельность нервных центров. После курса процедур RANC к пациенту возвращается способность контролировать собственные движения , тремор в конечностях уменьшается и со временем исчезает.
Автор метода RANC — российский невролог А.А. Пономаренко . Он предполагает, что дофаминовые нейроны (те, которые отвечают за двигательные функции человека) не погибают, а лишь в максимально возможной степени снижают свою активность под действием определенных факторов и, таким образом, перестают выполнять свои функции.
Лечение болезни Паркинсона методом RANC включает инъекцию 5% АНАЛГИНА пациенту во все болезненных участков трапециевидных мышц, так как они соответствуют участкам мозга с нарушенными функциями.Кратковременная боль от процедуры запускает в мозгу процесс, который перезапускает работу дофаминовых нейронов, таким образом возобновляя производство дофамина.
Новый метод RANC быстро стал популярным в лечении болезни Паркинсона в России, так как показывает хороших результатов за короткое время — часто пациентам назначают 2-3 процедуры в течение 6 недель.
МЕДИЦИНСКОЕ ЛЕЧЕНИЕ БОЛЕЗНИ ПАРКИНСОНА
Как мы уже говорили, «дрожащий паралич» вызывает дефицит дофамина в головном мозге.Следовательно, препараты нацелены на , имитирующее функций этого нейромедиатора. Дофаминергические препараты способствуют снижению мышечного тонуса, улучшают координацию движений, уменьшают тремор в голове и конечностях.
наиболее распространенных препаратов для лечения болезни Паркинсона:
- Леводопа — первое и наиболее эффективное средство против болезни Паркинсона. Действие этого вещества обусловлено его превращением в дофамин непосредственно в центральной нервной системе, что восполняет его дефицит и впоследствии устраняет симптомы болезни.
- Сегелин — это ингибитор, который способствует более длительному воздействию дофамина на мозг.
- Антихолинергические препараты блокируют нервные импульсы, контролирующие движение мышц. Наиболее эффективен для пациентов старше 70 лет с сильным тремором и слюнотечением.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ БОЛЕЗНИ ПАРКИНСОНА
Когда болезнь быстро прогрессирует и пациенту трудно двигаться , разговаривать, работать и жить полноценной жизнью, специалисты рекомендуют и обсуждают с пациентами другие возможности лечения. проведение хирургического вмешательства.
Самый современный хирургический метод лечения болезни Паркинсона — это глубокая стимуляция головного мозга (DBS). Процедура предполагает введение в мозг специальных электродов, которые создают электрические импульсы.
Стимуляция определенных участков мозга с нарушенными функциями электрическими импульсами избавляет пациента от тремора, восстанавливает контроль над телом и эмоциями.
БОЛЕЗНЬ ПАРКИНСОНА — ШАНСЫ ИЗБЕЖАНИЯ
Несмотря на наличие эффективных современных методов лечения болезни Паркинсона, болезнь не излечима на 100% .
Тщательно подобранное лечение может улучшить качество жизни пациента, дать ему возможность контролировать движения, речь и эмоции.
Помните, болезнь Паркинсона больше не «трепетный паралич».
Да, это комплекс и загадочное неврологическое заболевание .
Но это излечимо.
Новые методы лечения болезни Паркинсона помогают надолго устранить симптомы недуга и вернуть пациенту радость жизни.
Будьте здоровыми с MediGlobus .
Получить бесплатное предложение
Работает в сфере медицинского копирайтинга 2 года. Она учится в аспирантуре психологического факультета. Автор ряда научных публикаций в области клинической психологии. Кроме того, она изучает физиологию центральной нервной системы, нейропсихологию и психиатрию. В свободное время изучает практики внимательности и проводит психологические консультации.
Врач общей практики, Врач-эксперт, Заведующий отделением врачей-координаторов.
Как новый метод MRI-HIFU может помочь пациентам с эссенциальным тремором и болезнью Паркинсона?
Диагностика и лечение мальформации Киари за рубежом
ТОП-5 клиник в области нейрохирургии
Болезнь Паркинсона в России: распространенность и заболеваемость
Резюме:Обобщены результаты региональных исследований частоты болезни Паркинсона (БП) и заболеваемости ею в России, выявлены основные факторы, определяющие качество оценок эпидемиологических показателей этого заболевания.В статье обобщены данные 19 оригинальных исследований по эпидемиологии паркинсонизма и болезни Паркинсона в России, опубликованных в период с 2005 по 2015 год. Из-за статистической неоднородности первичных результатов вычислительная аналитика к данным не применялась; Однако объединение данных позволило провести анализ тенденций эпидемиологических показателей. Методологической основой большинства исследований являлась обращаемость за медицинской помощью; в двух исследованиях использовались поквартирные опросы. Одно из исследований показало сомнительно низкие эпидемиологические показатели, полученные из медицинских карт, а остальные показали стандартизованную распространенность 30.0–139,9 / 100 000 и заболеваемость 7,63–21,8 / 100 000 в год. Вклад болезни Паркинсона в нозологическую структуру паркинсонизма составил> 61,3%. Оценка количества больных БП в России составляет около 210 000 человек. Сделаны выводы о распространенности БП в России по результатам сквозного исследования уровня показателей в западных странах. Распространенность БП по обращаемости в 2-3 раза меньше, чем при постоянных исследованиях, как отечественных, так и зарубежных.Заболеваемость БП, продемонстрированная в половине исследований, стабильна от региона к региону и сопоставима с общепризнанными значениями.
Библиография:
1. Lau LM de, Breteler MM. Эпидемиология болезни Паркинсона. Lancet Neurol 2006; 5 (6): 525-535
2. Левин О.С. Клиническая эпидемиология болезни Паркинсона. В кн .: Иллариошкин С.Н., Левин О.С., ред. Болезнь Паркинсона и двигательные расстройства: Руководство для врачей: матер. II Nat. Конгресс.М., 2011; п. 5-9
3. Муангпайсан В., Мэтьюз А., Хори Н. и др. Систематический обзор распространенности и заболеваемости болезнью Паркинсона во всем мире. J Med Assoc Thai 2011; 94 (6): 749-55
4. Информация о симптомах Паркинсона: У кого болезнь Паркинсона начинается рано? Американская ассоциация болезни Паркинсона (APDA). http://www.apdaparkinson.org/parkinsons-disease/information-on-parkinsons-symptoms/ (13.06.2016)
5. Chen JJ. Болезнь Паркинсона: качество жизни, связанное со здоровьем, экономические затраты и последствия раннего лечения.Am J Manag Care 2010; 16 (4 приложения): 87-93
6. Роменская Л.Х. Вопросы эпидемиологии, клиники и лекарственной терапии болезни Паркинсона: автореф. М., 1976: 22 с.
7. Катунина Е.А., Авакян Г.Н., Бездольный Ю.Н. и др. Эпидемиология болезни Паркинсона. Ж. Неврол Психиатр им С.С. Корсакова 2009; 109 (11): 76-80
8. Страчунская Е.Ю. Паркинсонизм с позиций современных информационных концепций медицины. Смоленск, 2008; 208 с.
9. Левин О.С., Докадина Л.V. Эпидемиология паркинсонизма и болезни Паркинсона. Неврологический Журнал (Москва) 2005; 10 (5): 41-49
10. Гашилова Ф.Ф. Клинические и параклинические аспекты болезни Паркинсона в Томске: автореф. Новосибирск, 2006; 22 п.
11. Байтимеров А.Р. Эпидемиологическое, клинико-генетическое исследование болезни Паркинсона в Республике Башкортостан: автореф. Уфа, 2007; 22 п.
12. Антонен Э.Г. Структура паркинсонизма в Республике Карелия. В кн .: Иллариошкин С.Н., Яхно Н.Н., ред.Болезнь Паркинсона и двигательные расстройства: Руководство для врачей: в материале I Nat Congress. Москва: ООО «Диалог», 2008; п. 260
13. Маркин С.П., Маркина В.А., Чуприна С.Е. Эпидемиологические исследования распространенности болезни Паркинсона в Воронежской области. В кн .: Иллариошкин С.Н., Яхно Н.Н., ред. Болезнь Паркинсона и двигательные расстройства: Руководство для врачей: матер. Я Нат. Конгресс. Москва: ООО «Диалог», 2008; п. 276
14. Похабов Д.В., Абрамов В.Г., Нестерова Ю.В. и др. Эпидемиология экстрапирамидных расстройств в Красноярском крае.В кн .: Иллариошкин С.Н., Яхно Н.Н., ред. Болезнь Паркинсона и двигательные расстройства: Руководство для врачей: матер. II Nat. Конгресс. Москва, 2011; п. 10-13
15. Сичинава Д.К., Барабанова М.А. Эпидемиология болезней Паркинсона и Паркинсона в Краснодарском крае. В кн .: Иллариошкин С.Н., Яхно Н.Н., ред. Болезнь Паркинсона и двигательные расстройства: Руководство для врачей: матер. Я Нат. Конгресс. Москва: ООО «Диалог», 2008; п. 282
16. Саютина С.Б., Шпрах В.В., Валиулин М.А. и др.Проблемы диагностики и лечения болезни паркинсона в Иркутской области. Сибирский Мед Журнал 2009; 110 (7): 173-175
17. Шиндряева Н.Н. Анализ рельефной работы регионального отделения у больных с экстрапирамидной патологией. Аспирантский вестник Поволжья 2010; (3-4): 89-93
18. Василенко А.Ф., Шамуров Ю.С., Костенкова Л.Ю. Болезнь Паркинсона в деятельности врача общей практики: клинико-диагностические подходы. Медицинский вестник Башкортостана 2010; 5 (6): 35-39
19. Залялова З.А., Калашниковва О.С., Абдулгалимова Д.М. Паркинсонизм в Республике Татарстан по данным Республиканского клинико-диагностического центра экстрапирамидной патологии и ботулинотерапии. Неврологический Вестник 2011; XLIII (2): 92-96
20. Ковальчук А.Ю., Быканова М.А., Пизова Н.В. и др. Клинико-эпидемиологические аспекты болезни Паркинсона. Ж. Неврол и Психиатр им С.С. Корсакова 2011; 111 (12): 74-76
21. Блохина И.А., Саютина С.Б. Проблемы диагностики и лечения болезни Паркинсона в сельской местности.В кн .: Гусев Эл, изд. Мат. X Всероссийский съезд неврологов с международным участием. Нижний Новгород, 2012; п. 324
22. Раздорская В.В., Воскресенская О.Н., Юдина Г.К. Диагностическая надежность амбулаторной неврологической помощи пациентам с болезнью Паркинсона. Саратовский научно-медицинский журнал 2012; 8 (2): 513-517
23. Сапронова М.Р., Шнайдер Н.А. Эпидемиологические, клинические и генетические особенности болезни Паркинсона (на примере г. Железногорска). Неврология, нейропсихиатрия и психосоматика 2014; (4): 59-64
24.Росинская А.В. Эпидемиология экстрапирамидных расстройств в Приморском крае. В кн .: Клинические проблемы диагностики и лечения двигательных расстройств: Тихоокеанская научно-практическая конференция с международным участием, Владивосток, 11-13 сентября 2015 г. Владивосток, 2015: 13-16
25. Иллариошкин С.Н., Иванова-Смоленская И.А. Трясущийся гиперкинез. Москва: Атмосфера, 2011; 360 с.
26. Райк МС де, Рокка В.А., Андерсон Д.В. и др. Популяционный взгляд на диагностические критерии болезни Паркинсона.Neurol 1997; 48 (5): 1277-1281
27. Раздорская В.В., Воскресенская О.Н., Юдина Г.К. Заболеваемость паркинсонизмом в Саратове. В кн .: Иллариошкин С.Н., Яхно Н.Н., ред. Болезнь Паркинсона и двигательные расстройства: Руководство для врачей: Материалы III Национального конгресса по болезни Паркинсона и двигательным расстройствам. Москва: ООО «РЦТ Соверо пресс», 2014; п. 342
28. Раздорская В.В., Юдина Г.К., Воскресенская О.Н. Статистика амбулаторных случаев болезни Паркинсона. Ж. Неврол Психиатр им С.С. Корсакова 2012; 112 (9): 72-76.
Российские исследователи создают программное обеспечение для прогнозирования симптомов Паркинсона
Новое программное обеспечение может с точностью до 96 процентов предсказать форму болезни Паркинсона и будущие симптомы, которые могут возникнуть у пациента.
Программа является результатом сотрудничества исследователей Санкт-Петербургского политехнического университета Петра Великого (СПбПУ), Института экспериментальной медицины и Университета ИТМО в России.
Эта технология может улучшить раннюю диагностику, способствовать профилактике и, в конечном итоге, улучшить общее состояние здоровья пациентов.
Программа была разработана на основе метода дискриминантного анализа, который позволяет исследователям более легко анализировать большие объемы данных и создавать группы с одинаковыми характеристиками. Технология объединяет клиническую информацию, результаты тестов и данные о прогрессировании заболевания, которые могут предоставить общие шаблоны, используемые для идентификации пациентов или конкретных признаков в соответствии с этими конкретными характеристиками.
Эта стратегия позволяет клиницистам оценить, какие методы лечения с большей вероятностью подействуют на пациента или группу пациентов.Кроме того, программное обеспечение могло предсказать, вероятно ли у пациентов разовьются определенные расстройства или симптомы.
Например, в предыдущем исследовании исследователи обнаружили, что пациенты с болезнью Паркинсона, у которых очень низкий уровень меди в крови, имеют повышенные шансы на развитие неправильной осанки. «Если врач заранее знает о потенциальной угрозе, он может заранее начать подготовку к лечению», — сообщила в пресс-релизе кандидат медицинских наук, доцент кафедры биофизики СПбПУ Марина Карпенко.
Построенное на основе искусственного интеллекта программное обеспечение способно постоянно улучшать свои прогностические способности, как пояснил Карпенко: «Программу можно« обучить »: чем больше информации в нее загружено, тем более точные выводы и рекомендации она дает. предоставить », — сказала она.
В целом, программное обеспечение может дать врачам возможность диагностировать болезнь Паркинсона на более раннем этапе, что будет способствовать быстрому и целенаправленному лечению для обеспечения наилучшего ухода за пациентами и результатов.
Исследователи планируют сделать программное обеспечение доступным в ближайшем будущем в формате, который можно будет установить на любой компьютер или смартфон.
российских химиков создают лекарство от болезней Паркинсона и Альцгеймера, Новости отрасли, Медиацентр, НоваМедика
Химики Уральского федерального университета и Университета Шри Венкатешвара (Тирупати, Индия) синтезировали новые нейропротекторные антиоксиданты на основе производных α-метил-L-ДОФА и мочевины.Результаты исследования представлены в журнале Bioorganic Chemistry.
«Клетки периферической нервной системы способны превращать L-ДОФА в дофамин, но его накопление в периферической нервной системе, например, при болезни Паркинсона, приводит к нежелательным побочным эффектам. Поэтому хорошей клинической практикой является использование L-DOPA в сочетании с карбидопой, ингибитором DOPA-декарбоксилазы », — поясняет Григорий Зырянов, соавтор статьи, профессор кафедры органической и биомолекулярной химии УрФУ.- В данном исследовании мы используем производные мочевины на основе α-метил-L-DOPA, (S) -2-амино-3- (3,4-дигидроксифенил) -2-метилпропионовой кислоты, аналог L-DOPA и карбидопы. . В этом случае, как донор водородных связей, мочевина действует как дополнительный координирующий фрагмент и помогает удерживать лекарственное соединение в рецепторах нейронов, ответственных за окислительный процесс ».
В ходе исследования уральские и индийские химики сравнили, какие из соединений α-метил-L-ДОФА и мочевины успешно преодолевают гематоэнцефалический барьер и проявляют наибольшую антиоксидантную активность, позволяя предотвратить и устранить патогенные эффекты окислительного стресса. .
Эти данные свидетельствуют о хороших перспективах использования соединений в качестве компонентов лекарственных средств: в соответствии с правилом Липинского соединения имеют не более 5 групп доноров водородных связей, не более 10 групп акцепторов водородных связей, имеют молекулярную структуру. массой менее 500 дальтон (более тяжелые вещества не преодолевают гематоэнцефалический барьер) и, наконец, обладают высокой растворимостью в воде и октаноле.
Следующий этап работы — исследования in vitro и in vivo биологической активности соединений.Ученые хотят выявить потенциальных кандидатов на роль лекарственных антиоксидантов, определить пути введения лекарств: таблетки, капсулы, внутривенные или внутримышечные инъекции или ингаляции.
Источник
Распечататьграниц | Клинико-эпидемиологические аспекты болезни Паркинсона на юге Западной Сибири
Фон
Болезнь Паркинсона — хроническое прогрессирующее заболевание головного мозга, в основном связанное с дегенерацией дофаминергических нейронов черной субстанции с внутринейрональным накоплением белка α-синуклеина и образованием внутриклеточных включений (тельца Леви).Они проявляются сочетанием гипокинезии с ригидностью, тремором покоя и нестабильностью позы, а также широким спектром немоторных проявлений (психических, вегетативных, сенсорных и т. Д.) (1–3).
Болезнь Паркинсона классифицируется как преимущественно моторное расстройство, хотя клинический немоторный полиморфизм в последние годы стал предметом обширных исследований (4–6). Это объясняется значительным влиянием немоторных симптомов на качество жизни, прогрессирование инвалидности иногда превышает негативные последствия моторно-неврологического дефицита (7–9).
На сегодняшний день не существует конкретных инструментальных или лабораторных маркеров этого заболевания, которые можно было бы надежно использовать в повседневной клинической практике. Несмотря на быстрый научно-технический прогресс в медицине, диагностика БП в рутинной практике остается клинической и основана на выявлении основных моторных признаков паркинсонизма (гипокинезия, ригидность, тремор покоя и нарушения осанки) и отсутствии атипичных симптомов. В связи с этим тщательное изучение клинических особенностей и особенностей течения заболевания чрезвычайно важно и является залогом успеха в сложном диагностическом процессе.
Изучение особенностей течения различных прогрессирующих заболеваний, в том числе болезни Паркинсона, актуально в связи с климатогеографическими особенностями Омской области, расположенной на юге Западно-Сибирской равнины. Особенности географического положения открывают эту территорию для вмешательства воздушных масс: северной Арктики, теплого юга Центральной Азии, засушливой западной части Центральной Азии и холодного востока. Различный характер воздушного потока приводит к резким перепадам температуры, что делает погоду в регионе нестабильной.Климат Омска умеренно-континентальный. По данным https://world-weather.ru, полученным в ходе многолетних наблюдений за температурой воздуха, можно представить все особенности климата Омской области:
Самая низкая средняя температура –16.9 ° C (в январе).
Самая высокая средняя температура + 18,9 ° C (июль).
Абсолютный минимум −50 ° C.
Абсолютный максимум + 40 ° C.
Из этих данных видно, насколько велики колебания температуры в течение года: 40 ° между средними значениями и 90 ° между минимальными и максимальными значениями.Это одна из особенностей континентального климата. Для Омска характерно преобладание ясных солнечных дней даже в осенне-зимний период — от 223 до 300 в течение года. Самый пасмурный месяц — декабрь; в мае количество таких дней минимально. Эти климатогеографические особенности, вероятно, могут влиять на течение хронических прогрессирующих заболеваний, таких как болезнь Паркинсона.
В соответствии с актуальностью проблемы в Омском государственном медицинском университете проведена ретроспективная клинико-эпидемиологическая оценка клинического течения болезни Паркинсона на юге Западной Сибири.
В соответствии с актуальностью проблемы, поставленной в Омском государственном медицинском университете, проведена ретроспективная клинико-эпидемиологическая оценка клинического течения болезни Паркинсона на юге Западной Сибири. Цель нашего исследования — оценить влияние климатических, географических и этнических факторов на течение болезни Паркинсона в сибирской когорте пациентов.
Методы
Пациенты
Всем пациентам (россиянам, проживающим в Сибирской части России) был поставлен диагноз БП в Омском государственном медицинском университете.Все пациенты с болезнью Паркинсона были отобраны и изучены в соответствии с международной унифицированной шкалой оценки болезни Паркинсона (UPDRS) и оценками Хоэна и Яра (10, 11). Диагноз БП основывался на критериях Банка мозга Великобритании PD (12). Кроме того, использовалась шкала депрессии Бека и тест Монреальской когнитивной оценки (MoCA) (13). Тяжесть обонятельной дисфункции оценивалась с помощью теста на определение запаха Sniffin Stick.
В данной работе мы оценили клинико-эпидемиологические особенности течения болезни у 140 пациентов с болезнью Паркинсона.Проведен ретроспективный анализ медицинской документации и оценка клинических показателей в дебюте заболевания и на момент обследования.
Это были критерии включения пациентов в исследование:
— Надежный диагноз болезни Паркинсона в соответствии с критериями Европейской федерации неврологических обществ (EFNS) совместно с Обществом двигательных расстройств 2013 г.
— подписанное информированное согласие на участие в исследовании.
— Отсутствие у пациента других нейродегенеративных заболеваний.
Критерии исключения пациентов из исследования:
— Вторичный паркинсонизм и паркинсонизм — плюс выявленные при первом посещении.
— Наличие тяжелой сопутствующей соматической патологии в стадии декомпенсации.
— Отказ пациента от участия в исследовании.
— Участие пациентов в других клинических исследованиях.
— У пациента другие заболевания, имеющие генетический компонент в патогенезе, из-за высокого риска искажения полученной информации.
Статистический анализ
Описательная статистика качественных показателей бухгалтерского учета представлена в форме абсолютных значений, процентов, их стандартных ошибок (m) и стандартных отклонений (σ). Данные для вариационных рядов с непараметрическим распределением описываются как медианы и квартили (Me [25-й; 75-й процентиль]). Для сравнения непараметрических данных использовались критерии Манна – Уитни U . Критический уровень значимости тестов определен при p ≤ 0.05. Статистическая обработка результатов проводилась с использованием лицензионных пакетов программ Statistica 10 (StatSoft, США).
Исследование одобрено этическим комитетом Омского государственного медицинского университета.
Результаты
Согласно критериям включения / исключения в исследование были включены 140 пациентов с болезнью Паркинсона, в том числе 55 мужчин и 85 женщин (у большинства пациентов была БП со средней продолжительностью 3–10 лет с симптомами, эффективно купируемыми комбинацией адекватных варианты лечения (агонисты дофамина, леводопа, амантадин).Соотношение мужчин и женщин в группе составляло 1: 1,5, с преобладанием женщин. Возраст пациентов колебался от 37 до 82 лет (медиана [25-й; 75-й процентиль], 67 лет [61; 73]): женщины — 85 (66,3 ± 9,5; возраст 68 лет [61; 72]) и мужчины, 55 лет (66,5 ± 9,7; возраст 68 лет [61; 74]). Средний возраст всех пациентов на момент обследования составил 66,4 ± 9,5 года. Леченные пациенты с БП получали различные препараты (агонисты дофаминовых рецепторов: прамипексол в дозе 1,5 мг / сут или пирибедил в дозе 150 мг / сут, л, -допа в дозе 150–200 мг / сут и амантадин. в дозировке 300 мг / сут) либо в виде монотерапии, либо в различных комбинациях.
Исследуемую группу пациентов составили 14 (10%) монголоидов и 126 (90%) пациентов европейской расы. По уровню образования группа была разделена на следующие категории: 13 (9%) человек имели среднее образование, 25 (18%) пациентов получили среднее специальное образование, 102 (73%) пациента окончили высшие учебные заведения.
Средний вес в основной группе составил 76,0 ± 14,3 кг (73,5 [65; 86]). Средний рост в исследуемой группе был 165.4 ± 8,0 см (164,0 [160; 170]). Таким образом, средний индекс массы тела составляет 27,8 ± 4,7 (27,0 [24,7; 30,7]), что свидетельствует о преобладании пациентов с избыточной массой тела.
В ходе исследования проведен анализ факторов риска развития БП и факторов защиты. Данные представлены в таблице 1.
Таблица 1 . Факторы риска / защиты для пациентов с болезнью Паркинсона.
Анализ анамнестической информации о наличии сопутствующих заболеваний показал, что пациенты с БП достаточно коморбидны и обычно имеют несколько нозологических форм в структуре диагноза.Данные представлены в таблице 2.
Таблица 2 . Коморбидность пациентов с болезнью Паркинсона.
О наличии депрессивных симптомов сообщили 4 (2,9%) пациента с БП, но депрессия различной степени тяжести при оценке по шкале депрессии Бека, проведенной в рамках данного исследования, была выявлена у 46 (71%) из 65 пациентов. осмотрел. Средний уровень депрессии в группе составил 15,6 ± 9,1 балла, что соответствует легкой степени депрессии.
Двигательные симптомы в сибирской когорте
В исследуемой группе пациентов стадия определялась по классификации Хен-Яр (1967): у 31 пациента установлена одна стадия заболевания, у 63 пациентов — две стадии, у 45 пациентов — три стадии, и у одного пациента четыре стадии заболевания.
Средняя длительность заболевания в наблюдаемой группе больных составила 6,9 ± 4,9 года. Дебют БП с моторными симптомами отмечен у 129 (92,1%) пациентов, дебют с немоторными симптомами — у 11 (7.9%) пациенты с БП. Из моторных симптомов дебюта облигатным симптомом была гипокинезия, которая анамнестически установлена у всех 140 (100%) пациентов. Остальные двигательные симптомы дебюта БП по частоте располагались в порядке убывания: тремор покоя — 76 (54,3%) пациентов, ригидность мышц — 65 (46,4%) пациентов, постуральной нестабильности в дебюте БП не отмечалось.
При анализе текущей клинической картины у больных БП гипокинезия выявлена у 140 (100%) пациентов, тремор покоя диагностирован у 95 (67.9%) пациентов, ригидность у 97 (69,3%) и постуральная нестабильность у 43 (30,7%) пациентов с БП.
Таким образом, увеличение частоты встречаемости основных моторных симптомов болезни Паркинсона в сибирской когорте за 7-летний период составило 14% для тремора покоя, 23% для ригидности мышц и 31% для постуральной нестабильности.
В нашей когорте пациентов 98 (70%) пациентов со смешанной формой болезни, 22 (16%) пациентов с ригидно-дрожащей формой и 20 (14%) пациентов с акинетико-ригидной формой болезни Паркинсона. наблюдались.Мы сравнили наши данные о двигательной недостаточности с другими когортами пациентов, которые были собраны и систематизированы в этом году (14). Данные представлены в таблице 3.
Таблица 3 . Подтипы двигателей в корпусах de novo PD по странам.
В таблице 3 представлены многочисленные исследования двигательной недостаточности при болезни Паркинсона в различных этнических группах (14–26).
Немоторные симптомы в сибирской когорте
Наиболее частыми немоторными симптомами дебюта БП в исследуемой группе были запор у 47 (33.6%) пациентов, когнитивные нарушения у 24 (17,1%) из 140 пациентов, нарушения поведения в фазе быстрого сна у 24 (17,1%) пациентов, бессонница, диагностированная в различных вариациях у 38 (27,1%) пациентов, дневная сонливость у пациентов 43 (30,7%) пациента, субъективные нарушения обонятельных ощущений на момент моторного дебюта БП у 19 (13,6%) пациентов, внеплановое похудание у 8 (5,7%) пациентов, ангидроз кожи у 7 (5%) пациентов потливость уже в дебюте БП у 21 (15%) пациента, себорея (указана как дополнительный немоторный симптом дебюта БП) у 4 (2.У 9%) пациентов, ортостатическая гипотензия — у 35 (25%) пациентов, дисфагия — у 5 (3,6%) пациентов, дисфункция органов малого таза по типу ночного мочеиспускания и недержания кала — у 17 (12,1%) пациентов.
При анализе текущих немоторных симптомов когнитивные нарушения выявлены у 61 (43,6%) пациента, психотические расстройства в виде галлюцинаций — у 7 (5%), поведенческие нарушения в фазе быстрого сна — у 65 (46,4%). %), обонятельная дисфункция — у 28 (20%), дневная сонливость — у 84 (60%), бессонница в различных вариациях — у 59 (42.1%) пациентов, незапланированная потеря веса у 12 (8,6%) пациентов, ортостатическая гипотензия у 80 (57,1%), сухость кожи у 6 (4,3%), гипергидроз у 29 (20,7%), дисфагия у 21 (15%), запор у 85 (60,7%) и ночное мочеиспускание у 41 (29,3%) пациента.
Таким образом, увеличение распространенности немоторных симптомов болезни Паркинсона в сибирской когорте за 7-летний период составило запор у 27%, когнитивные нарушения у 27%, REM-расстройства у 29%, гипосмию у 6%, ортостатический гипотония — 32%, бессонница — 15%, дневная сонливость — 29%, никтурия — 17%.Динамика АД за 7-летний период показана на Рисунке 1.
Рисунок 1 . Особенности клинической картины в дебюте БП и на момент обследования с учетом средней длительности заболевания.
Обонятельный тест (Sniffin Stick) или тест на определение запаха Sniffin Sticks (фирма Bürghard, Гамбург, Германия) был проведен у 83 пациентов, средний балл составил 7,6 ± 3,3, что соответствует аносмии. Идентификационный тест: способность обнаруживать запахи от предложенных четырех наименований.Пациенту дают карандаш для вдоха запаха и предлагают четыре варианта, один из которых он должен выбрать. Результат — сумма положительных ответов. Результат <8 баллов соответствует аносмии, 9–11 баллов - гипосмии, 12–16 баллов - нормосмии. В этой группе пациентов обонятельная дисфункция, достигающая степени аносмии, диагностирована у 47 (56,2%) пациентов, гипосмия - у 26 (31,3%) пациентов, нормосмия - у 11 (12,5%) пациентов. Данные представлены на рисунке 2.
Рисунок 2 .Распространенность и выраженность обонятельной дисфункции в основной группе пациентов с БП.
Статистический анализ группы пациентов с болезнью Паркинсона в дебюте болезни и на момент исследования с учетом средней продолжительности течения болезни 6,9 ± 4,9 года с использованием непараметрического метода Манна-Уитни U -тест показал достоверные различия в выраженности основных моторных и немоторных симптомов. На момент исследования у пациентов был более выраженный тремор покоя ( U, = 1021.5; p <0,0000001), общая брадикинезия ( p = 1,854; p <0,001) и ригидность ( p = 1,630,0; p <0,0007). При сравнении выраженности немоторных симптомов в дебюте АД и через 7 лет более выраженный запор ( U = 1387,5; p <0,000001), когнитивные нарушения ( U = 1,683,5; p <0,0002 ) поведенческие расстройства отмечены в фазе быстрого сна ( U, = 1775.5; p <0,0004), бессонница ( U = 1,082,5; p <0,0000001), дневная сонливость ( U = 1,534,0; p <0,000008), ортостатическая гипотензия ( U = 1826,0; p 90 <0,000008) и гипосмия ( U = 836,0; p <0,00004). Также наблюдается тенденция к увеличению выраженности ночного мочеиспускания ( U = 1814,5; p <0,02).
Мы сравнили результаты оценки некоторых немоторных симптомов в нашей когорте пациентов с болезнью Паркинсона с симптомами в других когортах пациентов по всему миру; данные, по которым были систематизированы в этом году (27).Данные представлены в таблице 4.
Таблица 4 . Некоторые немоторные симптомы у пациентов с БП по странам.
В таблице 4 показана распространенность основных немоторных симптомов, выявленных в ходе исследований в разных уголках земного шара (8, 28–37).
Средний балл при нейропсихологическом тестировании когнитивной сферы с использованием Монреальской шкалы оценки когнитивных функций составил 23,4 ± 3,9, что соответствует умеренным когнитивным нарушениям. Результат 20 и ниже был равен 13 (15.1%) пациентов, а в диапазоне 21–25 баллов наблюдались 43 (51,8%) пациента; нормальные значения этого теста [т.е. 26–30 были отмечены у 28 (33,1%) пациентов с БП].
Заключение
Конечно, такие факторы, как этническая принадлежность (38), географическое положение региона проживания (39), диета (40), общая продолжительность жизни (41), генетические характеристики населения (42, 43) и наличие сопутствующих заболеваний. болезни (44) влияют на развитие и характер течения как нейродегенеративных, так и других хронических прогрессирующих неврологических заболеваний.Сравнительная оценка клинических параметров болезни Паркинсона в популяциях до некоторой степени затруднена из-за разнообразия подходов к получению клинических данных и их интерпретации. Кроме того, критерии Банка мозга, разработанные в Великобритании PD, используемые в большинстве исследований, обеспечивают диагностическую точность только 82,7% для диагностики болезни Паркинсона (45). Этот показатель, безусловно, влияет на статистическую достоверность клинических и эпидемиологических исследований болезни Паркинсона и может привести к некоторым искажениям, особенно на ранних стадиях, когда клиническая картина обычно неполная, реакция на дофаминергические препараты неясна или признаки атипичный паркинсонизм пока не появился.Несмотря на значительные успехи в понимании патогенетических аспектов этого заболевания, нам все еще не хватает четких изображений или биохимических маркеров для точной диагностики болезни Паркинсона.
В своей работе мы оценили распространенность моторных и немоторных неврологических нарушений, а также некоторых факторов риска и сопутствующих заболеваний в сибирской когорте пациентов с болезнью Паркинсона. Преобладающий дебют ВР — моторный дебют. Прогрессирование болезни характеризуется учащением как моторных, так и немоторных симптомов.При сравнении распространенности моторных симптомов с другими когортами пациентов (таблица 3) мы обнаружили наибольшее сходство с канадскими (24) и, в меньшей степени, британскими (15) когортами пациентов, у которых также наблюдались смешанные формы болезни Паркинсона. преобладали. Это сходство может быть связано с близостью климатических и географических особенностей Западной Сибири и Канады с резко континентальным климатом и преобладанием в нашей когорте пациентов европейской расы. В ходе анализа также отмечено преобладание тремора в структуре клинической картины болезни Паркинсона в итальянской (14, 23), норвежской (18, 26) и южнокорейской (16) когортах.На этом фоне выглядит исследование Reinoso et al., Проведенное в 2014 г., которое показывает преобладание акинетико-ригидной формы или постуральной нестабильности с нарушениями походки до 66,5% в когорте пациентов с болезнью Паркинсона (21). довольно интересно. Соотношение форм заболеваний в когортах США (22) и Китая (19) было примерно одинаковым.
В этой статье мы сравнили распространенность немоторных симптомов болезни Паркинсона в сибирских и других когортах по всему миру.Основываясь на этих данных, сибирская когорта демонстрирует более высокую распространенность обонятельных нарушений, дневной сонливости, ортостатической гипотензии, депрессивных расстройств и поведенческих расстройств в фазе быстрого сна по сравнению с когортами, близкими по длительности болезни Паркинсона (29–33 , 35, 36). Однако распространенность дисфагии, никтурии, изменения веса и галлюцинаций оказалась ниже, чем в когортах пациентов, близких по размеру выборки и продолжительности заболевания.Рассматривать эти параметры можно только ориентировочно, поскольку они имеют различия в методике оценки немоторных симптомов, когорты имеют этнические различия, что, вероятно, влияет на конечный результат.
В исследуемой группе пациентов отмечались легкие депрессивные симптомы, легкие когнитивные нарушения и тяжелые обонятельные нарушения (аносмия).
Выраженность моторных и большинства немоторных симптомов напрямую коррелирует с длительностью БП и стадией заболевания, что подтверждается большинством клинических исследований этого заболевания (46–48).
Коморбидность пациентов с болезнью Паркинсона — актуальная проблема общественного здравоохранения. Исследование Mollenhauer et al. отражала отрицательную динамику быстрого прогрессирования болезни Паркинсона у пациентов с сердечно-сосудистыми факторами риска, нарушением регуляции уровня глюкозы в крови, нарушением метаболизма мочевой кислоты и воспалением (49). По словам Хуан Ю.Ф. у пациентов с БП риск инсульта выше, чем в популяции (50). В сибирской когорте пациентов с болезнью Паркинсона преобладали женщины с высшим образованием, избыточной массой тела, сопутствующей артериальной гипертензией, ишемической болезнью сердца и дислипидемией.Преобладание женщин в анализируемой когорте пациентов с болезнью Паркинсона, вероятно, связано с региональными особенностями более высокой медицинской потребности женщин. Данные, полученные в ходе исследования, согласуются с результатами других исследований в различных когортах и в разных частях мира (51–53).
Курение как защитный фактор риска при болезни Паркинсона подтверждается большим количеством научных исследований (54–57). Наши данные косвенно подтверждают и согласуются с ранее опубликованными исследованиями.Анализ показал, что 75% респондентов никогда не курят. Исследование показало, что домашний контакт с различными пестицидами актуален для 30% респондентов.
Сибирская когорта пациентов с болезнью Паркинсона имеет свои особенности в клинической картине болезни, в вопросах коморбидности, что требует дальнейшего изучения различных клинических, эпидемиологических и генетических аспектов заболевания с использованием единых протоколов для лучшего понимания природы болезни.Представленные в статье результаты указывают на основные направления дальнейшего более глубокого изучения данной патологии.
Заявление о доступности данныхНеобработанные данные, подтверждающие выводы этой статьи, будут предоставлены авторами без излишних оговорок. Запросы на доступ к базам данных следует направлять Роману Андреевичу Деловому, [email protected].
Заявление об этике
Исследования с участием людей были рассмотрены и одобрены этическим комитетом Омского государственного медицинского университета.Пациенты / участники предоставили письменное информированное согласие на участие в этом исследовании.
Авторские взносы
AR: концепция и дизайн исследования. IG, EK, EM и RD: сбор данных. RD: анализ и интерпретация данных, составление рукописи и критическая редакция.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Благодарности
Мы хотели бы поблагодарить за плодотворные обсуждения с Люксембургским центром системной биомедицины, особенно профессора доктора Рейко Крюгера и профессора доктора Руди Баллинга. Мы также хотим поблагодарить членов консорциума GeoPD, в частности ученого-исследователя Венкату Сатагопама из LCSB, за помощь в решении программных и технических вопросов. Благодарим IT-специалиста Павла Негодуйко за помощь в работе с электронной базой данных.
Список литературы
1.Макканн Х., Стивенс Х., Картрайт Х., Халлидей Г. М. Фенотипы α-синуклеинопатии. Park Relat Disord. (2014) 20 (Дополнение 1): S62–7. DOI: 10.1016 / S1353-8020 (13) 70017-8
CrossRef Полный текст | Google Scholar
2. Левин О.С., Федорова Н.В. Болезнь Паркинсона . 6-е изд. Москва: МЕДпресс-информ (2016). п. 384.
Google Scholar
3. Руководство по диагностике и лечению болезни Паркинсона / Иллариошкин СНОС. Левин. 3-е изд.(2019). п. 336.
Google Scholar
4. Галлахер Д.А., Лис А.Дж., Шраг А. Каковы наиболее важные немоторные симптомы у пациентов с болезнью Паркинсона и упускаем ли мы их? Mov Disord . (2010) 25: 2493–500. DOI: 10.1002 / mds.23394
CrossRef Полный текст | Google Scholar
5. Зис П., Мартинес-Мартин П., Зауэрбье А., Ризос А., Шарма Дж. К., Уорт П. Ф. и др. Бремя немоторных симптомов у леченных и нелеченных пациентов с болезнью Паркинсона на ранней стадии: аргумент в пользу немоторных подтипов. евро J Neurol . (2015) 22: 1145–50. DOI: 10.1111 / ene.12733
PubMed Аннотация | CrossRef Полный текст | Google Scholar
6. Чаудхури К.Р., Мартинес-Мартин П., Браун Р.Г., Сетхи К., Стокки Ф., Один П. и др. Метрические свойства новой шкалы немоторных симптомов болезни Паркинсона: результаты международного пилотного исследования. Mov Disord . (2007) 22: 1901–11. DOI: 10.1002 / mds.21596
PubMed Аннотация | CrossRef Полный текст | Google Scholar
7.Мартинес-Мартин П., Родригес-Бласкес С., Куртис М.М., Чаудхури К.Р., Группа валидации NMSS. Влияние немоторных симптомов на качество жизни пациентов с болезнью Паркинсона, связанное со здоровьем. Mov Disord . (2011) 26: 399–406. DOI: 10.1002 / mds.23462
PubMed Аннотация | CrossRef Полный текст | Google Scholar
8. Дункан Г.В., Кху Т.К., Ярнолл А.Дж., О’Брайен Д.Т., Коулман С.Ю., Брукс Д.Д. и др. Качество жизни, связанное со здоровьем, на ранних стадиях болезни Паркинсона: влияние немоторных симптомов. Mov Disord . (2014) 29: 195–202. DOI: 10.1002 / mds.25664
PubMed Аннотация | CrossRef Полный текст | Google Scholar
9. Бугальо П., Лампрейя Т., Мигель Р., Мендонса, доктор медицины, Каэтано А., Барбоса Р. и др. Немоторные симптомы у португальских пациентов с болезнью Паркинсона: корреляция и влияние на качество жизни и повседневную деятельность. Научный доклад (2016) 6: 32267. DOI: 10.1038 / srep32267
PubMed Аннотация | CrossRef Полный текст | Google Scholar
10.Goetz CG, Fahn S, Martinez-Martin P, Poewe W, Sampaio C, Stebbins GT и др. Пересмотр единой рейтинговой шкалы болезни Паркинсона (MDS-UPDRS), спонсируемой обществом по поводу двигательного расстройства: процесс, формат и план клинических испытаний. Mov Disord . (2007). 22: 41–7. DOI: 10.1002 / mds.21198
PubMed Аннотация | CrossRef Полный текст | Google Scholar
12. Хьюз А.Дж., Дэниел С.Е., Килфорд Л., Лис А.Дж. Точность клинического диагноза идиопатической болезни Паркинсона: клинико-патологическое исследование 100 случаев. J Neurol Neurosurg Psychiatry. (1992) 55: 181–4. DOI: 10.1136 / jnnp.55.3.181
PubMed Аннотация | CrossRef Полный текст | Google Scholar
13. Насреддин З.С., Филлипс Н.А., Бедириан В., Шарбонно С., Уайтхед В., Коллин И. и др. Монреальская когнитивная оценка, MoCA: краткий инструмент для выявления легких когнитивных нарушений. Дж. Ам Гериатр Соц . (2005) 53: 695–9. DOI: 10.1111 / j.1532-5415.2005.53221.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
14.Мочча М., Тедески Э., Угга Л., Эрро Р., Пичилло М., Каранчи Ф. и др. Изменения белого вещества и развитие моторных фенотипов при болезни Паркинсона de novo . J Neurol Sci. (2016) 367: 215–9. DOI: 10.1016 / j.jns.2016.06.015
PubMed Аннотация | CrossRef Полный текст | Google Scholar
15. Рамани Л., Малек Н., Паттерсон Дж., Ниссен Т., Ньюман Э.Дж. Связь между [(123) I] -FP-CIT SPECT и клиническим прогрессированием болезни Паркинсона. Acta Neurol Scand .(2017) 135: 400–6. DOI: 10.1111 / ane.12613
PubMed Аннотация | CrossRef Полный текст | Google Scholar
16. Choi SM, Kim BC, Cho BH, Kang KW, Choi KH, Kim JT, et al. Сравнение двух классификаций моторных подтипов при болезни Паркинсона de novo . Расстройство, связанное с паркинсонизмом . (2018) 54: 74–8. DOI: 10.1016 / j.parkreldis.2018.04.021
PubMed Аннотация | CrossRef Полный текст | Google Scholar
17. Алвес Дж., Ларсен Дж. П., Эмре М., Вентцель-Ларсен Т., Арсланд Д.Изменения моторного подтипа и риск развития деменции при болезни Паркинсона. Mov Disord . (2006) 21: 1123–30. DOI: 10.1002 / mds.20897
PubMed Аннотация | CrossRef Полный текст | Google Scholar
18. Мюллер Б., Ларсен Дж. П., Вентцель-Ларсен Т., Скей Г.О., Тиснес ОБ. Вегетативные и сенсорные симптомы и признаки при нелеченной болезни Паркинсона: частые, но легкие. Mov Disord . (2011) 26: 65–72. DOI: 10.1002 / mds.23387
PubMed Аннотация | CrossRef Полный текст | Google Scholar
19.Юань Ю.С., Чжоу XJ, Тонг Q, Zhang L, Zhang L, Qi ZQ и др. Изменение уровней аминокислотных нейромедиаторов в плазме и его корреляция с клинической неоднородностью у пациентов с ранней стадией болезни Паркинсона. ЦНС Neurosci Ther . (2013) 19: 889–96. DOI: 10.1111 / cns.12165
PubMed Аннотация | CrossRef Полный текст | Google Scholar
20. Полетти М., Фрозини Д., Паньи С., Лучетти С., Дель Дотто П., Тоньони Дж. И др. Связь между моторными подтипами и алекситимией в de novo болезни Паркинсона. Дж. Neurol . (2011) 258: 1042–5. DOI: 10.1007 / s00415-010-5878-8
PubMed Аннотация | CrossRef Полный текст | Google Scholar
21. Reinoso G, Allen JC Jr, Au WL, Seah SH, Tay KY, Tan LC Клиническая эволюция болезни Паркинсона и прогностические факторы, влияющие на двигательную прогрессию: последующее 9-летнее исследование. евро J Neurol . (2015) 22: 457–63. DOI: 10.1111 / ene.12476
PubMed Аннотация | CrossRef Полный текст | Google Scholar
22. Конно Т., Дойчлендер А., Хекман М.Г., Осси М., Варгас Э.Р., Стронгоски А.Дж. и др.Клиническая эволюция болезни Паркинсона и прогностические факторы, влияющие на двигательную прогрессию: 9-летнее наблюдение. Eur J Neurol. (2018) 386: 39–45. DOI: 10.1016 / j.jns.2018.01.013
PubMed Аннотация | CrossRef Полный текст
23. Николетти А., Мостил Дж., Николетти Дж., Арабия Дж., Иличо Дж., Ламберти П. и др. Сравнение клинических характеристик подтипов болезни Паркинсона: большое ретроспективное исследование в одном центре. Дж. Neurol Sci . (2016) 263: 888–94.DOI: 10.1007 / s00415-016-8075-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
25. Auyeung M, Tsoi TH, Mok V, Cheung CM, Lee CN, Li R, et al. Десятилетняя выживаемость и исходы в предполагаемой когорте пациентов с китайской болезнью Паркинсона с новым началом. J Neurol Neurosurg Psychiatry . (2012) 83: 607–11. DOI: 10.1136 / jnnp-2011-301590
PubMed Аннотация | CrossRef Полный текст | Google Scholar
26. Hiorth YH, Lode K, Larsen JP. Частота падений и связанные с ними особенности на разных стадиях болезни Паркинсона. евро J Neurol . (2013) 20: 160–6. DOI: 10.1111 / j.1468-1331.2012.03821.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
28. Ли Х.Дж., Чжан М.Ф., Чен М.Х., Ху А.Л., Ли Дж.Б., Чжан Б. и др. Проверка анкеты немоторных симптомов болезни Паркинсона: результаты китайского пилотного исследования. Инт Дж. Neurosci . (2015) 125: 929–35. DOI: 10.3109 / 00207454.2014.986573
PubMed Аннотация | CrossRef Полный текст | Google Scholar
29.Хедр Э.М., Эль-Фетох Н.А., Халифа Х., Ахмед М.А., Эль-Бех К.М. Распространенность немоторных особенностей в когорте пациентов с болезнью Паркинсона. Clin Neurol Neurosurg . (2013) 115: 673–7. DOI: 10.1016 / j.clineuro.2012.07.032
PubMed Аннотация | CrossRef Полный текст | Google Scholar
30. Bostantjopoulou S, Katsarou Z, Karakasis C., Peitsidou E., Milioni D, Rossopoulos N. Оценка немоторных симптомов болезни Паркинсона: недооцененная необходимость. Гиппократия. (2013) 17: 214–9.
PubMed Аннотация | Google Scholar
31. Мартинес-Мартин П., Шапира А.Х., Стокки Ф., Сетхи К., Один П., Макфи Г. и др. Распространенность немоторных симптомов при болезни Паркинсона в международном исследовании с использованием опросника немоторных симптомов у 545 пациентов. Mov Disord. (2007) 22: 1623–9. DOI: 10.1002 / mds.21586
PubMed Аннотация | CrossRef Полный текст | Google Scholar
32. Rodriguez-Violante M, Cervantes-Arriaga A, Villar-Velarde A, Corona T.Взаимосвязь типа и стороны двигательных симптомов с преобладанием немоторных симптомов при болезни Паркинсона. Neurologia. (2011) 26: 319–24. DOI: 10.1016 / S2173-5808 (11) 70076-1
PubMed Аннотация | CrossRef Полный текст | Google Scholar
34. Косентино С., Нуньес Ю., Торрес Л. Частота немоторных симптомов у перуанских пациентов с болезнью Паркинсона. Arq Neuropsiquiatr. (2013) 71: 216–9. DOI: 10.1590 / 0004-282X20130005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
35.Чхон С.М., Ха М.С., Пак MJ, Ким JW. Немоторные симптомы болезни Паркинсона: распространенность и осведомленность пациентов и их семей. Паркинсонизм, связанный с расстройством. (2008) 14: 286–90. DOI: 10.1016 / j.parkreldis.2007.09.002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
36. Чаудхури К.Р., Прието-Юрчинска С., Найду Й., Митра Т., Фрадес-Пайо Б., Тлук С. и др. Недекларирование немоторных симптомов болезни Паркинсона медицинским работникам: международное исследование с использованием опросника немоторных симптомов. Mov Disord. (2010) 25: 704–9. DOI: 10.1002 / mds.22868
PubMed Аннотация | CrossRef Полный текст | Google Scholar
37. Роменец С.Р., Вольфсон С., Галатас С., Пеллетье А., Альтман Р., Вадуп Л. и др. Валидация анкеты по немоторным симптомам (NMS-Quest). Паркинсонизм, связанный с расстройством. (2012) 18: 54–8. DOI: 10.1016 / j.parkreldis.2011.08.013
PubMed Аннотация | CrossRef Полный текст | Google Scholar
38. Райт Уиллис А., Эванофф Б.А., Лиан М., Крисвелл С.Р., Рететт Б.А.Географические и этнические различия в болезни Паркинсона: популяционное исследование участников программы Medicare в США. Нейроэпидемиология. (2010) 34: 143–51. DOI: 10.1159 / 000275491
PubMed Аннотация | CrossRef Полный текст | Google Scholar
39. Соавторы ГББ, 2016 г. по болезни Паркинсона. Глобальное, региональное и национальное бремя болезни Паркинсона, 1990–2016 гг .: систематический анализ исследования глобального бремени болезней. Lancet Neurol. (2016) 17: 939–53. DOI: 10.1016 / S1474-4422 (18) 30295-3
CrossRef Полный текст | Google Scholar
42. Алкалай Р.Н., Мирельман А., Сондерс-Пулман Р., Тан М.Х., Мехиа Сантана Н., Раймонд Д. и др. Фенотип болезни Паркинсона у евреев ашкенази с мутациями LRRK2 G2019S и без них. Mov Disord. (2013) 28: 1966–71. DOI: 10.1002 / mds.25647
PubMed Аннотация | CrossRef Полный текст | Google Scholar
44. Branson CO, Ferree A, Hohler AD, Saint-Hilaire MH. Расовые различия при болезни Паркинсона: систематический обзор литературы. Adv Parkinsons Dis. (2016) 5: 87–96. DOI: 10.4236 / apd.2016.54011
CrossRef Полный текст | Google Scholar
45. Риццо Г., Копетти М., Аркути С., Мартино Д., Фонтана А., Логрошино Г. Точность клинической диагностики болезни Паркинсона: как систематический обзор и метаанализ. Неврология. (2016) 86: 566–76. DOI: 10.1212 / WNL.0000000000002350
PubMed Аннотация | CrossRef Полный текст | Google Scholar
46. Станкович И., Петрович И., Пекмезович Т., Маркович В., Стойкович Т., Драгашевич-Мишкович Н. и др. Продольная оценка вегетативной дисфункции на ранних стадиях болезни Паркинсона. Паркинсонизм, связанный с расстройством. (2019) 66: 74–9. DOI: 10.1016 / j.parkreldis.2019.07.008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
47. Валентино Ф, Бартолотта Т.В., Косентино Дж., Мастрилли С., Арнао В., Аридон П. и др. Урологические дисфункции у пациентов с болезнью Паркинсона: ключи от клинической и неинвазивной урологической оценки. BMC Neurol . (2018) 18: 148. DOI: 10.1186 / s12883-018-1151-z
PubMed Аннотация | CrossRef Полный текст | Google Scholar
48. Тибар Х., Эль Баяд К., Бухуш А., Айт Бен Хадду Е. Х., Беномар А., Яхьяуи М. и др. Немоторные симптомы болезни Паркинсона и их влияние на качество жизни в когорте марокканских пациентов. Передний Neurol . (2018) 9: 170. DOI: 10.3389 / fneur.2018.00170
PubMed Аннотация | CrossRef Полный текст | Google Scholar
49.Молленхауэр Б., Циммерманн Дж., Сиксель-Деринг Ф., Фокке Н.К., Вик Т., Эбентойер Дж. И др. Исходные предикторы прогрессирования через 4 года после постановки диагноза болезни Паркинсона в когорте De novo Parkinson Cohort (DeNoPa). Move Disord. (2019) 34: 67–77. DOI: 10.1002 / mds.27492
PubMed Аннотация | CrossRef Полный текст | Google Scholar
51. Малек Н., Лоутон М.А., Ласточка Д.М., Гроссет К.А., Марринан С.Л., Баджадж Н. и др. Сосудистые заболевания и факторы риска сосудов в отношении двигательных функций и когнитивных функций на ранних стадиях болезни Паркинсона. Move Disord. (2016) 31: 1518–26. DOI: 10.1002 / mds.26698
PubMed Аннотация | CrossRef Полный текст | Google Scholar
52. Fanciulli A, Göbel G, Ndayisaba JP, Granata R, Duerr S, Strano S, et al. Гипертензия на спине при болезни Паркинсона и множественной системной атрофии. Clin Auton Res. (2016) 26: 97–105. DOI: 10.1007 / s10286-015-0336-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
53. Ли Х.Дж., Юй Ю, Чен И, Лян Х.Й.Факторы сосудистого риска усугубляют прогрессирование болезни Паркинсона: пятилетнее последующее исследование у китайских пациентов. Int J Clin Exp Med. (2015) 8: 9897–903.
PubMed Аннотация | Google Scholar
54. Галло В., Винейс П., Канчеллиери М., Чиодини П., Баркер Р.А., Брейн С. и др. Изучение причинно-следственной связи между курением и болезнью Паркинсона. Int J Epidemiol. (2019) 48: 912–25. DOI: 10.1093 / ije / dyy230
PubMed Аннотация | CrossRef Полный текст | Google Scholar
55.Ким И.Ю., О’Рейли ЭДЖ, Хьюз К.С., Гао Х, Шварцшильд М.А., Ханнан М.Т. и др. Интеграция факторов риска болезни Паркинсона в 2 больших продольных когортах. Невролог. (2018) 90: e1646–53. DOI: 10.1212 / WNL.0000000000005473
PubMed Аннотация | CrossRef Полный текст | Google Scholar
56. Breckenridge CB, Berry C, Chang ET, Sielken RL Jr, Mandel JS. Связь между болезнью Паркинсона и курением сигарет, сельской жизнью, потреблением колодезной воды, сельским хозяйством и использованием пестицидов: систематический обзор и метаанализ. PLoS ONE. (2016) 11: e0151841. DOI: 10.1371 / journal.pone.0151841
PubMed Аннотация | CrossRef Полный текст | Google Scholar
57. Мартино Р., Кандундо Х., Лисхаут П.В., Шин С., Криспо Дж., Баракат-Хаддад С. Факторы начала и прогрессирования болезни Паркинсона: систематический обзор. Нейротоксикология. (2017) 61: 132–41. DOI: 10.1016 / j.neuro.2016.04.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
В России распространяется повальное увлечение «терапией стволовыми клетками»
Когда Светлана Галиева нашла клинику, предлагающую лечить ее рассеянный склероз с помощью эмбриональных стволовых клеток, она ухватилась за эту возможность.Спустя двадцать тысяч долларов она все еще находится в инвалидном кресле и в отчаянии.
И нет никаких доказательств того, что ее инъекции имели какое-либо отношение к стволовым клеткам.
В то время как ученые всего мира изучают только стволовые клетки, десятки российских клиник и салонов красоты заявляют, что они уже используют как взрослые, так и эмбриональные стволовые клетки для лечения всего, от морщин до болезни Паркинсона и импотенции.
Ученые предупреждают, что, хотя стволовые клетки все еще исследуются в лабораториях, лечение в клиниках, заявляющих об использовании стволовых клеток, может стоить пациентам их здоровья и состояния.Более того, они говорят, что даже несмотря на то, что это незаконно, меры по обеспечению соблюдения неэффективны, и никто не знает, содержат ли пациенты инъекции стволовых клеток.
Стволовые клетки — это строительные блоки человеческого тела — незрелые клетки, которые могут расти в кости, мышцы и другие ткани. Их много у эмбриона и плода, и считается, что они более универсальны, чем стволовые клетки из костного мозга и жира взрослых. Но эмбриональные стволовые клетки вызывают споры, потому что они связаны с разрушением человеческих эмбрионов.
В ведущих клиниках мира большая часть исследований стволовых клеток ограничивается лабораторными чашками и животными.В России же другая история.
Галиева, 40-летняя гинеколог из Уральского города Перми, девять лет назад заболела рассеянным склерозом. Она постепенно теряла контроль над своими мышцами и испытывала почти постоянные мышечные спазмы, из-за чего врачи пессимистично оценивали ее способность восстанавливать силы.
«Я поняла, что меня ждет, либо смерть, либо …», — сказала Галиева по телефону из Перми.
«Бесполезные» процедуры
В отчаянии Галиева поехала в московскую клинику, чтобы сделать серию инъекций, которые, по словам ее врачей, были эмбриональными стволовыми клетками, которые обошлись ей примерно в 560 000 рублей (20 000 долларов) — огромная сумма для страны, где среднемесячная заработная плата составляет около 300 долларов.
Изначально ее организм почти отказался от лечения из-за лихорадки 40 C (104 F). Затем к ее конечностям вернулась некоторая чувствительность, но это длилось недолго.
«Продолжать это лечение было бесполезно, — с горечью сказала она.
На этом не все закончилось. Она говорит, что ее состояние улучшилось после новой серии инъекций, которые, как сообщается, содержат взрослые стволовые клетки, в Beauty Plaza, частной клинике в Москве, которая рекламирует лечение стволовыми клетками при различных заболеваниях. По ее словам, она все еще не может ходить, но может недолго стоять без посторонней помощи.
Тем временем сотни пациентов спешат в российские клиники и салоны красоты, которые заявляют, что предлагают терапию эмбриональными стволовыми клетками для лечения целого ряда заболеваний, а также косметическую терапию.
Клиника «Целлюлит» доктора Романа Князева в центре Москвы рекламирует инъекции стволовых клеток абортированного плода в бедра, ягодицы и живот, чтобы помочь женщинам избавиться от целлюлита и выглядеть моложе.
Елена, 37-летняя московская предпринимательница, говорит, что они работали на нее. «После родов мой живот свисал как тряпка, и у меня было много растяжек.Теперь все пропало », — сказала она, потратив 80 000 рублей (2850 долларов) на инъекции в клинике Князева. Она отказалась назвать свою фамилию.
Опасные побочные эффекты
Но эксперты говорят, что процедура имеет потенциально опасные побочные эффекты.
«Ни у кого не было лицензий на инъекции (стволовые клетки) — это только эксперименты. Все это делается на их страх и риск. Все это незаконно », — сказал Владимир Смирнов, директор Института экспериментальной кардиологии, который управляет банком взрослых стволовых клеток.
Он сказал, что знает о нескольких государственных исследовательских институтах, которые время от времени пытались экспериментально лечить с использованием взрослых стволовых клеток из костного мозга и жира. Однако многие другие клиники практически не регулируют то, что они рекламируют и вводят, — сказал Смирнов.
Ученые говорят, что культивирование и выделение стволовых клеток требует навыков и дорогостоящего оборудования, которого в клиниках нет. Следовательно, то, что считается стволовыми клетками, может быть чем угодно, от экстракта ткани плода до клеток кожи.Сообщается, что некоторые клиники используют стволовые клетки животных.
«Если бы я был пациентом, я бы не хотел, чтобы это делали со мной … риски потенциально очень высоки», — сказал Джошуа Хейр, директор отделения сердечно-сосудистой системы в Институте клеточной инженерии Джонса Хопкинса в Балтиморе.
Андрей Юрьев, заместитель руководителя Федеральной службы по надзору в сфере здравоохранения, сказал, что закон разрешает только извлечение и хранение стволовых клеток, но не их использование в лечении. Юрьев сказал, что его служба исследует около 20 косметических клиник, которые заявляют, что практикуют терапию стволовыми клетками.
Но при таком расплывчатом регламенте десятки клиник продолжают работать.
Доктор Александр Тепляшин, глава Beauty Plaza, говорит, что использовал взрослые стволовые клетки из жира и костного мозга пациентов или доноров для лечения диабета, нарушений зрения и других заболеваний. Он признает, что то, что он делает, технически запрещено.
«Мы пользуемся лазейками в законе … разрешено то, что не запрещено», — сказал он AP в своей клинике в центре Москвы.
Президент России Владимир Путин уйдет в отставку? Наблюдатели говорят, что у него серьезная болезнь
Вопреки предположениям о том, что президент России Владимир Путин будет править страной всю свою жизнь, у него могут быть планы уйти в отставку уже в январе следующего года из-за опасений, что у него может быть болезнь Паркинсона, говорится в отчете. . Как заявил кремлевский обозреватель и московский политолог профессор Валерий Соловей, 68-летний российский силач имеет симптомы болезни Паркинсона, сообщает The US Sun.
Проблема может быть серьезной, поскольку его давняя подруга Алина Каваева, 37 лет, как сообщается, умоляет его потерять контроль над властью и сосредоточиться на своем здоровье. Известно, что его дочери Мария Воронцова, 35 лет, и Катерина Тихонова, 34 года, также убедили президента России повесить ботинки. «Есть семья, она имеет на него большое влияние. Он намерен обнародовать свои планы передачи власти в январе», — сказал Соловей газете США.
Читайте также: Россия запускает первую вакцину от коронавируса; Дочь Владимира Путина получила прививку
Наблюдатели, проанализировавшие его недавние кадры, считают, что ему, казалось, было больно, когда он держался за подлокотник стула.Его ноги также, казалось, были в постоянном движении. Другие признаки, такие как подергивание пальцев, когда он держит ручку или чашку, указывают на то, что у него может быть какое-то осложнение со здоровьем.
Россия, очевидно, разрабатывает правила, которые сделают его пожизненным сенатором после того, как он уйдет в отставку с самого высокого поста в стране. Это также породило широко распространенные предположения о том, что 20-летнему правлению Путина — второго после Иосифа Сталина — близится конец.

 interfax.ru), 18/03/2019
interfax.ru), 18/03/2019 ru/ekaterinburg, 18/03/2019
ru/ekaterinburg, 18/03/2019