Ишемический инсульт что это такое последствия: Ишемический инсульт: прогнозы, последствия и реабилитация
что это такое? / Рекомендации / Семейная клиника «Танар»
ОНМК: что это такое?
ОНМК по ишемическому типу.
Многие задают вопрос о том, что такое ОНМК и какие последствия после него бывают. В этой статье будут разобраны основные причины проявления ОНМК и последствия
ОНМК — что это такое.
Многие люди, которые не имеют никакого отношение к медицине, наверняка не знают, что такое ОНМК. Итак, острое нарушение кровообращения в головном мозге – это инсульт, который становится причиной повреждения и отмирания клеток головного мозга. Причиной возникновения данного заболевания является образование тромба в кровеносных сосудах головного мозга или же разрыв некоторых кровеносных сосудов, что становится причиной отмирания огромного количества нервных клеток и клеток крови. По статистике, именно ОНМК стоит на первом месте среди болезней, которые становятся причиной смерти человека. Ежегодно во всем мире, как указывает федеральный регистр больных ОНМК, от этого заболевания умирает 14 процентов людей, а также 16 от других видов заболеваний кровеносной системы.
Причины, по которым может проявиться ОНМК.
Для того чтобы предотвратить появление этого заболевания, необходимо с раннего возраста обратить внимание на свой образ жизни. Например, постоянное занятие спортом позволяет существенно снизить возможность проявления ОНМК. Что это такое, вы уже знаете, дальше будут рассмотрены некоторые причины возникновения этого недуга.
Как правило, эта болезнь не приходит внезапно, очень часто диагноз «ОНМК» может быть установлен как последствие некоторых заболеваний.
Часто причиной этого состояния могут стать:
- гипертония;
- ожирение;
- диабет;
- высокий уровень холестерина;
- заболевания сердца;
- алкоголь и курение;
- различного рода медикаменты;
- высокий уровень гемоглобина;
- возраст;
- черепно-мозговая травма;
- генетическая предрасположенность и так далее.

Теперь понятно, что такое ОНМК. Это последствия неправильного образа жизни. Поэтому очень важно следить за своим здоровьем и физическим состоянием
Ишемический ОНМК.
Ишемический ОНМК – это инсульт, вызванный повреждением тканей головного мозга и нарушением поступления крови к тому или иному его отделу.
У большинства больных ОНМК по ишемическому типу обнаруживаются общие болезни сердечно-сосудистой системы. К таким болезням также можно отнести артериосклероз, заболевание сердца (аритмию, ревматический порок), сахарный диабет. Для ОНМК данного типа характерны резкие и частые проявления болевых ощущений, последствием которых является ухудшение кровообращения в коре головного мозга. Как правило, такие приступы могут давать знать о себе несколько раз в час и длиться на протяжении 24 часов.
Причины ишемического инсульта ОНМК.
Главной причиной проявления ОНМК по ишемическому типу является снижение притока крови к головному мозгу. Очень часто именно поэтому причиной смерти человека становится ишемический инсульт. Итак, мы выяснили особенности ишемического ОНМК, что это такое и каковы его симптомы.
Очень часто именно поэтому причиной смерти человека становится ишемический инсульт. Итак, мы выяснили особенности ишемического ОНМК, что это такое и каковы его симптомы.
Это, как правило, результат повреждения сосудов шеи и некоторых артерий головного мозга в виде окклюзионных поражений и стеноза. Давайте выясним основные причины его возникновения.
К основным факторам, которые могут повлиять на снижение кровотока, можно отнести следующие:
- Окклюзии и стенозы основных артерий головного мозга и сосудов шеи.
- Тромботические наслоения на поверхности атеросклеротической бляшки.
- Кардиогенная эмболия, которая происходит в случае наличия искусственных клапанов в сердце человека.
- Расслоение магистральных артерий шейного отдела.
- Гиалиноз мелких артерий, вследствие чего развивается микроангиопатия, что приводит к формированию лакунарного инфаркта головного мозга человека.
- Гемореологические изменения состава крови, что происходит при васкулитах, а также коагулопатиях.

Очень редко причиной проявления этого заболевания могут стать внешние травмы сонных артерий и различные воспалительные процессы, которые способны существенно ухудшить проходимость крови по сосудам. Также очень часто основной причиной ОНМК головного мозга может стать остеохондроз шейного отдела позвоночника, в процессе чего существенно защемляются кровеносные сосуды, которые могут привести к уменьшению потока крови. Больным остеохондрозом постоянно рекомендуется делать массаж шейного отдела позвоночника и мазать его различными согревающими препаратами, которые способны существенно расширить сосуды и улучшить циркуляцию крови.
Симптомы ОНМК.
Признаки этого заболевания очень часто могут проявляться резко или же нарастать постепенно. Как правило, к основным симптомам этой болезни можно отнести расстройство речи и зрения у больного, нарушения различных рефлексов, координации движения, головные боли, дезориентации, нарушение сна, шум в голове, нарушение памяти, паралич лица, языка, отсутствие ощущения некоторых конечностей и так далее.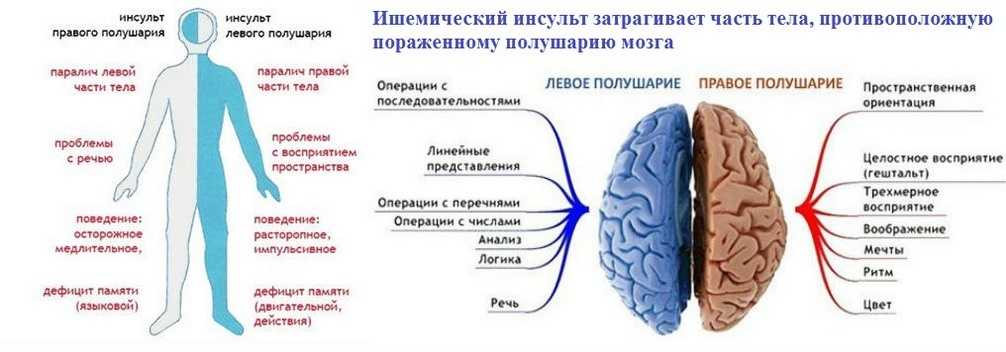
При остром нарушении мозгового кровообращения характерно возникновение следующих последствий — инсульт головного мозга, нарушение кровообращения в коре мозга при образовании тромбов в сосудах и главных кровеносных артериях головы и т. д.
При симптомах острого нарушения мозгового кровообращения, которые длятся более чем сутки, диагностируется инсульт. При первой стадии этого заболевания может проявляться также сильная головная боль, головокружение, тошнота, рвотные рефлексы и так далее. Если не обратить сразу внимание на эти проявления, это может стать причиной смерти человека.
Как утверждает регистр больных с ОНМК, по статистике, основной причиной этих проявлений может стать высокое давление, которое может наблюдаться при сильных физических нагрузках. Резкое повышение артериального давления может стать причиной разрыва сосудов головного мозга, после чего произойдет кровоизлияние и внутримозговая гематома.
В большинстве случаев перед ишемией наблюдаются вышеперечисленные симптомы.
Диагностика острого нарушения мозгового кровообращения по ишемическому типу.
Для выявления проблемы необходимо проводить диагностику и различные исследования по системе МКБ. ОНМК врачи смогут диагностировать после проведения следующих процедур:
- Анализ крови на электролиты, глюкозу, гемостазы, липидный спектр, антифосфолипидные антитела.
- Электрокардиография изменений артериального давления.
- Компьютерная томография коры головного мозга, вследствие чего можно будет без каких-либо проблем обнаружить пораженные части головного мозга и образовавшиеся гематомы.

- Церебральная ангиография и так далее.
Лечение острого нарушения мозгового кровообращения при ишемическом типе.
Самой частой причиной смерти становится именно ОНМК. Лечение поэтому должно происходить под наблюдением опытных врачей. При данном заболевании проводится следующая терапия:
- Поддержание жизненно важных функций организма человека. Больной должен употреблять антигипертензивные средства, в том случае, когда давление крови в организме составляет 200 на 120 мм. рт. ст. Также назначается употребление антикоагулянтов (применяются при сопутствующих патологиях и употребляются на протяжении длительного времени после нормализации состояния), вазоактивных препаратов, антиагрегантов, противоотечных средств, нейропротекторов и так далее.
- Производятся различные комплексы упражнений – логопедические занятия и дыхательная гимнастика.
- Рассматривается вопрос о тромболизисе при поступлении больного в медучреждение в период 3-6 часов с момента проявления болезни.

- Вторичная профилактика заболевания.
- Проводятся различные реабилитационные мероприятия и так далее.
Как правило, основные моменты лечения будут назначены только врачом, который более подробно ознакомится с болезнью пострадавшего.
В том случае, если имеются подозрения на острое нарушение мозгового кровообращения, необходимо обратиться к высококвалифицированным специалистам в данной области деятельности. Как правило, в первую очередь необходимо будет пройти магнитно-резонансную томографию, которая с точностью сможет определить все патологии коры головного мозга. Таким образом удастся предотвратить возможность осложнения заболевания и начать лечение еще до того, как оно полностью проявится. Специализированное отделение ОНМК, как правило, должно иметь специальное оборудование, которое позволит существенно улучшить лечение.
Первая помощь при ОНМК.
Самое первое, что необходимо сделать при обнаружении симптомов этой болезни, — это вызвать бригаду скорой помощи. Больного во время проявления симптомов этого заболевания ни в коем случае нельзя беспокоить без причины, поэтому сразу же после первых признаков необходимо изолировать его.
Больного во время проявления симптомов этого заболевания ни в коем случае нельзя беспокоить без причины, поэтому сразу же после первых признаков необходимо изолировать его.
На следующем этапе все больные с ОНМК должны лежать таким образом, чтобы верхняя часть туловища и голова были приподняты, также необходимо растереть воротниковую зону тела, для того чтобы облегчить дыхание больному. Также необходимо обеспечить в помещение, где находится больной, доступ свежего воздуха (открыть форточку, двери и так далее).
В том случае, если у больного возникают рвотные спазмы, необходимо его голову повернуть на левую сторону и прочистить полость рта марлей или же просто чистой салфеткой. Это делается для того, чтобы предотвратить возможность попадания рвотных выделений в легкие при дыхании, что может привести к образованию дополнительных проблем.
Одним из наиболее частых симптомом ОНМК является эпилептический припадок – человек полностью теряет сознание, по истечении нескольких секунд по телу проносится волна судорог, которые могут продолжаться несколько минут. Также стоит отметить, что такие приступы могут повторяться несколько раз.
Также стоит отметить, что такие приступы могут повторяться несколько раз.
Как предотвратить возникновение заболеваний ОНМК.
Исходя из вышеприведенной статистики, видно, что данное заболевание проявляется даже у детей. Несложно догадаться, что с каждым годом людей, которые страдают этой болезнью, становится все больше и больше. Все это связано с неправильным питанием, неактивным образом жизни и с высокими умственными нагрузками.
Если человек не ведет активный образ жизни и постоянно проводит время за компьютером, у него велики шансы заболеть этой болезнью. Ожирение, как говорилось, — основная причина данного заболевания, именно поэтому вопрос поддержания физической формы сегодня очень актуален для молодого поколения.
Резкие нагрузки также очень часто становятся источником проблемы, так как с ростом артериального давления существует риск разрыва кровеносных артерий и вен, что также приведет к ОНМК. Поэтому необходимо постоянно заниматься спортом, вести активный образ жизни, правильно питаться — и риск возникновения ОНМК существенно уменьшится.
Самым смертоносным и страшным заболеванием в наше время является именно ОНМК. Что это такое и из-за чего возникает данное заболевание, вы уже знаете, поэтому необходимо придерживаться вышеперечисленных рекомендаций, для того чтобы предотвратить болезнь в будущем.-
Транзиторная ишемическая атака и инсульт
Инсульт может развиваться остро или иметь «предвестники» — те же самые повторяющиеся ТИА, резкие перепады артериального давления. Клиническая картина инсульта очень похожа на транзиторную ишемическую атаку; по сути, это более тяжелый вариант дисфункции кровотока, когда проходимость сосуда не только не восстанавливается, но и прекращается так надолго, что клетки участка мозга погибают из-за гипоксии (кислородного голодания).Клиническая картина инсульта складывается из двух синдромов:
1. Общемозговой:
- сильная головная боль
- головокружение, неустойчивость при ходьбе
- тошнота, рвота
- иногда — судороги, обморок
- сонливость или, наоборот, возбуждение
чувство оглушенности - боль в глазных яблоках при их движении
- ощущение «волны жара», сухости во рту
- избыточная потливость
 Очаговый неврологический (зависит от того, какие анатомо-функциональные зоны головного мозга затронуты):
Очаговый неврологический (зависит от того, какие анатомо-функциональные зоны головного мозга затронуты):- нарушения подвижности разных областей тела (лицо, руки, ноги с одной или двух сторон)
- расстройства чувствительности
- расстройства речи, зрения, слуха, в особенно тяжелых случаях — также дыхания, сердечного ритма
- нарушение памяти, восприятия информации
- расстройства психической сферы (эмоциональная расторможенность, галлюцинации)
- нарушения сознания вплоть до комы
Что опаснее: ТИА или инсульт?
После прочтения предыдущих разделов статьи ответ на этот вопрос должен быть очевиден. Инсульт является тяжелым необратимым нарушением, тогда как ТИА может завершиться самостоятельно без явных последствий. Но это не повод относиться к ней пренебрежительно.
Еще несколько десятилетий назад этим «грешили» даже врачи — но сегодня отношение к ТИА совершенно иное. Почему? Есть несколько причин:
- Пациенты, которые часто переносят ишемические атаки, имеют высокий риск развития тяжелого (!!!) ишемического инсульта
- Зная, что симптомы пройдут, пациенты не обращаются к врачу — а их состояние тем временем усугубляется, ведь заболевания, ставшие причиной атаки, прогрессируют
- ТИА требует грамотного лечения (в стационаре, затем амбулаторно) и постоянного контроля уровня артериального давления
Поэтому, хотя прогноз при инсульте для пациента, безусловно, хуже, любые варианты ТИА являются поводом для немедленного обращения к врачу и неотложной госпитализации в стационар. Больные с транзиторными ишемическими атаками должны знать, чем угрожает это состояние, и совместно с врачом предпринимать необходимые меры для профилактики развития инсульта.
Инсульт: ишемический и геморрагический — что это, в чем разница
. .. На дворе стоял теплый осенний день. Они сидели в парке и разговаривали. Один из собеседников, пожилой человек, лет 70-75 на вид, периодически улыбался — по-видимому тому, о чем говорила его собеседница. Лица обоих были спокойны и безмятежны. Я сидел немного поодаль и невольно наблюдал за беседой этих двух людей, периодически смотря на играющих здесь же детей, голубей и просто наслаждаясь окружающей меня картиной.
.. На дворе стоял теплый осенний день. Они сидели в парке и разговаривали. Один из собеседников, пожилой человек, лет 70-75 на вид, периодически улыбался — по-видимому тому, о чем говорила его собеседница. Лица обоих были спокойны и безмятежны. Я сидел немного поодаль и невольно наблюдал за беседой этих двух людей, периодически смотря на играющих здесь же детей, голубей и просто наслаждаясь окружающей меня картиной.
В следующий момент я услышал встревоженный голос женщины. «Что с тобой? Я тебя не понимаю… Что ты сказал?»
Мой взгляд перешел на пожилого человека. Лицо его было изменено, один из уголков рта был перекошен, а сам он, вероятно пытаясь успокоить свою спутницу, пытался поднять руку и что-то сказать, но рука его не слушалась, а слова были бессвязными.
Вы когда-нибудь сталкивались с тем, о чем прочли выше? При любом ответе статья ниже будет полезной: возможно, когда-нибудь именно вы сможете спасти чью-то жизнь.
Инсульт: что это такое
В основе данного заболевания лежит сосудистое нарушение, говоря без преувеличения «сосудистая катастрофа», последствием которой является повреждение ткани головного мозга. Ряд возникающих при этом нарушений проявляется в виде клинических признаков.
Ряд возникающих при этом нарушений проявляется в виде клинических признаков.
Первые признаки инсульта
Они могут быть разнообразными. Всё зависит от того, какой отдел (или отделы) головного мозга вовлечен(ы) в патологический процесс и, что не менее важно, в какой степени. Некоторые признаки заболевания: онемение разных частей тела (например руки, ноги, носо-губного треугольника), нарушения движения в виде невозможности поднять руку или ногу или удерживать их в поднятом положении, перекосы лица, рта, невнятная речь или полное ее отсутствие.
Существует небольшой алгоритм, пользуясь которым вы сравнительно достоверно и обоснованно можете заподозрить наличие у человека инсульта.
1. Попросите человека улыбнуться. При наличии инсульта улыбка получится несимметричной, будет отмечаться перекос лица.
2. Попросите человека что-нибудь сказать. Речь его может быть трудно разборчивой.
3. Попросите человека высунуть язык — при инсульте он может быть перекошен в ту или иную сторону.
4. Попросите поднять руки и удерживать их поднятыми. Одна из рук при инсульте опускается, больной не может ее удержать.
Геморрагический и ишемический инсульт: сравнение
Говоря об инсульте, одним из принципиальных моментов его классификационной характеристики является деление на так называемый геморрагический и ишемический варианты. Данная классификация не есть простая медицинская прихоть: во многом выяснение варианта инсульта определяет дальнейшую лечебную тактику у пациента.
Геморрагический инсульт, его суть и признаки
В основе геморрагического инсульта лежит разрыв кровеносного сосуда, как правило артерии, в головном мозге, с последующим кровоизлиянием. Одной из наиболее частых причин, приводящих к разрыву сосуда, является гипертоническая болезнь, вызывающая патологические изменения сосудов.
Признаками геморрагического инсульта являются вероятное наличие у человека гипертонической болезни, внезапное начало и быстрое ухудшение состояния.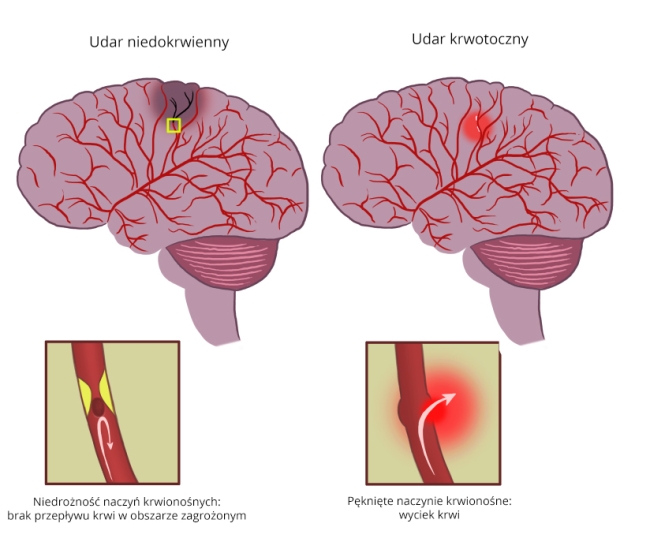 При внешнем осмотре может отмечаться более или менее длительная потеря сознания, лицо часто багрово-красное (в особенно тяжелых случаях бледное), могут наблюдаться головная боль, судороги, тошнота и рвота, нарушения движений в различных частях тела.
При внешнем осмотре может отмечаться более или менее длительная потеря сознания, лицо часто багрово-красное (в особенно тяжелых случаях бледное), могут наблюдаться головная боль, судороги, тошнота и рвота, нарушения движений в различных частях тела.
Ишемический инсульт, его суть и признаки
В основе ишемического инсульта лежит закупорка артерии головного мозга и, как следствие, резкое уменьшение или полное прекращение кровоснабжения соответствующего пораженной артерии отдела мозга. Одной из наиболее частых причин возникновения непроходимости артерии является атеросклероз.
Признаками этого варианта заболевания являются возможное наличие у человека ишемической болезни сердца (ИБС), перенесенный в прошлом инфаркт миокарда, менее яркое, чем при геморрагическом варианте инсульта, развитие процесса. Сознание часто сохранено, артериальное давление в момент начала заболевания может быть нормальным либо пониженным. Отмечаются очаговые признаки поражения нервной системы в виде онемения и нарушения движений в различных частях тела, лица, нарушения равновесия и координации движения, слуха и зрения.
Следует помнить, что клинические признаки должны обязательно подтверждаться различными лабораторно-инструментальными методами диагностики (например, магнитно-резонансной или компьютерной томографией, ультразвуковым исследованием сосудов головы, рентгенконтрастной ангиографией), посредством которых уточняется вариант инсульта, его расположение и ряд других показателей.
Последствия инсульта и прогноз
Последствия и прогноз зависят от целого ряда факторов, в частности от разновидности инсульта, обширности зоны поражения в головном мозге, длительности существования сосудистых нарушений, своевременности, объема и качества оказанной специализированной медицинской помощи. Последствия данной патологии у пожилых зависят, помимо перечисленных выше факторов, от сопутствующих заболеваний, относительно часто встречающихся у людей в данной возрастной категории.
Что делать при первых симптомах инсульта?
1. Без промедления вызвать «скорую». Этот момент имеет принципиально важное значение: по различным данным оказание помощи при ишемическом инсульте в промежутке от 3 до 4,5 часов достоверно и значительно увеличивает шансы на ликвидацию непроходимости сосуда и является мерой, способной предотвратить развитие необратимого повреждения нервной ткани.
Этот момент имеет принципиально важное значение: по различным данным оказание помощи при ишемическом инсульте в промежутке от 3 до 4,5 часов достоверно и значительно увеличивает шансы на ликвидацию непроходимости сосуда и является мерой, способной предотвратить развитие необратимого повреждения нервной ткани.
2. Открыть окно или форточку для обеспечения доступа в комнату свежего воздуха.
3. При отсутствии сознания у человека переложить его на кровать, голову повернуть вбок, проверить, не запал ли язык, ослабить ворот рубашки.
4. Если человек в сознании, постараться успокоить его, придать ему лежачее или полулежачее положение.
Специальность врача, занимающегося лечением больных с инсультом головного мозга
Лечением данной категории больных занимаются неврологи, привлекая, при необходимости, нейрохирургов.
Реабилитация после инсульта
Реабилитационные мероприятия при инсульте многогранны и направлены на смягчение или полную ликвидацию его последствий.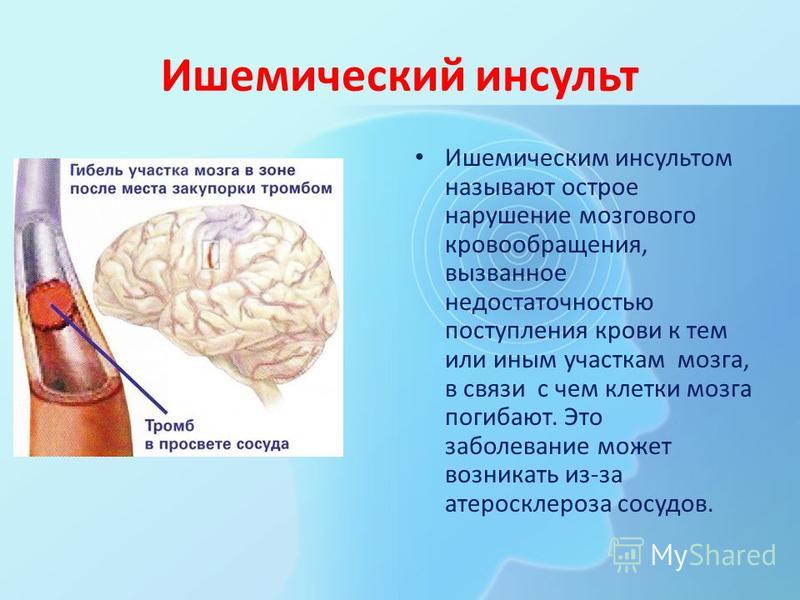
Программа зависит от того, какие функции головного мозга были нарушены, и направлена на восстановление чувствительности, движений в пораженных частях тела, речи, высших психических функций. Поскольку при инсульте нарушения затрагивают разные функциональные сферы, с пациентом работают специалисты из нескольких областей медицины: неврологи, реабилитологи, физиотерапевты, логопеды, психологи и психиатры, работники социальной службы.
Успешность реабилитационных мероприятий зависит от обширности пораженной области головного мозга, а также от заинтересованности и упорства больного и его окружения в деле преодоления возникших нарушений. Благодаря развиваемой в последние десятилетия теории пластичности головного мозга, т.е. его способности восстанавливаться после повреждений, некоторые постинсультные последствия могут в значительной степени ослабевать или полностью исчезать при использовании квалифицированных и целенаправленных реабилитационных мероприятий.
Причины и последствия тромботического инсульта
Тромботический инсульт — это тип ишемического инсульта, который возникает, когда сгусток крови, также называемый тромбом, образует и блокирует кровоток через артерию, в которой он образовался. Сгусток крови может блокировать поток богатой кислородом крови к часть мозга, вызывающая долговременное повреждение мозга. Это повреждение головного мозга, вызванное недостаточным кровоснабжением, вызывает инсульт.
Сгусток крови может блокировать поток богатой кислородом крови к часть мозга, вызывающая долговременное повреждение мозга. Это повреждение головного мозга, вызванное недостаточным кровоснабжением, вызывает инсульт.
Типы тромботического инсульта
Тромботический инсульт также может называться церебральным тромбозом, инфарктом головного мозга или инфарктом головного мозга.
Тромботические инсульты делятся на две категории в зависимости от размера области закупорки в головном мозге: тромбоз крупных сосудов и тромбоз мелких сосудов.
Инсульт большого сосуда происходит в более крупных кровоснабжающих артериях головного мозга, таких как сонная артерия или средняя мозговая артерия. Тромботические инсульты крупных сосудов обычно вызывают серьезные симптомы и долгосрочные последствия, такие как афазия (проблемы с языком) или гемипарез (слабость одной стороны тела.)
Инсульт по мелкому сосуду происходит, когда кровоток блокируется в маленьком и глубоко проникающем артериальном кровеносном сосуде. Этот тип инсульта также известен как лакунарный или подкорковый инсульт. Тромб из мелких сосудов также может привести к инсульту ствола мозга. Инсульты мелких сосудов буквально малы по размеру и затрагивают только ограниченную область мозга. В зависимости от области, пораженной небольшим тромботическим инсультом, он может вызывать незначительные эффекты или вызывать значительные затруднения, если он воздействует на область мозга, которая отвечает за важные и заметные физические или когнитивные способности.
Этот тип инсульта также известен как лакунарный или подкорковый инсульт. Тромб из мелких сосудов также может привести к инсульту ствола мозга. Инсульты мелких сосудов буквально малы по размеру и затрагивают только ограниченную область мозга. В зависимости от области, пораженной небольшим тромботическим инсультом, он может вызывать незначительные эффекты или вызывать значительные затруднения, если он воздействует на область мозга, которая отвечает за важные и заметные физические или когнитивные способности.
Симптомы и последствия
Тромботический инсульт может возникнуть в любой области мозга, а непосредственные симптомы и долгосрочные последствия тромботического инсульта коррелируют с областью мозга, на которую влияет недостаток кровоснабжения.
Симптомы тромботического инсульта могут включать любую комбинацию из следующих:
- Проблемы с пониманием слов или затруднения при разговоре
- Внезапное замешательство
- Потеря сознания
- Слабость лица, руки или ноги с одной стороны тела
- Онемение лица, руки или ноги с одной стороны тела
- Нечеткое зрение в одном или обоих глазах
- Двойное зрение
- Внезапная сильная головная боль
- Головокружение
- Затруднения при ходьбе
- Потеря равновесия или координации
Причины и факторы риска
Есть несколько причин тромботического инсульта.
- Атеросклероз или сужение кровеносных сосудов: Тромботический инсульт чаще всего вызывается сужением артерий головы или шеи. Чаще всего из-за атеросклероза артерии становятся больными и нерегулярными. Это происходит в результате высокого кровяного давления, диабета и накопления холестерина, жира и мусора в участках кровеносных сосудов. Со временем этот материал может стать «липким», заставляя клетки крови собираться и образовывать сгусток крови.Атеросклероз и сужение кровеносных сосудов в головном мозге часто называют цереброваскулярным заболеванием.
- Высокое кровяное давление: Постоянно высокое кровяное давление, также называемое гипертонией, может вызвать заболевание и сужение кровеносных сосудов, предрасполагая к тромботическим инсультам. Гипертония и атеросклероз — это состояния, которые часто возникают вместе, что приводит к еще большему повреждению кровеносных сосудов.
- Высокий уровень холестерина: Высокий уровень холестерина в организме может привести к отложению холестерина и жира в кровеносных сосудах, что увеличивает риск тромботического инсульта.

- Диабет: Диабет — хорошо известный фактор риска тромботического инсульта. Это может вызвать сужение крупных и мелких кровеносных сосудов, что приведет к образованию тромба и последующему инсульту.
- Нарушения свертывания крови: При некоторых нарушениях свертывания крови повышается вероятность образования чрезмерных сгустков крови, что увеличивает вероятность тромботического инсульта.
- Курение: Курение является одним из основных факторов риска инсульта и сердечных заболеваний, поскольку оно вызывает повреждение кровеносных сосудов по всему телу.
- Рекреационные наркотики: Определенные наркотики, такие как кокаин, метамфетамин и вещества, повышающие работоспособность, могут способствовать замедлению развития цереброваскулярных заболеваний. Эти препараты могут также вызвать внезапное сужение и / или «спазм» кровеносных сосудов, внезапно перекрывая приток крови к определенной области мозга на короткий период времени.

- Травма кровеносных сосудов шеи: Хотя это не является обычным явлением, есть случаи, когда тяжелая травма может вызвать образование тромба, что приводит к инсульту.
- Транзиторная ишемическая атака: Тромботическому инсульту может предшествовать серия из одной или нескольких преходящих ишемических атак, также известных как «мини-инсульты» или ТИА. ТИА может длиться несколько минут или часов и часто бывает признак надвигающегося инсульта. Симптомы ТИА аналогичны симптомам инсульта.
Факторы риска инсульта у женщин
Рекомендации по профилактике инсульта, опубликованные совместно Американской кардиологической ассоциацией и Американской ассоциацией инсультов, отмечают, что определенные факторы риска, включая диабет, гипертензию, мигрень с аурой и фибрилляцию предсердий, сильнее или более распространены у женщин, чем у мужчин.
Слово от Verywell
Тромботический инсульт — одна из самых частых причин инсульта. Существует ряд методов лечения тромботического инсульта, в том числе антикоагулянты, такие как TPA, и процедуры, которые могут помочь растворить и удалить сгусток крови. Если вы или ваш любимый человек пережили тромботический инсульт, вам может потребоваться участие в программе реабилитации после инсульта, которая может помочь в вашем выздоровлении.
Существует ряд методов лечения тромботического инсульта, в том числе антикоагулянты, такие как TPA, и процедуры, которые могут помочь растворить и удалить сгусток крови. Если вы или ваш любимый человек пережили тромботический инсульт, вам может потребоваться участие в программе реабилитации после инсульта, которая может помочь в вашем выздоровлении.
Влияние ишемического инсульта на градиенты связности
Основные моменты
- •
Воздействие инсульта следует за непрерывной архитектурой градиентов связности.
- •
Широко распространенные эффекты инсульта можно обнаружить на уровне коннектома.
- •
Расстояние от очага поражения в пространстве подключения позволяет фиксировать изменения во время восстановления.
- •
Градиенты подключения предлагают шаблон для отражения реорганизации на уровне коннектома.
Abstract
Функциональную организацию мозга можно представить как низкоразмерное пространство, которое отражает его иерархию на макроуровне. Размеры этого пространства, описываемые как градиенты связности, отражают сходство связей областей вдоль непрерывного пространства. Изучение того, как патологические возмущения с известным воздействием на функциональную связность влияют на эти градиенты связности, подтверждает их биологическое значение. Предыдущая работа показала, что локализованные поражения вызывают широко распространенные функциональные изменения связности в структурно неповрежденных областях, влияя на сеть взаимосвязанных областей. Используя острый инсульт в качестве модели воздействия очаговых поражений на коннектом, мы применяем структуру градиента связности, чтобы изобразить, как функциональная реорганизация происходит во всем мозге, не ограничиваясь традиционными определениями функциональных границ сети.Мы определяем трехмерный шаблон пространства подключения на основе данных о функциональном подключении из исправных элементов управления. Путем проецирования участков поражения в это пространство мы демонстрируем, что ишемические инсульты приводят к определенным по размерам изменениям функциональной связности в течение первой недели после появления симптомов.
Размеры этого пространства, описываемые как градиенты связности, отражают сходство связей областей вдоль непрерывного пространства. Изучение того, как патологические возмущения с известным воздействием на функциональную связность влияют на эти градиенты связности, подтверждает их биологическое значение. Предыдущая работа показала, что локализованные поражения вызывают широко распространенные функциональные изменения связности в структурно неповрежденных областях, влияя на сеть взаимосвязанных областей. Используя острый инсульт в качестве модели воздействия очаговых поражений на коннектом, мы применяем структуру градиента связности, чтобы изобразить, как функциональная реорганизация происходит во всем мозге, не ограничиваясь традиционными определениями функциональных границ сети.Мы определяем трехмерный шаблон пространства подключения на основе данных о функциональном подключении из исправных элементов управления. Путем проецирования участков поражения в это пространство мы демонстрируем, что ишемические инсульты приводят к определенным по размерам изменениям функциональной связности в течение первой недели после появления симптомов. В частности, изменения функциональной связности были зафиксированы по градиентам связности 1 и 3. Степень изменения функциональной связности была связана с расстоянием от поражения по этим градиентам связности (мера функционального сходства) независимо от анатомического расстояния от поражения.Вместе эти результаты подтверждают биологическую достоверность градиентов связности и предлагают новую основу для характеристики изменений связности после инсульта.
В частности, изменения функциональной связности были зафиксированы по градиентам связности 1 и 3. Степень изменения функциональной связности была связана с расстоянием от поражения по этим градиентам связности (мера функционального сходства) независимо от анатомического расстояния от поражения.Вместе эти результаты подтверждают биологическую достоверность градиентов связности и предлагают новую основу для характеристики изменений связности после инсульта.
Ключевые слова
Градиенты связности
Внутренние функциональные возможности связности
Диашизис
ФМРТ в состоянии покоя
Коннектом
Диффузионное встраивание
Рекомендуемые статьи Цитирующие статьи (0)
Обзор авторов. Опубликовано Elsevier Inc.
Рекомендуемые статьи
Цитирующие статьи
Тромбовоспаление при остром ишемическом инсульте — значение для лечения
Global Burden of Disease Study 2013 Соавторы. Глобальная, региональная и национальная заболеваемость, распространенность и годы, прожитые с инвалидностью для 301 острого и хронического заболевания и травмы в 188 странах, 1990–2013 гг . : систематический анализ для Глобального исследования бремени болезней, 2013 г. Lancet 386 , 22–28 (2015).
: систематический анализ для Глобального исследования бремени болезней, 2013 г. Lancet 386 , 22–28 (2015).
Google Scholar
Коломинский-Рабас, П.Л., Вебер, М., Гефеллер, О., Нойндёрфер, Б., Хойшманн, П.У. Эпидемиология подтипов ишемического инсульта по критериям TOAST: частота, рецидивы и длительная выживаемость в Подтипы ишемического инсульта: популяционное исследование. Инсульт 32 , 2735–2740 (2001).
CAS PubMed Google Scholar
Hart, R.G. et al. Эмболические инсульты неустановленного источника: случай новой клинической конструкции. Lancet Neurol. 13 , 429–438 (2014).
PubMed Google Scholar
Лип, Г. Ю. и Лейн, Д. А. Профилактика инсульта при фибрилляции предсердий: систематический обзор. JAMA 313 , 1950–1962 (2015).
PubMed Google Scholar
Stoll, G. & Bendszus, M. Воспаление и атеросклероз: новое понимание образования и дестабилизации бляшек. Инсульт 37 , 1923–1932 (2006).
CAS PubMed Google Scholar
Bhatia, R. et al. Низкие показатели острой реканализации с внутривенным введением рекомбинантного тканевого активатора плазминогена при ишемическом инсульте: реальный опыт и призыв к действию. Инсульт 41 , 2254–2258 (2010).
CAS PubMed Google Scholar
Ноур М., Скальцо Ф. и Либескинд Д. С. Ишемия-реперфузионное повреждение при инсульте. Интерв. Neurol. 1 , 185–199 (2013).
PubMed PubMed Central Google Scholar
Мизума, А., Ю, Дж. С. и Йенари, М. А. Целенаправленное реперфузионное повреждение в эпоху механической тромбэктомии. Инсульт 49 , 1796–1802 (2018). В этой статье представлен актуальный обзор последствий восстановления мозгового кровотока с помощью механической тромбэктомии и новых мишеней для дополнительного лечения .
PubMed PubMed Central Google Scholar
Stoll, G., Jander, S. & Schroeter, M. Воспаление и глиальные реакции при ишемических поражениях головного мозга. Прог. Neurobiol. 56 , 149–171 (1998).
CAS PubMed Google Scholar
Schroeter, M., Jander, S., Witte, O. W. & Stoll, G. Местные иммунные ответы в коре головного мозга крыс после окклюзии средней мозговой артерии. J. Neuroimmunol. 55 , 195–203 (1994).
CAS PubMed Google Scholar
Gelderblom, M. et al. Временная и пространственная динамика накопления церебральных иммунных клеток при инсульте. Инсульт 40 , 1849–1857 (2009).
PubMed Google Scholar
Zrzavy, T. et al. Доминирующая роль врожденных иммунных ответов микроглии и макрофагов при ишемических инфарктах человека. Brain Pathol. 28 , 791–805 (2018).
CAS PubMed Google Scholar
del Zoppo, G. et al. Воспаление и инсульт: предполагаемая роль цитокинов, молекул адгезии и iNOS в ответе мозга на ишемию. Brain Pathol. 10 , 95–112 (2000).
PubMed Google Scholar
Столл Г., Джандер С. и Шретер М. Цитокины при расстройствах ЦНС: нейротоксичность по сравнению с нейропротекцией. J. Neural Transm. Дополнение 59 , 81–89 (2000).
CAS PubMed Google Scholar
Chamorro, A. et al. Иммунология острого инсульта. Nat. Rev. Neurol. 8 , 401–410 (2012).
CAS PubMed Google Scholar
Фу, Ю., Лю, К., Анратер, Дж. И Ши, Ф. Д. Иммунные вмешательства при инсульте. Nat. Rev. Neurol. 11 , 524–535 (2015).
CAS PubMed PubMed Central Google Scholar
Strecker, J. K., Schmidt, A., Schabitz, W.Р. и Миннеруп, Дж. Нейтрофильные гранулоциты при церебральной ишемии — эволюция от убийц к ключевым игрокам. Neurochem. Int. 107 , 117–126 (2017).
CAS PubMed Google Scholar
Национальный институт неврологических расстройств и инсульта Группа исследования инсульта rt-PA. Активатор тканевого плазминогена при остром ишемическом инсульте. N. Engl. J. Med. 333 , 1581–1587 (1995).
Google Scholar
Катанезе, Л., Тарсия, Дж. И Фишер, М. Обзор терапии острого ишемического инсульта. Circ. Res. 120 , 541–558 (2017).
CAS PubMed Google Scholar
Thomalla, G. et al. Тромболизис под контролем МРТ при инсульте с неизвестным временем начала. N. Engl. J. Med. 379 , 611–622 (2018).
PubMed Google Scholar
Goyal, M. et al. Эндоваскулярная тромбэктомия после ишемического инсульта крупных сосудов: метаанализ данных отдельных пациентов из пяти рандомизированных исследований. Ланцет 387 , 1723–1731 (2016). В этой статье представлен метаанализ результатов пяти рандомизированных исследований эндоваскулярной тромбэктомии при остром инсульте .
PubMed Google Scholar
Albers, G. W. et al. Тромбэктомия при инсульте через 6–16 часов с выбором перфузионной томографии. N. Engl. J. Med. 378 , 708–718 (2018).
PubMed PubMed Central Google Scholar
Nogueira, R.G. et al. Тромбэктомия через 6–24 часа после инсульта с несоответствием между дефицитом и инфарктом. N. Engl. J. Med. 378 , 11–21 (2018).
PubMed Google Scholar
de Los Rios la Rosa, F. et al. Право на внутривенное введение рекомбинантного тканевого активатора плазминогена в популяции: влияние европейского совместного исследования острого инсульта (ECASS) III. Инсульт 43 , 1591–1595 (2012).
PubMed Google Scholar
Leischner, H. et al. Причины неудачных попыток эндоваскулярной реканализации у пациентов с инсультом. J. Neurointerv. Surg. 11 , 439–442 (2018).
PubMed Google Scholar
Braeuninger, S., Kleinschnitz, C., Nieswandt, B. & Stoll, G. Фокальная церебральная ишемия. Methods Mol. Биол. 788 , 29–42 (2012).
CAS PubMed Google Scholar
Шаллер Б. и Граф Р. Церебральная ишемия и реперфузия: патофизиологическая концепция как основа клинической терапии. J. Cereb. Blood Flow Metab. 24 , 351–371 (2004).
PubMed Google Scholar
Хаузенлой, Д. Дж. И Йеллон, Д. М. Ишемия-реперфузионное повреждение миокарда: терапевтическая цель, которой не уделяется должного внимания. J. Clin. Вкладывать деньги. 123 , 92–100 (2013).
CAS PubMed PubMed Central Google Scholar
Эльцшиг, Х.К. и Экл, Т. Ишемия и реперфузия — от механизма к трансляции. Nat. Med. 17 , 1391–1401 (2011).
CAS PubMed Google Scholar
Olah, L., Wecker, S. & Hoehn, M. Вторичное ухудшение кажущегося коэффициента диффузии после 1-часовой временной фокальной церебральной ишемии у крыс. J. Cereb. Blood Flow Metab. 20 , 1474–1482 (2000).
CAS PubMed Google Scholar
Neumann-Haefelin, T. et al. Серийная МРТ после преходящей очаговой ишемии головного мозга у крыс: динамика повреждения тканей, повреждения гематоэнцефалического барьера и образования отека. Инсульт 31 , 1965–1972 (2000).
CAS PubMed Google Scholar
Mestas, J. & Hughes, C. C. Мышей, а не людей: различия между иммунологией мыши и человека. J. Immunol. 172 , 2731–2738 (2004).
CAS PubMed Google Scholar
Хейли, П. Дж. Видовые различия в структуре и функции иммунной системы. Токсикология 188 , 49–71 (2003).
CAS PubMed Google Scholar
Йилмаз, Г., Арумугам, Т. В., Стокс, К. Ю. и Грейнджер, Д. Н. Роль Т-лимфоцитов и гамма-интерферона в ишемическом инсульте. Тираж 113 , 2105–2112 (2006). Эта основополагающая статья демонстрирует, что Т-клетки вносят существенный вклад в ишемию-реперфузионное повреждение после транзиторной церебральной ишемии у мышей .
PubMed Google Scholar
Kleinschnitz, C. et al. Ранние пагубные эффекты Т-клеток при экспериментальной ишемии головного мозга не связаны ни с адаптивным иммунитетом, ни с образованием тромбов. Кровь 115 , 3835–3842 (2010). В этой статье представлен всесторонний анализ субпопуляций Т-клеток, костимулирующих факторов и их эффектов на ишемию-реперфузионное повреждение на мышиной модели tMCAO.
CAS PubMed Google Scholar
Hofmann, U. & Frantz, S. Роль Т-клеток в инфаркте миокарда. Eur. Харт J. 37 , 873–879 (2015).
PubMed Google Scholar
Ysebaert, D. K. et al. Т-клетки как медиаторы при ишемии / реперфузии почек. Kidney Int. 66 , 491–496 (2004).
CAS PubMed Google Scholar
Zwacka, R.M. et al. CD4 + Т-лимфоциты опосредуют вызванные ишемией / реперфузией воспалительные реакции в печени мыши. J. Clin. Вкладывать деньги. 100 , 279–289 (1997).
CAS PubMed PubMed Central Google Scholar
Romer, C. et al. Блокирование иммунодефицита, вызванного инсультом, увеличивает антиген-специфическую аутореактивность ЦНС, но не ухудшает функциональный результат после экспериментального инсульта. J. Neurosci. 35 , 7777–7794 (2015).
PubMed Google Scholar
Ren, X. et al. Регуляторные В-клетки ограничивают воспаление ЦНС и неврологический дефицит при экспериментальном инсульте у мышей. J. Neurosci. 31 , 8556–8563 (2011).
CAS PubMed PubMed Central Google Scholar
Бодханкар, С., Чен, Ю., Ванденбарк, А. А., Мерфи, С. Дж. И Оффнер, Х. В-клетки, продуцирующие ИЛ-10, ограничивают воспаление ЦНС и объем инфаркта при экспериментальном инсульте. Metab. Brain Dis. 28 , 375–386 (2013).
CAS Google Scholar
Shichita, T. et al. Ключевая роль церебральных клеток гаммадельтаТ, продуцирующих интерлейкин-17, в отсроченной фазе ишемического повреждения головного мозга. Nat. Med. 15 , 946–950 (2009). Это исследование описывает роль Т-клеток и IL-17 в отсроченной фазе ишемического повреждения мозга у мышей .
CAS PubMed Google Scholar
Kleinschnitz, C. et al. Регуляторные Т-клетки являются сильными промоторами острого ишемического инсульта у мышей, вызывая дисфункцию микрососудов головного мозга. Кровь 121 , 679–691 (2013). Эта статья представляет первую демонстрацию того, что пагубные эффекты Т-клеток при церебральной ишемии-реперфузионном повреждении зависят от присутствия тромбоцитов у мышей .
CAS PubMed PubMed Central Google Scholar
Schuhmann, M. K. et al. Опосредованное суперагонистом CD28 усиление регуляторных Т-клеток увеличивает тромбовоспалительное действие и ишемическую нейродегенерацию во время острой фазы экспериментального инсульта. J. Cereb. Blood Flow Metab. 35 , 6–10 (2015).
CAS PubMed Google Scholar
Сандеркок, П. А., Конселл, К., Ценг, М. К. и Чеккони, Е. Пероральная антитромбоцитарная терапия острого ишемического инсульта. Кокрановская база данных Syst. Ред. 3 , CD000029 (2014).
Google Scholar
Zinkstok, S. M. et al.Раннее ухудшение после тромболизиса плюс аспирин при остром инсульте: апостериорный анализ антитромбоцитарной терапии в сочетании с рекомбинантным тромболизисом t-PA в исследовании ишемического инсульта. Инсульт 45 , 3080–3082 (2014).
CAS PubMed Google Scholar
Del Zoppo, G.J. et al. Экспериментальный острый тромботический инсульт у павианов. Инсульт 17 , 1254–1265 (1986).
PubMed Google Scholar
Okada, Y., Copeland, B.R., Fitridge, R., Koziol, J. A. & del Zoppo, G.J. Фибрин способствует микрососудистым обструкциям и изменениям паренхимы во время ранней очаговой церебральной ишемии и реперфузии. Инсульт 25 , 1847–1853 (1994).
CAS PubMed Google Scholar
Обренович, Т. П. и Халленбек, Дж. М. Накопление тромбоцитов в регионах с низким кровотоком в постишемический период. Инсульт 16 , 224–234 (1985).
CAS PubMed Google Scholar
Берндт, М. К., Шен, Ю., Допхайде, С. М., Гардинер, Э. Э. и Эндрюс, Р. К. Биология сосудов гликопротеинового комплекса Ib-IX-V. Тромб. Гемост. 86 , 178–188 (2001).
CAS PubMed Google Scholar
Сэвидж, Б., Saldivar, E. & Ruggeri, Z. M. Инициирование адгезии тромбоцитов путем остановки фибриногена или транслокации фактора фон Виллебранда. Cell 84 , 289–297 (1996).
CAS PubMed Google Scholar
Канаджи, С., Фах, С. А., Ши, К., Хаберихтер, С. Л. и Монтгомери, Р. Р. Вклад тромбоцитов по сравнению с эндотелиальным VWF в адгезию тромбоцитов и гемостаз. J. Thromb. Гемост. 10 , 1646–1652 (2012).
CAS PubMed PubMed Central Google Scholar
Massberg, S. et al. Решающая роль гликопротеина VI в привлечении тромбоцитов к поврежденной артериальной стенке in vivo. J. Exp. Med. 197 , 41–49 (2003).
CAS PubMed PubMed Central Google Scholar
Kleinschnitz, C. et al. Ориентация на тромбоциты при остром экспериментальном инсульте: влияние блокады гликопротеина Ib, VI и IIb / IIIa на размер инфаркта, функциональный результат и внутричерепное кровотечение. Тираж 115 , 2323–2330 (2007). Это исследование демонстрирует, что связывание и активация тромбоцитов с помощью передачи сигналов GPIb и GPVI, но не GPIIb / IIIa-опосредованная агрегация тромбоцитов, участвует в образовании ишемических повреждений при экспериментальном инсульте .
CAS PubMed Google Scholar
Kleinschnitz, C. et al. Дефицит фактора фон Виллебранда защищает мышей от ишемического инсульта. Кровь 113 , 3600–3603 (2009).
CAS PubMed Google Scholar
De Meyer, S. F. et al. Связывание фактора фон Виллебранда с коллагеном и гликопротеином Ibalpha, но не с гликопротеином IIb / IIIa, способствует ишемическому инсульту у мышей — краткий отчет. Артериосклер. Тромб. Васк. Биол. 30 , 1949–1951 (2010).
PubMed Google Scholar
Rayes, J., Уотсон, С. П. и Нисвандт, Б. Функциональное значение иммунных рецепторов тромбоцитов GPVI и CLEC-2. J. Clin. Вкладывать деньги. 129 , 12–23 (2019).
PubMed Google Scholar
Nieswandt, B. & Watson, S.P. Взаимодействие тромбоцитов и коллагена: является ли GPVI центральным рецептором? Кровь 102 , 449–461 (2003).
CAS PubMed Google Scholar
Goebel, S. et al. Слитый белок GPVI-Fc Revacept улучшает объем инфаркта головного мозга и функциональные результаты при инсульте. PLOS ONE 8 , e66960 (2013).
CAS PubMed PubMed Central Google Scholar
Даттинг С., Бендер М. и Нисвандт Б. Тромбоцитарный GPVI: цель антитромботической терапии ?! Trends Pharmacol. Sci. 33 , 583–590 (2012).
PubMed Google Scholar
Muller, F. et al. Полифосфаты тромбоцитов являются провоспалительными и прокоагулянтными медиаторами in vivo. Cell 139 , 1143–1156 (2009).
CAS PubMed PubMed Central Google Scholar
Kleinschnitz, C. et al. Фактор XII свертывания крови обеспечивает защиту от патологического тромбоза при ишемии головного мозга, не нарушая гемостаза. J. Exp. Med. 203 , 513–518 (2006).
CAS PubMed PubMed Central Google Scholar
Hagedorn, I. et al. Ингибитор фактора XIIa рекомбинантный человеческий альбумин Инфестин-4 устраняет образование окклюзионных артериальных тромбов, не влияя на кровотечение. Тираж 121 , 1510–1517 (2010).
CAS PubMed Google Scholar
Austinat, M. et al. Блокада рецептора брадикинина B1, но не рецептора брадикинина B2, обеспечивает защиту от церебрального инфаркта и отека мозга. Инсульт 40 , 285–293 (2009).
CAS PubMed Google Scholar
Heydenreich, N. et al. Ингибитор С1 защищает от ишемии-реперфузии головного мозга за счет сочетания противовоспалительных и антитромботических механизмов. Инсульт 43 , 2457–2467 (2012).
CAS PubMed Google Scholar
Gob, E. et al.Блокирование калликреина в плазме облегчает инсульт за счет уменьшения тромбовоспаления. Ann. Neurol. 77 , 784–803 (2015).
PubMed Google Scholar
Шаттил, С. Дж., Ким, К. и Гинзберг, М. Х. Заключительные этапы активации интегрина: конец игры. Nat. Rev. Mol. Cell Biol. 11 , 288–300 (2010).
CAS PubMed PubMed Central Google Scholar
Bergmeier, W. et al. Проточно-цитометрическое определение активированного мышиного интегрина alphaIIbbeta3 с новым моноклональным антителом. Цитометрия 48 , 80–86 (2002).
CAS PubMed Google Scholar
Kraft, P. et al. Эффективность и безопасность блокады гликопротеиновых рецепторов тромбоцитов у старых и сопутствующих им мышей с острым экспериментальным инсультом. Инсульт 46 , 3502–3506 (2015).
CAS PubMed Google Scholar
Adams, H.P. Jr. et al. Экстренное введение абциксимаба для лечения пациентов с острым ишемическим инсультом: результаты международного исследования фазы III: Испытание абциксимаба в неотложном лечении инсульта (AbESTT-II). Инсульт 39 , 87–99 (2008).
CAS PubMed Google Scholar
Deppermann, C. et al. Секреция тромбоцитов имеет решающее значение для предотвращения кровотечения в ишемическом мозге, но не в воспаленной коже или легком у мышей. Кровь 129 , 1702–1706 (2017).
CAS PubMed Google Scholar
Stoll, G., Kleinschnitz, C. & Nieswandt, B. Борьба с врожденным воспалением: новая парадигма лечения острого инсульта? Ann. NY Acad. Sci. 1207 , 149–154 (2010).
CAS PubMed Google Scholar
Nieswandt, B., Kleinschnitz, C. & Stoll, G. Ишемический инсульт: тромбовоспалительное заболевание? J. Physiol. 589 , 4115–4123 (2011).
CAS PubMed PubMed Central Google Scholar
Nieswandt, B. Тромбоциты направляют лимфоциты к участкам повреждения сосудов. Тромб. Гемост. 108 , 207 (2012).
CAS PubMed Google Scholar
Spectre, G. et al. Тромбоциты избирательно усиливают адгезию лимфоцитов на субэндотелиальном матриксе в условиях артериального кровотока. Тромб. Гемост. 108 , 328–337 (2012).
CAS PubMed Google Scholar
Йилмаз, Г. и Грейнджер, Д. Н. Рекрутирование лейкоцитов и ишемическое повреждение головного мозга. Neuromolecular Med. 12 , 193–204 (2010).
CAS PubMed Google Scholar
Shih, A. Y. et al. Двухфотонная микроскопия как инструмент для изучения кровотока и нервно-сосудистых связей в мозге грызунов. J. Cereb. Blood Flow Metab. 32 , 1277–1309 (2012).
CAS PubMed PubMed Central Google Scholar
Ishikawa, M. et al. Взаимодействие тромбоцитов, лейкоцитов и эндотелиальных клеток после окклюзии и реперфузии средней мозговой артерии. J. Cereb. Blood Flow Metab. 24 , 907–915 (2004).
CAS PubMed Google Scholar
Sallusto, F. et al. Торговля Т-клетками в центральной нервной системе. Immunol. Ред. 248 , 216–227 (2012).
PubMed Google Scholar
Rudick, R.A. et al. Натализумаб плюс интерферон бета-1а при рецидивирующем рассеянном склерозе. Н.Англ. J. Med. 354 , 911–923 (2006).
CAS PubMed Google Scholar
Llovera, G. et al. Сосудистое сплетение — это ключевой путь инвазии Т-клеток в мозг после инсульта. Acta Neuropathol. 134 , 851–868 (2017).
CAS PubMed Google Scholar
Беккер, К., Киндрик, Д., Релтон, Дж., Харлан, Дж.& Winn, R. Антитела к интегрину альфа4 уменьшают размер инфаркта при временной очаговой ишемии головного мозга у крыс. Инсульт 32 , 206–211 (2001).
CAS PubMed Google Scholar
Relton, J. K. et al. Ингибирование интегрина альфа4 защищает от преходящей очаговой церебральной ишемии у крыс с нормальным и гипертензивным давлением. Инсульт 32 , 199–205 (2001).
CAS PubMed Google Scholar
Llovera, G. et al. Результаты доклинического рандомизированного контролируемого многоцентрового исследования (pRCT): лечение острой ишемии головного мозга анти-CD49d. Sci. Transl Med. 7 , 299ra121 (2015). В этой статье представлены результаты первого доклинического рандомизированного контролируемого многоцентрового исследования по оценке вклада α4-интегрин-опосредованных Т-клеточных ответов в различных экспериментальных моделях ишемии головного мозга .
PubMed Google Scholar
Langhauser, F. et al. Блокирование интегрина альфа4 не защищает мышей от острого ишемического инсульта. Инсульт 45 , 1799–1806 (2014).
CAS PubMed Google Scholar
Elkins, J. et al. Безопасность и эффективность натализумаба у пациентов с острым ишемическим инсультом (ACTION): рандомизированное плацебо-контролируемое двойное слепое исследование фазы 2. Lancet Neurol. 16 , 217–226 (2017).
CAS PubMed Google Scholar
Kappos, L. et al. Пероральный финголимод (FTY720) при рецидивирующем рассеянном склерозе. N. Engl. J. Med. 355 , 1124–1140 (2006).
CAS PubMed Google Scholar
Kraft, P. et al. FTY720 облегчает острый ишемический инсульт у мышей за счет уменьшения тромбовоспаления, но не за счет прямой нейропротекции. Инсульт 44 , 3202–3210 (2013).
CAS PubMed Google Scholar
Fu, Y. et al. Влияние иммуномодулятора финголимода на острый ишемический инсульт. Proc. Natl Acad. Sci. США 111 , 18315–18320 (2014).
CAS PubMed Google Scholar
Zhu, Z. et al. Комбинация иммуномодулятора финголимода с альтеплазой при остром ишемическом инсульте: пилотное исследование. Тираж 132 , 1104–1112 (2015). В данной статье представлены результаты пилотного клинического испытания, в котором иммуномодулятор финголимод был объединен с альтеплазой для лечения острого ишемического инсульта .
CAS PubMed PubMed Central Google Scholar
Tian, D. C. et al. Финголимод усиливает эффективность отсроченного введения альтеплазы при остром ишемическом инсульте, способствуя антероградной реперфузии и ретроградному коллатеральному кровотоку. Ann. Neurol. 84 , 717–728 (2018).
CAS PubMed PubMed Central Google Scholar
Zhang, S. et al. Обоснование и дизайн комбинации иммуномодулятора финголимода с альтеплазным мостиком с механической тромбэктомией в исследовании острого ишемического инсульта (FAMTAIS). Внутр. Дж. Инсульт 12 , 906–909 (2017).
PubMed Google Scholar
Jin, W. N. et al. Ишемия головного мозга вызывает разнообразные нейроантиген-специфические Т-клеточные ответы, которые усугубляют повреждение головного мозга. Инсульт 49 , 1471–1478 (2018).
PubMed PubMed Central Google Scholar
Na, S. Y., Mracsko, E., Liesz, A., Hunig, T. и Veltkamp, R. Амплификация регуляторных Т-клеток с использованием суперагониста CD28 снижает повреждение мозга после ишемического инсульта у мышей. Инсульт 46 , 212–220 (2015).
CAS PubMed Google Scholar
Liesz, A. et al. Регуляторные Т-клетки являются ключевыми церебропротекторными иммуномодуляторами при остром экспериментальном инсульте. Nat. Med. 15 , 192–199 (2009).
CAS PubMed Google Scholar
Li, P. et al. Адоптивная терапия регуляторными Т-клетками защищает от церебральной ишемии. Ann. Neurol. 74 , 458–471 (2013).
CAS PubMed PubMed Central Google Scholar
Liesz, A., Hu, X., Kleinschnitz, C. & Offner, H. Функциональная роль регуляторных лимфоцитов при инсульте: факты и противоречия. Инсульт 46 , 1422–1430 (2015).
PubMed PubMed Central Google Scholar
Лис, А.и другие. FTY720 снижает приток постишемических лимфоцитов в мозг, но не улучшает исход при перманентной ишемии головного мозга у мышей. PLOS ONE 6 , e21312 (2011).
CAS PubMed PubMed Central Google Scholar
Gelderblom, M. et al. Обычные дендритные клетки, продуцирующие IL-23 (интерлейкин-23), контролируют пагубный ответ IL-17 (интерлейкин-17) при инсульте. Инсульт 49 , 155–164 (2018).
CAS PubMed Google Scholar
Gelderblom, M. et al. Нейтрализация оси IL-17 снижает инвазию нейтрофилов и защищает от ишемического инсульта. Кровь 120 , 3793–3802 (2012).
CAS PubMed Google Scholar
Benakis, C. et al. Комменсальная микробиота влияет на исход ишемического инсульта, регулируя кишечные гаммадельта-Т-клетки. Nat. Med. 22 , 516–523 (2016).
CAS PubMed PubMed Central Google Scholar
Singh, V. et al. Микробиом кишечника запускает церебропротекторный иммунный ответ после инсульта. J. Cereb. Blood Flow Metab. 38 , 1293–1298 (2018).
CAS PubMed Google Scholar
Vermeij, J. D., Westendorp, W. F., Dippel, D. W., van de Beek, D. & Nederkoorn, P. J. Антибактериальная терапия для предотвращения инфекций у людей с острым инсультом. Кокрановская база данных Syst. Ред. 1 , CD008530 (2018).
PubMed Google Scholar
Prass, K. et al. Индуцированный инсультом иммунодефицит способствует спонтанным бактериальным инфекциям и опосредуется обращением активации симпатической нервной системы за счет иммуностимуляции, подобной постинсультному Т-хелперу типа 1. J. Exp. Med. 198 , 725–736 (2003). В этой статье дается первое описание вызванной инсультом иммунодепрессии у мышей и лежащей в основе активации симпатической нервной системы .
CAS PubMed PubMed Central Google Scholar
Salas-Perdomo, A. et al. Т-клетки предотвращают геморрагическую трансформацию при ишемическом инсульте за счет связывания Р-селектина. Артериосклер. Тромб.Васк. Биол. 38 , 1761–1771 (2018).
CAS PubMed Google Scholar
Mao, L. et al. Регуляторные Т-клетки улучшают кровоизлияние в мозг, вызванное тканевым активатором плазминогена, после инсульта. Мозг 140 , 1914–1931 (2017).
PubMed PubMed Central Google Scholar
Schuhmann, M. K. et al. Влияние тромболизиса на безопасность и эффективность блокирования адгезии тромбоцитов или секреторной активности при остром ишемическом инсульте у мышей. Transl Stroke Res. 9 , 493–498 (2018).
PubMed Google Scholar
Schuhmann, M. K. et al. Целенаправленное введение тромбоцитов GPVI плюс rt-PA, но не связывание коллагена, опосредованное альфа2бета1, защищает от ишемического повреждения мозга у мышей. Внутр. J. Mol. Sci. 20 , E2019 (2019).
PubMed Google Scholar
Эймс, А. 3-й, Райт, Р. Л., Ковада, М., Терстон, Дж. М. и Майно, Г. Церебральная ишемия. II. Феномен отсутствия оплавления. Am. J. Pathol. 52 , 437–453 (1968).
PubMed PubMed Central Google Scholar
Халленбек, Дж. М. и Дутка, А. Дж. Общий обзор и современные концепции реперфузионного повреждения. Arch. Neurol. 47 , 1245–1254 (1990).
CAS PubMed Google Scholar
Hallenbeck, J. M. et al. Накопление полиморфноядерных лейкоцитов в областях мозга с низким кровотоком в раннем постишемическом периоде. Инсульт 17 , 246–253 (1986).
CAS PubMed Google Scholar
дель Зоппо, Дж. Дж. И Мабучи Т. Ответы микрососудов головного мозга на очаговую ишемию. J. Cereb. Blood Flow Metab. 23 , 879–894 (2003).
PubMed Google Scholar
Влияние COVID-19 на ишемический инсульт | Диагностическая патология
Вспышка нового коронавируса с 12 декабря 2019 года стала чрезвычайной ситуацией, имеющей серьезное международное значение, и представляет собой серьезную проблему для врачей.Типичными симптомами являются жар, боль в горле, усталость, кашель или одышка в сочетании с недавним контактом. Инфекция SARS-CoV-2 имеет кластерное начало, которое с большей вероятностью поражает пожилых мужчин с сопутствующими заболеваниями [10]. У пожилых людей всегда есть более высокие факторы риска, связанные с острым ишемическим инсультом или эмболизацией сосудов. Учитывая, что этому пациенту 79 лет и иммунный ответ не такой сильный, как у молодых мужчин, типичных симптомов инфекции SARS-CoV-2 не наблюдалось.Через 10 дней после посещения друзей он начал слегка кашлять. Средний инкубационный период COVID-19 составляет 6,4 дня в диапазоне от 2,1 до 11,1 дня (от 2,5 до 97,5 процентиля) [11]. Мы подозреваем, что он подвергся воздействию вирусной среды, в которой некоторые аэрозоли могут переносить SARS-CoV-2. Этот пациент был госпитализирован со слабостью правой конечности и затрудненной речью, а компьютерная томография грудной клетки позже обнаружила типичные изображения COVID-19, предполагая, что неврологам следует запросить дополнительную информацию об истории контактов.Кроме того, для диагностики COVID-19 должны быть назначены КТ грудной клетки и лабораторные исследования, в том числе мазки.
В этом случае, чтобы объяснить слабость правой конечности как начальный симптом, была выдвинута гипотеза, что инфекция SARS-CoV-2 вызвала гипоксемию и чрезмерную секрецию воспалительных цитокинов, что привело к острому ишемическому инсульту. Гипоксемия значительно снижает энергию, необходимую для клеточного метаболизма, увеличивает анаэробную ферментацию и вызывает внутриклеточный ацидоз и свободные радикалы кислорода.При продолжении гипоксии внутриклеточная концентрация ионов кальция значительно увеличивается, вызывая серию повреждений клеток, включая апоптоз. Более того, гипоксия также может вызывать воспалительные реакции, включая инфильтрацию воспалительных клеток и высвобождение цитокинов, что приводит к дальнейшей ишемии тканей [12]. Воспаление играет важную роль в возникновении, развитии и прогнозе сердечно-сосудистых и цереброваскулярных заболеваний. По сравнению с пациентами, не получающими ОИТ, пациенты с ОИТ с инфекцией SARS-CoV-2 имели более высокие уровни цитокинов в плазме, включая IL-2, IL-7, IL-10, GSCF, IP10, MCP1, MIP1A и TNFα [2].Воспаление способствует развитию атеросклероза и влияет на стабильность бляшек [13]. Кроме того, вирус SARS-CoV-2 связывается с ангиотензин-превращающим ферментом 2 (ACE2), присутствующим на эндотелиальных и гладкомышечных клетках головного мозга. Истощение ACE2 SARS-CoV-2 может склонить чашу весов в пользу «вредной» оси ACE1 / ангиотензин II и способствовать повреждению тканей, включая инсульт [14]. Следуя этим идеям, мы предполагаем, что инфекционная пневмония, вызванная SARS-CoV-2, является одним из патогенов ишемического инсульта. Последние полученные последовательности полноразмерных геномов показали, что SARS-CoV-2 использует рецептор входа в клетку ACE2 [15].Структурный анализ показывает, что ACE2 может связываться с B 0 AT1 (SLC6A19), который является переносчиком нейтральных аминокислот, что дает важные ключи к разгадке молекулярной основы распознавания коронавируса и инфицирования [16]. Из-за комбинации SARS-CoV-2 с рецептором ACE2 некоторые пациенты с гипертонией и инфекцией SARS-CoV-2 могут испытывать аномально повышенное кровяное давление, что увеличивает риск внутримозгового кровоизлияния. В семейном кластере пневмонии, связанной с SARS-CoV-2, пожилые пациенты (в возрасте> 60 лет) имеют более системные симптомы, такие как тромбоцитопения, что увеличивает вероятность острых цереброваскулярных событий [5].В клинике у некоторых пациентов с COVID-19 наблюдаются симптомы внутричерепной инфекции, включая головную боль, эпилепсию и нарушения сознания; у некоторых пациентов с COVID-19 наблюдаются симптомы острого цереброваскулярного заболевания, включая паралич конечностей; и у некоторых есть невралгия и парестезия.
Ранняя диагностика, карантин и поддерживающее лечение необходимы для излечения пациентов. Поскольку SARS-CoV-2 является новым вирусом, противовирусные препараты не рекомендуются для лечения коронавирусной инфекции [17]. В этом случае применялась терапия дексаметазоном в низких дозах, чтобы избежать воспалительных бурь.Кортикостероиды подавляют воспаление легких, но также подавляют иммунные реакции и выведение патогенов. Клинические результаты коронавируса и подобных вспышек не подтверждают использование кортикостероидов [18,19,20]. Текущее временное руководство ВОЗ по клиническому ведению тяжелой острой респираторной инфекции при подозрении на инфекцию SARS-CoV-2 (выпущено 28 января 2020 г.) не рекомендует использовать кортикостероиды, если не указано иное. Для лечения гипертензии блокаторы рецептора AT1 (БРА), такие как лозартан, могут быть защитными при инсульте.Хотя были некоторые опасения, что БРА и ингибиторы АПФ могут быть вредными для пациентов с COVID-19, увеличивая экспрессию связывания ACE2 и SARS-CoV-2, совместное заявление Американской кардиологической ассоциации. В связи с этим спорным вопросом таблетки безилата амлодипина назначались для снижения артериального давления.
Рецидивирующий ишемический инсульт: стратегии профилактики
1. Mozaffarian D, Бенджамин Э.Дж., Идти КАК, и другие.; Статистический комитет Американской кардиологической ассоциации; Подкомитет по статистике инсульта.Обновление статистики сердечных заболеваний и инсульта за 2016 г .: отчет Американской кардиологической ассоциации [опубликованное исправление опубликовано в Circulation. 2016; 133 (15): e599]. Тираж . 2016; 133 (4): e38 – e360 ….
2. Истон Дж. Д., Saver JL, Альберс GW, и другие. Определение и оценка транзиторной ишемической атаки: научное заявление для медицинских работников от Совета по инсульту Американской кардиологической ассоциации / Американской ассоциации по инсульту; Совет по сердечно-сосудистой хирургии и анестезии; Совет по сердечно-сосудистой радиологии и интервенции; Совет по уходу за сердечно-сосудистыми заболеваниями; и Междисциплинарный совет по заболеваниям периферических сосудов. Ход . 2009. 40 (6): 2276–2293.
3. Сакко Р.Л., Kasner SE, Бродерик JP, и другие.; Совет по инсульту Американской кардиологической ассоциации, Совет по сердечно-сосудистой хирургии и анестезии; Совет по сердечно-сосудистой радиологии и интервенции; Совет по сердечно-сосудистым заболеваниям и инсульту; Совет по эпидемиологии и профилактике; Совет по заболеваниям периферических сосудов; Совет по питанию, физической активности и метаболизму. Обновленное определение инсульта для 21 века: заявление для медицинских работников Американской кардиологической ассоциации / Американской ассоциации инсульта. Ход . 2013. 44 (7): 2064–2089.
4. Арсава Е.М., Ким GM, Оливейра-Филью Дж., и другие. Прогнозирование раннего рецидива после острого ишемического инсульта. JAMA Neurol . 2016; 73 (4): 396–401.
5. Kernan WN, Овбьягеле Б, Черный HR, и другие.; Совет Американской кардиологической ассоциации по инсульту, Совет по сердечно-сосудистым заболеваниям и уходу за больными после инсульта, Совет по клинической кардиологии и Совет по заболеваниям периферических сосудов.Рекомендации по профилактике инсульта у пациентов с инсультом и транзиторной ишемической атакой: руководство для медицинских работников от Американской кардиологической ассоциации / Американской ассоциации инсульта [опубликованная поправка опубликована в Stroke. 2015; 46 (2): e54]. Ход . 2014. 45 (7): 2160–2236.
6. Коллективная группа «ПРОГРЕСС». Рандомизированное исследование схемы снижения артериального давления на основе периндоприла среди 6105 человек, перенесших инсульт или преходящую ишемическую атаку [опубликованные исправления опубликованы в Lancet.2002; 359 (9323): 2120 и Lancet 2001; 358 (9292): 1556]. Ланцет . 2001. 358 (9287): 1033–1041.
7. Группа сотрудничества PATS. Исследование гипотензивной терапии после инсульта. Предварительный результат. Chin Med J (англ.) . 1995. 108 (9): 710–717.
8. Джеймс П.А., Опарил С, Картер Б.Л., и другие. Основанное на фактах руководство 2014 года по лечению высокого кровяного давления у взрослых: отчет членов комиссии, назначенных в Восьмой объединенный национальный комитет (JNC 8) [опубликованное исправление опубликовано в JAMA.2014; 311 (17): 1809]. ЯМА . 2014. 311 (5): 507–520.
9. Стоун, штат Нью-Джерси, Робинсон Дж. Г., Лихтенштейн AH, и другие.; Группа рекомендаций ACC / AHA по холестерину, 2013 г. Лечение холестерина в крови для снижения риска атеросклеротических сердечно-сосудистых заболеваний у взрослых: синопсис руководства по холестерину Американского колледжа кардиологов / Американской кардиологической ассоциации 2013 г. Энн Интерн Мед. . 2014; 160 (5): 339–343.
10.Кернан WN, Inzucchi SE, Саван С, Макко РФ, Furie KL. Ожирение: очевидная цель для профилактики инсульта. Ход . 2013. 44 (1): 278–286.
11. Amarenco P, Богоуславский Ж, Каллахан А III, и другие.; Профилактика инсульта с помощью исследователей агрессивного снижения уровня холестерина (SPARCL). Высокие дозы аторвастатина после инсульта или транзиторной ишемической атаки. N Engl J Med .2006. 355 (6): 549–559.
12. Наси Х, Брюгц Дж. Дж., Флёренс Р, Ades AE. Сравнительные эффекты статинов на основные цереброваскулярные события: метаанализ нескольких курсов лечения плацебо-контролируемых исследований и исследований активного компаратора. QJM . 2013. 106 (4): 299–306.
13. Карам Дж. Г., Лони-Хатчинсон Л, McFarlane SI. Высокие дозы аторвастатина после инсульта или транзиторной ишемической атаки: Исследователи по предотвращению инсульта путем агрессивного снижения уровня холестерина (SPARCL). Дж. Кардиометаб Синдр . 2008. 3 (1): 68–69.
14. Джозеф Дж. П., Афонсу М, Бердай Д, и другие. Преимущества и риски первичной профилактики статинами у пожилых [на французском]. Пресс Мед . 2015; 44 (12 п.1): 1219–1225.
15. Руланд С, Hung E, Ричардсон Д, Мисра С, Горелик ПБ; Афро-американские исследователи исследования профилактики инсульта. Влияние ожирения и метаболического синдрома на факторы риска у афроамериканцев, перенесших инсульт: отчет AAASPS. Arch Neurol . 2005. 62 (3): 386–390.
16. Овбиагеле Б, Баня PM, Хлопок D, Виниско Р, Diener HC. Ожирение и рецидивирующий сосудистый риск после недавнего ишемического инсульта. Ход . 2011; 42 (12): 3397–3402.
17. Doehner W, Шенкель Дж. Анкер С.Д., Спрингер Дж. Audebert HJ. Избыточный вес и ожирение связаны с улучшением выживаемости, функционального результата и рецидивов инсульта после острого инсульта или транзиторной ишемической атаки: наблюдения из исследования TEMPiS. Eur Heart J . 2013. 34 (4): 268–277.
18. Веммос К, Нтайос Г, Спенгос К, и другие. Связь между ожирением и смертностью после острого первого инсульта: парадокс ожирения и инсульта. Ход . 2011. 42 (1): 30–36.
19. Эпштейн Л.Дж., Кристо Д, Strollo PJ Jr, и другие.; Целевая группа по обструктивному апноэ сна для взрослых Американской академии медицины сна. Клинические рекомендации по оценке, ведению и долгосрочному лечению обструктивного апноэ во сне у взрослых. Дж. Клин Сон Мед . 2009. 5 (3): 263–276.
20. Colten HR, Altevogt BM. Нарушения сна и депривация сна: неудовлетворенная проблема общественного здравоохранения. Вашингтон, округ Колумбия: Институт медицины, Национальная академия прессы; 2006.
21. Путаала Дж., Куркинен М, Тарвос V, Салонен О, Kaste M, Татлисумак Т. Тихие инфаркты головного мозга и лейкоареоз у молодых людей с первым в истории ишемическим инсультом. Неврология . 2009. 72 (21): 1823–1829.
22. Mendis S, Абегунде Д, Юсуф С, и другие. Исследование ВОЗ по профилактике рецидивов инфаркта миокарда и инсульта (ВОЗ-PREMISE). Орган здоровья Bull World . 2005. 83 (11): 820–829.
23. ЖК Каплан, Тиршвелл Д.Л., Longstreth WT Jr, и другие. Сосудистые события, смертность и профилактическая терапия после ишемического инсульта у пожилых людей. [опубликованное исправление опубликовано в Neurology 2006; 66 (4): 493]. Неврология . 2005. 65 (6): 835–842.
24. Мостофский Э, Бургер MR, Шлауг G, Мукамал К.Дж., Розамонд В.Д., Mittleman MA. Алкоголь и начало острого ишемического инсульта: исследование начала инсульта. Ход . 2010. 41 (9): 1845–1849.
25. MacKay-Lyons M, Губиц Г, Джакомантонио Н, и другие. Программа реабилитационных упражнений и обучения для предотвращения сосудистых событий после инсульта, не приводящего к инвалидности, или транзиторной ишемической атаки (исследование PREVENT): многоцентровое рандомизированное контролируемое исследование. BMC Neurol . 2010; 10: 122.
26. Приор ПЛ, Хачинский В, Ансуорт К., и другие. Комплексная кардиологическая реабилитация для вторичной профилактики после транзиторной ишемической атаки или легкого инсульта: I: осуществимость и факторы риска. Ход . 2011. 42 (11): 3207–3213.
27. Сотрудничество исследователей антитромботических препаратов. Совместный метаанализ рандомизированных исследований антитромбоцитарной терапии для предотвращения смерти, инфаркта миокарда и инсульта у пациентов с высоким риском [опубликованная поправка появляется в BMJ.2002, 324 (7330): 141]. BMJ . 2002. 324 (7329): 71–86.
28. Дикерсон Л.М., Карек ПиДжей, Quattlebaum RG. Профилактика повторного ишемического инсульта. Ам Фам Врач . 2007. 76 (3): 382–388.
29. Фаррелл Б., Годвин Дж, Ричардс С., Варлоу К. Испытание аспирина в Соединенном Королевстве при транзиторной ишемической атаке (UK-TIA): окончательные результаты. J Neurol Neurosurg Psychiatry . 1991. 54 (12): 1044–1054.
30. Голландская группа по исследованию TIA. Сравнение двух доз аспирина (30 мг против 283 мг в день) у пациентов после транзиторной ишемической атаки или легкого ишемического инсульта. N Engl J Med . 1991. 325 (18): 1261–1266.
31. Канадская группа совместных исследований. Рандомизированное исследование аспирина и сульфинпиразона при угрозе инсульта. N Engl J Med . 1978. 299 (2): 53–59.
32. Джонсон Э.С., Дорожки SF, Вентворт CE III, Саттерфилд MH, Абебе Б.Л., Дикер Л.В.Метарегрессионный анализ дозозависимого эффекта аспирина при инсульте. Arch Intern Med . 1999. 159 (11): 1248–1253.
33. Группа сотрудничества ОСВ. Шведское исследование низких доз аспирина (SALT) 75 мг аспирина в качестве вторичной профилактики после цереброваскулярных ишемических событий. Ланцет . 1991; 338 (8779): 1345–1349.
34. Дреппер М.Д., Спар Л, Frossard JL. Клопидогрель и ингибиторы протонной помпы — где мы находимся в 2012 году? Мир Дж. Гастроэнтерол .2012. 18 (18): 2161–2171.
35. Diener HC, Богоуславский Ж, Латунь LM, и другие.; Следователи МАТЧ. Сравнение аспирина и клопидогреля с одним клопидогрелом после недавнего ишемического инсульта или транзиторной ишемической атаки у пациентов с высоким риском (MATCH): рандомизированное двойное слепое плацебо-контролируемое исследование. Ланцет . 2004. 364 (9431): 331–337.
36. Mega JL, Закрыть SL, Wiviott SD, и другие.Полиморфизм цитохрома p-450 и ответ на клопидогрель. N Engl J Med . 2009. 360 (4): 354–362.
37. Pezalla E, День D, Пуллиадат I. Первоначальная оценка клинического воздействия лекарственного взаимодействия между клопидогрелом и ингибиторами протонной помпы. Дж. Ам Колл Кардиол . 2008. 52 (12): 1038–1039.
38. Ван Ю, Пан Y, Чжао X, и другие.; ШАНС Следователи. Клопидогрел с аспирином при остром малом инсульте или транзиторной ишемической атаке (CHANCE): результаты через год. Тираж . 2015; 132 (1): 40–46.
39. Bhatt DL, Фокс К.А., Хаке W, и другие.; ХАРИЗМА Следователи. Клопидогрель и аспирин по сравнению с одним аспирином для предотвращения атеротромботических событий. N Engl J Med . 2006. 354 (16): 1706–1717.
40. Группа ESPS. Европейское исследование профилактики инсульта (ESPS). Основные конечные точки. Ланцет . 1987. 2 (8572): 1351–1354.
41. Diener HC, Cunha L, Forbes C, Сивениус Дж, Смец П, Ловенталь А. Европейское исследование профилактики инсульта. 2. Дипиридамол и ацетилсалициловая кислота во вторичной профилактике инсульта. J Neurol Sci . 1996. 143 (1–2): 1–13.
42. Исследовательская группа исследования «Профилактика инсульта при обратимой ишемии» (SPIRIT). Рандомизированное испытание антикоагулянтов по сравнению с аспирином после церебральной ишемии предполагаемого артериального происхождения. Энн Нейрол . 1997. 42 (6): 857–865.
43. Halkes PH, ван Гийн Дж., Каппелле ЖЖ, Коудсталь П.Дж., Альгра А; Исследовательская группа ESPRIT. Пероральные антикоагулянты средней интенсивности в сравнении с аспирином после церебральной ишемии артериального происхождения (ESPRIT): рандомизированное контролируемое исследование. Ланцет Нейрол . 2007. 6 (2): 115–124.
44. Chimowitz MI, Линн MJ, Хоулетт-Смит H, и другие.; Исследователи по клиническим испытаниям симптоматического внутричерепного заболевания варфарин-аспирин.Сравнение варфарина и аспирина при симптоматическом стенозе внутричерепных артерий. N Engl J Med . 2005. 352 (13): 1305–1316.
45. Ezekowitz JA, Straus SE, Маджумдар SR, Макалистер Ф.А. Инсульт: стратегии первичной профилактики. Ам Фам Врач . 2003. 68 (12): 2379–2386.
46. Райан М, Расчески G, Penix LP. Профилактика инсульта у пациентов с преходящими ишемическими атаками. Ам Фам Врач .1999. 60 (8): 2329–2336.
47. Харт Р.Г., Бенавенте О. Инсульт: часть I. Обновленная клиническая информация о профилактике. Ам Фам Врач . 1999. 59 (9): 2475–2482.
Инсульт часто возникает при COVID-19, приводит к «разрушительным последствиям» для пациентов
23 сентября 2020
Читать 3 мин.
Источник / Раскрытие информацииРаскрытие информации: Фридман не сообщает о раскрытии соответствующей финансовой информации.Пожалуйста, просмотрите полное исследование для раскрытия финансовой информации всех других авторов.
ДОБАВИТЬ ТЕМУ В ОПОВЕЩЕНИЯ ПО ЭЛЕКТРОННОЙ ПОЧТЕ
Получать электронное письмо, когда новые статьи публикуются на
Укажите свой адрес электронной почты, чтобы получать сообщения о публикации новых статей. Подписаться Нам не удалось обработать ваш запрос.Пожалуйста, повторите попытку позже. Если у вас по-прежнему возникает эта проблема, обратитесь по адресу [email protected].Вернуться в Healio
Согласно систематическому обзору, опубликованному в Neurology , тяжесть респираторных симптомов служила наиболее значимым показателем внутрибольничной смертности среди пациентов с COVID-19, перенесших инсульт.
Как показали результаты исследования, пожилой возраст и большее количество сопутствующих сердечно-сосудистых заболеваний также коррелировали с внутрибольничной смертностью в этой популяции пациентов.
«На сегодняшний день относительно мало известно о частоте, клинических характеристиках и исходах острых цереброваскулярных событий у пациентов с COVID-19», — пишут исследователи. «Мы предположили, что инсульт является частым осложнением среди пациентов с COVID-19, что внутрибольничная смертность выше у пациентов с инсультом и COVID-19 по сравнению с историческими когортами без COVID-19, и что молодые пациенты будут демонстрировать более высокую смертность из-за к более высокой частоте окклюзии крупных сосудов (LVO).”
Исследователи добавили, что нагрузка на систему здравоохранения и другие факторы, связанные с пандемией, привели к недооценке частоты инсультов.
Себастьян Фридман , MD, MPH, кафедры клинических неврологических наук в Школе медицины и стоматологии им. Шулиха, Западный университет, Онтарио, и в систематическом обзоре коллег были проанализированы исследования, опубликованные в период с 1 ноября 2019 г. 29 мая 2020 г., с метаанализом случайных эффектов.Обзор включал исследования, в которых изучалась доля пациентов с COVID-19, перенесших инсульт, тип цереброваскулярного события и уровень смертности.
Предполагаемые результаты обзора заключались в оценке доли пациентов с COVID-19, перенесших инсульт; проанализировать сопутствующие заболевания, клинические характеристики и исходы; определить клинические фенотипы; и сравнить внутрибольничную смертность между этими клиническими фенотипами.
Фридман и его коллеги проанализировали данные 10 опубликованных исследований, которые были объединены с одной неопубликованной серией из Канады.Они применили метаанализ случайных эффектов, чтобы определить количество инсультов, которые произошли среди пациентов с COVID-19. Они также провели дополнительный систематический поиск серий случаев инсультов у пациентов с COVID-19 (n = 125) и объединили эти данные с 35 неопубликованными исследованиями из Канады, США и Ирана.
Исследователи оценили внутрибольничную смертность пациентов, перенесших инсульт в период от 14 дней до и через 60 дней после диагноза COVID-19, и сравнили результаты между пациентами в возрасте до 50, в возрасте от 51 до 70 и старше 70 лет.Они применили кластерный анализ для определения различных клинических фенотипов и их взаимосвязи со смертностью.
Фридман и его коллеги обнаружили, что у 1,8% пациентов с COVID-19 случился инсульт (95% ДИ, 0,9–3,7%), в том числе у 1,5% был ишемический инсульт (95% ДИ, 0,8% -2,8%). Они также сообщили о внутрибольничной летальности 34,4% (95% ДИ, 27,2–42,2%). По словам исследователей, как частота инсультов, так и госпитальная смертность были «чрезвычайно высокими».
У пациентов в возрасте до 50 лет уровень смертности был на 67% ниже по сравнению с пациентами в возрасте старше 70 лет (OR = 0.33; 95% ДИ, 0,12-0,94). Окклюзия крупных сосудов происходила в два раза чаще, чем в предыдущих исследованиях (46,9%), и была высокой во всех возрастных группах, «даже при отсутствии факторов риска или сопутствующих заболеваний». Фридман и его коллеги обнаружили, что клинический фенотип, характеризующийся пожилым возрастом, повышенным бременем сопутствующих заболеваний и тяжелыми респираторными симптомами, связанными с COVID-19, коррелирует с самыми высокими показателями госпитальной смертности (58,6%) и риском смерти в три раза большим, чем у остальных. когорты (OR = 3.52; 95% ДИ 1,53-8,09).
«Интересно, что 50% пациентов младше 50 лет перенесли инсульт до появления респираторных симптомов COVID-19, и это было значительно чаще, чем в других возрастных группах», — пишут исследователи. «Это открытие может означать, что в эпоху COVID-19 более молодые пациенты, поступающие в [ED] с острым инсультом, должны быть проверены на SARS-COV-2 даже при отсутствии конкретных симптомов или независимо от того, у них был COVID. -19 экран ».
Исследователи обнаружили, что инсульт «относительно часто» встречается у пациентов с COVID-19 с «разрушительными последствиями» для пациентов любого возраста.
«Наши результаты должны служить информацией для прогнозирования, распределения ресурсов и консультирования пациентов и их семей», — написали Фридман и его коллеги.
ДОБАВИТЬ ТЕМУ В ОПОВЕЩЕНИЯ ПО ЭЛЕКТРОННОЙ ПОЧТЕ
Получать электронное письмо, когда новые статьи публикуются на
Укажите свой адрес электронной почты, чтобы получать сообщения о публикации новых статей.Подписаться Нам не удалось обработать ваш запрос. Пожалуйста, повторите попытку позже. Если у вас по-прежнему возникает эта проблема, обратитесь по адресу [email protected].Вернуться в Healio
Последствия транзиторной ишемической атаки
Вот кое-что, о чем вы, вероятно, не услышите в отделении неотложной помощи: транзиторная ишемическая атака (ТИА, или мини-инсульт) может иметь симптомы, которые после этого сохраняются в течение месяцев или лет.Многие медицинские работники думают, что эти симптомы редки или, по крайней мере, краткосрочны, но опрос, проведенный в 2013 году Британской ассоциацией инсультов, показал иное. Семьдесят процентов респондентов сообщили о долгосрочных последствиях, таких как когнитивные трудности или плохая мобильность. А у шестидесяти процентов после инцидента произошли эмоциональные изменения.
Как бы это ни расстраивало, легко понять, почему этим пациентам не уделяется должного внимания. Занятые медицинские работники уделяют время самым насущным потребностям; когда жертвы инсульта выходят живыми, это победа.Но многим требуется интенсивная физическая и когнитивная терапия для повторного изучения основных функций, таких как ходьба, разговор и уход за собой. Не все из них могут делать это снова. Для сравнения, большинство выживших после ТИА могут ходить, разговаривать и есть сами; из-за этого они теряются в перемешивании.
Но стойкие симптомы, такие как проблемы с памятью, затуманенное мышление, эмоциональные изменения и трудности с самовыражением, не должны оставаться без лечения. Они существенно влияют на качество вашей жизни. Вы заслуживаете того, чтобы знать, что эти симптомы могут возникать в результате ТИА, и вы заслуживаете получения соответствующей консультации и медицинской помощи.
В нашей клинике мы лечим хронические физические и когнитивные симптомы травм головного мозга, такие как сотрясение мозга, бактериальные и вирусные инфекции, отравление угарным газом, «химический мозг», транзиторная ишемическая атака и многое другое.
Пациенты с ТИА, которые обратились к нам, не подозревали, что ТИА может вызывать затяжные симптомы, когда они впервые проходили лечение в местной больнице. Они были так рады узнать, что им доступна помощь.
Мы считаем, что каждый пациент с ТИА должен знать о последствиях ТИА и о том, как получить помощь в случае необходимости.В этом посте мы рассмотрим некоторую основную информацию о том, как происходят TIA и как распознать, есть ли у вас такое, но в основном мы сосредоточимся на двух темах:
Самое главное: немедленно обратитесь за медицинской помощью для ТИА и следуйте инструкциям врача по профилактике инсульта. После этого вы можете работать над преодолением долгосрочных эффектов ТИА, если они у вас возникнут.
Если после ТИА у вас сохраняются симптомы, значит, вы не одиноки и не сумасшедшие.ТИА может вызывать и вызывает стойкие симптомы, которые не исчезнут без лечения. У 95% наших пациентов после лечения в нашей клинике наблюдается статистически подтвержденное восстановление функции мозга. Закажите бесплатную консультацию с нашей командой, чтобы узнать, можем ли мы вам помочь.
Что такое транзиторная ишемическая атака?
Преходящая ишемическая атака — это преходящая закупорка сосудов (сгусток), которая устраняет или снижает приток крови к какой-либо части мозга.«Переходный» относится к тому, как долго он длится: обычно менее одного часа, но иногда и дольше. Ишемический инсульт вызван скорее сгустком, чем разрывом кровеносных сосудов. Эпизод заканчивается, когда сгусток разрушается и позволяет возобновить кровоток.
ТИА не вызывает обширных и необратимых повреждений, но может привести к появлению небольших очагов мертвых клеток мозга. Его часто называют «предупреждающим инсультом», потому что он предшествует 12% всех инсультов, а у 9–17% пациентов с ТИА инсульт случается в течение 90 дней.Это означает, что крайне важно обратиться за медицинской помощью и за последующим наблюдением из-за повышенного риска инсульта.
Симптомы TIA
В настоящий момент вы можете не знать, есть ли у вас мини-удар или полный ход, потому что многие признаки одинаковы. Вы можете запомнить предупреждающие признаки и симптомы инсульта с помощью аббревиатуры BE FAST:
.- Проблемы с равновесием: У вас кружится голова? Ты упал?
- Проблемы со зрением: Вы потеряли зрение? Ваше зрение нечеткое?
- Слабость лица: Умеешь ли ты улыбаться? У вас опущены уши или глаза?
- Слабость в руке: Можете ли вы нормально поднять обе руки? Есть ли у вас онемение или покалывание в мышцах?
- Проблемы с речью: Вы четко говорите? Могут ли другие понять вас? Вы их понимаете?
- Пора немедленно обратиться за медицинской помощью, если присутствует какой-либо из этих признаков.Каждая минута имеет значение.
Симптомы ТИА появляются внезапно и могут так же быстро исчезнуть. Люди часто принимают их за мигрень или защемление нерва. Другие симптомы инсульта включают онемение или покалывание на одной стороне тела, потерю памяти и спутанность сознания.
Отнеситесь к этим знакам серьезно. В случае ложной тревоги лучше обратиться в скорую помощь или в инсульт в местной больнице, чем при недиагностированной ТИА или полном инсульте. Проконсультируйтесь с врачом, чтобы определить факторы риска инсульта (такие как высокое кровяное давление, фибрилляция предсердий или семейный анамнез), принять все необходимые профилактические препараты (например, статины или антиагреганты) и внести рекомендуемые изменения в образ жизни, чтобы снизить риск в будущем. инсульт (например, диета и упражнения).
После оказания неотложной помощи и выздоровления вы можете заметить любое количество из этих долгосрочных эффектов ТИА:
Хотя эти симптомы могут исчезнуть со временем, если они все еще присутствуют через три месяца после ТИА, они, вероятно, не исчезнут сами по себе. Вам понадобится соответствующая терапия, чтобы помочь им разрешиться.
Что вызывает последствия ТИА?
Во время транзиторной ишемической атаки сгусток крови ограничивает или препятствует попаданию крови в определенные части мозга.Эти части мозга могут обходиться без необходимых ресурсов, таких как сахар и кислород, от минут до часов. После разрешения ТИА мозг не полностью возвращается в нормальное состояние. Исследования функциональной МРТ (фМРТ) показывают, что даже МРТ в состоянии покоя пациентов с ТИА является ненормальной. (Это означает, что их мозг не похож на нормальный здоровый мозг, даже когда он отдыхает от задач).
Этих минут или часов ограниченного кровотока во время ТИА может быть достаточно, чтобы вызвать дисфункциональную нервно-сосудистую связь, которая представляет собой отношения между вашими нейронами и кровеносными сосудами, которые их снабжают.
Короче говоря, нервно-сосудистая связь — это то, как нейроны получают кислород и другие питательные вещества, которые им необходимы для функционирования. Когда эти отношения нарушаются, часть мозга может начать задачу и не выполнить ее из-за нехватки ресурсов. Или это может потребовать большего кровоснабжения, чем нужно, лишив другие части мозга того, что им нужно. На изображениях мы видим эту дисфункцию как гиперактивные (слишком много или слишком много ресурсов) или гипоактивные (слишком мало) участки мозга.
Эта сигнальная дисфункция стоит за многими сохраняющимися симптомами после ТИА.
Но это еще не все. ТИА часто возникает глубоко в центре мозга. Кровь по сонным артериям поступает в мозг, а кровеносные сосуды все меньшего и меньшего размера направляются к определенным частям, таким как ветви деревьев.
После того, как закупорка разрушается, кусочки сгустка могут перемещаться по более мелким кровеносным сосудам (капиллярам), пока снова не застрянут на месте.В результате у вас может образоваться скопление клеток мозга, которые погибают, когда перестают получать свежий кислород.
На этом рисунке мы видим пациента до (A) и после (B) ТИА, вызвавшего небольшой кластер мертвых клеток головного мозга. Источник .
Если ТИА вызывает гибель каких-либо клеток мозга, это проявляется в виде маленьких белых точек на магнитно-резонансной томографии (МРТ) мозга, как показано выше. Нейрорадиолог может увидеть это пятно и отметить его как «неспецифический результат», потому что этот крошечный кластер мертвых клеток не убьет вас.Но помните, эти клетки что-то делали до вашего ТИА. И теперь какая-то другая часть мозга должна компенсировать погибшие клетки.
Чтобы оправиться от этого повреждения, нужно научить мозг направлять связь между поврежденными участками и восстановить здоровую нервно-сосудистую связь.
Сколько времени нужно, чтобы оправиться от транзиторной ишемической атаки?
Пациенты с ТИА обычно чувствуют себя лучше в течение нескольких дней или недель после события. Но если у вас сохраняются симптомы, трудно сказать, как будет выглядеть выздоровление.Это зависит от того, какие части вашего мозга повреждены, насколько хорошо ваш мозг учится обходить их и насколько хороша ваша программа лечения.
Тем не менее, мы твердо убеждены в том, что вы можете всегда продолжать выздоравливать, если вы работаете над этим, даже когда вы закончили терапию.
Где получить лечение затяжных симптомов после ТИА
Пациентам с сохраняющимися симптомами после ТИА необходима когнитивная и физиотерапия для достижения максимального прогресса.
Травма головного мозга никогда не бывает универсальной.Определенные области вашего мозга, на которые повлияла ТИА, не будут такими же, как у следующего пациента, который войдет в нашу клинику. Наличие одного стандартного варианта лечения приводит к плохим результатам для пациентов, поскольку не учитывает их уникальные потребности.
Вот почему мы используем функциональную нейрокогнитивную визуализацию (fNCI), особый тип fMRI, для всех наших пациентов. Он показывает нам , какие конкретные области мозга гиперактивны, а какие — гипоактивны. Затем мы можем адаптировать лечение пациентов, основываясь на их конкретных результатах сканирования , вместо того, чтобы связывать вместе несколько методов лечения и надеяться, что это сработает.
Взаимосвязанность мозга означает, что междисциплинарный подход к лечению является лучшим. Заманчиво найти терапевта, который займется только одной проблемой. Например, пациенты, которые замечают проблемы с памятью, найдут когнитивного терапевта и будут работать конкретно над памятью.
Но «память» — это больше, чем просто улучшение вашей способности вспоминать. Создание и сохранение памяти включает в себя другие процессы, такие как сенсорная обработка, внимание и исполнительные функции. Если на эти процессы повлияла травма головного мозга, то попытки «исправить» вашу память должны работать и с этими процессами.
Вот почему мы предлагаем комбинацию терапий, основанную на потребностях наших пациентов, включая нервно-мышечную терапию, когнитивную терапию, трудотерапию, сенсомоторную терапию и многое другое.
Подробнее о том, как выглядит неделя лечения, можно узнать здесь.
Примечание. Большинство пациентов, которых мы лечим, страдают постконтузионным синдромом, поэтому большинство наших онлайн-ресурсов написано специально для них. Многие из этих ресурсов также применимы к TIA. Причина в том, что, хотя сотрясения мозга являются наиболее частой причиной дисфункции нервно-сосудистой связи, они не единственная причина.Мы успешно лечили пациентов с ТИА, потому что симптомы вызывает та же проблема (проблемы с ННО). Неважно, как вы повредили свой мозг; Если ваши симптомы связаны с дисфункцией NVC, мы можем помочь.
Заключение
Да, сохраняющиеся симптомы возникают после ТИА. Да, ТИА иногда может приводить к образованию небольших скоплений мертвых клеток головного мозга. Но это не значит, что ваши симптомы постоянны. Даже пациенты с тяжелой черепно-мозговой травмой (ЧМТ) могут добиться значительного прогресса после травмы при хорошем лечении и настойчивости.
Пациенты с ТИА, которых мы лечим, часто значительно улучшают симптомы, потому что повреждение их мозга не является широко распространенным и необратимым.
Если вы хотите узнать, можем ли мы вам помочь, закажите бесплатную консультацию у нашей команды.






