Болезнь паркинсона лечится или нет: Болезнь Паркинсона – причины возникновения, признаки и симптомы, лечение болезни Паркинсона
Как болезнь Паркинсона вредит мозгу, почему сейчас ее не вылечить и что делать для профилактики? Рассказывает исследовательница заболевания
Почему ученые не могут понять, как возникает болезнь Паркинсона, можно ли ее унаследовать и когда может появиться первое эффективное лекарство от заболевания?
Сотрудница Института трансляционной биомедицины СПбГУ Наталия Католикова рассказывает о проблемах в изучении и лечении болезни Паркинсона.
— Болезнь Паркинсона относится к так называемым нейродегенеративным заболеваниям, для которых характерна постепенная гибель различных типов нейронов, что приводит к снижению или выпадению каких-либо функций центральной нервной системы. К этой же группе относится и болезнь Альцгеймера.
При болезни Паркинсона гибнут дофаминергические нейроны, вырабатывающие дофамин. Они в основном располагаются в среднем мозге (отделе головного мозга, отвечающим за многие его функции, в том числе зрение, слух и координацию движений — прим. «Бумаги») и относятся к системе базальных ганглиев (скоплений серого вещества, отвечающих за двигательные и вегетативные функции — прим. «Бумаги»), принимающих участие в регулировании движений, мотивации и системы подкрепления.
Из-за уменьшения количества дофамина именно эти функции мозга выпадают: появляется тремор, нарушается походка, мышцы становятся ригидными (находятся в постоянном напряжении — прим. «Бумаги»). В конечной стадии заболевания, когда дофамина становится катастрофически мало, люди, в отсутствие терапии, становятся очень малоподвижными, их даже называют «замороженными». При этом мыслительные способности при Паркинсоне как правило нарушаются в меньшей степени.
— Ранняя диагностика этой болезни — очень большая проблема. И поиск новых методов диагностики — одна из приоритетных задач, которые стоят перед исследователями. Сейчас диагноз ставится на основании клинических проявлений, а они появляются, только когда погибли уже около 80 % дофаминергических нейронов.
Также в постановке диагноза может помочь позитронно-эмиссионная томография (ПЭТ) головного мозга, но это достаточно дорогостоящая процедура и провести ее возможно не везде.
Первые проявления болезни бывают разные. Мне сложно сказать, какие симптомы станут первыми, поскольку я не работаю с пациентами, но, насколько я знаю, чаще всего поводом для обращения к врачу становится появление тремора рук и некоторая заторможенность пациентов. На остальные же симптомы больные обращают внимание уже после визита к врачу, когда им начинают задавать конкретные вопросы [о симптомах].
— Паркинсон — это болезнь пожилых людей. Около 1–2 % вероятность возникновения после 60 лет, до 3 % — после 80. Бывают и более ранние формы болезни, но они встречаются очень редко. У молодых людей возникновение болезни Паркинсона может быть связано с каким-то токсическим воздействием.
Развивается болезнь тоже очень по-разному. У кого-то быстро, у кого-то — на протяжении 20 лет. С чем это связано, пока не очень понятно. Скорее всего, с особенностями генетического бэкграунда каждого человека.
Говорить о причинах возникновения болезни Паркинсона сейчас очень сложно. Исследователи рассматривают генетические причины, но процент таких случаев очень небольшой, около 20 %. Есть некоторое количество генов, мутации в которых, предположительно, могут привести к болезни. Так что генетика в данном случае имеет влияние, но не прямое. Болезнь родственников, например, не повлияет на развитие Паркинсона.
То есть причины могут быть разными, но в целом науке сейчас неизвестно, что является непосредственной причиной болезни Паркинсона.
Многие заболевания, связанные с центральной нервной системой, сложны в расшифровке, потому что сама эта система очень сложно организована. Отсюда и проблемы с диагностикой и изучением причин развития болезни Паркинсона.
— На данный момент болезнь Паркинсона неизлечима, есть только симптоматическое лечение. Основной препарат для лечения болезни Паркинсона — L-DOPA. Это предшественник дофамина, который в мозге человека превращается в дофамин и на какое-то время восполняет его недостаток.
Помимо L-DOPA используются и другие препараты, которые влияют на дофаминергическую систему, а также препараты, убирающие некоторые симптомы болезни. Но в двух словах можно сказать, что суть лечения сводится к стимулированию дофаминергической системы, чтобы восполнять утраченные функции мозга.
Но в двух словах можно сказать, что суть лечения сводится к стимулированию дофаминергической системы, чтобы восполнять утраченные функции мозга.
Но у современного лечения есть много недостатков. Во-первых, лекарства не лечат саму болезнь, и она постоянно прогрессирует. Во-вторых, препараты не могут полностью заместить утраченные функции. В-третьих, прием L-DOPA приводит к развитию побочных эффектов, основной из которых — привыкание, необходимость постоянного увеличения дозы препарата.
Кроме того, возникает L-DOPA-индуцированная дискинезия — неконтролируемые движения, связанные с приемом препарата. Чем именно вызвана дискинезия, на данный момент неясно, и поэтому непонятно, как это можно лечить.
Современное лечение нельзя назвать достаточно эффективным. Но его всё равно нужно обязательно проходить: оно облегчает жизнь и на какое-то время позволяет вернуться к относительно нормальному состоянию и контролировать проявления болезни. Кому-то это лечение может помогать не один десяток лет.
— Сейчас есть большой интерес к заместительной клеточной терапии, то есть созданию определенного типа клеток, которые помогут замещать утраченные функции. Болезнь Паркинсона стала одним из первых направлений, где такое лечение уже дошло до клинических испытаний, проверки эффективности и безопасности препарата на людях.
Несколько клинических испытаний лечения от болезни Паркинсона уже начаты. Еще несколько должны начаться в конце 2019-го — начале 2020-го. В каждом случае используются разные источники дофаминергических нейронов. При этом надо отметить, что исследователи в разных частях мира не работают по-отдельности, пытаясь опередить друг друга, а объединились в сообщество, которое встречается раз в год и делится полученными результатами. Вместе они выявляют какие-либо сложности, особенности, новые подходы. Именно это и нужно для как можно более быстрого решения проблемы.
Первые испытания были начаты в прошлом году в Японии, и уже в ноябре 2018 года первому пациенту пересадили [необходимые клетки]. В Китае тоже начали клинические испытания, но я не знаю, на каком этапе они находятся. Также в ближайшее время должны быть начаты клинические испытания в Швеции и США. Надеюсь, что со временем подключится и Россия.
В Китае тоже начали клинические испытания, но я не знаю, на каком этапе они находятся. Также в ближайшее время должны быть начаты клинические испытания в Швеции и США. Надеюсь, что со временем подключится и Россия.
Результаты японских испытаний должны стать известны к 2023 году.
Специфической профилактики болезни Паркинсона нет. Но есть рекомендации по профилактике нейродегенеративных заболеваний в целом.
Сводятся эти рекомендации к ведению здорового образа жизни. Нужен нормальный режим работы, физическая активность: было доказано, что бег значительно снижает прогрессию таких заболеваний. Показана любая мелкая моторика и игра на музыкальных инструментах. Кроме того, здоровое питание. Некоторые наркотические вещества могут быть токсичными для дофаминергических нейронов, так что стоит избегать вредных привычек.
Как распознать болезнь Паркинсона на ранних стадиях?
До сих медицина не может дать определенного и четкого ответа на вопрос, когда и почему у человека начинает развиваться болезнь Паркинсона? В какой именно момент начинает происходить потеря производящих дофамин клеток в части мозга, отвечающей за тонкую моторику?Болезнь Паркинсона — причины, факторы развития
Причина дегенерации неизвестна, хотя среди небольшого процента пациентов можно определить генетическую связь. Некоторые ученые предполагают, что изменения в определенном гене являются решающим фактором появления и развития болезни. Как правило, заболевание начинается в возрасте около 50-60, но может проявиться и раньше. Различные исследования пытались найти связь между развитием болезни Паркинсона с экологическими факторами, такими как загрязнение химическими веществами. Другие полагали, что никотин может играть определенную роль, но серьезные доказательства так и не были найдены до сегодняшнего дня.Болезнь Паркинсона представляет собой прогрессирующее дегенеративное заболевание головного мозга, характеризующееся следующими клиническими признаками: дрожанием конечностей (тремор в состоянии покоя), жесткостью мышц и замедленностью движений.
Диагностика болезни Паркинсона
Самая главная проблема болезни Паркинсона в том, что признаки болезни долгое время остаются незаметными, болезнь развивается медленно, в течение многих лет человек не чувствует ничего подозрительного в своем состоянии и поведении. Клинические симптомы обычно становятся явными на очень поздних стадиях, когда более половины клеток черной субстанции мозга уже мертвы. Именно эти клетки играют важную роль в настройке моторной функции организма. Нервные клетки начинают умирать уже на ранних стадиях заболевания, процесс происходит постепенно, мозг может справляться с этой проблемой самостоятельно. Но с течением времени процесс гибели клеток ускоряется, и к моменту постановки диагноза, большая часть нейронов погибает. В такой ситуации медицина на нынешнем этапе ее развития может предложить только поддерживающую терапию. Диагностика болезни Паркинсона основывается на общей клинической картине, полученной после консультации с врачом-неврологом. Диагностические обследования – МРТ, УЗИ головного мозга – делаются, в основном для того, чтобы исключить другие патологии мозга, такие, как инсульт, опухоли.Специалисты неврологических отделений медицинских клиник Израиля говорят о том, что главный вопрос, стоящий сейчас, это найти оптимальные и эффективные методы обследования, которые могли бы решить проблему раннего выявления признаков заболевания. Это важно, потому что в начале развития дегенеративного процесса еще можно вмешаться и остановить гибель клеток.
Как распознать ранние признаки болезни и предрасположенность к ней?
- Можно заподозрить первые признаки, если заметить у близкого человека появившийся характерный жест потирания пальцами: большим и указательным пальцами он как будто считает мелкие монеты.

- Изменяется мимика лица – она становится беднее, более скованной.
- Может исчезнуть обоняние. Кстати, очень характерный признак для начала развития болезни Паркинсона, и повод для посещения невролога.
- Человеку трудно бывает подняться с места, начать какое-либо движение
- Человек может находиться в постоянном состоянии депрессии
Лечение болезни Паркинсона | Клиника китайской медицины ТАО
Заболевание, названное «дрожательный паралич» впервые в истории медицины было описано в 1817 году Паркинсоном, в связи с чем впоследствии и получило более известное современникам название «болезнь Паркинсона». К счастью, в мире таких пациентов не более 1%, однако это заболевание признают одним из самых проблематичных для пациентов старшей возрастной группы (дебют заболевания наступает в 60-65 лет, но вовсе не исключено его возникновение и у более молодых людей, как правило, трудоспособного и активного возраста). Читать полностьюБолезнь Паркинсона
Причины заболевания
В настоящее время достоверной информации о причинах возникновения болезни Паркинсона нет. Однако известно, что в основе заболевания – дегенерации нейронов головного мозга – лежат возрастные изменения нервных клеток (дегенерация меланин-содержащих нейронов и нарушение функции рецепторов к дофамину). Общепризнано, что наличие болезни Паркинсона у ближайших родственников повышает риск ее возникновения примерно в два раза, но все же наиболее часто болезнь возникает спорадически, то есть без генетической обусловленности.
Исследования пациентов, страдающих болезнью Паркинсона, показывают ряд специфических признаков: дефицит синтеза дофамина, избыток возбуждающего нейромедиатора ацетилхолина при значительном сокращении синтеза норадреналина и серотонина. Все эти вещества в сбалансированном состоянии играют важную роль в процессах возбуждения и передачи информации по нейронам головного мозга.
Симптомы заболевания
На первый план в клинической картине болезни Паркинсона выходят двигательные нарушения, причем симптомы нарастают постепенно, затрагивая сначала одну конечность. Пациенты отмечают снижение двигательной активности, в том числе, замедленность привычных действий. С дальнейшим развитием патологического процесса симптомы усиливаются: пациент с большим трудом встает со стула и поворачивается с боку на бок, при ходьбе занимает вынужденное сутулое положение, прижав к туловищу согнутые в локтях руки (симптом носит название «поза просителя»), также отмечается шаркающая походка, замедление темпа ходьбы. Наиболее узнаваемым признаком заболевания является дрожание (тремор) пальцев рук, возникающий в покое. Чуть позже тремор охватывает и ноги, нижнюю челюсть. Если вовремя не принять адекватные меры, формируется симптом пошатывания при ходьбе, пациент часто падает, нуждается в дополнительной опоре. Со стороны мышечной системы наблюдается усиление тонуса мускулатуры. В абсолютном большинстве случаев заболевание сопровождается возникновением депрессивного состояния, когнитивными расстройствами (ухудшение памяти, восприятия информации), неврозами. В процесс вовлечена и вегетативная нервная система, что проявляется резким снижением артериального давления во время смены положения (ортостатическая гипотензия), запорами, неконтролируемым слюнотечением, нарушением мочеиспускания, иногда – болевой симптоматикой.
Немало проблем доставляет пациенту угнетение автоматических рефлексов. Такие привычные и даже почти незаметные для здорового человека действия, как моргание, улыбка человеку с болезнью Паркинсона практически недоступны. В случаях значительной степени поражения можно наблюдать застывшую мимику лица с немигающим взглядом. В ряде случаев страдает речь — голос становится тихим, исчезают интонации и четкость произношения слов, что также связано с нарушениями со стороны мышц и нервной системы.
Для заболевания характерно прогрессирование, при этом темпы динамики развития болезни зависят от возраста пациента, когда патология манифестировала, клинической формы, исходного статуса организма, своевременности и эффективности назначенного лечения. В настоящее время принято выделять три основных темпа прогрессирования этой болезни. Быстрый темп предполагает смену клинических стадий всего на протяжении двух лет, а иногда и менее. Развитие в умеренном темпе происходит в течение 3-5 лет. Медленный темп предполагает нарастание симптоматики за 5 и более лет.
Лечение болезни Паркинсона
В традиционной европейской медицине применяют группу противопаркинсонических фармакологических препаратов, комплекс лечебной физкультуры и по показаниям — нейрохирургическое вмешательство. Цель такой терапии состоит в коррекции симптомов, реабилитации пациента, что имеет колоссальное значение как для самого пациента, так и для его социальной адаптации.
У специалистов китайской медицины собственный взгляд на эту проблему. В древних трактатах симптомы, сходные с болезнью Паркинсона, описывают в связи с ослаблением энергии Инь почек и печени и накоплением внутреннего «ветра». Именно поэтому, подбирая больному индивидуальную схему лечения, врачи клиники «ТАО», учитывают необходимость дополнительного питания энергии почек и печени (для этого используются фитопрепараты) и успокоение возникшего синдрома «ветра», для чего применяют массаж, иглоукалывание. Результатом применения такого комплекса становится быстрая и эффективная реабилитация пациентов, существенное улучшение качества их жизни.
Результатом применения такого комплекса становится быстрая и эффективная реабилитация пациентов, существенное улучшение качества их жизни.
На первом приеме специалисты клиники китайской медицины «ТАО» проведут бесплатную пульсовую диагностику и дадут полноценную консультацию по нюансам лечения, восстановления пациентов и профилактики рецидивов.
Новосибирские ученые подобрали вещество для лечения болезни Паркинсона
Ученые Новосибирского института органической химии имени Ворожцова (НИОХ) подобрали вещество, восстанавливающее поврежденные болезнью Паркинсона нейроны.
«Нами обнаружен новый класс веществ, которые не только устраняют симптомы болезни Паркинсона, но и способствуют регенерации нейронов», — сообщил главный научный сотрудник НИОХ Константин Волчо на симпозиуме «Генные и клеточные технологии в моделировании и терапии заболеваний человека».
Он отметил, что ранее в НИОХ было синтезировано вещество, восстанавливающее двигательную активность у животных, у которых была искусственно вызвана болезнь Паркинсона с помощью особого нейротоксина. В настоящее время доклинические исследования успешно завершены, однако этот препарат воздействует на симптомы, не восстанавливая поврежденную нервную ткань.
В дальнейшем были синтезированы производные этого вещества, причем некоторые из них существенно превосходят исходный препарат.
«По сути, мы нашли целый класс антипаркинсонических агентов», — сказал ученый.
Одно из производных, как установлено в ходе экспериментов, поддерживало выживаемость нейронов, не влияя при этом на рост других тканей, что снимает проблему онкологии.
Пока что результат подтвержден на клетках и на мышах. «Оказалось, что нами достигнут полный успех, нейроны, которые поражаются токсином, практически полностью восстановились. Это означает, что появляется надежда не только на симптоматическую, но и реальную терапию болезни Паркинсона с восстановлением нейронов», — отметил Константин Волчо.
По его словам, продолжение экспериментов на обезьянах сталкивается с финансовыми и этическими ограничениями. При этом не факт, что соединение, эффективное для мышей, подействует на приматов, подчеркнул специалист.
Выходом могли бы стать испытания на клеточных линиях людей, страдающих паркинсонизмом, и создание «библиотеки» соединений, эффективных против заболевания, считает Константин Волчо.
Пациентам с болезнью Паркинсона устанавливают стимуляторы в тюменском ФЦН
Общество, 13:17 06 ноября 2019
Версия для печати
| Фото: Федеральный центр нейрохирургии во ВКонтактеДо 60 электростимуляторов в год устанавливают пациентам при прогрессирующей болезни Паркинсона в Федеральном центре нейрохирургии в Тюмени. Очередь людей, которым показана установка прибора, на 2020 год уже сформирована, сообщает центр.
Первые симптомы заболевания у пациентки из Кургана появились в 2008 году, стала чувствовать слабость в левой руке и ноге. Правильный диагноз врачи смогли поставить через полгода. Болезнь прогрессировала, настал момент, когда консервативное лечение перестало помогать, требовались другие методы. В 2015 году Светлану направили в Федеральный центр нейрохирургии в Тюмени. После тестирования и обследования ей провели операцию и установили систему глубинной стимуляции головного мозга.
«Уникальность этого случая в том, что не все пациенты с болезнью Паркинсона могут вернуться к нормальному образу жизни. Наша пациентка после установки электростимулятора снова вышла на работу, вернулась к своим привычкам. За четыре года стимулятор выработал свой ресурс, его нужно было заменить на новый. Мы провели еще одну операцию и установили аппарат, который прослужит 10 лет», — рассказал врач-нейрохирург, к.м.н., заведующий нейрохирургическим отделением Федерального центра нейрохирургии в Тюмени Александр Орлов.
Он пояснил, что отбор пациентов на операции по установке стимуляторов проводится тщательно. Если пациенту предложить операцию на первых этапах заболевания, он не ощутит изменений. Оперативное вмешательство планируется только тогда, когда от консервативного лечения эффекта уже нет, появляются побочные явления от лекарственных препаратов. Как правило, такие пациенты уже на инвалидности, у них возникают проблемы в быту и общении.
«Я конечно счастлива, когда все возвращается в норму. Радуюсь и забываю о болезни, — признается Светлана, — у меня ответственная работа, я экономист, есть семья. Спасибо врачам, что помогли снова вернуться к нормальной жизни».
Во время общения Светлана держит в руках дистанционку, так называемый пульт пациента, который позволяет переводить стимулятор с одной программы на другую: сон, бодрствование. За несколько лет пациентка приноровилась жить со стимулятором и не испытывает сложностей. Как только прибор отключается, все симптомы болезни Паркинсона возвращаются мгновенно.
Первую операцию по установке прибора в ФЦН провели в 2012 году, а в год в Федеральном центре нейрохирургии таких аппаратов устанавливают до 60. На 2020 год сформирована очередь для пациентов, которым показана их установка. Стимулятор и операция по его установке дорогостоящие, на это выделяются средства из федерального бюджета по квоте.
Электростимулятор при болезни Паркинсона используется для уменьшения выраженности симптомов.
«Эффект от таких операций очевиден. Методики, которыми владеют врачи нашего центра, направлены на малую травматизацию организма. При использовании метода по установке стимулятора не нужно целенаправленно уничтожать определенный участок мозга, что снижает вероятность развития осложнений», — отметил врач-нейрохирург, д.м.н., профессор, заслуженный врач РФ, заведующий Федеральным центром нейрохирургии в Тюмени Альберт Суфианов.
Лечение болезни Паркинсона | MediGlobus
Альбина Головина Работает в сфере медицинского копирайтинга 2 года. Учится на аспирантуре факультета психологии. Автор нескольких научных публикаций в области клинической психологии. Дополнительно изучает физиологию ЦНС, нейропсихологию и психиатрию. В свободное время изучает практики mindfulness и проводит психологические консультации.
Учится на аспирантуре факультета психологии. Автор нескольких научных публикаций в области клинической психологии. Дополнительно изучает физиологию ЦНС, нейропсихологию и психиатрию. В свободное время изучает практики mindfulness и проводит психологические консультации.
Что объединяет художника Сальвадора Дали, актера Майкла Джей Фокса, боксера Мохаммеда Али, музыканта Оззи Осборна и Папу Римского Иоанна Павла II? Врачебный диагноз. Все они наряду с ещё 10-ю миллионами людей по всему миру страдают от болезни Паркинсона. Коротко о заболевании и подробно о его сложном лечении — читайте прямо сейчас в новом материале MediGlobus.
Болезнь Паркинсона: причины, симптомы, признаки
Болезнь Паркинсона – это хроническое медленно прогрессирующее заболевание нервной системы, при котором у человека страдают функции движения. Впервые об этой болезни упоминается в 175 году н.э. Древнеримский врач Гален посвятил ей работу «О дрожании, пульсации, конвульсиях и треморе», в которой описал симптомы заболевания и предполагаемое лечение. Первое исследование болезни провел английский врач Джеймс Паркинсон в 1817 году. Оно легло в основу его «Эссе о дрожательном параличе», а фамилия доктора – в название заболевания.
В наши дни — болезнь Паркинсона является 2-м по распространенности возрастным неврологическим заболеванием после Альцгеймера и одной из самых загадочных патологий. Причины возникновения болезни Паркинсона до сих пор изучаются, а методы лечения совершенствуются.
Причины болезни Паркинсона: новое исследование
Согласно американскому порталу Parkinson.org современные исследования сосредоточены на попытке определить и найти гены (или комбинацию генов), которые приводят к болезни Паркинсона. На сегодняшний день обнаружены мутации в 4-х генах, которые напрямую связаны с заболеванием. Исследователи выявили, что эти мутации приводят к гибели дофаминовых нейронов.
Дофамин — это не только гормон счастья. Он также является нейромедиатором и отвечает за двигательную активность человека. Потеря 70-80% нейронов, которые высвобождают дофамин, приводит к нарушению движения и дрожи в конечностях.
Он также является нейромедиатором и отвечает за двигательную активность человека. Потеря 70-80% нейронов, которые высвобождают дофамин, приводит к нарушению движения и дрожи в конечностях.
По информации новостного сайта Рarkinsonsnewstoday от 2 мая 2018 года, в журнале «Neurology» появилось описание последнего исследования заболевания «Mild TBI and risk of Parkinson disease/A Chronic Effects of Neurotrauma Consortium Study». Его результаты гласят, что черепно-мозговые травмы, в частности, сотрясение мозга, может на 50% увеличить риск возникновения у человека болезни Паркинсона.
Симптомы болезни Паркинсона
Первым симптомом заболевания является дрожь одной руки в состоянии покоя. Человек зачастую не придает значения легкому тремору, списывая его на переутомление, личные переживания, излишнюю эмоциональность.
Болезнь Паркинсона развивается медленно, впоследствии начинают дрожать обе руки и голова. Когда человека что-то волнует, тремор становится сильнее, в то время как при обыденных делах он может вовсе сходить на нет.
Признаки болезни Паркинсона
Зачастую заболевание диагностируют у мужчин старше 60-ти лет. Женщин болезнь Паркинсона поражает в 1,5 раза реже. На первых порах недуг протекает практически бессимптомно. По мере развития болезни начинают появляться его явные признаки.
Основные признаки болезни Паркинсона:
Методы лечения болезни Паркинсона
Лечение болезни Паркинсона новым методом RANC
Одним из современных методов лечения этого неврологического заболевания является RANC (The Restoration Of The Activity Of Nerve Centers). Его главная цель — восстановление активности нервных центров. После курса RANC-процедур к пациенту может контролировать собственные движения, дрожь в конечностях становится меньше и в конце концов исчезает.
Автор метода RANC — российский невролог А. А. Пономаренко. Он предполагает, что дофаминовые нейроны (те самые, которые отвечают за двигательные функции человека) не гибнут, а лишь максимально снижают свою активность под воздействием определенных факторов и от этого перестают выполнять свои функции.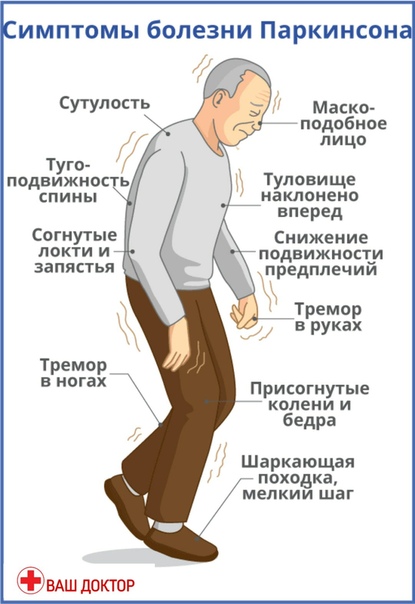
Лечение болезни Паркинсона методом RANC предполагает введение больному инъекций 5% АНАЛЬГИНа во все болезненные участки трапециевидных мышц, так как они соответствуют участкам головного мозга с нарушенными функциями. Короткая боль от процедуры запускает в мозге процесс, который перезапускает работу дофаминовых нейронов и они возобновляют выработку дофамина.
Новый RANC метод быстро стал ходовым в лечении болезни Паркинсона в России, так как показывает хорошие результаты за короткий срок — зачастую больным назначают 2-3 процедуры в течение 6 недель.
Медикаментозное лечение болезни Паркинсона
Как мы уже говорили, «дрожательный паралич» вызывает нехватка дофамина в головном мозге. Следовательно, лекарственные препараты направлены на имитацию функций этого нейромедиатора. Дофаминергические препараты помогают снизить тонус мышц, улучшить координацию движений, уменьшить тремор головы и конечностей. Наиболее распространенными препаратами для лечения болезни Паркинсона являются:
Хирургическое лечение болезни Паркинсона
Когда заболевание стремительно прогрессирует и больному становится сложно двигаться, разговаривать, работать и жить полноценной жизнью, специалист обсуждает с ним возможность проведения оперативного вмешательства. Наиболее современный хирургический метод лечения болезни Паркинсона — глубокая стимуляция головного мозга (DBS). Процедура предполагает введение в головной мозг специальных электродов, которые создают электрические импульсы.
Стимуляция электрическими импульсами участков головного мозга с нарушенными функциями избавляет пациента от тремора (дрожания конечностей), возвращает ему контроль над телом и эмоциями. Эту операцию можно пройти в большинстве ведущих медцентров. При этом иностранные пациенты отдают предпочтение таким учреждениям, как: клиника Текнон в Испании, медицинский центр им. Сураски (Ихилов) в Израиле, клиника Лив Хоспитал в Турции, госпиталь при университете СунЧонХян в Южной Корее, университетская клиника Мюнхена им. Людвига-Максимилиана в Германии, больница Мотол в Чехии и т.д.
Людвига-Максимилиана в Германии, больница Мотол в Чехии и т.д.
Болезнь Паркинсона — шансы на излечение
Несмотря на существование эффективных современных методов лечения болезни Паркинсона, на сегодняшний день заболевание все еще нельзя вылечить на все 100%. Правильно подобранное лечение позволяет улучшить качество жизни больного, вернуть ему возможность контролировать движения, речь, эмоции.
Помните, болезнь Паркинсона — больше не «дрожательный паралич». Да, это сложное и загадочное неврологическое заболевание. Но оно поддается лечению. Новые методы лечения болезни Паркинсона помогают устранить симптомы недуга на длительное время и вернуть больному радость жизни.
Больше информации о лечении болезни Паркинсона за границей можно узнать, обратившись к специалистам нашей компании. Врачи-координаторы ответят на все Ваши вопросы, сориентируют по стоимости и помогут с организацией медицинской поездки. Будьте здоровы — будьте с MediGlobus.
Получить бесплатную консультацию
Альбина Головина
Работает в сфере медицинского копирайтинга 2 года. Учится на аспирантуре факультета психологии. Автор нескольких научных публикаций в области клинической психологии. Дополнительно изучает физиологию ЦНС, нейропсихологию и психиатрию. В свободное время изучает практики mindfulness и проводит психологические консультации.
Доктор Вадим БережнойОснователь платформы MediGlobus. Медицинский эксперт, Заведующий отделением врачей-координаторов.
Похожие посты
О диагностике и лечении неврита лицевого нерва — какую клинику выбрать и сколько это стоит
Читать дальшеЛЕЧЕНИЕ НЕЙРОФИБРОМАТОЗА ЗА РУБЕЖОМ — ОПЕРАЦИЯ, ПРОГНОЗЫ ВРАЧЕЙ, КЛИНИКИ
Читать дальшеБолезнь Паркинсона (вторичный паркинсонизм) | Неврология
Что такое паркинсонизм.
 Лечение болезни Паркинсона в Липецке.
Лечение болезни Паркинсона в Липецке.Термин паркинсонизм используется для обозначения любого синдрома, при котором наблюдается неврологическое нарушение произвольных движений человека (дрожание конечностей, скованность мышц, замедление действий и общее снижение активности, а также неустойчивое равновесие).
Различают первичный (идиопатический) паркинсонизм или болезнь Паркинсона, которая вызывается инволюционным хроническим прогрессирующим разрушением и гибелью особых клеток центральной нервной системы (дофаминовых нейронов).
Вторичный паркинсонизм вызывается различными инфекциями, избыточным приемом лекарственных препаратов, черепно-мозговыми травмами.
Симптомы паркинсонизма
- Непроизвольное дрожание конечностей – один из наиболее ярких симптомов паркинсонизма. Во время произвольного движения тремор исчезает и появляется снова при двигательной пассивности больного.
- Скованность мышц обусловлено повышенным мышечным тонусом скелетной мускулатуры.
- Характерна для паркинсонизма «поза просителя», вызванная изменением рефлексов, отвечающих за вертикальность положения тела.
- Дополнительными симптомами паркинсонизма замедленность движений, обеднение мимики, нарушения равновесия.
Диагностика паркинсонизма
Симптомы заболевания проявляются уже при гибели значительных количества двигательных нейронов. На этой стадии заболевания постановка диагноза уже не вызывает сложностей.
Возможности МРТ Клиники «Андромемда» позволят выявить внутреннюю и наружную атрофию вещества мозга, в том числе в зоне базальных ганглиев, сопутствующие очаговые изменения, а также обнаружить снижение сигнала в области базальных ганглиев.
Для уточнения диагноза и подбора схемы лечения необходимо обратиться к врачу неврологу.
вариантов лечения болезни Паркинсона | Johns Hopkins Medicine
Специфическое лечение болезни Паркинсона будет назначено вашим врачом на основании:
Ваш возраст, общее состояние здоровья и история болезни
Степень условия
Тип состояния
Ваша переносимость определенных лекарств, процедур или методов лечения
Ожидания по ходу состояния
Ваше мнение или предпочтение
При сегодняшней медицине нам еще предстоит найти лекарство от болезни Паркинсона.Однако, исходя из тяжести симптомов и медицинского профиля, врач разработает соответствующий протокол лечения. Лечение болезни Паркинсона может включать следующее:
Лекарства
Хирургия
Дополнительные и поддерживающие методы лечения, такие как диета, упражнения, физиотерапия, трудотерапия и логопедия
[6 безлекарственных способов улучшить самочувствие при болезни Паркинсона]
Лекарство от болезни Паркинсона
После того, как врач диагностирует болезнь Паркинсона, следующее решение заключается в том, следует ли пациенту принимать лекарства, что зависит от следующего:
Степень функционального нарушения
Степень когнитивных нарушений
Способность переносить противопаркинсонические препараты
Консультация лечащего врача
Нет двух пациентов, которые одинаково реагируют на то или иное лекарство, поэтому требуется время и терпение, чтобы найти подходящее лекарство и дозировку для облегчения симптомов.
[Физическая терапия болезни Паркинсона]
Хирургия болезни Паркинсона
В зависимости от тяжести состояния и медицинского профиля врач может порекомендовать операцию в качестве одного из вариантов лечения болезни Паркинсона.
Существует несколько типов хирургических вмешательств, которые могут помочь пациентам с болезнью Паркинсона. Большинство методов лечения направлено на уменьшение тремора или ригидности, которые возникают при болезни. У некоторых пациентов хирургическое вмешательство может уменьшить количество лекарств, необходимых для контроля симптомов.
Есть три типа операций, которые могут быть выполнены при болезни Паркинсона, включая следующие:
Хирургия повреждений (ожог тканей). В этой процедуре нацелены на глубокие части мозга и небольшие повреждения в критических частях мозга, которые помогают контролировать движение. Операция может быть сделана, пока пациент не спит, чтобы определить точное расположение поражения. Повреждение помещается, чтобы помочь контролировать или остановить область мозга, вызывающую тремор.
Глубокая стимуляция мозга (DBS). При этом типе хирургии небольшой электрод помещается в критически важные части мозга, которые помогают контролировать движение. Электрод прикреплен к небольшой батарее в грудной стенке и соединен проводами, которые помещаются под кожу. Затем включается стимулятор, который прерывает нормальный поток информации в головном мозге и может помочь уменьшить симптомы болезни Паркинсона.
Нервная трансплантация или трансплантация тканей. Проводятся экспериментальные исследования, чтобы найти замену той части мозга, которая неправильно функционирует при болезни Паркинсона.
Важно помнить, что операция может помочь при симптомах болезни Паркинсона, но не излечивает болезнь и не останавливает ее прогрессирование.
Немедикаментозное лечение болезни Паркинсона
Лечение болезни Паркинсона
Болезнь Паркинсона — это заболевание головного мозга, которое вызывает дрожь, скованность и проблемы с равновесием и координацией.По данным Фонда Паркинсона, почти 60 000 американцев ежегодно диагностируются.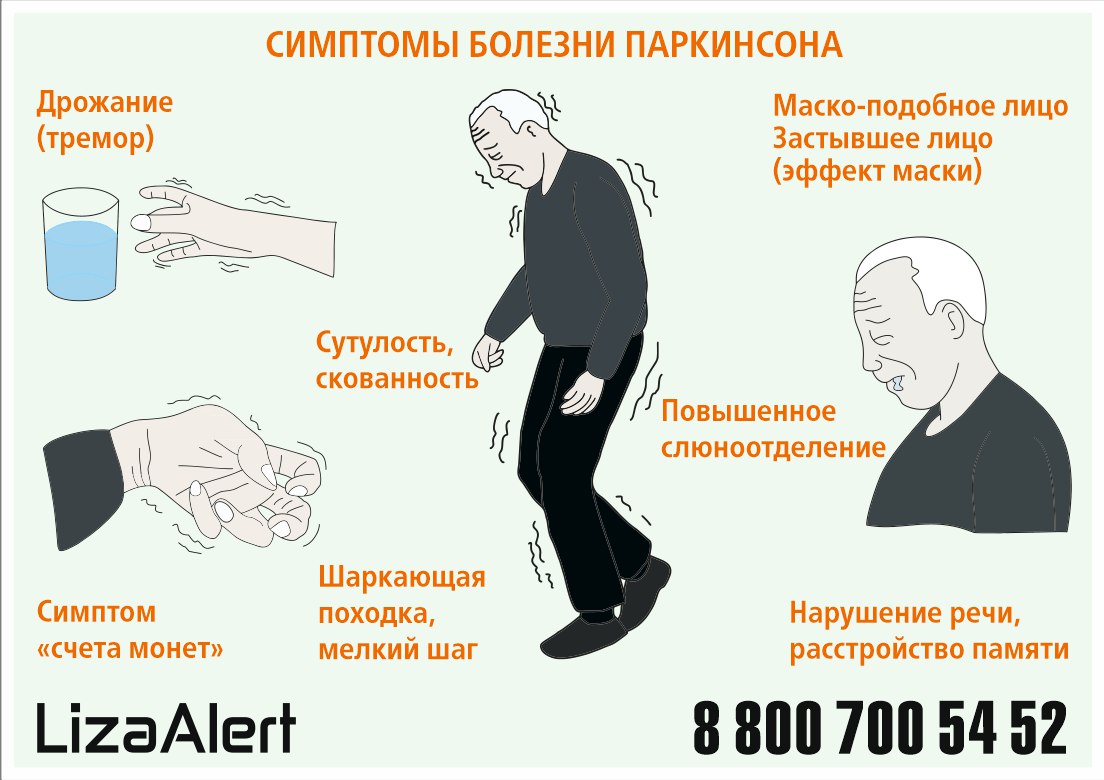 Лекарства от болезни Паркинсона нет, но существует лечение, помогающее уменьшить симптомы.
Лекарства от болезни Паркинсона нет, но существует лечение, помогающее уменьшить симптомы.
Каковы основные симптомы болезни Паркинсона?
Болезнь Паркинсона возникает, когда нервные клетки, контролирующие движения в головном и спинном мозге, повреждаются и умирают. Заболевание медленно развивается с годами. Симптомы обычно начинаются на одной стороне тела. По мере прогрессирования болезни симптомы будут влиять на обе стороны.Симптомы болезни Паркинсона могут включать:
- Непроизвольная дрожь в руках, руках, ногах, челюсти и лице
- Скованность или скованность в руках или ногах
- Замедление движений
- Плохое равновесие и координация
- Тихая или медленная речь
- На поздних стадиях слабоумие также может наблюдаться
Как диагностируется болезнь Паркинсона?
Не существует анализов крови или изображений, которые могли бы проверить на болезнь Паркинсона.Вместо этого ваш врач спросит о вашей истории болезни и симптомах, которые вы испытываете. Он или она также проведет физическое и неврологическое обследование. Это будет включать проверку вашего слуха, зрения, рефлексов, равновесия, силы, памяти и концентрации.
Симптомы болезни Паркинсона аналогичны некоторым другим неврологическим состояниям. Ваш врач может назначить анализы крови или сканирование, чтобы исключить другие причины. Он или она может также прописать лекарства от болезни Паркинсона и посмотреть, помогает ли оно вашим симптомам.Если это так, это будет означать, что ваши симптомы вызваны болезнью Паркинсона.
Нужен терапевт? См. Список врачей PHH.Как лечится болезнь Паркинсона?
В настоящее время нет лекарства от болезни Паркинсона. Однако существуют методы лечения, которые эффективно контролируют симптомы и замедляют прогрессирование заболевания. Как правило, лекарства работают очень хорошо, особенно на ранних стадиях заболевания. В конце концов, операция — особенно глубокая стимуляция мозга — может быть рекомендована, если лекарства перестают контролировать ваши симптомы.
Изменение образа жизни также может помочь справиться с симптомами. Ваш врач может порекомендовать постоянные аэробные упражнения, амбулаторную физиотерапию, которая концентрируется на тренировке равновесия и растяжке, логопедию, включая специальную программу под названием LSVT, и трудотерапию.
Реабилитационный центр Penn Highlands Healthcare предлагает специальную терапевтическую программу для людей с болезнью Паркинсона и другими неврологическими заболеваниями. Он включает амбулаторную физиотерапию, логопед и трудотерапию.Мы также предлагаем LSVT LOUD и LSVT BIG при болезни Паркинсона.
LSVT Loud и LSVT Big для пациентов с болезнью Паркинсона
Голосовое лечение Ли Сильвермана, или LSVT, представляет собой интенсивный протокол лечения, помогающий замедлить снижение двигательных и речевых навыков у пациентов с болезнью Паркинсона. Существует два типа LSVT-терапии: LSVT LOUD и LSVT BIG. Мы предлагаем и то, и другое в Реабилитационном центре Penn Highlands Healthcare.
Программы LSVT специально разработаны для лечения симптомов болезни Паркинсона.Пациенты с болезнью Паркинсона, которые начинают говорить тише или медленнее, могут получить пользу от LSVT LOUD, при котором используются вокальные упражнения, помогающие им говорить громче и яснее. LSVT BIG помогает решить проблемы с походкой и движением с помощью амбулаторной физиотерапии и трудотерапии, чтобы помочь пациентам иметь более плавные и безопасные движения.
LSVT доступен по телефону:
• Реабилитационный центр в Penn Highlands Clearfield предлагает как LSVT BIG, так и LSVT LOUD. Для получения информации позвоните 814-768-2285.
• Реабилитационный центр в Penn Highlands Elk предлагает LSVT LOUD.Для получения информации позвоните 814-788-8490.
Познакомьтесь с Мусом, пациентом LSVT
com/embed/NHzxtlwKav8″/>Группы поддержки Паркинсона
Диагноз болезни Паркинсона может сказаться на вашем психическом состоянии, особенно если симптомы ухудшают качество вашей жизни. Penn Highlands предлагает две группы поддержки болезни Паркинсона — одну в Дюбуа и одну в Клирфилде. Эти группы открыты для людей, у которых была диагностирована болезнь Паркинсона, а также для членов их семей. Обе группы поддержки предоставляют пациентам и их семьям безопасное место для обсуждения своих проблем, получения поддержки от других и обмена советами по борьбе с болезнью.предназначены для того, чтобы дать пациентам и членам их семей возможность поговорить и помочь им научиться справляться с болезнью Паркинсона.
Руководство по симптомам, стадиям и лечению болезни Паркинсона | Обновлено на 2021 год
Симптомы и признаки болезни Паркинсона
Трудно напрямую диагностировать болезнь Паркинсона. Не существует специальных тестов, которые врачи могут провести для подтверждения диагноза, поэтому важно, чтобы исследования продолжали определять постоянно развивающееся определение болезни Паркинсона.Помимо выявления многих из этих симптомов, врачи также исследуют семейный анамнез и проведут общее обследование мозга, чтобы официально поставить диагноз.
Частота появления этих симптомов варьируется в зависимости от человека, и нет определенного количества времени, которое вы гарантированно проживете после постановки диагноза. Он может быстро развиться или вы можете прожить 30 лет, прежде чем начнется самое тяжелое заболевание. Хотя сам Паркинсон определил шесть основных качеств болезни, когда он впервые подробно описал ее, симптомы болезни Паркинсона со временем развились.Они включают, но не ограничиваются полностью, следующее:
- Медлительность движений : Это определяется как неспособность двигаться так быстро, как обычно, при этом мышцы движутся медленнее в координации друг с другом. В мире медицины он известен как «брадикинезия» и является одним из определяющих симптомов болезни Паркинсона.
 Исследователи объясняют, что болезнь заставляет мозг вырабатывать меньше клеток головного мозга определенного типа (базальных ганглиев), которые помогают части головного мозга приказывать нам двигать мышцами.Замедленность движений может проявляться во многих формах (которые мы вскоре обсудим), а брадикинезия может вынудить больных тратить больше времени на выполнение рутинных действий и в конечном итоге потерять координацию.
Исследователи объясняют, что болезнь заставляет мозг вырабатывать меньше клеток головного мозга определенного типа (базальных ганглиев), которые помогают части головного мозга приказывать нам двигать мышцами.Замедленность движений может проявляться во многих формах (которые мы вскоре обсудим), а брадикинезия может вынудить больных тратить больше времени на выполнение рутинных действий и в конечном итоге потерять координацию. - Снижение мимики : По мере прогрессирования болезни Паркинсона вы можете обнаружить, что лицо пациента со временем становится менее выразительным. Кто-то, кто раньше часто улыбался или хмурился, может быть не в состоянии показать выражение так сильно, как раньше. Это состояние, известное как «гипомимия», имеет некоторую связь с брадикинезией.Пациенты могут быть не в состоянии выражать эмоции и мимику так хорошо, как раньше, просто потому, что их тело не позволяет им быстро улыбаться, изгибать брови, хмуриться или задействовать какие-либо лицевые мышцы в конкретный момент. Кажется, будто человек с болезнью носит постоянную маску, скрывающую его реакционные эмоции — вы не сможете сказать, как он себя чувствует, если он это не произнесет.
- Тремор : Официально известный как дискинезия, тремор определяется Национальным институтом здравоохранения как «непроизвольное ритмичное сокращение мышц, приводящее к дрожащим движениям в одной или нескольких частях тела».Эти сокращения могут быть постоянными или происходить в случайное время, и они не у всех, страдающих болезнью Паркинсона. Этот тремор чаще всего возникает в кистях, руках, ногах и в области головы / шеи. Хотя врачи не могут в явной форме объяснить, почему у пациентов с болезнью Паркинсона возникает тремор (исследования показали, что этому может способствовать недостаток определенных химических веществ в мозге), было обнаружено, что тремор является побочным эффектом людей, принимающих леводопу — лекарство, используемое для лечения болезни Паркинсона.
- Неустойчивое равновесие : На более поздних стадиях болезни Паркинсона ваше равновесие может начать теряться, что может повлиять на основные действия, такие как ходьба, надевание одежды и купание.
 Как и уменьшение выражений лица, неустойчивый баланс частично связан с брадикинезией, поскольку неспособность вашего тела двигать мускулами так быстро при реакции на определенные движения может вызвать падения и общую нестабильность. Неустойчивое равновесие — и попытки чрезмерной компенсации, наклоняясь или наклоняясь определенным образом, чтобы предотвратить постоянные падения, — могут привести к неправильной осанке. Многие из этих симптомов взаимосвязаны, так как один может вызвать цепную реакцию, вызывая другие.
Как и уменьшение выражений лица, неустойчивый баланс частично связан с брадикинезией, поскольку неспособность вашего тела двигать мускулами так быстро при реакции на определенные движения может вызвать падения и общую нестабильность. Неустойчивое равновесие — и попытки чрезмерной компенсации, наклоняясь или наклоняясь определенным образом, чтобы предотвратить постоянные падения, — могут привести к неправильной осанке. Многие из этих симптомов взаимосвязаны, так как один может вызвать цепную реакцию, вызывая другие. - Монотонный голосовой тон / тихая речь : Ваше лицо может стать менее выразительным, так же как и ваш голос, потому что мышцы, окружающие ваши губы и шею, предоставляют меньше возможностей для выражения громким и изменчивым голосом.(В медицине это известно как «дизартрия».) Из-за этого врачам становится сложнее лечить пациентов, а лицам, осуществляющим уход, понимать потребности пациента. Как и брадикинезия, нарушения речи возникают в результате заболевания, поражающего ту часть мозга, которая отвечает за гладкую моторику, например речь. То, как человек с болезнью Паркинсона говорит, не ограничивается медленным монотонным тоном. Возможно, что у пациента может быть быстрая речь, что также затрудняет понимание. В целом, пациенты с болезнью Паркинсона с трудом поддерживают разговоры из-за всех этих эффектов.
- Снижение способности сгибаться (ригидность) : По мере прогрессирования болезни вам может быть труднее сгибать руки, ноги и спину, что делает ваши движения в целом менее плавными. Это может затруднить одевание, встать и встать с постели, переворачиваться в постели, ходить в плавном темпе и выполнять другие повседневные дела. В целом, болезнь Паркинсона вызывает спазмы и боли в мышцах на постоянной основе. Хотя этот симптом до конца не изучен, исследователи полагают, что он вызван резким снижением дофамина — химического вещества, которое помогает клеткам мозга и нервам оставаться связанными — у пациентов с болезнью Паркинсона.
 У людей, страдающих этим заболеванием, дофамина на 60-80 процентов меньше, чем у среднего человека.
У людей, страдающих этим заболеванием, дофамина на 60-80 процентов меньше, чем у среднего человека. - Шаркающая походка : На походку человека — плавность его ходьбы — может влиять болезнь Паркинсона. Хотя это часто бывает временным, пациенты сообщают, что им кажется, что их ноги приклеиваются к полу, когда они пытаются переместить их. И когда их ноги действительно двигаются, это больше похоже на шарканье, чем на то, чтобы поднимать одну ногу и ставить ее перед другой. Как и многие другие симптомы, это вызвано повреждением части мозга, которая способствует плавности двигательных движений.Если человек с болезнью Паркинсона не шаркает ногами, его шаги могут быть короче при более быстрой ходьбе. Все это может происходить при чрезмерной компенсации плохого равновесия, что может сделать ходьбу чрезвычайно трудной и болезненной.
Приводит ли болезнь Паркинсона к слабоумию?
На последней стадии болезни Паркинсона симптомы могут прогрессировать от серьезного угнетения двигательной функции до потери памяти. Обычно любая форма потери памяти называется деменцией.
Существует несколько форм деменции, например:
- Болезнь Альцгеймера (наиболее частая)
- Болезнь Хантингтона
- Сосудистая деменция
- Деменция с тельцами Леви
- Деменция, вызванная травмой головы
- Деменция, вызванная злоупотреблением алкоголем и наркотиками
Болезнь Паркинсона указана как форма деменции просто потому, что потеря памяти происходит на более поздних стадиях.Подсчитано, что потеря памяти не вызывает беспокойства, по крайней мере, через 10 лет после первоначального диагноза. Хотя потеря памяти не является основным признаком болезни, более чем у половины пациентов с болезнью Паркинсона развивается какая-либо форма деменции. Подобно болезни Альцгеймера, деменция, связанная с болезнью Паркинсона, прогрессивно ухудшается.
Ассоциация Альцгеймера утверждает, что если деменция действительно возникает из-за болезни Паркинсона, ее симптомы аналогичны деменции с тельцами Леви. Это связано с тем, что у пациентов начинают накапливаться эти белковые отложения (тельца Леви) в тех частях мозга, которые влияют на движение и познание, что затем может повлиять на память.
Это связано с тем, что у пациентов начинают накапливаться эти белковые отложения (тельца Леви) в тех частях мозга, которые влияют на движение и познание, что затем может повлиять на память.
Симптомы деменции включают:
- Галлюцинации
- Изменения в рассуждениях
- Изменение уровня бдительности, которое меняется изо дня в день
- Заблуждения
- Сложность интерпретации визуальной информации
- Депрессия
Деменция не может быть явным симптомом болезни Паркинсона. Возможно, люди с этим заболеванием имеют более высокий риск развития деменции, чем люди без него. Также может быть, что потеря памяти происходит отдельно от болезни.Большинство пациентов с болезнью Паркинсона, страдающих слабоумием, старше 70 лет, и именно тогда показатели потери памяти также начинают увеличиваться. Тем не менее, это значительный шаг вперед в прогрессировании болезни Паркинсона, и врачи должны учитывать это в процессе лечения.
Стадии болезни Паркинсона
Поскольку болезнь Паркинсона развивается с течением времени, существуют различные стадии, которые помогают определить, как развивались симптомы и чего ожидать дальше.
Как правило, врачи следуют пяти этапам, описанным ниже:
1 этапНачальная стадия болезни Паркинсона иногда вообще не проявляется.Если симптомы заметны, это обычно тремор, поражающий одну сторону тела. Симптомы обычно не влияют на ваш распорядок дня, но к ним следует относиться серьезно и доводить до сведения врача, если они еще этого не сделали.
2 этапНа этой стадии болезнь начинает поражать все ваше тело. Тремор и скованность приводят к тому, что выполнение рутинных действий занимает немного больше времени, и это начинает влиять на ваше движение в целом. Ваша осанка и выражение лица могут начать меняться, что может повлиять на вашу способность ходить в обычном темпе или общаться, как вы привыкли.
3 этап На этой стадии усугубляются все симптомы, которые начали постепенно ухудшаться на стадии 2, но вы также начинаете испытывать потерю равновесия и координации, а также скорость ваших рефлексов.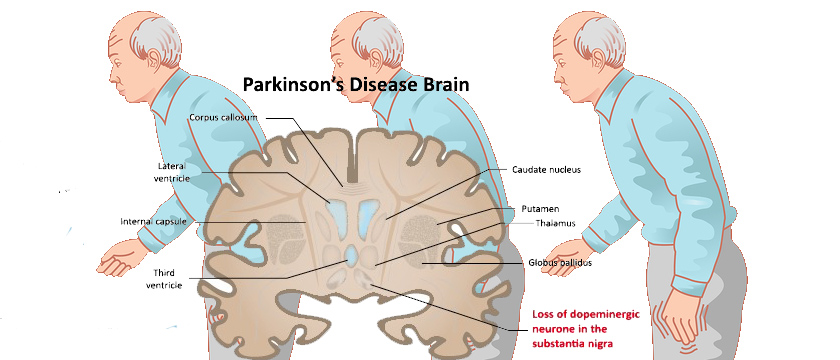 По мере того, как эти симптомы начинают проявляться, люди с заболеванием начинают больше падать, что может стать причиной их собственных травм и ослабления. Такие действия, как вставание с постели, прием пищи и одевание, становятся все труднее.
По мере того, как эти симптомы начинают проявляться, люди с заболеванием начинают больше падать, что может стать причиной их собственных травм и ослабления. Такие действия, как вставание с постели, прием пищи и одевание, становятся все труднее.
На данном этапе практически невозможно жить самостоятельно. Ваша способность выполнять повседневные действия (одеваться, принимать душ, принимать пищу) серьезно ограничивается, и вам не следует выполнять их без посторонней помощи, потому что это опасно, особенно готовить пищу и пытаться искупаться. Ходьба также ограничена, ваше движение ограничено только ходящим (если возможно).
5 этапЭто заключительный и самый тяжелый этап, и здесь уже нельзя жить без посторонней помощи.По сути, все двигательные функции утрачиваются, и вы прикованы к кровати или инвалидному креслу для передвижения. На пятой стадии начинается слабоумие, галлюцинации и спутанность сознания.
Помимо того, что начало болезни развивается медленно, существует не одна единичная форма болезни Паркинсона, а несколько, которые проявляются с разной скоростью и вызывают разные симптомы. В то время как различные формы болезни имеют подробные рейтинговые симптомы о том, насколько серьезно болезнь прогрессирует, вышеупомянутая рейтинговая система представляет устойчивое прогрессирование симптомов при всех формах болезни Паркинсона.
Болезнь Паркинсона не всегда является явной причиной смерти людей, страдающих этим заболеванием, а скорее опасностями и запретами (неподвижность, ведущая к сердечным заболеваниям, нестабильность, ведущая к смертельным падениям) болезни, которая может привести к летальному исходу.
Различные типы болезни Паркинсона
Когда болезнь Паркинсона начинает проявляться в полной мере, болезнь может поражать различные части мозга и вызывать различные симптомы. От этого зависит диагноз того, какой у вас тип болезни Паркинсона (симптомы, где она начинается и т. Д.). Иногда врачи также не знают точной причины, но они знают, что у вас проявляются симптомы, сходные с симптомами болезни Паркинсона. Давайте углубимся в различные формы злого недуга:
Д.). Иногда врачи также не знают точной причины, но они знают, что у вас проявляются симптомы, сходные с симптомами болезни Паркинсона. Давайте углубимся в различные формы злого недуга:
- Сосудистый паркинсонизм : Сосудистый паркинсонизм вызывается ограничением кровотока в головном мозге, особенно в тех частях мозга, которые влияют на движение и речь. Когда у кого-то случается обширный инсульт или даже несколько более мелких, немедленное ограничение поступления крови в определенные части мозга может вызвать симптомы, подобные болезни Паркинсона.В отличие от нормальной болезни Паркинсона, симптомы сосудистого паркинсонизма — чаще всего проблемы с ходьбой и потеря памяти — обычно проявляются очень быстро из-за немедленного ограничения крови.
- Идиопатическая болезнь Паркинсона : наиболее распространенная форма болезни Паркинсона, диагностируется, когда корень болезни неизвестен. В то время как потерю моторики и устойчивости можно подробно объяснить в других случаях, врачи часто не знают, почему заболевание развилось.
- Паркинсонизм, индуцированный лекарствами : Болезнь Паркинсона может развиться после длительного приема определенных лекарств. Из-за этого она развивается от 5 до 10 процентов людей с болезнью Паркинсона. Антипсихотические и нейролептические препараты, которые используются для лечения таких состояний, как шизофрения и психоз, могут вызывать болезнь Паркинсона, поскольку они влияют на естественный уровень дофамина в головном мозге. Хотя они блокируют дофамин в ближайшем будущем, это долгосрочное истощение может начать размножаться в виде симптомов Паркинсона.Если болезнь действительно развивается из-за этих типов лекарств, она часто обратима в течение недель и месяцев после прекращения приема лекарств.
- Кортикобазальная дегенерация : более редкая форма заболевания, возникает, когда белок, называемый тау, накапливается в определенных частях мозга. Кортикобазальная дегенерация развивается медленнее и часто поражает одну сторону тела, прежде чем в течение пары лет постепенно отразится на всем теле.
 Его можно диагностировать в возрасте 40 лет, но чаще всего заболевание развивается в возрасте от 50 до 70 лет.
Его можно диагностировать в возрасте 40 лет, но чаще всего заболевание развивается в возрасте от 50 до 70 лет.
Есть и другие поколения болезни, но они самые редкие формы. Тем не менее они несут такие же симптомы, как и все другие формы болезни.
Лечение болезни Паркинсона и его будущее
Болезнь Паркинсона неизлечима. Тем не менее, миллионы долларов ежегодно расходуются на исследования, чтобы лучше понять болезнь, начиная с ее определения и заканчивая методами лечения. Конечная конечная цель — разработать лекарство от болезни Паркинсона, но тем временем врачи и исследователи разработали планы лечения, основанные на том, что, как они предполагают, в первую очередь вызывает болезнь, — чаще всего на недостатке определенных химических веществ и клеток мозга, таких как дофамин.
Планы варьируются в зависимости от пациента, и некоторые из этих вариантов лечения включают:
- Леводопа : это основное лекарство, используемое для лечения симптомов болезни Паркинсона. Было обнаружено, что у людей с этим заболеванием уровень дофамина значительно ниже, и леводопа решает эту проблему и стимулирует нервную систему. Леводопа увеличивает уровень дофамина в вашем теле и направлен на решение проблем, связанных с нервной системой, таких как тремор, мышечный контроль и координация.Как правило, леводопа принимается вместе с препаратом под названием карбидопа, который действует как защитник леводопы, поэтому он действительно достигает мозга и позволяет ему быть эффективным. К сожалению, леводопа имеет некоторые недостатки, в том числе рвоту, тошноту, бессонницу и диарею, а также другие побочные эффекты. При длительном применении леводопа может усилить тремор и другие мышечные спазмы. Комбинация этих препаратов принимается несколько раз в день.
- Агонисты дофамина : В отличие от леводопы, которая превращается в дофамин, некоторым пациентам назначают агонисты дофамина, имитирующие действие дофамина.Эти агонисты активируют дофаминовые рецепторы в вашем мозгу и создают впечатление, что ваши дофаминовые рецепторы работают нормально.
 В некоторых случаях агонисты дофамина принимают вместе с леводопой, чтобы помочь найти здоровый баланс между двумя лекарствами и ограничить побочные эффекты от обоих методов лечения. Побочные эффекты агонистов дофамина аналогичны побочным эффектам леводопы, но есть и другие серьезные побочные эффекты, включая галлюцинации и спорадическое поведение за пределами вашей личности.
В некоторых случаях агонисты дофамина принимают вместе с леводопой, чтобы помочь найти здоровый баланс между двумя лекарствами и ограничить побочные эффекты от обоих методов лечения. Побочные эффекты агонистов дофамина аналогичны побочным эффектам леводопы, но есть и другие серьезные побочные эффекты, включая галлюцинации и спорадическое поведение за пределами вашей личности. - Хирургия / стимуляция мозга : Доступны хирургические варианты для пациентов с болезнью Паркинсона.Первичная форма хирургического вмешательства, которую получают пациенты с болезнью Паркинсона, — это глубокая стимуляция головного мозга (DBS), направленная на воздействие на определенные части мозга, такие как кора. Во время операции в мозг посылаются электрические волны, чтобы стимулировать те части органа, которые страдают от болезни Паркинсона. Конечная цель — облегчить некоторые симптомы, вызываемые болезнью. Еще одна операция, которую могут сделать пациенты с болезнью Паркинсона, — это имплант, который постоянно выделяет агонисты дофамина или леводопу, чтобы лекарство принималось по расписанию.
- Медицинская марихуана : Медицинская марихуана не была официально рекомендована Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов для лечения болезни Паркинсона, поскольку не было научно доказано, что каннабиноиды явно помогают бороться с болезнью. Однако на протяжении десятилетий его использовали для лечения заболеваний, подобных тем, которые проявляются при болезни Паркинсона, таких как тремор и замедленность движений. Чтобы узнать больше, прочтите наше полное руководство по медицинской марихуане для пожилых людей.
- Другие лекарства : Существуют и другие лекарства, включая Элдеприл, Зелапар, Дуопа (комбинация леводопы и карбидопы), Азилект и многие другие, которые снижают уровень дофамина в головном мозге и различные симптомы, которые могут возникнуть из-за болезни.
Также нет реального способа окончательно предотвратить болезнь. Как и в случае с профилактикой любых заболеваний или недомоганий, рекомендуется вести здоровый образ жизни до и после постановки диагноза. Сохранение физической активности посредством таких видов деятельности, как бег, йога и поднятие тяжестей, а также здоровое питание — это оба способа предоставить вашему телу наилучшие возможности для здорового образа жизни.
Как и в случае с профилактикой любых заболеваний или недомоганий, рекомендуется вести здоровый образ жизни до и после постановки диагноза. Сохранение физической активности посредством таких видов деятельности, как бег, йога и поднятие тяжестей, а также здоровое питание — это оба способа предоставить вашему телу наилучшие возможности для здорового образа жизни.
также рассматриваются как «вариант лечения», потому что они могут дать вам такой же шанс облегчения симптомов, как и другие уже существующие методы лечения.Клинические испытания проводятся круглый год в различных учреждениях и фондах, и ваши демографические данные могут соответствовать исследованию на начальной доклинической стадии или на продвинутой стадии.
Поговорите со своим врачом о любых доступных клинических испытаниях, на участие в которых вы можете претендовать, и о том, как стать их участником. Также оставайтесь на связи со своим врачом относительно любых проблем, которые могут у вас возникнуть с болезнью Паркинсона, или о том, как лечить.
Что такое болезнь Паркинсона? Симптомы, причины, диагностика, лечение и профилактика
Большинство случаев болезни Паркинсона являются идиопатическими, то есть причина неясна.
Широко распространено мнение, что человек с болезнью Паркинсона мог быть генетически уязвим к этой болезни, и что один или несколько неизвестных факторов окружающей среды в конечном итоге спровоцировали болезнь.
Большинство симптомов болезни Паркинсона возникают из-за потери нейронов в области мозга, называемой черной субстанцией . (7)
Обычно нейроны в этой части мозга вырабатывают химический посланник (нейротрансмиттер) дофамин, который обеспечивает связь с другой областью мозга, полосатым телом.
Это общение помогает производить плавное и целенаправленное движение. Когда нейроны в черной субстанции умирают, потеря связи приводит к моторным (связанным с движением) симптомам болезни Паркинсона. (8)
(8)
Хотя причина этой гибели клеток неизвестна, многие исследователи полагают, что клетки убиваются слипшимися белками, называемыми тельцами Леви. (8)
Что такое тельца Леви?
Было обнаружено, что пораженные нейроны людей с болезнью Паркинсона содержат слипшиеся белки, называемые тельцами Леви, но исследователи еще не уверены, почему формируются тельца Леви и какую роль они играют в заболевании.(9)
Тельца Леви представляют собой скопления белка, называемого альфа-синуклеином (A-синуклеин). Нейроны не могут расщеплять эти белковые сгустки, что может привести к гибели этих клеток. (9)
Некоторые другие теории о причинах гибели клеток мозга у людей с болезнью Паркинсона включают повреждение свободными радикалами, воспаление или токсины.
Каковы факторы риска болезни Паркинсона?
Факторы риска болезни Паркинсона включают:
Генетика
Люди, у которых есть родственники первой степени (родитель или брат или сестра) с болезнью Паркинсона, подвергаются повышенному риску заболевания — возможно, на 9 процентов выше.
У 15–25 процентов людей с болезнью Паркинсона есть известные родственники с этой болезнью, но состояние, называемое семейной болезнью Паркинсона, с известной генетической связью, встречается относительно редко. (10)
Возраст
Средний возраст начала заболевания составляет 60 лет, и заболеваемость растет с увеличением возраста. Около 10 процентов людей страдают «ранним» или «молодым» заболеванием, которое начинается в возрасте до 50 лет. (11)
Пол
Болезнь Паркинсона по неизвестным причинам поражает примерно на 50 процентов больше мужчин, чем женщин.(12)
Воздействие пестицидов
Было показано, что воздействие некоторых пестицидов повышает риск развития болезни Паркинсона.
Проблемные химические вещества включают хлорорганические пестициды, такие как ДДТ, диэльдрин и хлордан. Также замешаны ротенон и перметрин. (13)
Также замешаны ротенон и перметрин. (13)
Воздействие фунгицидов и гербицидов
Воздействие фунгицида манеб или гербицидов 2,4-дихлорфеноксиуксусная кислота (2,4-D), паракват или агент апельсин может повысить риск болезни Паркинсона.
Управление здравоохранения ветеранов США рассматривает болезнь Паркинсона как возможное заболевание, связанное с оказанием услуг, если человек подвергся воздействию значительных количеств Agent Orange. (14)
Травмы головы
Травмы головы могут способствовать развитию болезни Паркинсона у некоторых людей. (15)
Кофе и курение
Было обнаружено, что люди, которые пьют кофе или курят табак, имеют более низкий риск болезни Паркинсона по неизвестным причинам.(16)
Узнайте больше о причинах болезни Паркинсона: общие факторы риска, генетика и многое другое
Болезнь Паркинсона: диагностика и лечение
1. de Lau LM, Гисберген ПК, de Rijk MC, Хофман А, Коудсталь П.Дж., Бретелер ММ. Заболеваемость паркинсонизмом и болезнью Паркинсона среди населения в целом: Роттердамское исследование. Неврология . 2004; 63: 1240–4 ….
2. Натт Дж. Г., Wooten GF.Клиническая практика. Диагностика и начальное лечение болезни Паркинсона. N Engl J Med . 2005; 353: 1021–7.
3. Оланов CW, Watts RL, Коллер WC. Алгоритм (дерево решений) для лечения болезни Паркинсона (2001 г.): рекомендации по лечению. Неврология . 2001; 56 (11 доп. 5): S1–88.
4. Кларк CE. Нейропротекция и фармакотерапия двигательных симптомов при болезни Паркинсона. Ланцет Нейрол .2004; 3: 466–74.
5. Итальянское неврологическое общество, Итальянское общество клинической нейрофизиологии. Руководство по лечению болезни Паркинсона 2002. Диагностика болезни Паркинсона. Neurol Sci . 2003; (24 доп. 3): S157–64.
2003; (24 доп. 3): S157–64.
6. Рао Г, Фиш Л, Шринивасан S, Д’Амико Ф, Окада Т, Итон С, и другие. Болеет ли этот пациент болезнью Паркинсона? ЯМА . 2003. 289: 347–53.
7. Агентство медицинских исследований и качества. Диагностика и лечение болезни Паркинсона: систематический обзор литературы. По состоянию на 19 июня 2006 г., по адресу: http://www.ahrq.gov/clinic/epcsums/parksum.htm.
8. Серитан А.Л., Мендес М.Ф., Сильверман Д.Х., Херли Р.А., Taber KH. Функциональная визуализация как окно к деменции: кортикобазальная дегенерация. J Neuropsychiatry Clin Neurosci . 2004; 16: 393–9.
9. Суховерский О, Райх С, Перлмуттер Дж., Зесевич Т, Гронсет G, Вайнер WJ.Параметр практики: диагностика и прогноз нового начала болезни Паркинсона (обзор, основанный на фактах): отчет Подкомитета по стандартам качества Американской академии неврологии. Неврология . 2006; 66: 968–75.
10. Шульц CW, Оукс D, Кибурц К, Бил М.Ф., Haas R, Отвес S, и другие., для группы изучения болезни Паркинсона. Влияние коэнзима Q10 на раннюю стадию болезни Паркинсона: свидетельство замедления функционального спада. Arch Neurol . 2002; 59: 1541–50.
11. Группа изучения болезни Паркинсона. Визуализация мозга переносчика дофамина для оценки эффектов прамипексола по сравнению с леводопой на прогрессирование болезни Паркинсона. ЯМА . 2002; 287: 1653–61.
12. Whone AL,
Watts RL,
Штёссл А.Дж.,
Дэвис М,
Реске С,
Нахмиас С,
и другие.
Более медленное прогрессирование болезни Паркинсона при применении ропинирола по сравнению с леводопой: исследование REAL-PET. Энн Нейрол .
2003. 54: 93–101.
54: 93–101.
13. Целевая группа Общества по двигательным расстройствам по рейтинговым шкалам для болезни Паркинсона. Единая шкала оценки болезни Паркинсона (UPDRS): статус и рекомендации. Mov Disord . 2003; 18; 738–50.
14. Миясаки Дж. М., Мартин В, Суховерский О, Вайнер WJ, Lang AE. Параметр практики: начало лечения болезни Паркинсона: обзор, основанный на фактах: отчет Подкомитета по стандартам качества Американской академии неврологии. Неврология . 2002; 58: 11–7.
15. Goetz CG, Poewe W, Раскол О, Сампайо К. Обновленный медицинский обзор, основанный на фактических данных: фармакологические и хирургические методы лечения болезни Паркинсона: 2001–2004 гг. Mov Disord . 2005; 20: 523–39.
16. Самии А, Выкуп BR. Двигательные расстройства: обзор и варианты лечения. ПиТ . 2005; 30: 228–38.
17. Шеннон К.М., Беннетт Дж. П. Младший, Фридман Дж. Х., для группы исследования прамипексола.Эффективность прамипексола, нового агониста дофамина, в качестве монотерапии при болезни Паркинсона от легкой до умеренной [Опубликованная поправка опубликована в Neurology 1998; 50: 838]. Неврология . 1997; 49: 724–8.
18. Адлер СН, Сетхи К.Д., Хаузер Р.А., Дэвис Т.Л., Хаммерстад JP, Бертони Дж. и другие., для группы изучения ропинирола. Ропинирол для лечения болезни Паркинсона на ранних стадиях [Опубликованная поправка опубликована в Neurology 1997; 49: 1484]. Неврология . 1997; 49: 393–9.
19. Бароне П.,
Брави Д,
Бермеджо-Пареха Ф,
Маркони Р.,
Кулисевский Ж,
Малагу S,
и другие.,
для группы исследования монотерапии перголидом.
Монотерапия перголидом в лечении ранней БП: рандомизированное контролируемое исследование. Неврология .
1999; 53: 573–9.
Неврология .
1999; 53: 573–9.
20. Раскол О, Брукс DJ, Корчин А.Д., Де Дейн П.П., Кларк CE, Lang AE, для исследовательской группы 056.Пятилетнее исследование частоты дискинезии у пациентов с ранней стадией болезни Паркинсона, получавших ропинирол или леводопу. N Engl J Med . 2000; 342: 1484–91.
21. Группа изучения болезни Паркинсона. Прамипексол против леводопы в качестве начального лечения болезни Паркинсона: рандомизированное контролируемое исследование. ЯМА . 2000; 284: 1931–8.
22. Ивс, штат Нью-Джерси, Стоу Р.Л., Марро Дж, Советник C, Маклауд А, Кларк CE, и другие.Ингибиторы моноаминоксидазы типа B на ранних стадиях болезни Паркинсона: метаанализ 17 рандомизированных исследований с участием 3525 пациентов. BMJ . 2004; 329: 593.
23. Ahlskog JE, Мюнтер MD. Частота дискинезий и двигательных колебаний, связанных с леводопой, по оценке из совокупной литературы. Mov Disord . 2001. 16: 448–58.
24. Кларк CE, Спеллер Дж. М., Кларк Дж. Прамипексол при осложнениях болезни Паркинсона, вызванных леводопой. Кокрановская база данных Syst Rev . 2000; (2): CD002261.
25. Кларк CE, Дин К.Х. Ропинирол для лечения вызванных леводопой осложнений болезни Паркинсона. Кокрановская база данных Syst Rev . 2001; (1): CD001516.
26. Дин К.Х., Spieker S, Кларк CE. Ингибиторы катехол-O-метилтрансферазы для лечения вызванных леводопой осложнений при болезни Паркинсона. Кокрановская база данных Syst Rev . 2004; (4): CD004554.
27. Раскол О,
Брукс DJ,
Меламед Э,
и другие.
Сравнительное рандомизированное исследование разагилина по сравнению с плацебо или энтакапоном в качестве дополнения к леводопе у пациентов с болезнью Паркинсона (БП) с двигательными колебаниями (исследование LARGO). 56-е ежегодное собрание Американской академии неврологии, Сан-Франциско, Калифорния, 2004 г. Аннотация S38.004. Неврология .
2004; 62 (7 доп. 5): A1–626.
56-е ежегодное собрание Американской академии неврологии, Сан-Франциско, Калифорния, 2004 г. Аннотация S38.004. Неврология .
2004; 62 (7 доп. 5): A1–626.
28. Томас А., Яконо D, Лучано А.Л., Армеллино К, Ди Иорио А, Онофрж М.Продолжительность действия амантадина при дискинезии тяжелой болезни Паркинсона. J Neurol Neurosurg Psychiatry . 2004; 75: 141–14.
29. Пахва р, Фактор SA, Lyons KE, Ондо РГ, Гронсет G, Бронте-Стюарт Х, и другие. Параметр практики: лечение болезни Паркинсона с двигательными колебаниями и дискинезией (обзор, основанный на фактах): отчет Подкомитета по стандартам качества Американской академии неврологии. Неврология . 2006; 66: 983–95.
30. Миясаки Дж. М., Шеннон К., Вун В., Равина Б., Кляйнер-Фисман Дж., Андерсон К. и др. Параметр практики: оценка и лечение депрессии, психоза и деменции при болезни Паркинсона (обзор, основанный на фактах). По состоянию на 19 июня 2006 г., по адресу: http://www.aan.com/professionals/practice/guidelines/pda/eval_dementia_pd.pdf.
31. Aarsland D, Андерсен К, Ларсен JP, Лолк А, Краг-Соренсен П. Распространенность и характеристики деменции при болезни Паркинсона: 8-летнее проспективное исследование. Arch Neurol . 2003. 60: 387–92.
32. Дин К.Х., Эллис-Хилл C, Плейфорд ЭД, Бен-Шломо Y, Кларк CE. Трудотерапия для пациентов с болезнью Паркинсона. Кокрановская база данных Syst Rev . 2001; (2): CD002813.
33. Дин К.Х., Джонс Д, Плейфорд ЭД, Бен-Шломо Y, Кларк CE. Физиотерапия для пациентов с болезнью Паркинсона: сравнение методик. Кокрановская база данных Syst Rev .2001; (3): CD002817.
34. Дин К.Х.,
Whurr R,
Плейфорд ЭД,
Бен-Шломо Y,
Кларк CE. Речевая и языковая терапия дизартрии при болезни Паркинсона. Кокрановская база данных Syst Rev .
2001; (2): CD002812.
Речевая и языковая терапия дизартрии при болезни Паркинсона. Кокрановская база данных Syst Rev .
2001; (2): CD002812.
35. Хирш М.А., Тул Т, Мейтленд К.Г., Райдер РА. Влияние тренировок на равновесие и высокоинтенсивных тренировок с отягощениями на людей с идиопатической болезнью Паркинсона. Arch Phys Med Rehabil .2003. 84: 1109–17.
36. Эллис Т., де Геде CJ, Фельдман Р.Г., Wolters EC, Кваккель Г, Wagenaar RC. Эффективность программы физиотерапии у пациентов с болезнью Паркинсона: рандомизированное контролируемое исследование. Arch Phys Med Rehabil . 2005. 86: 626–32.
37. Рамиг ЛО, Сапир С, Лиса C, Земляк С. Изменения громкости голоса после интенсивной обработки голоса (LSVT) у людей с болезнью Паркинсона: сравнение с нелеченными пациентами и контрольной группой нормального возраста. Mov Disord . 2001; 16: 79–83.
38. Шимбо Т, Гото М, Моримото Т, Хира К, Такемура М, Мацуи К, и другие. Связь между обучением пациентов и качеством жизни, связанным со здоровьем, у пациентов с болезнью Паркинсона. Качество жизни . 2004; 13: 81–9.
Текущее и будущее лекарственное лечение болезни Паркинсона
- COMT, катехол- O -метилтрансфераза
- GDNF, фактор роста нервов, полученный из глиальных клеток
- MAO, моноаминоксидаза
- MPP000, 1-метил-4-фенилпи-8000 MPTP, 1-метил, 4-фенил 1,2,3,6 тетрагидропиридин
- PD, болезнь Паркинсона
- ПЭТ, позитронно-эмиссионная томография
- UPDRS, Единая шкала оценки болезни Паркинсона
- SPECT, компьютерная томография с однофотонной эмиссией
Впервые официально описанная почти 200 лет назад, болезнь Паркинсона (БП) является одним из наиболее распространенных дегенеративных заболеваний человека и оказывает серьезное социально-экономическое воздействие. Прямые медицинские расходы в Великобритании в 1992 году оценивались в 383 миллиона фунтов стерлингов и почти наверняка сильно занижены. Более 75% этих затрат связано с лечением в специализированных учреждениях, но косвенные затраты и бремя болезней для пациентов и лиц, осуществляющих уход, неоценимы. По мере старения населения лечение болезни Паркинсона, вероятно, станет все более важным и сложным аспектом медицинской практики. Стоимость разработки и использования новых методов лечения, следовательно, должна быть определена в этом контексте.
Прямые медицинские расходы в Великобритании в 1992 году оценивались в 383 миллиона фунтов стерлингов и почти наверняка сильно занижены. Более 75% этих затрат связано с лечением в специализированных учреждениях, но косвенные затраты и бремя болезней для пациентов и лиц, осуществляющих уход, неоценимы. По мере старения населения лечение болезни Паркинсона, вероятно, станет все более важным и сложным аспектом медицинской практики. Стоимость разработки и использования новых методов лечения, следовательно, должна быть определена в этом контексте.
Значительный прогресс был достигнут в определении этиологии, патогенеза и патологии БП, и эти достижения, в свою очередь, привели к развитию и быстрому расширению фармакопеи, доступной для лечения. Однако лечение остается неудовлетворительным, поскольку оно в основном направлено только на дофаминергические особенности заболевания и не влияет на его прогрессирующее течение. Будущее медикаментозного лечения БП должно быть сосредоточено на симптоматическом лечении недофаминергических и немоторных особенностей заболевания и на необходимости модификации заболевания с точки зрения задержки или предотвращения прогрессирования.В этой статье делается попытка установить текущие варианты лечения в контексте, рассмотреть появляющиеся и новые лекарственные препараты для лечения БП и оценить перспективы модификации болезни. Хирургическое лечение рассматриваться не будет.
ПАТОЛОГИЯ
PD — это многоцентровое нейродегенеративное заболевание, при котором развитие патологических аномалий следует определенной последовательности. Недавние исследования показывают, что самые ранние изменения наблюдаются в дорсальном двигательном ядре, а также в обонятельных луковицах и ядре — стадия Браака 1. 1 В этом контексте следует отметить, что потеря обонятельной функции может произойти до появления дофаминергических симптомов или признаков и может служить для определения группы риска. 2 Затем потеря клеток и образование телец Леви развиваются в голубом пятне и прогрессируют в мозговом веществе и мосту — стадия Браака 2. 3 Появление потери клеток и образования включений в компактной части черной субстанции определяет начало стадии Браака. 3. На этой стадии также наблюдается дегенерация педункулопонтиального ядра, ядер дорсального шва и гипоталамуса.Стадии 5 и 6 включают прогрессирующее вовлечение коры головного мозга и нейродегенерацию в уже затронутых областях.
3 Появление потери клеток и образования включений в компактной части черной субстанции определяет начало стадии Браака. 3. На этой стадии также наблюдается дегенерация педункулопонтиального ядра, ядер дорсального шва и гипоталамуса.Стадии 5 и 6 включают прогрессирующее вовлечение коры головного мозга и нейродегенерацию в уже затронутых областях.
Согласно классификации Браака, клинические признаки болезни Паркинсона проявляются на стадии 3. Подразумевается, что успешное терапевтическое вмешательство, изменяющее заболевание, на / или до стадии 3 предотвратит прогрессирование до точки, когда дофаминергические признаки станут серьезными. Важно отметить, что такое лечение, если оно будет эффективным для недофаминергических систем, предотвратит клиническое развитие немоторных осложнений, которые характерны для более поздних стадий БП.
ДОПАМИНЕРГИЧЕСКИЕ ОСОБЕННОСТИ И ИХ ЛЕЧЕНИЕ
Пациенты с БП обычно имеют признаки, указывающие на дегенерацию нигростриатных путей. Полезное клиническое определение БП — «асимметричное начало акинетического (брадикинетического) ригидного синдрома с тремором покоя и хорошим ответом на леводопу». При применении неврологами, интересующимися двигательными расстройствами, это определение имеет патологическую корреляцию, превышающую 98%. 4 Когда лечение считается подходящим, и эта тема подробно обсуждается ниже, доступны различные варианты.Использование дофаминергических препаратов улучшает двигательную функцию, значительно снижает как заболеваемость, так и смертность от БП, а также улучшает качество жизни. 5– 7
Леводопа остается препаратом, наиболее часто используемым при БП. Он очень эффективен для улучшения брадикинезии и ригидности и на практике остается золотым стандартом, по которому оцениваются другие препараты. Некоторые исследования, преимущественно in vitro, показали, что леводопа может быть токсичным. 8, 9, 10 Однако такие данные противоречивы, 11, 12 и некоторые лабораторные исследования показали эффект, подобный фактору роста, для леводопы.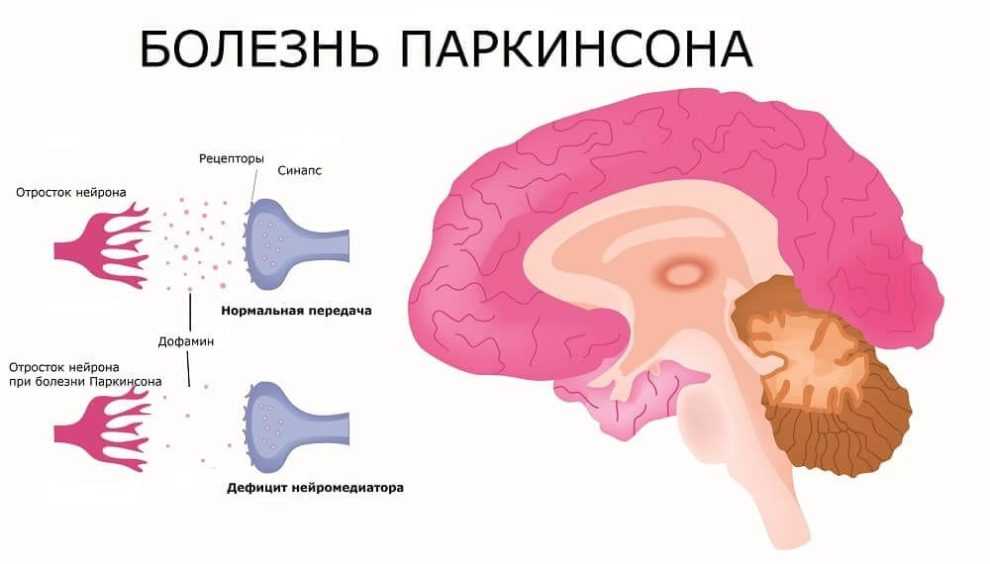 13 В целом доклинические данные о токсичности леводопы неубедительны, и нет данных, указывающих на то, что какое-либо токсическое действие имеет клиническое значение. 14, 15
13 В целом доклинические данные о токсичности леводопы неубедительны, и нет данных, указывающих на то, что какое-либо токсическое действие имеет клиническое значение. 14, 15
Леводопа остается эффективной на протяжении всего протекания болезни Паркинсона, но его эффекты видоизменяются вследствие прогрессирования заболевания и потери дофаминергических клеток, необходимых для метаболизма лекарственного средства, а также для хранения и высвобождения дофамина. Кроме того, употребление леводопы действительно приводит к двигательным осложнениям, включая дискинезии и «истощение».Механизмы, с помощью которых развиваются эти эффекты, полностью не изучены, но включают пульсирующую стимуляцию дофаминовых рецепторов агентами короткого действия, такими как леводопа, и степень денервации полосатого тела. 16 Двигательные осложнения развиваются со скоростью примерно 10% в год у тех, кому поставлен диагноз старше 60 лет, но быстрее у более молодых пациентов, у 70% из которых есть двигательные осложнения через 3 года после постановки диагноза. 17 Эффективность леводопы может быть усилена совместным введением ингибитора катехол- O -метилтрансферазы (COMT), который снижает метилирование O в кишечнике, увеличивает абсорбцию леводопы и продлевает период полувыведения. 18 Толкапон был первым лицензированным ингибитором СОМТ, но был отменен из-за токсичности для печени. Однако недавно он был повторно введен с ограниченной лицензией и требует соответствующего мониторинга. Его следует использовать только тем, кто не переносит энтакапон или не получает от него никакой пользы. Энтакапон является наиболее широко используемым ингибитором СОМТ и в сочетании с леводопой увеличивает время «включения» и сокращает время «выключения». 19 На модели БП приматов с 1-метил, 4-фенил 1,2,3,6 тетрагидропиридином (МРТР) получены данные о том, что леводопа в сочетании с энтакапоном четыре раза в день приводит к значительно меньшей дискинезии, чем без энтакапона или если давать реже. 20 Сталево — препарат, сочетающий леводопу с ингибитором допа-декарбоксилазы и энтакапоном. В настоящее время проводится исследование, чтобы определить, влияет ли эффект, наблюдаемый в модели MPTP, на более низкую частоту дискинезии у пациентов, начавших лечение Сталево, а не леводопой.
20 Сталево — препарат, сочетающий леводопу с ингибитором допа-декарбоксилазы и энтакапоном. В настоящее время проводится исследование, чтобы определить, влияет ли эффект, наблюдаемый в модели MPTP, на более низкую частоту дискинезии у пациентов, начавших лечение Сталево, а не леводопой.
Агонисты дофамина эффективны при использовании отдельно или в качестве дополнения к леводопе. 21 Монотерапия агонистами может эффективно контролировать дофаминергические симптомы на некоторое время 22, 23 (таблица 1), но пациентам неизбежно потребуется прием леводопы в какой-то момент во время болезни.Возможно, одна из наиболее распространенных причин неэффективности агонистов на ранних стадиях заболевания заключается в том, что они слишком часто используются в слишком низких дозах и отказываются от них до того, как будет достигнут соответствующий уровень. При правильном использовании они могут обеспечить контроль симптомов, сравнимый с таковым при применении леводопы. Хотя два исследования монотерапии 22, 23 показали, что использование леводопы увеличило баллы по унифицированной шкале оценки болезни Паркинсона (UPDRS) на пять пунктов, пациенты в группах агонистов не нуждались в дополнительном приеме лекарств для достижения эквивалентной клинической пользы, т.е. Считали ли пациенты и врачи, что группы агонистов и леводопа клинически одинаковы в контексте слепого исследования.Оценка качества жизни также была эквивалентной за 4-летний период. 22 Это означает, что пациенты одинаково хорошо контролировались агонистом (с добавлением леводопы при необходимости) или только леводопой. Конечно, в группе леводопы было больше дискинезий, но через 4 года они не оказали существенного влияния на качество жизни пациентов и пока не начали ограничивать возможности лечения для контроля моторики.
Стол 1Процент пациентов, оставшихся на монотерапии агонистами дофамина в течение 1–4 лет (CALM-PD) и 1–5 лет (ропинирол 056) во время клинических испытаний
Одно открытое исследование продемонстрировало, что добавление каберголина, спорыньи длительного действия, к прамипексолу или ропиниролу, не относящимся к спорынье, привело к улучшению моторного контроля. 24 Агонисты длительного действия полезны при лечении дискинезий у части пациентов, предположительно из-за их способности обеспечивать более продолжительную дофаминергическую стимуляцию, избегая при этом быстрых колебаний стимуляции рецепторов. 25 Ротигитин, новый агонист дофамина, будет доступен для использования в качестве пластыря для кожи и предлагает еще одну возможность для устойчивого дофаминергического эффекта. Аналогичный эффект может быть получен с помощью инфузий леводопы или апоморфина, 26 , и вскоре будет доступен препарат для вливания леводопы в двенадцатиперстную кишку.Общие побочные эффекты агонистов дофамина — это побочные эффекты дофаминергических агентов в целом в дополнение к более высокому уровню когнитивных нарушений (спутанность сознания, галлюцинации), сонливости и отеков ног. Недавнее сообщение связывало перголид с фиброзом сердечного клапана. 27 В настоящее время недостаточно данных, чтобы установить, связано ли это только с агонистами спорыньи или со всеми агонистами дофамина, и зависит ли эффект от дозы и / или времени. В настоящее время возможность фиброзного порока сердечных клапанов контролируется путем бдительности, соответствующих обследований (эхокардиограмма, x луча грудной клетки и СОЭ) и направления в отделения кардиологии в определенных случаях.
24 Агонисты длительного действия полезны при лечении дискинезий у части пациентов, предположительно из-за их способности обеспечивать более продолжительную дофаминергическую стимуляцию, избегая при этом быстрых колебаний стимуляции рецепторов. 25 Ротигитин, новый агонист дофамина, будет доступен для использования в качестве пластыря для кожи и предлагает еще одну возможность для устойчивого дофаминергического эффекта. Аналогичный эффект может быть получен с помощью инфузий леводопы или апоморфина, 26 , и вскоре будет доступен препарат для вливания леводопы в двенадцатиперстную кишку.Общие побочные эффекты агонистов дофамина — это побочные эффекты дофаминергических агентов в целом в дополнение к более высокому уровню когнитивных нарушений (спутанность сознания, галлюцинации), сонливости и отеков ног. Недавнее сообщение связывало перголид с фиброзом сердечного клапана. 27 В настоящее время недостаточно данных, чтобы установить, связано ли это только с агонистами спорыньи или со всеми агонистами дофамина, и зависит ли эффект от дозы и / или времени. В настоящее время возможность фиброзного порока сердечных клапанов контролируется путем бдительности, соответствующих обследований (эхокардиограмма, x луча грудной клетки и СОЭ) и направления в отделения кардиологии в определенных случаях.
Ингибиторы моноаминоксидазы (МАО) B, такие как селегилин и разагилин, улучшают двигательную функцию на ранних и поздних стадиях болезни Паркинсона. 28– 30 Несмотря на то, что существовала некоторая озабоченность относительно долгосрочной безопасности селегилина, несколько исследований развеяли эти опасения и показали, что этот препарат является одновременно эффективным и безопасным для пациентов с БП. 31
Любые рекомендации относительно характера и последовательности терапии всегда следует учитывать с учетом того факта, что лечение БП всегда адаптируется к конкретным потребностям и обстоятельствам пациента. Ниже приводится индивидуальный подход к начальному лечению дофаминергических особенностей БП. Традиционно медикаментозное лечение начинают только тогда, когда симптомы пациента существенно мешают его занятости или социальной деятельности. Однако введение препаратов, которые хорошо переносятся с низким и приемлемым профилем побочных эффектов в краткосрочной и долгосрочной перспективе, заставило некоторых клиницистов пересмотреть этот подход. На мой взгляд, возможность раннего лечения для улучшения тех самых симптомов, которые привлекли пациента к медицинской помощи, следует обсудить с пациентом.Людям в возрасте 70–75 лет и младше, без когнитивных нарушений и значительных сопутствующих заболеваний, следует рассмотреть возможность введения агониста дофамина или ингибитора МАО-В. Агонист улучшит двигательную дисфункцию в большей степени, чем ингибитор МАО-В, но последний, вероятно, лучше переносится, и выбор между ними будет зависеть от степени симптоматической дисфункции пациента. Для пациентов в возрасте старше 70–75 лет с когнитивной дисфункцией или значительной сопутствующей патологией леводопа будет препаратом выбора для начала терапии.В какой-то момент всем пациентам, независимо от того, начали ли они терапию агонистом дофамина или ингибитором МАО-B, потребуется добавить леводопа к их режиму. В настоящее время леводопа начинается без энтакапона, но это может измениться, если продолжающееся исследование продемонстрирует, что введение леводопы в форме Сталево связано с более низким риском двигательных осложнений.
Ниже приводится индивидуальный подход к начальному лечению дофаминергических особенностей БП. Традиционно медикаментозное лечение начинают только тогда, когда симптомы пациента существенно мешают его занятости или социальной деятельности. Однако введение препаратов, которые хорошо переносятся с низким и приемлемым профилем побочных эффектов в краткосрочной и долгосрочной перспективе, заставило некоторых клиницистов пересмотреть этот подход. На мой взгляд, возможность раннего лечения для улучшения тех самых симптомов, которые привлекли пациента к медицинской помощи, следует обсудить с пациентом.Людям в возрасте 70–75 лет и младше, без когнитивных нарушений и значительных сопутствующих заболеваний, следует рассмотреть возможность введения агониста дофамина или ингибитора МАО-В. Агонист улучшит двигательную дисфункцию в большей степени, чем ингибитор МАО-В, но последний, вероятно, лучше переносится, и выбор между ними будет зависеть от степени симптоматической дисфункции пациента. Для пациентов в возрасте старше 70–75 лет с когнитивной дисфункцией или значительной сопутствующей патологией леводопа будет препаратом выбора для начала терапии.В какой-то момент всем пациентам, независимо от того, начали ли они терапию агонистом дофамина или ингибитором МАО-B, потребуется добавить леводопа к их режиму. В настоящее время леводопа начинается без энтакапона, но это может измениться, если продолжающееся исследование продемонстрирует, что введение леводопы в форме Сталево связано с более низким риском двигательных осложнений.
НЕДОПАМИНЕРГИЧЕСКИЕ СВОЙСТВА И ИХ ЛЕЧЕНИЕ
Широко распространенная и прогрессирующая нейродегенерация в головном мозге с болезнью Паркинсона приводит к появлению множества особенностей, которые вместе сгруппированы под названием немоторных симптомов.Это преимущественно, но не исключительно, следствие потери недофаминергических путей. Немоторные симптомы БП варьируются от когнитивных проблем, таких как апатия, депрессия, тревожные расстройства и галлюцинации, до утомляемости, нарушений походки и равновесия, гипофонии, нарушений сна, сексуальной дисфункции, проблем с кишечником, обильного потоотделения, сиалореи и боли. Эти симптомы часто вызывают наибольшее беспокойство у пациентов и вносят значительный вклад в заболеваемость и ухудшение качества жизни. 32 Медикаментозное лечение, доступное для решения этих проблем, ограничено.
Эти симптомы часто вызывают наибольшее беспокойство у пациентов и вносят значительный вклад в заболеваемость и ухудшение качества жизни. 32 Медикаментозное лечение, доступное для решения этих проблем, ограничено.
Депрессия и до некоторой степени апатия (ангедония) могут реагировать на трициклические препараты, такие как амитриптилин, или СИОЗС. Прамипексол может быть полезен в качестве антидепрессанта, отдельно от его действия по улучшению моторных характеристик БП, и показал некоторую пользу как у пациентов с депрессией без БП 33 , так и у пациентов с депрессией БП, 34 , хотя для подтверждения этого требуются дальнейшие исследования. эффект.Тревога и панические атаки могут быть заметными при БП, и хотя иногда они могут быть связаны со старением и, таким образом, реагировать на дофаминергическую терапию, может потребоваться дополнительная анксиолитическая терапия. Галлюцинации могут возникать как следствие нейродегенерации при БП и дофаминергических препаратов, используемых при лечении. Исследования показали, что агонисты дофамина в большей степени, чем леводопа, связаны с развитием галлюцинаций, особенно у пожилых людей. Если вызывает затруднения, модификация существующей терапии является самой простой стратегией для уменьшения или прекращения галлюцинаций, но у некоторых пациентов это сложно из-за повторного появления двигательных функций.Хорошо контролируемые клинические испытания показали, что низкие дозы клозапина могут значительно улучшить состояние пациентов с БП и психозами 35, 36 ; в качестве альтернативы некоторые могут реагировать на кветиапин. 37 Галлюцинации, безусловно, являются важным симптомом диффузной болезни с тельцами Леви, и их появление на ранних стадиях болезни Паркинсона является фактором риска деменции. Пациенты с болезнью Паркинсона, у которых развилось слабоумие по крайней мере через 2 года после появления двигательных особенностей, показали умеренное, но значительное улучшение когнитивных способностей с ривастигмином до степени, аналогичной той, которая наблюдается с этим лекарством при болезни Альцгеймера.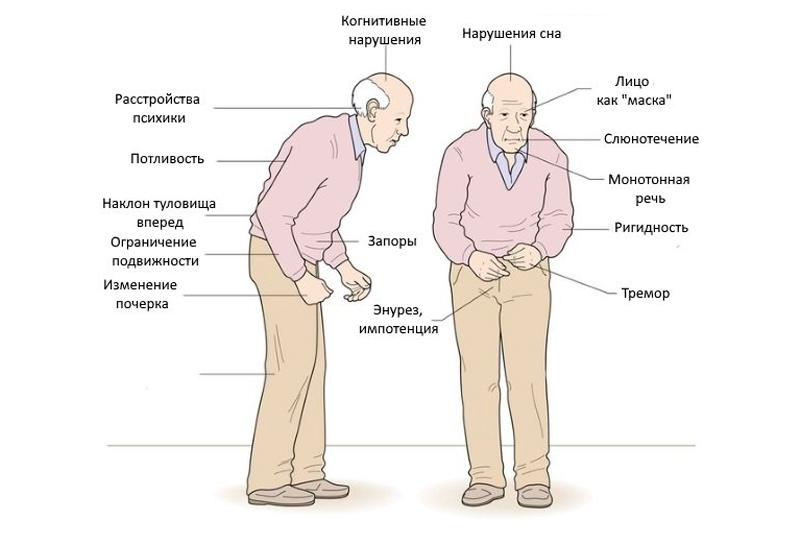 38
38
Нарушения сна обычны при БП и являются результатом естественных последствий старения, патологии основного заболевания, 39 моторных и немоторных осложнений, 40, 41 и лекарств. 42 Нарушение сна часто приводит к чрезмерной дневной сонливости, что, в свою очередь, может усугубляться седативным действием дофаминергических препаратов. 43 Доступно несколько стратегий для улучшения как ночного сна, так и дневной активности при БП, включая улучшение гигиены сна, лечение ночных двигательных проблем, лучшее лечение никтурии, изменение лекарств, 44 и использование модафинила у рефрактерных пациентов с дневная сонливость. 45
Половая дисфункция и дисфункция мочевого пузыря встречаются у обоих полов. Дофаминергическое лечение БП может привести к усилению полового влечения, но последствия болезни часто приводят к ухудшению сексуальной активности. 46 Неудивительно, что эта комбинация может вызвать расстройство, и силденафил или апоморфин в отдельных случаях могут эффективно справиться с этим. 47– 49 Аномалии мочевого пузыря вызывают проблемы особенно ночью, но с ними можно успешно справиться с помощью ряда методов, которые включают немедикаментозные, а также фармакологические стратегии. 50 Последние включают использование оксибутинина или детруситола или амитриптилина у пациентов с сопутствующей депрессией. Сиалорея и слюнотечение часто являются результатом уменьшения частоты глотания, и им могут помочь простые вещи, такие как жевательная резинка или сосание сладостей. Иногда могут помочь антихолинергические препараты, но часто они вызывают нежелательные побочные эффекты. Ботулинический токсин можно использовать в резистентных случаях. 51
Боль — частый симптом при БП, и у некоторых пациентов особенно проявляется боль в плече.Боль, беспокойство, акатизия, респираторный дистресс, депрессивные перепады настроения, замедленное и нарушенное мышление — это симптомы, которые могут возникать в периоды «выключения» и которые, по крайней мере частично, будут реагировать на дофаминергическую терапию. 52– 54 Признание того, что ряд немоторных свойств может улучшиться с помощью дофаминергических препаратов, важно для улучшения качества жизни пациентов с БП. 55
52– 54 Признание того, что ряд немоторных свойств может улучшиться с помощью дофаминергических препаратов, важно для улучшения качества жизни пациентов с БП. 55
НЕДОПАМИНЕРГИЧЕСКИЕ ПРОЦЕДУРЫ ДЛЯ PD
Использование антихолинергических средств при БП до введения леводопы и для некоторых врачей все еще остается терапией первой линии.Это особенно верно для пациентов с тремор-доминантным БП, хотя нет убедительных доказательств того, что антихолинергические препараты лучше, чем дофаминергические средства в этом отношении, 56 и оба часто имеют ограниченную ценность. Однако применение антихолинергических средств часто связано со значительными побочными эффектами, включая сухость во рту, когнитивные нарушения и, у мужчин, задержку мочи. Амантадин также использовался для лечения БП в течение нескольких лет и все еще может предложить некоторые полезные симптоматические средства контроля двигательных функций у части пациентов, хотя он значительно менее эффективен, чем дофаминергические средства. 57 Амантадин может быть полезен для уменьшения дискинезий, особенно при пиковых дозах, хотя данные ограничены, и польза обычно ограничивается 6–12 месяцами. 58
Альфа-2-адренергические рецепторы α-2a и 2c широко распространены в базальных ганглиях, включая черную субстанцию. Идазоксан и фипамезол, антагонисты α-2, уменьшают дискинезию, вызванную леводопой, и увеличивают продолжительность действия леводопы у приматов, получавших MPTP. 59– 62 Идазоксан показал различную пользу в клинических испытаниях. 63, 64 Интересно, что миртазапин, антидепрессант, основным действием которого является антагонизм рецептора α-2, уменьшал вызванные леводопой дискинезии у пациентов с БП. 65
Базальные ганглии получают значительный серотонинергический вход от ядер шва, и многие типы рецепторов 5HT присутствуют в полосатом теле и других областях базальных ганглиев.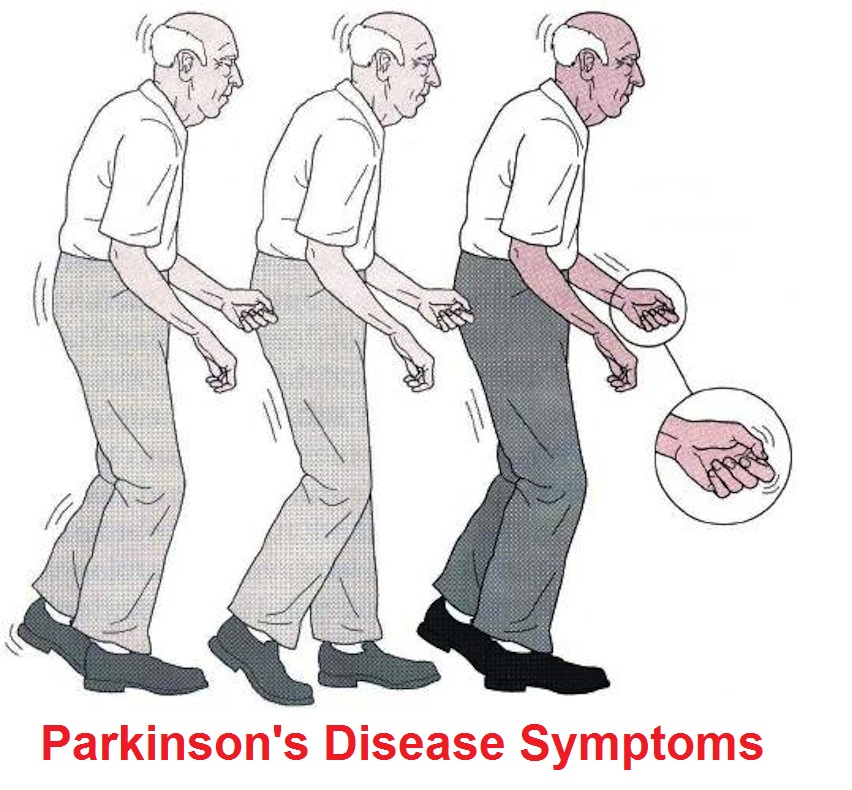 Флуоксетин, ингибитор обратного захвата 5HT, может подавлять вызванные леводопой дискинезии у пациентов с БП, 66, 67 , хотя, по-видимому, нет никаких различий в возникновении дискинезий у тех пациентов с БП, которые получают и не получают лечение СИОЗС. . 68 Использование СИОЗС иногда может быть связано с ухудшением двигательных функций БП.
Флуоксетин, ингибитор обратного захвата 5HT, может подавлять вызванные леводопой дискинезии у пациентов с БП, 66, 67 , хотя, по-видимому, нет никаких различий в возникновении дискинезий у тех пациентов с БП, которые получают и не получают лечение СИОЗС. . 68 Использование СИОЗС иногда может быть связано с ухудшением двигательных функций БП.
Антагонисты аденозиновых рецепторов A2a привлекли внимание как потенциальные симптоматические препараты для лечения болезни Паркинсона. Рецепторы A2a локализованы на шиповатых нейронах среднего стриатума и модулируют высвобождение ГАМК. 69– 71 Антагонисты A2a также влияют на высвобождение ацетилхолина из холинергических интернейронов полосатого тела и высвобождают дофамин из нигро-полосатого тракта. 71 Антагонист A2a, KW 6002, увеличивает двигательную активность у мышей, получавших МРТР, и потенцирует вращательное поведение, продуцируемое леводопой или агонистами дофамина, у крыс с односторонним поражением 6-OHDA. 72– 78 Такие препараты могут иметь важное значение не только для контроля симптомов БП, но и для предотвращения износа, наблюдаемого при длительном лечении. В модели приматов MPTP KW 6002 вызывал длительное улучшение двигательной активности без развития дискинезий. 79 Преимущества KW 6002 были добавлены к леводопе или агонисту дофамина даже при введении через 24–48 часов и не приводили к увеличению дискинезий. 80 Поскольку рецепторы A2a присутствуют в лимбических областях, гиппокампе и миндалине, антагонисты A2a также могут быть эффективными при лечении тревоги и депрессии при БП.
ИЗМЕНЕНИЕ ЗАБОЛЕВАНИЯ
Потенциальные преимущества успешной терапии модифицирующей болезнь при БП огромны. Однако истинная эффективность такой терапии может зависеть от того, способен ли предполагаемый агент защищать только дофаминергические нейроны или, предпочтительно, все типы нейронов, которые дегенерируют при этом заболевании. Если бы только первое, пациенту не удалось бы избежать недофаминергических свойств БП, которые доминируют над заболеванием на его более поздних стадиях.Однако в последнем случае преимущества будут серьезными и отсрочат или предотвратят инвалидность из-за как моторных, так и немоторных симптомов.
Если бы только первое, пациенту не удалось бы избежать недофаминергических свойств БП, которые доминируют над заболеванием на его более поздних стадиях.Однако в последнем случае преимущества будут серьезными и отсрочат или предотвратят инвалидность из-за как моторных, так и немоторных симптомов.
В нашем понимании этиологии и патогенеза БП достигнут значительный прогресс. 81 Было идентифицировано несколько генных мутаций, а другие локусы ждут уточнения и характеристики. 82 Факторы риска окружающей среды и воздействие потенциальных токсинов могут влиять на начало БП либо сами по себе, либо в сочетании с генетической предрасположенностью. 83 Биохимические аномалии, включая митохондриальную дисфункцию, повреждения, опосредованные свободными радикалами, эксайтотоксичность, воспалительные изменения и протеосомную дисфункцию, были идентифицированы в головном мозге при БП. Важно отметить, что эти аномалии стали мишенями для лекарств, потенциально изменяющих болезнь (рис. 1). Некоторые из этих препаратов были исследованы на лабораторных моделях БП, а некоторые из них, в свою очередь, изучались в клинических испытаниях (таблица 2). 84– 86
Стол 2Предполагаемые нейрозащитные агенты, которые были исследованы или в настоящее время проходят испытания для модификации болезни в PD
Рисунок 1Основные факторы, которые в настоящее время определены как способствующие этиологии и патогенезу БП.
Несколько соединений были изучены, и многие другие находятся в стадии оценки на предмет модификации болезни при БП. Исследование DATATOP показало, что селегилин (депренил) может отсрочить введение леводопы на ранних стадиях БП на 9–12 месяцев. 87 Интерпретация этого результата была затруднена из-за симптоматического эффекта селегилина. Чтобы избежать этого, селегилин сравнивали с плацебо, используя в качестве первичной конечной точки изменение моторной оценки между исходным визитом без лечения и последним визитом без лечения, проведенным после 12 месяцев лечения и 2 месяцев отмены исследуемого препарата. 88 У пациентов, получавших селегилин, ухудшение по сравнению с исходным уровнем было меньше, чем у пациентов, получавших плацебо, что снова указывает на то, что селегилин может обладать нейропротективным действием. Тем не менее, это исследование могло также быть затруднено из-за способности селегилина оказывать длительные симптоматические эффекты. Тем не менее, в долгосрочном последующем исследовании леводопы у пациентов, которые принимали селегилин в течение 7 лет по сравнению с теми, кто был переведен на плацебо через 5 лет, наблюдалось значительно более медленное снижение, меньшее истощение, включение-выключение и замерзание. , но больше дискинезий у тех, кто принимает селегилин. 89
88 У пациентов, получавших селегилин, ухудшение по сравнению с исходным уровнем было меньше, чем у пациентов, получавших плацебо, что снова указывает на то, что селегилин может обладать нейропротективным действием. Тем не менее, это исследование могло также быть затруднено из-за способности селегилина оказывать длительные симптоматические эффекты. Тем не менее, в долгосрочном последующем исследовании леводопы у пациентов, которые принимали селегилин в течение 7 лет по сравнению с теми, кто был переведен на плацебо через 5 лет, наблюдалось значительно более медленное снижение, меньшее истощение, включение-выключение и замерзание. , но больше дискинезий у тех, кто принимает селегилин. 89
Разагилин является более сильным ингибитором МАО-В, чем селегилин, и было показано, что он обеспечивает симптоматическое улучшение у пациентов с БП как с ранним, так и с поздним заболеванием. 28– 30 Этот препарат также продемонстрировал нейропротекторные эффекты на моделях БП in vitro и in vivo. Например, он защищает от токсичности MPTP / MPP и 6-гидроксидофамина и эксайтотоксических повреждений, а также стабилизирует потенциал митохондриальной мембраны для снижения апоптотической гибели клеток. 90– 93 Эти эффекты не зависят от его ингибирования MAO-B. В исследовании TEMPO пациенты с ранней стадией БП рандомизировались на группу плацебо или разагилина в дозе 1 или 2 мг и оценивалось прогрессирование с изменением по сравнению с исходным уровнем показателей UPDRS в течение 6 месяцев. На этом этапе группа плацебо была помещена на 2 мг разагилина, и все группы наблюдались в течение следующих 6 месяцев. В конце исследования скорость прогрессирования у пациентов, получавших разагилин, и у пациентов, перешедших на этот препарат, была ниже, чем в группе плацебо в течение первых 6 месяцев, при этом наклон двух групп, получавших лечение, проходил параллельно в течение второй половины периода. исследование (рис. 2). 94 Интерпретация результата ТЕМПО сложна. 95 Результаты не могут быть объяснены только симптоматическим эффектом, и, на первый взгляд, они представляют собой эффект ранней модификации болезни. Однако есть потенциальные побочные эффекты, в том числе длительная польза от более раннего лечения.
2). 94 Интерпретация результата ТЕМПО сложна. 95 Результаты не могут быть объяснены только симптоматическим эффектом, и, на первый взгляд, они представляют собой эффект ранней модификации болезни. Однако есть потенциальные побочные эффекты, в том числе длительная польза от более раннего лечения.
Сравнение между разагилином в течение 1 года и разагилином отсроченного действия. Величина эффекта при сравнении разагилина 1 мг / день в течение 1 года с разагилином отсроченного действия составила -1.8 ЕД (95% ДИ: от -3,64 до 0,01, p = 0,05), а величина эффекта при сравнении разагилина 2 мг / день в течение 1 года с разагилином отсроченного действия составила -2,3 Ед (95% ДИ: от -4,11 до -0,48, p = 0,01). 94
Коэнзим Q10 был оценен в пилотном исследовании ранних пациентов с БП, чтобы определить, может ли он иметь способность изменять болезнь. 96 Обоснование использования кофермента Q10 при БП было основано на наблюдении, что активность митохондриального комплекса I снижена при БП черной субстанции, у пациентов БП снижены уровни кофермента Q10, и это соединение защищает от токсичности МРТР.Коэнзим Q10 является одновременно антиоксидантом и неотъемлемым компонентом окислительного фосфорилирования, которое, как было показано, усиливает транспорт электронов. Пациенты были рандомизированы в группу плацебо или одну из трех доз коэнзима Q10 (300, 600 или 1200 мг) и наблюдались в течение 16 месяцев. Было отмечено значительное преимущество коэнзима Q10 в дозе 1200 мг с точки зрения изменения общих баллов UPDRS по сравнению с плацебо через 16 месяцев, а также незначительная тенденция к положительному эффекту для более низких доз. Этого интересного и важного результата достаточно, чтобы поддержать дальнейшее изучение кофермента Q10, но в настоящее время недостаточно, чтобы отстаивать то, что пациенты с БП должны использовать это соединение.
Агонисты дофамина продемонстрировали нейрозащитное действие в лабораторных условиях in vitro и in vivo. Они могут защищать клетки в тканевой культуре от токсического действия 1-метил-4-фенилпиридиния (MPP + ), 6-гидроксидофамина, ротенона и 3-нитропропионовой кислоты, а in vivo прамипексол защищает от дофаминергической потери клеток в субстанции. nigra в модели приматов MPTP. 97 Интересно, что исследования с использованием прамипексола показали, что защитное действие агонистов дофамина может не зависеть от наличия дофаминовых рецепторов. 98 Предварительная инкубация клеток культуры ткани или предшествующее воздействие агониста, по-видимому, является важным фактором действия агониста и может означать, что лекарство должно достичь определенных внутриклеточных компартментов или инициировать защитные клеточные реакции до воздействия токсина. Такое требование не препятствует клиническому применению, а скорее подчеркивает необходимость введения защитного агента на как можно более раннем этапе развития болезни.
Два исследования у пациентов с БП с ранним заболеванием были направлены на определение того, могут ли агонисты влиять на течение болезни.В исследовании CALM-PD использовалась однофотонная эмиссионная компьютерная томография (ОФЭКТ) beta-CIT для отслеживания скорости потери переносчика дофамина в качестве маркера плотности дофаминергических нигростриатных клеток. 99 Пациенты с БП были рандомизированы для приема прамипексола или леводопы и наблюдались в общей сложности в течение 4 лет; Добавки леводопы разрешались в обеих группах. Через 2, 3 и 4 года наблюдалось значительное снижение скорости потери переносчика в группе прамипексола, в среднем примерно на 40%.Аналогичный результат был получен в исследовании ропинирола REAL-PET, в котором использовался аналогичный дизайн исследования, но использовалась позитронно-эмиссионная томография (ПЭТ) для отслеживания потери плотности нигростриатных клеток при применении флуородопы. 100 Это продемонстрировало снижение примерно на 34% в группе ропинирола по сравнению с таковыми в группе леводопы. Как и в предыдущих исследованиях нейрозащиты, интерпретация результатов сложна. К сожалению, группа плацебо не была включена ни в одно исследование, поэтому неизвестно, был ли агонист защитным или токсичным для леводопы.
100 Это продемонстрировало снижение примерно на 34% в группе ропинирола по сравнению с таковыми в группе леводопы. Как и в предыдущих исследованиях нейрозащиты, интерпретация результатов сложна. К сожалению, группа плацебо не была включена ни в одно исследование, поэтому неизвестно, был ли агонист защитным или токсичным для леводопы.
В исследовании ELLDOPA пациенты с ранней стадией БП были рандомизированы в группу плацебо или в одну из трех групп лечения леводопой (150, 300 или 600 мг в день) и проводился анализ ОФЭКТ до и через 40 недель. 101 Группы леводопа показали более высокую скорость потери сигнала переносчика, чем группа плацебо, в течение периода испытания. Пациенты, получавшие леводопу, имели лучший балл по шкале UPDRS, чем пациенты, получавшие плацебо, после отмывания, хотя это было только в течение 2 недель, и нельзя было исключить продолжительный симптоматический эффект.Пациенты в группе высоких доз леводопы имели значительно больше дискинезий, чем в других группах.
Интерпретация приведенных выше исследований изображений осложняется возможностью того, что агонисты или леводопа сами могли модифицировать соответствующую экспрессию сигнала в ОФЭКТ или ПЭТ. Например, воздействие леводопа и / или агонистов может регулировать метаболизм дофамина или экспрессию переносчика. Однако объяснение результатов только на этой основе требует сложной модели, которая в настоящее время не поддерживается лабораторными данными. 86
Фактор роста нервов, происходящий из глиальных клеток (GDNF), важен для роста и поддержания дофаминергических клеток. Интрастриатальное или внутрижелудочковое введение GDNF приматам, не относящимся к человеку, получавшим МРТР, увеличивало плотность дофаминергических нейронов и улучшало двигательную функцию без дискинезий. 102, 103 Внутрижелудочковая инъекция GDNF пациентам не принесла пользы. 104 Пилотное исследование с участием пяти пациентов с БП, получавших интрапутаминальные инфузии GDNF, продемонстрировало значительное клиническое улучшение как моторных дефицитов и дискинезий, так и параллельное увеличение поглощения фтородопы на ПЭТ. 105 Крупное и слепое клиническое испытание интрапутаминального GDNF при БП было недавно прекращено, и, хотя результаты еще не опубликованы, неофициальные презентации позволяют предположить профиль нежелательных явлений.
105 Крупное и слепое клиническое испытание интрапутаминального GDNF при БП было недавно прекращено, и, хотя результаты еще не опубликованы, неофициальные презентации позволяют предположить профиль нежелательных явлений.
ВЫВОДЫ
Текущие варианты терапии БП по-прежнему сосредоточены на симптоматическом улучшении двигательных функций, связанных преимущественно с потерей дофаминергических нейронов в черной субстанции. Такое лечение эффективно снижает заболеваемость и смертность.Недавние исследования этиологии, патологии и патогенеза БП предоставляют важные возможности для разработки модифицирующих заболевание методов лечения, которые окажут даже большее влияние на болезнь, чем введение леводопы. Важно отметить, что текущие попытки определить группу риска по генетическим или клиническим причинам должны обеспечить идеальную группу для изучения потенциальных защитных методов лечения. Для более адекватной оценки лекарственных препаратов-кандидатов необходимы улучшения в дизайне испытаний, возможно, с введением проверенных клинических маркеров.Несмотря на все предостережения в интерпретации существующих исследований по изменению заболевания, лечащие врачи нуждаются в практическом руководстве, чтобы помочь пациентам принять решение о том, какое лекарство использовать и когда его начинать. Это остается во многом индивидуальным решением, и необходимо будет учитывать ряд факторов, включая возраст пациента и сопутствующие заболевания, а также собственную интерпретацию врачом имеющихся данных и информации, представленной здесь.
ССЫЛКИ
- ↵
Del Tredici K , Rub U, De Vos RA, et al. Где в головном мозге начинается патология болезни Паркинсона? J Neuropathol Exp Neurol 2002; 61: 413–26.
- ↵
Ponsen MM , Stoffers D, Booij J, et al. Идиопатическая гипосмия как доклинический признак болезни Паркинсона.
 Энн Нейрол 2004; 56: 173–81.
Энн Нейрол 2004; 56: 173–81. - ↵
Braak H , Del Tredici K, Rub U, et al. Стадия патологии головного мозга, связанной со спорадической болезнью Паркинсона.Neurobiol Aging 2003; 24: 197–211.
- ↵
Hughes AJ , Daniel SE, Ben Shlomo Y, et al. Точность диагностики паркинсонических синдромов в специализированной службе двигательных расстройств. Мозг 2002; 125: 861–70.
- ↵
Раджпут АХ . Леводопа продлевает продолжительность жизни и не токсичен для черной субстанции. Паркинсонизм, связанный с расстройством, 2001; 8: 95–100.
Karlsen KH , Tandberg E, Arsland D, et al. Качество жизни, связанное со здоровьем, при болезни Паркинсона: проспективное лонгитюдное исследование. J Neurol Neurosurg Psychiatry 2000; 69: 584–9.
- ↵
Clarke CE , Zobkiw RM, Gullaksen E. Качество жизни и помощь при болезни Паркинсона. Br J Clin Pract1995; 49: 288–93.
- ↵
Холливелл В . Окислители и центральная нервная система: некоторые фундаментальные вопросы. Имеет ли отношение окислительное повреждение к болезни Паркинсона, болезни Альцгеймера, травматическому повреждению или инсульту? Acta Neurol Scand Suppl1989; 126: 23–33.
- ↵
Пардо B , Мена М.А., Касарехос М.Дж., и др. Токсическое действие l-ДОФА на культуры мезэнцефальных клеток: защита с помощью антиоксидантов. Brain Res 1995; 682: 133–43.
- ↵
Walkinshaw G , Уотерс CM. Индукция апоптоза в катехоламинергических клетках PC12 с помощью L-DOPA.
 Значение для лечения болезни Паркинсона. Дж. Клин Инвест, 1995; 95: 2458–64.
Значение для лечения болезни Паркинсона. Дж. Клин Инвест, 1995; 95: 2458–64. - ↵
Dziewczapolski G , Murer G, Agid Y, et al. Отсутствие нейротоксичности хронической L-ДОФА у крыс с поражением 6-гидроксидофамином. Нейроотчет 1997; 8: 975–9.
- ↵
Murer MG , Dziewczapolski G, Menalled LB, et al. Хроническая леводопа не токсична для оставшихся дофаминовых нейронов, но вместо этого способствует их выздоровлению у крыс с умеренными нигростриатными поражениями.Энн Нейрол 1998; 43: 561–75.
- ↵
Ferrario JE , Taravini IR, Mourlevat S, et al. Дифференциальная экспрессия генов, индуцированная хроническим лечением леводопой в полосатом теле крыс с поражениями нигростриатальной системы. Журнал Neurochem 2004; 90: 1348–58.
- ↵
Agid Y , Olanow CW, Mizuno Y. Levodopa: почему полемика? Ланцет, 2002; 360: 575.
- ↵
Olanow CW , Agid Y, Mizuno Y, et al. Леводопа в лечении болезни Паркинсона: текущие споры. Mov Disord 2004; 19: 997–1005.
- ↵
Obeso JA , Olanow CW, Nutt JG. Моторные осложнения леводопы при болезни Паркинсона. Trends Neurosci2000; 23: S2–7.
- ↵
Kostic V , Przedborski S, Flaster E, et al. Раннее развитие дискинезий, вызванных леводопой, и колебания ответной реакции при болезни Паркинсона с ранним началом.Неврология 1991; 41: 202–5.
- ↵
Nutt JG , Woodward WR, Beckner RM, et al. Влияние периферического ингибирования катехол- O -метилтрансферазы на фармакокинетику и фармакодинамику леводопы у пациентов с паркинсонизмом.
 Неврология 1994; 44: 913–9.
Неврология 1994; 44: 913–9. - ↵
Heikkinen H , Nutt JG, LeWitt PA, et al. Влияние различных повторных доз энтакапона на фармакокинетику L-допа и клинический ответ на L-допа при болезни Паркинсона.Clin Neuropharmacol 2001; 24: 150–7.
- ↵
Jenner P , Al-Barghuthy G, Smith L, et al. Энтакапон в сочетании с L-допа усиливает противопаркинсоническую активность и предотвращает дискинезию на модели болезни Паркинсона (БП) приматов, получавших лечение МРТР. Mov Disord 2002; 17: S58.
- ↵
Общество расстройств движения (Комиссия целевой группы) . Управление болезнью Паркинсона: обзор, основанный на фактах.Mov Disord, 2002; 17 (приложение 4): S1–166.
- ↵
Holloway RG , Shoulson I, Fahn S, et al. Прамипексол против леводопы в качестве начального лечения болезни Паркинсона: 4-летнее рандомизированное контролируемое исследование. Arch Neurol 2004; 61: 1044–53.
- ↵
Rascol O , Brooks DJ, Korczyn AD, et al. Пятилетнее исследование частоты дискинезии у пациентов с ранней стадией болезни Паркинсона, получавших ропинирол или леводопу.056 Study Group. N Engl J Med 2000; 342: 1484–91.
- ↵
Stocchi F , Vacca L, Berardelli A, et al. Лечение двойным агонистом дофамина при болезни Паркинсона. Журнал Neurol 2003; 250: 822–6.
- ↵
Марко нашей эры , Аппиа-Куби Л.С., Чаудхури, КР. Использование агониста дофамина каберголина при лечении двигательных расстройств. Мнение эксперта Pharmacother2002; 3: 1481–7.
- ↵
Nutt JG , Obeso JA, Stocchi F.
 Непрерывная стимуляция дофаминовых рецепторов на поздних стадиях болезни Паркинсона. Trends Neurosci2000; 23: S109–15.
Непрерывная стимуляция дофаминовых рецепторов на поздних стадиях болезни Паркинсона. Trends Neurosci2000; 23: S109–15. - ↵
Van Camp G , Flamez A, Cosyns B, et al. Лечение болезни Паркинсона перголидом и в связи с рестриктивным пороком сердца. Ланцет 2004; 363: 1179–83.
- ↵
Rabey JM , Sagi I, Huberman M, et al. Разагилин мезилат, новый ингибитор МАО-B для лечения болезни Паркинсона: двойное слепое исследование в качестве дополнительной терапии к леводопе. Clin Neuropharmacol 2000; 23: 324–30.
Rascol O , Brooks DJ, Melamed E, et al. Сравнительное рандомизированное исследование разагилина по сравнению с плацебо или энтакапоном в качестве дополнения к леводопе у пациентов с болезнью Паркинсона (БП) с двигательными колебаниями (исследование LARGO). От имени исследовательской группы LARGO.Eur J Neurol 2003; 10: 234–44.
- ↵
Группа по изучению болезни Паркинсона . Контролируемое испытание разагилина на ранних стадиях болезни Паркинсона: исследование TEMPO. Arch Neurol, 2002; 59: 1937–43.
- ↵
Ives NJ , Stowe RL, Marro J, et al. Ингибиторы моноаминоксидазы типа B на ранних стадиях болезни Паркинсона: метаанализ 17 рандомизированных исследований с участием 3525 пациентов. BMJ 2004; 329: 593.
- ↵
Hely MA , Morris JG, Reid WG, et al. Сиднейское многоцентровое исследование болезни Паркинсона: проблемы, не связанные с L-допа, преобладают в возрасте 15 лет. Mov Disord 2005; 20 (2): 190–2.
- ↵
Corrigan MH , Denahan AQ, Wright CE, et al.
 Сравнение прамипексола, флуоксетина и плацебо у пациентов с большой депрессией. Депрессия тревоги 2000; 11: 58–65.
Сравнение прамипексола, флуоксетина и плацебо у пациентов с большой депрессией. Депрессия тревоги 2000; 11: 58–65. - ↵
Ректорова И , Ректор И, Барес М, и др. Прамипексол и перголид в лечении депрессии при болезни Паркинсона: национальное многоцентровое проспективное рандомизированное исследование. Eur J Neurol 2003; 10: 399–406.
- ↵
Pollak P , Tison F, Rascol O, et al. Клозапин при лекарственном психозе при болезни Паркинсона: рандомизированное плацебо-контролируемое исследование с открытым последующим наблюдением.J Neurol Neurosurg Psychiatry 2004; 75: 689–95.
- ↵
Группа по изучению болезни Паркинсона . Клозапин в низких дозах для лечения психоза, вызванного лекарственными препаратами, при болезни Паркинсона. N Engl J Med1999; 340: 757–63.
- ↵
Fernandez HH , Trieschmann ME, Burke MA, et al. Отдаленные результаты применения кветиапина при психозах у пациентов с паркинсонизмом. Mov Disord 2003; 18: 510–4.
- ↵
Emre M , Aarsland D, Albanese A, et al. Ривастигмин для лечения деменции, связанной с болезнью Паркинсона. N Engl J Med 2004; 351: 2509–18.
- ↵
Еллингер КА . Патология болезни Паркинсона. Изменения, отличные от нигростриатального пути. Mol Chem Neuropathol, 1991; 14: 153–97.
- ↵
Lees AJ , Blackburn NA, Campbell VL.Ночные проблемы болезни Паркинсона. Clin Neuropharmacol 1988; 11: 512–9.
- ↵
van Hilten B , Hoff JI, Middelkoop HA, et al.
 Нарушение сна при болезни Паркинсона. Оценка путем постоянного мониторинга активности. Arch Neurol 1994; 51: 922–8.
Нарушение сна при болезни Паркинсона. Оценка путем постоянного мониторинга активности. Arch Neurol 1994; 51: 922–8. - ↵
Paus S , Brecht HM, Koster J, et al. Приступы сна, дневная сонливость и агонисты дофамина при болезни Паркинсона.Mov Disord 2003; 18: 659–67.
- ↵
Hobson DE , Lang AE, Martin WR, et al. Чрезмерная дневная сонливость и внезапное начало сна при болезни Паркинсона: исследование Canadian Movement Disorders Group. JAMA 2002; 287: 455–63.
- ↵
Шапира АН . Чрезмерная дневная сонливость при болезни Паркинсона. Неврология 2004; 63: S24–7.
- ↵
Happe S , Pirker W, Sauter C, et al. Успешное лечение чрезмерной дневной сонливости при болезни Паркинсона с помощью модафинила. Журнал Neurol 2001; 248: 632–4.
- ↵
Бассон R . Секс и идиопатическая болезнь Паркинсона. Adv Neurol2001; 86: 295–300.
- ↵
Hussain IF , Brady CM, Swinn MJ, et al. Лечение эректильной дисфункции цитратом силденафила (Виагра) при паркинсонизме, вызванном болезнью Паркинсона или множественной системной атрофией, с наблюдениями за ортостатической гипотензией.J Neurol Neurosurg Psychiatry 2001; 71: 371–4.
Raffaele R , Vecchio I, Giammusso B, et al. Эффективность и безопасность перорального силденафила в фиксированной дозе при лечении сексуальной дисфункции у пациентов с депрессией и идиопатической болезнью Паркинсона. Eur Urol 2002; 41: 382–6.
- ↵
O’Sullivan JD .
 Апоморфин как альтернатива силденафилу при болезни Паркинсона.Журнал Neurol Neurosurg Psychiatry, 2002; 72: 681.
Апоморфин как альтернатива силденафилу при болезни Паркинсона.Журнал Neurol Neurosurg Psychiatry, 2002; 72: 681. - ↵
Stocchi F , Carbone A, Inghilleri M, et al. Уродинамическая и нейрофизиологическая оценка при болезни Паркинсона и множественной системной атрофии. J Neurol Neurosurg Psychiatry 1997; 62: 507–11.
- ↵
Mancini F , Zangaglia R, Cristina S, et al. Двойное слепое плацебо-контролируемое исследование по оценке эффективности и безопасности ботулинического токсина типа А при лечении слюнотечения при паркинсонизме.Mov Disord 2003; 18: 685–8.
- ↵
Марсден CD . Проблемы с длительной терапией леводопой при болезни Паркинсона. Clin Neuropharmacol1994; 17 (приложение 2): S32–44.
Hillen ME , Sage JI. Немоторные колебания у пациентов с болезнью Паркинсона. Неврология 1996; 47: 1180–3.
- ↵
Goetz CG , Tanner CM, Levy M, et al. Боль при болезни Паркинсона. Mov Disord 1986; 1: 45–9.
- ↵
Schenkman M , Wei ZC, Cutson TM, et al. Продольная оценка экономических и физических последствий болезни Паркинсона. Паркинсонизм относится к разногласиям 2001; 8: 41–50.
- ↵
Katzenschlager R , Sampaio C, Costa J, et al. Антихолинергические средства для симптоматического лечения болезни Паркинсона.Кокрановская база данных Syst Rev 2003; (2): CD003735.
- ↵
Кросби Нью-Джерси , Дин К. Х., Кларк CE. Амантадин при дискинезии при болезни Паркинсона.
 Кокрановская база данных Syst Rev2003; (1): CD003468.
Кокрановская база данных Syst Rev2003; (1): CD003468. - ↵
Thomas A , Iacono D, Luciano AL, et al. Продолжительность действия амантадина при дискинезии тяжелой болезни Паркинсона. Журнал Neurol Neurosurg Psychiatry 2004; 75: 141–3.
- ↵
Colpaert FC , Degryse AD, Van Craenendonck HV. Эффекты антагониста альфа-2 у 20-летней яванской обезьяны с симптомами паркинсонизма, вызванными МРТР. Brain Res Bull1991; 26: 627–31.
Grondin R , Hadj TA, Doan VD, et al. Антагонизм норадренорецепторов идазоксаном улучшает L-допа-индуцированные дискинезии у MPTP обезьян. Наунин Шмидебергс Arch Pharmacol 2000; 361: 181–6.
Генри Б. , Фокс С.Х., Пеггс Д., и др. Антагонист альфа2-адренергических рецепторов идазоксан снижает дискинезию и усиливает антипаркинсоническое действие L-допа в модели болезни Паркинсона с поражением МРТР у приматов. Mov Disord 1999; 14: 744–53.
- ↵
Savola JM , Hill M, Engstrom M, et al. Фипамезол (JP-1730) является мощным антагонистом альфа2-адренергических рецепторов, который снижает вызванную леводопой дискинезию в модели болезни Паркинсона у приматов, пораженных МРТР.Mov Disord 2003; 18: 872–83.
- ↵
Peyro-Saint-Paul H , Rascol O, Blin O, et al. Пилотное исследование идазоксана, антагониста альфа2, при болезни Паркинсона. Mov Disord 1996; 11: 116.
- ↵
Rascol O , Arnulf I, Brefel C, et al. Уменьшение индуцированных L-допа дискинезий антагонистом α2, идазоксаном, у пациентов с болезнью Паркинсона.
 Mov Disord 1991; 12: 111.
Mov Disord 1991; 12: 111. - ↵
Пакт V , Гидуз Т. Миртазапин лечит тремор покоя, эссенциальный тремор и дискинезии, вызванные леводопой. Неврология 1999; 53: 1154.
- ↵
Durif F , Vidailhet M, Bonnet AM, et al. Дискинезии, вызванные леводопой, снимаются флуоксетином. Неврология 1995; 45: 1855–8.
- ↵
Gomez-Mancilla B , Bedard PJ.Влияние недопаминергических препаратов на L-допа-индуцированные дискинезии у обезьян, получавших МФТП. Clin Neuropharmacol1993; 16: 418–27.
- ↵
Gony M , Lapeyre-Mestre M, Montastruc JL. Риск серьезных экстрапирамидных симптомов у пациентов с болезнью Паркинсона, получающих антидепрессанты: фармакоэпидемиологическое исследование, сравнивающее ингибиторы обратного захвата серотонина и другие антидепрессанты. Clin Neuropharmacol, 2003; 26: 142–5.
- ↵
Мори А , Синдо Т.Физиология аденозиновых рецепторов в регуляции полосатого тела проекционных нейронов полосатого тела. В: Kase H, Richardson PJ, Jenner P, eds. Аденозиновые рецепторы и болезнь Паркинсона. Сан-Диего: Academic Press, 2000.
Ochi M , Koga K, Kurokawa M, et al. Системное введение антагониста рецептора аденозина A (2A) обращает вспять повышенное высвобождение ГАМК в бледном глобусе крыс с односторонним поражением 6-гидроксидофамином: исследование микродиализа.Неврология 2000; 100: 53–62.
- ↵
Hauber W , Neuscheler P, Nagel J, et al. Каталепсия, вызванная блокадой дофаминовых рецепторов D1 или D2, была отменена сопутствующей блокадой аденозиновых рецепторов A (2A) в хвостатой скорлупе крыс.
 Eur J Neurosci 2001; 14: 1287–93.
Eur J Neurosci 2001; 14: 1287–93. - ↵
Shiozaki S , Ichikawa S, Nakamura J, et al. Действия антагониста аденозиновых рецепторов A2A KW-6002 на лекарственную каталепсию и гипокинезию, вызванные резерпином или MPTP.Психофармакология (Берл) 1999; 147: 90–5.
Wardas J , Konieczny J, Lorenc-Koci E. SCH 58261, антагонист рецептора аденозина A (2A), противодействует паркинсонической жесткости мышц у крыс. Synapse2001; 41: 160–71.
Carta AR , Pinna A, Tronci E, et al. Аденозин A2A и взаимодействия рецепторов дофамина в базальных ганглиях крыс, денервированных дофамином.Неврология 2003; 61: S39–43.
Кога К , Курокава М., Очи М., и др. Антагонисты рецепторов аденозина A (2A) KF17837 и KW-6002 потенцируют вращение, индуцированное дофаминергическими препаратами у крыс с паркинсонизмом. Eur J Pharmacol 2000; 408: 249–55.
Pinna A , Fenu S, Morelli M. Моторные стимулирующие эффекты антагониста рецептора аденозина A2A SCH 58261 не вызывают толерантности после повторных обработок у крыс с поражением 6-гидроксидофамином.Synapse2001; 39: 233–8.
Канда Т. , Джексон М.Дж., Смит Л.А., и др. Антагонист аденозина A2A: новый противопаркинсонический агент, не вызывающий дискинезии у паркинсонических обезьян. Энн Нейрол 1998; 43: 507–13.
- ↵
Канда Т. , Джексон М.Дж., Смит Л.А., и др. Комбинированное применение антагониста аденозина A (2A) KW-6002 с L-DOPA или с селективными агонистами дофамина D1 или D2 увеличивает противопаркинсоническую активность, но не дискинезию, у обезьян, получавших MPTP.
 Exp Neurol 2000; 162: 321–7.
Exp Neurol 2000; 162: 321–7. - ↵
Канда Т. , Джексон М.Дж., Смит Л.А., и др. Антагонист аденозина A2A: новый противопаркинсонический агент, не вызывающий дискинезии у паркинсонических обезьян. Энн Нейрол 1998; 43: 507–13.
- ↵
Канда Т. , Джексон М.Дж., Смит Л.А., и др. Комбинированное применение антагониста аденозина A (2A) KW-6002 с L-DOPA или с селективными агонистами дофамина D1 или D2 увеличивает противопаркинсоническую активность, но не дискинезию, у обезьян, получавших MPTP.Exp Neurol 2000; 162: 321–7.
- ↵
Dawson TM , Dawson VL. Молекулярные пути нейродегенерации при болезни Паркинсона. Science2003; 302: 819–22.
- ↵
Healy DG , Abou-Sleiman PM, Wood NW. РОЗОВЫЙ, ПАНК или ПАРК? Справочник клиницистов по семейному паркинсонизму. Lancet Neurol 2004; 3: 652–62.
- ↵
Ди Монте DA .Окружающая среда и болезнь Паркинсона: является ли нигростриатальная система мишенью преимущественно нейротоксинов? Ланцет Neurol 2003; 2: 531–8.
- ↵
Кларк CE . Нейропротекция и фармакотерапия двигательных симптомов при болезни Паркинсона. Lancet Neurol 2004; 3: 466–74.
Шапира АН . Модификация болезни при болезни Паркинсона. Ланцет Neurol 2004; 3: 362–8.
- ↵
Schapira AH , Olanow CW.Нейропротекция при болезни Паркинсона. JAMA2004; 291: 358–64.
- ↵
Группа по изучению болезни Паркинсона . Влияние токоферола и депренила на прогрессирование инвалидности на ранних стадиях болезни Паркинсона.
 N Engl J Med1993; 328: 176–83.
N Engl J Med1993; 328: 176–83. - ↵
Olanow CW , Hauser RA, Gauger L, et al. Влияние депренила и леводопы на прогрессирование болезни Паркинсона.Энн Нейрол 1995; 38: 771–7.
- ↵
Shoulson I , Oakes D, Fahn S, et al. Влияние длительного депренила (селегилина) на болезнь Паркинсона, леченную леводопой: рандомизированное плацебо-контролируемое расширение антиоксидантной терапии депренилом и токоферолом в испытании паркинсонизма. Энн Нейрол 2002; 51: 604–12.
- ↵
Akao Y , Maruyama W, Yi H, et al. Лекарственное средство против болезни Паркинсона, N -пропаргил-1 ( R ) -аминоиндан (разагилин), усиливает экспрессию антиапоптотического bcl-2 в дофаминергических SH-SY5Y клетках человека. Neurosci Lett 2002; 326: 105–8.
Am OB , Amit T, Youdim MB. Противопоставление нейропротекторного и нейротоксического действия соответствующих метаболитов антипаркинсонических препаратов разагилина и селегилина. Neurosci Lett, 2004; 355: 169–72.
Maruyama W , Takahashi T, Youdim M, et al. Препарат против Паркинсона, разагилин, предотвращает апоптотическое повреждение ДНК, вызванное пероксинитритом в клетках дофаминергической нейробластомы человека SH-SY5Y. Журнал Neural Transm 2002; 109: 467–81.
- ↵
Дженнер П. . Доклинические доказательства нейропротекции ингибиторами моноаминоксидазы-B при болезни Паркинсона. Неврология 2004; 63: S13–22.
- ↵
Группа по изучению болезни Паркинсона .Контролируемое рандомизированное исследование с отложенным началом применения разагилина на ранних стадиях болезни Паркинсона.
 Arch Neurol 2004; 61: 561–6.
Arch Neurol 2004; 61: 561–6. - ↵
Раскол О . Ингибиторы моноаминоксидазы — пора ли переходить на ТЕМПО? Lancet Neurol 2003; 2: 142–3.
- ↵
Shults CW , Oakes D, Kieburtz K, et al. Эффекты коэнзима Q10 на ранних стадиях болезни Паркинсона: свидетельство замедления функционального спада.Arch Neurol 2002; 59: 1541–50.
- ↵
Schapira AH , Olanow CW. Обоснование использования агонистов дофамина в качестве нейрозащитных средств при болезни Паркинсона. Энн Нейрол, 2003; 53 (приложение 3): S149–57.
- ↵
Gu M , Irvani M, Cooper JM, et al. Прамипексол защищает от апоптотической гибели клеток недофаминергическими механизмами. Журнал Neurochem 2004; 91: 1075–81.
- ↵
Группа по изучению болезни Паркинсона . Визуализация мозга переносчика дофамина для оценки эффектов прамипексола по сравнению с леводопой на прогрессирование болезни Паркинсона. JAMA2002; 287: 1653–61.
- ↵
Whone AL , Watts RL, Stoessl AJ, et al. Более медленное прогрессирование болезни Паркинсона при применении ропинирола по сравнению с леводопой: исследование REAL-PET. Энн Нейрол 2003; 54: 93–101.
- ↵
Fahn S , Oakes D, Shoulson I, et al. Леводопа и прогрессирование болезни Паркинсона. N Engl J Med 2004; 351: 2498–508.
- ↵
Kordower JH , Emborg ME, Bloch J, et al. Нейродегенерация предотвращается за счет доставки GDNF лентивирусным вектором в моделях болезни Паркинсона на приматах.
 Наука 2000; 290: 767–73.
Наука 2000; 290: 767–73. - ↵
Grondin R , Zhang Z, Yi A, et al. Хроническая контролируемая инфузия GDNF способствует структурному и функциональному восстановлению у продвинутых паркинсонических обезьян.Мозг 2002; 125: 2191–201.
- ↵
Nutt JG , Burchiel KJ, Comella CL, et al. Рандомизированное двойное слепое испытание нейротрофического фактора линии глиальных клеток (GDNF) при БП. Неврология 2003; 60: 69–73.
- ↵
Gill SS , Patel NK, Hotton GR, et al. Прямая инфузия нейротрофического фактора линии глиальных клеток при болезни Паркинсона.Нат Мед 2003; 9: 589–95.
Болезнь Паркинсона | Сидарс-Синай
Не то, что вы ищете?Что такое болезнь Паркинсона?
Болезнь Паркинсона (также называемая БП или Паркинсон) — наиболее распространенная форма паркинсонизма, группа двигательной системы. расстройства. Это заболевание, которое со временем постепенно ухудшается. Пока диагностика БП это событие, изменившее жизнь, было обнаружено, что у большинства людей и их семей есть хорошо качество жизни после начального периода адаптации.
PD вызвано потерей мозга клетки, вырабатывающие дофамин. Дофамин — это вещество, которое помогает сглаживать и скоординировано движение мышц. Паркинсон часто вызывает следующие симптомы:
- Тремор или дрожание рук, челюсти, ноги и лицо
- Скованность или жесткость конечностей и сундук
- Замедленность движения (брадикинезия)
- Проблемы с балансом и координация
Что вызывает болезнь Паркинсона?
Причина болезни Паркинсона неизвестна. Эксперты считают, что симптомы связаны с химическим дисбалансом в мозге, вызванным:
от
смерть клеток головного мозга. Паркинсон хронический. Симптомы со временем ухудшаются.
Эксперты считают, что симптомы связаны с химическим дисбалансом в мозге, вызванным:
от
смерть клеток головного мозга. Паркинсон хронический. Симптомы со временем ухудшаются.
Заболевание может появиться у молодых люди (даже подростки). Но часто это поражает людей в позднем среднем возрасте. Нет заразительный.
Эксперты считают, что у большинства людей Причина болезни Паркинсона — сочетание генов и окружающей среды.Исследования показали, что сельская жизнь, воздействие колодезной воды, а также воздействие сельскохозяйственных пестицидов и гербициды связаны с болезнью Паркинсона. Но эти факторы не гарантируют, что вы получите в болезнь. Этому не мешает и их отсутствие.
При других формах паркинсонизма, либо причина известна, либо подозревается. Или расстройство возникает как вторичный эффект из какая-то другая неврологическая проблема.Эти формы иногда называют синдромом Паркинсона, атипичный Паркинсон, или попросту паркинсонизм. Они могут быть вызваны:
- Опухоли головного мозга
- Повторная травма головы, например, из бокса
- Длительное употребление некоторых лекарств, таких как фенотиазины, бутирофеноны, или резерпин при проблемах с психическим здоровьем и метоклопрамид при расстройстве желудка
- Токсины, такие как марганец и окись углерода отравление
- Постэнцефалитный паркинсонизм, вирусное заболевание, вызывающее «сонная болезнь»
- Стриатонигральная дегенерация, заболевание, поражающее часть мозга, называемая черной субстанцией
Паркинсонизм также может возникать при других проблемах нервной системы. К ним относятся:
К ним относятся:
- Синдром Шай-Драгера
- Прогрессирующий надъядерный паралич
- Болезнь Вильсона
- Болезнь Хантингтона
- Синдром Халлервордена-Шпатца
- Болезнь Альцгеймера
- Болезнь Крейтцфельдта-Якоба
- Оливопонтоцеребеллярная атрофия
- Посттравматическая энцефалопатия
- Деменция с тельцами Леви
Кто подвержен риску болезни Паркинсона?
Самый большой фактор риска Паркинсон стареет.Средний возраст появления симптомов Паркинсона — 70 лет. годы. Мужчины страдают больше, чем женщины. Но причина этого неясна.
Семейный анамнез — еще один ключевой риск фактор. У человека с заболевшим родителем или братом или сестрой больше шансов получить Паркинсон. Этот более высокий риск, скорее всего, связан с сочетанием факторов окружающей среды и генетических факторов. факторы. Наличие одного или нескольких близких родственников с болезнью Паркинсона повышает риск болезнь, как и воздействие токсинов окружающей среды.
Каковы симптомы болезни Паркинсона?
Это наиболее частые симптомы болезни Паркинсона:
- Жесткие мышцы. Жесткость при рука, нога или шея двигаются вперед и назад.
- Тремор покоя. Тремор (непроизвольный движение от сокращающихся мышц), что наиболее очевидно в состоянии покоя.
- Брадикинезия. Медленный запуск
движение.

- Постуральная нестабильность. Плохая осанка и равновесие, которое может вызвать падения или проблемы с походкой.
Симптомы Паркинсона варьируются от С глазу на глаз. Симптомы могут проявляться медленно и в произвольном порядке. Ранние симптомы может быть тонким.Они могут медленно ухудшаться в течение многих лет, прежде чем достигнут точки, когда они нарушают нормальную повседневную деятельность.
Остальные симптомы делятся на моторные (связанные с движением) и немоторные симптомы.
Двигательные симптомы:
- Тремор
- Замедленное движение (брадикинезия)
- Жесткость и примерзание
- Наклонная осанка
- Шаркающая походка
- Уменьшение размаха рук при ходьбе
- Проблемы с вставанием со стула
- Мелкий, сжатый почерк (микрофотография)
- Отсутствие мимики
- Замедленная повседневная активность (например, еда, одевание и купание)
- Проблемы с переворачиванием в постели
- Длительное пребывание в определенной позиции
Немоторные симптомы
- Нарушение обоняния
- Низкая громкость голоса (гипофония)
- Проблемы с речью (дизартрия)
- Болезненные судороги стопы
- Проблемы со сном
- Депрессия
- Эмоциональные изменения (пугающие и неуверенные)
- Проблемы с кожей
- Запор
- Слюни
- Повышенное потоотделение
- Частое или неотложное мочеиспускание
- Мужская эректильная дисфункция
По мере обострения болезни ходьба
может пострадать. Это может привести к тому, что человек остановится на полпути или «замерзнет» в
место,
и может даже упасть. Люди также могут начать ходить с серии быстрых, небольших
шаги, словно торопясь вперед, чтобы удержать равновесие. Это называется фестинацией.
Это может привести к тому, что человек остановится на полпути или «замерзнет» в
место,
и может даже упасть. Люди также могут начать ходить с серии быстрых, небольших
шаги, словно торопясь вперед, чтобы удержать равновесие. Это называется фестинацией.
Симптомы болезни Паркинсона могут выглядеть как и другие проблемы со здоровьем. Всегда обращайтесь к своему врачу за диагнозом.
Как диагностируется болезнь Паркинсона?
Диагностика Паркинсона на ранней стадии этапы могут быть трудными.Сначала признаки и симптомы могут выглядеть как другие проблемы со здоровьем. или же последствия нормального старения. По этой причине ваш лечащий врач может захотеть смотреть ваши симптомы в течение некоторого времени, пока они не исчезнут постоянно.
Прямо сейчас нет ни крови, ни лабораторные тесты для диагностики Паркинсона. Диагностика Паркинсона основывается главным образом на состоянии здоровья. анамнез и обследование нервной системы. Сканирование мозга или лабораторные тесты могут быть выполнены, чтобы помочь правилу. вне другие заболевания или состояния.Но сканирование мозга в целом окажется нормальным. с участием Паркинсон.
Вам может понадобиться:
- Неврологический осмотр. Это включает изучение симптомов и насколько они серьезны.
- Пробные испытания лекарственных средств. Когда симптомы тяжелые, испытание
можно использовать тест на лекарства (в основном леводопа или L-допа).Если симптомы облегчаются из-за
использование леводопы, это предполагает болезнь Паркинсона.

- Компьютерная томография. В этом тесте визуализации используются рентгеновские лучи и компьютер для делать изображения тела, включая кости, мышцы, жир и органы. КТ сканирование более подробный, чем обычные рентгеновские снимки.
- МРТ. В этом тесте используются большие магниты, радиоволны и компьютер, чтобы делать подробные изображения органов и структур внутри тела.
Как лечится болезнь Паркинсона?
Пока нет лекарства от Паркинсон. Но ваш лечащий врач может спланировать лечение в зависимости от тяжести в симптомы и прогрессирование болезни. PD не влияет на людей одинаково. Ты может потребоваться:
- Медицина
- Хирургия
- Дополняющая и поддерживающая методы лечения, такие как диета, упражнения, консультации, управление стрессом, физиотерапия, трудотерапия и логопедия
После постановки диагноза, следующее решение — это лекарство.Это зависит от:
- Насколько сильно поразило заболевание ваша физическая активность и мышление
- Способность терпеть противопаркинсоническая медицина
- Совет врача и ваши предпочтения
Нет двух людей, которые одинаково реагируют на
данное лекарство.Требуются время и терпение, чтобы найти правильное лекарство и дозу.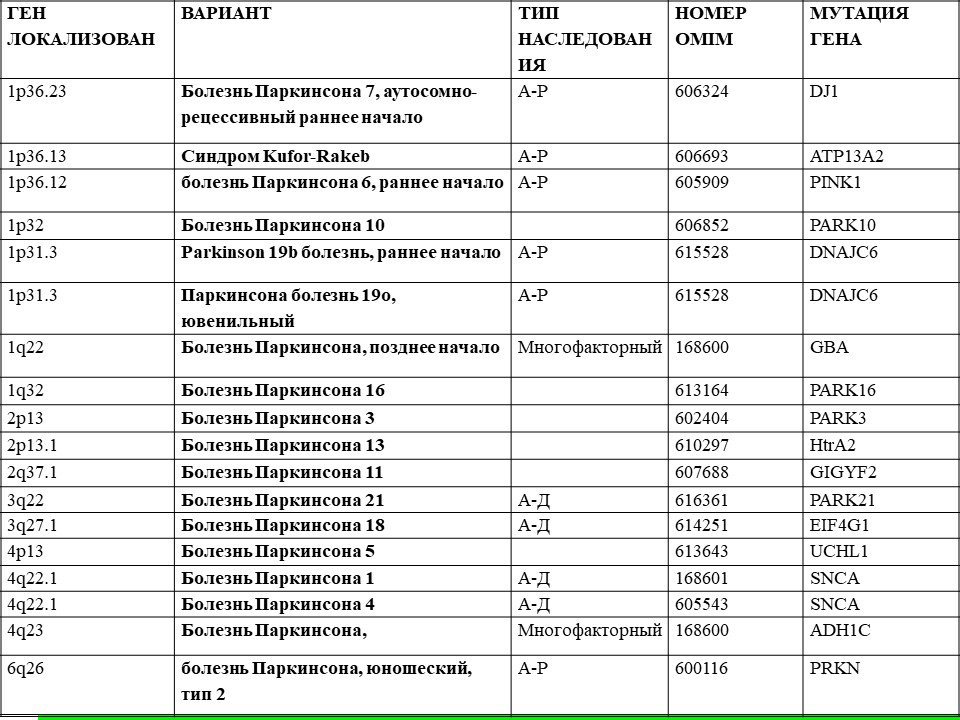 простота
симптомы.
простота
симптомы.
В некоторых случаях ваше Поставщик может посоветовать операцию. Хирургия может помочь с симптомами. Но это не лечит в болезнь или остановить ее ухудшение.
Может помочь при треморе или ригидности что приходит с болезнью. У некоторых людей операция может уменьшить количество лекарства. необходимо контролировать симптомы болезни Паркинсона.
Есть два типа операций при болезни Паркинсона:
- Хирургия повреждений (рубцевание тканей). В этой процедуре небольшие повреждения или шрамы остаются в глубоких частях мозга, которые помогают контролировать движение. Операция может быть сделана, пока вы не спите, чтобы помочь найти точный размещение поражения. Повреждение помещается, чтобы помочь контролировать или остановить область в мозг, вызывающий тремор.
- Глубокая стимуляция мозга (DBS). При этом типе хирургии небольшой электрод помещается в глубокие части мозга, которые помогают контролировать движение. Электрод прикреплен к небольшой батарее в грудной стенке. Это связано провода, которые кладут под кожу. Затем включается стимулятор. Это прерывает нормальный поток информации в мозгу и может помочь уменьшить симптомы Паркинсон.
Жизнь с болезнью Паркинсона
Хотя болезнь Паркинсона хроническое неизлечимое заболевание, лечение может помочь облегчить симптомы и улучшить ваше качество из жизнь. Вы также можете многое сделать, чтобы оставаться независимым, например:
- Правильное питание
- Сохранение мобильности с помощью вспомогательных устройств, при необходимости
- Регулярно занимаются спортом
- Занятия физиотерапией, трудотерапией и речью терапия, при необходимости
Также поговорите со своим врачом о депрессии, тревоге или
другие проблемы с психическим здоровьем, которые могут возникнуть.
Общественные агентства могут помочь вам и вашей семье приспособиться к диагностика болезни Паркинсона. Фонд Паркинсона предоставляет различные образовательные ресурсы для пациентов и членов их семей. Здесь также есть телефон доверия. со специалистами по болезни Паркинсона, которые могут предложить поддержку людям с болезнью Паркинсона, лицам, осуществляющим уход, и поставщики медицинских услуг. По телефону доверия можно получить информацию об эмоциональной поддержке, текущих Медицинская информация, связанная с PD, и местные ресурсы.Телефон доверия доступен по адресу 800-4PD-INFO (800-473-4636) или [email protected] .
Основные сведения о болезни Паркинсона
- Паркинсон — заболевание двигательной системы. Со временем ситуация постепенно ухудшается, но лечение, здоровый образ жизни и община поддержка может улучшить общее качество жизни человека.
- Наиболее частые симптомы — мышечные ригидность, тремор покоя, медленное начало движения и осанка нестабильность.
- Не существует известного лекарства от Паркинсона. Но лекарства и хирургическое вмешательство могут помочь контролировать симптомы.
- Здоровое питание, регулярные упражнения, физиотерапия, трудотерапия и логопедия могут способствовать независимость.
Следующие шаги
Советы, которые помогут вам получить максимальную пользу от посещения врача:
- Знайте причину вашего визита и то, что вы хотите.
- Перед визитом запишите вопросы, на которые хотите получить ответы.


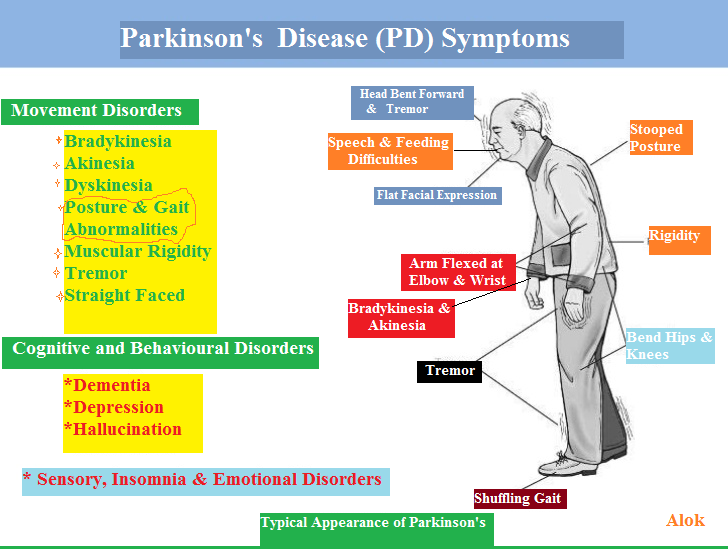 Исследователи объясняют, что болезнь заставляет мозг вырабатывать меньше клеток головного мозга определенного типа (базальных ганглиев), которые помогают части головного мозга приказывать нам двигать мышцами.Замедленность движений может проявляться во многих формах (которые мы вскоре обсудим), а брадикинезия может вынудить больных тратить больше времени на выполнение рутинных действий и в конечном итоге потерять координацию.
Исследователи объясняют, что болезнь заставляет мозг вырабатывать меньше клеток головного мозга определенного типа (базальных ганглиев), которые помогают части головного мозга приказывать нам двигать мышцами.Замедленность движений может проявляться во многих формах (которые мы вскоре обсудим), а брадикинезия может вынудить больных тратить больше времени на выполнение рутинных действий и в конечном итоге потерять координацию. Как и уменьшение выражений лица, неустойчивый баланс частично связан с брадикинезией, поскольку неспособность вашего тела двигать мускулами так быстро при реакции на определенные движения может вызвать падения и общую нестабильность. Неустойчивое равновесие — и попытки чрезмерной компенсации, наклоняясь или наклоняясь определенным образом, чтобы предотвратить постоянные падения, — могут привести к неправильной осанке. Многие из этих симптомов взаимосвязаны, так как один может вызвать цепную реакцию, вызывая другие.
Как и уменьшение выражений лица, неустойчивый баланс частично связан с брадикинезией, поскольку неспособность вашего тела двигать мускулами так быстро при реакции на определенные движения может вызвать падения и общую нестабильность. Неустойчивое равновесие — и попытки чрезмерной компенсации, наклоняясь или наклоняясь определенным образом, чтобы предотвратить постоянные падения, — могут привести к неправильной осанке. Многие из этих симптомов взаимосвязаны, так как один может вызвать цепную реакцию, вызывая другие. У людей, страдающих этим заболеванием, дофамина на 60-80 процентов меньше, чем у среднего человека.
У людей, страдающих этим заболеванием, дофамина на 60-80 процентов меньше, чем у среднего человека. В некоторых случаях агонисты дофамина принимают вместе с леводопой, чтобы помочь найти здоровый баланс между двумя лекарствами и ограничить побочные эффекты от обоих методов лечения. Побочные эффекты агонистов дофамина аналогичны побочным эффектам леводопы, но есть и другие серьезные побочные эффекты, включая галлюцинации и спорадическое поведение за пределами вашей личности.
В некоторых случаях агонисты дофамина принимают вместе с леводопой, чтобы помочь найти здоровый баланс между двумя лекарствами и ограничить побочные эффекты от обоих методов лечения. Побочные эффекты агонистов дофамина аналогичны побочным эффектам леводопы, но есть и другие серьезные побочные эффекты, включая галлюцинации и спорадическое поведение за пределами вашей личности. Энн Нейрол 2004; 56: 173–81.
Энн Нейрол 2004; 56: 173–81.  Значение для лечения болезни Паркинсона. Дж. Клин Инвест, 1995; 95: 2458–64.
Значение для лечения болезни Паркинсона. Дж. Клин Инвест, 1995; 95: 2458–64. Неврология 1994; 44: 913–9.
Неврология 1994; 44: 913–9.  Непрерывная стимуляция дофаминовых рецепторов на поздних стадиях болезни Паркинсона. Trends Neurosci2000; 23: S109–15.
Непрерывная стимуляция дофаминовых рецепторов на поздних стадиях болезни Паркинсона. Trends Neurosci2000; 23: S109–15.  Сравнение прамипексола, флуоксетина и плацебо у пациентов с большой депрессией. Депрессия тревоги 2000; 11: 58–65.
Сравнение прамипексола, флуоксетина и плацебо у пациентов с большой депрессией. Депрессия тревоги 2000; 11: 58–65. Нарушение сна при болезни Паркинсона. Оценка путем постоянного мониторинга активности. Arch Neurol 1994; 51: 922–8.
Нарушение сна при болезни Паркинсона. Оценка путем постоянного мониторинга активности. Arch Neurol 1994; 51: 922–8.  Апоморфин как альтернатива силденафилу при болезни Паркинсона.Журнал Neurol Neurosurg Psychiatry, 2002; 72: 681.
Апоморфин как альтернатива силденафилу при болезни Паркинсона.Журнал Neurol Neurosurg Psychiatry, 2002; 72: 681. 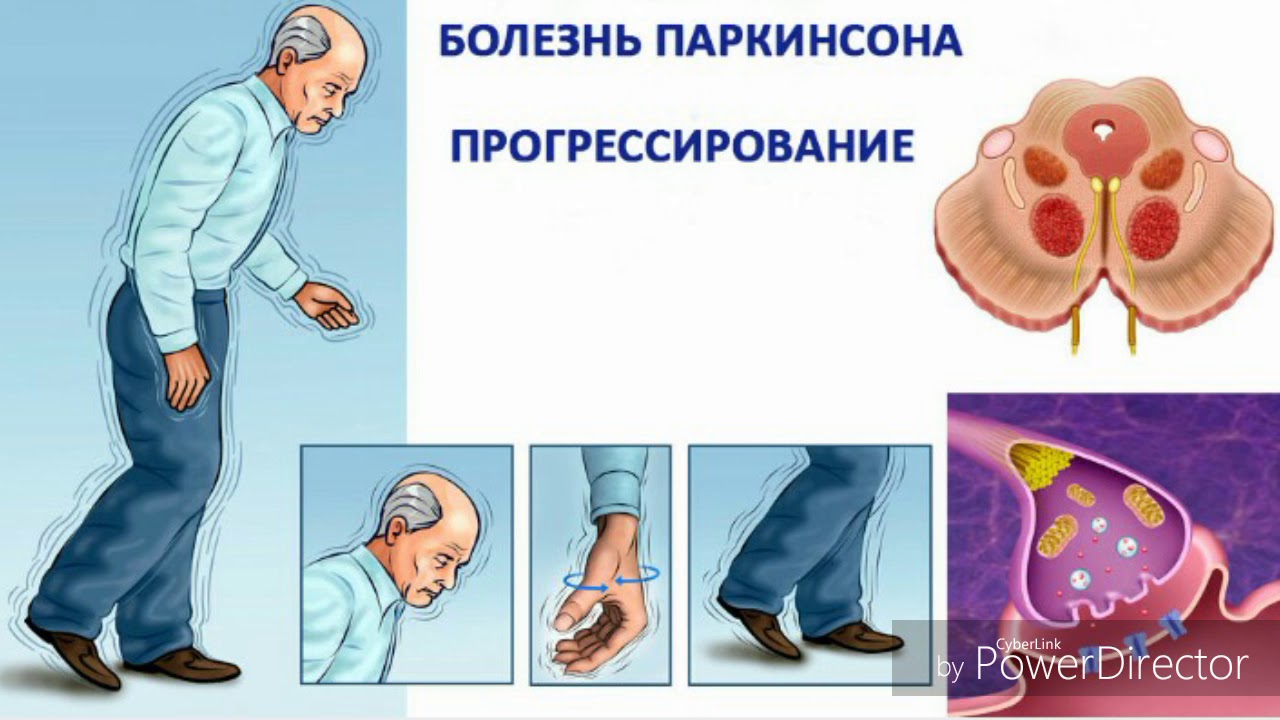 Кокрановская база данных Syst Rev2003; (1): CD003468.
Кокрановская база данных Syst Rev2003; (1): CD003468.  Mov Disord 1991; 12: 111.
Mov Disord 1991; 12: 111.  Eur J Neurosci 2001; 14: 1287–93.
Eur J Neurosci 2001; 14: 1287–93.  Exp Neurol 2000; 162: 321–7.
Exp Neurol 2000; 162: 321–7. 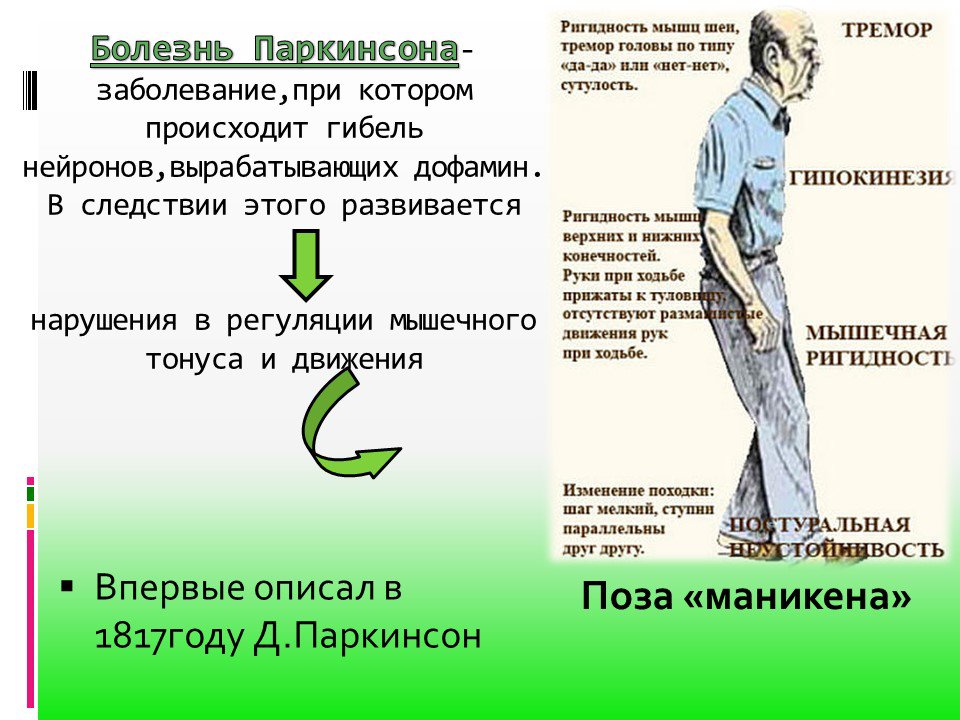 N Engl J Med1993; 328: 176–83.
N Engl J Med1993; 328: 176–83.  Наука 2000; 290: 767–73.
Наука 2000; 290: 767–73. 