Болезнь паркинсона формы: симптомы, признаки и причины, диагностика и лечение
Моногенные формы болезни Паркинсона Текст научной статьи по специальности «Клиническая медицина»
На территориях ОЛ нет случаев присасывания клещей. На высоком уровне организована санитарно-просветительная работа. Качество
медицинского сопровождения летней оздоровительной кампании в ЗАТО г. Железногорск может служить примером для других территорий
ОБЗОР
© ШНАЙДЕР Н.А., САПРОНОВА М.Р
МОНОГЕННЫЕ ФОРМЫ БОЛЕЗНИ ПАРКИНСОНА Н.А. Шнайдер, М.Р. Сапронова
ФГБУЗ Клиническая больница №51 ФМБА, Кабинет экстрапирамидной патологии, Железногорск Красноярского края; ГБОУ ВПО Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого Министерства здравоохранения и социального
развития Российской Федерации, Красноярск, РФ
660022, Красноярск, ул. Партизана Железняка, 1. E-mail: [email protected]
Партизана Железняка, 1. E-mail: [email protected]
Резюме. Болезнь Паркинсона — нейродегенеративное заболевание, характеризующееся гибелью нигростриарных дофаминергических нейронов. В большинстве случаев болезнь Паркинсона является мультифакториальной патологией. Однако в последние годы убедительно доказано, что наследственный компонент играет важную роль в развитии заболевания. К настоящему времени известно 11 генов, ассоциированных с развитием семейной формы болезни Паркинсона. В статье представлен обзор генетических исследований зарубежных и отечественных авторов. Выявлено 7 генов, ассоциированных с развитием наследственной формы болезни Паркинсона с аутосомно-доминантным типом наследования и 4 гена — с аутосомно-рецессивным типом наследования. Ключевые слова: болезнь Паркинсона, генетика.
Введение. Болезнь Паркинсона (БП) -прогрессирующее нейродегенеративное заболевание центральной нервной системы. В большинстве случаев БП является мультифактор-ным заболеванием, в развитии которого играют роль как генетические, так и внешнесредовые факторы. Приблизительно у 10-20 % пациентов с БП прослеживается семейный анамнез, моногенные формы заболевания достаточно редки и встречаются в среднем в 5-10% случаев [1]. Частота встречаемости заболевания достигает 1% среди населения старше 65 лет и более 4% среди населения в возрасте 85 лет [2].
В большинстве случаев БП является мультифактор-ным заболеванием, в развитии которого играют роль как генетические, так и внешнесредовые факторы. Приблизительно у 10-20 % пациентов с БП прослеживается семейный анамнез, моногенные формы заболевания достаточно редки и встречаются в среднем в 5-10% случаев [1]. Частота встречаемости заболевания достигает 1% среди населения старше 65 лет и более 4% среди населения в возрасте 85 лет [2].
Ядро клинической картины БП составляют моторные симптомы. Однако, в последние годы установлено, что БП — это мультисистем-ная патология с поражением различных меди-аторных систем, что обусловливает развитие широкого спектра не моторных симптомов, таких как вегетативная дисфункция, когнитивные нарушения, депрессия, обонятельный дефицит, психические расстройства и нарушение сна. Моторные симптомы являются результатом прогрессивной потери дофаминергических нейронов компактной части черной субстанции. Клинические симптомы становятся очевидными, когда уровень стриального дофамина снижается до 20%.
Гены, ассоциированные с развитием аутосомно-доминантной формы БП. Мутации генного локуса PARK1 приводят к развитию семейной формы БП с аутосомно-доминантным типом наследования. Заболевание часто дебю-
тирует в молодом возрасте и обычно быстро прогрессирует. У членов семьи, носителей мутации гена PARK1, иногда наблюдаются нетипичные для БП клинические признаки, такие как миоклонус и синдром гиповентиляции. Известны три миссенс мутации (А53Т, 12 А30Р, 34 и Е46К, 35), дупликация 36-39 и трипликация 40,41 гена альфа-синуклеина. Замена А53Т была первой идентифицированной мутацией при БП с аутосомно-доминантным типом наследования. Позже были идентифицированы А30Р и замены Е46К в немецкой и испанской семьях, соответственно [4]. Миссенс мутации и мультипликации — чрезвычайно редкие причины семейного паркинсонизма.

грессией и без атипичных особенностей), что подтверждает предположение о том, что количество копий гена может играть роль в развитии болезни. Дупликация и мутация A30P гена редко сочетаются с развитием деменции, тогда как трипликация и E46K мутация часто сочетают клинику БП и деменции [3].
Положение третьего локуса PARK3 на хромосоме 2р13 было открыто Гассером. Мутации PARK3 ведут к развитию семейной формы БП с аутосомно-доминантным типом наследования. Клиническая картина заболевания во многом схожа со спорадической формой БП, однако нередко помимо паркинсонизма у больных встречается деменция. Локус располагается на хромосоме 2р13, белок не известен. В качестве генов-кандидатов рассматриваются преобразователь фактора роста альфа, дина-стин и семафорин, однако мутация остается не идентифицированной. Патоморфологические исследования показали помимо дегенерации черной субстанции и присутствия телец Леви в стволе мозга наличие нейрофибриллярных клубков и Альцгеймеровских бляшек. Поэтому искомая мутация может быть связана с рядом фенотипов, включая различные степени деменции и болезнь Альцгеймера, а также идиопати-ческую форму БП.
Локус располагается на хромосоме 2р13, белок не известен. В качестве генов-кандидатов рассматриваются преобразователь фактора роста альфа, дина-стин и семафорин, однако мутация остается не идентифицированной. Патоморфологические исследования показали помимо дегенерации черной субстанции и присутствия телец Леви в стволе мозга наличие нейрофибриллярных клубков и Альцгеймеровских бляшек. Поэтому искомая мутация может быть связана с рядом фенотипов, включая различные степени деменции и болезнь Альцгеймера, а также идиопати-ческую форму БП.
Клиническая картина БП при наличии мутации в локусе PARK4, расположенном на хромосоме 4р16, характеризуется развитием леводопа-чувствительного паркинсонизма с ранним дебютом (в среднем в 33 года). Заболевание быстро прогрессирует. Для этой формы БП характерно снижение массы тела уже на ранних стадиях заболевания, вегетативные расстройства и деменция [3]. Морфологически (помимо дегенерации черной субстанции и обнаружения телец Леви) у таких пациентов формируются полости в гиппокампе и в некоторых других областях мозга [9].
Мутация гена UCHL1 (ubiquitin C-terminal hydrolase L1, англ.), картированная на хромосоме 4р14, сцепленная с локусом PARK5, также является причиной развития семейной формы БП с аутосомно-доминантным типом наследования. Клиническая картина заболевания не отличается от спорадической формы БП. Миссенс-мутация I93M была идентифицирована в немецкой семье у двух родных братьев. Белок UCH-L1, известный также как PGP9.5, является ферментом нейрона и одним из самых распространенных белков в мозге, его количество в мозге достигает 1-2 % от всех растворимых белков. Белок UCH-L1 является компонентом убиквинин-протеосомальной системы, которая утилизирует поврежденные белки [9].
Семейная форма БП с аутосомно-доминантным типом наследования, сцепленная с локусом PARK8, впервые была идентифицирована в японской семье Сагамихара в 1978 году. Заболевание развивается по типичному сценарию БП с поздним дебютом.
 ), ROC (Ras of complex proteins, англ.), COR (carboxy terminal of ROC, англ.), MAPKKK (mitogen-activated protein kinase kinase kinase, англ.), и область WD 40, которая богата повторениями аспартата и триптофана. Функции гена изучены недостаточно [3]. По некоторым данным, дардарин является цитоплазматиче-ской ГТФ-зависимой киназой [10]. ROC домен в состоянии связать гуанозинтрифосфат. Продукты некоторых мутаций LRRK2 проявляют повышенную киназную активность. Другие функциональные домены, как полагают, важны во взаимодействии белок-белок. Установлено, что мутации гена LRRK2 ведут к митохон-дриальной элонгации, снижению мембранных потенциалов митохондрий и, как следствие, к снижению продукции внутриклеточной АТФ [11]. LRRK2 также взаимодействует с другими белками ответственными за развитие семейной формы БП. Например, LRRK2 может взаимодействовать с паркином через ROC домен. Описано более чем 40 миссенс и нонсенс мутаций в LRRK2, но патогенность большинства из них еще не определена. В настоящее время очевидна роль 6 мутаций в развитии БП (R1441C, R1441G, R1441H, Y1699C, G2019S, и I2020T) [3, 11].
), ROC (Ras of complex proteins, англ.), COR (carboxy terminal of ROC, англ.), MAPKKK (mitogen-activated protein kinase kinase kinase, англ.), и область WD 40, которая богата повторениями аспартата и триптофана. Функции гена изучены недостаточно [3]. По некоторым данным, дардарин является цитоплазматиче-ской ГТФ-зависимой киназой [10]. ROC домен в состоянии связать гуанозинтрифосфат. Продукты некоторых мутаций LRRK2 проявляют повышенную киназную активность. Другие функциональные домены, как полагают, важны во взаимодействии белок-белок. Установлено, что мутации гена LRRK2 ведут к митохон-дриальной элонгации, снижению мембранных потенциалов митохондрий и, как следствие, к снижению продукции внутриклеточной АТФ [11]. LRRK2 также взаимодействует с другими белками ответственными за развитие семейной формы БП. Например, LRRK2 может взаимодействовать с паркином через ROC домен. Описано более чем 40 миссенс и нонсенс мутаций в LRRK2, но патогенность большинства из них еще не определена. В настоящее время очевидна роль 6 мутаций в развитии БП (R1441C, R1441G, R1441H, Y1699C, G2019S, и I2020T) [3, 11].
у 1 — 2 % пациентов с БП европейского происхождения, 15 — 20 % еврейских пациентов (евреи-ашкенази), и приблизительно в 40 % — среди северных африканских арабов [12].
Гены, ассоциированные с развитием аутосомно-рецессивной формы БП. Впервые ювенильный паркинсонизм был описан около 100 лет назад. Это особая форма первичного паркинсонизма. Его нозологическая самостоятельность определилась около 15 лет назад в результате идентификации молекулярных основ данного заболевания [13]. Клиническими особенностями ювенильного паркинсонизма является частое сочетание паркинсонизма с дистонией, может отсутствовать тремор покоя, характерна ранняя вегетативная дисфункция, более медленное прогрессирова-ние, хороший многолетний эффект препаратов леводопы, часто развиваются осложнения от леводопатерапии [14]. Патологоанатомическая картина ювенильного паркинсонизма характеризуется отсутствием телец Леви — гистологическим маркером БП, а также гибелью нейронов с реактивным глиозом в компактной части черной субстанции и в области голубоватого пятна [13]. К1 (PARK6), DJ1 PARK7 и АТР13А2 (PARK9). Каждая из этих мутаций имеет аутосомно-рецессивный тип наследования. Типичным для этих мутаций является развитие заболевания в молодом возрасте, однако мутации могут быть причиной развития и БП с поздним началом (старше 40). Большую часть случаев ювенильного паркинсонизма составляют мутации гена паркина [14]. Заболевание дебютирует в молодом возрасте (до 40 лет). Часто симптомы паркинсонизма сопровождаются дистонией. Пациенты хорошо отвечают на препараты леводопы. Основной ген аутосомно-рецессивного ювенильного паркинсонизма локализован на хромосоме 6q25.2-27, содержит 12 экзонов и охватывает приблизительно 1.38 мб, кодирует белок паркин, который состоит из 465 аминокислот. В клетке белок локализуется в цитозоле, комплексе Гольджи, внешней мембране митохондрий, а также в синаптических пузырьках [15]. В настоящее время описано более 100 мутаций гена PARK2, включая миссенс и нонсенс мутации, экзонные делеции, перестановки нуклеотидов и дупликации [16].
К1 (PARK6), DJ1 PARK7 и АТР13А2 (PARK9). Каждая из этих мутаций имеет аутосомно-рецессивный тип наследования. Типичным для этих мутаций является развитие заболевания в молодом возрасте, однако мутации могут быть причиной развития и БП с поздним началом (старше 40). Большую часть случаев ювенильного паркинсонизма составляют мутации гена паркина [14]. Заболевание дебютирует в молодом возрасте (до 40 лет). Часто симптомы паркинсонизма сопровождаются дистонией. Пациенты хорошо отвечают на препараты леводопы. Основной ген аутосомно-рецессивного ювенильного паркинсонизма локализован на хромосоме 6q25.2-27, содержит 12 экзонов и охватывает приблизительно 1.38 мб, кодирует белок паркин, который состоит из 465 аминокислот. В клетке белок локализуется в цитозоле, комплексе Гольджи, внешней мембране митохондрий, а также в синаптических пузырьках [15]. В настоящее время описано более 100 мутаций гена PARK2, включая миссенс и нонсенс мутации, экзонные делеции, перестановки нуклеотидов и дупликации [16]. Одни мутации гена изменяют первоначальный вид белка, его локализацию, растворимость, повышают аггрегирующие свойства, другие (инсерции, де-леции) — приводят к потере функции белка. Хотя у пациентов с мутациями гена PARK2 показана дегенерация нейронов черной субстанции,
Одни мутации гена изменяют первоначальный вид белка, его локализацию, растворимость, повышают аггрегирующие свойства, другие (инсерции, де-леции) — приводят к потере функции белка. Хотя у пациентов с мутациями гена PARK2 показана дегенерация нейронов черной субстанции,
тельца Леви обычно не обнаруживаются. Мутации охватывают всю длину гена. Большинство мутаций гена PARK2 представлены делецией 4 экзона, реже — делецией 3 экзона, делецией 3 и 4 экзонов одновременно, точечной мутацией в 7 экзоне (924C>T) и парной делецией во 2 экзоне (255/256delA). Эти пять вариантов составляют 35% всех мутаций гена PARK2. Точко-вые мутации наиболее часто концентрируются в экзонах 2 и 7, тогда как перестановки экзонов наиболее вероятно произойдут в интронах 2-4 [3]. Более чем 50% пациентов с ювенильным паркинсонизмом (возраст начала до 20 лет) имеют мутации в гене PARK2, с увеличением возраста дебюта заболевания частота мутаций существенно уменьшается [16]. Вопрос о влиянии гетерозиготной мутации PARK2 на развитие заболевания до сих пор остается спорным. Некоторые исследования сообщают, что средний возраст дебюта заболевания у пациентов с гетерозиготной мутацией гена PARK2 был на 11,7 лет раньше, чем у пациентов без неё. Также у носителей гетерозиготной мутации гена PARK2 с помощью позитронно-эмиссионной томографии установлено наличие дофаминергической дисфункции [17]. Однако при проведении большого случай-контролированного исследования существенного различия между носителями гетерозиготной мутации PARK2 и лицами группы контроля не найдено [16]. Для определения роли носительства гетерозиготной мутации гена PARK2 в риске развития БП необходимы дальнейшие исследования.
Вопрос о влиянии гетерозиготной мутации PARK2 на развитие заболевания до сих пор остается спорным. Некоторые исследования сообщают, что средний возраст дебюта заболевания у пациентов с гетерозиготной мутацией гена PARK2 был на 11,7 лет раньше, чем у пациентов без неё. Также у носителей гетерозиготной мутации гена PARK2 с помощью позитронно-эмиссионной томографии установлено наличие дофаминергической дисфункции [17]. Однако при проведении большого случай-контролированного исследования существенного различия между носителями гетерозиготной мутации PARK2 и лицами группы контроля не найдено [16]. Для определения роли носительства гетерозиготной мутации гена PARK2 в риске развития БП необходимы дальнейшие исследования.
Мутации генного локуса PARK7 приводит к развитию наследственной формы БП с аутосомно-рецессивным типом наследования. Впервые мутации были идентифицированы в двух европейских семьях с дебютом БП в 2040 лет. Ассоциированная с локусом PARK7 БП встречается редко. В среднем, в 1-2% случаях от всех случаев БП с ранним началом, поэтому наши знания относительно клинических особенностей этой формы заболевания ограничены. В дополнение к паркинсонизму у пациентов наблюдаются психические симптомы, а также брахидактелия. Ген DJ1 расположен на хромосоме 1p36.23, содержит 7 экзонов и кодирует белок, состоящий из 189 аминокислот. Экспрессия DJ1 характерна для всех млекопитающих, белок обнаруживают в большинстве тканях организма, включая нейроны мозга и глиаль-ные клетки. Белок DJ1 относится к семейству пептидаз [18]. Это цитоплазматический белок, но также он может транслоцироваться в митохондрии и проявлять свойства антиоксиданта. Его антиоксидантные свойства могут зависеть от остатка цистеина в позиции 106. Функции
В среднем, в 1-2% случаях от всех случаев БП с ранним началом, поэтому наши знания относительно клинических особенностей этой формы заболевания ограничены. В дополнение к паркинсонизму у пациентов наблюдаются психические симптомы, а также брахидактелия. Ген DJ1 расположен на хромосоме 1p36.23, содержит 7 экзонов и кодирует белок, состоящий из 189 аминокислот. Экспрессия DJ1 характерна для всех млекопитающих, белок обнаруживают в большинстве тканях организма, включая нейроны мозга и глиаль-ные клетки. Белок DJ1 относится к семейству пептидаз [18]. Это цитоплазматический белок, но также он может транслоцироваться в митохондрии и проявлять свойства антиоксиданта. Его антиоксидантные свойства могут зависеть от остатка цистеина в позиции 106. Функции
DJ1 особенно важны для дофаминергических нейронов черной субстанции, так как они особенно уязвимы к высокому уровню оксидантно-го стресса [19]. Снижение уровня эндогенного белка DJ1 повышает смерть нейронов, индуцированную окислительным стрессом. К1 или дестабилизируя белок, или разрушая его ки-назную активность.
К1 или дестабилизируя белок, или разрушая его ки-назную активность.
Таблица 1. Семейные формы болезни Паркинсона
Локус Хромосома Белок Тип наследования Наличие телец Леви
PARK1 4q21-23 Альфа-синуклеин Аутосомно-доминантный +
PARK2 6q25.20-27 Паркин Аутосомно-рецессивный ±
PARK3 2p13 Неизвестен Аутосомно-доминантный +
PARK4 4q21-23 Альфа-синуклеин Аутосомно-доминантный +
PARK5 4p14 UCH-L1 Аутосомно-доминантный
PARK6 1p35-36 PINK1 Аутосомно-рецессивный +
PARK7 1p36 DJ-1 Аутосомно-рецессивный
PARK8 12p11. 2-q13.1 LRRK2 Аутосомно-доминантный ±
2-q13.1 LRRK2 Аутосомно-доминантный ±
PARK9 1p36 ATP13A2 Аутосомно-рецессивный
PARK11 2q36-37 Неизвестен Аутосомно-доминантный
PARK13 2p13 Omi/HtrA2 Аутосомно-доминантный?
Мутация в гене аденозинтрифосфотазы (АТР13А2) впервые была найдена в иорданской и чилийской семье у пациенттов с синдромом Куфора-Ракеба, который клинически характеризуется наличием паркинсонизма с очень ранним дебютом (11-16 лет), чувствительного к леводопе. Симптомы паркинсонизма дополняют пирамидальные знаки, деменция, а также надъядерные глазные симптомы. Магнитно-резонансная томография обнаруживает существенную атрофию бледного шара, пирамид и диффузную атрофию на более поздних стадиях. У некоторых больных развиваются лицевые, глоточные и кистевые миоклонии, а также оку-логирный дистонический спазм. Ген АТР13А2 (PARK9) картирован на хромосоме 1р36, содержит 29 экзонов. Белок АТР13А2 состоит из 1180 аминокислоты и имеет 10 трансмембранных доменов. АТР13А2 — мембранный лизосомаль-ный белок. Он транспортирует неорганические катионы и другие субстраты. Точная функция белка АТР13А2 все еще неизвестна. Экспрессия АТР13А2 наиболее значительна в тканях мозга. Все известные мутации АТР13А2 прямо или косвенно затрагивают трансмембранные домены. Гомозиготная миссенс мутация (G504R) была идентифицирована в одном спорадическом случае у пациента с ювенильным паркинсонизмом из Бразилии. Дебют заболевания был в 12 лет, паркинсонизм чувствительный к леводопе, акинетико-ригидная форма, с наличием лекарственных моторных флюктуаций и дискинезий, выраженными зрительными галлюцинации и надъядерным параличом взора. У пациента визуализировалась умеренная диффузная атрофия, однако ни деменция, ни пирамидные знаки у пациента не выявлялись [3].
Белок АТР13А2 состоит из 1180 аминокислоты и имеет 10 трансмембранных доменов. АТР13А2 — мембранный лизосомаль-ный белок. Он транспортирует неорганические катионы и другие субстраты. Точная функция белка АТР13А2 все еще неизвестна. Экспрессия АТР13А2 наиболее значительна в тканях мозга. Все известные мутации АТР13А2 прямо или косвенно затрагивают трансмембранные домены. Гомозиготная миссенс мутация (G504R) была идентифицирована в одном спорадическом случае у пациента с ювенильным паркинсонизмом из Бразилии. Дебют заболевания был в 12 лет, паркинсонизм чувствительный к леводопе, акинетико-ригидная форма, с наличием лекарственных моторных флюктуаций и дискинезий, выраженными зрительными галлюцинации и надъядерным параличом взора. У пациента визуализировалась умеренная диффузная атрофия, однако ни деменция, ни пирамидные знаки у пациента не выявлялись [3].
Заключение. Таким образом, достижения молекулярной генетики последних лет свидетельствуют о клинико-генетической гетерогенности моногенных форм болезни Паркинсона (табл. 1), что необходимо учитывать при планировании диспансерного наблюдения членов родословной больных в отягощенных по рассматриваемому заболеванию семьях.
1), что необходимо учитывать при планировании диспансерного наблюдения членов родословной больных в отягощенных по рассматриваемому заболеванию семьях.
Литература:
1. Farrer M.J. Genetics of Parkinson disease: paradigm shifts and future prospects // Nat. Rev. Genet.
— 2006. — Vol. 7, № 4. — Р. 306-318.
2. de Rijk M.C., Launer L.J., Berger K. et al. Prevalence of Parkinson’s disease in Europe: a collaborative study of population-based cohorts // Neurologic Diseases in the Elderly Research Group. Neurol. -2000. — Vol. 54, № 11, 5. — Р. 21-23.
3. Lynn M.B., Ignacio F.M., Cyrus P.Z. The Genetics of Parkinson Disease // J. Geriatr. Psychiatr. Neurol. -2010. — Vol. 23, № 4. — P. 228-242.
4. Bekris L.M., Mata I.F., Zabetian C.P. The genetics of Parkinson disease // J. Geriatr. Psychiatr. Neurol. -2010. — Vol. 23(4). — P. 228-242.
Bekris L.M., Mata I.F., Zabetian C.P. The genetics of Parkinson disease // J. Geriatr. Psychiatr. Neurol. -2010. — Vol. 23(4). — P. 228-242.
5. Winslow A.R., Chen C.W., Corrochano S. et al. a-Synuclein impairs macroautophagy: implications for Parkinson’s disease // J. Cell. Biol. — 2010. — Vol. 190(6). — Р. 1023-1037.
6. Chen A., Richard H. Snare-mediated membrane fusion // Yu Natur. Review. Mol. Cell. Biol. — 2001. -Vol. 2. — Р. 98 -106.
7. Kamp F., Exner N., Lutz A.K., Wender N. et al. Inhibition of mitochondrial fusion by a-synuclein is rescued by PINK1, Parkin and DJ-1// EMBO J. — 2010.
— Vol. 29(20). — Р. 3571-3589.
8. Иллариошкин С.Н., Загоровская Т.Б., Иванова-Смоленская И.А. и др. Генетические аспекты болезни Паркинсона // Невролог. журн. 2002. №5. С. 47 — 51.
журн. 2002. №5. С. 47 — 51.
9. Belin А.С., Westerlund М. Parkinson’s disease:
а genetic // FEBS. — 2008. — Vol. 275. — Р. 13771383.
10. Шнайдер Н.А., Сапронова М.Р. Современные представления о генетике болезни Паркинсона // Вестн. Клинич. больницы №51. — 2011. Т. 4 /2-3. С. 39-46.
11. Mortiboys H., Johansen K.K., Aasly J.O. et al. Mitochondrial impairment in patients with Parkinson disease with the G2019S mutation in LRRK2 // Neurol. — 2010. — Vol. 75(22). — Р. 2017-2020.
12. Orr-Urtreger A., Shifrin C., Rozovski U. et al. The LRRK2 G2019S mutation in Ashkenazi Jews with Parkinson disease: is there a gender effect? // Neurol. — 2007. — Vol. 69(16). — Р. 1595-1602.
13. Загородская Т.Б., Иллариошкин С.Н., Сломинский П.А. и др. Клинико-генетический анализ ювенильного паркинсонизма в России // Журн. неврол. и психиатр. 2004. №8. С. 66-72.
Загородская Т.Б., Иллариошкин С.Н., Сломинский П.А. и др. Клинико-генетический анализ ювенильного паркинсонизма в России // Журн. неврол. и психиатр. 2004. №8. С. 66-72.
14. Teri R., Rodnitzky T., Rodnitzky R.L. Juvenile Parkinsonism Epidemiology, Diagnosis and Treatment // Drugs. — 2010. — Vol. 24 (6). — Р. 467477.
15. Berthier A., Navarro S., Jiménez-Sâinz J. et al. PINK1 displays tissue-specific subcellular location
and regulates apoptosis and cell growth in breast cancer cells // Hum. Pathol. — 2011. — Vol. 42(1). — P. 75-87.
16. Kay D.M., Stevens C.F., Hamza T.H. et al. A comprehensive analysis of deletions, multiplications, and copy number variations in PARK2 // Neurol. —
2010. — Vol. 75(13). — P. 1189-1194.
17. KhanN.L.,ScherflerC.,GrahamE.etal.Dopaminergic dysfunction in unrelated, asymptomatic carriers of a single parkin mutation // Neurol. — 2005. — Vol. 64(1). — P. 134- 136.
KhanN.L.,ScherflerC.,GrahamE.etal.Dopaminergic dysfunction in unrelated, asymptomatic carriers of a single parkin mutation // Neurol. — 2005. — Vol. 64(1). — P. 134- 136.
18. Zhiquan W., Yu Z., Shi Z. et al. DJ-1 can inhibit microtubule associated protein-1 B-formed aggregates // Mol. Neurodegener. — 2011. — Vol. 6:38. — P. 1-10.
19. Sanyal J., Sarkar B., Banerjee T.K. et al. Evaluating intra-genetic variants of DJ-1 among Parkinson’s disease patients of Eastern India // Neurol. Res.-
2011. — Vol. 33(4). -P. 349-353.
20. Khan N.L., Valente E.M., Bentivoglio A.R. et al. Clinical and subclinical dopaminergic dysfunction in PARK6-linked parkinsonism: an 18F-dopa PET study // Ann. Neurol. — 2002. — Vol. 52(6). — P. 849853.
MONOGENIC FORMS OF PARKINSONS DISEASE N. A. Shnayder, M.R. Sapronova
A. Shnayder, M.R. Sapronova
Clinical Hospital №51 of FMBA of Russia, Zhelenogorsk, Krasnoyarsk region; Krasnoyarsk State Medical University named after Prof. V.F. Voyno-Yasenetsky, Neurological Center of Epileptology, Neurogenetics and Brain Research of University Clinic, Krasnoyarsk , RF
Abstract. Parkinson’s disease is neurodegenerative disorder characterized by loss of dopamine neuron. In most cases Parkinson’s disease is a multifactorial pathology. However last years it is convincingly proved, that the hereditary component play the important role in disease development. By present time 11 genes which associate with familial form of Parkinson’s disease are known. The paper presents an overview of genetic studies of foreign and domestic authors. Seven genes which associate with autosomal dominant inheritance type and four genes which associate with autosomal recessive inheritance type are known. Key words: Parkinson’s disease, genetics.
Key words: Parkinson’s disease, genetics.
Статья принята к печати 27.08.2012г.
ОРИГИНАЛЬНАЯ СТАТЬЯ
© КОРЕЦКАЯ Н.М., ГРИНЬ Е.Н.
СРАВНИТЕЛЬНЫЙ АНАЛИЗ ОСОБЕННОСТЕЙ ТУБЕРКУЛЕЗА ЛЕГКИХ И ЭФФЕКТИВНОСТИ ЕГО ЛЕЧЕНИЯ С УЧЕТОМ ПУТЕЙ ВЫЯВЛЕНИЯ ЗАБОЛЕВАНИЯ
Н.М. Корецкая, Е.Н. Гринь
ГБОУ ВПО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого», Красноярск, ФГБУЗ Клиническая больница №51 ФМБА России,
г. Железногорск Красноярского края, РФ
660022, г. Красноярск, ул. Партизана Железняка, 1, ГБОУ ВПО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого МЗ и соцразвития РФ».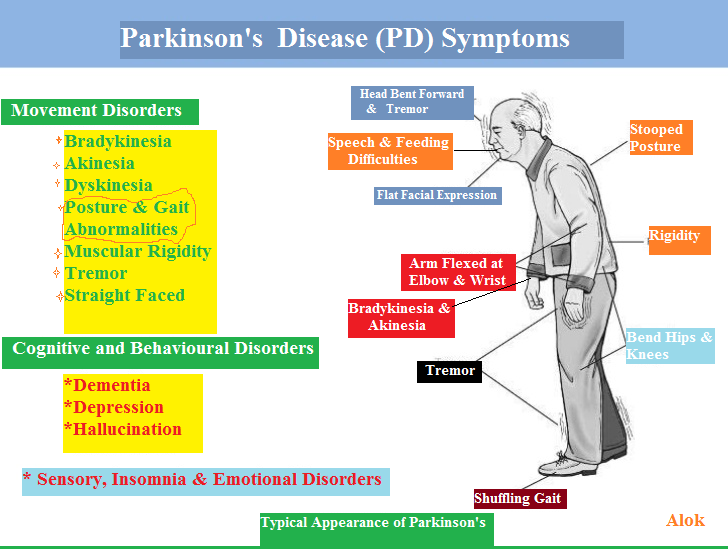 662990, Красноярский край, г. Железногорск, ул. Кирова, д. 5, ФГБУЗ «КБ №51 ФМБА России». E-mail: kb-51@ kb-51.ru
662990, Красноярский край, г. Железногорск, ул. Кирова, д. 5, ФГБУЗ «КБ №51 ФМБА России». E-mail: kb-51@ kb-51.ru
Резюме. Проведен сравнительный анализ структуры клинических форм туберкулеза легких, характеристики специфического процесса, эффективности его лечения и социального состава больных, впервые выявленных при обращении к врачу и при проверочных флюорографических осмотрах на территории
Болезнь Паркинсона, комплексная диагностика, ч. м. (Parkinson’s disease, multiplex mutations detection assay)
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т. д.
д.
Единицы измерения: тест качественный.
Референсные значения
Изменение копийности генов PARK1 (SNCA), PARK2 (Parkin), PARK5 (UCHL1), PARK6 (PINK1), PARK7 (DJ1), PARK8 (Dardarin) и ATP13A2, а также точечных мутаций SNCA A30P и LRRK2 G2019S обнаружено не было.
Интерпретация результатов
PARK1 (SNCA)
Гетерозиготная точечная мутация A30P и делеции и дупликации гена PARK1 (SNCA) вызывают раннюю форму болезни Паркинсона (появление первых симптомов до 50 лет) с первичным хорошим ответом на терапию леводопой, но быстрой прогрессией, ранним развитием деменции и когнитивной дисфункции, а также появлением атипичной симптоматики: центральной гиповентиляции и миоклонуса. Нужно отметить, что пенетрантность мутаций в гене PARK1 составляет 85%.
PARK8 (LRRK2)
Гетерозиготная мутация G2019S и делеции и дупликации гена PARK8 (LRRK2) вызывают позднюю форму болезни Паркинсона с медленной прогрессией. Пациенты хорошо отвечают на терапию леводопой и развитие деменции наблюдается редко.
Пациенты хорошо отвечают на терапию леводопой и развитие деменции наблюдается редко.
PARK2 (Parkin)
Гомозиготные делеции и дупликации гена PARK2 (Parkin) вызывают аутосомно-рецессивную раннюю форму болезни Паркинсона (начало симптоматики в 30-40 лет). Кроме этого, при некоторых формах гетерозиготных мутаций и гомозиготных аберраций симптоматика может возникать в раннем детстве (ювенильная форма болезни Паркинсона). Обычно PARK2–ассоциированная форма болезни Паркинсона характеризуется медленной прогрессией и хорошим ответом на леводопу. Клинический фенотип пациентов с данной мутацией не отличим от случаев PINK1- и DJ1-ассоциированной болезни Паркинсона.
PARK7 (DJ1)
Гомозиготные точечные мутации и делеции и дупликации гена PARK7 (DJ1) вызывают аутосомно-рецессивную раннюю форму болезни Паркинсона (начало симптоматики в 30-40 лет). Клинический фенотип пациентов с данной мутацией не отличим от случаев Parkin- и PINK1-ассоциированных болезни Паркинсона. Обычно PARK7 (DJ1) ассоциированная форма болезни Паркинсона характеризуется медленной прогрессией и хорошим ответом на леводопу.
Обычно PARK7 (DJ1) ассоциированная форма болезни Паркинсона характеризуется медленной прогрессией и хорошим ответом на леводопу.
ATP13A2
Гомозиготные точечные мутации и делеции и дупликации гена ATP13A2 вызывают аутосомно-рецессивную раннюю форму болезни Паркинсона (начало симптоматики в 30-40 лет). Кроме этого, мутации в данном гене вызывают атипичную форму болезни Паркинсона (Куфора-Ракеба), характеризующуюся ювенильной манифестацией, быстрой прогрессией, ассоциированной с деменцией, пирамидными знаками и надъядерным параличом взгляда.
PARK5 (UCHL1)
Точечные мутации и делеции и дупликации гена PARK5 (UCHL1) повышают риск развития болезни Паркинсона, но их патогенность до сих пор полностью не доказана.
Отрицательный результат исследования не исключает наследственную этиологию болезни Паркинсона, но значительно снижает ее вероятность, так как в тесте выявляются наиболее частые аберрации.
Транскраниальная сонография при болезни Паркинсона | Байбородина
1. Жукова И.А., Жукова Н.Г., Ижболдина О.П., Никити- на М.А., Алифирова В.М. Анализ методов оценки обоняния у пациентов с болезнью Паркинсона. Журнал неврологии и психиатрии им. С.С. Корсакова. Неврология и психиатрия пожилого возраста. 2015; 2: 47–52.
Жукова И.А., Жукова Н.Г., Ижболдина О.П., Никити- на М.А., Алифирова В.М. Анализ методов оценки обоняния у пациентов с болезнью Паркинсона. Журнал неврологии и психиатрии им. С.С. Корсакова. Неврология и психиатрия пожилого возраста. 2015; 2: 47–52.
2. Becker С., Berg D. Neuroimaging in basal ganglia disorders: Perspectives for transcranial ultrasound. Mov. Disord. 2001; 16: 23–32.
3. Berg D., Godau J., Walter U. Transcranial sonography in movement disorders. Lancet Neurol. 2008; 7: 1044–1055.
4. Puts I., Berg D., Maeurer M. Transcranial sonography of the brain parenchyma: Comparison of B-mode imaging and tissue harmonic imaging. Ultrasound. Med. Biol. 2000; 26: 189–194.
5. Berg D., Hochstrasser H. Iron metabolism in parkinsonian syndromes. Mov. Disord. 2011; 21: 1299–1310.
Berg D., Hochstrasser H. Iron metabolism in parkinsonian syndromes. Mov. Disord. 2011; 21: 1299–1310.
6. Весk G., Seuferl J., Bogdahn U. Degeneration of substantia nigra in chronic Parkinsons disease visualized by transkranial color-coded real-time sonography. Neurology. 2013; 45; 182–184.
7. Lyoo C.H., Ryu Y.H., Lee M.S.J. Cerebral cortical areas in which thickness correlates with severity of motor deficits of Parkinson’s disease. Neurology. 2011; 258: 1871–1876.
8. Труфанов А.Г., Литвиненко И.В., Воронков Л.В., Ра- мешвилли Т.Е. Деменция при болезни Паркинсона: роль атрофических изменений коры и возможности прогноза с помощью магнитно-резонансной морфометрии. Вестник Российской военно-медицинской академии. 2012; 3: 116–123.
9. Чечеткин А.О. Транскраниальное ультразвуковое сканирование мозга при болезни Паркинсона. Визуализация в клинике. 2000; 17: 45–48.
Чечеткин А.О. Транскраниальное ультразвуковое сканирование мозга при болезни Паркинсона. Визуализация в клинике. 2000; 17: 45–48.
10. Berg D., Behnke S., Walter U. Application of transcranial Sonography in extrapyramidal disorder: Updated Recommendation. Ultraschall Med. 2009; 27: 12–19.
11. Becker С., Berg D. Neuroimaging in basal ganglia disorders: Perspectives for transcranial ultrasound. Mov. Disord. 2011; 16: 23–32.
12. Berg D., Roggendorf W., Schroeder U. Echogenicity of the substantia nigra: Association with increased iron content and marker forsusceptibility to nigrostriatal injury. Arch. Neurol. 2002; 59: 999–1005.
13. Morrish P.K., Sawle G.V., Brooks D.J. An 18F-dopa PET and clinical study of the rate of progression in Parkinson’s disease. Brain. 1996; 119: 223–591.
Brain. 1996; 119: 223–591.
14. Berg D. Disturbans of iron metabolism as a contributing factor to SN hiperechogenicity in Parkinsons disease: implicaty ons for idiopathic end monogenetic forms. Neurogem. Res. 2010; 32: 1646–1654.
15. Федотова Е.Ю., Чечеткин А.О., Шадрина М.И. Транскраниальная сонография при болезни Паркинсона. Журнал неврология и психиатрия. 2011; 111: 49–55.
16. Голубев В.Л., Левин Я.И., Вейн А.М. Болезнь Паркинсона и синдром паркинсонизма. М.: МЕДпресс-Информ, 2010: 416.
17. Razdorskaya V.V., Yudina G.K., Voskresenskaya O.N. Clinical efficiency of symptomatic therapy of an atypical variant of hemiparkinsonism-hemiatrophy. 15 Congress of the European Federation of Neurological Societies EFNS, 2011: 522.
18. Berg D., Siefker C., Becker G. Echogenicity of the substantia nigra in Parkinson’s disease and its relation to clinical findings. J. Neurol. 2001; 8: 429–433.
19. Юдина В.В., Воскресенская О.Н., Юдина Г.К. Особенности постинсультного варианта сосудистого паркинсонизма. Актуальные вопросы практической нейрохирургии: материалы юбилейной научно-практической конференции. Балаково, 2009: 172–174.
20. Berg D., Behnke S., Walter U. Application of transcranial Sonography in extrapyramidal disorder: Updated Recommendation. Ultraschall. Med. 2009; 27: 12–19.
21. Berg D., Roggendorf W., Schroder U.Echogenicity of the substantia nigra: association with increased iron content and marker for susceptibilit to nigrostriatal injury. Arch. Neurol. 2012; 59: 999–1050.
Arch. Neurol. 2012; 59: 999–1050.
Болезнь Паркинсона, комплексная диагностика, ч. м. (Parkinson’s disease, multiplex mutations detection assay)
Интерпретация результатов
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Единицы измерения: тест качественный.
Референсные значения
Изменение копийности генов PARK1 (SNCA), PARK2 (Parkin), PARK5 (UCHL1), PARK6 (PINK1), PARK7 (DJ1), PARK8 (Dardarin) и ATP13A2, а также точечных мутаций SNCA A30P и LRRK2 G2019S обнаружено не было.
Интерпретация результатов
PARK1 (SNCA)
Гетерозиготная точечная мутация A30P и делеции и дупликации гена PARK1 (SNCA) вызывают раннюю форму болезни Паркинсона (появление первых симптомов до 50 лет) с первичным хорошим ответом на терапию леводопой, но быстрой прогрессией, ранним развитием деменции и когнитивной дисфункции, а также появлением атипичной симптоматики: центральной гиповентиляции и миоклонуса. Нужно отметить, что пенетрантность мутаций в гене PARK1 составляет 85%.
Нужно отметить, что пенетрантность мутаций в гене PARK1 составляет 85%.
PARK8 (LRRK2)
Гетерозиготная мутация G2019S и делеции и дупликации гена PARK8 (LRRK2) вызывают позднюю форму болезни Паркинсона с медленной прогрессией. Пациенты хорошо отвечают на терапию леводопой и развитие деменции наблюдается редко.
PARK2 (Parkin)
Гомозиготные делеции и дупликации гена PARK2 (Parkin) вызывают аутосомно-рецессивную раннюю форму болезни Паркинсона (начало симптоматики в 30-40 лет). Кроме этого, при некоторых формах гетерозиготных мутаций и гомозиготных аберраций симптоматика может возникать в раннем детстве (ювенильная форма болезни Паркинсона). Обычно PARK2–ассоциированная форма болезни Паркинсона характеризуется медленной прогрессией и хорошим ответом на леводопу. Клинический фенотип пациентов с данной мутацией не отличим от случаев PINK1- и DJ1-ассоциированной болезни Паркинсона.
PARK7 (DJ1)
Гомозиготные точечные мутации и делеции и дупликации гена PARK7 (DJ1) вызывают аутосомно-рецессивную раннюю форму болезни Паркинсона (начало симптоматики в 30-40 лет). Клинический фенотип пациентов с данной мутацией не отличим от случаев Parkin- и PINK1-ассоциированных болезни Паркинсона. Обычно PARK7 (DJ1) ассоциированная форма болезни Паркинсона характеризуется медленной прогрессией и хорошим ответом на леводопу.
Клинический фенотип пациентов с данной мутацией не отличим от случаев Parkin- и PINK1-ассоциированных болезни Паркинсона. Обычно PARK7 (DJ1) ассоциированная форма болезни Паркинсона характеризуется медленной прогрессией и хорошим ответом на леводопу.
ATP13A2
Гомозиготные точечные мутации и делеции и дупликации гена ATP13A2 вызывают аутосомно-рецессивную раннюю форму болезни Паркинсона (начало симптоматики в 30-40 лет). Кроме этого, мутации в данном гене вызывают атипичную форму болезни Паркинсона (Куфора-Ракеба), характеризующуюся ювенильной манифестацией, быстрой прогрессией, ассоциированной с деменцией, пирамидными знаками и надъядерным параличом взгляда.
PARK5 (UCHL1)
Точечные мутации и делеции и дупликации гена PARK5 (UCHL1) повышают риск развития болезни Паркинсона, но их патогенность до сих пор полностью не доказана.
Отрицательный результат исследования не исключает наследственную этиологию болезни Паркинсона, но значительно снижает ее вероятность, так как в тесте выявляются наиболее частые аберрации.
Литература
- Bonifati V. Genetics of Parkinson’s disease—state of the art, 2013. Parkinsonism Relat Disord. 2014;20(Suppl 1):S23–8.
- Periquet M. et al. Origin of the mutations in the parkin gene in Europe: Exon rearrangements are independent recurrent events, whereas point mutations may result from founder effects. American Journal of Human Genetics. 2001.
Болезнь Паркинсона
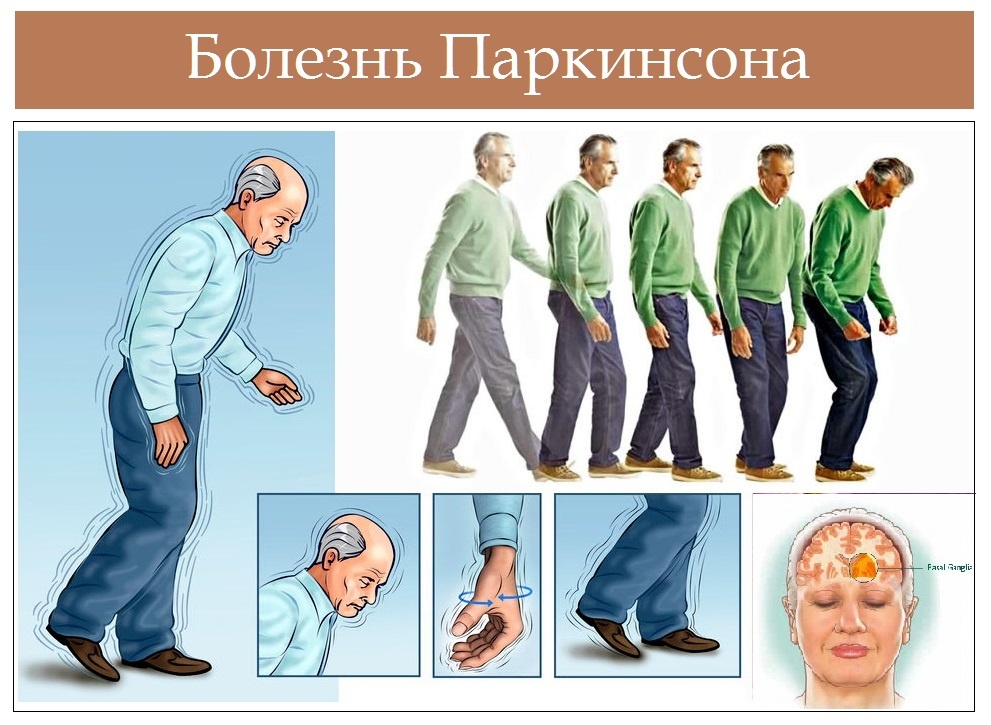
Болезнь Паркинсона — медленно прогрессирующее хроническое неврологическое заболевание из группы дегенеративных заболеваний экстрапирамидной моторной системы вследствие прогрессирующего разрушения и гибели нейронов, вырабатывающих нейромедиатор дофамин.
Болезнь Паркинсона составляют нарушения движений и расстройства интеллекта и психики в разной степени выраженности.
Ведущими симптомами нарушения движений являются:
- гипокинезия – уменьшение количества движений;
- тремор – дрожание головы и/или рук и/или ног;
- мышечная ригидность – напряжение и скованность мышц;
- постуральная неустойчивость – нарушение способности удерживать равновесие.

Современная медицина пока не может излечить заболевание, однако существующие методы позволяют значительно улучшить качество жизни больных и замедлить прогрессирование болезни.
Болезнь Паркинсона составляет 70—80% случаев синдрома паркинсонизма. Термин «паркинсонизм» является общим понятием для ряда заболеваний и состояний с вышеназванными ведущими симптомами. Однако наиболее значимой из форм паркинсонизма является болезнь Паркинсона.
Болезнь Паркинсона — наиболее частое нейродегенеративное заболевание вместе с болезнью Альцгеймера. Заболевание встречается повсеместно. Его частота колеблется от 60 до 140 человек на 100 тысяч населения, число больных значительно увеличивается среди представителей старшей возрастной группы. Удельный вес людей с болезнью Паркинсона в возрастной группе старше 60 лет составляет 1%, а старше 85 лет— около 5%. Чаще всего первые симптомы заболевания появляются в 55—60 лет. Однако в ряде случаев болезнь может развиться и в возрасте до 40 (болезнь Паркинсона с ранним началом) или до 20 лет (ювенильная форма заболевания). Мужчины болеют несколько чаще, чем женщины. Впервые состояние было описано в 1817 году и получило название в честь Джеймса Паркинсона.
Мужчины болеют несколько чаще, чем женщины. Впервые состояние было описано в 1817 году и получило название в честь Джеймса Паркинсона.
Болезнь Паркинсона – одно из многочисленных нарушений деятельности экстрапирамидной системы.
Экстрапирамидные расстройства – заболевания с избыточными движениями или, наоборот, их недостаточным количеством и активностью.
Нарушения экстрапирамидной системы может проявляться с разными симптомами и синдромами: акатизия, баллизм, дистония, миоклонус, паркинсонизм, тики, тремор, хорея.
Паркинсонизм – это нарушение в работе головного мозга, сопровождающееся дрожанием головы, рук и ног, скованностью движений и повышением мышечного тонуса. Болезнь Паркинсона характеризуется аналогичными явлениями, но в отличие от нее паркинсонизм может возникать вторично (после черепно-мозговых травм, отравлений и т. д.). Именно паркинсонизм (дрожательный паралич)– это не отдельное заболевание, а синдром (совокупность симптомов).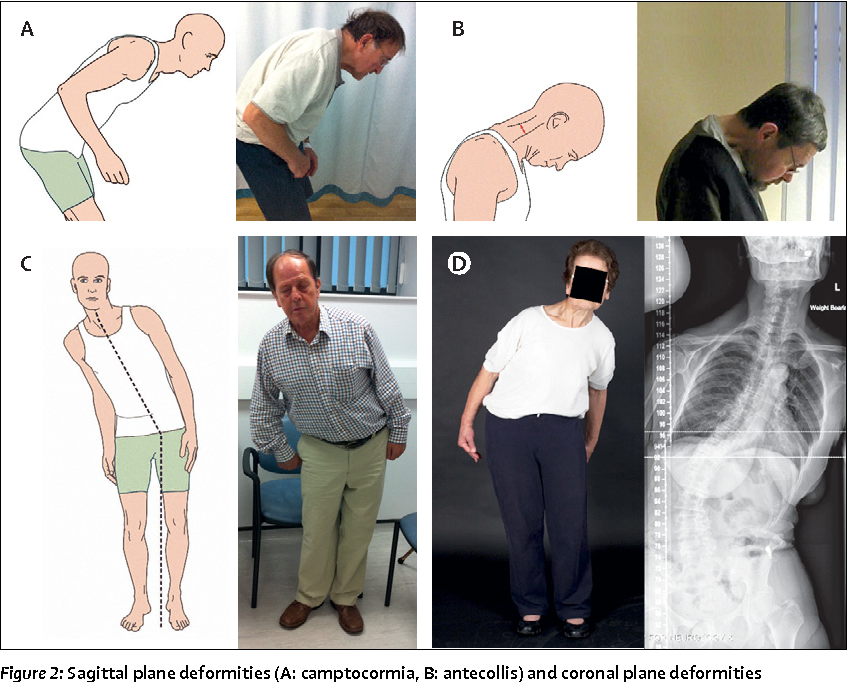 Синдром паркинсонизма проявляется при ряде неврологических расстройств.
Синдром паркинсонизма проявляется при ряде неврологических расстройств.
В зависимости от причины возникновения нарушения выделяют:
- Первичный (идиопатический). В этом случае синдром вызывает гибель дофаминовых нейронов в нервной системе организма. Они регулируют двигательную активность, их недостаток приводит к нарушению двигательной функции.
- Вторичный синдром провоцируют внешние факторы: прием лекарственных препаратов, травмы головы, инфекции и т. д.
Тремор — быстрые ритмичные движения небольшой амплитуды, похожие на дрожание являются одним из экстрапирамидных синдромов. Наиболее ярко прослеживается при попытке удержания позы (например, вытянутых вперёд рук) или приближении к цели (приближении пальца к носу). Чем ближе к цели, тем сильнее тремор. Также он усиливается при удержании позы.
Тики – подергивании мышц и/или частей тела – проявляются чаще всего в стрессовых ситуациях, нервном напряжении. Это могут быть подёргивания плечом, шеей, наморщивание лба, запрокидывание головы, подмигивание.
Хорея — тяжёлое нарушение движений, характеризующееся отрывистостью, нерегулярностью, беспорядочностью.
Акатизия (кроличий синдром) – выраженная неусидчивость, с характерными определенными психомоторными нарушения.
Мышечная дистония —произвольные и неконтролируемые сокращения мышечной системы, во время которых человек может принять неестественную позу. Такие непроизвольные, нерегулярные и неконтролируемые движения могут происходить в различных частях тела.
Таким образом, диагностика и лечение болезни Паркинсона и экстрапирамидных расстройств – сложная и ответственная задача исключительно для специалиста – невролога!!!
Лечение болезни Паркинсона, запись на прием в Нижнем Новгороде
Основным клиническим проявлением болезни Паркинсона является синдром паркинсонизма. Симптомы болезни появляются исподволь.
Гипокинезия считается основным (облигатным) признаком паркинсонизма. Лицо становится маскообразным (гипомимия), речь – монотонной.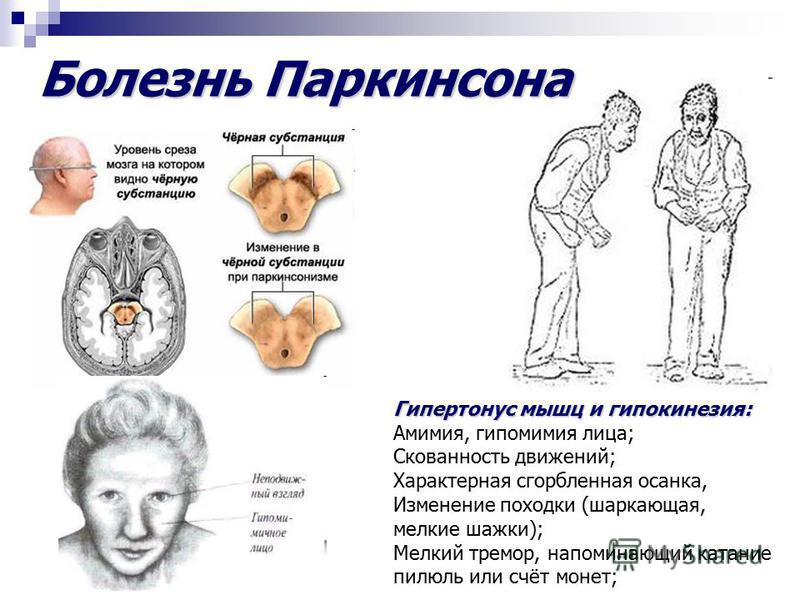 Постепенно нарастают нарушения мелкой моторики (больному трудно застегнуть пуговицы), изменяется почерк (уменьшается размер букв и чёткость их написания), нарушается походка (больной передвигается мелкими, семенящими шажками).
Постепенно нарастают нарушения мелкой моторики (больному трудно застегнуть пуговицы), изменяется почерк (уменьшается размер букв и чёткость их написания), нарушается походка (больной передвигается мелкими, семенящими шажками).
Наиболее известным проявлением болезни Паркинсона является тремор, особенно заметный в руках. Как правило, тремор более выражен в состоянии покоя и уменьшается при выполнении целенаправленных действий. Тремор может распространиться и на другие мышечные группы – руки, ноги, нижнюю челюсть, что доставляет существенный дискомфорт.
Еще одним характерным симптомом паркинсонизма является мышечная ригидность. Процесс начинается, как правило, с одной руки, постепенно распространяется на ногу, затем – на противоположную сторону и всё тело. При попытке сгибания-разгибания рук или ног больного, можно ощутить сопротивление в мышцах. При этом конечности сгибаются и разгибаются как на шестерёнках (феномен «зубчатого колеса»). Уже на ранних стадиях появляются ощущение скованности в теле, боли в спине, суставах. Весьма характерна «согбенная» поза – голова наклонена вперёд, спина сгорблена, ноги слегка согнуты в коленных и тазобедренных суставах.
Весьма характерна «согбенная» поза – голова наклонена вперёд, спина сгорблена, ноги слегка согнуты в коленных и тазобедренных суставах.
Кроме перечисленных двигательных нарушений, для болезни Паркинсона характерны и другие, «немоторные» проявления: вегетативные (запоры, учащённое мочеиспускание, артериальная гипотензия), когнитивные (нарушения памяти, концентрации внимания), аффективные (тревога, депрессия), психотические (галлюцинации, бред). «Немоторные» проявления болезни Паркинсона, наряду с ограничением двигательной активности, значительно снижают качество жизни больных.
ОЦЕНКА ПЕРИФЕРИЧЕСКИХ ПОРАЖЕНИЙ ПРИ БОЛЕЗНИ ПАРКИНСОНА
Таряник Е. А.
Об авторе:
Рубрика:
КЛИНИЧЕСКАЯ И ЭКСПЕРИМЕНТАЛЬНАЯ МЕДИЦИНА
Тип статьи:
Научная статья.
Аннотация:
Статья посвящена изучению факторов развития невропатий при болезни Паркинсона и их влияния на ход, тяжесть заболевания. Выявлено, что кроме основных признаков болезни Паркинсона – тремора
покоя, бради- или акинезии, ригидности, в медицинской картине преобладают признаки периферической
нейропатии верхних конечностей. Характер неврологических нарушений зависит от формы болезни.
Целью исследования стало изучение частоты возникновения и течение туннельных нейропатий верхних
конечностей у пациентов с болезнью Паркинсона.
С помощью электронейромиографического обследования периферических нервов верхних конечностей
проведен анализ нарушений нервно-мышечной проводимости на разных уровнях. Так, у пациентов с акинетико-ригидной формой преобладают признаки нарушения нервно-мышечной проводимости по срединному
и локтевом нервам демиелинизирующего характера. Это может быть объяснено преобладанием в клинической картине брадикинезией, пребывание длительное время в вынужденном положении. В группе пациентов с акинетико-ригидно-дрожащей формой заболевания диагностировано преобладание признаков
туннельной невропатии срединного нерва на уровне карпального канала, что может указывать на травматические поражения запястного канала вследствие частых повторяющихся движений при треморе.
Особенности течения различных форм заболевания нужно учитывать при ведении пациентов на любой
стадии заболевания.
Это может быть объяснено преобладанием в клинической картине брадикинезией, пребывание длительное время в вынужденном положении. В группе пациентов с акинетико-ригидно-дрожащей формой заболевания диагностировано преобладание признаков
туннельной невропатии срединного нерва на уровне карпального канала, что может указывать на травматические поражения запястного канала вследствие частых повторяющихся движений при треморе.
Особенности течения различных форм заболевания нужно учитывать при ведении пациентов на любой
стадии заболевания.
Ключевые слова:
болезнь Паркинсона, туннельный синдром, нейропатия, электронейромиография.
Список цитируемой литературы:
- Karaban IM. Khvoroba Parkinsona: patohenetychni aspekty medykamentoznoi terapii ta klinichnoho perebihu.
 Naukovyi zhurnal MOZ Ukrainy. 2014;2(6):60-70. [in Ukrainian].
Naukovyi zhurnal MOZ Ukrainy. 2014;2(6):60-70. [in Ukrainian]. - Bolezn’ Parkinsona (etiologiya, patogenez, klinika, diagnostika, lechenie, profilaktika). M.: Medicina; 2002. 335 s. [in Russian].
- Shtok VN. Bolezn’ Parkinsona. Ekstrapiramidnye rasstrojstva. Rukovodstvo po diagnostike i lecheniyu. M.: Medpress-inform; 2002. s. 87-124. [in Russian].
- Barone P, Antonini A, Colosimo C. The PRIAMO study: a multicenter assessment of nonmotor symptoms and their impact on quality of life in Parkinson’s disease. Movement Disorders. 2009;24(11):1641-9.
- Stacy MA. Dopamine agonists. Handbook of Parkinson’s disease. 4th edition. NY, London: Informa Healthcare; 2007. р. 335-8.
- Karaban’ IN, Shalenko OV, Krizhanovskij SN. Nemotornye simptomy v klinicheskoj kartine bolezni Parkinsona. Mezhdunarodnіj nevrologicheskij zhurnal. 2017;1(87):58-63. [in Russian].
- Levin OS. Bolezn’ Parkinsona: sovremennye podhody k diagnostike i lecheniyu. Prakticheskaya medicina. 2017;1(102):45-51. [in Russian].
- Ha AD, Jankovic J. Pain in Parkinson’s disease. Mov. Disord. 2012 Apr;27(4):485-91.
- Ford B. Pain in Parkinson’s disease. Mov Disord. 2010;25(1):98-103.
- Cossu G, Melis M. The peripheral nerve involvement in Parkinson Disease: a multifaceted phenomenon. Parkinsonism & Related Disorders. 2016;25:17-20.
- Yang SN, Kang HJ, Yoon JS, Won SJ, Seo WK, Koh SB. Is median nerve enlargement at the wrist associated with tremor in Parkinson disease. Journal of Ultrasound in Medicine. 2014;33(12):2079-83.
- Cingoz M, Kandemirli SG, Can Alis D, Samanci C. Evaluation of median nerve by shear wave elastography and diffusion tensor imaging in carpal tunnel syndrome. Research article. 2018 Apr;101:59-64.
- Mengi-Ozsarac G. Erratum to “Carpal tunnel syndrome in Parkinson’s disease”. European Journal of Radiology. 2008;67(3):503-50.
- Anouti A, Koller WC. Tremor disorders. Diagnosis and management. West J Med. 1995 June;162:510-3.
- Yardimci N, Cem Eroglu O, Oz Turk E, Gürlü G, Şahin E, Bozkurt S, Cengiz T. Median and Ulnar Neuropathy Assessment in Parkinson’s Disease regarding Symptom Severity and Asymmetry. Parkinson’s Disease. 2016;2016:4958068.
- Werner CO, Ohlin P, Elmqvis D. Pressures recorded in ulnar neuropathy. Acta Orthopaedica. 1985;56(5):404-6.
- Van Rijn RM, Huisstede BM, Koes BW, Burdorf A. Associations between work-related factors and specific disorders at the elbow: a systematic literature revie. Rheumatology. 2009;48(5):528-36.
Публикация статьи:
«Вестник проблем биологии и медицины» Выпуск 2 (156), 2020 год, 170-174 страницы, код УДК 616.858.616.833-07
DOI:
Ранние признаки, причины и факторы риска
Болезнь Паркинсона — это двигательное расстройство, поражающее нервную систему. Его симптомы возникают из-за низкого уровня дофамина в головном мозге.
Эксперты не знают, почему развивается болезнь Паркинсона, но в настоящее время они считают, что генетические изменения и воздействие факторов окружающей среды, таких как токсины, играют ключевую роль.
Читайте дальше, чтобы узнать больше о ранних признаках болезни Паркинсона и причинах ее возникновения.
Симптомы болезни Паркинсона развиваются постепенно.Часто они начинаются с легкого тремора в одной руке и ощущения скованности в теле. Со временем развиваются другие симптомы, и у некоторых людей может развиться слабоумие.
Некоторые ранние признаки болезни Паркинсона могут включать:
- изменения движений, такие как тремор
- нарушения координации и равновесия, которые могут привести к тому, что человек роняет вещи или падает с высоты
- потеря обоняния
- изменения походки, поэтому человек слегка наклоняется вперед или шаркает при ходьбе
- фиксированное выражение лица из-за изменений нервов, которые контролируют мышцы лица
- голосовое дрожание или более мягкий голос
- более сжатый и мелкий почерк
- проблемы со сном, вызванные беспокойными ногами и другими факторы
- Расстройство сна с быстрым движением глаз может быть мощным предиктором, согласно исследованию 2015 года.
Симптомы движения могут начинаться на одной стороне тела и постепенно влиять на обе стороны.
Другие общие симптомы включают:
- изменения настроения, включая депрессию
- трудности с жеванием и глотанием
- усталость
- запор
- кожные проблемы
- слабоумие, бред и галлюцинации, которые могут развиться со временем
наличие этих симптомов не означает, что у человека болезнь Паркинсона. Различные другие состояния могут иметь похожие симптомы, например:
В настоящее время нет тестов на болезнь Паркинсона.Его сходство с другими состояниями может затруднить диагностику на ранних стадиях.
Узнайте больше о том, как врачи диагностируют болезнь Паркинсона.
Покрывает ли Medicare болезнь Паркинсона?
Болезнь Паркинсона — это неврологическое заболевание, которое развивается, когда в головном мозге происходят изменения. Неясно, почему именно это происходит, но ученые определили некоторые возможные вариации.
Низкий уровень дофамина
Симптомы болезни Паркинсона в основном возникают из-за низкого или падающего уровня дофамина, нейромедиатора.Это происходит, когда клетки, производящие дофамин, умирают в головном мозге.
Дофамин играет роль в отправке сообщений той части мозга, которая контролирует движение и координацию. Таким образом, из-за низкого уровня дофамина людям становится сложнее контролировать свои движения.
По мере того, как уровень дофамина продолжает падать, симптомы постепенно становятся более серьезными.
Низкий уровень норадреналина
Болезнь Паркинсона может также включать повреждение нервных окончаний, вырабатывающих другой нейромедиатор, норадреналин, который способствует кровообращению и другим автоматическим функциям организма.
Низкий уровень норадреналина при болезни Паркинсона может увеличить риск как двигательных, так и немоторных симптомов, таких как:
- ригидность и ригидность
- нестабильность осанки
- тремор
- тревога
- трудности с фокусировкой
- деменция
- депрессия
Это может объяснить, почему люди с болезнью Паркинсона обычно испытывают ортостатическую гипотензию. Это относится к случаям, когда у человека изменяется кровяное давление, когда он встает, что приводит к головокружению и риску падения.
Тельца Леви
У человека с болезнью Паркинсона в мозгу могут быть скопления белка, известные как альфа-синуклеин, или тельца Леви.
Накопление тельцов Леви может вызвать потерю нервных клеток, что приведет к изменениям в движении, мышлении, поведении и настроении. Это также может привести к слабоумию.
Деменция с тельцами Леви — это не то же самое, что болезнь Паркинсона, но у людей может быть и то, и другое, поскольку симптомы схожи.
Узнайте больше о деменции с тельцами Леви.
Генетические факторы
Эксперты определили изменения в нескольких генах, которые, по-видимому, связаны с болезнью Паркинсона, но не считают это наследственным заболеванием.
Генетические факторы, по-видимому, вызывают только 10% случаев, в основном среди людей с ранним началом заболевания.
Аутоиммунные факторы
В исследовании 2017 года ученые обнаружили возможную генетическую связь между болезнью Паркинсона и аутоиммунными заболеваниями, такими как ревматоидный артрит.
В 2018 году исследователи, изучающие медицинские карты Тайваня, обнаружили, что люди с аутоиммунными ревматическими заболеваниями имели 1.37-более высокий шанс также иметь болезнь Паркинсона.
Несколько факторов окружающей среды могут увеличить риск развития болезни Паркинсона.
К ним относятся:
- Перенесенная черепно-мозговая травма: Травмы головы, например, в результате контактных видов спорта, могут повысить риск заболевания.
- Воздействие токсинов: Например, пестициды, растворители, металлы и другие загрязнители.
- Пол: У мужчин на 50% больше шансов заболеть этим заболеванием, чем у женщин, хотя одно исследование 2016 года предполагает, что риск для женщин может увеличиваться с возрастом.
- Возраст: Состояние часто появляется в возрасте от 60 лет.
- Некоторые лекарства и медикаменты: Некоторые лекарства могут вызывать паркинсонизм, когда человек испытывает тремор и другие симптомы, но не страдает болезнью Паркинсона.
Симптомы обычно появляются с 60 лет. Однако у 5–10% людей болезнь Паркинсона проявляется в раннем возрасте, который начинается в возрасте до 50 лет.
Влияют ли расовые факторы на риск?
В прошлом статистика предполагала, что болезнь Паркинсона с меньшей вероятностью поражает чернокожих людей, чем других людей других национальностей в Соединенных Штатах.
Однако теперь эксперты говорят, что это может быть связано с недостаточной осведомленностью о том, как болезнь может повлиять на чернокожих, и с более высокой вероятностью ошибочного диагноза из-за неравенства в обеспечении здоровья.
Дополнительную информацию по вопросам справедливости в отношении здоровья см. В нашем специализированном центре.
Невозможно предотвратить болезнь Паркинсона, но некоторые жизненные привычки могут помочь снизить риск.
Как избежать токсинов
Люди должны принимать меры предосторожности при использовании потенциально токсичных химикатов, таких как гербициды, пестициды и растворители.
По возможности, люди должны предпринять следующие шаги:
- избегать ненужного использования пестицидов и гербицидов
- использовать альтернативы продуктам, содержащим известные токсины, такие как паракват
- принимать меры предосторожности, такие как ношение защитной одежды, когда это необходимо. их невозможно избежать
Узнайте больше о пестицидах в продуктах питания.
Избегайте травм головы
Для защиты от черепно-мозговой травмы люди могут предпринять следующие шаги:
- носить защитный головной убор во время контактных видов спорта
- носить шлем во время езды на велосипеде или мотоцикле
- использовать ремень безопасности при поездке на автомобиле
- обратиться за медицинской помощью при сотрясении мозга и избежать будущих рисков, пока врач не скажет, что это безопасно.
Физические упражнения
Согласно обзору 2018 года, регулярные физические упражнения могут помочь предотвратить или вылечить болезнь Паркинсона.Авторы отмечают, что физическая активность может помочь поддерживать уровень дофамина в мозге.
Диетические факторы
Некоторые варианты питания также могут помочь снизить риск болезни Паркинсона и других заболеваний. Исследования показали, что могут помочь следующие продукты:
- Куркума: Слабая пряность, которую люди могут добавлять в карри, супы, чаи и другие продукты. Он содержит куркумин, антиоксидантный ингредиент. Согласно одному лабораторному исследованию, это может помочь снизить риск болезни Паркинсона, предотвращая окислительный стресс и скопление альфа-синуклеинового белка.
- Флавоноиды: Исследования показывают, что этот антиоксидант может снизить риск развития болезни Паркинсона. Ягоды, яблоки, некоторые овощи, чай и красный виноград содержат флавоноиды.
- Избегание альдегидов: Нагревание и повторное использование некоторых кулинарных масел, таких как подсолнечное масло, может вызвать образование альдегидов, которые являются токсичными химическими веществами, связанными с болезнью Паркинсона и другими заболеваниями. Исследования 2020 года показывают, что картофель, обжаренный в ранее использовавшемся кулинарном масле, может иметь высокий уровень альдегидов.
Получите здесь еще несколько советов о том, как диета может помочь в лечении болезни Паркинсона.
Болезнь Паркинсона — это пожизненное заболевание, сопровождающееся неврологическими изменениями в организме.
Эксперты не знают, почему возникает болезнь Паркинсона, но генетические факторы и факторы окружающей среды могут иметь значение. В частности, эксперты обнаружили тесную связь с прошлыми черепно-мозговыми травмами и воздействием токсинов.
Упражнения, здоровое питание и отказ от токсинов — все это может помочь предотвратить болезнь Паркинсона, но в настоящее время нет доказательств, подтверждающих конкретную причину.
Ранние признаки, причины и факторы риска
Болезнь Паркинсона — это двигательное расстройство, поражающее нервную систему. Его симптомы возникают из-за низкого уровня дофамина в головном мозге.
Эксперты не знают, почему развивается болезнь Паркинсона, но в настоящее время они считают, что генетические изменения и воздействие факторов окружающей среды, таких как токсины, играют ключевую роль.
Читайте дальше, чтобы узнать больше о ранних признаках болезни Паркинсона и причинах ее возникновения.
Симптомы болезни Паркинсона развиваются постепенно.Часто они начинаются с легкого тремора в одной руке и ощущения скованности в теле. Со временем развиваются другие симптомы, и у некоторых людей может развиться слабоумие.
Некоторые ранние признаки болезни Паркинсона могут включать:
- изменения движений, такие как тремор
- нарушения координации и равновесия, которые могут привести к тому, что человек роняет вещи или падает с высоты
- потеря обоняния
- изменения походки, поэтому человек слегка наклоняется вперед или шаркает при ходьбе
- фиксированное выражение лица из-за изменений нервов, которые контролируют мышцы лица
- голосовое дрожание или более мягкий голос
- более сжатый и мелкий почерк
- проблемы со сном, вызванные беспокойными ногами и другими факторы
- Расстройство сна с быстрым движением глаз может быть мощным предиктором, согласно исследованию 2015 года.
Симптомы движения могут начинаться на одной стороне тела и постепенно влиять на обе стороны.
Другие общие симптомы включают:
- изменения настроения, включая депрессию
- трудности с жеванием и глотанием
- усталость
- запор
- кожные проблемы
- слабоумие, бред и галлюцинации, которые могут развиться со временем
наличие этих симптомов не означает, что у человека болезнь Паркинсона. Различные другие состояния могут иметь похожие симптомы, например:
В настоящее время нет тестов на болезнь Паркинсона.Его сходство с другими состояниями может затруднить диагностику на ранних стадиях.
Узнайте больше о том, как врачи диагностируют болезнь Паркинсона.
Покрывает ли Medicare болезнь Паркинсона?
Болезнь Паркинсона — это неврологическое заболевание, которое развивается, когда в головном мозге происходят изменения. Неясно, почему именно это происходит, но ученые определили некоторые возможные вариации.
Низкий уровень дофамина
Симптомы болезни Паркинсона в основном возникают из-за низкого или падающего уровня дофамина, нейромедиатора.Это происходит, когда клетки, производящие дофамин, умирают в головном мозге.
Дофамин играет роль в отправке сообщений той части мозга, которая контролирует движение и координацию. Таким образом, из-за низкого уровня дофамина людям становится сложнее контролировать свои движения.
По мере того, как уровень дофамина продолжает падать, симптомы постепенно становятся более серьезными.
Низкий уровень норадреналина
Болезнь Паркинсона может также включать повреждение нервных окончаний, вырабатывающих другой нейромедиатор, норадреналин, который способствует кровообращению и другим автоматическим функциям организма.
Низкий уровень норадреналина при болезни Паркинсона может увеличить риск как двигательных, так и немоторных симптомов, таких как:
- ригидность и ригидность
- нестабильность осанки
- тремор
- тревога
- трудности с фокусировкой
- деменция
- депрессия
Это может объяснить, почему люди с болезнью Паркинсона обычно испытывают ортостатическую гипотензию. Это относится к случаям, когда у человека изменяется кровяное давление, когда он встает, что приводит к головокружению и риску падения.
Тельца Леви
У человека с болезнью Паркинсона в мозгу могут быть скопления белка, известные как альфа-синуклеин, или тельца Леви.
Накопление тельцов Леви может вызвать потерю нервных клеток, что приведет к изменениям в движении, мышлении, поведении и настроении. Это также может привести к слабоумию.
Деменция с тельцами Леви — это не то же самое, что болезнь Паркинсона, но у людей может быть и то, и другое, поскольку симптомы схожи.
Узнайте больше о деменции с тельцами Леви.
Генетические факторы
Эксперты определили изменения в нескольких генах, которые, по-видимому, связаны с болезнью Паркинсона, но не считают это наследственным заболеванием.
Генетические факторы, по-видимому, вызывают только 10% случаев, в основном среди людей с ранним началом заболевания.
Аутоиммунные факторы
В исследовании 2017 года ученые обнаружили возможную генетическую связь между болезнью Паркинсона и аутоиммунными заболеваниями, такими как ревматоидный артрит.
В 2018 году исследователи, изучающие медицинские карты Тайваня, обнаружили, что люди с аутоиммунными ревматическими заболеваниями имели 1.37-более высокий шанс также иметь болезнь Паркинсона.
Несколько факторов окружающей среды могут увеличить риск развития болезни Паркинсона.
К ним относятся:
- Перенесенная черепно-мозговая травма: Травмы головы, например, в результате контактных видов спорта, могут повысить риск заболевания.
- Воздействие токсинов: Например, пестициды, растворители, металлы и другие загрязнители.
- Пол: У мужчин на 50% больше шансов заболеть этим заболеванием, чем у женщин, хотя одно исследование 2016 года предполагает, что риск для женщин может увеличиваться с возрастом.
- Возраст: Состояние часто появляется в возрасте от 60 лет.
- Некоторые лекарства и медикаменты: Некоторые лекарства могут вызывать паркинсонизм, когда человек испытывает тремор и другие симптомы, но не страдает болезнью Паркинсона.
Симптомы обычно появляются с 60 лет. Однако у 5–10% людей болезнь Паркинсона проявляется в раннем возрасте, который начинается в возрасте до 50 лет.
Влияют ли расовые факторы на риск?
В прошлом статистика предполагала, что болезнь Паркинсона с меньшей вероятностью поражает чернокожих людей, чем других людей других национальностей в Соединенных Штатах.
Однако теперь эксперты говорят, что это может быть связано с недостаточной осведомленностью о том, как болезнь может повлиять на чернокожих, и с более высокой вероятностью ошибочного диагноза из-за неравенства в обеспечении здоровья.
Дополнительную информацию по вопросам справедливости в отношении здоровья см. В нашем специализированном центре.
Невозможно предотвратить болезнь Паркинсона, но некоторые жизненные привычки могут помочь снизить риск.
Как избежать токсинов
Люди должны принимать меры предосторожности при использовании потенциально токсичных химикатов, таких как гербициды, пестициды и растворители.
По возможности, люди должны предпринять следующие шаги:
- избегать ненужного использования пестицидов и гербицидов
- использовать альтернативы продуктам, содержащим известные токсины, такие как паракват
- принимать меры предосторожности, такие как ношение защитной одежды, когда это необходимо. их невозможно избежать
Узнайте больше о пестицидах в продуктах питания.
Избегайте травм головы
Для защиты от черепно-мозговой травмы люди могут предпринять следующие шаги:
- носить защитный головной убор во время контактных видов спорта
- носить шлем во время езды на велосипеде или мотоцикле
- использовать ремень безопасности при поездке на автомобиле
- обратиться за медицинской помощью при сотрясении мозга и избежать будущих рисков, пока врач не скажет, что это безопасно.
Физические упражнения
Согласно обзору 2018 года, регулярные физические упражнения могут помочь предотвратить или вылечить болезнь Паркинсона.Авторы отмечают, что физическая активность может помочь поддерживать уровень дофамина в мозге.
Диетические факторы
Некоторые варианты питания также могут помочь снизить риск болезни Паркинсона и других заболеваний. Исследования показали, что могут помочь следующие продукты:
- Куркума: Слабая пряность, которую люди могут добавлять в карри, супы, чаи и другие продукты. Он содержит куркумин, антиоксидантный ингредиент. Согласно одному лабораторному исследованию, это может помочь снизить риск болезни Паркинсона, предотвращая окислительный стресс и скопление альфа-синуклеинового белка.
- Флавоноиды: Исследования показывают, что этот антиоксидант может снизить риск развития болезни Паркинсона. Ягоды, яблоки, некоторые овощи, чай и красный виноград содержат флавоноиды.
- Избегание альдегидов: Нагревание и повторное использование некоторых кулинарных масел, таких как подсолнечное масло, может вызвать образование альдегидов, которые являются токсичными химическими веществами, связанными с болезнью Паркинсона и другими заболеваниями. Исследования 2020 года показывают, что картофель, обжаренный в ранее использовавшемся кулинарном масле, может иметь высокий уровень альдегидов.
Получите здесь еще несколько советов о том, как диета может помочь в лечении болезни Паркинсона.
Болезнь Паркинсона — это пожизненное заболевание, сопровождающееся неврологическими изменениями в организме.
Эксперты не знают, почему возникает болезнь Паркинсона, но генетические факторы и факторы окружающей среды могут иметь значение. В частности, эксперты обнаружили тесную связь с прошлыми черепно-мозговыми травмами и воздействием токсинов.
Упражнения, здоровое питание и отказ от токсинов — все это может помочь предотвратить болезнь Паркинсона, но в настоящее время нет доказательств, подтверждающих конкретную причину.
Ранние признаки, причины и факторы риска
Болезнь Паркинсона — это двигательное расстройство, поражающее нервную систему. Его симптомы возникают из-за низкого уровня дофамина в головном мозге.
Эксперты не знают, почему развивается болезнь Паркинсона, но в настоящее время они считают, что генетические изменения и воздействие факторов окружающей среды, таких как токсины, играют ключевую роль.
Читайте дальше, чтобы узнать больше о ранних признаках болезни Паркинсона и причинах ее возникновения.
Симптомы болезни Паркинсона развиваются постепенно.Часто они начинаются с легкого тремора в одной руке и ощущения скованности в теле. Со временем развиваются другие симптомы, и у некоторых людей может развиться слабоумие.
Некоторые ранние признаки болезни Паркинсона могут включать:
- изменения движений, такие как тремор
- нарушения координации и равновесия, которые могут привести к тому, что человек роняет вещи или падает с высоты
- потеря обоняния
- изменения походки, поэтому человек слегка наклоняется вперед или шаркает при ходьбе
- фиксированное выражение лица из-за изменений нервов, которые контролируют мышцы лица
- голосовое дрожание или более мягкий голос
- более сжатый и мелкий почерк
- проблемы со сном, вызванные беспокойными ногами и другими факторы
- Расстройство сна с быстрым движением глаз может быть мощным предиктором, согласно исследованию 2015 года.
Симптомы движения могут начинаться на одной стороне тела и постепенно влиять на обе стороны.
Другие общие симптомы включают:
- изменения настроения, включая депрессию
- трудности с жеванием и глотанием
- усталость
- запор
- кожные проблемы
- слабоумие, бред и галлюцинации, которые могут развиться со временем
наличие этих симптомов не означает, что у человека болезнь Паркинсона. Различные другие состояния могут иметь похожие симптомы, например:
В настоящее время нет тестов на болезнь Паркинсона.Его сходство с другими состояниями может затруднить диагностику на ранних стадиях.
Узнайте больше о том, как врачи диагностируют болезнь Паркинсона.
Покрывает ли Medicare болезнь Паркинсона?
Болезнь Паркинсона — это неврологическое заболевание, которое развивается, когда в головном мозге происходят изменения. Неясно, почему именно это происходит, но ученые определили некоторые возможные вариации.
Низкий уровень дофамина
Симптомы болезни Паркинсона в основном возникают из-за низкого или падающего уровня дофамина, нейромедиатора.Это происходит, когда клетки, производящие дофамин, умирают в головном мозге.
Дофамин играет роль в отправке сообщений той части мозга, которая контролирует движение и координацию. Таким образом, из-за низкого уровня дофамина людям становится сложнее контролировать свои движения.
По мере того, как уровень дофамина продолжает падать, симптомы постепенно становятся более серьезными.
Низкий уровень норадреналина
Болезнь Паркинсона может также включать повреждение нервных окончаний, вырабатывающих другой нейромедиатор, норадреналин, который способствует кровообращению и другим автоматическим функциям организма.
Низкий уровень норадреналина при болезни Паркинсона может увеличить риск как двигательных, так и немоторных симптомов, таких как:
- ригидность и ригидность
- нестабильность осанки
- тремор
- тревога
- трудности с фокусировкой
- деменция
- депрессия
Это может объяснить, почему люди с болезнью Паркинсона обычно испытывают ортостатическую гипотензию. Это относится к случаям, когда у человека изменяется кровяное давление, когда он встает, что приводит к головокружению и риску падения.
Тельца Леви
У человека с болезнью Паркинсона в мозгу могут быть скопления белка, известные как альфа-синуклеин, или тельца Леви.
Накопление тельцов Леви может вызвать потерю нервных клеток, что приведет к изменениям в движении, мышлении, поведении и настроении. Это также может привести к слабоумию.
Деменция с тельцами Леви — это не то же самое, что болезнь Паркинсона, но у людей может быть и то, и другое, поскольку симптомы схожи.
Узнайте больше о деменции с тельцами Леви.
Генетические факторы
Эксперты определили изменения в нескольких генах, которые, по-видимому, связаны с болезнью Паркинсона, но не считают это наследственным заболеванием.
Генетические факторы, по-видимому, вызывают только 10% случаев, в основном среди людей с ранним началом заболевания.
Аутоиммунные факторы
В исследовании 2017 года ученые обнаружили возможную генетическую связь между болезнью Паркинсона и аутоиммунными заболеваниями, такими как ревматоидный артрит.
В 2018 году исследователи, изучающие медицинские карты Тайваня, обнаружили, что люди с аутоиммунными ревматическими заболеваниями имели 1.37-более высокий шанс также иметь болезнь Паркинсона.
Несколько факторов окружающей среды могут увеличить риск развития болезни Паркинсона.
К ним относятся:
- Перенесенная черепно-мозговая травма: Травмы головы, например, в результате контактных видов спорта, могут повысить риск заболевания.
- Воздействие токсинов: Например, пестициды, растворители, металлы и другие загрязнители.
- Пол: У мужчин на 50% больше шансов заболеть этим заболеванием, чем у женщин, хотя одно исследование 2016 года предполагает, что риск для женщин может увеличиваться с возрастом.
- Возраст: Состояние часто появляется в возрасте от 60 лет.
- Некоторые лекарства и медикаменты: Некоторые лекарства могут вызывать паркинсонизм, когда человек испытывает тремор и другие симптомы, но не страдает болезнью Паркинсона.
Симптомы обычно появляются с 60 лет. Однако у 5–10% людей болезнь Паркинсона проявляется в раннем возрасте, который начинается в возрасте до 50 лет.
Влияют ли расовые факторы на риск?
В прошлом статистика предполагала, что болезнь Паркинсона с меньшей вероятностью поражает чернокожих людей, чем других людей других национальностей в Соединенных Штатах.
Однако теперь эксперты говорят, что это может быть связано с недостаточной осведомленностью о том, как болезнь может повлиять на чернокожих, и с более высокой вероятностью ошибочного диагноза из-за неравенства в обеспечении здоровья.
Дополнительную информацию по вопросам справедливости в отношении здоровья см. В нашем специализированном центре.
Невозможно предотвратить болезнь Паркинсона, но некоторые жизненные привычки могут помочь снизить риск.
Как избежать токсинов
Люди должны принимать меры предосторожности при использовании потенциально токсичных химикатов, таких как гербициды, пестициды и растворители.
По возможности, люди должны предпринять следующие шаги:
- избегать ненужного использования пестицидов и гербицидов
- использовать альтернативы продуктам, содержащим известные токсины, такие как паракват
- принимать меры предосторожности, такие как ношение защитной одежды, когда это необходимо. их невозможно избежать
Узнайте больше о пестицидах в продуктах питания.
Избегайте травм головы
Для защиты от черепно-мозговой травмы люди могут предпринять следующие шаги:
- носить защитный головной убор во время контактных видов спорта
- носить шлем во время езды на велосипеде или мотоцикле
- использовать ремень безопасности при поездке на автомобиле
- обратиться за медицинской помощью при сотрясении мозга и избежать будущих рисков, пока врач не скажет, что это безопасно.
Физические упражнения
Согласно обзору 2018 года, регулярные физические упражнения могут помочь предотвратить или вылечить болезнь Паркинсона.Авторы отмечают, что физическая активность может помочь поддерживать уровень дофамина в мозге.
Диетические факторы
Некоторые варианты питания также могут помочь снизить риск болезни Паркинсона и других заболеваний. Исследования показали, что могут помочь следующие продукты:
- Куркума: Слабая пряность, которую люди могут добавлять в карри, супы, чаи и другие продукты. Он содержит куркумин, антиоксидантный ингредиент. Согласно одному лабораторному исследованию, это может помочь снизить риск болезни Паркинсона, предотвращая окислительный стресс и скопление альфа-синуклеинового белка.
- Флавоноиды: Исследования показывают, что этот антиоксидант может снизить риск развития болезни Паркинсона. Ягоды, яблоки, некоторые овощи, чай и красный виноград содержат флавоноиды.
- Избегание альдегидов: Нагревание и повторное использование некоторых кулинарных масел, таких как подсолнечное масло, может вызвать образование альдегидов, которые являются токсичными химическими веществами, связанными с болезнью Паркинсона и другими заболеваниями. Исследования 2020 года показывают, что картофель, обжаренный в ранее использовавшемся кулинарном масле, может иметь высокий уровень альдегидов.
Получите здесь еще несколько советов о том, как диета может помочь в лечении болезни Паркинсона.
Болезнь Паркинсона — это пожизненное заболевание, сопровождающееся неврологическими изменениями в организме.
Эксперты не знают, почему возникает болезнь Паркинсона, но генетические факторы и факторы окружающей среды могут иметь значение. В частности, эксперты обнаружили тесную связь с прошлыми черепно-мозговыми травмами и воздействием токсинов.
Упражнения, здоровое питание и отказ от токсинов — все это может помочь предотвратить болезнь Паркинсона, но в настоящее время нет доказательств, подтверждающих конкретную причину.
Как «Партнерская поддержка» помогает улучшить жизнь с помощью PD
Итак, что я скажу кому-то, если они спросят меня: «Чем я могу помочь?»
Совместное использование того, что я называю «партнерством поддержки», означает делиться моментом и одновременно понимать общий смысл. Задача в этот момент может быть любой. Это экзистенциальное знание означает, что партнеры в этом поддерживающем партнерстве разделяют понимание и понимание природы существования в данный момент.Оба рассматривают взаимно согласованные задачи поддержки как необходимые для удовлетворения потребностей.
Многие проблемы могут возникнуть, когда партнеры не согласны с необходимостью поддержки.
Миссис доктор С. и я все еще время от времени сталкиваемся с этой проблемой. Она очень хорошо приспособлена к тому, что мне нужно ежедневно: поддержанию дома, выполнению поручений, поддержанию контакта с друзьями и семьей, а также тому, чтобы быть лицом к лицу, например, когда дело доходит до общения о проектах.
Она говорит, что я вижу «общую картину», а не детали.В большинстве случаев я могу сообщить то, что мне нужно. В большинстве случаев она это понимает.
Однако бывают моменты, когда нам обоим требуется сочувствие и поддержка, потому что болезнь Паркинсона и потеря зрения создают серьезные препятствия. Г-жа доктор С. говорит, что люди, не связанные с болезнью Паркинсона, например семья и друзья, не понимают, что значит жить с болезнью каждый день и все время. Я согласен с тем, что «жизнь кажется лишь промежуточной между отношениями». Наши отношения поддержки облегчают преодоление приливной волны трудностей.
Г-жа Д-р С. говорит: «Я стараюсь показать позитивное отношение к друзьям, семье и публике. Это были годы изучения отлаженных отношений поддержки. В день диагностики БП никто не вручил нам мануал. Было такое ощущение, что нас выбросило за борт, оставив цепляться за обломки коряги ».
Одна из глав в книге, которую я пишу, посвящена партнерской поддержке. Поддержка, если она работает хорошо, — это партнерство. Желаю, чтобы когда я был моложе, я понимал это так же ясно, как сейчас.На своем пути я совершил множество ошибок в отношениях, которые являются одними из самых больших демонов, прячущихся в моем шкафу. Замена этих демонов — это взаимопомощь в партнерстве. Это взаимное качество состоит из сочувствия и понимания, а также искреннего стремления помочь как пациенту с ПД, так и его опекуну. Для меня это ответ на вопрос: «Чем я могу помочь?»
Сочувствие часто считается нашей женской чувствительностью к страданию другого человека. Я вижу сочувствие как способность человека резонировать с эмоциональным состоянием другого человека в данный момент.Именно это общее эмоциональное состояние становится важной частью поддерживающего партнерства.
Мы обнаружили, что это процесс «по очереди». Мы не можем одновременно испытывать эмоциональный стресс. Один человек должен сделать шаг назад и практиковать по-настоящему чуткие и активные навыки слушания. Это взаимно согласованный процесс, хотя иногда и подсознательный, который улучшает преимущества партнерства поддержки.
В рамках партнерства поддержки есть нечто большее, чем болезнь Паркинсона.Мой мозг всегда размышляет о состоянии человечества. Так всегда работал мой ум. Я называю это «проектным погружением», и это была моя работа и академический стиль для творческого решения проблем. Сложно сформулировать.
В моем исследовании изучались описания священных опытов исцеления, предлагаемых людьми, которые их пережили. Эти люди сказали, что им было трудно делиться своим опытом даже с близкими. Когда этот опыт выходит за рамки нормального восприятия, почти невозможно точно передать интенсивность события.
Даже с моими навыками словаря это довольно сложно. Но мне нравится делиться.
Ответ на вопрос «Чем могу помочь?» предложить сочувствие.
Сочувствие, понимание и экзистенциальное знание делают партнерство с высококачественной поддержкой. Требуется упорный труд и много лет, чтобы научиться предлагать партнерскую поддержку. К сожалению, наше общество решило, что культурно вознагражденным достижениям одного члена этого партнерства следует придавать большее значение, чем другому.
В течение этого месяца осведомленности о болезни Паркинсона я предлагаю всем, у кого есть болезнь Паркинсона, выделить момент, чтобы поблагодарить тех, кто помогает сделать их жизнь максимально счастливой и которые помогают достигать общих целей с помощью повседневных задач, которые обеспечивают основу.
Партнерство поддержки, когда оно работает хорошо, — это вещь изящества и красоты, более священная, чем кольцо Фродо.
***
Примечание: Новости Паркинсона сегодня — это строго новостной и информационный веб-сайт об этой болезни.Он не предоставляет медицинские консультации, диагностику или лечение . Этот контент не предназначен для замены профессиональных медицинских консультаций, диагностики или лечения . Всегда обращайтесь за советом к своему врачу или другому квалифицированному поставщику медицинских услуг по любым вопросам, которые могут у вас возникнуть относительно состояния здоровья. Никогда не игнорируйте профессиональные медицинские советы и не откладывайте их поиск из-за того, что вы прочитали на этом веб-сайте. Мнения, выраженные в этой колонке, не совпадают с мнениями Parkinson’s News Today или ее материнской компании BioNews и предназначены для того, чтобы вызвать обсуждение вопросов, относящихся к болезни Паркинсона.
Доктор С. — знакомый псевдоним читателям, которые посещают «Возможности болезни Паркинсона». Любовь к писательству охватила его карьеру теоретика-исследователя, клинициста по реабилитации мозга и профессора колледжа. У доктора С. впервые диагностировали болезнь Паркинсона на ранней стадии в 2014 году. Его интерес к тому, как болезнь Паркинсона может проявляться в других телесных и психических симптомах, стал предметом его исследований и написания статей.Его цель — поделиться текущими медицинскими исследованиями о том, как можно диагностировать болезнь Паркинсона на ранних стадиях, и помочь другим пациентам с ранней стадией болезни Паркинсона управлять своим процессом болезни с помощью целостного подхода к лечению.
Почему генеральный директор Фонда Паркинсона проявил смелость перед лицом пандемии
Апрель — это месяц осведомленности о болезни Паркинсона, который чествует более миллиона американцев, которые в настоящее время страдают болезнью Паркинсона, и 60 000 американцев, которым ежегодно ставится новый диагноз.При таких цифрах вполне вероятно, что болезнь Паркинсона каким-то образом повлияла на более широкое сообщество генеральных директоров — будь то любимый человек, коллега или наставник.
Я разговаривал с Джоном Л. Лером, президентом и генеральным директором Фонда Паркинсона, который подтвердил эти цифры и подчеркнул важность адаптации во время пандемии COVID-19 для обслуживания этого сообщества. Мы также обсудили, почему Фонд Паркинсона продолжал выдвигать смелые инициативы перед лицом пандемии и как другие руководители могут продолжать фокусироваться на росте в трудные времена.
Президент и главный исполнительный директор Фонда Джона Л. Лера Паркинсона
Предоставлено Фондом ПаркинсонаРоберт Рейсс: Расскажите, чем выделяется Фонд Паркинсона.
Джон Л. Лер: Фонд Паркинсона — ведущее в стране сообщество людей, живущих с болезнью Паркинсона, тех, кто их любит, и тех, кто работает над тем, чтобы положить конец этой болезни. Наша миссия — сделать жизнь людей с болезнью Паркинсона лучше, улучшая лечение и продвигая исследования в направлении лечения.
Reiss: А как конкретно вы улучшаете жизнь людей с этим заболеванием?
Lehr: Мы объединяем людей с болезнью Паркинсона, партнеров по уходу, медицинских работников и исследователей, чтобы обеспечить каждому человеку с болезнью Паркинсона доступ к наилучшей помощи. Мы финансируем передовые исследования, которые приводят к прорывам в лечении и дают сообществу людей с болезнью Паркинсона ресурсы и эмоциональную поддержку, такие как наша двуязычная горячая линия, 1-800-4PD-INFO (473-4636).Все наши ресурсы и образовательные мероприятия бесплатны.
Reiss: Расскажите о своем важном прорыве в области геномики.
Лер: Прямо сейчас меня больше всего радует PD GENEration: Mapping the Future of Parkinson, наша национальная инициатива, которая предлагает бесплатное генетическое тестирование и генетическое консультирование для людей с болезнью Паркинсона. Наша инициатива направлена на то, чтобы дать людям с болезнью Паркинсона подробные сведения об их генетическом статусе, чтобы они могли больше узнать о болезни.
УчастникиPD GENEration получают генетическую консультацию, чтобы понять свои результаты. Новые знания позволяют им работать вместе со своим лечащим врачом, чтобы извлечь выгоду из этой новой информации. Когда дело доходит до ухода, врачи будут лучше информированы о своих пациентах, смогут составить более эффективный план лечения и порекомендовать более индивидуализированные клинические испытания. По сути, мы закладываем основу точной медицины при болезни Паркинсона.
В прошлом году мы объявили о возможности тестирования PD GENEration в домашних условиях.Мы продолжим использовать вариант на дому, чтобы тестировать большее количество людей, особенно в сельской местности. Мы также уделяем особое внимание привлечению латиноамериканского сообщества, которое исторически недопредставлено в клинических испытаниях.
Reiss: Как руководители могут адаптироваться к серьезным препятствиям на пути, например к пандемии COVID-19?
Лер: Никогда не упускайте из виду, что в какой-то момент вы вернетесь к росту, и будьте готовы вернуться к нападению. Когда началась пандемия, мы были на пути к рекордному году по доходам.Мы знали, что в последней трети финансового года нам нанесут удар, но также верили, что к концу года, нашему самому продуктивному сезону сбора средств, мы восстановимся.
Мы сделали все возможное, чтобы перейти от одной стороны спада к другой, не делая драконовских сокращений; мы сохранили подавляющее большинство нашей команды и перегруппировались, чтобы запустить новые виртуальные программы, которые отвечали потребностям нашего сообщества во время пандемии. Это очень окупилось. Сообщество оставалось вовлеченным, моральный дух в команде оставался высоким, и, в конце концов, мы пережили рекордный год сбора средств.Ни у кого нет хрустального шара, и случаются экономические спады, но планирование лучших дней всегда должно быть частью вашей стратегии.
Reiss: Что вы посоветуете руководителям компаний, чтобы они продолжали стимулировать рост в трудные времена?
Лер: Не упускайте из виду свое видение и цели миссии. Во-первых, прислушайтесь к мнению своих основных заинтересованных сторон и убедитесь, что их потребности удовлетворены. Затем сосредоточьтесь на получении дохода и распределении его на свои наиболее существенные или смелые программы.Например, наша инициатива PD GENEration — это то, чего наши доноры никогда раньше не видели, и она может произвести революцию в лечении болезни Паркинсона. Мы переработали нашу стратегию, чтобы привлечь больше внимания к инициативе, ее потенциалу и распространению на домашнее тестирование.
Пандемия действительно изменила то, как мы обслуживаем наших избирателей. Мы добились успеха, выяснив, где они были (в основном дома) и что им больше всего нужно, и адаптировали наши существующие программы и внедрили новые в соответствии с их потребностями.Фактически, мы сохраним многие из этих программ даже после того, как пандемия COVID-19 закончится, чтобы продолжать расширять нашу деятельность. Хотя в это трудно поверить, но в трудные времена могут появиться хорошие возможности; иногда нужно их переосмыслить и отыскать.
Для получения дополнительной информации о болезни Паркинсона и мероприятиях Фонда Паркинсона посетите веб-сайт Parkinson.org.
Что такое болезнь Паркинсона? | Американская ассоциация болезни Паркинсона.
Болезнь Паркинсона
Что это такое и как оно влияет на тех, кому поставили диагноз?
Болезнь Паркинсона (БП) — это тип двигательного расстройства, которое может влиять на способность выполнять обычные повседневные дела.Это хроническое и прогрессирующее заболевание, что означает, что симптомы со временем ухудшаются. Он характеризуется наиболее распространенными двигательными симптомами — тремором (форма ритмического тряски), ригидностью или ригидностью мышц и медлительностью движений (так называемая брадикинезия) — но также проявляется немоторными симптомами, включая проблемы со сном, запоры и т. беспокойство, депрессия и усталость, среди прочего.
По оценкам, 1 миллион человек в США живет с болезнью Паркинсона и более 10 миллионов человек во всем мире.Большинство людей, у которых развиваются симптомы болезни Паркинсона, развиваются примерно после 50 лет, но болезнь Паркинсона может поражать и молодых людей. Примерно 10% диагнозов Паркинсона ставятся в возрасте до 50 лет — эти диагнозы называются болезнью Паркинсона с ранним (или молодым) началом.
Как болезнь Паркинсона влияет на мозг
Болезнь Паркинсона отличается от других двигательных расстройств тем, что потеря клеток происходит в очень специфической области мозга, называемой черной субстанцией (sub-STAN-she-uh NYE-gruh).Нервные клетки или нейроны в этой области на самом деле кажутся темными под микроскопом (черная субстанция в переводе с латыни означает «черное вещество»).
Эти темные нейроны производят нейромедиатор особого типа (химический мессенджер, который позволяет нейронам общаться), называемый дофамином. Нейромедиатор дофамин помогает регулировать движение. Эта потеря дофамина является причиной того, что многие методы лечения болезни Паркинсона направлены на повышение уровня дофамина в головном мозге. Будем надеяться, что дальнейшие исследования расскажут нам больше об альфа-синуклеине.Узнайте больше об исследовательских инициативах APDA здесь.
Помимо снижения уровня дофамина и клеток, производящих дофамин, вы также можете прочитать или услышать об альфа-синуклеине (AL-fa-sin-NUKE-lee-un). Мы еще не знаем, что этот белок делает в здоровом мозге, но при болезни Паркинсона он накапливается в так называемых тельцах Леви (LOO-ee). Исследователи считают, что накопление альфа-синуклеина способствует возникновению болезни Паркинсона и что, возможно, можно будет разработать новые методы лечения, основанные на этой идее.
Узнайте больше о болезни Паркинсона
Болезнь Паркинсона: основы
Если вы впервые столкнулись с болезнью Паркинсона и хотите получить хороший обзор, который поможет вам лучше понять болезнь, просмотрите нашу презентацию Болезнь Паркинсона: Основы . Это отличное место для начала работы с надежной и краткой информацией.
Причины
Точная причина болезни Паркинсона до сих пор неизвестна, но проводится огромное количество исследований, чтобы узнать больше.Это исследование побудило ученых сформулировать ряд теорий о причине этого заболевания.
Диагностика
Хотя не существует однозначного теста, который можно было бы провести, чтобы определить, есть ли у человека болезнь Паркинсона, специалисты по двигательным расстройствам ищут симптомы и используют технологию визуализации мозга для точной диагностики болезни Паркинсона.
Симптомы
Несмотря на то, что болезнь Паркинсона классифицируется как двигательное расстройство, а его двигательные симптомы являются наиболее обсуждаемыми и хорошо известными, существует множество немоторных симптомов, которые также проявляются у людей с болезнью Паркинсона.
Процедуры
На сегодняшний день лекарства от болезни Паркинсона не существует. Но есть много способов вылечить болезнь, чтобы облегчить симптомы.
Жизнь с болезнью Паркинсона
Можно вести активный и позитивный образ жизни с помощью здорового выбора, медицинской помощи и поддержки со стороны семьи, друзей и общества.
Будьте в курсе последних новостей о болезни Паркинсона
Подробнее с доктором.Ребекка Гилберт
Более внимательный взгляд — это наша текущая серия статей, написанная доктором Ребеккой Гилберт, вице-президентом APDA и главным научным сотрудником. Доктор Гилберт обсуждает актуальные и вечные темы болезни Паркинсона и дает читателям идеи, применимые к их повседневной жизни.
Посетите более пристальный взглядЧто такое болезнь Паркинсона? — Новости Паркинсона сегодня
Болезнь названа в честь британского врача Джеймса Паркинсона, который впервые описал ее в «Очерке дрожащего паралича» в 1817 году.
При болезни Паркинсона нервные клетки, также называемые нейронами, в области мозга, называемой черной субстанцией, начинают работать со сбоями или умирать — процесс, называемый нейродегенерацией. Некоторые из нейронов отвечают за производство химического вещества, называемого дофамином. Дофамин действует как нейромедиатор, который передает сигналы между нейронами. Это важно для отправки сообщений из мозга, чтобы управлять движением и координацией мышц.
Болезнь Паркинсона — прогрессирующее заболевание, что означает, что симптомы со временем ухудшаются.По мере гибели большего количества нейронов, продуцирующих дофамин, уровни дофамина в головном мозге снижаются до тех пор, пока пациенты не могут контролировать нормальные движения. Это прогрессирование очень медленное, и симптомы обычно видны после потери примерно 70-80 процентов нервных клеток.
Симптомы
Симптомы болезни Паркинсона могут быть разными, но наиболее частыми идентифицирующими симптомами являются непроизвольный тремор, замедленное движение (брадикинезия), ригидность или скованность, а также нарушение равновесия. Болезнь Паркинсона также может вызывать ряд немоторных или «невидимых» симптомов, таких как проблемы со сном, запоры, невнятная речь и расстройства настроения.
Диагностика болезни Паркинсона
Поскольку не существует единого окончательного диагностического теста для болезни Паркинсона, и многие ранние симптомы также связаны со старением, может быть трудно диагностировать болезнь Паркинсона. Большинство людей, у которых диагностировано заболевание, старше 60 лет, хотя болезнь Паркинсона в раннем возрасте диагностирована в возрасте 40 лет и моложе.
Заболевание чаще встречается у мужчин, чем у женщин.
Причины болезни Паркинсона
Основная причина нейродегенерации, связанной с болезнью Паркинсона, в настоящее время неизвестна, хотя исследования процессов болезни продолжаются.Считается, что это заболевание является комбинацией генетических факторов и факторов окружающей среды.
Причину можно определить при более редких типах паркинсонизма. Этот диагноз можно назвать «болезнь Паркинсона плюс» или атипичный паркинсонизм.
Прогноз
Сама болезнь Паркинсонане считается смертельной, однако прогрессирование симптомов может снизить качество жизни и способствовать возникновению таких осложнений, как пневмония, которая может быть смертельной, если ее не лечить.


 Naukovyi zhurnal MOZ Ukrainy. 2014;2(6):60-70. [in Ukrainian].
Naukovyi zhurnal MOZ Ukrainy. 2014;2(6):60-70. [in Ukrainian].