Таблица боли: Шкала боли для невербальных пациентов — Про Паллиатив
Невыносимая боль: что такое шкала боли и нужно ли терпеть
Эдгар Дега, «Прачки, страдающие от зубной боли». Изображение с сайта forbes.ruОбезболивание – одна из самых болевых точек нашей медицины. Несмотря на некоторое упрощение порядка получения необходимых препаратов раковыми больными, проблема далека от решения, при этом в системе отечественного здравоохранения менеджмент боли не выделяется в отдельную отрасль знания и медицинского сервиса.
Между тем, в этой сфере медицины существуют международные стандарты, основанные на рекомендациях Всемирной организации здравоохранения. Они касаются обезболивания не только пациентов в последней стадии рака, но и других случаев острой и хронической боли и предполагают наличие в медицинских центрах специалистов по менеджменту боли, которые непременно участвуют в консилиумах других врачей, совместно разрабатывающих план лечения больного и ухода за ним.
Первая ступень в работе – это оценка боли.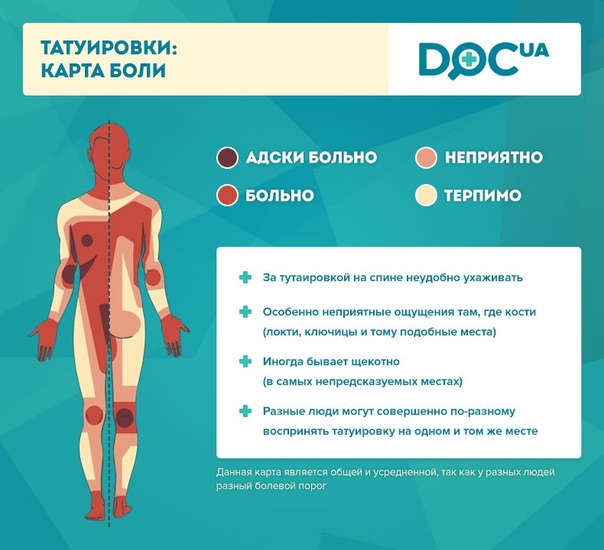
Шкала боли
0 – это полное отсутствие боли.
Дальше идет слабая боль (раздражает, но не очень мешает нормальной жизнедеятельности).
1 – боль очень слабая, едва заметная. Большую часть времени пациент о ней не думает.
2 – несильная боль. Она может раздражать и время от времени приступообразно усиливаться.
3 – боль заметна, она отвлекает, однако к ней можно привыкнуть и приспособиться.
Далее – боль средней тяжести (мешает нормальной жизнедеятельности).
4 – умеренная боль. Если человек глубоко погружен в какое-то занятие, он может игнорировать ее, но только в течение какого-то времени, однако затем она обязательно отвлечет внимание на себя.
5 – умеренно сильная боль. Ее нельзя игнорировать больше, чем несколько минут, но сделав над собой усилие, человек может выполнять какую-то работу или участвовать в каком-то мероприятии.
6 – умеренно сильная боль, которая мешает выполнять нормальные ежедневные действия, так как сосредоточение на чем-то становится чрезвычайно сложной задачей.
Следом идет жестокая боль (инвалидизирует, не позволяет выполнять обычные обязанности, общаться с людьми).
7 – тяжелая боль, подчиняющая себе все ощущения и существенно ограничивающая способность человека производить обычные действия и общаться с другими. Мешает спать.
8 – интенсивная боль. Физическая активность сильно ограничена. Словесное общение требует огромного усилия.
9 – мучительная боль. Человек не в состоянии разговаривать. Возможны неконтролируемые стоны или плач.
10 – невыносимая боль. Человек привязан к постели и, возможно, в бреду. Болевые ощущения такой силы приходится испытывать в течение жизни очень малому количеству людей.
Для того, чтобы сориентировать пациента, врач может повесить в своем кабинете шкалу с эмотиконами (смайликами), соответствующими ее делениям, от счастливой улыбки при 0 до лица, рыдающего в агонии при 10. Еще один ориентир, но только для женщин и только для рожавших, – это подсказка: естественные роды без обезболивания соответствуют отметке 8.
Шкала боли может показаться очень простой, но, по словам Стивена Коена, профессора отделения боли в Школе медицины имени Джона Хопкинса (Балтимор, США), она основана на довольно глубоких исследованиях.
Боль — это отдельное расстройство, требующее вмешательства
В западной медицине в отношении хронической боли с некоторых пор сместился акцент: ее больше не рассматривают просто как симптом того или иного заболевания, но как самостоятельное расстройство, требующее вмешательства. И если для большинства пациентов шкала боли является полезным инструментом, для некоторых она становится определяющей при выборе лечения.
«Шкала особенно важна для тех, кто имеет проблемы в коммуникации», – говорит Коен, имея в виду прежде всего маленьких детей и пациентов с когнитивными нарушениями.
Врачу, помимо оценки боли по шкале, важно знать и другие параметры. Так, доктор Седдон Сэвэдж, президент Американского сообщества боли и профессор анестезиологии в Дартмутской школе медицины (США), просит пациента рассказать о том, как менялся уровень боли в течение последней недели, как ведет себя боль в течение дня, усиливается ли к вечеру, дает ли возможность выспаться и так далее.
Если в работе с пациентом использовать шкалу постоянно, то с течением времени можно получить картину того, как влияет хроническая боль на его качество жизни, как работают терапии и обезболивающие препараты.
«Я также прошу больного показать мне на шкале, какой уровень боли будет приемлемым для него, – говорит Сэвэдж. – При хронических заболеваниях мы не всегда можем свести боль на нет, но возможно достичь того уровня, который позволит пациенту все-таки вести приемлемый образ жизни».
Специалисты по боли обязательно уточняют у пациента, каков ее характер: стреляющая, тупая, пульсирующая, есть ли ощущения жжения, покалывания или онемения, а также какие внешние факторы влияют на боль, что усиливает ее, а что ослабляет.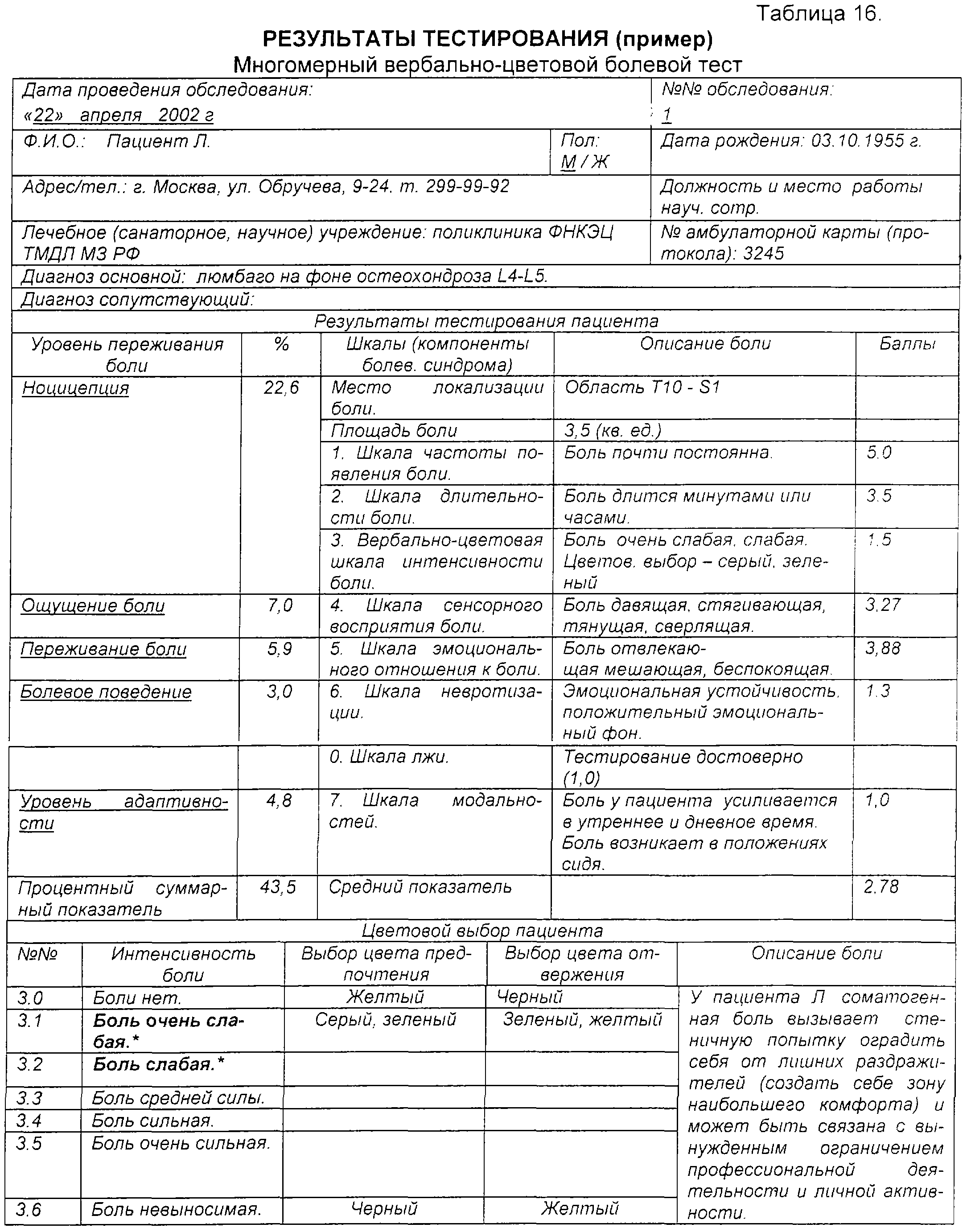
Жизненно важно не только то, насколько сильна боль пациента и каков ее характер, но также и то, как она влияет на его повседневную жизнь. Именно это и имеется в виду под сдвигом акцента. Врач должен сосредоточиться не только на лечении самого заболевания (что, безусловно, чрезвычайно важно), но и найти способ помочь пациенту как можно меньше отклоняться из-за боли от ведения нормального образа жизни.
Для этого, по словам Сэвэдж, необходимы совместные усилия ряда специалистов: лечащего врача, специалиста по боли, физического терапевта, психолога и психиатра, и, самое главное, самого пациента, который должен играть активную роль в процессе лечения.
Три ступени обезболивания
Стандарты обезболивания, применяемые в большинстве развитых стран, разработаны Всемирной организацией здравоохранения для онкологических больных, однако ими руководствуются специалисты по боли и в других случаях: при травмах, почечной колике, невралгиях, мигренях и других острых и хронических заболеваниях.
Для взрослых это трехступенчатая система обезболивания.
На первой ступени, то есть при слабой боли, больной получает ненаркотический анальгетик (парацетомол, аспирин, нестероидные противовоспалительные средства (далее – НПВС)) плюс адъювант. Под адъювантом понимается препарат, не имеющий обезболивающего действия, но купирующий страх или тревогу пациента, успокаивающий его.
Вторая ступень – при боли от слабой до умеренной. Для обезболивания применяется либо комбинация двух препаратов, парацетамол (ацетаминофен) или нестероидное противовоспалительное средство (ибупрофен, диклофенак и т.п.) плюс слабый наркотический препарат (кодеин, трамадол), либо один препарат из двух ингредиентов, например, Перкоцет (опиоид оксикодон плюс ацетаминофен), Викодин (гидрокодон плюс ацетаминофен). Как и в предыдущем случае, больному показано дополнительное средство для купирования тревоги.
На третьей ступени, при сильной боли, применяется сильный опиоид группы морфина плюс ненаркотический анальгетик плюс адъювант.
Золотой стандарт обезболивания – препарат морфин. Фентанил имеет меньше побочных эффектов, а также хорош тем, что может использоваться в форме пластыря, что очень удобно при хронической боли. В США одобрен ряд быстродействующих фармацевтических продуктов фентанила для лечения прорывной боли.
Прорывная боль – это болевой приступ, случающийся в промежутках между регулярным приемом анальгетиков. По стандартам ВОЗ, анальгетики вводятся больному каждые 3-6 часов, независимо от того, испытывает ли он в данный момент боль, или она еще не началась. В случае же прорывной боли он получает дополнительную дозу. При этом у пациента, находящегося дома, обязательно под рукой должно быть средство, позволяющее купировать боль быстро и самостоятельно, без помощи медицинского персонала.
Дети — особый случай
Стандарты обезболивания для детей отличаются от взрослых стандартов. В этом случае система не трех-, а двухступенчатая, исключающая взрослую вторую ступень. Объясняется это следующим образом.
У детей до 5 лет активность данного фермента составляет лишь 25% от того же показателя у взрослых, а потому кодеин для них неэффективен. Что касается другого слабого наркотического препарата, трамадола, широко применяющегося для обезболивания взрослых пациентов, он недостаточно хорошо изучен для применения в педиатрической практике и на сегодняшний день не лицензирован для нее.
Рекомендации ВОЗ по обезболиванию детей основаны на трех принципах:
- Введение дозы обезболивающего препарата через регулярные промежутки времени;
- Использование наименее инвазивного способа введения препарата;
- Индивидуальный подход.
Как и в рекомендациях по обезболиванию взрослых пациентов, эксперты ВОЗ предлагают вводить препараты «по часам», а не «по необходимости», однако подчеркивают, что, если возникает прорывная боль, наготове должно быть средство для ее купирования.
Для ребенка предпочтительнее оральный способ приема препаратов (в форме таблеток), а если это по какой-то причине невозможно, то ректальный (в форме свечей) или трансдермальный (пластырь). По возможности стоит избегать уколов, которые являются дополнительным источником боли и стресса для маленького ребенка.
Индивидуальный подход – это прежде всего, аккуратный подбор дозы, подходящей конкретному ребенку, и самого препарата с учетом побочных эффектов.
На первой ступени обезболивания эксперты рекомендуют парацетамол и ибупрофен (единственный из всех НПВС), на второй – морфин. Важная рекомендация экспертов – обязательное наличие как лекарственных форм морфина пролонгированного действия (для принятия через регулярные промежутки времени), так и быстродействующих форм на случай прорывной боли. При этом в рекомендациях отдельно оговаривается тот факт, что не существует верхней пороговой дозы морфина, и, если стандартная дозировка не дает облегчения, ее необходимо повысить.
Говорите о своей боли
Существуют и стандартные протоколы использования анальгетиков при разных заболеваниях.
При головной боли рекомендуется парацетамол и НПВС.
При мигрени – препараты первой линии также парацетамол и НПВС, однако если они не помогают, предлагается использовать триптаны.
При небольшой травме (синяки, царапины, растяжения) рекомендуется обойтись парацетамолом и НПВС, не прибегая к опиоидам.
При тяжелой травме (рана, ожог, перелом, очень сильное растяжение) следует применять опиоиды сроком до 2-х недель.
При послеопреационной боли рекомендуется применять парацетамол и НПВС, если операция была нетяжелой и, соответственно, послеоперационная боль не очень сильная, в противном случае – опиоиды.
Почечная колика – в зависимости от тяжести – парацетамол и НПВС либо опиоиды.
Изжога и гастроэнтеральный рефлюкс – антацидные средства, антогонисты Н2, ингибиторы протонной помпы; следует избегать аспирина и НПВС.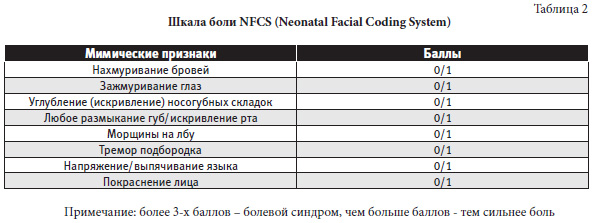
Хронические боли в спине – парацетамол и НПВС, в особо тяжелых случаях – опиоиды.
Фибромиалгия – антидепрессанты, антиконвульсанты.
Один из важных принципов менеджмента боли – это поощрение пациента к тому, чтобы он постоянно давал обратную связь, говорил откровенно о своих болевых ощущениях, высказывал мнение о лечении, даже если не согласен с мнением врача.
«Не нужно слушать тех, кто подвергает сомнению вашу боль, – говорит доктор Майкл Ферранте, директор Центра менеджмента боли (Лос-Анджелес). – Не уступайте их негативизму. Верьте себе и стремитесь к тому, чтобы получить правильное лечение».
Источники
:Using the Pain Scale Effectively
Using the Pain Scale: How to Talk About Pain
WHO’s cancer pain ladder for adults
WHO guidelines on persisting pain in children
| В последние 10 лет возрастает внимание к проблеме боли у детей. Это обусловлено медико-технологическими достижениями, такими как новейшие хирургические вмешательства и методы лечения, а также появлением новых взглядов на боль у детей. В связи с этим в 1993 г. по просьбе тогдашнего государственного секретаря Министерства благосостояния, здравоохранения и культуры программной комиссией по исследованию боли голландской организации по научным исследованиям, являющейся подразделением центральной программной комиссии по хроническим болезням, была составлена записка о боли и оценке степени боли у детей. Эти материалы легли в основу данной статьи, содержащей краткий обзор имеющихся знаний о боли и оценке степени боли у детей, а также отражающей пробелы, которые, как сообщают голландские специалисты, имеются в научной литературе Для картирования международного опыта в области измерения боли было проведено исследование литературы с помощью баз данных Medline и Psychlit. .gif) Мы ограничиваемся обзорными статьями, упоминаемыми в Current contens, и учебниками о боли у детей, изданными за период с 1986 по 1994 г. Также были изучены публикации в голландских научных журналах, посвященные боли и ее измерению у детей Мы ограничиваемся обзорными статьями, упоминаемыми в Current contens, и учебниками о боли у детей, изданными за период с 1986 по 1994 г. Также были изучены публикации в голландских научных журналах, посвященные боли и ее измерению у детейБоль и оценка степени боли у детей Определение боли, видов боли и восприятия боли. Наиболее употребительным является определение Международной ассоциации по изучению боли (МАИБ): «Боль — неприятное сенсорное и эмоциональное переживание, сопровождающееся фактическим или возможным повреждением тканей, или состояние, словесное описание которого соответствует подобному повреждению» Рис 1. Яйцо Loesor; 4 круга отражают переменный Таблица 1. «Шкала комфорта», с помощью которой регистрируется интенсивность некоторых реакций организма Состояние готовности
Рис 2. Выражение лица новорожденного: реакция на укол пятки. Доступные невербальные способы оценки степени боли при отсутствии «золотого стандарта» исследуются путем сопоставления результатов с другими мерами (например, физиологическими) и с ожидаемыми изменениями в переживании боли в условиях анестезии и по истечении времени после вмешательства. Таким образом, может быть установлена их «конструктивная состоятельность», другими словами, измеряют ли они то, что должны измерять Рис 3. Шкала Oucher. Для оценки степени боли ребенок может выбрать одну из фотографий лиц детей с возрастающей экспрессией боли и без нее. На основе «Шкалы боли детской больницы Восточного Онтарио» (ШБДБВО) для недоношенных (менее 37 нед) и доношенных новорожденных (с 37 нед до 6 нед после рождения) разработана «Неонатальная детская шкала боли» (НДШБ) для регистрации острой боли (от иглы) и индуцированного болью «дистресса». Недостаток методов оценки боли у детей Из-за большого числа доступных методов может сложиться впечатление, что дальнейшая разработка способов оценки боли — дело бесперспективное. Это неправильно. Многим пациентам имеющиеся способы оценки боли не подходят, потому что они не могут адекватно выразить боль. Это касается в первую очередь боли у новорожденных (в особенности недоношенных) с врожденными отклонениями, у которых степень боли еще невозможно правильно оценить. Кроме того, их движения часто скованы из-за обилия современной медицинской аппаратуры, поддерживающей жизнь. Еще неизвестно, подходят ли для них имеющиеся поведенческие методы оценки боли или же должны быть разработаны новые инструменты. Это также верно в отношении боли у психически или физически инвалидизированного ребенка и для детей из различных этнических групп Заключение За последние 10 лет в Голландии усиливается внимание как к оценке степени боли у детей, так и к борьбе с ней. Обычно для голландского населения адаптируются способы оценки боли, разработанные в США и Великобритании. В настоящее время в различных учреждениях Голландии осуществляются интегрированные проекты, целью которых является разработка методов измерения степени боли у детей от 0 до 3 лет. Также начата разработка методов регистрации качества жизни ребенка с хронической болью. Применяя имеющиеся методы и разрабатывая новые, необходимо все время помнить о том что многие способы можно реализовать в рамках исследования, но они часто требуют слишком больших затрат времени и труда, и это делает невозможным их рутинное применение в клинической практике. При разработке новых методов необходимо в большей степени считаться с тем, что оценивать степень боли приходится в повседневной жизни: дома, в школе и в больнице Литература: 1. Ministerie van Welzijn. Volksgezondheid en Cultuur (WVC). Pijn en pijnmeting bij кinderen. Notitie van de Programmacommissie Pijnonderzoek. Rijswijk: Ministerie van WVC, 1993 | ||||||
| Наблюдение поведения; использовать у новорожденных и как дополнительный метод у детей до 12 лет | Физиологические реакции использовать у новорожденных | Методы самоотчета для детей
старше 3 лет |
Методы самоотчета для детей
старше 12 лет |
|||
| Поза | Рефлексы | Уровень: | Шкалы интенсивности | |||
| Специфический дистресс | Сердцебиение | катехоламинов | (ВАШ, болевой | Интервью | ||
| Выражение лица | Артериальное давление | гормонов роста | термометр, шкала | Опросные листы | ||
| Вокализация/характер плача | Дыхание | глюкагона | Outcher,словесные категории | Дневники | ||
| Показатель рО2 | инсулина | Проективные
тесты (цвет, форма, рисунок) |
Шкала
качества жизни |
|||
| (чрескожное измерение) | b-эндорфинов | |||||
| Почтовый индекс | ||||||
.
Прогнозирование риска развития головной боли напряжения у подростков
Аннотация
Головная боль напряжения является актуальной проблемой подростковой неврологии, что связано с широкой распространённостью заболевания, тенденцией этой патологии к хронизации и негативным влиянием на успеваемость, трудоспособность и качество жизни пациентов.
Цель работы – разработать способ прогнозирования возникновения головной боли напряжения у подростков.
Материалы и методы. Проведено исследование популяционного среза 2342 подростков обоего пола в возрасте 13–17 лет в школах Харькова. Для выявления головной боли использовали анкетирование. Была отобрана группа подростков с головной болью напряжения – 1430 человек (61,1 %). Группа контроля составила 246 здоровых подростков. Возможные факторы риска в формировании головной боли напряжения были разделены на 4 группы: генетические, медико-биологические, психосоциальные и социально-бытовые.
Математическое прогнозирование риска головной боли напряжения у подростков выполнено с использованием метода нормирования интенсивных показателей Е. Н. Шигана, основанного на вероятностном методе Байеса, и результат представлен в виде прогностических коэффициентов.
Результаты. Наиболее информативными факторами риска развития головной боли напряжения оказались заболевания, которые перенёс подросток после 1 года (нарушения сна, желудочно-кишечные заболевания), также большое значение имеет наличие вегетативных нарушений в семейном анамнезе, перенесённая черепно-мозговая травма, гиподинамия, плохая адаптация пациента в детском саду и школе, стрессы. Была разработана диагностическая шкала, позволяющая прогнозировать риск развития головной боли напряжения. Она включает в себя все 23 отобранных для прогнозирования фактора с их градацией и значениями интегрированного показателя риска, зависящего от силы влияния отдельного фактора.
Диапазон риска развития головной боли напряжения находился в пределах 25,27–81,43 значений прогностического коэффициента (слабая вероятность (25,27–43,99), средняя вероятность (43,99–62,71) и высокая вероятность (62,71–81,43)).
Выводы. Результаты исследования факторов риска возникновения головной боли напряжения, полученные при использовании оценочно-прогностической таблицы, показывают значимость наследственно-семейной предрасположенности к головной боли и вегетативной дисфункции, патологии новорождённого, заболеваний, перенесённых детьми после года, и психосоциальных нарушений у подростков.
Библиографические ссылки
(2015). Global Burden of Disease Study 2013 Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet, 22, 386(9995), 743–800. doi: 10.1016/S0140-6736(15)60692-4.
Straube, A., Heinen, F., Ebinger, F., & von Kries, R. (2013). Headache in school children: prevalence and risk factors. Dtsch Arztebl Int., 29 Suppl 110(48), 811–8. doi: 10.3238/arztebl.2013.0811.
Lehmann, S., Milde-Busch, A., Straube, A., von Kries, R., & Heinen, F. (2013). How specific are risk factors for headache in adolescents? Results from a cross-sectional study in Germany. Neuropediatrics, 44(1), 46–54. doi: 10.1055/s-0032-1333432.
(2013). Headache Classification Committee of International Headache Society: International Classification of Headache Disorders 3rd Edition (beta version). Cephalalgia, 33(9), 659–664. doi: 10.1177/0333102413485658.
Shigan, E. N. (1986) Metody prognozirovaniya i modelirovaniya v social´no-gigienicheskikh issledovaniyakh. [The methods of forecasting and modeling in socio-hygienic studies]. Moscow: Medicina. [in Russian].
Оценка интенсивности боли у пациентов после перенесенных артроскопических операций на коленном суставе
Научный журнал «МЕДИЦИНА. СОЦИОЛОГИЯ. ФИЛОСОФИЯ. Прикладные исследования»/ № 5 2020
Рябко Евгения Валентиновна, заведующий отделением физических методов лечения «Научно-производственного отдела восстановительного лечения, физиотерапии и курортологии», ФБУН «Екатеринбургский медицинский-научный центр профилактики и охраны здоровья рабочих промышленных предприятий» Роспотребнадзора
Рябчиков Илья Владимирович, д.м.н., профессор, ФГАОУ ВО «Казанский (Приволжский) федеральный университет»
Вараксин Анатолий Николаевич, д-р физ.-мат. наук, профессор, ФГБУН «Институт промышленной экологии» УрО РАН, главный научный сотрудник лаборатории математического моделирования в экологии и медицине Института промышленной экологии УрО РАН
Цель работы: оценить интенсивности боли у пациентов после перенесенных артроскопических операций на коленном суставе.
Материал и методы исследования: 75 пациентов, имевших травму коленного сустава, перенесших малоинвазивное оперативное артроскопическое вмешательство. Из них из них: 46,67% мужчин (35 мужчин и 40 женщин), средний возраст 37,84 лет (минимум 13 лет, максимум 71 год), средний индекс массы тела равен 26,17 у.е. (минимум 16,82; максимум 39,52). Основные клинические жалобы пациентов – это боли чаще при физической нагрузке, отек коленного сустава, гипотрофия мышц бедра, ограничение амплитуды движений в оперированном суставе, ощущение неустойчивости при ходьбе, страх снова повредить колено.
Методом простой рандомизации пациенты были разделены на 2 группы: опытную и контрольную, сопоставимые по полу, возрасту, срокам после оперативного вмешательства. Критерии включения: наличие лечебно-диагностической артроскопии в анамнезе по поводу травматического повреждения внутреннего мениска и передней крестообразной связки, наличие письменного добровольного информированного согласия пациента на участие в исследовании согласно действующему законодательству. Первая группа получала стандартный реабилитационный комплекс лечения.
Вторая группа пациентов получала дополнительно к первому комплексу реабилитационно-тренировочные занятия на стабилоплатформе (аппарат нейромышечной реабилитации и диагностики HUBER360 MD). Обеим группам до и после курса реабилитации проводили стабилометрическую диагностику.
Результаты: В обеих группах получено уменьшение показателя боли по ВАШ, но статистически значимое уменьшение показателя ВАШ наблюдается только во второй группе, дополнительно получавшей реабилитационно-тренировочные занятия на стабилоплатформе: уменьшение боли как при движении, так в покое. Выводы: Произведена оценка интенсивности боли у пациентов после перенесенных артроскопических операций на коленном суставе. Сравнение эффектов двух методов реабилитации показывает, что эффект реабилитации с использованием аппарата нейромышечной реабилитации и диагностики HUBER360 MD статистически значимо выше эффекта стандартной методики реабилитации. При использовании в программе реабилитации HUBER360 MD получен феномен более эффективного воздействия реабилитационно-тренировочных программ у мужчин по сравнению с женщинами.
Ключевые слова: боль, коленный сустав, артроскопическая операция, медицинская реабилитация, биомеханика
Введение
Современным методом лечения повреждений связочного аппарата коленного сустава являются малоинвазивные артроскопические лечебно-диагностические вмешательства [1, 2, 3].
Полноценное восстановление функции коленного сустава после перенесенных операций – важная задача современной реабилитации, требующая всестороннего изучения и разработки эффективных программ реабилитации [4, 5]. В связи с изложенным выше исследование интенсивности боли у данной категории пациентов в рамках совершенствования системы диагностических и реабилитационных мероприятий у пациентов после артроскопических операций является актуальной проблемой современной реабилитации [6, 7]. Проблема эффективной медицинской реабилитации пациентов после артроскопических операций, включающей диагностику нарушений баланса, опорной и опорно-динамической функции нижних конечностей остается до конца нерешённой.
Цель исследования: оценить интенсивность боли у пациентов после перенесенных артроскопических операций на коленном суставе.
Материалы и методы: исследование проводилось на базе ФБУН ЕМНЦ ПОЗРПП Роспотребнадзора с соблюдением правил Хельсинкской Декларации Всемирной ассоциации Хельсинской декларации Всемирной медицинской ассоциации «Рекомендации для врачей, занимающихся биомедицинскими исследованиями с участием людей» (в редакции 2013 г., изменения внесены на 64-ой Генеральной Ассамблее ВМА, Форталеза, Бразилия, октябрь 2013 г.)
Всего прошло реабилитацию 75 пациентов, имевших травму коленного сустава, перенесших малоинвазивное оперативное артроскопическое вмешательство. Из них из них: 46,67% мужчин (35 мужчин и 40 женщин), средний возраст 37,84 лет (минимум 13 лет, максимум 71 год), средний индекс массы тела равен 26,17 у.е. (минимум 16,82; максимум 39,52).
Критерии включения: наличие лечебно-диагностической артроскопии в анамнезе по поводу травматического повреждения внутреннего мениска и передней крестообразной связки, наличие письменного добровольного информированного согласия пациента на участие в исследовании согласно действующему законодательству. Критерии невключения: патология опорно-двигательного аппарата: другие травмы и переломы нижних конечностей в анамнезе, сколиозы, разная длина нижних конечностей, деформации стоп, последствия заболеваний и травм опорно-двигательного аппарата со стойкой ортопедической деформацией; поражения нервной системы: наличие в анамнезе дегенеративно-дистрофических изменений поясничного отдела позвоночника с корешковыми синдромами, полинейропатии нижних конечностей любого генеза, последствия перенесенных инсультов, параличей, парезов, черепно-мозговых травм, интоксикаций с поражением различных отделов центральной и периферической нервной системы; вестибулопатии, любые оториноларингологические заболевания, зрительного анализатора, заболевания внутреннего уха, слухового нерва; заболевания глаз: в прошлом и настоящем различные виды косоглазия, другие заболевания органов зрения; постоянный прием барбитуратов, нейролептиков, препаратов, влияющих на психоэмоциональную сферу; эпизоды обмороков, падений, нарушений равновесия в анамнезе, выраженные когнитивные расстройства.
Методом простой рандомизации пациенты были разделены на 2 группы: опытную и контрольную, сопоставимые по полу, возрасту, срокам после оперативного вмешательства. Первая группа получала стандартный реабилитационный комплекс лечения, включающий лечебный массаж, магнитотерапию на коленный сустав (аппарат магнитотерапевтический QS в исполнениях: EASY QS, ЗМТ QS с принадлежностями), электростимуляцию четырехглавой мышцы бедра (аппарат физиотерапевтический ntelect Advanced Chattanooga с принадлежностями), комплекс занятий лечебной физкультуры и пассивную роботизированную механотерапию (аппарат для двигательной продолжительной пассивной и активной мобилизации суставов ARTROMOT ACTIVE-К с принадлежностями).
Вторая группа пациентов получала дополнительно к первому комплексу реабилитационно-тренировочные занятия на стабилоплатформе (аппарат нейромышечной реабилитации и диагностики HUBER 360 MD. Обеим группам до и после курса реабилитации проводили стабилометрическую диагностику.
Основные клинические жалобы пациентов – это боли чаще при физической нагрузке, отек коленного сустава, гипотрофия мышц бедра, ограничение амплитуды движений в оперированном суставе, ощущение неустойчивости при ходьбе, страх снова повредить колено.
Оценка интенсивности боли производилась при помощи визуально-аналоговой шкалы (ВАШ) – Visual Analogue Scale (VAS) (Huskisson E. С., 1974) до и после реабилитации, а также в 2 позициях – в покое и при движении. Этот метод субъективной оценки боли заключается в том, что пациента просят отметить на неградуированной линии длиной 10 см точку, которая соответствует степени выраженности боли.
Левая граница линии соответствует определению «боли нет», правая – «худшая боль, какую можно себе представить». Устройство системы стабилоплатформы HUBER 360 MD реализует в себе как диагностическую, так и реабилитационную составляющую и позволяет использовать оборудование для диагностики и в дальнейшем применять его в создании реабилитационных тренировочных программ с последующей оценкой эффективности реабилитационных мероприятий. На основе данных полученных при стабилодиагностике составляется индивидуальный комплекс упражнений на основе биологической обратной связи. В процессе тренировок происходит улучшение количественных и качественных характеристик стабилометрического исследования.
Эффективность реабилитации оценивали по изменению величин показателей относительно значений показателей диагностики до начала реабилитационных мероприятий. Оценка результатов стабилометрического исследования осуществляется путем анализа показателей проведенных тестов на стабильность, оценку баланса на устойчивость на одной ноге, теста оценки ходьбы (Фукуда) и теста на пределы устойчивости. Основным стабилометрическим критерием эффективности проведенной реабилитации для пациентов после артроскопических операций является достоверная тенденция динамики регистрируемых значений тестируемых параметров после реабилитации к показателям зафиксированных до начала реабилитации.
Результаты и их обсуждение. Итоговые показатели оценки боли по шкале ВАШ представлены в таблице 1.
Таблица 2. Описательная статистика – разделение по группам Стьюдент для независимых наблюдений: группа 1 – стандартное лечение, группа 2 – с использованием HUBER360 MD) – представлена в таблице 2.
Распределения значений показателей (гистограммы): ВАШ при движении до реабилитации показаны на рис. 1. Показатели ВАШ при движении – эффект лечения представлены на рис. 3. Распределения значений показателей (гистограммы): ВАШ в покое до реабилитации показаны на рис. 4.
Рис. 1. Распределения значений показателей (гистограммы): ВАШ при движении до реабилитации
Распределения значений показателей (гистограммы): ВАШ при движении после реабилитации показаны на рис. 2.
Рис. 2. Распределения значений показателей (гистограммы): ВАШ при движении после реабилитации.
Рис. 3. Показатели ВАШ при движении – эффект лечения
Рис. 4. Распределения значений показателей (гистограммы): ВАШ в покое до реабилитации
Рис. 5. Распределения значений показателей (гистограммы): ВАШ в покое после реабилитации
Оценка эффекта реабилитации (определение величины эффекта лечения и его статистической значимости путем сравнения показателей до и после для каждого метода реабилитации отдельно) для показателя «ВАШ при движении» представлены в таблицах 3, 4, 5 – используется критерий Стьюдента для парных наблюдений.
Результат: есть статистически значимый эффект лечения стандартным методом для показателя «ВАШ при движении». После лечения среднее значение ВАШ уменьшилось с 4,071 до 2,200 (эффект реабилитации = 1,871 у.е.).
Результат: есть статистически значимый эффект лечения с HUBER360 MD для показателя «ВАШ при движении». После лечения среднее значение ВАШ уменьшилось с 3,625 до 0,950 (эффект = 2,675 у.е.). с HUBER360 MD эффект больше (2,675 у.е. против 1,871).
Оценка эффекта реабилитации (определение величины эффекта лечения и его статистической значимости путем сравнения показателей до и после для каждого метода реабилитации отдельно) для показателя «ВАШ в покое» представлены в таблицах 6, 7, 8 – используется критерий Стьюдента для парных наблюдений. Результат: есть статистически значимый эффект лечения стандартным методом для показателя «ВАШ в покое». После лечения среднее значение ВАШ уменьшилось с 3,386 до 1,857 (эффект = 1,529 у.е.).
Результат: есть статистически значимый эффект лечения с HUBER360 MD для показателя «ВАШ в покое». После лечения среднее значение ВАШ уменьшилось с 2,625 до 0,600 (эффект = 2,025 у.е.)
Результат: для показателя «ВАШ в покое» эффект с HUBER360 MD статистически значимо выше эффекта стандартной реабилитации только на уровне значимости 0,10 (р=0,0923)
Далее проведена оценка эффекта реабилитации в двух группах отдельно для мужчин и для женщин. Зависимость эффекта реабилитации от метода реабилитации и от пола представлена рис. 7 и 8.
На вертикальной оси отложен средний эффект реабилитации, на горизонтальной – пол (0-женщины, 1-мужчины), синей линией выделена стандартная методика реабилитации, черной – результат после HUBER 360 MD.
Рис. 5. Распределения значений показателей (гистограммы): ВАШ в покое после реабилитации
Рис. 6. Показатели ВАШ в покое – эффект лечения
Рис. 7. Зависимость эффекта реабилитации от метода реабилитации и от пола для показателя «ВАШ при движении»
Рис. 8. Зависимость эффекта реабилитации от метода реабилитации и от пола для показателя «ВАШ в покое»
Боль по ВАШ при движении до лечения равен 3,83 (минимум – ноль; максимум 8), в покое равен 2,98 у.е. (минимум – ноль; максимум 7). После курса реабилитации боль при движении уменьшилась до 1,53 у.е. (минимум – нуль; максимум 6), в покое после до 1,19 у.е. (минимум – нуль; максимум 6) (таблица 1).
В обеих группах получено уменьшение показателя боли по ВАШ, но статистически значимое уменьшение показателя ВАШ наблюдается только во второй группе, дополнительно получавшей реабилитационно-тренировочные занятия на стабилоплатформе: уменьшение боли как при движении, так в покое. Кроме того, обращает на себя внимание скорость достижения эффекта, а именно уменьшения боли, которая достигается быстрее во второй группе (таблица 2).
При проведении двухфакторного дисперсионного анализа для нахождения эффектов реабилитации, разделенных по методике реабилитации (это первый фактор) и по полу (это второй фактор) получен феномен более эффективного воздействия реабилитационно- тренировочных программ у мужчин по сравнению с женщинами. Возможно, это обусловлено физической подготовкой мужчин и большей мотивированностью на выполнение активных физических упражнений по сравнению с женщинами.
Выводы. Произведена оценка интенсивности боли у пациентов после перенесенных артроскопических операций на коленном суставе. Сравнение эффектов двух методов реабилитации показывает, что эффект реабилитации с использованием аппарата нейромышечной реабилитации и диагностики HUBER360 MD статистически значимо выше эффекта стандартной методики реабилитации. При использовании в программе реабилитации HUBER 360 MD получен феномен более эффективного воздействия реабилитационно-тренировочных программ у мужчин по сравнению с женщинами.
Оценка боли у новорожденных и детей раннего возраста
Боль — неприятное сенсорноэмоциональное переживание, связанное с истинным или потенциальным повреждением тканей [4].
Долгое время бытовало мнение, что дети устойчивы к болевому воздействию, а польза от проводимой лечебной процедуры значительно важнее, чем эмоциональная реакция ребенка [2]. До середины 1970х годов адекватную анальгезию в неонатальном периоде не проводили, исходя из убеждения о незрелости периферических болевых рецепторов, неполной миелинизации проводящих нервных волокон [3, 4]. Исследования последних лет показали, что болевые воздействия вызывают у детей патологические реакции. К их числу относятся такие нарушения, как энурез, потеря недавно сформировавшихся навыков, перевозбуждение, трудности засыпания, ночные кошмары, негативные эмоциональные реакции, избегающее поведение ребенка [1]. У новорожденных, которые подвергались обрезанию без анестезии, отмечалась более сильная реакция дистресса при обычной иммунизации в возрасте 4 и 6 месяцев по сравнению со сверстниками, не подвергшимися обрезанию или перенесшими обрезание под местной анестезией [10]. Работы Anand и соавт. показали, что у недоношенных новорожденных после хирургического вмешательства с минимальной анестезией возникали более сильные ответные реакции (возрастание концентрации катехоламинов, глюкагона, кортикостероидов), у них наблюдалось больше послеоперационных осложнений, выше оказывалась смертность по сравнению с группой новорожденных, получивших полную анестезию. McCrath и Unruh доказали, что незрелость новорожденных касается не их способности переживать боль, а исключительно неспособности сигнализировать о ней взрослым [6, 7].
Во время и после болевого воздействия отмечается повышение артериального давления (АД), изменение частоты (ЧСС) и ритма сердечных сокращений, частоты и механики дыхания, при длительном плаче ребенка возможно повышение внутричерепного давления [4].
Боль является одной из рано формирующихся психофизических функций, связанной с самыми «древними» структурами мозга. Все нейрофизиологические компоненты, необходимые для восприятия боли новорожденным ребенком, имеются у плода уже с середины гестационного периода. Незавершенная миелинизация вовсе не подразумевает отсутствие функции, а лишь немного замедляет время передачи импульсов, что компенсируется более короткими межнейронными расстояниями. Поэтому анестезиолог всегда должен помнить, что новорожденные, даже глубоко недоношенные, способны испытывать боль и реагируют на нее гипертензией, тахикардией, увеличением внутричерепного давления, выраженной нейроэндокринной реакцией. Более того, болевой порог у новорожденных значительно ниже, чем у старших детей или взрослых. Маленький ребенок не может локализовать боль, и ответная реакция имеет более диффузный характер, быстро истощая компенсаторные возможности. При этом в первую очередь нарушается нормальное функционирование системы дыхания и кровообращения [4].
Причин возникновения боли даже у новорожденных детей может быть множество, и свидетельствовать они могут о различных заболеваниях: родовой травме, гнойновоспалительных заболеваниях, некротическом энтероколите, остеомиелите, менингоэнцефалите, гидроцефалии, врожденных пороках развития. Кроме того, появление боли может быть связано с медицинскими манипуляциями и оперативными вмешательствами [8].
Субъективный характер боли делает ее трудноизмеримым понятием. Особенно это касается тех, кто не может выразить свою боль словами. Вот почему важную роль в распознавании и оценке болевого синдрома у новорожденного играет способность врача правильно интерпретировать клинические данные. С этой целью разработано несколько шкал оценки болевого синдрома, в основе которых лежат физиологические и поведенческие реакции новорожденного в ответ на болевое раздражение.
Первыми клиническими симптомами «болевого прорыва» у новорожденного ребенка являются нарушение сна, беспокойство и плач, затем повышается ЧСС и артериальное давление, уменьшается дыхательный объем и жизненная емкость легких, снижается сатурация (табл. 1).
Оценить выраженность болевых реакций можно с помощью оценочных шкал, использующихся в неонатальной анестезиологии.
Одной из наиболее популярных шкал оценки боли у новорожденных является шкала DAN (Douleur Aiguedu Nouveaune). Она используется для оценки острой и хронической боли у новорожденных по внешним признакам (табл. 2) [9].
Еще один метод, разработанный для использования у младенцев и детей до 7 лет, называется «Лицо — ноги — активность — плач — утешаемость» (FLACC: face, legs, activity, cry, consolabylitу). Этот метод оценивает боль по пяти поведенческим признакам, соответственно — выражению лица, движению ног, подвижности, плачу и утешаемости (табл. 3).
Шкала CRIES (табл. 4) разработана для использования у новорожденных с 32 недель гестационного возраста до 6 месяцев. Каждый из пяти показателей этой шкалы (плач, потребность в кислороде при сатурации ниже 95 %, повышение АД и ЧСС, выражение лица и сон) оценивается от 0 до 2 баллов.
Для оценки степени боли в послеоперационном периоде используют следующие методы:
1. Шкала CHEOPS (табл. 5) [10], которая включает в себя следующие категории: крик (1), гримаса (2), вербальный ответ (3), тонус мышц спины (4), активность в ответ на прикасание к хирургической ране (5) и движения ног (6). Каждый признак оценивается в баллах от 0 до
3. Первоначально шкала CHEOPS использовалась только у детей от 1 до 7 лет.
2. Объективная шкала боли (OPS) является достоверным и надежным методом оценки боли (табл. 6) [10].
В OPS оцениваются артериальное давление (1), крик (2), движение (3), возбуждение (4) и вербализация (5). Каждый параметр оценивается в баллах от 0 до 2. Особенность данного метода в том, что он включает оценку состояния сердечнососудистой системы как фактора боли в послеоперационном периоде. Однако одновременно могут присутствовать другие причины, которые влияют на гемодинамику у ребенка. Шкала OPS чаще используется для оценки боли у детей старше 1 года, у новорожденных — редко, что связано с неспособностью вербально выразить боль.
3. Более часто для оценки боли у новорожденных, которые находятся на искусственной вентиляции легких (ИВЛ), используют шкалу COMFORT (табл. 7).
В ней оцениваются девять показателей: тревожность, беспокойство и ажитация, дыхательные нарушения, плач, физическая подвижность, мышечный тонус, мимический тонус, среднее артериальное давление и ЧСС [12]. Каждый показатель оценивается по шкале от 1 до 5. Суммарное значение может варьировать от 9 до 45. Значения от 17 до 26 свидетельствуют об адекватной седации и обезболивании.
Оценка боли должна проводиться каждые 4–6 часов с документацией результатов. Для этого должен привлекаться обученный средний медицинский персонал.
Как же обстоят дела в диагностике боли у новорожденных с позиций доказательной медицины? С.А. Бочкаревой и А.Б. Пальчик (СанктПетербургская государственная педиатрическая медицинская академия) были обследованы две группы детей, в одной из которых болевое раздражение (внутримышечная инъекция) наносилось без предварительной анальгезии, а во второй место инъекции предварительно обрабатывали смесью местных анестетиков. Оценка болевого синдрома проводилась с помощью существующих оценочных шкал, применяемых в неонатологии. Исследование показало, что применение смеси местных анестетиков влияет на болевой ответ новорожденного: уменьшается продолжительность крика и флексорная реакция, наступает более быстрое успокоение, изменяются вегетососудистые показатели по данным пульсоксиметрии. Однако по большинству сравниваемых показателей (более 20) достоверных различий между группами не получено.
Это скорее всего свидетельствует о том, что большинство рассматриваемых общепринятых болевых параметров не являются специфичными для болевого стресса у новорожденного, а служат показателями реакции новорожденного на внешнее вмешательство. Следовательно, значительная часть физиологических поведенческих показателей, принятых как возможные маркеры боли у новорожденного, не являются специфичными, а следовательно, на изменении этих параметров не может строиться корректная диагностика боли с позиций доказательной медицины [5]. Данное исследование убеждает в необходимости дальнейшей разработки специфичных и достоверных методов определения болевого синдрома у новорожденных.
Bibliography1. Клипинина Н.В. Некоторые особенности восприятия и переживания боли детьми: взгляд психолога // Рус. мед. журн. — 2007. — 9.
2. Снисарь В.И. Боль у детей // Здоровье Украины. — 2007. — 1518.
3. Степанов А.А., Яцык Г.В., Намазова Л.С. Метод профилактики боли у детей раннего возраста при вакцинации // Педиатрич. фармакол. — 2007. — Т. 4, № 1. — С. 8285.
4. Шабалов Н.П., Иванов С.Л. Боль и обезболивание в неонатологии. — М., 2004. — 156 с.
5. Бочкарева С.А. Принципы доказательной медицины в диагностике боли у новорожденных детей / Пальчик А.Б., Бочкарева С.А. // Сборник материалов Междисциплинарного конгресса «Ребенок и лекарство». — СПб., 2006. — С. 3335.
6. Cowley Ch. Business briefing: longterm healthcare strategies. — 2003.
7. Wintgens М.A. et al. Posttraumatic stress symptoms and medical procedures in children // Can. J. Psychiatry. — 1997. — Vol. 42. — 611616.
8. Pain response in newborns to the order of injecting BCG and HepatitisB vaccines: a randomized trial // Indian J. Pediatr. — 2011. — 78(6). — 6937.
9. Carbajal R., Chauvet X. et al. Randomised trial of analgesic effects of sucrose glucose and pacifiers in term neonates // BMJ. — 1999. — 319. — 13931397.
10. McGrath P.J., Johnson G., Goodman J.T. CHEOPS: A Behavioral Scale for Rating Postoperative Pain in Children // Advances in Pain Researchand Therapy. — New York, NY: Raven Press, 1985. — Vol. 9. — 395402.
11. Hannallah R.S., Broadman L.M., Belman A.B. et al. Comparison of caudal and ilioinguinal/iliohypogastric nerve blocks for control of postorchiopexy pain in pediatric ambulatory surgery // Anesthesiology. — 1987. — 66(6). — 8324.
12. Van Dijk M., de Boer J.B., Koot H.M. et al. The reliability and validity of the COMFORT scale as a postoperative pain instrument in 0 to 3yearold infants // Pain. —2000. — 84 (2–3). — 3677.
Спастическая абдоминальная боль в клинической практике
Резюме. Ведущую роль в структуре абдоминального болевого синдрома играет спастическая боль при различной патологии желудочно-кишечного тракта, являющаяся одним из наиболее частых поводов для вызова скорой медицинской помощи и госпитализации пациентов в хирургические и терапевтические отделения. При отсутствии необходимости экстренного хирургического вмешательства основным способом купирования спастической абдоминальной боли (как органического, так и функционального генеза) является введение анальгетиков и спазмолитических средств. В настоящее время с этой целью все чаще применяют комбинированные препараты, обеспечивающие быстрое и эффективное обезболивание и устранение спазма гладких мышц. Примером такой комбинации является препарат Спазмалгон («Sopharma», Болгария), широко применяющийся во многих странах мира для лечения пациентов с абдоминальной болью спастического происхождения.
Актуальность проблемы
Острую абдоминальную боль рассматривают как ургентную ситуацию: хирургическая оценка этого распространенного в клинической практике симптома необходима для опровержения или подтверждения острой хирургической патологии. В США из 5–10 млн человек, ежегодно обращающихся за медицинской помощью с жалобами на острую боль в животе, у 40% диагностируют признаки острого живота. В то же время у каждого четвертого отмечают «функциональную», или «неспецифическую» абдоминальную боль (Бабак О.Я., 2006).
Следует отметить, что функциональные расстройства (ФР) желудочно-кишечного тракта (ЖКТ) чрезвычайно распространены в популяции: у 20–30% населения земного шара отмечают те или иные их проявления. При этом большинство ФР сопровождается гиперкинетическими реакциями гладких мышц и развитием спазма (Вейн А.М. (ред.), 2000; Белоусова Е.А., 2002). По данным Э.П. Яковенко и соавторов (2009), почти у половины всех больных гастроэнтерологического профиля (в том числе с органической патологией органов пищеварения) отмечают симптомы гипермоторной, и в первую очередь — спастической, дискинезии гладких мышц ЖКТ.
Нередко спазм гладких мышц при ФР ЖКТ является ведущим проявлением заболевания и главной причиной боли. Так, функциональная дисфагия, функциональная боль за грудиной, пилороспазм, кишечные дисфункции (синдром раздраженного кишечника, функциональная диарея, функциональный запор, функциональная абдоминальная боль) в большинстве случаев проявляются нарушением кишечного транзита и спастической болью в животе.
Нарушение эвакуации желчи и растяжение желчного пузыря (ЖП) при ФР его работы также сопровождается абдоминальной болью спастического характера. Среди факторов, способствующих развитию дисфункции ЖП, существует и ряд специфических причин (генетически обусловленная патология гладких мышц ЖП, дискоординация работы ЖП и пузырного или общего желчного протока, воспалительные изменения стенки ЖП и др.) (Белоусова Е.А., 2002).
По данным А.А. Ильченко (2004), 85–90% всех нарушений функции желчевыводящей системы возникает в результате развития органической билиарной патологии. При этом основными причинами боли являются спазм гладких мышц, перерастяжение стенки ЖП и желчных протоков в результате развития билиарной гипертензии, механическое раздражение стенки ЖП и протоковой системы билиарным сладжем или конкрементом.
Тесная анатомо-функциональная взаимосвязь билиарной системы и гастропанкреатодуоденальной зоны обусловливает смешанный характер боли при билиарной патологии. Так, дисфункция сфинктера печеночно-поджелудочной ампулы (сфинктера Одди) проявляется симптомами поражения билиарного тракта, поджелудочной железы или обоими симптомокомплексами. Нарушения работы сфинктерного аппарата также могут быть вызваны органическими нарушениями (стенозом сфинктера Одди или дистальной части общего желчного протока после холецистэктомии, опухолью большого дуоденального (Фатерова) соска).
Спастическая абдоминальная боль при органической патологии ЖКТ (пилороспазм при язвенной болезни, спазм шейки ЖП при желчнокаменной болезни и др.) имеет вторичный характер и усугубляет болевой синдром, вызванный основным деструктивным, воспалительным или неопластическим процессом (Белоусова Е.А., 2002).
Таким образом, в симптомокомплексе различных заболеваний ЖКТ спастическая висцеральная боль является ведущим клиническим проявлением органической и/или функциональной патологии.
Патофизиологические механизмы развития спастической висцеральной боли
В формировании абдоминальной боли участвуют висцеральные болевые рецепторы (ноцицепторы) и окончания чувствительных нервных волокон. Висцеральные ноцицепторы включают:
- высокопороговые механорецепторы (находятся в сердце, пищеводе, бронхах, желчевыводящих путях, тонкой и толстой кишке, мочеточнике, мочевом пузыре, матке), которые реагируют только на выраженный стимул (например чрезмерное сокращение и спазм полых органов), формируя острую боль;
- ноцицепторы «интенсивности» (находятся в сердце, пищеводе, толстой кишке, мочевом пузыре), возбуждающиеся в ответ на слабые механические стимулы;
- «немые», или «молчащие», ноцицепторы, которые активизируются только при повреждении клеток в результате воспаления, ишемии, некроза и обусловливают длительную диффузную боль (Баранская Е.К., 2009; Яковенко Э.П. и соавт., 2009).
Болевые рецепторы локализуются в мышечной и серозной оболочке стенок полых органов и капсуле паренхиматозных органов брюшной полости. Брыжейка и париетальная брюшина также обладают чувствительностью к болевым стимулам, тогда как висцеральная брюшина и большой сальник ее лишены (Яковенко Э.П. и соавт., 2009).
Истинно висцеральная боль возникает при возбуждении ноцицепторов в результате растяжения стенки полого органа (в комбинации с сокращением его гладких мышц) или капсулы паренхиматозного органа, натяжении брыжейки, сосудистых нарушениях. Таким образом, по механизму развития выделяют: спастическую (обусловленную спазмом гладких мышц ЖКТ), дистензионную (связанную с гипомоторной дискинезией гладких мышц и растяжением полого органа), перитонеальную (в основе которой лежит натяжение капсулы или висцерального листка брюшины) и сосудистую висцеральную боль (Садовникова И.И., 2009; Яковенко Э.П. и соавт., 2009).
Сообщение о ноцицептивном раздражении, воспринятое болевыми рецепторами, передается по различным каналам периферической нервной системы (в большинстве случаев проводниками висцеральной боли являются немиелинизированные С-волокна малого диаметра, обладающие низкой скоростью проведения импульса, при раздражении которых ощущается отсроченная тупая диффузная жгучая длительная боль) и затем обрабатывается в центральной нервной системе сложным нейрофизиологическим комплексом, включающим как специфические, так и неспецифические механизмы (Лиманский Ю.П., 1986; Ивашкин В.Т., Шульпекова Ю.О., 2002; Хвисюк А.Н., Федоренко Н.А., 2007; Баранская Е.К., 2009).
Регуляция моторной функции ЖКТМоторная функция ЖКТ контролируется многочисленными регулирующими влияниями со стороны центральной и периферической нервной системы, а также большой группой желудочно-кишечных пептидов и биоактивных молекул, действующих на уровне подслизистого (Мейснеровского) и межмышечного (Ауэрбаховского) нервных сплетений ЖКТ. Все компоненты этой системы поддерживают равновесие между стимулирующими и ингибирующими импульсами, что способствует поддержанию нормального тонуса и сократительной активности гладких мышц.
Вегетативная нервная система (внешняя иннервация двигательной функции ЖКТ) оказывает разнонаправленное сбалансированное действие: парасимпатическая стимуляция вызывает сокращение, симпатическая — расслабление гладких мышц. Таким образом, усиление парасимпатических или ослабление симпатических влияний способствует нарушению двигательной функции ЖКТ. Наличие интрамуральных нейронов в межмышечном сплетении (внутренняя иннервация) позволяет осуществлять автономный контроль двигательной активности ЖКТ (Белоусова Е.А., 2002; Садовникова И.И., 2009).
Немаловажную роль в развитии спастической абдоминальной боли играет нарушение баланса нейротрансмиттеров и регуляторных пептидов, контролирующих основные кишечные функции.
Серотонин, активирующий несколько подтипов рецепторов (наиболее изучены 5-НТ3 и 5-НТ4), играет существенную роль в регуляции моторики ЖКТ, вызывая диаметрально противоположные эффекты. Так, его связь с рецепторами 5-НТ3 способствует расслаблению, с 5-НТ4 — сокращению мышечного волокна.
Определенная роль в регуляции моторной функции кишечника отводится эндогенным опиатам: при связывании их с μ- и δ-опиоидными рецепторами миоцитов происходит стимуляция, а с κ- рецепторами — замедление моторики ЖКТ.
Субстанция Р (группа тахикининов), связываясь с рецепторами миоцитов, повышает моторную функцию последних за счет прямой активации и выделения ацетилхолина.
Соматостатин может как стимулировать, так и ингибировать интрамуральные нейроны, что приводит к аналогичным изменениям моторики.
Непосредственное влияние полипептида мотилина на рецепторы мышечных клеток повышает тонус нижнепищеводного сфинктера, ускоряет опорожнение желудка и усиливает сократительную активность толстого кишечника.
Вазоактивный интестинальный пептид (преимущественная область секреции — подслизистое и межмышечное сплетения в толстом кишечнике) способствует расслаблению мышц нижнепищеводного сфинктера, фундальной части желудка, толстой кишки (Белоусова Е.А., 2002; Ивашкин В.Т. (ред), 2003; Садовникова И.И., 2009).
Таким образом, патогенез гладкомышечного спазма, независимо от уровня поражения, обусловлен нарушением взаимодействий между больным органом-мишенью и регуляторными системами, поскольку любой висцеральный орган и весь ЖКТ в целом находятся под контролем многочисленных регулирующих влияний (Белоусова Е.А., 2002).
Механизмы сокращения и расслабления гладких мышцСостояние сократительного аппарата гладкомышечных клеток находится в прямой зависимости от ионного состава, где главенствующую роль играют ионы кальция (Са2+). Повышение их концентрации в цитоплазме миоцитов сопровождается сокращением, а снижение — релаксацией мышечного волокна.
Транспорт ионов Са2+ через клеточные мембраны осуществляется посредством специальных кальциевых, или медленных, каналов, которые представлены встроенными в мембрану клетки макромолекулярными белками, содержащими рецепторы, распознающие ионы Са2+. В регуляции транспорта ионов Са2+ участвует ряд нейрогенных медиаторов — ацетилхолин, катехоламины (норадреналин), серотонин, холецистокинин, мотилин и др. Так, связывание ацетилхолина с М-холинорецепторами способствует открытию натриевых каналов и вхождению ионов натрия в клетку, что сопровождается деполяризацией мембраны и открытием потенциалзависимых кальциевых каналов, через которые ионы Са2+ поступают в клетку. Взаимодействуя с цитоплазматическим кальцийсвязывающим белком кальмодулином, они активируют киназу легких цепей двигательного белка миозина. Последняя отщепляет фосфорный остаток от молекулы аденозинтрифосфорной кислоты, связанной с волокнами миозина. Благодаря этому миозин приобретает способность к взаимодействию с другим двигательным белком — актином. В результате между актином и миозином устанавливаются «молекулярные мостики», благодаря которым они «сдвигаются» по отношению друг к другу, что приводит к укорочению клетки.
Одним из условий, необходимых для сокращения мышечного волокна, является высокая активность фермента фосфодиэстеразы, которая участвует в расщеплении циклического аденозинмонофосфата (цАМФ) и циклического гуанозинмонофосфата (цГМФ), молекулы которых снижают содержание ионов Са2+ в цитоплазме и тем самым способствуют снижению сократительной активности клетки (Ивашкин В.Т. (ред), 2003; Яковенко Э.П. и соавт., 2009).
Основной механизм снижения тонуса и сократительной активности гладких мышц зависит от импульсов со стороны симпатической нервной системы и стимуляции норадреналином α1-адренегических рецепторов наружной мембраны миоцитов, что приводит к открытию быстрых ионных каналов, утечке положительно заряженных ионов из клетки и ее гиперполяризации. В условиях нарастания мембранного потенциала медленные кальциевые каналы прекращают функционировать, концентрация цитозольного Са2+ резко падает и наступает релаксация мышечного волокна.
Клиническая характеристика спастической абдоминальной боли
Классическое проявление висцеральной абдоминальной боли — колика (греч. kōlikē — кишечная болезнь) — характеризуется схваткообразной болью в животе высокой интенсивности, при которой периоды нарастания боли чередуются со «светлыми промежутками». Во время очередной «схватки» интенсивность боли быстро нарастает, затем наступает «плато» — период, когда выраженность боли максимальна по интенсивности (продолжается от 15 мин до нескольких часов), после чего боль постепенно стихает. Между приступами болевые ощущения полностью отсутствуют (Губергриц Н.Б., 2010).
Коликообразная боль, как правило, характеризуется высокой интенсивностью. На высоте боли пациенты беспокойны, часто меняют положение тела, мечутся либо принимают вынужденную позу, стараясь найти положение, которое уменьшит страдания.
При чрезмерной интенсивности импульса (например при прохождении камня) или анатомическом повреждении органа (например ущемлении кишки) возникает иррадиирующая боль в участках тела, имеющих общую корешковую иннервацию с пораженным органом (Бабак О.Я., 2006; Яковенко Э.П. и соавт., 2009).
Висцеральная боль характеризуется отсутствием четкой локализации — зоны восприятия ее, как правило, размыты. При повреждении пищевода, желудка, ЖП, билиарных протоков, поджелудочной железы боль локализуется в эпигастральной; при патологии тонкой, слепой кишки — мезогастральной; при поражении толстой кишки, органов малого таза — гипогастральной области. При этом боль ощущается ближе к срединной линии живота, поскольку внутренние органы имеют билатеральную иннервацию.
Абдоминальная боль редко отмечается как самостоятельный симптом и часто сопровождается тошнотой, рвотой, горечью во рту, изжогой, ощущением переполнения в желудке, метеоризмом, поносом, запором и другими симптомами. При острой висцеральной боли нередко отмечают сопутствующие вегетативные реакции (слабость, бледность, потливость, одышку и др.), лихорадку рефлекторного генеза, локальное напряжение мышц передней брюшной стенки (Баранская Е.К., 2005; Садовникова И.И., 2009).
Дифференциально-диагностические признаки различных типов висцеральной абдоминальной боли представлены в таблице.
Таблица. Характеристика висцеральной абдоминальной боли (Яковенко Э.П. и др., 2009)
| Показатель | Висцеральная боль, обусловленная | ||
|---|---|---|---|
| гипертонической (спастической) и гиперкинетической дискинезией полого органа | гипотонической дискинезией полого органа | растяжением капсулы, брыжейки органа | |
| Характер | Острая или тупая, приступообразная, жгучая | Давящая, тупая, монотонная | Острая, колющая, тянущая, сверлящая, режущая, кинжальная |
| Локализация | Разлитая, неопределенная, чаще по срединной линии | Разлитая, неопределенная, по срединной линии | Разлитая, но может соответствовать пораженному органу |
| Длительность | От минуты до месяцев | Длительная (от недели до месяцев) | Длительная (от недели до месяцев) |
| Ритмичность (связь с приемом пищи, временем суток, актом дефекации и др.) | Характерна (ритм может быть правильным и неправильным) | Неотчетлива | Усиливается при физических нагрузках, в определенных положениях тела, в ночные часы |
| Иррадиация | Возникает при интенсивном характере и соответствует пораженному органу | Отсутствует | Характерна и соответствует пораженному органу |
| Болезненность при пальпации | В месте локализации боли | В месте локализации боли | В месте локализации больного органа |
| Лекарственная терапия | Эффективны спазмолитические препараты | Эффективны прокинетики | Эффективны анальгетики (возможно сочетание с миотропными спазмолитиками) |
| Клинические примеры | Неосложненная язвенная болезнь, хронический обструктивный панкреатит, синдром раздраженного кишечника, желчная колика, функциональное нарушение сфинктера Одди, спастическая дискинезия толстой кишки, ассоциированная с любым заболеванием органов пищеварения (дивертикулярная болезнь, язвенный колит и др.), тенезмы при патологии прямой кишки | Гастродуоденостаз, гипомоторная дискинезия кишечника, функциональное расстройство ЖП гипомоторного типа | Острый панкреатит, хронический кальцифицирующий панкреатит, поражение лимфатических узлов, острый гепатит, опухоли органов брюшной полости |
Купирование спастической абдоминальной боли: Спазмалгон
Известно, что пациентам с неуточненным диагнозом и/или признаками острого живота введение анальгетиков противопоказано. Так, большинство авторов считают ошибочным решение купировать острую абдоминальную боль на догоспитальном этапе в связи с риском нивелирования картины острой хирургической патологии: обезболивание может затруднить диагностику и создать впечатление мнимого благополучия. Отличить в этот период острое хирургическое заболевание от нехирургических причин боли в животе трудно, поэтому при любых проявлениях острой абдоминальной боли от применения анальгетиков следует воздержаться (Бабак О.Я., 2006). В то же время клиническая практика свидетельствует, что в большинстве случаев приступ спастической абдоминальной боли сопровождается значительно выраженным болевым синдромом: страдания пациента в этот период настолько мучительны, что требуют обезболивания. Таким образом, при отсутствии необходимости экстренного оперативного вмешательства применение анальгетиков является необходимым компонентом лечения.
Спазмолитическая терапия не сопровождается непосредственным вмешательством в механизмы болевой чувствительности, не затрудняет диагностику острой хирургической патологии (Ивашкин В.Т. (ред.), 2003). Кроме того, применение спазмолитиков в данном случае является патофизиологически обоснованным. Так, с целью достижения релаксационного эффекта на периферическом уровне, снижения сократительной активности гладких мьшц, устранения спазма и восстановления нормального транзита показано применение релаксантов гладких мышц ЖКТ — холинолитиков и миотропных спазмолитиков, терапевтический эффект которых основан на вмешательстве в механизмы сокращения гладкомышечных клеток.
Антихолинергические средства обладают способностью блокировать мускариновые рецепторы клеточной мембраны, в результате чего снижается внутриклеточная концентрация ионов Са2+, что в конечном итоге приводит к расслаблению мышечного волокна. В настоящее время применение антихолинергических средств в купировании спастической боли считается абсолютно обоснованным и достаточно эффективным. В свою очередь, миотропные спазмолитики, являющиеся препаратами выбора для устранения спазма любого генеза и купирования боли (особенно при ФР), способствуют расслаблению гладких мышц, что сопровождается снижением тонуса полого органа и внутрипросветного давления, восстановлением пассажа содержимого и улучшением кровоснабжения стенки органа (Белоусова Е.А., 2002).
В настоящее время для купирования боли спастического характера все чаще применяют комбинированные препараты, активные компоненты которых обладают взаимодополняющими механизмами действия и способствуют быстрому и эффективному устранению и боли, и спазма.
Оптимальным примером такой комбинации является препарат Спазмалгон («Sopharma», Болгария). Согласно унифицированной анатомо-терапевтической и химической классификации лекарственных средств — классификационной системе АТС (Anatomical Therapeutic Chemical classification system), препарат относят к спазмолитическим средствам в комбинации с анальгетиками (код препарата — А03D А02) (Компендиум 2010 — лекарственные препараты, 2010). В его составе — три действующих вещества (ненаркотический анальгетик метамизол натрий, миотропный спазмолитик питофенона гидрохлорид и антихолинергическое средство фенпивериния бромид), оказывающих выраженный анальгезирующий и спазмолитический эффект.
Представитель нестероидных противовоспалительных препаратов (НПВП) группы производных пиразолона — метамизол натрий, входящий в состав препарата Спазмалгон, с 1922 г. известен клиницистам как лекарственное средство, обладающее мощным анальгезирующим и жаропонижающим эффектом в сочетании с менее выраженной противовоспалительной и спазмолитической активностью (Fendrich Z., 2000). Отметим, что НПВП нашли широкое применение во всем мире и включены в алгоритмы обезболивающей терапии при болевом синдроме различной степени выраженности (Мазуренко О., 2006). За долгую историю применения фармакологические свойства метамизола натрия подробно изучены, а терапевтическая эффективность подтверждена многими исследованиями. В настоящее время препарат по-прежнему очень популярен во многих странах в качестве монокомпонента терапии и в комбинации со спазмолитиками.
По сути метамизол натрий является пролекарством — предшественником лекарственного средства, который превращается в организме в активную форму. Хорошо всасываясь в пищеварительном тракте, он гидролизируется с образованием активного метаболита, 50–60% которого связывается с белками плазмы крови.
Механизм противовоспалительного, анальгезирующего и жаропонижающего действия метамизола натрия обусловлен ингибированием фермента циклооксигеназы и блокированием синтеза простагландинов из арахидоновой кислоты (напомним, что являясь медиаторами воспалительного процесса, эти вещества повышают чувствительность ноцицепторов и таким образом участвуют в механизме восприятия боли). Помимо этого, под влиянием метамизола натрия происходит нарушение проведения болевых экстра- и проприоцептивных импульсов, повышение порога возбудимости таламических центров болевой чувствительности, повышение теплоотдачи (Денисенко П.П. и соавт., 2004; Компендиум 2010 — лекарственные препараты, 2010).
Благодаря вышеуказанным свойствам метамизол натрий незаменим при сильной боли, обусловленной спазмом гладких мышц. Его высокая анальгезирующая активность подтверждена в ряде контролируемых исследований (Бутров А.В. и соавт., 2009), а по наблюдениям некоторых авторов, при применении в равных дозах анальгезирующий эффект препарата сравним и в отдельных случаях даже превосходит таковой некоторых опиоидных анальгетиков (Schmieder G. et al., 1993; Fendrich Z., 2000; Haen Е., 2007). Обзор литературы, проведенный F. Arellano, J.A. Sacristán (1990), свидетельствует о целесообразности парентерального введения метамизола натрия в качестве препарата первого выбора при колике в случаях необходимости применения ненаркотических анальгетиков. По наблюдениям Z. Fendrich (2000), побочные эффекты терапии метамизолом натрием выражены нечетко, а лекарственное взаимодействие — минимально, что делает возможным его применение для купирования болевого синдрома различного происхождения.
Второй активный компонент препарата Спазмалгон — питофенона гидрохлорид — обладает прямым миотропным (по отношению к гладким мышцам) спазмолитическим (папавериноподобным) действием. По механизму релаксирующего действия питофенона гидрохлорид является ингибитором фосфодиэстеразы (последняя, как отмечено выше, разрушает внутриклеточный цАМФ и цГМФ, участвующие в механизмах регуляции гомеостаза Са2+ в миоцитах). Это способствует накоплению в миоците цАМФ и цГМФ, что снижает концентрацию Са2+ и приводит к расслаблению гладких мышц. Выраженный и продолжительный антиспастический эффект питофенона гидрохлорида подтвержден в исследованиях in vitro и in vivo, проведенных S. Bal-Tembe и соавторами (1997).
Фенпивериния бромид, оказывая М-холиноблокирующее действие, способствует дополнительному расслаблению гладких мышц ЖКТ.
Таким образом, выраженная спазмолитическая и анальгезирующая активность препарата Спазмалгон позволяют применять его с целью симптоматического лечения приступов желчной и кишечной колики, спастической дискинезии желчевыводящих путей и другой патологии, сопровождающейся абдоминальной болью спастического характера.
Форма выпуска препарата (раствор для внутримышечного введения в ампулах по 2 и 5 мл) удобна при необходимости быстрого купирования боли как в домашних условиях, так и в стационаре. При острых эпизодах боли препарат применяют однократно (при необходимости дозу повторяют через 6–8 ч) или короткими курсами — 2–3 дня. После достижения быстрого терапевтического эффекта можно продолжить лечение пероральными обезболивающими и спазмолитическими средствами.
Литература
- Бабак О.Я. (2006) Острая боль в животе: где хирург, где терапевт? Острые и неотложные состояния в практике врача, 2: 8–13.
- Баранская Е.К. (2005) Боль в животе: клинический подход к больному и алгоритм лечения. Место спазмолитической терапии в лечении абдоминальной боли. Гастроэнтерология, 14(109): 49–57.
- Баранская Е.К. (2009) Терапия абдоминальной боли. Справочник поликлинического врача, 1: 40–43.
- Белоусова Е.А. (2002) Спазмолитики в гастроэнтерологии: сравнительная характеристика и показания к применению. Фарматека, 9: 40–46.
- Бутров А.В., Кондрашенко Е.Н., Ибарра-Пенья Н.А. (2009) Современные НПВП в практике врача анестезиолога-реаниматолога. РМЖ (Русский медицинский журнал), 17(25): 1631–1635.
- Вейн А.М. (ред.) (2000) Вегетативные расстройства: клиника, лечение, диагностика. Медицинское информационное агентство, Москва, 752 с.
- Губергриц Н.Б. (2010) Желчнокаменная болезнь: от классики к современности. Гастроэнтерология, 1: 83–95.
- Денисенко П.П., Бурбелло А.Т., Шабров А.В. (2004) Современные лекарственные средства: клинико-фармакологический справочник практического врача. Нева, Санкт-Петербург, 896 с.
- Ивашкин В.Т. (ред.) (2003) Рациональная фармакотерапия заболеваний органов пищеварения: руководство для практикующих врачей. Литтерра, Москва, 1046 с.
- Ивашкин В.Т., Шульпекова Ю.О. (2002) Нервные механизмы болевой чувствительности. Российский журнал гастроэнтерологии, гепатологии, колопроктологии, 4(12): 16–20.
- Ильченко А.А. (2004) Билиарная патология и абдоминальная боль. Врач, 2: 51–53.
- Компендиум 2010 — лекарственные препараты (2010) В.Н. Коваленко, А.П. Викторов (ред.) МОРИОН, Киев, с. С-122.
- Лиманский Ю.П. (1986) Физиология боли. Здоров’я, Киев, 96 с.
- Мазуренко О. (2006) Если боль застала врасплох… Препарат выбирает посетитель аптеки. Еженедельник Аптека, 19(540) .
- Садовникова И.И. (2009) Абдоминальный болевой синдром: диагностика, лечение. РМЖ (Русский медицинский журнал), 2: 72–75.
- Хвисюк А.Н., Федоренко Н.А. (2007) Нейрофизиологические механизмы боли. Медицина неотложных состояний, 6(13): 7–11.
- Яковенко Э.П., Яковенко А.В., Агафонова Н.А. и др. (2009) Абдоминальные боли: механизмы формирования, рациональный подход к выбору терапии. РМЖ (Русский медицинский журнал), 11(2): 48–53.
- Arellano F., Sacristán J.A. (1990) Metamizole: reassessment of its therapeutic role. Eur. J. Clin. Pharmacol., 38(6): 617–619.
- Bal-Tembe S., Bhedi D.N., Mishra A.K. et al. (1997) HL 752: a potent and long-acting antispasmodic agent. Bioorg. Med. Chem., 5(7): 1381–1387.
- Fendrich Z. (2000) Metamizol — a new effective analgesic with a long history. Overview of its pharmacology and clinical use. Cas. Lek. Cesk., 139(14): 440–444.
- Haen E. (2007) Clinical pharmacology of analgesics. Orthopade, 36(1): 17–22.
- Schmieder G., Stankov G., Zerle G. et al. (1993) Observer-blind study with metamizole versus tramadol and butylscopolamine in acute biliary colic pain. Arzneimittelforschung, 43(11): 1216–1221.
Шкала боли: оцениваем боль в цифрах
Боль – это всегда неприятное ощущение. Но ее интенсивность может быть разной: она зависит от того, какая болезнь развилась, и какой болевой порог имеет человек.
Чтобы врач мог понять, как именно болит – нестерпимо или более-менее умеренно– придуманы так называемые шкалы боли. С их помощью вы можете не только описать свою боль на данный момент, но и сказать, что изменилось с назначением лечения.
Визуальная аналоговая шкала
Это та шкала, которой чаще всего пользуются анестезиологи и онкологи. Она представляет собой возможность оценить интенсивность боли – без всяких подсказок.
Визуальная аналоговая шкала представляет собой линию длиной 10 см, нарисованную на чистом листе бумаги – без клеточек. 0 см – это «боли нет», самая правая точка (10 см) – «боль самая нестерпимая, которая вот-вот приведет к гибели». Линия может быть как горизонтальной, так и вертикальной.
Пациент должен поставить точку там, где, как он чувствует, располагается его боль. Врач берет линейку и смотрит, на какой отметке находится точка пациента:
- 0-1 см – боль крайне слабая;
- от 2 до 4 см – слабая;
- от 4 до 6 см – умеренная;
- от 6 до 8 см – очень сильная;
- 8-10 баллов – нестерпимая.
При оценке боли врач не только смотрит на эту точку, а и на все поведение человека. Если человека можно отвлечь вопросами, если он спокойно прошел по кабинету до выхода, возможно, он завышает степень боли. Поэтому ему можно предложить повторно оценить свою боль – по той же шкале. А если это женщина, то попросить сравнить с болью при родах (она оценивается в 8 баллов для каждой женщины). Если она говорит: «Вы что, рожать было вдвое больнее», то стоит оценить ее боль в 4-5 баллов.
Модифицированная визуальная аналоговая шкала
Суть оценки боли – такая же, как и в предыдущем случае. Единственное отличие этой шкалы – в цветовой маркировке, на фоне которой и нарисована линия. Цвет идет градиентом: от зеленого, который начинается от 0, к 4 см сменяется желтым, а к 8 см – красным.
Вербальная ранговая шкала
Она очень напоминает визуальную аналоговую шкалу: так же линия длиной в 10 см, которую можно прочертить при пациенте самостоятельно. Но отличие есть: каждые 2 см следует надпись:
- на 0 см – боли нет;
- на 2 см – слабая боль;
- на отметке 4 см – умеренная боль;
- на 6 см – сильная;
- на 8 см – очень сильная;
- в конечной точке – невыносимая боль.
В этом случае человеку уже легче сориентироваться, и он ставит точку, исходя из того, с каким эпитетом у него больше всего ассоциируется собственное состояние.
Положительные стороны этого метода оценки боли в том, что с ее помощью можно оценивать и острый, и хронический болевой синдром. Кроме того, шкалу можно применять у детей, начиная от младших школьников, а также людей с начальными степенями деменции.
Шкала боли «в лицах» (лицевая)
Эта шкала может применяться для определения интенсивности боли у людей в глубокой деменции. Она состоит из 7 рисунков лиц с эмоциями, каждая из которых схематично передает силу болевого синдрома. Расположены они по нарастанию боли.
Почему именно рисунки, да еще и такие примитивные? Потому, что с таких рисунков эмоцию легче считать и труднее неверно истолковать, чем с произведения искусства или фотографии.
Перед тем, как человек укажет лицо, отображающее соответствующую степень боли, ему нужно объяснить картинку. Врач говорит: «Смотри, у первого человека ничего не болит, дальше показаны люди, которые чувствуют боль – с каждым разом все сильнее. Самый правый человек ужасно мучается от боли. Покажи мне, какую боль чувствуешь ты». После этого человек указывает или обводит нужное лицо.
Модифицированная лицевая шкала
Она состоит из 6 лиц, каждое из которых изображает эмоцию, соответствующую описанию боли по вербальной ранговой шкале. Она также используется для оценки интенсивности болевого синдрома при деменции и тоже проводится после короткого вступительного слова.
Шкала, которую используют для лежачих и потерявших речь больных
Реаниматологи применяют шкалу CPOT, которая позволяет им, не разговаривая с пациентом, оценить степень его боли. Они учитывают 4 параметра:
- Напряжение мышц рук.
- Выражение лица.
- Попытки говорить или сопротивление дыхательному аппарату.
- Двигательные реакции.
Каждый параметр оценивается от 0 до 2 баллов, после чего баллы суммируются.
Трактовка такая:
0-2 балла – боли нет;
3-4 балла – слабая боль;
5-6 баллов – умеренная боль;
7-8 баллов – боль сильная;
9-10 – очень сильная боль.
Наиболее полная оценка боли – опросник Мак-Гилла
Благодаря этому опроснику (анкете) можно оценить три основные системы формирования и проведения боли:- нервные волокна, которые проводят непосредственно болевые ощущения;
- структуры, которые есть и в спинном, и головном мозге: ретикулярная формация и лимбическая система;
- отделы в коре головного мозга, которые занимаются оценкой и уже конечной интерпретацией боли.
Поэтому анкета условно разделена на 4 группы:
- для определения сенсорных характеристик боли;
- для оценки того, какие боль затрагивает эмоциональные компоненты;
- для оценки того, как боль оценивается головным мозгом;
- группа слов, которые направлены на оценку сразу всех критериев.
Физически опросник выглядит как 20 граф, в каждой из которых расположено от 1 до 5 эпитетов, расположенных по порядку – в соответствии с интенсивностью боли. Человеку нужно обвести столько из них, сколько поможет ему точно описать свои ощущения.
Оценка болевого индекса производится по тому, сколько слов было использовано для описания боли по каждому из 4 параметров. Также важно, какие порядковые номера применялись для оценки в каждом аспекте. И, наконец, суммируются порядковые номера выбранных эпитетов, вычисляется их среднеарифметическая величина.
Для чего нужны шкалы боли
Шкалами боли пользуются не все врачи. Их применяют, в основном, анестезиологи-реаниматологи, терапевты и онкологи. Иногда с ними сталкиваются врачи и других специальностей, когда речь идет о хронических больных.
В зависимости от того, как оценена боль, будет назначаться обезболивающее средство:
- При слабой боли – это ненаркотическое обезболивающее: «Ибупрофен», «Анальгин», «Диклофенак», «Парацетамол».
- При умеренной – 2 ненаркотических анальгетика, имеющих несколько разные точки приложения, или комбинация из слабого наркотического средства и ненаркотического анальгетика.
- Сильная боль требует назначения сильного наркотического и ненаркотического анальгетиков. Часто приходится прибегать и к дополнительным методам: блокадам нервных путей, алкоголизации (введении этанола) в нервные окончания, которые являются причиной хронической сильной боли.
Любой из указанных препаратов имеет массу побочных эффектов. Поэтому в интересах пациента – максимально объективно оценивать собственную боль, а при ее изменениях – сообщать об этом врачу. Вот уже если врач никак не реагирует – то его нужно менять на другого специалиста.
Столы с С-дугой для обезболивания | Хирургические столы Inc
Surgical Tables специализируется на столах для обезболивания. Разработанный для размещения c-дуги, конечный пользователь имеет наилучший доступ для получения качественных изображений.
Серии Streamline, EconoMAX и MAX идеально подходят для обезболивания. Каждый стол в стиле трамплина поставляется с парой ремней для пациента, вырезом для лица (который можно заполнить) и ручным управлением.
Мы производим столы в США с учетом их прочности.Процедуры обезболивания часто требуют точного позиционирования. Наши столы с C-образным кронштейном бесшумны и не подвержены вибрации, поэтому конечный пользователь не беспокоится. Кроме того, рентгенопрозрачная столешница не имеет поперечин, что обеспечивает полную визуализацию под флюоресцентным датчиком.
Таблицы болиSTI предлагают не только качество, но и отличную цену.
Если вы посмотрите на функции, которые мы включили в наши таблицы управления болью, вы поймете, почему их используют практики по всей стране:
- Консольная конструкция в стиле трамплина для легкого доступа к С-образной дуге
- Максимальный вес пациента 500 фунтов
- Удобная высококачественная набивка 2 дюйма для большего комфорта пациента
- Вырез для лица для процедур на животе
- Легкий и маневренный стол
- Ширина стола 24 ″ в большинстве случаев устраняет необходимость в подлокотнике.
- Повышенная безопасность и стабильность благодаря простым в использовании колесным замкам
- Превосходная маневренность означает простой и безопасный перенос пациента от стола к столу
- Несколько моделей на выбор
STI предлагает множество различных моделей на любой бюджет, при этом удовлетворяя потребности пациентов.Наши столы с С-образной дугой идеально подходят как для больниц, так и для отделений неотложной медицинской помощи и кабинетов врачей. Они используются для малоинвазивных процедур на позвоночнике, таких как радиочастотная абляция, блокада нервов, кифопластика, вертебропластика, стимуляторы спинного мозга, инъекции стероидов и многое другое.
STI предлагает как экономически эффективную универсальность, так и технологию в каждой из наших таблиц обезболивания. Вы легко сможете удовлетворить потребности своих пациентов, не выходя при этом из бюджета. Предоставьте своему помещению для обезболивания гибкость и эффективность, которые дает Surgical Tables Inc.таблица обезболивания.
Чтобы получить ценовое предложение или дополнительную информацию, позвоните 888-737-5044 или напишите по адресу [email protected] сегодня.
столов для ИППП — визуализация, обезболивание, УЗИ и др.
Surgical Tables — ведущий производитель качественных хирургических столов, который занимается производством столов с 2004 года. Их основное внимание уделяется основным рынкам здравоохранения со значительным потенциалом роста, обусловленным спросом на более качественные и экономически эффективные методы лечения, которые предлагают пациентам улучшенные качество ухода.Каждая из их продуктовых линеек обладает следующими характеристиками:
Универсальность —
STI предлагает гибкое решение медицинских и бюджетных проблем для любой хирургической среды.
Технологически продвинутый —
Разработан для поддержки последних достижений в хирургических процедурах и методах визуализации, устанавливая стандарты операционной эффективности.
Рентабельность —
Привлекательное соотношение цены и производительности освобождает место при планировании инвестиций, а надежные технические характеристики позволяют снизить последующие расходы.
Безопасность —
Хирургические столы предлагают полностью автоматизированную настройку всех функций стола для безопасного позиционирования пациента без травм без ущерба для здоровья и безопасности медицинского персонала.
Соответствие —
Surgical Tables Incorporated (STI) производит медицинские устройства, соответствующие Кодексу Центра устройств и радиологического здоровья (CDRH) Федерального постановления 21, подраздел J, часть 1020, раздел 30 (CFR21, подраздел J, часть 1020.30), стандарт производительности для продуктов, излучающих ионизирующее излучение. Кроме того, продукция STI производится в соответствии с действующей надлежащей производственной практикой (CGMP) Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA).
Качество —
Универсальность, технология, стоимость, безопасность и соответствие требованиям. По всем этим и другим причинам компания Surgical Tables Inc. быстро становится лидером в области качества хирургических столов.
Давнее партнерство —
Integrity Medical Systems работает с ИППП на протяжении многих лет.У них прочные отношения, и они сделают все, что в их силах, чтобы вы остались довольны покупкой стола.
Все особенности конкурса за небольшую часть стоимости
Столы для рентгеновских снимков серии компании STI можно приобрести с 5-позиционными регуляторами, включая высоту, поперечный наклон, тренделенбург, продольное и поперечное перемещение. Контроль точности означает, что ваши пациенты находятся именно там, где они вам нужны, во время деликатных процедур, когда миллиметры могут иметь значение.
ТаблицыSTI созданы, чтобы выдерживать повседневное использование, которое приходит с жизнью в интенсивной практике визуализации или радиологии. Вот почему они встроили множество функций, чтобы сделать свой стол самым полезным и универсальным на рынке:
- Верх из углеродного волокна, ширина 24 ″ — устраняет необходимость в подлокотниках.
- Длина стола 84 ″ подойдет даже для самых высоких пациентов
- Стол в стиле трамплина для легкого доступа с помощью С-дуги для оборудования и персонала для визуализации
- Легкая конструкция позволяет персоналу легко перемещать стол
Визуализация и радиология имеют очень специфический набор потребностей, когда дело касается хирургических столов и Surgical Tables, Inc., у вас будет возможность удовлетворить потребности большего числа пациентов с помощью стола для визуализации, который будет обслуживать каждого пациента каждый раз.
Придайте вашей процедурной комнате гибкость, которую обеспечивает стол для визуализации Surgical Tables, Inc. от Integrity Medical Systems, Inc.
Что такое стол для декомпрессии позвоночника?
Как и при любом лечении, результаты декомпрессии позвоночника будут зависеть от пациента, врача и используемого протокола.Пациенты не испытывают сильного облегчения после первого сеанса лечения. Скорее, после нескольких сеансов декомпрессии позвоночника облегчение должно быть очевидным. В некоторых случаях пациентам может потребоваться завершить весь протокол лечения, прежде чем они почувствуют полное облегчение своих симптомов.
Исследование стола декомпрессии позвоночникаИсследования в области спинномозговой декомпрессионной терапии продолжаются, и ряд исследований показывает пользу для пациентов, испытывающих хроническую или острую боль.Например, исследование Региональной больницы и Центра медицинских наук Рио-Гранде и Техасского университета показало:
Специфическое и важное клиническое действие декомпрессионной терапии, делающее ее эффективной. Измерение интрадискального давления выполнялось путем подсоединения канюли, вставленной в дисковое пространство L4-L5 пациента, к датчику давления. Была введена декомпрессия позвоночника, и изменения давления регистрировались в состоянии покоя и снова при приложении контролируемого напряжения с помощью оборудования.Результаты этого исследования показывают, что можно снизить давление в пульпозном ядре грыжи поясничных дисков до уровня ниже -100 мм рт.ст., когда напряжение дистракции применяется в соответствии с протоколом, описанным для декомпрессионной терапии. Самое низкое внутридисковое давление, измеренное во время прогрессирующего вытяжения, составило 40 мм рт. Ст. По сравнению с 75 мм рт. Ст. В положении лежа на спине. (2) Таким образом, стандартная декомпрессионная терапия отличается от стандартной тракции тем, что создает уникальные клинические обстоятельства длительного отрицательного внутридискового давления.
Снижение давления в межпозвоночной грыже — объективный способ определить, работает ли декомпрессия, поскольку более низкое давление по определению означает меньшую компрессию. Когда давление внутри поясничного диска ниже, пациенты будут меньше испытывать боли в пояснице.
В исследовании результатов 1998 года спинальная декомпрессионная терапия была эффективной в 71% случаев, при этом пациенты сообщали об уменьшении боли до 0 или 1 по шкале от 0 до 5.
Другое исследование боли в пояснице показало, что пациенты с хронической болью избавляются от спинальной декомпрессионной терапии всего за восемь недель.Важно отметить, что 80% пациентов в этом конкретном исследовании испытывали симптомы более 6 месяцев и пробовали как минимум два других вмешательства для облегчения боли, прежде чем обратиться к столу для декомпрессии позвоночника.
Несмотря на противоречивые сообщения об эффективности спинномозговой декомпрессионной терапии, очевидно, что существует сегмент населения, для которого декомпрессионный стол может облегчить хроническую боль там, где никакие другие вмешательства не принесли успеха.
Чтобы узнать больше о том, как таблицы декомпрессии позвоночника помогают пациентам получить нужные им результаты, вы можете скачать наши тематические исследования здесь:
Альтернативные столы для декомпрессии позвоночникаКак и любая другая проблема здравоохранения, декомпрессионная терапия позвоночника с декомпрессионным столом — не единственный вариант лечения грыжи межпозвоночного диска, фасеточного синдрома или других проблем с болью в спине.Действительно, многие пациенты, которым помогает спинальная декомпрессионная терапия, делают это только после того, как другие варианты не принесли им облегчения.
Ниже приведены некоторые альтернативы декомпрессионной терапии позвоночника с использованием декомпрессионного стола:
- Инвазивная хирургия
- Мануальные хиропрактические манипуляции
- Физиотерапия
- Иглоукалывание
- Йога
- Фармацевтическое вмешательство
- Инъекции стероидов
В зависимости от пациента и его состояния эти альтернативы могут оказаться неэффективными.Только зная полный анамнез пациента и проведя тщательную оценку его текущего состояния, можно рекомендовать подход к лечению.
Некоторые медицинские работники, практикующие декомпрессионную терапию позвоночника, также назначают другие сопутствующие методы лечения, такие как тепловая или холодная терапия, упражнения, растяжка, планы питания и многое другое, что может помочь пациенту достичь лучших результатов.
Результаты любой декомпрессионной терапии позвоночника будут различаться в зависимости от пациента и практикующего врача.Кроме того, затраты, связанные с каждым протоколом, зависят от медицинского страхования и объема лечения.
Чтобы узнать больше о том, как стол для декомпрессии позвоночника может помочь вашим пациентам избавиться от боли, запланируйте звонок с командой HillDT. Или посетите страницу продукта, чтобы узнать больше:
Аккумулятор под покраску | Научные отчеты
Линден, Д. и Редди, Т. Б. (ред.) Справочник по батареям, гл. 35, 3 rd edn (McGraw-Hill, 2002).
Spare, B. L. Проектирование и изготовление непрямоугольных батарей. Публикация патента США № US 2012/0015236 A1.
Нисидэ, Х. и Ояйзу, К. К гибким батареям. Science 319, 737–738 (2008).
CAS Статья Google Scholar
Hu, L., Wu, H., La Mantia, F., Yang, Y. & Cui, Y. Тонкие, гибкие вторичные литий-ионные бумажные батареи. АСУ Нано 4, 5843–5848 (2010).
CAS Статья Google Scholar
Hu, L. et al. Эластичный, пористый и проводящий энергетический текстиль. Nano Lett. 2010. Т. 10. С. 708–714.
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Лю Ю., Горгуца С., Сантато С. и Скоробогатий М. Гибкая литиевая батарея на основе твердого электролита, состоящая из катода LiFePO4 и анода Li4Ti5O12, для применения в умном текстиле.J. Electrochem. Soc. 159, A349 – A356 (2012).
CAS Статья Google Scholar
Пушпарадж, В. Л. и др. Гибкие накопители энергии на основе нанокомпозитной бумаги. Proceedings of the National Academy of Sciences 104, 13574–13577 (2007).
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Джонс, С. Д. и Акридж, Дж. Р. Тонкопленочная твердотельная микробатарея.J. Источники энергии 44, 505–513 (1993).
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Yang, Y. et al. Прозрачные литий-ионные аккумуляторы. Proceedings of the National Academy of Sciences 108, 13013–13018 (2011).
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Харб, Дж. Н., Лафоллетт, Р. М., Селфридж, Р. Х. и Хауэлл, Л. Л. Микробатареи для автономных гибридных источников питания.J. Источники энергии 104, 46–51 (2002).
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Леонов В. и Вуллерс Р. Дж. М. Носимая электроника с автономным питанием за счет использования тепла человеческого тела: современное состояние и перспективы. Journal of Renewable and Sustainable Energy 1, 062701–062701–14 (2009).
Артикул Google Scholar
Гамота, Д. Р., Бразис, П., Kalyanasundaram, K. & Zhang, J. (eds) Печатная органическая и молекулярная электроника. (Kluwer Academic Press, Массачусетс, 2004 г.).
Megahed, S. & Ebner, W. Литий-ионный аккумулятор для электронных устройств. J. Источники энергии 54, 155–162 (1995).
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Тараскон, Ж.-М. & Арман, М. Проблемы и проблемы, с которыми сталкиваются литиевые аккумуляторные батареи. Nature 414. С. 359–367 (2001).
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Шэн Шуй З. Обзор сепараторов литий-ионных аккумуляторов с жидким электролитом. J. Источники энергии 164, 351–364 (2007).
Артикул Google Scholar
Ferg, E., Gummow, R.J., de Kock, A. & Thackeray, M. M. Шпинелевые аноды для литий-ионных батарей. J. Electrochem. Soc. 141, L147 – L150 (1994).
CAS Статья Google Scholar
Скросати, Б.& Гарше, Дж. Литиевые батареи: состояние, перспективы и будущее. J. Источники энергии 195, 2419–2430 (2010).
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Кибеле А. и Грюнер Г. Архитектура батареи на основе углеродных нанотрубок. Письма по прикладной физике 91, 144104–144104–3 (2007).
ADS Статья Google Scholar
Moore, V.C. et al. Индивидуально суспендированные одностенные углеродные нанотрубки в различных поверхностно-активных веществах.Nano Lett. 3, 1379–1382 (2003).
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Ислам, М. Ф., Рохас, Э., Бергей, Д. М., Джонсон, А. Т. и Йод, А. Г. Солюбилизация одностенных углеродных нанотрубок с использованием поверхностно-активных веществ с высокой долей веса. Nano Lett. 3, 269–273 (2003).
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Тан Б.З. и Сюй Х. Получение, выравнивание и оптические свойства растворимых углеродных нанотрубок с оболочкой из поли (фенилацетилена).Macromolecules 32, 2569–2576 (1999).
CAS ОБЪЯВЛЕНИЯ MathSciNet Статья Google Scholar
Симмонс, Т. Дж., Хашим, Д., Вайтай, Р. и Аджаян, П. М. Выровненные по площади массивы прямого нанесения одностенных чернил на углеродных нанотрубках. Варенье. Chem. Soc. 129, 10088–10089 (2007).
CAS Статья Google Scholar
Ausman, K. D. et al.Дисперсия однослойных углеродных нанотрубок в органических растворителях: к растворам чистых нанотрубок. J. Phys. Chem. В 104, 8911–8915 (2000).
CAS Статья Google Scholar
Хонг, Дж. К., Ли, Дж. Х. и О, С. М. Влияние углеродной добавки на электрохимические характеристики композитных катодов LiCoO2. J. Источники энергии 111, 90–96 (2002).
CAS ОБЪЯВЛЕНИЯ Статья Google Scholar
Li, Z., Су, Г., Ван, X. и Гао, Д. Микропористый полимерный электролит на основе P (VDF-HFP), заполненный наночастицами Al2O3. Ионика твердого тела 176, 1903–1908 (2005).
CAS Статья Google Scholar
Буден, Ф., Андрие, X., Джеуле, К. и Олсен, И. Микропористый гель PVdF для литий-ионных аккумуляторов. J. Источники энергии 81–82, 804–807 (1999).
Артикул Google Scholar
Тараскон, Дж.-M., Gozdz, A.S., Schmutz, C., Shokoohi, F. и Warren, P.C. Характеристики пластиковых перезаряжаемых литий-ионных батарей Bellcore. Ионика твердого тела 86–88, 49–54 (1996).
Артикул Google Scholar
Юн, W.-S. И Ким, К.-Б. Синтез LiCoO2 с использованием акриловой кислоты и ее электрохимические свойства для литиевых вторичных батарей. J. Источники энергии 81–82, 517–523 (1999).
Артикул Google Scholar
Wu, H.M. et al. Разработка системы LiNi0.5Mn1.5O4 / Li4Ti5O12 с длительным жизненным циклом. .J. Электрохим. Soc. 156, A1047 – A1050 (2009).
CAS Статья Google Scholar
Song, M-Sang et al. Заряд / разряд и срок службы элемента Li4Ti5O12 / LiCoO2-LiNi1-x-yCoxAlyO2 для аккумулирования электроэнергии: влияние параметров конструкции элемента. .Clean Technology ISBN-978-1-4398-3419-0 (2010).
Ву, Х-Чанг., Ли, Э., Ву, Н-Ли. И Джоу, Т. Р. Влияние токосъемников на энергетические характеристики анода Li4Ti5O12 для литий-ионной батареи. J Источники энергии 197, 301–304 (2012).
CAS Статья Google Scholar
Дженовезе, М. П., Лайткап, И. В. и Камат, П. В. Солнечно-правдоподобная краска. Преобразующий одноэтапный подход к проектированию нанокристаллических солнечных элементов. АСУ Нано 6. 2011. С. 865–872.
Артикул Google Scholar
Острая раздавливающая боль, отдающая в челюсть или руку Боль при физической нагрузке, купирующаяся в покое (стенокардия) Иногда систолические шумы митральной регургитации Часто обнаруживается красный флаг ‡ | Нагрузочный визуализирующий тест или КТ-ангиография рассматриваются у пациентов с отрицательными или неизменными результатами ЭКГ и без повышения сердечных маркеров при серийном тестировании | |
Внезапная рвущая боль, отдающая в спину У некоторых пациентов наблюдаются обмороки, инсульт или ишемия ног Пульс или АД, которые могут быть неодинаковыми в конечностях | Рентген грудной клетки, позволяющий предположить диагноз Расширенная компьютерная томография аорты для подтверждения | |
Лихорадка, одышка, утомляемость, боль в груди (при миоперикардите), недавняя вирусная или другая инфекция Иногда обнаружение сердечной недостаточности, перикардита или того и другого | Обычно эхокардиография или МРТ сердца | |
Постоянная или периодическая острая боль, часто усиливающаяся при дыхании, глотании пищи или положении лежа на спине и уменьшающаяся при сидении или наклоне вперед Вздутие яремных вен | Кардиальные маркеры в сыворотке крови (иногда показывают минимальное повышение уровней тропонина и CK-MB при наличии ассоциированного миокардита) Трансторакальная эхокардиография | |
Внезапная сильная боль после рвоты или применения инструментов (например, эзофагогастроскопии или чреспищеводной эхокардиографии) Подкожная крепитация обнаружена при аускультации Несколько выводов «красных флажков» ‡ | Эзофагография с водорастворимым контрастом для подтверждения | |
Боль в эпигастрии или нижней части грудной клетки, которая часто усиливается в положении лежа и облегчается при наклоне вперед Болезненность верхней части живота Часто злоупотребление алкоголем или заболевание желчевыводящих путей в анамнезе | ||
Рецидивирующий дискомфорт в правом подреберье или в эпигастрии после еды (но не физической нагрузки) | УЗИ желчного пузыря | |
Длительная боль с коварным началом, которая может сопровождать или не сопровождать глотание Обычно также затруднено глотание | ||
Рецидивирующая жгучая боль, иррадияющая от эпигастрия к горлу, усиливающаяся при наклоне или лежании и облегчающаяся антацидами | Иногда исследования моторики | |
Рецидивирующий неопределенный дискомфорт в эпигастрии, особенно у пациента, который курит или чрезмерно употребляет алкоголь, который облегчается приемом пищи, антацидами или обоими способами | Иногда тестирование на Helicobacter pylori | |
Часто плевритная боль, одышка, тахикардия Иногда умеренная температура, кровохарканье, шок Более вероятно при наличии факторов риска | Зависит от клинического подозрения (критерии Уэллса) Иногда КТ ангиография легких | |
Значительная одышка, гипотензия, вздутие шейных вен, одностороннее ослабление звуков дыхания и гиперрезонанс на перкуссию Иногда подкожный воздух | ||
Лихорадка, озноб, кашель и гнойная мокрота Часто одышка, тахикардия, признаки уплотнения | ||
Иногда одностороннее ослабленное дыхание, подкожный воздух | Иногда УЗИ или КТ грудной клетки | |
Может иметь предшествующую пневмонию, тромбоэмболию легочной артерии или респираторную вирусную инфекцию Боль при дыхании, кашель Иногда шум трения плевры, в остальном осмотр без особенностей | Обычно клиническая оценка | |
2 Различные виды рака грудной клетки | Переменная, но иногда плевритная боль Иногда хронический кашель, курение в анамнезе, признаки хронического заболевания (похудание, лихорадка), шейная лимфаденопатия | КТ грудной клетки, если результаты рентгенологического исследования наводят на мысль Сканирование костей рассматривается при стойкой очаговой боли в ребрах |
Почти постоянная боль, затрагивающая несколько участков тела, а также грудную клетку Обычно утомляемость и плохой сон | ||
Острая, полосатая боль в грудной клетке односторонне Классическая линейная, везикулярная сыпь Боль может предшествовать высыпанию на несколько дней | ||
3 Боль в скелетно-мышечной стенке грудной клетки (например, из-за травмы, чрезмерного использования или реберохондрита) | Часто подсказывается историей Боль обычно постоянная (обычно несколько дней или дольше), усиливающаяся при пассивном и активном движении Рассеянная или очаговая болезненность | |
Таблица шкалы боли: от 1 до 10 уровней
Дата публикации: 20 мая 2016 г. — Обновлено: 12 марта 2020 г.
Автор: Disabled World — Контактное лицо: www.disabled-world.com
Сводка *: Диаграмма шкалы боли и диаграмма, которая включает объяснение каждого из от одного до десяти классифицированных уровней боли. Одна из самых сложных вещей, связанных с хронической болью, заключается в том, что только ВЫ знаете, насколько сильна ваша боль. Наша диаграмма шкалы боли и диаграмма включают объяснение каждого из уровней боли, которые могут помочь вам лучше объяснить другим боль, которую вы чувствуете. Боль передается через определенные нервные волокна, которые переносят болевые импульсы в мозг …
Main Digest
Боль определяется как чувство, вызываемое нервной системой.Боль может быть острой или тупой. Он может приходить и уходить, а может быть постоянным.
Боль опосредуется определенными нервными волокнами, которые переносят болевые импульсы в мозг, где их сознательное восприятие может быть изменено многими факторами.
Боль может помочь в диагностике проблемы. Без боли вы можете серьезно повредить себя, не зная об этом, или вы можете не осознавать, что у вас есть медицинская проблема, требующая лечения. Как только вы решите проблему, боль обычно проходит. Однако иногда боль продолжается неделями, месяцами или даже годами.Это называется хронической болью. Иногда хроническая боль возникает из-за постоянной причины, например рака или артрита.
Типы боли включают:
Психогенная боль
Психалгия или соматоформная боль — это физическая боль, которая вызывается, усиливается или продлевается под воздействием психических, эмоциональных или поведенческих факторов. Головная боль, боль в спине или боли в животе — одни из наиболее распространенных типов психогенной боли.
Призрачная боль
Ощущение боли в конечности или органе, которые были потеряны или от которых человек больше не получает физических сигналов.Призрачная боль в конечностях — это опыт, о котором почти всегда сообщают инвалиды и парализованные. Фантомная боль — это невропатическая боль.
Острая боль
Боль, которая возникает быстро, может быть сильной, но длится относительно недолго. В отличие от хронической боли. Острая боль служит предупреждением о болезни или угрозе для организма.
Хроническая боль
Определяется как боль, которая сохраняется дольше, чем временное течение естественного заживления, связанное с определенным типом травмы или болезненного процесса.Хроническая боль ухудшает способность направлять внимание, в частности, по сравнению со сверстниками с низкой интенсивностью или без хронической боли, у людей с хронической болью высокой интенсивности значительно снижена способность выполнять задачи, требующие внимания.
Одна из сложностей хронической боли заключается в том, что только вы знаете, насколько сильна эта боль. Нет тестов, которые показали бы, насколько вы страдаете. Часто отсутствуют внешние признаки, свидетельствующие о том, насколько сильно человек испытывает боль.
Шкала боли
Шкала боли измеряет интенсивность боли человека и основана на самоотчетах, наблюдениях (поведенческих) или физиологических данных.Доступны различные шкалы боли для новорожденных, младенцев, детей, подростков, взрослых, пожилых людей и людей с нарушенной коммуникацией. Оценка боли часто рассматривается как «пятый жизненно важный знак».
Универсальный скрининг боли становится все более распространенной практикой, в основном из-за требования Объединенной комиссии по аккредитации медицинских организаций (JCAHO), согласно которому аккредитованные больницы и клиники должны регулярно оценивать всех пациентов на предмет боли. Скрининг боли предназначен для улучшения качества лечения боли путем систематического выявления пациентов, страдающих болью, в клинических условиях.
Таблица шкалы боли
Для обслуживающего персонала и ветеранов может лучше подойти использование шкалы оценки боли обороны и ветеранов DVPRS 2.0 — инструмента оценки боли с использованием шкалы оценок, словесных дескрипторов, цветового кодирования, графических выражений лица, соответствующих уровню боли.
В таблице базовой шкалы боли ниже приведены некоторые примеры различных уровней, определяющих шкалу боли от 0 до 10.
| Сравнительная шкала боли от 0 до 10 | |
|---|---|
| |
| Нет боли | |
| Никакой боли, ты чувствуешь себя совершенно нормально. |
| Незначительные уровни боли | |
| Значок легкой боли | Незначительный уровень боли обычно не мешает повседневной деятельности. Способен адаптироваться к боли психологически и с помощью лекарств или устройств, таких как подушки. |
Уровень боли 1 | Боль первого уровня означает очень легкую, едва заметную боль, как укус комара или зуд ядовитого плюща. Большую часть времени вы никогда не думаете о боли. |
Уровень боли 2 | Боль второго уровня — это незначительная дискомфортная боль, например, легкое защемление складки кожи между большим и указательным пальцами другой рукой ногтями.Люди могут по-разному отреагировать на эту самопроверку. |
Уровень боли 3 | Боль третьего уровня — это терпимая, но очень заметная боль, такая как случайный порез, удар в нос, вызывающий кровь из носа, или укол, сделанный врачом. Боль не настолько сильная, чтобы к ней невозможно было привыкнуть. В конце концов, большую часть времени вы не замечаете боли, поскольку вы к ней адаптировались. |
| Умеренный уровень боли | |
| Значок умеренной боли | Умеренный уровень боли мешает выполнять многие повседневные дела.Эти уровни боли обычно требуют некоторых изменений в образе жизни, но вы можете оставаться независимым, однако вы не можете адаптироваться к боли. |
Уровень боли 4 | Боль четвертого уровня — это мучительная сильная и глубокая боль, похожая на обычную зубную боль, начальную боль от укуса пчелы или незначительную травму части тела, например, очень сильную ушибленную ногу. Настолько сильная, что вы все время замечаете боль и не можете полностью адаптироваться. Этот уровень боли можно смоделировать, ущипнув складку кожи между большим и указательным пальцами другой рукой, используя ногти и сильно сжимая.Обратите внимание на то, как имитируемая боль сначала пронизывает, но затем становится тупой. |
Уровень боли 5 | Боль пятого уровня — это очень мучительная сильная, глубокая, пронзительная боль, такая как вывихнутая лодыжка, когда вы встаете на нее неправильно, или легкая боль в спине. Вы не только все время замечаете боль, но и настолько озабочены ее устранением, что ваш нормальный образ жизни сокращается. Нередки временные расстройства личности. |
Уровень боли 6 | Боль шестого уровня — это сильная, глубокая и пронзительная боль.Боль настолько сильна, что кажется, что она частично овладевает вашими чувствами, заставляя думать нечетко. На этом этапе у вас начинаются проблемы с удержанием работы или нормальными социальными отношениями. Сравнимо с сильной немигренозной головной болью в сочетании с несколькими укусами пчел или сильной болью в спине |
| Уровни сильной боли | |
| Значок сильной боли | Сильный уровень боли, означающий, что вы не можете заниматься своими обычными делами.Пациент считается инвалидом и не может самостоятельно функционировать. |
Уровень боли 7 | Боль седьмого уровня состоит из очень сильной боли. Практически то же самое, что и уровень 6, за исключением того, что боль полностью доминирует над вашими чувствами, заставляя вас думать нечетко примерно в половине случаев. На данный момент вы фактически инвалид и часто не можете жить один. Сравнимо со средней головной болью при мигрени. |
| Боль восьмого уровня — ужасная боль.Боль, которую вы чувствуете, настолько сильна, что вы больше не можете ясно мыслить, и часто претерпевает серьезные изменения личности, если боль присутствует в течение длительного времени. Часто думают о самоубийстве, а иногда и пытаются. Сравнимо с родами или настоящей головной болью — мигренью. |
Уровень боли 9 | Боль девятого уровня — мучительная боль, настолько сильная, что вы не можете ее терпеть и требовать обезболивающих или хирургического вмешательства, независимо от побочных эффектов или риска.Если это не сработает, часты самоубийства, потому что в жизни больше нет никакой радости. Сравним с раком горла. |
| Боль десятого уровня означает невообразимую боль. Этот уровень боли настолько силен, что вы скоро потеряете сознание. Большинство людей никогда не испытывали такой боли. Те, кто пострадали в тяжелой аварии, например, сломали руку, и потеряли сознание в результате боли, а не потери крови, испытали 10 уровень. |
Измерение боли
Толерантность к боли считается максимальным уровнем боли, который человек может переносить, не теряя сознание. Толерантность к боли отличается от «болевого порога», то есть точки, при которой боль начинает ощущаться.
Порог боли (болевой порог) — это точка на кривой возрастающего восприятия стимула, при которой начинает ощущаться боль. Измерения болевого порога включают:
- Давление, при котором звук становится болезненным для слушателя, называется «болевым пороговым давлением».
- Температура, при которой жар становится болезненным для человека, известна как «порог тепловой боли».
Что такое долориметр?
Долориметрия определяется как «измерение болевой чувствительности или интенсивности боли» . Долориметр — это инструмент, используемый для измерения болевого порога и толерантности к боли. Долориметры применяют к определенной области постоянное давление, тепло или электрическую стимуляцию. Иногда для приложения давления используется тупой предмет или путем увеличения давления воздуха на определенную область тела, а иногда путем прижатия острого инструмента к телу, чтобы сдвинуть соединение, t или другую часть тела, чтобы определить уровень тепла. давление, электрический ток или количество движений вызывают ощущение боли.
Было разработано несколько различных типов долориметров. Долориметр, известный как Sonic Palpometer, был разработан в Университете Виктории в Британской Колумбии, Канада. Sonic Palpometer использует ультразвуковые и компьютерные технологии для автоматизации техники пальпации для определения чувствительности области тела пациента.
Какие самые болезненные вещи вы можете испытать?
Список в алфавитном порядке, а не степень тяжести боли:
- Острый панкреатит
- Аппендицит
- Артрит
- Боль в спине
- Переломы костей (особенно бедра)
- Ожоги (тяжелые)
- Роды
- Кластерные головные боли
- Комплексный регионарный болевой синдром (КРБС)
- Болезнь Деркума
- Эмоциональная боль (депрессия — ПТСР)
- Эндометриоз
- Фибромиалгия
- Лопатка замороженная
- Перекрут гонад (перекручивание гонад)
- Подагра
- Сердечный приступ
- Синдром Ируканджи (укус коробчатой медузы)
- Камни в почках
- Мигрень
- Боль после операции
- Перелом полового члена
- Перитонит
- Головная боль после пункции (головная боль в позвоночнике)
- Дорожная сыпь
- Ишиас
- Битумная черепица
- Серповидно-клеточная анемия
- Диск скольжения
- Язва желудка
- Шип каменной рыбы
- Столбняк
- Зубная боль — абсцесс зуба
- Разрыв ахиллова сухожилия
- Невралгия тройничного нерва
Об авторе
Disabled World (Disabled-World.Com) — это независимое сообщество людей с ограниченными возможностями, созданное в 2004 году для предоставления новостей об инвалидах, обзоров вспомогательных технологий и спортивных мероприятий для инвалидов, а также общей информации для людей с ограниченными возможностями, пожилых людей, их семей и / или лиц, осуществляющих уход. Не забудьте заглянуть на нашу домашнюю страницу, чтобы найти информативные обзоры, эксклюзивные истории и инструкции. Вы также можете найти нас в Twitter, Facebook и LinkedIn.
Документы, связанные с острой / хронической болью
* Заявление об ограничении ответственности: Disabled World предоставляет только общую информацию.Представленные материалы никоим образом не предназначены для замены профессиональной медицинской помощи квалифицированным практикующим врачом и не должны рассматриваться как таковые. Любое стороннее предложение или реклама на disabled-world.com не означает одобрения Disabled World. Ознакомьтесь с нашей Политикой в отношении рекламы для получения дополнительной информации. Сообщите нам устаревшую или неточную информацию.
Цитируйте страницу: Журнал: Мир инвалидов . Язык: английский (США). Автор: Disabled World. Дата публикации в электронном виде: 20 мая 2016 г. - Последняя редакция: 12 марта 2020 г.Название: Таблица шкалы боли: от 1 до 10 уровней , Источник: Таблица шкалы боли: от 1 до 10 уровней . Получено 2021-04-25, из https://www.disabled-world.com/health/pain/scale.php - Ссылка: DW # 50-12182.
Могут ли инверсионные столы помочь при боли в пояснице
Инверсионные столы могут помочь пациентам, страдающим от болей в пояснице. Эти наклонные столы помогают растянуть мышцы и мягкие ткани вокруг позвоночника и обеспечивают легкое натяжение под действием силы тяжести (тяга), чтобы снять давление с нервов и диска между костями позвоночника (позвонками).
Инверсионные столы могут помочь пациентам, страдающим от боли в пояснице. Источник фото: 123RF.com. На данный момент Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило только инверсионные столы Teeter® для продажи в качестве медицинского устройства. Недавно FDA расширило список состояний, для которых разрешены для использования таблицы Teeter Inversion Tables, включая боль в спине, мышечное напряжение, остеохондроз, дегенеративное заболевание суставов позвоночника, стеноз позвоночника, грыжу межпозвоночного диска, искривление позвоночника из-за напряженных мышц, ишиас, мышечный спазм и фасеточный синдром. 1
Расширенный допуск FDA свидетельствует о том, что инверсионные столы становятся все более популярной терапией для лечения распространенных проблем со спиной. Исследования показали, что инверсионные столы помогают уменьшить боль, восстановить нормальное пространство между позвонками и уменьшить потребность в хирургии позвоночника. 2-4
Эффект инверсионной терапии на диск сродни дозированию зубной пасты. Если вы оказываете слишком сильное давление на тюбик и выдавливаете больше, чем необходимо, вы часто можете повторно расширить тюбик, сжимая его в другой плоскости, что приведет к тому, что часть зубной пасты втянется обратно.
Однако трудно предсказать, будут ли эти эффекты временными или продолжаться в течение дня. Вы, безусловно, можете почувствовать некоторое облегчение, пока находитесь на устройстве, но как только вы его отключите, гравитация начинает работать против вас. Также пока неясно, как долго человеку следует пользоваться инверсионным столом.
Как использовать инверсионные таблицыБольшинству моих пациентов я рекомендую попробовать инверсионную терапию в течение как минимум двух недель по 10 минут дважды в день, но не опускаться более чем на 45 градусов ниже горизонтали.Обычно вы можете почувствовать эффект инверсионной терапии при наклоне всего от 20 до 30 градусов.
Не рекомендуется ставить стол под большим углом, когда человек полностью перевернут. Чрезмерно агрессивная инверсия может привести к обратным результатам. Например, если диск уже порван, полная инверсия может вызвать дополнительную травму. Таким образом, инверсия может быть слишком хорошей вещью, и эти таблицы могут нанести дополнительный ущерб, если их неправильно использовать.
Кому не следует использовать инверсионные таблицы?Инверсионные столы не рекомендуются людям с нестабильностью поясничного отдела, например, переломом позвоночника или спондилолистезом.Кроме того, инверсионные столы лучше всего использовать только для лечения боли в пояснице; Людям с болью в шее могут быть полезны устройства для вытяжения шейного отдела позвоночника (например, пневматические устройства и устройства с аппарелями).
Кроме того, инверсионные таблицы не рекомендуются для людей с высоким кровяным давлением, сердечными заболеваниями или глаукомой, брюшной или паховой грыжей, остеопорозом, заболеваниями бедра / колена или беременными.
Перед тем, как попробовать инверсионные столы, обязательно поговорите со своим врачом, чтобы убедиться, что лечение подходит именно вам.

 A.M., Passchier J.
A.M., Passchier J.

 В научной литературе указываются периоды от 3 до 6 мес. У детей хроническая боль чаще всего имеет органический характер, например боль вследствие рака или артрита. О возвратной боли говорят в тех случаях, когда в течение 3 мес возникают 3 эпизода острой боли или более. Эти эпизоды могут быть следствием болезней, таких как артрит, но это могут быть и головная боль или боль в животе без выявляемого ноцицептивного (болевого рецепторного) субстрата. В таком случае боль связывается со стрессовой ситуацией и часто наблюдается у детей, у родителей которых в анамнезе имеются указания на такую боль
В научной литературе указываются периоды от 3 до 6 мес. У детей хроническая боль чаще всего имеет органический характер, например боль вследствие рака или артрита. О возвратной боли говорят в тех случаях, когда в течение 3 мес возникают 3 эпизода острой боли или более. Эти эпизоды могут быть следствием болезней, таких как артрит, но это могут быть и головная боль или боль в животе без выявляемого ноцицептивного (болевого рецепторного) субстрата. В таком случае боль связывается со стрессовой ситуацией и часто наблюдается у детей, у родителей которых в анамнезе имеются указания на такую боль Авторы описывают этот механизм как ворота. Когда ворота открыты, ноцицептивная информация достигает мозга. При частично или полностью закрытых воротах в мозг приходит меньше информации или она не поступает совсем. Периферические процессы (например, при трении поврежденной части тела) и центральные процессы (например, при повышенном уровне страха) могут влиять на передачу болевой информации и обусловливать уменьшение или усиление боли
Авторы описывают этот механизм как ворота. Когда ворота открыты, ноцицептивная информация достигает мозга. При частично или полностью закрытых воротах в мозг приходит меньше информации или она не поступает совсем. Периферические процессы (например, при трении поврежденной части тела) и центральные процессы (например, при повышенном уровне страха) могут влиять на передачу болевой информации и обусловливать уменьшение или усиление боли По мере увеличения продолжительности боли компоненты переживания и поведения все в большей степени влияют на то, как человек ощущает боль (рис.1)
По мере увеличения продолжительности боли компоненты переживания и поведения все в большей степени влияют на то, как человек ощущает боль (рис.1) Адаптированная для Голландии
Адаптированная для Голландии  Поэтому наблюдение за поведением рекомендуется в качестве метода оценки степени боли. Регистрируют движение, положение тела, выражение лица и характер плача ребенка (рис.2). Наблюдение за поведением может осуществляться непосредственно или позже с помощью видеопленки. В первом случае обычно это производит специально обученный средний медицинский персонал. При этом заранее проверяют, является ли их согласованность в оценках приемлемой (например, взвешенная k _ 70; каппа — статистическая переменная для измерения согласованности между наблюдателями с учетом меры случайной согласованности)
Поэтому наблюдение за поведением рекомендуется в качестве метода оценки степени боли. Регистрируют движение, положение тела, выражение лица и характер плача ребенка (рис.2). Наблюдение за поведением может осуществляться непосредственно или позже с помощью видеопленки. В первом случае обычно это производит специально обученный средний медицинский персонал. При этом заранее проверяют, является ли их согласованность в оценках приемлемой (например, взвешенная k _ 70; каппа — статистическая переменная для измерения согласованности между наблюдателями с учетом меры случайной согласованности)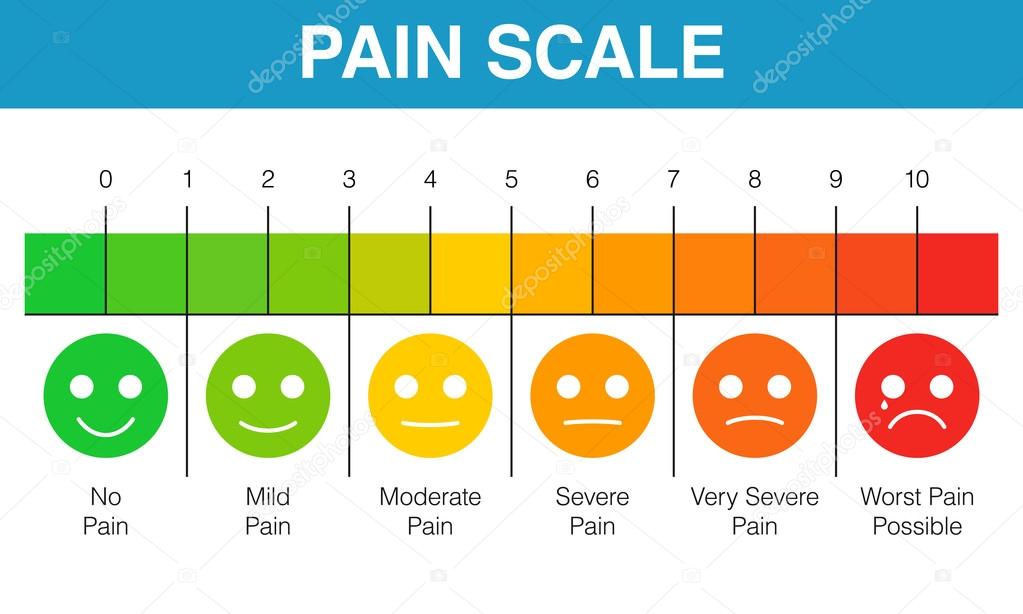 Для оценки послеоперационной боли у голландских детей Boelen van der Loo изменил ШБДБВО. Наблюдение за лицом составляет основу «Неонатальной лицевой кодирующей системы» (НЛКС), разработанной Grunau и Craig для измерения острой боли у новорожденных
Для оценки послеоперационной боли у голландских детей Boelen van der Loo изменил ШБДБВО. Наблюдение за лицом составляет основу «Неонатальной лицевой кодирующей системы» (НЛКС), разработанной Grunau и Craig для измерения острой боли у новорожденных Эта шкала обработана для Голландии и вместе c другими различными способами оценки степени боли в настоящее время исследуется в палате интенсивной терапии отделения детской хирургии Академической больницы Роттердама — Детской больницы София в сотрудничестве с отделением детской хирургии Академического медицинского центра в Амстердаме (табл.1; H.Koot, сообщение 1994 г.)
Эта шкала обработана для Голландии и вместе c другими различными способами оценки степени боли в настоящее время исследуется в палате интенсивной терапии отделения детской хирургии Академической больницы Роттердама — Детской больницы София в сотрудничестве с отделением детской хирургии Академического медицинского центра в Амстердаме (табл.1; H.Koot, сообщение 1994 г.)