Рак желудка у пожилых людей: ХИМИОТЕРАПИЯ У ПОЖИЛЫХ ПАЦИЕНТОВ, СТРАДАЮЩИХ РАКОМ ЖЕЛУДКА | Королева
ХИМИОТЕРАПИЯ У ПОЖИЛЫХ ПАЦИЕНТОВ, СТРАДАЮЩИХ РАКОМ ЖЕЛУДКА | Королева
1. Ferlay J., Soerjomataram I., Dikshit R., Eser S., Mathers C., Rebelo M. et al. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012. Int. J. Cancer. 2015. Vol. 136. P. E359–86.
2. GLOBOCAN 2012: Estimated Cancer Incidence, Mortality and Prevalence Worldwide in 2012. Lyon, France: International Agency for Research on Cancer, 2013. Available from: http://globocan.iarc.fr.
3. Parkin D. M. The global health burden of infection-associated cancers in the year 2002. Int. J. Cancer. 2006. Vol. 118. P. 3030–3044.
4. Siegel R., Ma J., Zou Z., Jemal A. Cancer statistics, 2014.
5. Статистика злокачественных новообразований в России и странах СНГ в 2013 г. / под ред. Давыдова М. И., Аксель Е. М. Москва, 2015.
6. Glimelius B., Ekstrom K., Hoffman K., Graf W., Sjoden P. O., Haglund U. et al. Randomized comparison between chemotherapy plus best supportive care with best supportive care in advanced gastric cancer. Ann. Oncol. 1997. Vol. 8. P. 163–168.
7. Pyrhonen S., Kuitunen T., Nyandoto P., Kouri M. Randomised comparison of fluorouracil, epidoxorubicin and methotrexate (FEMTX) plus supportive care with supportive care alone in patients with non-resectable gastric cancer. Br. J. Cancer. 1995. Vol. 71. P. 587–591.
8. Murad A. M., Santiago F. F., Petroianu A., Rocha P. R., Rodrigues M. A., Rausch M. Modified therapy with 5-fluorouracil, doxorubicin, and methotrexate in advanced gastric cancer. Cancer. 1993. Vol. 72. P. 37–41.
Murad A. M., Santiago F. F., Petroianu A., Rocha P. R., Rodrigues M. A., Rausch M. Modified therapy with 5-fluorouracil, doxorubicin, and methotrexate in advanced gastric cancer. Cancer. 1993. Vol. 72. P. 37–41.9. Polee M. B., Hop W. C., Kok T. C., Eskens F. A., van der Burg M. E., Splinter T. A. et al. Prognostic factors for survival in patients with advanced oesophageal cancer treated with cisplatin-based combination chemotherapy. Br. J. Cancer. 2003. Vol. 89. P. 2045–2050.
10. Chau I., Norman A. R., Cunningham D., Waters J. S., Oates J., Ross P. J. Multivariate prognostic factor analysis in locally advanced and metastatic esophago-gastric cancer—pooled analysis from three multicenter, randomized, controlled trials using individual patient data. J. Clin. Oncol. 2004. Vol. 22. P. 2395–2403.
11. Trumper M., Ross P. J., Cunningham D., Norman A. R., Hawkins R., Seymour M. et al. Efficacy and tolerability of chemotherapy in elderly patients with advanced oesophago-gastric cancer: A pooled analysis of three clinical trials. Eur. J. Cancer. 2006. Vol. 42. P. 827–834.
Trumper M., Ross P. J., Cunningham D., Norman A. R., Hawkins R., Seymour M. et al. Efficacy and tolerability of chemotherapy in elderly patients with advanced oesophago-gastric cancer: A pooled analysis of three clinical trials. Eur. J. Cancer. 2006. Vol. 42. P. 827–834.
12. Jatoi A., Foster N. R., Egner J. R., Burch P. A., Stella P. J., Rubin J. et al. Older versus younger patients with metastatic adenocarcinoma of the esophagus, gastroesophageal junction, and stomach: a pooled analysis of eight consecutive North Central Cancer Treatment Group (NCCTG) trials. Int. J. Oncol. 2010. Vol. 36. P. 601–606.
13. Hurria A., Lichtman S. M. Clinical pharmacology of cancer therapies in older adults. Br. J. Cancer. 2008. Vol. 98. P. 517–522.14. Repetto L., Fratino L. , Audisio R. A., Venturino A., Gianni W., Vercelli M. et al. Comprehensive geriatric assessment adds information to Eastern Cooperative Oncology Group performance status in elderly cancer patients: an Italian Group for Geriatric Oncology Study. J. Clin. Oncol. 2002. Vol. 20. P. 494–502.
, Audisio R. A., Venturino A., Gianni W., Vercelli M. et al. Comprehensive geriatric assessment adds information to Eastern Cooperative Oncology Group performance status in elderly cancer patients: an Italian Group for Geriatric Oncology Study. J. Clin. Oncol. 2002. Vol. 20. P. 494–502.
15. Wedding U., Kodding D., Pientka L., Steinmetz H. T., Schmitz S. Physicians’ judgement and comprehensive geriatric assessment (CGA) select different patients as fit for chemotherapy. Crit. Rev. Oncol. Hematol. 2007. Vol. 64. P. 1–9.
16. Extermann M., Aapro M., Bernabei R., Cohen H. J., Droz J. P., Lichtman S. et al. Use of comprehensive geriatric assessment in older cancer patients: recommendations from the task force on CGA of the International Society of Geriatric Oncology (SIOG). Crit. Rev. Oncol. Hematol. 2005. Vol. 55. P. 241–252.
17. Extermann M., Hurria A. Comprehensive geriatric assessment for older patients with cancer. J. Clin. Oncol. 2007. Vol. 25. P. 1824–1831.
Extermann M., Hurria A. Comprehensive geriatric assessment for older patients with cancer. J. Clin. Oncol. 2007. Vol. 25. P. 1824–1831.
18. Pal S. K., Katheria V., Hurria A. Evaluating the older patient with cancer: understanding frailty and the geriatric assessment. CA Cancer J. Clin. 2010. Vol. 60. P. 120–132.
19. Rodin M. B., Mohile S. G. A practical approach to geriatric assessment in oncology. J. Clin. Oncol. 2007. Vol. 25. P. 1936–1944.20. Hurria A., Gupta S., Zauderer M., Zuckerman E. L., Cohen H. J., Muss H. et al. Developing a cancer-specific geriatric assessment: a feasibility study. Cancer. 2005. Vol. 104. P. 1998–2005.
21. Hurria A., Cirrincione C. T., Muss H. B., Kornblith A. B., Barry W., Artz A. S. et al. Implementing a geriatric assessment in cooperative group clinical cancer trials: CALGB 360401. J. Clin. Oncol. 2011. Vol. 29. P. 1290–1296.
B., Kornblith A. B., Barry W., Artz A. S. et al. Implementing a geriatric assessment in cooperative group clinical cancer trials: CALGB 360401. J. Clin. Oncol. 2011. Vol. 29. P. 1290–1296.
22. Hurria A., Togawa K., Mohile S. G., Owusu C., Klepin H. D., Gross C. P. et al. Predicting chemotherapy toxicity in older adults with cancer: a prospective multicenter study. J. Clin. Oncol. 2011. Vol. 29. P. 3457–3465.
23. Cunningham D., Allum W. H., Stenning S. P., Thompson J. N., Van de Velde C. J., Nicolson M. Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer. N. Engl. J. Med. 2006. Vol. 355. P. 11–20.
24. Ychou M., Boige V., Pignon J. P., Conroy T., Bouche O., Lebreton G. et al. Perioperative chemotherapy compared with surgery alone for resectable gastroesophageal adenocarcinoma: an FNCLCC and FFCD multicenter phase III trial. J. Clin. Oncol. 2011. Vol. 29. P. 1715–1721.
J. Clin. Oncol. 2011. Vol. 29. P. 1715–1721.
26. Kulig J., Kolodziejczyk P., Sierzega M., Bobrzynski L., Jedrys J., Popiela T. et al. Adjuvant chemotherapy with etoposide, adriamycin and cisplatin compared with surgery alone in the treatment of gastric cancer: a phase III randomized, multicenter, clinical trial. Oncology. 2010. Vol. 78. P. 54–61.
27. Bouche O., Ychou M., Burtin P., Bedenne L., Ducreux M., Lebreton G. et al. Adjuvant chemotherapy with 5-fluorouracil and cisplatin compared with surgery alone for gastric cancer: 7-year results of the FFCD randomized phase III trial (8801).
28. Sakuramoto S., Sasako M., Yamaguchi T., Kinoshita T., Fujii M., Nashimoto A. et al. Adjuvant chemotherapy for gastric cancer with S-1, an oral fluoropyrimidine. N. Engl. J. Med. 2007. Vol. 357. P. 1810–1820.
29. Bang Y. J., Kim Y. W., Yang H. K., Chung H. C., Park Y. K., Lee K. H. et al. CLASSIC trial investigators. Adjuvant capecitabine and oxaliplatin for gastric cancer after D2 gastrectomy (CLASSIC): a phase 3 open-label, randomised controlled trial. Lancet. 2012. Vol. 379. P. 315–321.
30. Sasako M., Sakuramoto S., Katai H., Kinoshita T., Furukawa H., Yamaguchi T. et al. Five-year outcomes of a randomized phase III trial comparing adjuvant chemotherapy with S-1 versus surgery alone in stage II or III gastric cancer.
31. Noh S. H., Park S. R., Yang H. K., Chung H. C., Chung I. J., Kim S. W. et al. CLASSIC trial investigators. Adjuvant capecitabine plus oxaliplatin for gastric cancer after D2 gastrectomy (CLASSIC): 5-year follow-up of an open-label, randomized phase 3 trial. Lancet Oncol. 2014. Vol. 15. P. 1389–1396.
32. Wagner A. D., Unverzagt S., Grothe W., Kleber G., Grothey A., Haerting J., Fleig W. E. Chemotherapy for advanced gastric cancer. Cochrane Database Syst. Rev. 2010. CD004064.
33. Webb A., Cunningham D., Scarffe J. H., Harper P., Norman A., Joffe J. K. et al. Randomized trial comparing epirubicin, cisplatin, and fluorouracil versus fluorouracil, doxorubicin, and methotrexate in advanced esophagogastric cancer.
34. Kim N. K., Park Y. S., Heo D. S., Suh C., Kim S. Y., Park K. C. et al. A phase III randomized study of 5-fluorouracil and cisplatin versus 5-fluorouracil, doxorubicin, and mitomycin C versus 5-fluorouracil alone in the treatment of advanced gastric cancer. Cancer. 1993. Vol. 71. P. 3813–3818.
35. Ohtsu A., Shimada Y., Shirao K., Boku N., Hyodo I., Saito H. et al. Randomized phase III trial of fluorouracil alone versus fluorouracil plus cisplatin versus uracil and tegafur plus mitomycin in patients with unresectable, advanced gastric cancer: The Japan Clinical Oncology Group Study (JCOG9205). J. Clin. Oncol. 2003. Vol. 21. P. 54–59.
36. Lord S. R., Hall P. S., McShane P., Brown J., Seymour M. T. Factors predicting outcome for advanced gastroesophageal cancer in elderly patients receiving palliative chemotherapy. Clin. Oncol. 2010. Vol. 22. P. 107–113.
Clin. Oncol. 2010. Vol. 22. P. 107–113.
37. Cunningham D., Starling N., Rao S., Iveson T., Nicolson M., Coxon F. et al. Upper Gastrointestinal Clinical Studies Group of the National Cancer Research Institute of the United Kingdom. Capecitabine and oxaliplatin for advanced esophagogastric cancer. N. Engl. J. Med. 2008. Vol. 358. P. 36–46.
38. Al-Batran S. E., Hartmann J. T., Probst S., Schmalenberg H., Hollerbach S., Hofheinz R. et al. Phase III trial in metastatic gastroesophageal adenocarcinoma with fluorouracil, leucovorin plus either oxaliplatin or cisplatin: a study of the Arbeitsgemeinschaft Internistische Onkologie. J. Clin. Oncol. 2008. Vol. 26. P. 1435–1442.
39. Santini D., Graziano F., Catalano V., Di Seri M., Testa E., Baldelli A. M. et al. Weekly oxaliplatin, 5-fluorouracil and folinic acid (OXALF) as first-line chemotherapy for elderly patients with advanced gastric cancer: results of a phase II trial. BMC Cancer. 2006. Vol. 6. P. 125–131.
Weekly oxaliplatin, 5-fluorouracil and folinic acid (OXALF) as first-line chemotherapy for elderly patients with advanced gastric cancer: results of a phase II trial. BMC Cancer. 2006. Vol. 6. P. 125–131.
40. Choi I. S., Oh D. Y., Kim B. S., Lee K. W., Kim J. H., Lee J. S. Oxaliplatin, 5-FU, folinic acid as first-line palliative chemotherapy in elderly patients with metastatic or recurrent gastric cancer. Cancer Res. Treat. 2007. Vol. 39. P. 99–103.
41. Liu Z. F., Guo Q. S., Zhang X. Q., Yang X. G., Guan F., Fu Z., Wang M. Y. Biweekly oxaliplatin in combination with continuous infusional 5-fluorouracil and leucovorin (modified FOLFOX-4 regimen) as first-line chemotherapy for elderly patients with advanced gastric cancer. Am. J. Clin. Oncol. 2008. Vol. 31. P. 259–263.
42. Dong N., Jiang W., Li H., Liu Z., Xu X., Wang M. Triweekly oxaliplatin plus oral capecitabine as first-line chemotherapy in elderly patients with advanced gastric cancer. Am. J. Clin. Oncol. 2009. Vol. 32. P. 559–563.
Dong N., Jiang W., Li H., Liu Z., Xu X., Wang M. Triweekly oxaliplatin plus oral capecitabine as first-line chemotherapy in elderly patients with advanced gastric cancer. Am. J. Clin. Oncol. 2009. Vol. 32. P. 559–563.
43. Zhao J. G., Qiu F., Xiong J. P., Zhang L., Xiang X. J., Yu F. et al. A phase II study of modified FOLFOX as first-line chemotherapy in elderly patients with advanced gastric cancer. Anticancer Drugs. 2009. Vol. 20. P. 281–286.
44. Xiang X. J., Zhang L., Qiu F., Yu F., Zhan Z. Y., Feng M. et al. A phase II study of capecitabine plus oxaliplatin as first-line chemotherapy in elderly patients with advanced gastric cancer. Chemotherapy. 2012. Vol. 58. P. 1–7.
45. Catalano V., Bisonni R., Graziano F., Giordani P., Alessandroni P., Baldelli A.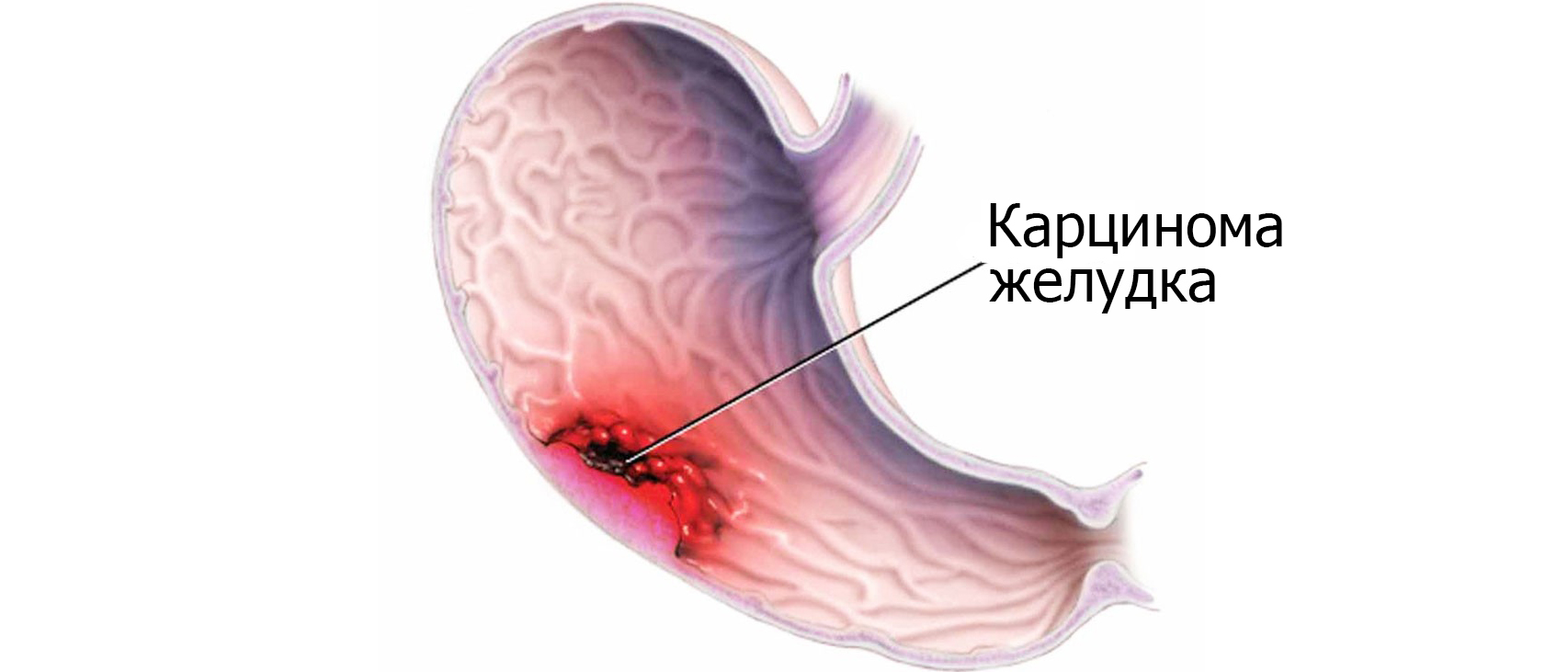 M. et al. A phase II study of modified FOLFOX as first-line chemotherapy for metastatic gastric cancer in elderly patients with associated diseases. Gastric Cancer. 2013. Vol. 16. P. 411–419.
M. et al. A phase II study of modified FOLFOX as first-line chemotherapy for metastatic gastric cancer in elderly patients with associated diseases. Gastric Cancer. 2013. Vol. 16. P. 411–419.
46. Nardi M., Azzarello D., Maisano R., Del Medico P., Giannicola R., Raffaele M. et al. FOLFOX-4 regimen as fist-line chemotherapy in elderly patients with advanced gastric cancer: a safety study. J. Chemother. 2007. Vol. 19. P. 85–89.
47. Kim H. S., Kim J. H., Kim H. J., Jang H. J., Kim J. B., Kim J. W. et al. Oxaliplatin, 5-fluorouracil and leucovorin (modified FOLFOX-6) as first-line chemotherapy for advanced gastric cancer patients with poor performance status. Oncol. Lett. 2012. Vol. 3. P. 425–428.
48. Cho Y. H., Kim S. Y., Hong Lee M., Yoo M. W., Bang H. Y. , Lee K. Y., Yoon S. Y. Comparative analysis of the efficacy and safety of chemotherapy with oxaliplatin plus fluorouracil / leucovorin between elderly patients over 65 years and younger patients with advanced gastric cancer. Gastric Cancer. 2012. Vol. 15. P. 389–395.
, Lee K. Y., Yoon S. Y. Comparative analysis of the efficacy and safety of chemotherapy with oxaliplatin plus fluorouracil / leucovorin between elderly patients over 65 years and younger patients with advanced gastric cancer. Gastric Cancer. 2012. Vol. 15. P. 389–395.
49. Al-Batran S. E., Pauligk C., Homann N., Hartmann J. T., Moehler M., Probst S. et al. The feasibility of triple-drug chemotherapy combination in older adult patients with oesophagogastric cancer: a randomised trial of the Arbeitsgemeinschaft Internistische Onkologie (FLOT65+). Eur. J. Cancer. 2013. Vol. 49. P. 835–842.
50. Kang Y. K., Kang W. K., Shin D. B., Chen J., Xiong J., Wang J. et al. Capecitabine / cisplatin versus 5-fluorouracil / cisplatin as first-line therapy in patients with advanced gastric cancer: a randomised phase III noninferiority trial. Ann. Oncol. 2009. Vol. 20. P. 666–673.
2009. Vol. 20. P. 666–673.
51. Okines A. F., Norman A. R., McCloud P., Kang Y. K., Cunningham D. Meta-analysis of the REAL-2 and ML17032 trials: evaluating capecitabine-based combination chemotherapy and infused 5-fluorouracil-based combination chemotherapy for the treatment of advanced oesophago-gastric cancer. Ann. Oncol. 2009. Vol. 20. P. 1529–1534.
52. Boku N., Yamamoto S., Fukuda H., Shirao K., Doi T., Sawaki A. et al. Fluorouracil versus combination of irinotecan plus cisplatin versus S-1 in metastatic gastric cancer: a randomised phase 3 study. Lancet Oncol. 2009. Vol. 10. P. 1063–1069.
53. Ajani J. A., Rodriguez W., Bodoky G., Moiseyenko V., Lichinitser M., Gorbunova V. et al. Multicenter phase III comparison of cisplatin / S-1 with cisplatin / infusional fluorouracil in advanced gastric or gastroesophageal adenocarcinoma study: the FLAGS trial. J. Clin. Oncol. 2010. Vol. 28. P. 1547–1553.
J. Clin. Oncol. 2010. Vol. 28. P. 1547–1553.
54. Lee J. L., Kang Y. K., Kang H. J., Lee K. H., Zang D. Y., Ryoo B. Y. et al. A randomized multicentre phase II trial of capecitabine vs S-1 as first-line treatment in elderly patients with metastatic or recurrent unresectable gastric cancer. Br. J. Cancer. 2008. Vol. 99. P. 584–590
55. Hwang I. G., Lee H. R., Lee H. Y., Ji J. H., Kang J. H., Lee S. I. et al. First-line capecitabine (X) monotherapy versus capecitabine plus oxaliplatin (XELOX) in elderly patients with advanced gastric cancer (AGC): results from the first interim analysis. J. Clin. Oncol. 2015. Vol. 33 (suppl). abstr4051.
56. Koizumi W., Akiya T., Sato A., Sakuyama T., Sasaki E., Tomidokoro T. et al. Phase II study of S-1 as first-line treatment for elderly patients over 75 years of age with advanced gastric cancer: the Tokyo Cooperative Oncology Group study. Cancer Chemother. Pharmacol. 2010. Vol. 65. P. 1093–1099.
Cancer Chemother. Pharmacol. 2010. Vol. 65. P. 1093–1099.
57. Petrioli R., Pascucci A., Francini E., Marsili S., Fiaschi A. I., Civitelli S. et al. Continuous oral capecitabine at fixed dose in patients older than 75 years with metastatic colorectal and gastric cancer: a study of the Multidisciplinary Oncology Group on Gastrointestinal Tumors. Anticancer Drugs. 2008. Vol. 19. P. 91–96.
58. Bang Y. J., Van Cutsem E., Feyereislova A., Chung H. C., Shen L., Sawaki A. et al. ToGA Trial Investigators. Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA): a phase 3, open-label, randomized controlled trial. Lancet. 2010. Vol. 376. P. 687–697.
59. Fuchs C.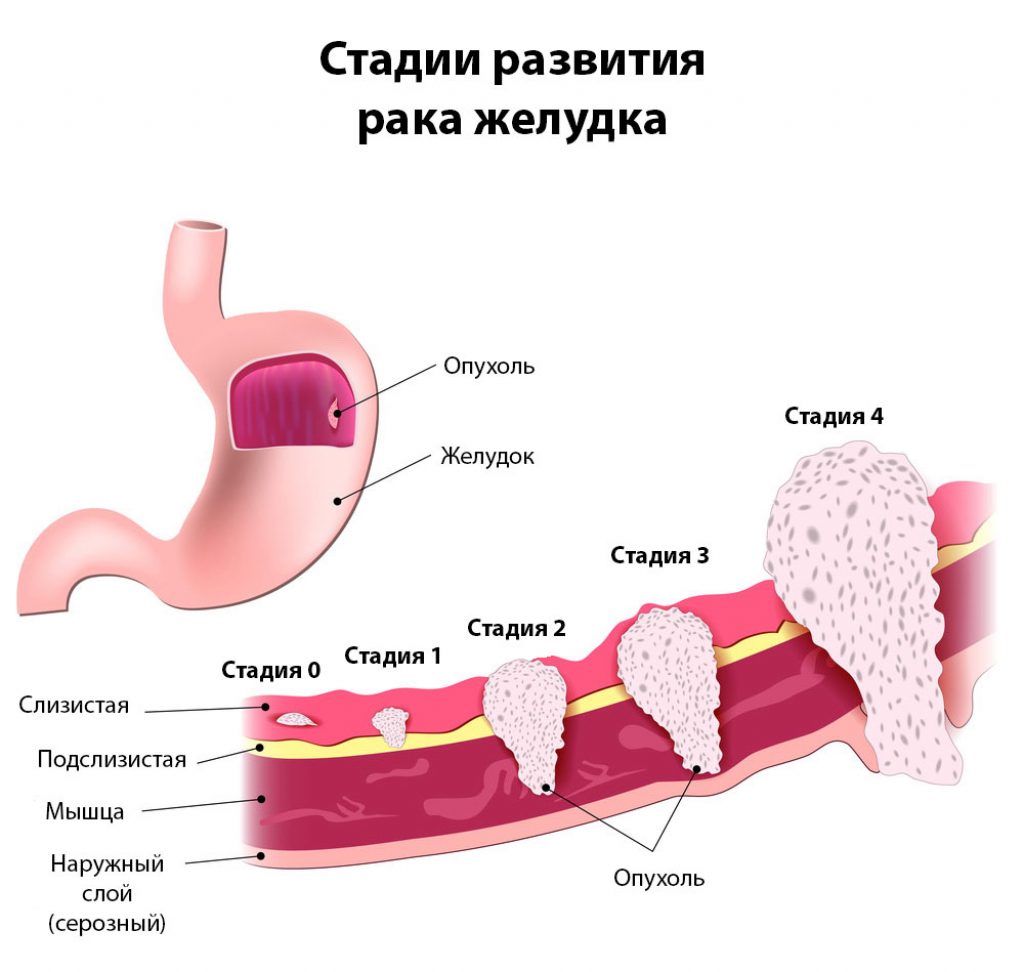 S., Tomasek J., Yong C. J., Dumitru F., Passalacqua R., Goswami C. et al. Ramucirumab monotherapy for previously treated advanced gastric or gastrooesophageal junction adenocarcinoma (REGARD): an international, randomised, multicentre, placebocontrolled, phase 3 trial. Lancet. 2014. Vol. 383. P. 31–39.
S., Tomasek J., Yong C. J., Dumitru F., Passalacqua R., Goswami C. et al. Ramucirumab monotherapy for previously treated advanced gastric or gastrooesophageal junction adenocarcinoma (REGARD): an international, randomised, multicentre, placebocontrolled, phase 3 trial. Lancet. 2014. Vol. 383. P. 31–39.
60. Wilke H., Muro K., Van Cutsem E., Oh S. C., Bodoky G., Shimada Y. et al. Ramucirumab plus paclitaxel versus placebo plus paclitaxel in patients with previously treated advanced gastric or gastro-oesophageal junction adenocarcinoma (RAINBOW): a double-blind, randomised phase 3 trial. Lancet Oncol. 2014. Vol. 15. P. 1224–1235.
61. Van Cutsem E., Moiseyenko V. M., Tjulandin S. et al. Phase III study of docetaxel and cisplatin plus fluorouracil compared with cisplatin and fluorouracil as first-line therapy for advanced gastric cancer: a report of the V325 Study Group. J. Clin. Oncol. 2006. Vol. 24. P. 4991–4997.
J. Clin. Oncol. 2006. Vol. 24. P. 4991–4997.
62. Ajani J. A., Moiseyenko V. M., Tjulandin S. et al. Quality of life with docetaxel plus cisplatin and fluorouracil compared with cisplatin and fluorouracil from a phase III trial for advanced gastric or gastroesophageal adenocarcinoma: the V-325 Study Group. J. Clin. Oncol. 2007. Vol. 25. P. 3210–3216.
63. Ilson D. H. Docetaxel, cisplatin, and fluorouracil in gastric cancer: does the punishment fit the crime? J. Clin. Oncol. 2007. Vol. 25 (22). P. 3188–3190.
64. Cunningham D., Starling N., Rao S. et al. Capecitabine and oxaliplatin for advanced esophagogastric cancer. N. Engl. J. Med. 2008. Vol. 358 (1). P. 36–46.
Рак желудка — симптомы и признаки
Содержание статьи:
Рак желудка – злокачественная опухоль, формирующаяся из клеток внутреннего слизистого слоя желудочной стенки. По мере увеличения она прорастает в средний мышечный и внешний серозный слои, соседние и отдаленные органы.Чаще возникает у мужчин. Средний возраст больных – 38 лет.
По мере увеличения она прорастает в средний мышечный и внешний серозный слои, соседние и отдаленные органы.Чаще возникает у мужчин. Средний возраст больных – 38 лет.
Патология занимает 3 место в мире по уровню смертности от онкозаболеваний: ежегодно от нее умирает 800 000 человек.По статистике выздоравливают 30% пациентов с раком желудка.Метастазы выявляют у 80-90% больных. При ранней диагностике 6-месячная выживаемость – 65%, при поздней – 15%. На практике чаще выявляется на 4-й стадии. У 1 из 50 больных с диспепсией диагностируют рак желудка.
Причины рака желудка и факторы риска
На вероятность возникновения заболевания влияют:
- наличие близких родственников с раком желудка в анамнезе;
- полипы желудка или аденоматозный полипоз;
- язвенная болезнь и хронический гастрит;
- повышенный уровень Helicobacter Pilory;
- дуодено-гастральный рефлюкс;
- кишечная метаплазия – замещение желудочного эпителия кишечным;
- неправильное питание – большое количество соленой, острой и копченой пищи, животных жиров, низкое содержание овощей и фруктов;
- недостаток витамина С;
- употребление низкокачественных и просроченных продуктов;
- курение и избыточное потребление алкоголя;
- возраст старше 60 лет, особенно у мужчин;
- срок 5-10 лет после операции на желудке.

Наличие факторов риска не означает, что вы точно заболеете. Отсутствие факторов риска не означает, что вы точно не заболеете.
Виды рака желудка
В зависимости от типа клеток опухоли различают плоскоклеточный и железистый рак – аденокарциному. Плоскоклеточный рак развивается из клеток слизистой пищевода, локализуется в верхнем отделе желудка и встречается редко – примерно у 1% пациентов группы.
Аденокарцинома развивается из клеток слизистой желудка в любой части органа. По строению бывает тубулярной, папиллярной и муцинозной.
Стадии
По степени злокачественности и распространенности процесса различают стадии заболевания:
- 0 – единичные атипичные клетки обнаруживают только в верхнем слое слизистой желудка;
- I – клетки опухоли поражают слизистый и подслизистый слои желудочной стенки.
I стадия делится на подстадии:
- IА – поражен только подслизистый слой;
- IВ – поражен также мышечный слой желудка, выявлены метастазы в 1-2 близлежащих лимфоузлах.

IIстадия делится на подстадии:
- IIA – опухоль распространяется:
- на подслизистый или мышечный слои желудочной стенки, в 1-2 близлежащих лимфоузлах выявлены метастазы;
- подслизистый слой с метастазами в 3-6 близлежащих лимфоузлах.
- IIB – опухоль распространяется:
- на внешний слой желудочной стенки;
- субсерозный слой ткани под внешней оболочкой с метастазами в 1-2 близлежащих лимфоузлах;
- мышечный слой желудочной стенки с метастазами в 3-6 близлежащих лимфоузлах;
- подслизистый слой желудочной стенки с метастазами в 7 или более близлежащих лимфоузлах.
III стадия делится на подстадии:
- IIIA – опухоль распространяется:
- на внешний слой желудочной стенки с метастазами в1-2 близлежащих лимфоузлах;
- серозный слой ткани под внешней оболочкой с метастазами в 3-6 близлежащих лимфоузлах;
- мышечный слой желудочной стенки с метастазами в 7 или более близлежащих лимфоузлах.

- IIIB – опухоль прорастает:
- в близлежащие органы – селезенку, печень, диафрагму, почку, надпочечник, поджелудочную железу, поперечно-ободочную или тонкую кишку с метастазами в 1-2 близлежащих лимфоузла;
- во внешний слой желудочной стенки с метастазамив 3-6 близлежащих лимфоузлах.
- IIIC– опухоль прорастает:
- в близлежащие органы – селезенку, печень, диафрагму, почку, надпочечник, поджелудочную железу, поперечно-ободочную или тонкую кишку с метастазами в 3 и более лимфоузла;
- во внешний слой желудочной стенки с метастазами в 7 и более близлежащих лимфоузла.
- IV– опухоль за счет метастазирования распространяется в отдаленные органы и ткани – печень, яичники, надключичные лимфоузлы и т.п.
Основные симптомы
Первые признаки заболевания – дискомфорт и боль в области желудка, диспепсия. Кроме них на ранних стадиях возникают Источник:
Бессимптомное течение рака желудка.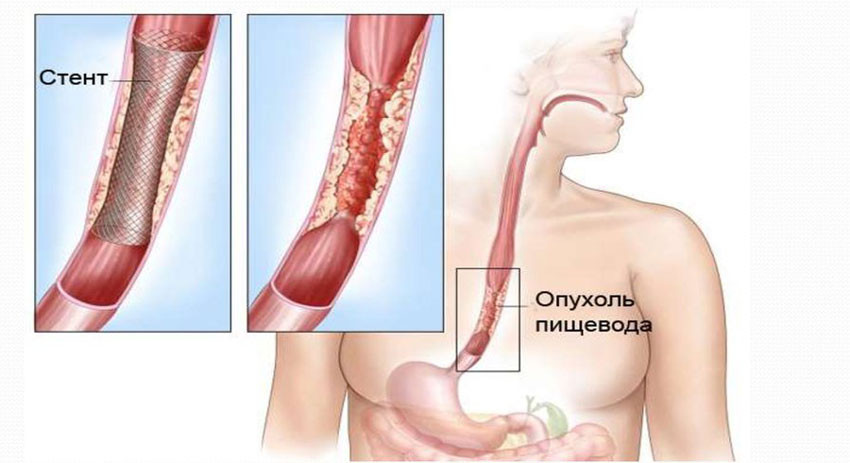 Шут.С.А., Платошкин Э.Н., Дорогокупец А.Ю.: Проблемы здоровья и экологии, 2019 г.:
Шут.С.А., Платошкин Э.Н., Дорогокупец А.Ю.: Проблемы здоровья и экологии, 2019 г.:
- изжога;
- тошнота;
- снижение аппетита;
- ощущение вздутия после еды;
- дискомфорт в верней части живота;
- повышенная утомляемость, слабость.
На более поздних стадиях симптомы рака желудка:
- рвота;
- кал черного цвета;
- отрыжка;
- чувство переполненного желудка;
- боли в животе;
- желтуха;
- асцит – увеличение объема живота из-за скопления жидкости;
- потеря веса.
Без лечения возможны осложнения рака желудка – кровотечения, перфорация опухоли, желудочная непроходимость, флегмона.
Диагностика
Чтобы поставить диагноз, проводят эндоскопическое исследование желудка ЭГДС. Через рот и пищевод вводят зонд с миниатюрной видеокамерой и источником света. Процедура позволяет выявлять местоположение опухоли. В ходе ее выполнения также делают биопсию– забор образца тканей для гистологического анализа. Диагноз подтверждают только после исследования тканей опухоли под микроскопом.
В ходе ее выполнения также делают биопсию– забор образца тканей для гистологического анализа. Диагноз подтверждают только после исследования тканей опухоли под микроскопом.
Для определения точных размеров новообразования проводят КТ, иногда – с контрастным усилением. Для оценки распространенности процессов, состояния лимфоузлов и выявления метастазов назначают УЗИ. Для уточнения специфических характеристик опухоли делают рентгенографию с препаратами бария.
Уточняющая диагностика помогает выбирать наиболее эффективную лечебную тактику. Так, исследование крови на мутацию гена HER2/neuпомогает подобрать наиболее эффективныепротивоопухолевыепрепараты.Кроме этого, назначают:
- анализы на онкомаркеры РЭА и СА-19,9;
- внутрижелудочное УЗИ;
- позитронно-эмиссионную томографию (ПЭТ).
Методы лечения
Основной метод лечения рака желудка – хирургический. Лучевую и химиотерапию проводят дополнительно для повышения эффективности лечения Источник:
Комбинированное лечение рака желудка. Афанасьев С.Г., Тузиков С.А., Давыдов И.М.: Сибирский онкологический журнал, 2015 г.. В качестве монометодик при раке желудка они малоэффективны и назначаются, если операция противопоказана.
Афанасьев С.Г., Тузиков С.А., Давыдов И.М.: Сибирский онкологический журнал, 2015 г.. В качестве монометодик при раке желудка они малоэффективны и назначаются, если операция противопоказана.
Хирургическое лечение
Хирургическое лечение проводят на всех стадиях рака желудка: на ранних для радикального удаления опухоли и полного восстановления пациента, на поздних –чтобы улучшить качество жизни больного и уменьшать выраженность симптоматики.Объем операции зависит от злокачественности и распространенностиновообразования, возраста и состояния здоровья пациента Источник:
Хирургическое лечение рака желудка. Рахов С.Б.:Вестник Казахского Национального медицинского университета, 2012 г..
Гастрэктомия – удаление всего желудка с опухолью, окружающей жировой клетчаткой и регионарными лимфоузлами. В ходе вмешательство возможна частичная либо полная резекция пораженных соседних органов. После иссечения формируют искусственное соустье – аностомоз – между пищеводом и тонким кишечником.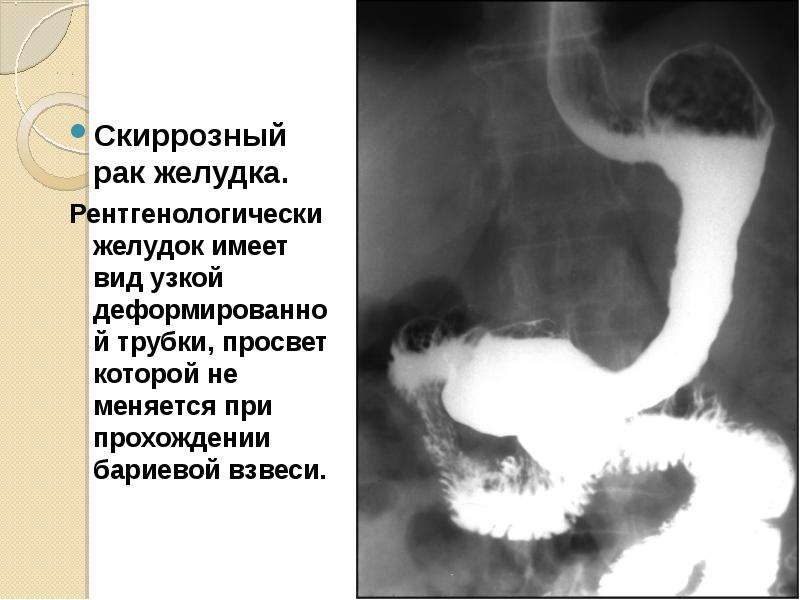
Резекция желудка дистальная либо проксимальная – удаление пораженной верхней либо нижней части с клетчаткой и регионарными лимфоузлами.
Эндоскопическая резекция желудочной слизистой – удаление пораженного участка слизистой через проколы без разрезов. Эффективна на начальной стадии онкопроцесса, а также у пожилых и ослабленных больных, которым из-за состояния противопоказана полноценная операция.
Паллиативное стентирование – установка специального стента, обеспечивающего просвет желудка. Показано больным на поздних стадиях для обеспечения беспрепятственного пищеварения.
Гастроэнтероаностомоз – паллиативная хирургическая помощь для восстановления просвета выходного отверстия из желудка в кишечник.
Химиотерапия
Лечение с помощью лекарственных препаратов, разрушающих раковые клетки либо блокирующих их деление. Введение одновременно нескольких таких медикаментов – полихимиотерапия – позволяет снизить дозировки каждого их них и негативные побочные эффекты лечения, повысить его эффективность. Назначается перед хирургической операцией либо после нее.
Назначается перед хирургической операцией либо после нее.
Лучевая терапия
Использование рентгеновских лучей для разрушения клеток опухоли или замедления ее роста. Показано до или после операции, при метастазах в лимфоузлах, на поздних стадиях и при невозможностихирургическоголечения. Для точной фокусировки (чтобы убивать опухоль, не воздействуя на близлежащие ткани)используют КТ-разметку.
Прогноз заболевания
Прогноз зависит от стадии онкопроцесса – насколько обширно и глубоко поражена желудочная стенка, поражены ли лимфоузлы и есть ли метастазы, а также от возраста и общего состояния здоровья пациента. При ранней диагностике и качественном лечении шанс на полное выздоровление значительно выше.
Пятилетняя выживаемость:
- у пациентов с 1-й стадией – 80%, из них 70% полностью выздоравливают;
- у больных со 2-й стадией – 56%, из них полностью выздоравливает 50%;
- у пациентов с 3-й стадией – 38%, из них полностью выздоравливает 25%;
- у больных с 4-й стадией – 5%, из них полностью выздоравливают 1,4%.

Если пациент прожил 5 лет после окончания лечения рака желудка, дальнейший прогноз улучшается. Риск рецидива зависит от стадии и обширности метастаз. Он выше через 2 года и снижается после 5-летней ремиссии.
Профилактика
- Сбалансированный рацион с преобладанием фруктов и овощей.
- Отказ от курения и злоупотребления алкоголем.
- Современное лечение болезней желудка – в частности HelicobacterPilory – с последующим врачебным наблюдением.
Важны также регулярные профилактические осмотры и скриниг людей с генетической и наследственной предрасположенностью к заболеванию. Чтобы проконсультироваться у профильного специалиста в СПб, заполните форму онлайн.
Источники:
- Бессимптомное течение рака желудка. Шут.С.А., Платошкин Э.Н., Дорогокупец А.Ю.: Проблемы здоровья и экологии, 2019 г.
- Комбинированное лечение рака желудка. Афанасьев С.Г., Тузиков С.А., Давыдов И.М.: Сибирский онкологический журнал, 2015 г.

- Хирургическое лечение рака желудка. Рахов С.Б.:Вестник Казахского Национального медицинского университета, 2012 г.
- Иммунотерапия рака желудка. Мансорунов Д.Ж., Алимов А.А., Апанович Н.В., Кузеванова А.Ю., Богуш Т.А., Стилиди И.С., Карпухин А.В.: Российский биотерапевтический журнал, 2019 г.
Информация в статье предоставлена в справочных целях и не заменяет консультации квалифицированного специалиста. Не занимайтесь самолечением! При первых признаках заболевания необходимо обратиться к врачу.
Читайте также
Рак желудка у молодых и пожилых пациентов — разные заболевания
Рак желудка у людей в возрасте до 60 лет существенно отличается генетически и клинически от заболевания, которое развивается у пожилых людей. О его особенностях рассказывает исследование, опубликованное в журнале Surgery. Форма болезни с ранним началом часто быстрее развивается и распространяется, имеет худший прогноз и более устойчива к стандартному лечению рака.
Рак желудка у людей в возрасте до 60 лет как генетически, так и клинически существенно отличается от заболевания, которое развивается у пожилых людей. О его особенностях рассказывает исследование, опубликованное в журнале Surgery. Форма заболевания с ранним началом часто быстрее развивается и распространяется, имеет худший прогноз и более устойчива к стандартному лечению рака.
За последние несколько десятилетий уровень заболеваемости раком желудка среди пожилых людей снизился, отмечают американские согласно данным, которые получены в США. В то же время количество случаев рака с ранним началом, напротив, растет.
«Я думаю, это тревожная тенденция, поскольку рак желудка является тяжелым заболеванием. Люди мало что знают о признаках и симптомах рака желудка, и многие молодые пациенты могут пройти диагностику поздно, когда лечение менее эффективно», – рассказал старший автор исследования Трэвис Гротц (Travis Grotz).
Ученые из клиники Мэйо, используя несколько баз данных, рассмотрели 75225 случаев рака желудка и получили статистику за 1973-2015 годы. Они выяснили, что в настоящее время в среднем рак желудка диагностируется в 68 лет, но у людей 30-50 лет он развивается все чаще.
Они выяснили, что в настоящее время в среднем рак желудка диагностируется в 68 лет, но у людей 30-50 лет он развивается все чаще.
Исследование показало, что заболеваемость раком желудка среди пожилых людей уменьшилась на 1,9%. При этом каждый третий диагноз рака желудка ставится людям более молодого возраста.
Увеличение показателей заболеваемости связано не с ранним выявлением или скринингом. Универсального скрининга рака желудка не существует, поэтому в молодом возрасте он зачастую диагностируется на более поздней стадии заболевания по сравнению с пожилыми людьми.
Ученые отметили, что рак желудка с ранним началом не только опасен для жизни, но и отличается на молекулярном и генетическом уровне. Связи между возникновением этого вида рака желудка и другими факторами риска (в частности, табакокурением) обнаружено не было.
Современные методы диагностики и лечения рака желудка
Почти каждый второй пациент из числа тех, у кого был диагностирован рак желудка, погибает в течение года. Причина — позднее выявление. Можно ли обнаружить эту болезнь рано? Существуют программы скрининга (раннего выявления) рака молочной и предстательной желез, легкого, толстого кишечника, но существует ли скрининг рака желудка? О том, как диагностируют и лечат это заболевание, рассказывает доктор медицинских наук Владимир Лядов, заведующий отделением онкологии №4 Первой городской клинической онкологической больницы г. Москвы.
Причина — позднее выявление. Можно ли обнаружить эту болезнь рано? Существуют программы скрининга (раннего выявления) рака молочной и предстательной желез, легкого, толстого кишечника, но существует ли скрининг рака желудка? О том, как диагностируют и лечат это заболевание, рассказывает доктор медицинских наук Владимир Лядов, заведующий отделением онкологии №4 Первой городской клинической онкологической больницы г. Москвы.
Что такое TNM и как определяют стадию болезни.
Начну с хорошего: россияне стали болеть раком желудка реже. Если в начале нулевых каждый год в нашей стране им заболевало более 40 тысяч человек, то за последние 10 лет заболеваемость снизилась на 15 процентов. Но есть и плохое: только треть пациентов приходят к врачам на ранних стадиях болезни, 40 процентов — на 4 стадии. Поэтому летальность в течение года от установления диагноза — 46,6 процентов.
Мы подошли к очень важному понятию стадии. Чтобы оценить, насколько далеко зашла болезнь, врачам нужны всего три буквы: T, N, M.
T– tumor, опухоль. Не так важно, каков рак по площади на стенке желудка, – главное, насколько глубоко образование проросло в стенку желудка, вышло ли оно за пределы органа. От этого зависит возможность клеток рака распространяться по организму и поражать лимфатические узлы (N) или же другие органы (метастазы, или отсевы опухоли, которые обозначаются буквой M). Поражение метастазами других органов говорит о 4 стадии рака желудка – ситуации, которую мы не должны допускать.
В зависимости от стадии выбирается тактика лечения, схема, которую предлагает врач. Допустим, 25 тысяч пациентов были пролечены одинаково, им была выполнена качественная операция. От стадии зависит, сколько из них выживут через пять лет. На первой стадии — почти все (хотя пациент, к сожалению, может погибнуть не только от рака желудка, но и от других болезней). Для более запущенных стадий характерны отсевы в другие органы, значит мы, врачи, должны предложить более интенсивное лечение.
Что показывает анализ крови на пепсиногены
Национальной программы скрининга рака желудка в нашей стране нет. Каждый человек должен оценивать собственные риски. Метод оценки — гастроскопия, осмотр желудка изнутри. А в Японии, где пациентов, страдающих раком желудка в 3-4 раза больше, чем в России, внедрен анализ крови на пепсиногены, который проводится и в российских лабораториях. Соотношение пепсиногенов I и II– проферментов, которые образуются в слизистой желудка – позволяет определить, насколько высока вероятность развития у пациента опухоли. Если соотношение не очень благоприятное, в любом случае проводится гастроскопия. Но при благоприятном результате теста необходимость проходить гастроскопию значительно меньше.
Для людей, которые не хотят периодически глотать гастроскоп, а также для врачей пепсиногеновый тест – это возможность получить информацию о риске развития злокачественной опухоли желудка у конкретного человека.
На сегодняшний день российские рекомендации таковы: пациенту, у которого есть жалобы со стороны желудка, нужно выполнить гастроскопию и биопсию опухоли, если таковая обнаружена.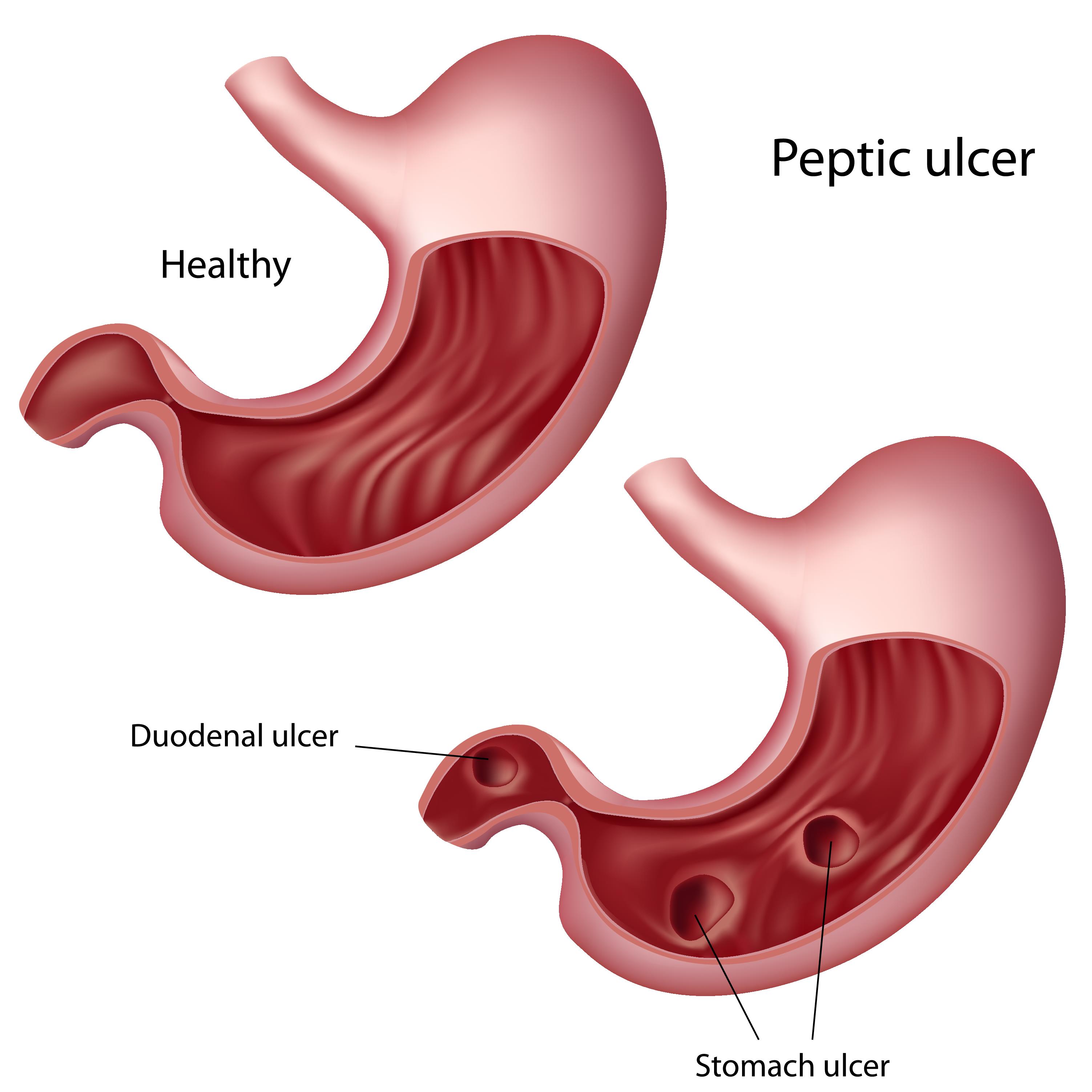 Ему так же выполняется КТ — не УЗИ и не рентгенография! — грудной клетки, брюшной полости и малого таза, то есть визуализируются все части тела, где могут быть отсевы опухоли. И, наконец, для большинства пациентов с достаточно значимыми по размеру опухолями проводится диагностическая лапароскопия. Это маленькая операция под наркозом, прокол брюшной стенки, в ходе которой врач оценивает, нет ли мелких отсевов опухоли, которые не видны на КТ или ПЭТ. Под микроскопом проводится исследование смыва с брюшины, то есть стерильного раствора, который вводят в брюшную полость и забирают обратно. Если выясняется, что в брюшной полости есть клетки рака желудка, пациента категорически нельзя оперировать. Диагностическая лапароскопия позволяет выявить такие метастазы у 20% пациентов. Раньше таким пациентам выполнялись операции, которые заканчивались либо диагностическим разрезом на животе, либо быстрым, в течение нескольких месяцев, развитием метастазов. Теперь в подобных ситуациях лечение начинают с химиотерапии.
Ему так же выполняется КТ — не УЗИ и не рентгенография! — грудной клетки, брюшной полости и малого таза, то есть визуализируются все части тела, где могут быть отсевы опухоли. И, наконец, для большинства пациентов с достаточно значимыми по размеру опухолями проводится диагностическая лапароскопия. Это маленькая операция под наркозом, прокол брюшной стенки, в ходе которой врач оценивает, нет ли мелких отсевов опухоли, которые не видны на КТ или ПЭТ. Под микроскопом проводится исследование смыва с брюшины, то есть стерильного раствора, который вводят в брюшную полость и забирают обратно. Если выясняется, что в брюшной полости есть клетки рака желудка, пациента категорически нельзя оперировать. Диагностическая лапароскопия позволяет выявить такие метастазы у 20% пациентов. Раньше таким пациентам выполнялись операции, которые заканчивались либо диагностическим разрезом на животе, либо быстрым, в течение нескольких месяцев, развитием метастазов. Теперь в подобных ситуациях лечение начинают с химиотерапии.
Как лечат рак желудка на разных стадиях
Если при обследовании у пациента выявлен полип — предраковое состояние, или диагностирована ранняя форма рака желудка, то во многих ситуациях можно обойтись без операции с разрезами на брюшной стенке, и выполнить эндоскопическое вмешательство. В этом случае удаление образования происходит через просвет желудка с помощью гастроскопа. Если опухоль более распространенная, но метастазы в других органах отсутствуют, то основой лечения будет хирургия, чаще в сочетании с химиотерапией. Лекарственное лечение на сегодняшний день также требуется подавляющему большинству пациентов на 4 стадии процесса, то есть при наличии метастазов в других органах.
Давайте посмотрим, какие методы используются в зависимости от стадии рака желудка.
На 1 стадии применяются эндоскопия и хирургия. Первая — если образование очень небольшое, имеет благоприятную структуру. Если оно чуть больше, чуть глубже проросло в стенку желудка, проводится его хирургическое удаление, чаще всего лапароскопически через проколы.
Если оно чуть больше, чуть глубже проросло в стенку желудка, проводится его хирургическое удаление, чаще всего лапароскопически через проколы.
На 2 стадии, когда опухоль глубже проросла в стенку желудка или имеется поражение 1-2 лимфоузлов, используется хирургия, нередко в сочетании с химиотерапией.
3 стадия — это прорастание насквозь стенки желудка и/или поражение нескольких лимфатических узлов. Обычно в таких случаях мы используем схему с назначением лекарственного лечения и до операции, и после нее.
На 4 стадии крайне редко используется хирургический метод лечения. Терапия лекарственная – используются химиотерапевтические препараты, у некоторых пациентов эффективна таргетная или иммунотерапия.
Чем больше манипуляций проводить с опухолью, чем больше касаться ее, тем больше клеток может попасть в брюшную полость. В Южной Корее проводились специальные исследования, которые показали, что сама операция при грубом исполнении может быть дополнительным негативным фактором распространения опухолевых клеток, поэтому она должна выполняться максимально аккуратно, с помощью современных инструментов для заваривания лимфатических и обычных сосудов, чтобы уменьшить вероятность распространения клеток рака. В том числе по этой причине малоинвазивные операции через проколы стремительно становятся стандартом современной хирургической онкологии. Проведены большие исследования, показавшие, что такая хирургия также эффективна в плане лечения рака желудка, в том числе распространенных опухолей, но сопровождается меньшим числом осложнений. Подобные операции показаны и больным старческого возраста.
В том числе по этой причине малоинвазивные операции через проколы стремительно становятся стандартом современной хирургической онкологии. Проведены большие исследования, показавшие, что такая хирургия также эффективна в плане лечения рака желудка, в том числе распространенных опухолей, но сопровождается меньшим числом осложнений. Подобные операции показаны и больным старческого возраста.
Система FLOT: когда лечение начинается с химиотерапии
Отнюдь не всегда операция позволяет вылечить пациента. Если у пациента опухолевые клетки имеются в крови и других органах, а такая ситуация характерна для II-III ст. рака желудка, ему требуется химиотерапия, которая позволяет воздействовать на них. К сожалению, иногда бывают и очень агрессивные, неблагоприятные формы рака — в том числе желудка. В этом случае, когда опухоль быстро развивается, операция может быть гибельна для пациента, поскольку ускорит развитие рака. Для решения задачи лечения таких пациентов разработано несколько вариантов химиотерапии, среди которых наибольшая эффективность у комбинации FLOT: это сочетание 4-х препаратов, которое довольно хорошо переносится и позволяет в сочетании с операцией намного улучшить результаты лечения. В ходе больших сравнительных испытаний в Германии были получены данные о том, что применение схемы FLOT почти в два раза увеличивает выживаемость пациентов. Если раньше пациенты с местно-распространенными формами рака желудка могли в среднем прожить 2-3 года, то сейчас мы стремимся к средним показателям более 4 лет, при этом многие пациенты имеют шанс полностью вылечиться.
В ходе больших сравнительных испытаний в Германии были получены данные о том, что применение схемы FLOT почти в два раза увеличивает выживаемость пациентов. Если раньше пациенты с местно-распространенными формами рака желудка могли в среднем прожить 2-3 года, то сейчас мы стремимся к средним показателям более 4 лет, при этом многие пациенты имеют шанс полностью вылечиться.
Есть и новые технологии — хирургия с помощью робота, которая потенциально еще точнее, чем лапароскопическая хирургия, лучевая терапия, которая пока не так часто используется при раке желудка, но все же появились определенные точки приложения и для новых радиохирургических методик. Мы видим колоссальный сдвиг в лечении многих опухолей за счет так называемой иммунотерапии: появился способ дать клеткам иммунной системы возможность распознать клетки опухоли как чужеродные и бороться с ними. При раке желудка этот метод работает пока лишь у отдельных пациентов, но тем не менее некоторым пациентам этот метод позволяет радикальным образом продлить жизнь. Еще недавно у нас в арсенале было 2 химиопрепарата для терапии рака желудка, а сегодня мы имеем уже 7-8 различных препаратов с доказанной эффективностью.
Еще недавно у нас в арсенале было 2 химиопрепарата для терапии рака желудка, а сегодня мы имеем уже 7-8 различных препаратов с доказанной эффективностью.
Рак желудка — распространенная болезнь. Но она хорошо поддается лечению при выявлении на ранних этапах. У многих пациентов есть все шансы вылечиться — это важно понимать и помнить, и ни в коем случае не отказываться от лечения, как иногда, к сожалению, бывает даже при вполне излечимых формах рака. Лучший способ профилактики — здоровый образ жизни с отказом от курения и любой физической активностью. Лучший способ диагностики — гастроскопия. Если все же обнаружен рак желудка, успешное лечение возможно – в современных специализированных центрах, где есть команда опытных врачей, способная предложить пациенту весь спектр методов лечения и правильно их применить.
Рак желудка
Рак желудка – это злокачественная опухоль, образующаяся из клеток желудка.
Это один из самых распространенных видов рака. Чаще всего он появляется в пожилом возрасте, причем мужчины заболевают в 2 раза чаще, чем женщины.
Успешность терапии зависит от типа рака и стадии, на которой он был выявлен. Основной метод лечения – удаление части или всего желудка.
Синонимы русские
Аденокарцинома желудка, карцинома желудка.
Синонимы английские
Stomach cancer, gastric cancer.
Симптомы
На ранних стадиях рак желудка часто протекает незаметно. Проявление большинства симптомов с высокой вероятностью указывает на запущенность заболевания.
Симптомы рака желудка:
- боль и дискомфорт в верхней части живота,
- тяжесть, вздутие, чувство переполнения живота,
- чувство быстрого насыщения,
- тошнота, рвота,
- изжога,
- отрыжка,
- потеря массы тела,
- изменения характера вкусовых предпочтений, отсутствие аппетита,
- слабость, утомляемость.
Общая информация о заболевании
Рак желудка – это злокачественная опухоль в области желудка.
Желудок – орган в виде мышечного мешка, который является «резервуаром» для поступающей пищи, вырабатывает желудочный сок и в небольшой степени выполняет функцию всасывания.
При раке здоровые клетки превращаются в измененные, раковые. В норме клетки, появляясь в нужном количестве, в определенное время отмирают, уступая место новым. Раковые же клетки начинают бесконтрольно размножаться, не отмирая в положенное время, и их скопления образуют опухоль.
Также раковые клетки могут распространяться в близлежащие ткани организма и образовывать метастазы (метастазировать). Рак желудка часто метастазирует в лимфатические узлы, находящиеся рядом с яичниками (у женщин), левой ключицей, прямой кишкой, а также в печень и другие органы.
На данный момент причины рака желудка не установлены. Он может быть связан с такими факторами, как употребление большого количества соленых, маринованных, копченых продуктов, курение, инфекция хеликобактер пилори, наследственная предрасположенность, язва желудка, атрофический гастрит, ожирение, полипы.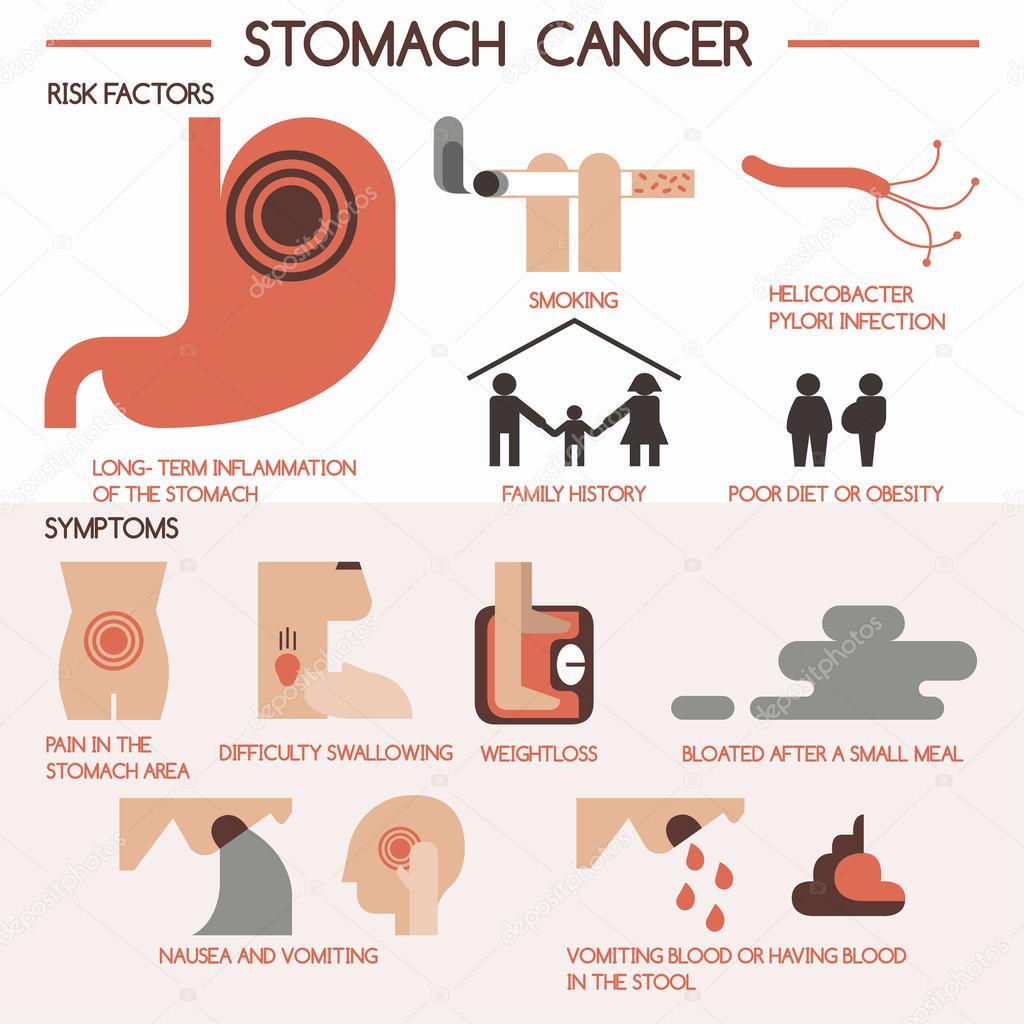 Одновременное воздействие нескольких факторов значительно увеличивает риск развития рака желудка.
Одновременное воздействие нескольких факторов значительно увеличивает риск развития рака желудка.
В зависимости от типа клеток, перерождающихся в раковые, выделяются основные типы рака желудка.
- Аденокарцинома – мутация железистых клеток эпителия, выстилающих внутреннюю поверхность желудка и вырабатывающих слизь для защиты от соляной кислоты. Это самый распространенный тип.
- Лимфома – в раковые перерождаются клетки иммунной системы, в небольшом количестве имеющиеся в стенках желудка. Встречается редко.
- Карциноидный рак желудка. В данном случае рак развивается из клеток, выделяющих гормоны. Также встречается нечасто.
Стадии развития рака желудка
1. Раковая опухоль небольшого размера находится в пределах верхнего слоя клеток, выстилающих внутреннюю поверхность желудка. Раковые клетки могут распространяться на некоторые близлежащие лимфатические узлы.
2. Рак распространяется глубже, поражая мышечную оболочку стенки желудка, иногда лимфатические узлы.
3. Рак поражает все слои желудка или распространяется на большое количество лимфатических узлов.
4. Раковая опухоль увеличивается. Рак распространяется на лимфатические узлы, печень, кишечник, поджелудочную железу и другие близлежащие органы; могут поражаться и отдаленные участки.
Кто в группе риска?
- Курящие.
- Страдающие ожирением.
- Лица с наследственной предрасположенностью к раку желудка.
- Инфицированные бактерией хеликобактер пилори. Она присутствует в желудке большого количества людей, в большинстве случаев бессимптомно.
- Перенесшие операции на желудке.
- Пациенты с язвой, с полипами желудка.
- Страдающие атрофическим гастритом, В12-дефицитной анемией.
Диагностика
В большинстве случаев рак желудка выявляется на поздних стадиях. При подозрении нанего проводится полный комплекс всех доступных исследований для подтверждения диагноза, составления прогноза заболевания и выбора стратегии лечения.
Лабораторные исследования:
Другие методы обследования
- Фиброгастродуоденоскопия (ФГДС) – через горло в желудок проводится тонкая трубка с объективом (эндоскопом). Производится биопсия – взятие клеток с измененных участков слизистой желудка для их последующего изучения под микроскопом. Именно биопсия позволяет определить тип рака.
- Рентгенография желудка. Пациент выпивает барий – вещество, которое видно на рентгеновских снимках. Попадая в желудок, он обволакивает складки слизистой, за счет чего возникает возможность оценить рельеф желудка, его контуры – при раке они изменяются.
- Компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) помогают обнаружить опухоль в желудке, определить ее размеры, расположение, а также наличие метастазов.
- Лапароскопия – обследование желудка через отверстия в брюшной стенке величиной 0,5-1,5 см, в которые вводится трубка с камерой. Лапароскопия позволяет осмотреть органы брюшной полости, выявить метастазы, осуществить биопсию.

- Эндоскопическое УЗИ используют, чтобы определить глубину проникновения опухоли и выявить метастазы в лимфатических узлах.
Лечение
- Хирургия. Целью операции является удаление раковой опухоли и минимального количества окружающих здоровых тканей. В зависимости от распространенности рака хирургическая операция может включать:
- Удаление раковой опухоли небольшого размера. Данная операция проводится на ранней стадии.
- Субтотальную резекцию желудка — удаление части желудка, пораженной раком.
- Тотальную гастрэктомию — удаление всего желудка. В ходе операции также удаляются окружающие здоровые ткани.
- Удаление лимфатических узлов, пораженных раком.
- Лучевая терапия. Лучевая терапия использует излучение, направленное на уничтожение раковых клеток. Может быть использована до или после проведения хирургической операции.
- Химиотерапия. Химиотерапией применяются препараты для уничтожения раковых клеток. Химиотерапия может применяться до или после проведения операции. Также химиотерапия может сочетаться с лучевой терапией.
- Паллиативная терапия применяется, когда заболевание неизлечимо, она проводится для облегчения симптомов. Для этого может использоваться хирургическая операция по удалению части желудка, применение лекарственных препаратов.
Профилактика
- Здоровое питание. Необходимо ограничить в рационе количество копченых, соленых, маринованных продуктов, употреблять больше овощей и фруктов.
- Отказ от курения.
Рекомендуемые анализы
- Общий анализ крови (ОАК)
- СА 72-4
- СА 19-9
- Раковый эмбриональный антиген (РЭА)
- Свободная β-субъединица хорионического гонадотропина человека (бета-ХГЧ свободный)
- Фрагменты цитокератина 19 CYFRA 21-1
Злокачественные опухоли желудка — Клиника 29
К злокачественным опухолям желудка относятся
• Рак желудка
• Саркома желудка
Рак желудка — злокачественная опухоль, происходящая из эпителия слизистой оболочки желудка. Является одним из наиболее распространённых онкологических заболеваний. Может развиваться в любом отделе желудка и распространяться на другие органы, особенно пищевод, лёгкие и печень.
Этиология
Среди факторов, способствующих развитию рака желудка, называются особенности диеты и факторы окружающей среды, курение, инфекционный и генетический факторы.
Доказана зависимость частоты возникновения рака желудка от недостатка употребления аскорбиновой кислоты, избыточного употребления соли, маринованных, пережаренных, копчёных продуктов, острой пищи, животного масла. Среди причин рака желудка называется злоупотребление алкоголем, особенно водкой. Отмечается прямая корреляционная связь частоты возникновения рака желудка с содержанием в почве меди, молибдена, кобальта и обратная — цинка и марганца.
Важным фактором развития рака желудка является дуоденогастральный рефлюкс, приводящий к хроническому рефлюкс-гастриту. Так, риск рака желудка увеличивается через 5—10 лет после операций на желудке, особенно после резекции по Бильрот II в модификации Гофмейстера-Финстерера, способствующих развитию рефлюкса.
Имеются убедительные данные о зависимости рака желудка от инфицированности Helicobacter pylori. Считается статистически доказанным, что у инфицированных этой бактерией повышен риск развития рака желудка (относительный коэффициент 2,5). В 1994 г. Международным агентством по изучению рака (IACR) ВОЗ H. Pylori отнесен к канцерогенам 1 группы. Эта бактерия вызывает гистологические изменения, приводящие к развитию рака — атрофию слизистой оболочки, кишечную метаплазию и дисплазию эпителия. Большинству случаев рака желудка предшествует длительный предраковый процесс, включающий в себя цепь событий: хронический гастрит — мультифокальная атрофия — кишечная метаплазия — интраэпителиальная неоплазия.
Симптомы
Рак желудка на ранних стадиях, как правило, имеет невыраженные клинические проявления и неспецифические симптомы (диспепсия, снижение аппетита). Другие симптомы рака желудка (так называемый синдром «малых признаков») — астения, отвращение к мясной пище, анемия, потеря веса, «желудочный дискомфорт» чаще наблюдаются при распространённых формах процесса. Раннее насыщение, чувство переполнения желудка после принятия малого количества пищи наиболее характерно для эндофитного рака, при котором желудок становится ригидным, не растяжимым пищей. Для рака кардии характерна дисфагия; рак пилорического отдела может нарушать эвакуацию содержимого желудка, приводя к рвоте.
На поздних стадиях присоединяются боли в эпигастрии, рвота, кровотечения при изъязвлении и распаде опухоли (изменение кала — мелена, рвота «кофейной гущей» или кровью). Характер болей может свидетельствовать о прорастании в соседние органы: опоясывающие боли характерны для прорастания опухоли в поджелудочную железу, схожие со стенокардией — при прорастании опухоли в диафрагму, вздутие живота, урчание в животе, задержка стула — при прорастании в поперечную ободочную кишку.
Диагностика
Методами диагностики рака желудка являются:
• гастроскопия — диагностический метод выбора (благодаря возможности не только визуализировать изменённые участки слизистой желудка, но и осуществлять биопсию ткани для последующей оценки)
• рентгеноскопия желудка с пероральным введением контрастного препарата (сульфат бария). Один из основных методов определения локализации и протяжённости поражения стенки желудка. Наиболее важными рентгенологическими признаками рака желудка являются:
1. наличие дефекта наполнения или ниши в пределах тени желудка
2. потеря эластичности и растяжимости желудочной стенки
3. локальное отсутствие или уменьшение перистальтики в районе опухоли
4. изменение рельефа слизистой оболочки в месте расположения опухоли
5. изменение формы и размеров желудка
• ультразвуковое исследование — УЗИ органов брюшной полости, забрюшинного пространства и лимфатических коллекторов шейно-надключичной области — обязательный метод обследования больных раком желудка, применяемый для выявления метастазов.
• компьютерная томография позволяет выявить рак желудка, однако основной целью исследования является оценка распространённости злокачественного процесса, наличия метастазов.
• лапароскопия не столько помогает в диагностике рака (что возможно лишь в поздних стадиях), сколько используется для определения стадии заболевания и выявления мелких субкапсулярных метастазов в печени и на париетальной брюшине, не видимых при УЗИ и КТ. Тем самым лапароскопия сводит до минимума число эксплоративных лапаротомий.
• онкомаркеры высокоспецифичны (95%), но малочувствительны. Наиболее распространенные онкомаркеры СА72.4, РЭА и СА19.9 по чувствительности варьируют в 40-50% случаев и повышаются при метастазах на 10-20%.
Дифференциальная диагностика
Следует проводить с гастритом, язвенной болезнью, доброкачественными опухолями (полипами, лейомиомой, фибромой), другими злокачественными опухолями — MALT-лимфомой, саркомами (лейомиосаркома, фибросаркома), гастроинтестинальной стромальной опухолью (GIST) желудка. Клиническая картина начальных излечимых стадий рака желудка мало отличается от проявлений большинства заболеваний системы пищеварения, поэтому первостепенное значение в дифференциальной диагностике принадлежит эндоскопии с гистологическим исследованием биоптата из стенки желудка.
Лечение
В настоящее время основной и практически единственный метод радикального лечения рака желудка — хирургическая операция. При запущенных опухолях операция применяется и как паллиативная мера: устраняется причина болей, дисфагии и кровотечений, уменьшается количество опухолевых клеток в организме, что способствует увеличению продолжительности жизни и значительному облегчению состояния больного. Лучевое воздействие и химиотерапия имеют вспомогательное значение.
Обычно удаляется весь желудок (гастрэктомия). Показанием к ней служит расположение опухоли выше угла желудка, субтотальном или тотальном поражении желудка.
Реже производится (на ранних стадиях болезни) его резекция (как правило, субтотальная): при раке антрального отдела — дистальная, при раке кардиального и субкардиального отделов I—II стадий — проксимальная. Помимо этого производится удаление большого и малого сальника, регионарных лимфатических узлов; при необходимости частично или полностью удаляются другие органы: яичники при метастазах Крукенберга, хвост поджелудочной железы, селезенка, левая доля или сегмент печени, поперечная ободочная кишка, левая почка и надпочечник, участок диафрагмы и т. д.
Диспансеризация
Для ранней диагностики рака большое значение имеет диспансеризация лиц, имеющих повышенный риск развития этого заболевания. В группу наблюдения должны быть включены больные старше 40 лет, имеющие следующие заболевания:
• язвенная болезнь желудка
• полипы желудка
• неэпителиальные опухоли желудка
• хронический атрофический гастрит с кишечной метаплазией
• больные, перенёсшие резекцию желудка
За этими пациентами необходимо вести активное наблюдение с ежегодным эндоскопическим и рентгенологическим контролем и исследованием кала на скрытую кровь каждые 6 месяцев.
Прогноз и выживаемость
Как и при многих других видах рака, исход и эффективность лечения рака желудка в настоящее время зависит от стадии заболевания.
В большинстве случаев рак желудка выявляется только на поздних стадиях и является уже распространённым, в этом случае общая 5-летняя выживаемость составляет лишь 15 %. Если человек прожил первые 5 лет, то дальнейшая выживаемость повышается — 10-летняя выживаемость составляет 11 %, что лишь на 4 % ниже 5-летней выживаемости.
Для лиц молодого возраста показатели выживаемости выше, чем у пожилых людей. У пациентов младше 50 лет пятилетняя выживаемость составляет 16-22 %, в то время как среди пациентов старше 70 лет этот показатель равен 5-12 %.
У пациентов с раком желудка I стадии высок шанс на полное выздоровление. Пятилетняя выживаемость составляет 80 %, из них 70 % полностью выздоравливают. Тогда как у пациентов с раком желудка IV стадии пятилетняя выживаемость обычно не превышает 5 %.
Лечение рака у пожилых людей в Израиле, особенности и методы терапии
Онкологические патологии часто называют «недугом пожилых» – средний возраст заболевания раком у обоих полов находится в коридоре 60-62 лет: чем старше мы становимся, тем больше негативных факторов собираются в одном месте в одно время – организм изнашивается, защитные реакции снижаются, отечественные врачи машут рукой и пожимают плечами. «А что вы хотели? Вам же 75 лет, у нас нет эликсира молодости», – самое безобидное, что приходится слышать людям после 70 в кабинетах медиков.Признаки онкологии в пожилом возрасте часто размыты и списываются на общие недомогания – полная диагностика состояния здоровья проводится крайне редко. Отечественные онкологи не только боятся возрастных больных, но и не хотят тратить на них время, а государство – средства: масса хронических болезней, длинный список поддерживающих препаратов, сложности с сердечно-сосудистой системой и подбором анестезии. Тяжелое восстановление после химио- и лучевой терапии, невозможность достоверно просчитать риски операции. Пожилые люди часто даже не обращаются в больницу, потому что знают, что их все равно не будут лечить. А если и идут, зачастую их отправляют домой доживать свои дни, в лучшем случае, сидя на обезболивающих препаратах.
Желаете получить бесплатную консультацию о возможностях лечения рака в пожилом возрасте в Израиле — отправьте нам заявку
или обратитесь по телефону +972-77-4450-480 или +8-800-707-6168 (для жителей России бесплатно).
Стоит ли лечить рак в старческом возрасте?
Ответ на этот вопрос можно найти в другом вопросе: разве вы не продлите жизнь близкому человеку даже на несколько месяцев, если есть такая возможность? В Израиле, Европе и США давно и успешно лечат самые тяжелые заболевания пожилых людей – не так давно мы рассказывали историю 93-летней пациентки из Хайфы, которой была проведена катетеризация сосудов головного мозга. Показателен и случай американца Альберта Гордона – операцию по удалению опухоли из прямой кишки с последующей лучевой и химиотерапией он перенес 10 лет назад. Сегодня Альберту 83, он прекрасно себя чувствует и принимает участие в марафонских забегах.
«Очевидный факт: вовремя диагностированный рак поддается лечению в любом возрасте, что может значительно продлить человеку жизнь и подарить еще несколько счастливых лет. Главный показатель к лечению – удовлетворительное общее состояние здоровья с учетом биологического, а не фактического возраста, поскольку возрастные изменения индивидуальны, и пациенты старшей категории сильно различаются по физическому и психическому состоянию» — делится опытом наш медицинский консультант Элла Сушин
Кроме того, онкология в среднем, пожилом и старческом возрасте развивается по-разному. Физиологические процессы в организме после 60 лет протекают медленней, соответственно, медленней происходит деление канцерогенных клеток. Например, рак молочных желез у пожилых женщин легче поддается лечению, чем у молодых, опухоль увеличивается в размерах продолжительное время и меньше метастазирует. В то время как другие виды рака, например, лейкемия, лечатся сложнее: с учетом тяжести сопутствующих заболеваний и агрессивности болезни на первый план выходит паллиативное лечение – симптоматическая терапия, направленная на создание максимально комфортных условий жизни и ее продления.
Как лечат онкологию в пожилом возрасте в Израиле?
Пожилые люди с диагнозом «онкология» живут в Израиле годами, сохраняя при этом бодрость духа и удовлетворительное самочувствие. Много внимания уделяется профилактике онкопатологий – регулярный медицинский осмотр позволяет диагностировать рак на нулевой и первой стадии до появления метастаз. В таком случае прогноз полного излечения человека в любом возрасте превышает отметку в 90%.При составлении схемы лечения израильскими врачами- онкологами учитываются основные показатели: как терапия отразится на продолжительности жизни, сможет ли пациент перенести облучение или химию, каковы шансы на восстановление до прежнего уровня жизни, будет ли лечение рака актуальным на фоне сопутствующих заболеваний. При наличии жизненных ресурсов организма операции проводятся в любом возрасте. 60% из них малоинвазивные и лапароскопические. Помимо терапевтических процедур, пациентам старшей возрастной категории оказывают психологическую поддержку, что особенно важно для пожилых людей с уязвимой нервной системой.
Читайте также:
Лечение боли при раке в Израиле
ТОП 5 инноваций в медицине Израиля, которые спасают жизни людей
Второе мнение специалиста – как пройти диагностику рака в Израиле онлайн
Диагностика и лечение рака в пожилом возрасте с DRA Medical
Лечение онкологии у пожилых людей – сложная задача, требующая комплексного индивидуального подхода к каждому пациенту. Главная ее цель – не навредить организму еще больше с помощью агрессивных методов терапии.Наш центр является узкопрофильным медицинским учреждением, успешно занимающимся лечением онкологии в Израиле у пациентов разных возрастных групп. Все диагностические процедуры проводятся на современном оборудовании крупнейших лабораторий страны в течение трех дней с момента обращения в центр. После исчерпывающего обследования врач составляет протокол терапии. В учет берется характер и стадия заболевания, наличие сопутствующих недугов и гериатрических симптомов, общее состояние и психологический настрой.
Самый эффективный метод разрушения раковых новообразований, в том числе у пожилых людей, – хирургическое иссечение больных тканей с последующим дополнением лучевой и химиотерапией. Однако если состояние здоровья не позволяет провести операцию, наши специалисты успешно применяют методики узкой направленности: лучевую и химиотерапию, абляцию, таргетную терапию, стереотоксическую радиохирургию, HIFU, криотерапию.
В случаях, когда организм истощен другими болезнями и не способен справиться с негативными последствиями химии или облучения, принекоторых видах рака возможно применение иммунотерапии. Важное место занимает сопроводительная терапия – она направлена на защиту здоровых тканей от токсичного воздействия противоопухолевых препаратов и их продуктов.
При запущенных формах рака с метастазами подбирается эффективное паллиативное лечение для облегчения состояние больного и продление жизни.
Подходящее лечение для пожилых пациентов с раком желудка — Pak
Пик заболеваемости раком желудка приходится на возраст от 50 до 70 лет, и наблюдается рост заболеваемости среди пожилых людей по мере увеличения продолжительности жизни (1-4). Текущие рекомендации по лечению и стандарты ухода обычно основаны на исследованиях и клинических испытаниях более молодых пациентов, и их необходимо оценить на предмет их непосредственного применения к пожилому населению, как в контексте увеличения числа сопутствующих заболеваний, так и потенциальных различий в патофизиологии их заболеваний. (1,5,6).В этой рукописи исследуется текущее состояние научных знаний в области лечения рака желудка и представлены данные из Национальной базы данных по раку (NCDB), с особым акцентом на важные вариации и соображения, которые необходимо учитывать для пожилых пациентов.
Заболеваемость и эпидемиология
Рак желудка является пятой по частоте причиной рака и третьей по значимости причиной смерти от рака во всем мире (7,8).Заболеваемость и смертность от рака желудка непропорционально различаются по географическим регионам, с более высокими показателями в странах Восточной Азии и относительно более низкими в странах Запада (9,10). В Восточной Азии чаще встречается рак дистального отдела желудка, тогда как рак проксимального отдела желудка чаще встречается на Западе (3,11).
Несколько факторов окружающей среды и образа жизни способствуют повышенному риску рака желудка. Helicobacter pylori (H.pylori) является основной причиной канцерогенеза желудка с потенциальным прогрессированием до рака желудка, а также является причиной непропорционально высокой распространенности рака желудка в азиатских странах (12,13). В Японии и Корее значительное снижение инфицирования H. pylori в последние десятилетия сопровождалось соответствующим снижением заболеваемости и смертности от рака желудка (14-18). Снижение смертности от рака желудка в этих странах также может быть связано с проведением строгих программ скрининга, поскольку все больше случаев рака диагностируется на более ранней стадии (19–22).Факторы питания и образа жизни, такие как высокое потребление натрия, повышенное потребление алкоголя и курение, также связаны с повышенным риском рака желудка (23–27). Диеты с высоким содержанием фруктов и овощей показали защитный эффект от рака желудка (28-30).
Пожилые люди и рак желудка
В настоящее время нет стандартного определения понятия «пожилой». Многие группы и организации, включая Всемирную организацию здравоохранения, использовали хронологический возраст 65 лет и старше для определения пожилого населения; однако, поскольку средняя продолжительность жизни во многих странах достигает, а иногда и превышает 80 лет, это определение быстро меняется (31,32).В результате также отсутствуют стандартные рекомендации по ведению и лечению пожилых людей с раком желудка.
Было выявлено несколько различий в представлении и патологических характеристиках рака желудка, диагностированного у пожилых людей, по сравнению с более молодыми пациентами. Как и ожидалось, пожилые пациенты обычно имеют больше сопутствующих заболеваний и имеют более высокие баллы по классификации Американского общества анестезиологов (ASA) (33–35). Пациенты пожилого возраста также имеют тенденцию к более поздней клинической стадии симптоматического заболевания (33,36,37).Первичные опухоли чаще встречаются в дистальной трети желудка (38–41). Гистопатологически у пожилых пациентов, как правило, наблюдаются множественные опухоли большего размера с хорошо дифференцированной гистологией кишечного типа (1,33,36,38,42-46). Несколько исследований также выявили потенциально разные паттерны метастазов в лимфатические узлы у пожилых пациентов с раком желудка по сравнению с более молодыми пациентами; однако результаты противоречивы, поскольку некоторые исследования продемонстрировали более высокую склонность к метастазам в лимфатические узлы у пожилых людей, некоторые — более низкую, а другие не показали никакой разницы (1,33,38,41,42,47-50) .Интерпретация этих различных результатов остается сложной, поскольку пожилые люди часто подвергаются ограниченной лимфаденэктомии по сравнению с расширенной лимфаденэктомией D2, которая является стандартом лечения среди более молодых пациентов. Мы обследовали 13836 пациентов, перенесших радикальную гастрэктомию в период с 2010 по 2014 год с использованием NCDB, из которых 2140 пациентов (15%) были в возрасте ≥80 лет. Пациенты старше 80 лет, как правило, имели более крупные опухоли и большее поражение лимфатических узлов, следовательно, имели более высокие стадии Американского объединенного комитета по раку (AJCC) по сравнению с более молодыми пациентами (P <0.0001). Эти наблюдения согласуются с предыдущими отчетами.
Хирургия пожилых людей
Степень резекции определяется стадией первичной опухоли и узловым статусом. Классификация AJCC TNM является одним из наиболее часто используемых критериев стадирования (51). Опухоли T1a, определяемые инвазией собственной пластинки слизистой оболочки или мышечной оболочки, обычно поддаются эндоскопической резекции. При стадии IB – III с первичной опухолью, которая проникает в подслизистую оболочку и за ее пределы, но не нарушает висцеральную брюшину или прилегающие структуры, рекомендуется частичная гастрэктомия с расширенной лимфаденэктомией D2 для достижения лечебной резекции всех микроскопических и макроскопических заболеваний ( 52).
Поскольку гастрэктомия — это серьезная операция на брюшной полости, пожилых пациентов необходимо тщательно обследовать перед операцией, учитывая повышенный риск заболеваемости и смертности при хирургическом вмешательстве. Fujiwara et al. сравнил 115 пациентов в возрасте ≥80 лет с 333 пациентами в возрасте ≤79 лет, которым была выполнена субтотальная или полная гастрэктомия с различной степенью лимфаденэктомии, и обнаружил, что пациенты в возрасте ≥80 лет имели больше послеоперационных осложнений и госпитальной смертности, а также как более низкая общая выживаемость (OS) и выживаемость при конкретном заболевании (DSS) (53).Используя анализ кривой рабочих характеристик приемника, зависящий от времени, оптимальное возрастное ограничение, определенное в этом исследовании для гастрэктомии с целью увеличения выживаемости через три года, составило 79,2 года. Hsu et al. оценил результаты 164 пациентов ≥80 лет, перенесших субтотальную или тотальную гастрэктомию с лимфаденэктомией D2, по сравнению с 2258 пациентами младше 80 лет, а также выявил значительно более высокую заболеваемость (18% против 13%, P = 0,035) и госпитальная летальность (7%, vs. 3%, P = 0,015) в пожилой группе (35). Однако, в отличие от предыдущего исследования, Hsu et al. не выявил каких-либо значительных различий в долгосрочной смертности от конкретных заболеваний (44%, против , 47%, P = 0,407) после среднего периода наблюдения 37,8 месяцев. Применяя еще более высокий возрастной предел для определения пожилого населения, Endo et al. сравнили 56 пациентов ≥85 лет, перенесших дистальную резекцию желудка, с 55 пациентами <85 лет, получившими наилучшую поддерживающую терапию, с использованием анализа с сопоставлением по шкале предрасположенности (54).Преимущество гастрэктомии по выживаемости по сравнению с наилучшей поддерживающей терапией в этой наиболее пожилой группе было продемонстрировано только среди женщин (медиана OS 67 против 12 месяцев, P <0,0001), но не у пациентов мужского пола (медиана OS 13 против 18 месяцев, P = 0,037). Послеоперационная пневмония, особенно среди пациентов мужского пола, была частым осложнением в этой исследуемой популяции и часто ассоциировалась со смертностью, о чем также сообщалось в других исследованиях (42,53,55-58). Разница в выживаемости по полу у пациентов с послеоперационной пневмонией также была выявлена в других популяциях пожилых и сильно коморбидных пациентов и потенциально является результатом взаимодействия между различными гормональными, иммунологическими и микробиологическими факторами (59-63).Общая высокая частота послеоперационной пневмонии у пожилых, вероятно, связана с исходным снижением легочной функции и резерва, которые затем еще больше уменьшаются после обширной открытой абдоминальной хирургии (64–69). Частота нелегочных послеоперационных осложнений, а также послеоперационная смерть после гастрэктомии также увеличивалась с увеличением возраста пациентов (34,45,70-72). Эти исследования указывают на важность предоперационной оценки риска и отбора пациентов из числа пожилых пациентов, рассматриваемых для открытой гастрэктомии.
Одним из методов снижения послеоперационной заболеваемости и смертности среди пожилых пациентов, перенесших гастрэктомию, является использование малоинвазивного подхода. Несколько исследований продемонстрировали сопоставимые, а иногда даже улучшенные результаты у пожилых пациентов, перенесших лапароскопическую или роботизированную гастрэктомию, по сравнению с открытым доступом (73–76). Измеряемые результаты в этих исследованиях включали интраоперационную кровопотерю, время до первого газообразования, время до первой пероральной диеты, индексную продолжительность пребывания в больнице, послеоперационные осложнения и выживаемость.Минимально-инвазивный подход вызывает меньшее физиологическое повреждение организма с меньшими длительными функциональными нарушениями (77,78). В отличие от предыдущих исследований открытой гастрэктомии, в которых у пожилых пациентов стабильно выше частота послеоперационных осложнений, чем у пациентов пожилого возраста, в нескольких исследованиях было обнаружено, что частота осложнений у пожилых и не пожилых пациентов схожа с минимально инвазивной техникой (45, 79-83). Недавно мы провели собственный обзор послеоперационных исходов у пациентов в возрасте ≥80 лет, перенесших минимально инвазивную по сравнению с открытой субтотальной или тотальной гастрэктомией с использованием NCDB.Мы обнаружили, что минимально инвазивная гастрэктомия была связана с уменьшением продолжительности пребывания в стационаре как минимум на 1 день (P <0,001) по сравнению с открытой гастрэктомией. Кроме того, не было разницы в частоте резекций с положительным краем (P = 0,27), адекватной выборке лимфатических узлов, определяемой как ≥15 лимфатических узлов (P = 0,08), повторных госпитализациях (P = 0,32) или 30- или 90- дневная смертность (P = 0,75, P = 0,82) между этими двумя подходами. Минимально инвазивный подход к лечебной резекции у пожилых людей должен быть высоко оценен, чтобы способствовать послеоперационному восстановлению и улучшить результаты лечения пациентов.
Объем лимфаденэктомии во время гастрэктомии и потенциальная выгода от расширенной D2-лимфаденэктомии у пожилых пациентов также были противоречивыми. В то время как лимфаденэктомия D2, которая включает узлы вдоль левой желудочной, общей печеночной, чревной и селезеночной артерий в дополнение к перигастральным лимфатическим узлам, удаленным при лимфаденэктомии D1, обычно рекомендуется при раке желудка IB – III стадии, онкологическая польза должна быть сбалансирована потенциально повышенная заболеваемость и смертность от этой более обширной процедуры у пожилого населения с большим количеством сопутствующих заболеваний и меньшим функциональным резервом.Brenkman et al. провела обзор 2387 пациентов <75 лет и 1377 пациентов ≥75 лет, перенесших лечебную субтотальную или тотальную резекцию желудка, и обнаружила, что высокий выход лимфатических узлов улучшает выживаемость в обеих возрастных группах без увеличения послеоперационной смертности (43). Однако трудность интерпретации этого и подобных исследований заключается в использовании выхода лимфатических узлов в качестве меры степени лимфаденэктомии. Выход лимфатических узлов регистрирует только количество лимфатических узлов, извлеченных во время операции, но не всегда может точно передать, были ли узлы взяты в достаточной степени со всех необходимых станций, которые определяют лимфаденэктомию D2.В голландском исследовании 1078 пациентов, которые были рандомизированы для лимфаденэктомии D1 или D2, пациенты старше 70 лет постоянно имели более высокие показатели заболеваемости и смертности по сравнению с пациентами ≤70 лет, и эти показатели были даже выше среди тех, кому старше 70 лет, которые перенесли D2, по сравнению с D1. лимфаденэктомия с ограниченным преимуществом выживаемости (84). Rausei et al. проанализировал 1322 пациента, перенесших лечебную гастрэктомию с лимфаденэктомией D2 по сравнению с D1 и, в дополнение к классификации пациентов по возрасту (<70 по сравнению с> 70 лет), также стратифицировал пациентов по их сопутствующим заболеваниям с использованием шкалы коморбидности Чарлсона (<5 vs.> 5) (85). В целом, больше послеоперационных осложнений произошло у пациентов старше 70 лет (34% против 28%, P <0,001), а в этой пожилой популяции у пациентов с высокими показателями Чарлсона частота осложнений была еще выше (38% vs 31%, P = 0,007). Пациенты> 70 лет с высокими показателями по шкале Charlson также имели тенденцию к большему количеству осложнений после лимфаденэктомии D2, но это не было статистически значимым (40% против 35%). Дополнительные исследования также продемонстрировали отсутствие преимущества в отношении выживаемости, связанного с расширенной лимфаденэктомией D2 по сравнению с более ограниченной лимфаденэктомией D1 у пожилых пациентов (46,86-88) (, таблица 1, ).Наше исследование, проведенное NCDB, показало, что пожилые пациенты могут не получить такого же преимущества выживания от лимфодиссекции D2, как более молодые пациенты. Из 2140 пациентов в возрасте ≥80 лет, перенесших субтотальную или тотальную гастрэктомию, у половины было исследовано менее 15 лимфатических узлов, а у половины — 15 или более лимфатических узлов. Используя это как показатель степени лимфаденэктомии, не было различий в OS между пожилыми пациентами, у которых была ограниченная по сравнению с обширной лимфаденэктомией (медиана OS 18.2 против 19,2 месяца, P = 0,29).
Таблица 1 Исследования, оценивающие потенциальную пользу выживаемости при расширенной лимфаденэктомии по сравнению с ограниченной у пожилых пациентовПолная таблица
Неоадъювантная терапия для пожилых людей
Пациентам с опухолями ≥T1b рекомендуется неоадъювантная химиотерапия комбинацией платина / фторпиримидин (52).Исследование MAGIC продемонстрировало значительное улучшение как общей (5-летняя, 36% против 23%), так и выживаемости без прогрессирования (ВБП) (ОР 0,66; 95% ДИ: 0,53–0,81) у пациентов с резектабельным раком желудка, пролеченных с тремя циклами до операции и тремя циклами послеоперационного лечения эпирубицином, цисплатином и фторурацилом по сравнению с теми, кто перенес только операцию (89). Дополнительные испытания подтвердили преимущество этой комбинации неоадъювантной химиотерапии в отношении выживаемости у пациентов с операбельным раком желудка (90,91).Однако многие пациенты в этих испытаниях были молодого или среднего возраста, с ограниченным числом пациентов пожилого возраста, особенно в возрасте ≥80 лет. Испытания, ориентированные конкретно на пожилых пациентов, продемонстрировали онкологические преимущества неоадъювантной химиотерапии, но за счет повышения токсичности и снижения качества жизни (92,93).
Роль неоадъювантной химиолучевой терапии остается неясной и остается активной областью исследований (94–97). Потребуются дополнительные исследования, чтобы определить, применимы ли потенциальные преимущества для пожилого населения.Наше исследование NCDB показало, что среди всех пожилых пациентов, перенесших радикальную гастрэктомию, только 7,5% получали неоадъювантную химио / лучевую терапию, тогда как доля гораздо выше в других возрастных группах (44,5% для пациентов <65 лет и 33,6% для пациентов в возрасте 65–79 лет, P <0,001).
Адъювантная терапия для пожилых людей
Пациентам, которые не получали неоадъювантную химиотерапию до резекции, рекомендуется адъювантная химиотерапия или химиолучевая терапия для пациентов с высоким риском рецидива заболевания (98).Преимущество адъювантной химиотерапии для пациентов с резекцией по сравнению с только хирургическим вмешательством хорошо задокументировано в двух рандомизированных испытаниях фазы III, проведенных в Азии. В исследовании CLASSIC сообщалось об улучшении 3-летней безрецидивной выживаемости (DFS) на 74% у пациентов, перенесших гастрэктомию D2 с последующей химиотерапией, по сравнению с 59% у пациентов, перенесших только операцию (99). В анализе подгрупп по возрасту пациенты ≥65 лет, получавшие адъювантную химиотерапию, также улучшили 3-летнюю DFS. В исследовании ACTS GC 5-летний DFS у пациентов, получавших адъювантную химиотерапию, составил 65% по сравнению с 53% в группе, получавшей только хирургическое вмешательство; 5-летняя выживаемость составила 72% и 61% в группах адъювантной химиотерапии и хирургии соответственно (100).Однако при анализе подгрупп по возрасту не было различий в DFS для пациентов ≥60 лет и не было различий в OS для пациентов ≥70 лет. На сегодняшний день не проводилось рандомизированных исследований для оценки пользы адъювантной химиотерапии, особенно у пожилых пациентов, перенесших гастрэктомию. Ретроспективные исследования, посвященные пожилым пациентам, показали противоречивые результаты, и без рандомизации их трудно интерпретировать из-за потенциального эффекта систематической ошибки отбора, когда пожилые пациенты получали дополнительную адъювантную химиотерапию (101-105).
Intergroup 0116 было первым рандомизированным исследованием фазы III, проведенным на западных пациентах, чтобы продемонстрировать преимущество адъювантной химиолучевой терапии после операции по сравнению с одной только операцией (106). В первоначальных результатах исследования, опубликованных в 2001 году, сообщалось об улучшении медианы ОВ на 36 месяцев у пациентов, получавших адъювантную химиолучевую терапию, по сравнению с 27 месяцами для тех, кто перенес только операцию (106). Последнее обновление из этой когорты исследования было опубликовано после более чем десяти лет наблюдения и продемонстрировало стойкую пользу как в отношении общей выживаемости, так и в отношении DFS для пациентов, получавших адъювантную химиолучевую терапию (107).Yeh et al. использовала базу данных «Надзор, эпидемиология и конечные результаты-Medicare» для обзора 1519 пациентов в возрасте ≥65 лет, перенесших гастрэктомию, из которых 42% получили адъювантную химиолучевую терапию (108). В этом ретроспективном популяционном исследовании адъювантная химиолучевая терапия продемонстрировала преимущество в выживаемости (HR 0,59, 95% CI: 0,50–0,67) по сравнению с одним хирургическим вмешательством, особенно у пациентов со стадиями II и III.
Преимущества адъювантной терапии продолжают подтверждаться в последующих исследованиях и обзорах; однако дополнительное преимущество адъювантной химиолучевой терапии по сравнению с одной адъювантной химиотерапией остается предметом обсуждения (109-112).Необходимо провести будущие проспективные клинические испытания, чтобы изучить потенциальную пользу адъювантной терапии у пожилых пациентов и определить оптимальные схемы лечения для максимального контроля над заболеванием, а также для поддержания качества их жизни.
В таблице 2 представлен обзор испытаний и исследований химиотерапии, лучевой терапии и химиолучевой терапии с участием пациентов с раком желудка всех возрастов. В таблице 3 приведены испытания и исследования, которые были посвящены лечению пациентов пожилого возраста.
Таблица 2 Обзор испытаний адъювантной терапии и обзоров лечения пациентов с раком желудка любого возрастаПолная таблица Таблица 3 Обзор испытаний и исследований адъювантной терапии у пожилых пациентов с раком желудка
Полная таблица
При метастатическом поражении рекомендуется комбинированная терапия платиной и фторпиримидином.В многоцентровом исследовании фазы III с участием 50 пациентов с метастатическим раком ≥70 лет двойная терапия оксалиплатином и капецитабином улучшила как ВБП, так и ОВ по сравнению с монотерапией капецитабином (ВБП 7,1 против 2,6 месяцев, ОВ 11,1 против 6,3 месяца) (113). Это сопоставимо со средним временем ОВ, указанным в исследованиях фазы III, в которых участвовали пациенты любого возраста с метастатическим раком желудка (114–116). Sasaki et al. сообщил в исследовании фазы II, что комбинация цисплатина и S-1, перорального фторпиримидина, также была безопасной и эффективной для пожилых пациентов ≥76 лет, со средним показателем PFS и OS 7.8 и 12,3 месяца соответственно (117). При анализе подгрупп пациентов ≥70 лет, которые были включены в японскую рандомизированную фазу III G-SOX, сравнивающую S-1 и оксалиплатин с S-1 и терапией цисплатином, не было различий в PFS или OS между двумя комбинированными схемами. но пожилые пациенты, получавшие S-1 и оксалиплатин, проявляли меньшую токсичность (118). Ретроспективный обзор 129 пациентов ≥65 лет с метастатическим или рецидивирующим раком желудка также показал, что комбинация S-1 и оксалиплатина хорошо переносилась в этой старшей возрастной группе (119) (, таблица 4, ).
Таблица 4 Обзор испытаний и исследований химиотерапии у пожилых пациентов с метастатическим раком желудкаПолная таблица
Сводная ведомость
- Пациенты и опухоли у пожилых пациентов: Пожилые пациенты, как правило, имеют больше сопутствующих заболеваний и имеют более позднюю стадию заболевания.Гистологически у пожилых пациентов, как правило, наблюдаются более крупные множественные опухоли хорошо дифференцированной гистологии кишечного типа.
- Хирургия у пожилых пациентов: Хирургия рака желудка, включая тотальную резекцию желудка, безопасна для физически здоровых пожилых пациентов. Мы рекомендуем минимально инвазивный подход с менее обширной диссекцией лимфатических узлов, чтобы минимизировать послеоперационную заболеваемость и смертность.
- Неоадъювантная терапия для пожилых людей: на основании клинических испытаний, проведенных среди участников всех возрастов, пациентам с опухолями ≥T1b рекомендуется получать неоадъювантную химиотерапию с комбинацией платины и фторпиримидина.Среди пожилых пациентов онкологические преимущества неоадъювантной терапии должны быть сбалансированы с потенциально повышенной токсичностью и снижением качества жизни.
- Адъювантная терапия для пожилых людей: на основании клинических испытаний, проведенных среди участников всех возрастов, пациенты, которые не получали неоадъювантную химиотерапию, должны получать адъювантную химиотерапию или химиолучевую терапию. Нет убедительных доказательств, подтверждающих дополнительную пользу адъювантной лучевой терапии для пациентов, получавших адъювантную химиотерапию.На сегодняшний день не проводилось рандомизированных исследований для оценки пользы адъювантной терапии, особенно у пожилых пациентов, перенесших гастрэктомию.
- Лечение метастазов у пожилых: Комбинированная терапия платиной и фторпиримидинами рекомендуется при метастатическом поражении. Было показано, что этот режим безопасен и хорошо переносится пожилыми пациентами.
Благодарности
Нет.
Конфликт интересов: Авторы не заявляют о конфликте интересов.
Список литературы
- Китамура К., Ямагути Т., Танигучи Н. и др. Клинико-патологическая характеристика рака желудка у пожилых людей. Br J Cancer 1996; 73: 798-802. [Crossref] [PubMed]
- Биттнер Р., Баттерс М., Ульрих М. и др.Тотальная гастрэктомия. Обновленная информация об оперативной смертности и долгосрочной выживаемости с особым вниманием к пациентам старше 70 лет. Энн Сург 1996; 224: 37-42. [Crossref] [PubMed]
- Экипаж К.Д., Нейгут А.И. Эпидемиология рака желудка. Всемирный журнал J Gastroenterol 2006; 12: 354-62. [Crossref] [PubMed]
- Таккар Дж. П., Маккарти Б. Дж., Виллано Дж. Л.. Повозрастная заболеваемость раком увеличивается среди самых старших возрастных групп. Am J Med Sci 2014; 348: 65-70.[Crossref] [PubMed]
- Li Y, Tan B, Fan L и др. Клинико-патологическая характеристика пожилых людей с раком желудка и факторы риска послеоперационных осложнений. Дж. Инвест Сург 2017; 30: 394-400. [Crossref] [PubMed]
- Kuo CY, Chao Y, Li CP. Обновленная информация о лечении рака желудка. J Chin Med Assoc 2014; 77: 345-53. [Crossref] [PubMed]
- Брей Ф., Джемал А., Грей Н. и др. Глобальная трансформация рака в соответствии с Индексом человеческого развития (2008-2030 гг.): Популяционное исследование.Ланцет Онкол 2012; 13: 790-801. [Crossref] [PubMed]
- Ferlay J, Soerjomataram I., Dikshit R, et al. Заболеваемость и смертность от рака во всем мире: источники, методы и основные закономерности в GLOBOCAN 2012. Int J Cancer 2015; 136: E359-86. [Crossref] [PubMed]
- Балакришнан М., Джордж Р., Шарма А. и др. Изменение тенденций рака желудка во всем мире. Curr Gastroenterol Rep 2017; 19:36. [Crossref] [PubMed]
- Ямамото С.Заболеваемость раком желудка в мире. Jpn J Clin Oncol 2001; 31: 471. [PubMed]
- Сасако М., Иноуэ М., Лин Дж. Т. и др. Отчет Рабочей группы по раку желудка. Jpn J Clin Oncol 2010; 40 Приложение 1: i28-37. [Crossref] [PubMed]
- Parsonnet J, Friedman GD, Vandersteen DP, et al. Инфекция Helicobacter pylori и риск рака желудка. N Engl J Med 1991; 325: 1127-31. [Crossref] [PubMed]
- Forman D, Newell DG, Fullerton F, et al.Связь между инфекцией Helicobacter pylori и риском рака желудка: данные проспективного исследования. BMJ 1991; 302: 1302-5. [Crossref] [PubMed]
- Кобаяши Т., Кикучи С., Лин И и др. Тенденции заболеваемости раком желудка в Японии и их связь с инфекцией Helicobacter pylori и атрофией слизистой оболочки желудка. Рак желудка 2004; 7: 233-9. [Crossref] [PubMed]
- Take S, Mizuno M, Ishiki K и др. Семнадцатилетний эффект искоренения Helicobacter pylori на профилактику рака желудка у пациентов с язвенной болезнью; проспективное когортное исследование.Журнал Гастроэнтерол 2015; 50: 638-44. [Crossref] [PubMed]
- Ким Н., Парк Р.Й., Чо С.И. и др. Инфекция Helicobacter pylori и развитие рака желудка в Корее: долгосрочное наблюдение. Дж. Клин Гастроэнтерол 2008; 42: 448-54. [Crossref] [PubMed]
- Иноуэ М. Изменение эпидемиологии Helicobacter pylori в Японии. Рак желудка 2017; 20: 3-7. [Crossref] [PubMed]
- Seta T, Takahashi Y, Noguchi Y, et al. Эффективность эрадикации Helicobacter pylori в профилактике первичного рака желудка у здоровых бессимптомных людей: систематический обзор и метаанализ, сравнивающий соотношение рисков с разницей в рисках.PLoS One 2017; 12: e0183321. [Crossref] [PubMed]
- Hamashima C. Текущие проблемы и перспективы скрининга рака желудка. Всемирный журнал J Gastroenterol 2014; 20: 13767-74. [Crossref] [PubMed]
- Пасечников В, Чуков С, Федоров Е и др. Рак желудка: профилактика, скрининг и ранняя диагностика. Всемирный журнал J Gastroenterol 2014; 20: 13842-62. [Crossref] [PubMed]
- Ким Х, Хван Й, Сунг Х и др. Эффективность скрининга рака желудка на заболеваемость и смертность от рака желудка в проспективной когорте на уровне сообщества.Cancer Res Treat 2017. [Epub перед печатью]. [Crossref] [PubMed]
- Jun JK, Choi KS, Lee HY, et al. Эффективность Корейской национальной программы скрининга рака в снижении смертности от рака желудка. Гастроэнтерология 2017; 152: 1319-28.e7. [Crossref] [PubMed]
- Pourfarzi F, Whelan A, Kaldor J, et al. Роль диеты и других факторов окружающей среды в возникновении рака желудка в Иране — популяционное исследование. Int J Cancer 2009; 125: 1953-60.[Crossref] [PubMed]
- Moy KA, Fan Y, Wang R, et al. Употребление алкоголя и табака в связи с раком желудка: проспективное исследование мужчин в Шанхае, Китай. Эпидемиологические биомаркеры рака до 2010 г .; 19: 2287-97. [Crossref] [PubMed]
- Sjodahl K, Lu Y, Nilsen T.I, et al. Курение и употребление алкоголя в связи с риском рака желудка: популяционное проспективное когортное исследование. Int J Cancer 2007; 120: 128-32. [Crossref] [PubMed]
- Lin SH, Li YH, Leung K, et al.Обработанные солью пищевые продукты и рак желудка у населения Китая. Азиатский Pac J Cancer Prev 2014; 15: 5293-8. [Crossref] [PubMed]
- Yang WG, Chen CB, Wang ZX и др. Исследование зависимости между потреблением соли, соленым вкусом и риском рака желудка. Мир Ж. Гастроэнтерол 2011; 17: 2049-53. [Crossref] [PubMed]
- Fang X, Wei J, He X и др. Пейзаж диетических факторов, связанных с риском рака желудка: систематический обзор и метаанализ доза-реакция проспективных когортных исследований.Eur J Cancer 2015; 51: 2820-32. [Crossref] [PubMed]
- Стоянович Дж., Хиральди Л., Арзани Д. и др. Соблюдение средиземноморской диеты и риск рака желудка: результаты исследования случай-контроль в Италии. Eur J Cancer Prev 2017; 26: 491-6. [Crossref] [PubMed]
- Ван Т., Цай Х., Сасадзуки С. и др. Потребление фруктов и овощей, антитела к Helicobacter pylori и риск рака желудка: объединенный анализ проспективных исследований в Китае, Японии и Корее.Int J Cancer 2017; 140: 591-9. [Crossref] [PubMed]
- Рамеш Х.С., Папа Д., Дженнари Р. и др. Оптимизация хирургического лечения онкологических больных пожилого возраста. Мир J Surg Oncol 2005; 3:17. [Crossref] [PubMed]
- Почему старение населения имеет значение: глобальная перспектива. 2007. По состоянию на 5 сентября 2017 г. Доступно в Интернете: https://www.nia.nih.gov/sites/default/files/2017-06/WPAM.pdf
- Eguchi T, Fujii M, Takayama T. Смертность от рака желудка у пожилых пациентов.J Surg Oncol 2003; 84: 132-6. [Crossref] [PubMed]
- Wu CW, Lo SS, Shen KH и др. Хирургическая смертность, выживаемость и качество жизни после резекции рака желудка у пожилых людей. Мировой журнал J Surg 2000; 24: 465-72. [Crossref] [PubMed]
- Hsu JT, Лю М.С., Ван Ф. и др. Стандартная радикальная резекция желудка у восьмидесятилетнего и девяностолетнего возраста с раком желудка: существенны ли краткосрочные хирургические результаты и долгосрочное выживание? J Gastrointest Surg 2012; 16: 728-37.[Crossref] [PubMed]
- Park HJ, Ahn JY, Jung HY и др. Клинические характеристики и исходы пациентов с раком желудка в возрасте старше 80 лет: ретроспективное исследование «случай-контроль». PLoS One 2016; 11: e0167615. [Crossref] [PubMed]
- Kim JH, Chin HM, Jun KH. Хирургические результаты и выживаемость после гастрэктомии у восьмидесятилетних детей с раком желудка. J Surg Res 2015; 198: 80-6. [Crossref] [PubMed]
- Arai T, Esaki Y, Inoshita N, et al.Патологические характеристики рака желудка у пожилых людей: ретроспективное исследование 994 хирургических пациентов. Рак желудка 2004; 7: 154-9. [Crossref] [PubMed]
- Medina-Franco H, Heslin MJ, Cortes-Gonzalez R. Клинико-патологические характеристики рака желудка у молодых и пожилых пациентов: сравнительное исследование. Энн Сург Онкол 2000; 7: 515-9. [Crossref] [PubMed]
- Кунисаки С., Акияма Х, Номура М. и др. Сравнение хирургических исходов рака желудка у пациентов пожилого и среднего возраста.Am J Surg 2006; 191: 216-24. [Crossref] [PubMed]
- Ким Д.Й., Джу Дж.К., Рю С.И. и др. Клинико-патологическая характеристика рака желудка у пожилых пациентов: сравнение с пациентами молодого возраста. World J Gastroenterol 2005; 11: 22-6. [Crossref] [PubMed]
- Otsuji E, Fujiyama J, Takagi T, et al. Результаты тотальной гастрэктомии с расширенной лимфаденэктомией по поводу рака желудка у пожилых пациентов. J Surg Oncol 2005; 91: 232-6. [Crossref] [PubMed]
- Brenkman HJ, Goense L, Brosens LA, et al.Высокий выход лимфатических узлов связан с длительной выживаемостью у пожилых пациентов, перенесших лечебную гастрэктомию по поводу рака: голландское популяционное когортное исследование. Энн Сург Онкол 2017; 24: 2213-23. [Crossref] [PubMed]
- Kolodziejczyk P, Kulig J, Popiela T, et al. Исход хирургического вмешательства при раке желудка у пожилых пациентов. Гепатогастроэнтерология 2005; 52: 1911-5. [PubMed]
- Cho GS, Kim W., Kim HH, et al. Многоцентровое исследование безопасности лапароскопической субтотальной гастрэктомии при раке желудка у пожилых людей.Br J Surg 2009; 96: 1437-42. [Crossref] [PubMed]
- Liang YX, Deng JY, Guo HH и др. Характеристики и прогноз рака желудка у пациентов в возрасте> / = 70 лет. Всемирный журнал J Gastroenterol 2013; 19: 6568-78. [Crossref] [PubMed]
- Саиф М.В., Макрилия Н., Залонис А. и др. Рак желудка у пожилых людей: обзор. Eur J Surg Oncol 2010; 36: 709-17. [Crossref] [PubMed]
- Lim JH, Lee DH, Shin CM и др. Клинико-патологические особенности и хирургическая безопасность рака желудка у пожилых пациентов.J Korean Med Sci 2014; 29: 1639-45. [Crossref] [PubMed]
- Сайто Х., Осаки Т., Мураками Д. и др. Влияние возраста на прогноз у больных раком желудка. ANZ J Surg 2006; 76: 458-61. [Crossref] [PubMed]
- Maehara Y, Emi Y, Tomisaki S, et al. Возрастные особенности рака желудка у молодых и пожилых пациентов. Рак 1996; 77: 1774-80. [Crossref] [PubMed]
- Edge S, Byrd DR, Compton CC и др. Руководство по стадированию рака AJCC.7-е изд. Нью-Йорк: Springer, 2010. .
- Смит ЕС, Верхей М., Аллум В. и др. Рак желудка: Руководство ESMO по клинической практике по диагностике, лечению и последующему наблюдению. Энн Онкол 2016; 27: v38-49. [Crossref] [PubMed]
- Fujiwara Y, Fukuda S, Tsujie M, et al. Влияние возраста на выживаемость и заболеваемость у пациентов с раком желудка, перенесших гастрэктомию. Всемирный журнал J Gastrointest Oncol 2017; 9: 257-62. [Crossref] [PubMed]
- Endo S, Shimizu Y, Ikenaga M и др.Выживаемость после гастрэктомии при раке желудка у пациентов> / = 85 лет: ретроспективный анализ предрасположенности, сопоставленный по шкале. Хирургия 2017; 161: 984-94. [Crossref] [PubMed]
- Ямада Х., Шинохара Т., Такешита М. и др. Послеоперационные осложнения у самых старых больных раком желудка. Int J Surg 2013; 11: 467-71. [Crossref] [PubMed]
- Kiuchi J, Komatsu S, Ichikawa D, et al. Предполагаемые факторы риска послеоперационной пневмонии, влияющие на плохой прогноз у пациентов с раком желудка.Int J Clin Oncol 2016; 21: 920-6. [Crossref] [PubMed]
- Инокучи М., Кодзима К., Като К. и др. Факторы риска послеоперационных легочных осложнений после гастрэктомии по поводу рака желудка. Surg Infect (Larchmt) 2014; 15: 314-21. [Crossref] [PubMed]
- Лю К.А., Хуанг К.Х., Чен М.Х. и др. Сравнение хирургических результатов минимально инвазивной и открытой хирургии у восьмидесятилетних и старше по сравнению с более молодыми пациентами с раком желудка: ретроспективное когортное исследование.BMC Surg 2017; 17:68. [Crossref] [PubMed]
- de Miguel-Diez J, Lopez-de-Andres A, Hernandez-Barrera V, et al. Снижение заболеваемости и смертности среди госпитализированных пациентов, страдающих вентиляционной пневмонией: анализ национальной базы данных о выписках из больниц Испании с 2010 по 2014 год. Медицина (Балтимор) 2017; 96: e7625. [Crossref] [PubMed]
- Rello J, Ollendorf DA, Oster G, et al. Эпидемиология и исходы респираторно-ассоциированной пневмонии в большой базе данных США.Сундук 2002; 122: 2115-21. [Crossref] [PubMed]
- Анджеле М.К., Аяла А., Монфилс Б.А. и др. Тестостерон и / или низкий уровень эстрадиола: обычно необходимы, но иммунологически вредны для мужчин после травмы-кровоизлияния. J. Trauma 1998; 44: 78-85. [Crossref] [PubMed]
- Reade MC, Yende S, D’Angelo G и др. Различия в иммунном ответе могут объяснить более низкую выживаемость среди пожилых мужчин с пневмонией. Crit Care Med 2009; 37: 1655-62. [Crossref] [PubMed]
- Knoferl MW, Angele MK, Diodato MD и др.Женские половые гормоны регулируют функцию макрофагов после травмы-кровотечения и предотвращают повышение смертности от последующего сепсиса. Энн Сург 2002; 235: 105-12. [Crossref] [PubMed]
- Ян CK, Teng A, Lee DY, et al. Легочные осложнения после обширной абдоминальной хирургии: анализ Национальной программы улучшения качества хирургии. J Surg Res 2015; 198: 441-9. [Crossref] [PubMed]
- Hasukic S, Mesic D, Dizdarevic E, et al. Функция легких после лапароскопической и открытой холецистэктомии.Surg Endosc 2002; 16: 163-5. [Crossref] [PubMed]
- Fernandez-Bustamante A, Frendl G, Sprung J, et al. Послеоперационные легочные осложнения, ранняя смертность и пребывание в больнице после некардиоторакальной хирургии: многоцентровое исследование исследователей сети периоперационных исследований. JAMA Surg 2017; 152: 157-66. [Crossref] [PubMed]
- Colucci DB, Fiore JF Jr, Paisani DM, et al. Нарушение кашля и риск послеоперационных легочных осложнений после открытых операций на верхних отделах брюшной полости.Respir Care 2015; 60: 673-8. [Crossref] [PubMed]
- Lai-Fook SJ, Hyatt RE. Влияние возраста на модули упругости легких человека. J. Appl Physiol (1985) 2000; 89: 163-8. [PubMed]
- Janssens JP. Старение дыхательной системы: влияние на тесты функции легких и адаптация к нагрузке. Clin Chest Med 2005; 26: 469-84. vi-vii. [Crossref] [PubMed]
- Персиани Р., Антоначчи В., Бионди А. и др. Детерминанты хирургической заболеваемости при лечении рака желудка.J Am Coll Surg 2008; 207: 13-9. [Crossref] [PubMed]
- Lee KG, Lee HJ, Yang JY и др. Факторы риска, связанные с осложнениями после гастрэктомии по поводу рака желудка: ретроспективный анализ проспективно собранных данных на основе системы Clavien-Dindo. Журнал Gastrointest Surg 2014; 18: 1269-77. [Crossref] [PubMed]
- Gretschel S, Estevez-Schwarz L, Hunerbein M и др. Хирургия рака желудка у пожилых пациентов. World J Surg 2006; 30: 1468-74.[Crossref] [PubMed]
- Квон И.Г., Чо И., Гунер А. и др. Минимально инвазивная хирургия как вариант лечения рака желудка у пожилых людей: сравнение с открытой операцией у пациентов 80 лет и старше. Хирургия эндоскопии 2015; 29: 2321-30. [Crossref] [PubMed]
- Инокучи М., Таниока Т., Накагава М. и др. Лапароскопическая дистальная гастрэктомия возможна у очень пожилых пациентов по сравнению с открытой дистальной гастрэктомией. J Invest Surg 2017.1-7. [Crossref] [PubMed]
- Ясуда К., Сонода К., Широшита Х. и др.Лапароскопически ассистированная дистальная резекция желудка при раннем раке желудка у пожилых людей. Br J Surg 2004; 91: 1061-5. [Crossref] [PubMed]
- Окумура Н., Сон Т., Ким Ю.М. и др. Роботизированная гастрэктомия у пожилых пациентов с раком желудка: сравнение с роботизированной гастрэктомией у молодых пациентов и лапароскопической гастрэктомией у пожилых. Рак желудка 2016; 19: 1125-34. [Crossref] [PubMed]
- Китано С., Сираиси Н., Фуджи К. и др. Рандомизированное контролируемое исследование по сравнению открытой и лапароскопической дистальной гастрэктомии для лечения рака желудка на ранних стадиях: промежуточный отчет.Хирургия 2002; 131: S306-11. [Crossref] [PubMed]
- Suzuki S, Накамура Т., Иманиши Т. и др. Пневмоперитонеум с углекислым газом не привел к серьезным осложнениям у пожилых людей во время лапароскопической дистальной гастрэктомии. Энн Сург Онкол 2015; 22: 1548-54. [Crossref] [PubMed]
- Ямада Х, Кодзима К., Инокучи М. и др. Гастрэктомия с применением лапароскопии у пациентов старше 80 лет. J Surg Res 2010; 161: 259-63. [Crossref] [PubMed]
- Tokunaga M, Hiki N, Fukunaga T, et al.Имеет ли значение возраст для показаний к лапароскопической гастрэктомии? J Gastrointest Surg 2008; 12: 1502-7. [Crossref] [PubMed]
- Кунисаки С., Макино Н., Такагава Р. и др. Эффективность лапароскопической дистальной гастрэктомии при раке желудка у пожилых людей. Surg Endosc 2009; 23: 377-83. [Crossref] [PubMed]
- Ким К.Х., Ким М.С., Юнг Г.Дж. Является ли частота послеоперационных осложнений после лапароскопической гастрэктомии выше у пожилых пациентов, чем у более молодых пациентов? Мир J Surg Oncol 2014; 12: 97.[Crossref] [PubMed]
- Wang JF, Zhang SZ, Zhang NY, et al. Лапароскопическая гастрэктомия в сравнении с открытой гастрэктомией у пожилых пациентов с раком желудка: систематический обзор и метаанализ. Мир J Surg Oncol 2016; 14: 90. [Crossref] [PubMed]
- Hartgrink HH, van de Velde CJ, Putter H, et al. Расширенная лимфодиссекция при раке желудка: кому может быть полезно? Окончательные результаты рандомизированного голландского группового исследования рака желудка. Дж. Клин Онкол 2004; 22: 2069-77.[Crossref] [PubMed]
- Rausei S, Ruspi L, Rosa F и др. Расширенная лимфаденэктомия у пациентов пожилого возраста и / или пациентов с очень коморбидным раком желудка: ретроспективное многоцентровое исследование. Eur J Surg Oncol 2016; 42: 1881-9. [Crossref] [PubMed]
- Passot G, Vaudoyer D, Messager M и др. Необходима ли расширенная лимфаденэктомия пожилым пациентам с аденокарциномой желудка? Энн Сург Онкол 2016; 23: 2391-7. [Crossref] [PubMed]
- Eguchi T, Takahashi Y, Ikarashi M, et al.Необходима ли расширенная лимфодиссекция при раке желудка у пожилых пациентов? Eur J Surg 2000; 166: 949-53. [Crossref] [PubMed]
- Такешита Х., Итикава Д., Комацу С. и др. Хирургические результаты гастрэктомии у пожилых больных раком желудка. World J Surg 2013; 37: 2891-8. [Crossref] [PubMed]
- Cunningham D, Allum WH, Stenning SP, et al. Периоперационная химиотерапия по сравнению с хирургическим вмешательством при резектабельном раке пищевода.N Engl J Med 2006; 355: 11-20. [Crossref] [PubMed]
- Ychou M, Boige V, Pignon JP, et al. Периоперационная химиотерапия в сравнении с хирургическим вмешательством при резектабельной гастроэзофагеальной аденокарциноме: многоцентровое исследование III фазы FNCLCC и FFCD. Дж. Клин Онкол 2011; 29: 1715-21. [Crossref] [PubMed]
- Brenner B, Shah MA, Karpeh MS, et al. Фаза II испытания неоадъювантного цисплатина-фторурацила с последующим послеоперационным внутрибрюшинным введением флоксуридин-лейковорин у пациентов с местнораспространенным раком желудка.Энн Онкол 2006; 17: 1404-11. [Crossref] [PubMed]
- Аль-Батран С.Е., Полигк С., Хоманн Н. и др. Возможность сочетания трех препаратов химиотерапии у пожилых пациентов с раком пищевода и желудка: рандомизированное исследование Arbeitsgemeinschaft Internistische Onkologie (FLOT65 +). Eur J Cancer 2013; 49: 835-42. [Crossref] [PubMed]
- Lorenzen S, Pauligk C, Homann N, et al. Возможность периоперационной химиотерапии с инфузией 5-ФУ, лейковорина и оксалиплатина с (FLOT) или без (FLO) доцетакселом у пожилых пациентов с местнораспространенным раком пищевода и желудка.Br J Cancer 2013; 108: 519-26. [Crossref] [PubMed]
- Stahl M, Walz MK, Stuschke M, et al. Сравнение фазы III предоперационной химиотерапии с химиолучевой терапией у пациентов с местнораспространенной аденокарциномой пищеводно-желудочного перехода. Дж. Клин Онкол 2009; 27: 851-6. [Crossref] [PubMed]
- Уолш Т.Н., Нунан Н., Голливуд Д. и др. Сравнение мультимодальной терапии и хирургии аденокарциномы пищевода. N Engl J Med 1996; 335: 462-7.[Crossref] [PubMed]
- Леонг Т., Смитерс Б.М., Хаустерманс К. и др. TOPGEAR: рандомизированное исследование фазы III периоперационной химиотерапии ECF с предоперационной химиолучевой терапией или без нее для резектабельного рака желудка: промежуточные результаты международного межгруппового исследования AGITG, TROG, EORTC и CCTG. Энн Сург Онкол 2017; 24: 2252-8. [Crossref] [PubMed]
- Shapiro J, van Lanschot JJ, Hulshof M, et al. Неоадъювантная химиолучевая терапия в сочетании с хирургическим вмешательством по сравнению с только хирургическим вмешательством при раке пищевода или соединения (CROSS): долгосрочные результаты рандомизированного контролируемого исследования.Ланцет Онкол 2015; 16: 1090-8. [Crossref] [PubMed]
- Сеть NCC. Рекомендации NCCN по раку желудка. Версия 4.2017. По состоянию на 6 октября 2017 г. Доступно в Интернете: https://www.nccn.org/professionals/physician_gls/pdf/gastric.pdf
- Bang YJ, Kim YW, Yang HK, et al. Адъювант капецитабин и оксалиплатин при раке желудка после гастрэктомии D2 (CLASSIC): открытое рандомизированное контролируемое исследование фазы 3. Ланцет 2012; 379: 315-21. [Crossref] [PubMed]
- Сасако М., Сакурамото С., Катай Х. и др.Пятилетние результаты рандомизированного исследования III фазы, сравнивающего адъювантную химиотерапию с S-1 и только хирургическое вмешательство при раке желудка II или III стадии. Дж. Клин Онкол 2011; 29: 4387-93. [Crossref] [PubMed]
- Jeong JW, Kwon IG, Son YG, et al. Может ли адъювантная химиотерапия после операции принести пользу пожилым пациентам с распространенным раком желудка? J Рак желудка 2016; 16: 260-5. [Crossref] [PubMed]
- Jo JC, Baek JH, Koh SJ, et al. Адъювантная химиотерапия для пожилых пациентов (в возрасте 70 лет и старше) с раком желудка после гастрэктомии с расслоением D2: опыт единого центра в Корее.Asia Pac J Clin Oncol 2015; 11: 282-7. [Crossref] [PubMed]
- Jin Y, Qiu MZ, Wang DS и др. Адъювантная химиотерапия для пожилых пациентов с раком желудка после гастрэктомии D2. PLoS One 2013; 8: e53149. [Crossref] [PubMed]
- Ханадзаки К., Мочизуки Ю., Игараси Дж. И др. Послеоперационная химиотерапия у пожилых пациентов с распространенным раком желудка. Гепатогастроэнтерология 2000; 47: 1761-4. [PubMed]
- Маэхара Ю., Ямамото М., Эндо К. и др.Послеоперационная химиотерапия рака желудка у пожилых людей. Химиотерапия 1994; 40: 279-86. [Crossref] [PubMed]
- Macdonald JS, Smalley SR, Benedetti J, et al. Химиолучевая терапия после хирургического вмешательства по сравнению с хирургическим вмешательством при аденокарциноме желудка или пищеводно-желудочного перехода. N Engl J Med 2001; 345: 725-30. [Crossref] [PubMed]
- Smalley SR, Benedetti JK, Haller DG, et al. Обновленный анализ межгруппового исследования под руководством SWOG 0116: исследование фазы III адъювантной радиохимиотерапии по сравнению с наблюдением после радикальной резекции рака желудка.Дж. Клин Онкол 2012; 30: 2327-33. [Crossref] [PubMed]
- Yeh JM, Tramontano AC, Hur C, et al. Сравнительная эффективность адъювантной химиолучевой терапии после резекции желудка у пожилых пациентов с аденокарциномой желудка: исследование SEER-Medicare. Рак желудка, 2017. [Epub перед печатью]. [Crossref] [PubMed]
- Park SH, Sohn TS, Lee J и др. Испытание фазы III для сравнения адъювантной химиотерапии капецитабином и цисплатином с одновременной химиолучевой терапией при раке желудка: окончательный отчет об адъювантной химиолучевой терапии в испытании опухолей желудка, включая анализ выживаемости и подгруппы.Дж. Клин Онкол 2015; 33: 3130-6. [Crossref] [PubMed]
- Zhou ML, Kang M, Li GC, et al. Сравнение послеоперационной химиолучевой терапии с химиотерапией при удалении R0 рака желудка с лимфодиссекцией D2: современный метаанализ. Мировой журнал J Surg Oncol 2016; 14: 209. [Crossref] [PubMed]
- Dikken JL, Jansen EP, Cats A, et al. Влияние объема хирургического вмешательства и послеоперационной химиолучевой терапии на рецидивы рака желудка. Дж. Клин Онкол 2010; 28: 2430-6.[Crossref] [PubMed]
- Ли Дж., Лим Д.Х., Ким С. и др. Испытание фазы III, сравнивающее капецитабин плюс цисплатин и капецитабин плюс цисплатин с одновременной лучевой терапией капецитабином при полностью удаленном раке желудка с лимфодиссекцией D2: исследование ARTIST. Дж. Клин Онкол 2012; 30: 268-73. [Crossref] [PubMed]
- Hwang IG, Ji JH, Kang JH, et al. Многоцентровое открытое рандомизированное исследование фазы III химиотерапии первой линии с монотерапией капецитабином по сравнению с капецитабином плюс оксалиплатин у пожилых пациентов с распространенным раком желудка.Журнал Гериатр Онкол 2017; 8: 170-5. [Crossref] [PubMed]
- Bang YJ, Van Cutsem E, Feyereislova A, et al. Трастузумаб в сочетании с химиотерапией по сравнению с одной химиотерапией для лечения HER2-положительного распространенного рака желудка или желудочно-пищеводного перехода (ToGA): открытое рандомизированное контролируемое исследование фазы 3. Ланцет 2010; 376: 687-97. [Crossref] [PubMed]
- Каннингем Д., Старлинг Н., Рао С. и др. Капецитабин и оксалиплатин при распространенном раке пищевода и желудка.N Engl J Med 2008; 358: 36-46. [Crossref] [PubMed]
- Ohtsu A, Shah MA, Van Cutsem E, et al. Бевацизумаб в сочетании с химиотерапией в качестве терапии первой линии при распространенном раке желудка: рандомизированное, двойное слепое, плацебо-контролируемое исследование фазы III. Дж. Клин Онкол 2011; 29: 3968-76. [Crossref] [PubMed]
- Sasaki Y, Iwasa S, Okazaki S, et al. Исследование фазы II комбинированной терапии пероральным S-1 и цисплатином у пожилых пациентов с распространенным раком желудка.Рак желудка, 2017. [Epub перед печатью]. [Crossref] [PubMed]
- Bando H, Yamada Y, Tanabe S, et al. Эффективность и безопасность комбинированной терапии S-1 и оксалиплатином у пожилых пациентов с распространенным раком желудка. Рак желудка 2016; 19: 919-26. [Crossref] [PubMed]
- Чжун Д.Т., Ву Р.П., Ван XL и др. Комбинированная химиотерапия с S-1 и оксалиплатином (SOX) в качестве лечения первой линии у пожилых пациентов с распространенным раком желудка. Патол Онкол Рез 2015; 21: 867-73.[Crossref] [PubMed]
doi: 10.21037 / aos.2017.11.02
Цитируйте эту статью как: Pak LM, Wang J. Подходящее лечение для пожилых пациентов с раком желудка. Арт-Сург 2017; 1: 4.
Долгосрочная выживаемость пожилого пациента с распространенным раком желудка после комбинированной терапии: отчет о болезни и обзор литературы | BMC Cancer
Thun MJ, DeLancey JO, Center MM, Jemal A, Ward EM. Глобальное бремя рака: приоритеты профилактики. Канцерогенез.2010. 31 (1): 100–10.
CAS Статья Google Scholar
Всемирная организация здравоохранения (2014) GLOBOCAN2012: Расчетная заболеваемость раком MaPWi.
Лю Дж, Чен Л. Текущее состояние и прогресс в лечении рака желудка с метастазами в печень. Чин Мед Дж. 2011; 124 (3): 445–56.
PubMed Google Scholar
Strong VE, Wu AW, Selby LV, Gonen M, Hsu M, Song KY, Park CH, Coit DG, Ji JF, Brennan MF.Различия в выживаемости при раке желудка между США и Китаем. J Surg Oncol. 2015; 112 (1): 31–7.
Артикул Google Scholar
Вигано Л., Веллоне М., Ферреро А., Джулианте Ф., Нуццо Дж., Капуссотти Л. Резекция печени при метастазах рака желудка. Гепатогастроэнтерология. 2013. 60 (123): 557–62.
PubMed Google Scholar
Hwang SE, Yang DH, Kim CY.Факторы прогноза выживаемости у пациентов с рецидивом печени после радикальной резекции рака желудка. World J Surg. 2009. 33 (7): 1468–72.
Артикул Google Scholar
Сакамото Ю., Сано Т., Шимада К., Эсаки М., Сака М., Фукагава Т., Катай Х., Косуге Т., Сасако М. Благоприятные показания для гепатэктомии у пациентов с метастазами в печени из-за рака желудка. J Surg Oncol. 2007. 95 (7): 534–9.
Артикул Google Scholar
Такемура Н., Сайура А., Кога Р., Арита Дж., Йошиока Р., Оно Й, Хики Н., Сано Т., Ямамото Дж., Кокудо Н. и др. Отдаленные результаты хирургической резекции метастазов рака желудка в печень: анализ 64 макроскопически полных резекций. Langenbeck’s Arch Surg. 2012. 397 (6): 951–7.
Артикул Google Scholar
Фукути М., Исигуро Т., Огата К., Сузуки О., Кумагаи Ю., Исибаши К., Исида Х., Кувано Х., Мочики Э. Прогностическая роль конверсионной хирургии при неоперабельном раке желудка.Энн Сург Онкол. 2015; 22 (11): 3618–24.
Артикул Google Scholar
Fujitani K, Yang HK, Mizusawa J, Kim YW, Terashima M, Han SU, Iwasaki Y, Hyung WJ, Takagane A, Park DJ, et al. Гастрэктомия плюс химиотерапия по сравнению с одной химиотерапией при распространенном раке желудка с одним неизлечимым фактором (REGATTA): рандомизированное контролируемое исследование фазы 3. Ланцет Онкол. 2016; 17 (3): 309–18.
CAS Статья Google Scholar
Edge SB, Комптон CC. Американский объединенный комитет по раку: седьмое издание руководства AJCC по стадированию рака и будущее TNM. Энн Сург Онкол. 2010. 17 (6): 1471–4.
Артикул Google Scholar
Маккартер, доктор медицины, Фонг Ю. Роль хирургической циторедукции в комплексном лечении рака. Энн Сург Онкол. 2001. 8 (1): 38–43.
CAS Статья Google Scholar
Саиди РФ, Ремайн С.Г., Дудрик П.С., Ханна Н.Н. Есть ли роль паллиативной гастрэктомии у пациентов с раком желудка IV стадии? World J Surg. 2006; 30 (1): 21–7.
Артикул Google Scholar
Cheon S, Rha S, Jeung HC, Im CK, Kim S, Kim H, Ahn J, Roh J, Noh S, Chung H. Выживаемость комбинированной лечебной резекции желудка (резекция D2) и печень у больных раком желудка с метастазами в печень. Энн Онкол.2008. 19 (6): 1146–53.
CAS Статья Google Scholar
Сакамото Ю., Охьяма С., Ямамото Дж., Ямада К., Секи М., Охта Ки, Кокудо Н., Ямагути Т., Муто Т., Макуучи М. Хирургическая резекция метастазов рака желудка в печень: анализ 17 -летний опыт работы с 22 пациентами. Операция. 2003. 133 (5): 507–11.
Артикул Google Scholar
Номура Т., Камио Ю., Такасу Н., Мория Т., Такешита А., Мизутани М., Хачия О, Хираи И., Кимура В.Внутрипеченочные микрометастазы вокруг метастазов рака желудка в печень. J. Hepato-Bili-Pancreat Surg. 2009. 16 (4): 493–501.
Артикул Google Scholar
Какеджи Ю., Морита М., Маэхара Ю. Стратегии лечения метастазов в печень от рака желудка. Хирург сегодня. 2010. 40 (4): 287–94.
Артикул Google Scholar
Ким Х.Р., Ха Чхон С., Ли КХ, Рюн Ан Дж, Чжунг Х.С., Сук Ли С., Чхоль Чунг Х, Хун Но С., Янг Ра С.Эффективность и возможность радиочастотной абляции метастазов аденокарциномы желудка в печень. Int J Hyperth. 2010. 26 (4): 305–15.
Артикул Google Scholar
Ким Хо, Хван С.И., Хонг ХП, Ю Ч. Радиочастотная абляция метахронных метастазов в печень при раке желудка. Surg Laparosc Endosc Percutan Tech. 2009. 19 (3): 208–12.
Артикул Google Scholar
Boutros C, Somasundar P, Garrean S, Saied A, Espat N. Микроволновая коагуляционная терапия опухолей печени: обзор литературы и критический анализ. Surg Oncol. 2010; 19 (1): e22–32.
CAS Статья Google Scholar
Yu J, Liang P, Yu X, Liu F, Chen L, Wang Y. Сравнение микроволновой абляции и биполярной радиочастотной абляции с зондом с внутренним охлаждением: результаты в печени свиньи ex vivo и in vivo.Eur J Radiol. 2011. 79 (1): 124–30.
Артикул Google Scholar
Mayo SC, Pawlik TM. Термическая абляционная терапия вторичных злокачественных новообразований печени. Рак J. 2010; 16 (2): 111–7.
Артикул Google Scholar
Chen J, Tang Z, Dong X, Gao S, Fang H, Wu D, Xiang D, Zhang S. Радиочастотная абляция метастазов в печень при раке желудка. Eur J Surg Oncol.2013. 39 (7): 701–6.
CAS Статья Google Scholar
Guner A, Son T, Cho I, Kwon IG, An JY, Kim HI, Cheong JH, Noh SH, Hyung WJ. Лечение метастазов в печени аденокарциномы желудка, направленное на печень: сравнение резекции печени и радиочастотной абляции. Рак желудка. 2016; 19 (3): 951–60.
CAS Статья Google Scholar
Нинхуэзер Х., Кунцманн Р., Сисич Л., Бланк С., Стровицк М.Дж., Брукнер Т., Ягер Д., Вайхерт В., Ульрих А., Бюхлер М.В. и др. Хирургия рака желудка и рака пищевода: имеет ли значение возраст? J Surg Oncol. 2015; 112 (4): 387–95.
Артикул Google Scholar
Шмидт Т., Аллдингер И., Бланк С., Клозе Дж., Спрингфельд С., Драйкхаузен Л., Вайхерт В., Гренахер Л., Брукнер Т., Лордик Ф. и др. Хирургия при раке пищевода и желудка с метастатическим поражением: лечение, прогноз и предоперационный отбор пациентов.Eur J Surg Oncol. 2015; 41 (10): 1340–7.
CAS Статья Google Scholar
Ассоциация JGC. Японское руководство по лечению рака желудка, 2014 г. (вер. 4). Рак желудка. 2017; 20 (1): 1–19.
Артикул Google Scholar
De La Cruz LM, Harhay MO, Zhang P, Ugras S. Влияние неоадъювантной химиотерапии на подтип рака груди: меняется ли подтип, и если да, то как? : Профиль ИГХ и неоадъювантная химиотерапия.Энн Сург Онкол. 2018; 25 (12): 3535–40.
Артикул Google Scholar
Ниикура Н., Томотаки А., Мията Х., Ивамото Т., Кавай М., Анан К., Хаяси Н., Аоги К., Исида Т., Масуока Х. и др. Изменения в опухолевой экспрессии HER2 и статуса рецепторов гормонов после неоадъювантной химиотерапии у 21 755 пациентов из японского регистра рака молочной железы. Энн Онкол. 2016; 27 (3): 480–7.
CAS Статья Google Scholar
Рак желудка у пожилых людей: обзор
Резюме
Цели
Рак желудка у пожилых людей представляет собой отдельную сущность со специфическими клинико-патологическими характеристиками, и большинство больных относятся к этой возрастной группе.Субтотальная или полная гастрэктомия с радикальной лимфодиссекцией, адъювантная химиолучевая терапия или периоперационная химиотерапия представляют собой единственные потенциально лечебные варианты лечения и, по-видимому, выполняются с приемлемыми показателями заболеваемости и смертности у отдельных пожилых пациентов. Опубликованные исследования очень ограничены из-за строгого отбора и недостаточной представленности пожилых пациентов в клинических испытаниях. Был проведен обзор текущих рекомендаций и практики.
Методы
Был проведен всесторонний обзор литературы с поиском в Medline статей, опубликованных с 1974 года, с использованием ключевых слов «рак желудка», «пожилые люди» и «лечение».
Наблюдения
Данные показывают, что пожилые пациенты, которые соответствуют критериям включения в клинические испытания, испытывают те же преимущества и токсичность химиотерапии, что и более молодые пациенты. Подходящие пожилые пациенты с операбельным раком желудка должны быть кандидатами на стандартную хирургическую резекцию при условии учета предоперационных сопутствующих заболеваний. В случае местнораспространенного заболевания следует добавить периоперационную химиотерапию или послеоперационную химиолучевую терапию.Похоже, что паллиативная системная химиотерапия продлевает выживаемость при рецидивирующих и метастатических заболеваниях.
Выводы
Один только хронологический возраст не является достаточной причиной для отказа от лечебного или паллиативного лечения пожилому пациенту с раком желудка. Статус работоспособности недостаточен для оценки общего состояния пожилых пациентов, и необходимо учитывать их функциональные, социальные и психические факторы.
Ключевые слова
Рак желудка
Пожилые
Лечение
Гастрэктомия
Химиотерапия
Рекомендуемые статьиЦитирующие статьи (0)
Полный текстCopyright © 2010 Elsevier Ltd.Все права защищены.
Рекомендуемые статьи
Цитирующие статьи
Симптомы и лечение рака желудка — Заболевания и состояния
Рекомендуемые методы лечения рака желудка будут зависеть от вашего общего состояния здоровья и степени распространения рака.
В большинстве больниц работают многопрофильные бригады, состоящие из разных специалистов (см. Ниже), которые работают вместе, чтобы спланировать и провести наилучшее лечение с учетом ваших обстоятельств.
Не стесняйтесь обсуждать лечение со своей командой в любое время и задавать вопросы.
Ваш план лечения
Основными видами лечения рака желудка являются хирургия, химиотерапия и лучевая терапия. Вам может быть назначено одно из этих методов лечения или их комбинация.
Если рекомендовано хирургическое вмешательство, вы можете предварительно пройти курс химиотерапии. Если опухоль находится в верхней части желудка, включая соединение между пищеводом и желудком, вам также может быть назначена лучевая терапия перед операцией.
Хирургия в основном используется, если рак желудка диагностируется на ранней стадии, тогда как химиотерапия и лучевая терапия, как правило, используются, когда заболевание диагностируется на более поздней стадии.
По возможности, основной целью лечения является полное удаление опухоли и любых других раковых клеток в организме. Подсчитано, что излечение возможно в 20-30% случаев рака желудка.
Если опухоль удалить невозможно, врачи постараются не допустить, чтобы опухоль стала больше и не причиняла дальнейшего вреда вашему организму. Это можно сделать с помощью хирургического вмешательства или химиотерапии.
В некоторых случаях невозможно устранить рак или замедлить его развитие.В этом случае ваше лечение будет направлено на облегчение ваших симптомов и обеспечение максимального комфорта, обычно с помощью операции или лучевой терапии.
Относительно новый препарат под названием трастузумаб (см. Ниже) также может использоваться для лечения некоторых типов запущенного рака желудка.
Ваша медицинская бригада обсудит с вами наиболее подходящие методы лечения.
Хирургия
Если у вас диагностирован рак желудка на ранней стадии, возможно, он удастся полностью удалить во время операции.
В некоторых случаях можно провести тонкую гибкую трубку (эндоскоп) по пищеводу (пищеводу) вместо того, чтобы делать надрезы в животе. Это называется эндоскопической хирургией, и ее можно использовать для удаления образца опухоли для исследования (биопсии). Его также можно использовать для полного удаления опухоли, если рак желудка диагностирован на ранней стадии.
Однако, если рак распространился за пределы желудка, полностью удалить его может быть невозможно. Если это так, вам все равно может быть сделана операция по удалению любого рака, блокирующего ваш желудок, чтобы облегчить симптомы.Это будет зависеть от того, можно ли контролировать ваши симптомы, а также от рисков и побочных эффектов проведения серьезной операции.
Любая операция при раке желудка требует большой операции и длительного периода восстановления. Если вам сделали операцию по поводу рака желудка, вам обычно нужно оставаться в больнице около 2 недель. Вам также понадобится несколько недель дома, чтобы выздороветь.
Операция по удалению желудка
Возможно, вам потребуется удалить часть или весь желудок.
Операция по удалению части желудка известна как частичная или субтотальная гастрэктомия, а операция по удалению всего желудка известна как полная гастрэктомия.В некоторых случаях хирург может удалить часть пищевода, а также весь желудок, используя процедуру, известную как эзофагогастрэктомия.
Эти операции могут выполняться с использованием либо большого разреза на животе (открытая операция), либо нескольких меньших разрезов, через которые можно провести хирургические инструменты (лапароскопическая операция или операция «замочная скважина»). Оба эти метода выполняются под общим наркозом, что означает, что вы будете без сознания на протяжении всей процедуры.
Во время этих операций ваш хирург также удалит лимфатические узлы (маленькие железы, которые помогают бороться с инфекцией), ближайшие к раку.Возможно, ваш рак желудка распространился на эти лимфатические узлы, и их удаление помогает предотвратить возвращение рака.
Частичная резекция желудка
Если ваш рак находится в нижней части желудка, вам может потребоваться частичная гастрэктомия, чтобы удалить его.
После операции ваш живот будет меньше, чем был до операции. Однако верхняя часть желудка, в которую впадает пищевод, не пострадает.
Тотальная гастрэктомия или эзофагогастрэктомия
Если ваш рак находится в средней или верхней части желудка, вам может потребоваться полная гастрэктомия.Если рак находится близко к концу пищевода, там, где он встречается с желудком, вам может потребоваться эзофагогастрэктомия.
Если у вас полная резекция желудка, конец пищевода будет соединен с верхушкой тощей кишки (верхняя часть тонкой кишки). Если у вас есть эзофагогастрэктомия, оставшаяся часть пищевода присоединится к тощей кишке.
Операция по облегчению симптомов
Если рак желудка распространился за пределы желудка, удалить его хирургическим путем может быть невозможно.
Однако, если ваш желудок серьезно пострадал от рака, это может вызвать закупорку, которая препятствует правильному перевариванию пищи. Заложенный желудок может вызывать такие симптомы, как боль в животе, рвота и чувство сытости после еды.
Если желудок заблокирован, есть несколько вариантов:
- стентирование — стент представляет собой трубку из пластмассы или проволочной сетки, вводимую через пищевод с помощью эндоскопа под местной анестезией; после установки стент расширяется и открывает желудок
- частичная или полная гастрэктомия — для устранения закупорки и улучшения симптомов
- шунтирование — операция, при которой часть желудка, расположенная над блокировкой, соединяется с тонкой кишкой, в результате чего заблокированная часть желудка не попадает в пищеварительную систему
Химиотерапия
Химиотерапия — это специальное лечение рака, при котором используются лекарства, называемые цитотоксическими лекарствами, для остановки деления и размножения раковых клеток.По мере того, как оно циркулирует по вашему телу, лекарство может нацеливаться на раковые клетки в вашем желудке и любые клетки, которые могли распространиться на другие части вашего тела.
Вы можете пройти химиотерапию рака желудка перед операцией, чтобы уменьшить количество рака, который необходимо удалить во время операции. Химиотерапию также можно использовать после операции, чтобы уничтожить оставшиеся раковые клетки и предотвратить рецидив рака.
Химиотерапия также может помочь замедлить прогрессирование рака и облегчить симптомы более запущенного рака желудка, который может не подходить для хирургического вмешательства.
If можно вводить перорально (в виде таблеток) или внутривенно (путем инъекции или капельного введения через вену непосредственно в кровоток) или их комбинации.
Внутривенная химиотерапия обычно проводится в больнице, а пероральная химиотерапия — дома. Химиотерапия часто проводится циклами, каждый обычно длится около трех недель.
В качестве альтернативы химиотерапия может вводиться через небольшую помпу, которая дает вам постоянную низкую дозу в течение нескольких недель или месяцев.Насосы портативны, и их можно носить дома, что означает меньшее количество поездок в больницу.
Побочные эффекты химиотерапии
Химиотерапия предотвращает быстрый рост раковых клеток. Однако он также разрушает незлокачественные клетки, такие как волосяные фолликулы, красные и белые кровяные тельца. Побочные эффекты могут включать:
- усталость
- тошнота и рвота
- повреждение нерва (периферическая невропатия)
- Выпадение волос
- понос
- анемия (недостаток эритроцитов)
- потеря веса
- изменения кожи, такие как покраснение, отек и покалывание в ладонях рук и / или подошвах ног
Побочные эффекты, которые вы испытываете после химиотерапии, будут зависеть от типа химиотерапии и количества необходимых вам сеансов лечения.Вам сообщат, к кому обратиться, если вы испытываете серьезные побочные эффекты от химиотерапии, и очень важно, чтобы эта контактная информация была тщательно записана.
Если вы испытываете тошноту и рвоту в результате химиотерапии, вы можете принять лекарство от болезней, чтобы противостоять этому. Его можно вводить внутривенно (путем инъекции непосредственно в кровоток) одновременно с химиотерапией.
Побочные эффекты химиотерапии будут длиться до тех пор, пока длится ваш курс лечения.По окончании лечения волосяные фолликулы и клетки крови восстановятся. Это означает, что ваши волосы вырастут снова, хотя они могут выглядеть или ощущаться иначе, чем до химиотерапии (например, они могут быть немного другого цвета, мягче или вьющимися, чем раньше).
Радиотерапия
Радиотерапия использует лучи высокоэнергетического излучения для уничтожения раковых клеток. Его не часто используют для лечения рака желудка, потому что есть риск того, что другие органы, расположенные рядом с вашим желудком, могут быть повреждены в результате лечения.
Однако, если у вас запущенный рак желудка, вызывающий боль или кровотечение, вам может потребоваться лучевая терапия. В некоторых случаях после операции вам могут пройти химиотерапию и / или лучевую терапию, чтобы предотвратить рецидив рака желудка.
Если рак кровоточит медленно и вызывает анемию, можно использовать одну фракцию лучевой терапии, чтобы попытаться предотвратить дальнейшее кровотечение.
Если вам нужна лучевая терапия, ваше лечение обычно начинается через 2 или 3 месяца после операции или химиотерапии, чтобы дать вашему организму шанс выздороветь.Это безболезненная процедура, когда вы лежите под аппаратом лучевой терапии, пока он направляет излучение на ваш живот. Вас назначит рентгенолог (специалист по лучевой терапии), чтобы аппарат нацелился на раковые клетки и избегал как можно большего количества здоровых тканей.
Радиотерапия часто включает сеансы лечения 5 дней в неделю. Каждое занятие длится всего несколько минут. После этого излучение не остается в вашем организме, и в перерывах между процедурами находиться рядом с другими людьми совершенно безопасно.
Как долго вам понадобится лучевая терапия, будет зависеть от того, как она используется. Радиотерапия, используемая после операции для предотвращения рецидива рака желудка, обычно длится 5 недель. Если его используют для контроля симптомов прогрессирующего рака желудка, он может длиться всего 1-2 недели.
Побочные эффекты лучевой терапии
После лучевой терапии у вас могут возникнуть следующие побочные эффекты:
- усталость
- тошнота
- понос
- раздражение и потемнение кожи в месте лечения
Эти побочные эффекты обычно проходят в течение нескольких недель после окончания лечения.
Трастузумаб
Трастузумаб (продается под торговой маркой Герцептин) — это лекарство, используемое для лечения рака груди и некоторых случаев распространенного рака желудка.
Некоторые виды рака желудка стимулируются белком, который называется рецептором 2 эпидермального фактора роста человека (HER2). Трастузумаб блокирует действие этого белка. Это не лечит рак желудка, но может замедлить его рост и увеличить время выживания.
Если у вас диагностирован рак желудка на поздней стадии и анализы показывают высокий уровень белка HER2 в раковых клетках, ваши врачи могут порекомендовать лечение с использованием комбинации химиотерапии и трастузумаба.
Трастузумаб вводят внутривенно, капельно, и вам предстоит лечение в больнице. Каждый сеанс лечения занимает до 1 часа, и вам обычно требуется сеанс один раз в 3 недели.
Трастузумаб может вызывать побочные эффекты, в том числе проблемы с сердцем. Поэтому он может не подходить, если у вас проблемы с сердцем, такие как стенокардия, неконтролируемое высокое кровяное давление (гипертония) или заболевание сердечного клапана. Если вам нужно принять трастузумаб, вам также потребуются регулярные анализы сердца, чтобы проверить наличие каких-либо проблем.
Другие побочные эффекты трастузумаба могут включать:
- первоначальная аллергическая реакция на лекарство, которая может вызвать тошноту, хрип, озноб и жар
- понос
- усталость
- боли
Рак желудка: Статистика | Cancer.Net
НА ЭТОЙ СТРАНИЦЕ: Вы найдете информацию о количестве людей, у которых ежегодно диагностируется рак желудка. Вы также прочтете общую информацию о том, как пережить болезнь.Помните, что выживаемость зависит от нескольких факторов. Используйте меню для просмотра других страниц.
В этом году примерно 26 560 человек (16 160 мужчин и 10 400 женщин) в Соединенных Штатах будет диагностирован рак желудка.
По оценкам, в этом году от этой болезни погибнет 11 180 (6740 мужчин и 4440 женщин).
Рак желудка чаще всего встречается у пожилых людей. Около 60% людей, которым поставлен диагноз, старше 64 лет. Средний возраст постановки диагноза — 68 лет.
Заболеваемость раком желудка варьируется в разных частях мира.В Соединенных Штатах за последнее десятилетие уровень заболеваемости снижался на 1,5% ежегодно. Частично это снижение может быть связано с использованием антибиотиков для лечения инфекций. Эти лекарства могут убить H. pylori (см. Факторы риска ). Однако рак желудка по-прежнему остается одним из наиболее распространенных видов рака и одной из основных причин смерти от рака во всем мире.
Пятилетняя выживаемость показывает, какой процент людей живет не менее пяти лет после обнаружения рака. Процент означает, сколько из 100.5-летняя выживаемость для людей с раком желудка составляет 32%. Эта статистика отражает тот факт, что 62% людей с раком желудка диагностируются после того, как рак уже распространился за пределы того места, где он возник. Если рак желудка обнаружен до того, как он распространился, 5-летняя выживаемость обычно выше, но зависит от стадии рака, обнаруженной во время операции.
Если рак диагностируется и лечится до того, как он распространился за пределы желудка, 5-летняя выживаемость составляет 70%. Если рак распространился на окружающие ткани или органы и / или региональные лимфатические узлы, 5-летняя выживаемость составляет 32%.Если рак распространился на отдаленную часть тела, 5-летняя выживаемость составляет 6%.
Важно помнить, что статистика выживаемости людей с раком желудка является приблизительной. Оценка основана на ежегодных данных, основанных на количестве людей с этим раком в Соединенных Штатах. Также каждые 5 лет специалисты измеряют статистику выживаемости. Таким образом, оценка может не отражать результаты более точной диагностики или лечения, доступного менее чем за 5 лет. Поговорите со своим врачом, если у вас есть какие-либо вопросы по поводу этой информации.Узнайте больше о статистике.
Статистика адаптирована из публикации Американского онкологического общества (ACS), Cancer Facts & Figures 2021, веб-сайта ACS и Программы надзора, эпидемиологии и конечных результатов (SEER) Национального института рака (источники по состоянию на февраль 2021 г. ).
Следующий раздел в этом руководстве — Медицинские иллюстрации . Предлагает рисунки частей тела, часто поражаемых раком желудка.Используйте меню, чтобы выбрать другой раздел для чтения в этом руководстве.
Основные статистические данные о раке желудка (желудка)
Насколько распространен рак желудка?
По оценкам Американского онкологического общества в отношении рака желудка (также известного как рак желудка) в США на 2021 год:
- Около 26 560 новых случаев рака желудка (16 160 у мужчин и 10400 у женщин)
- Около 11 180 случаев смерти от этого типа рака (6740 мужчин и 4440 женщин)
На рак желудка приходится около 1.5% всех новых видов рака, диагностируемых в США каждый год.
Кто заболевает раком желудка?
Рак желудка чаще всего поражает пожилых людей. Средний возраст людей, когда им ставят диагноз, составляет 68 лет. Около 6 из каждых 10 человек, у которых ежегодно диагностируется рак желудка, — 65 лет и старше.
Пожизненный риск развития рака желудка у мужчин выше (примерно у 1 из 96), чем у женщин (примерно у 1 из 152). Но на риск каждого человека может влиять множество других факторов.
Динамика рака желудка
В США количество новых случаев рака желудка снизилось примерно на 1.5% ежегодно в течение последних 10 лет.
На протяжении большей части начала 20 века рак желудка был основной причиной смерти от рака в Соединенных Штатах. но сегодня он находится далеко в этом списке. Причины этого не совсем ясны, но два основных фактора считаются важными:
- Более широкое использование холодильников для хранения продуктов, что привело к тому, что люди стали есть меньше соленой и копченой пищи (известные факторы риска рака желудка).
- Снижение числа людей, инфицированных бактериями Helicobacter pylori ( H pylori ), которые считаются основной причиной рака желудка.
Хотя рак желудка стал менее распространенным в США, он все еще гораздо чаще встречается в некоторых других частях мира, особенно в Восточной Азии. Он остается одной из ведущих причин смертности от рака в мире.
Статистические данные о выживаемости при раке желудка см. В разделе «Показатели выживаемости при раке желудка».
Посетите Центр онкологической статистики Американского онкологического общества, чтобы получить более подробную статистику.
Хирургическое лечение рака желудка у пожилых пациентов
- Pasquina M. C. Tomaiuolo
- Андреа Маццари
- Уго Гросси
- Антонио Круситти
Abstract
Аденокарцинома желудка считается пиком заболеваемости в седьмом и восьмом десятилетии жизни. У пожилых людей биохимические изменения в тканях и физиологии органов, связанные с инфекцией Helicobacter pylori , приводят к атрофическому гастриту с повышенным риском развития рака.Рак желудка у пожилых людей часто диагностируется на поздней стадии и связан с плохим прогнозом с точки зрения безрецидивной и общей выживаемости. Хирургическое лечение рака желудка у этих пациентов остается спорным из-за повышенного периоперационного риска; вместо этого предпочтительна субтотальная гастрэктомия, когда это возможно. Тотальная резекция желудка с комбинированной резекцией соседних органов или без нее связана с более высокими показателями послеоперационной заболеваемости и смертности. При запущенном раке паллиативная резекция по возможности предпочтительнее гастроэнтеростомии.Заболеваемость и смертность выше у пожилых людей, что, вероятно, связано с сопутствующими заболеваниями у этих пациентов. Стадия Т, метастазы в лимфатические узлы и глубина инвазии первичной опухоли считаются независимыми прогностическими факторами с точки зрения общей выживаемости. Невозможно однозначно оценить влияние комбинированного лечения на пожилых людей; в настоящее время адъювантная химиотерапия рекомендуется здоровым пациентам. В целом, только возраст не был окончательно подтвержден как негативный прогностический фактор у пациентов с раком желудка и не должен препятствовать резекции желудка.После радикальной резекции пожилые пациенты имеют такие же шансы на выживание, как и пациенты среднего возраста.
Ключевые слова
Пожилой возраст Рак желудка Гастрэктомия Лимфаденэктомия Коморбидность Атрофический гастрит Уровень выживаемости ХимиотерапияЭто предварительный просмотр содержания подписки,
войдите в, чтобы проверить доступ.
Ссылки
1.
Саиф М.В., Макрилия Н., Залонис А. и др. (2010) Рак желудка у пожилых людей: обзор. EJSO 36: 709–717
PubMedCrossRefGoogle Scholar2.
I опухолей в Италии — Отчет 2006.
http://www.registri-tumori.it/incidenza1998/2002/rapporto/I%20dati%20dei%20registri%20tumori.html. По состоянию на 16 ноября 2010 г.
3.
Altekruse SF, Kosary CL, Krapcho M et al: SEER Cancer Statistics Review, 1975-2007, Национальный институт рака. Bethesda, MD.
http://seer.cancer.gov/csr/1975_2007/index.html. По состоянию на 16 ноября 2010 г.
4.
Coniglio A, Tiberio GAM, Busti M et al (2004) Хирургическое лечение рака желудка у пожилых людей.J Surg Oncol 88: 201–205
PubMedCrossRefGoogle Scholar5.
Surgical Dong-Yi K, Jae-Kyoon J, Seong-Yeob R et al (2005) Клинико-патологические характеристики рака желудка у пожилых пациентов: сравнение с молодые пациенты. World J Gastroenterol 11: 22–26
Google Scholar6.
Орсениго Э., Томаджер В., Ди Пало С. и др. (2007) Влияние возраста на послеоперационные исходы у 1118 пациентов с раком желудка, перенесших хирургическое вмешательство. Рак желудка 10: 39–44
PubMedCrossRefGoogle Scholar7.
Levine JL, Zenilman ME (2001) Возрастные физиологические изменения в желудочно-кишечном тракте. В: Розенталь Р.А. (ред) Принципы и практика гериатрической хирургии. Springer, New Jork, pp 511–527
Google Scholar8.
Cima RR, Soybel DI (2001) Патофизиология и лечение доброкачественных заболеваний желудка и двенадцатиперстной кишки. В: Розенталь Р.А. (ред) Принципы и практика гериатрической хирургии. Springer, New Jork, pp 555–568
Google Scholar9.
Фурукава Х., Иванага Т., Хирацука М. и др. (1994) Рак желудка у молодых людей: ускоряющий рост эффект беременности и родов. J Surg Oncol 55: 3–6
PubMedCrossRefGoogle Scholar10.
Arai T, Esaki Y, Inoshita N et al (2004) Патологические характеристики рака желудка у пожилых людей: ретроспективное исследование 994 хирургических пациентов. Рак желудка 7: 154–159
PubMedCrossRefGoogle Scholar11.
Китамура К., Ямагути Т., Танигучи Х. и др. (1996) Клинико-патологические характеристики рака желудка у пожилых людей.Br J Cancer 73: 798–802
PubMedCrossRefGoogle Scholar12.
Kunisaki C, Akiyama H, Nomura M et al (2005) Сравнение хирургических исходов рака желудка у пациентов пожилого и среднего возраста. The Am J Surg 191: 216–224
CrossRefGoogle Scholar13.
Катай Х., Сасако М., Сано Т. и др. (2004) Хирургия рака желудка у пожилых людей без операционной смертности. Surg Oncol 13: 235–238
PubMedCrossRefGoogle Scholar14.
Oh J, Young-Kyu P, Seong-Yeob R et al (2010) Влияние возраста на хирургические результаты расширенной гастрэктомии с лимфодиссекцией D2 при карциноме желудка: проспективное когортное исследование. Ann Surg Oncol 17: 1589–1596
CrossRefGoogle Scholar15.
Winslet MC, Mohsen YMA, Powell J (1996) Влияние возраста на хирургическое лечение рака желудка. Eur J Surg Oncol 22: 220–224
PubMedCrossRefGoogle Scholar16.
Eguchi T, Fujii M, Takayama T (2003) Смертность от рака желудка у пожилых пациентов.J Surg Oncol 84: 132–136
PubMedCrossRefGoogle Scholar17.
Ozer I, Bostanci EB, Kou U et al (2010) Хирургическое лечение рака желудка у турецких пациентов старше 70 лет: ранние послеоперационные результаты и факторы риска смертность. Langenbecks Arch Surg 395: 1101–1106
PubMedCrossRefGoogle Scholar18.
Saidi RF, Bell JL, Dudrick PS (2003) Хирургическая резекция рака желудка у пожилых пациентов: есть ли разница в исходе? J Surg Res 118: 15–20
CrossRefGoogle Scholar19.
Martella B, Militello C, Spirch A et al (2005) Паллиативная хирургия рака желудка у пожилых пациентов. Acta BioMed 76: 49–51
PubMedGoogle Scholar20.
Chew-Wun W, Su-Shun L, King-Han S. et al (2000) Хирургическая смертность, выживаемость и качество жизни после резекции по поводу рака желудка в старший. World J Surg 24: 465–472
CrossRefGoogle Scholar21.
Hara H, Isozaki H, Nomura E et al (1999) Оценка стратегий лечения рака желудка у пожилых людей в соответствии с количеством аномальных параметров до операции экспертиза.Jpn J Surg 29: 837–841
CrossRefGoogle Scholar22.
Хироаки С., Томохиро О., Дайки М. и др. (2006) Влияние возраста на прогноз у пациентов с раком желудка. ANZ J Surg 76: 458–461
CrossRefGoogle Scholar23.
Kubota H, Kotoh T, Dhar DK et al (2000) Резекция желудка у пожилых (> или = 80 лет) с карциномой желудка: многомерный анализ прогностических факторов. Aust N Z J Surg 70: 254–257
PubMedCrossRefGoogle Scholar24.
Wedding U, Honecker F, Bokemeyer C и др. (2007) Толерантность к химиотерапии у пожилых больных раком. Cancer Control 14: 44–56
PubMedGoogle Scholar25.
Trumper M, Ross PJ, Cunningham D et al (2006) Эффективность и переносимость химиотерапии у пожилых пациентов с распространенным раком пищевода и желудка: объединенный анализ трех клинические испытания. EJC 42: 827–834
CrossRefGoogle Scholar
Информация об авторских правах
© Springer-Verlag Italia 2012
Авторы и аффилированные лица
- Pasquina M.C. Tomaiuolo






Добавить комментарий