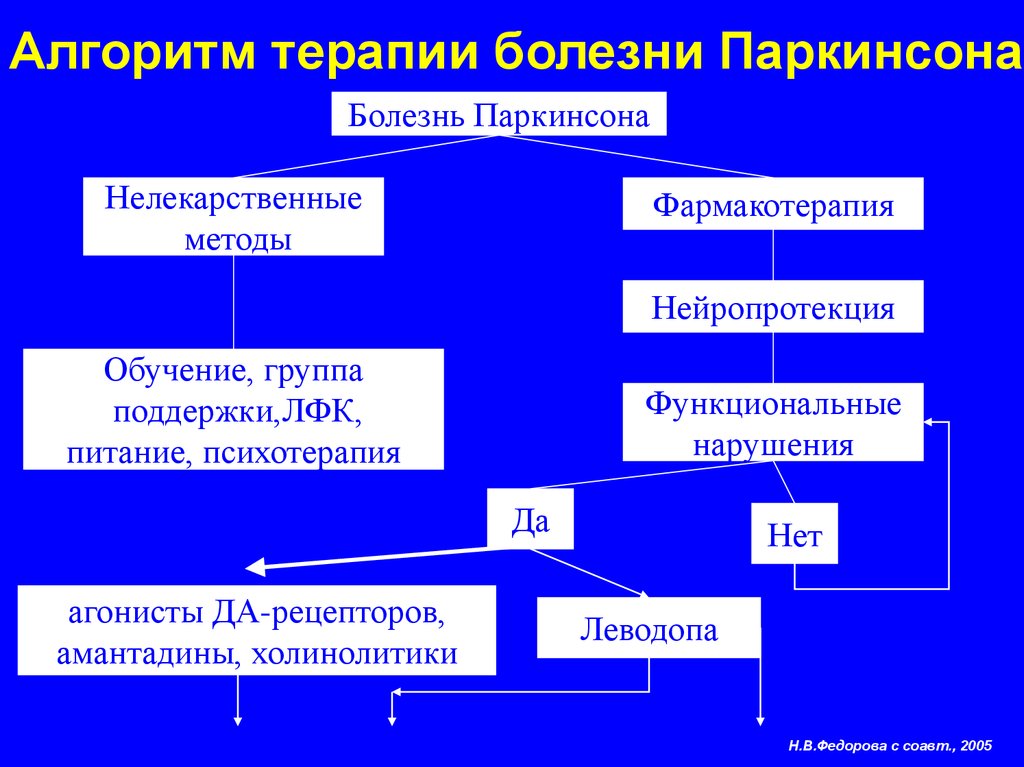
Паркинсона болезнь лечение: Болезнь Паркинсона — Лечение в многопрофильной семейной клинике «К медицина»
Хирургические методы лечения болезни Паркинсона | Токарев
1. Шток В.Н., Левин О.С., Федорова Н.В. Экстрапирамидные расстройства. М.: МИА, 2002:235.
2. Bucy P.C. Surgical relief of tremor at rest. Ann. Surg. 1945;122:933–941.
3. Putnam T.J. Relief from unilateral paralysis agitans by section of the pyramidal tract. Arch. Neurol. Psychiatry. 1938;40:1049– 1050.
4. Abel T.J., Walch T., Howard M.A .III. Russell Meyers (1905–1999): pioneer of functional and ultrasonic neurosurgery. J. Neurosurg. 2016;125:1589–1595. https://doi.org/10.3171/2015.9.JNS142811
5. Speelman J.D., Bosch D.A. Resurgence of functional neurosurgery for Parkinson’s disease: A historical perspective. Movement Disorders. 1998;13(3):582–588. https://doi.org/10.1002/mds.870130336
6. Spiegel E.A., Wycis H.T. Pallidothalamotomy in chorea. Arch. Neurol. Psychiatry. 1950;64:295–296.
7. Spiegel E.A., Wycis H.T., Thur C. The stereoencephalotome (model III of our stereotaxic apparatus for operations on the human brain). J. Neurosurg. 1951;8:452–453.
J. Neurosurg. 1951;8:452–453.
8. Cooper I.S. Anterior choroidal artery ligation for involuntary movements. Science. 1953;118:193.
9. Bravo G.J., Cooper I.S. A clinical and radiological correlation of the lesions produced by chemopallidectomy and thalamectomy. J. Neurol. Neurosurg. Psychiatry. 1959;22:1–10.
10. Connolly B.S., Lang A.E. Pharmacological treatment of Parkinson disease: a review. JAMA. 2014;311:1670–1683. https://doi.org/10.1001/jama.2014.3654
11. Defer G.L., Widner H., Marié R.M., Rémy P., Levivier M. Core assessment program for surgical interventional therapies in Parkinson’s disease (CAPSIT-PD). Mov. Disord. 1999;14:572–84. https://doi.org/10.1002/1531-8257(199907)14:43.0.co;2-c
12. Экстрапирамидные расстройства вчера, сегодня, завтра. [Сб. ст]. Под ред. проф. О.С. Левина. 2-е изд. М., 2015:408.
13. Ахметжанов В.К., Шашкин Ч.С., Джамантаева Б.Д. Болезнь Паркинсона. Патофизиология экстрапирамидной системы. Современные представления о причинах возникновения и патогенезе паркинсонизма. Нейрохирургия и неврология Казахстана. 2016;2(43):44–51.
Нейрохирургия и неврология Казахстана. 2016;2(43):44–51.
14. Schuurman P.R., Bosch D.A., Bossuyt P.M.M., Bonsel G.J., Someren E.J.W., Rob Bie M.A., et al. A comparison of continuous thalamic stimulation and thalamotomy for suppression of severe tremor. N. Engl. J. Med. 2000;342:461–468. https://doi.org/10.1056/NEJM200002173420703
15. Bergman H., Wichmann T., DeLong M.R. Reversal of experimental parkinsonism by lesions of the subthalamic nucleus. Science. 1990;249:1436–1438.
16. Aziz T.Z., Peggs D., Sambrook M.A., Crossman A.R. Lesion of the subthalamic nucleus for the alleviation of 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine (MPTP)-induced parkinsonism in the primate. Mov. Disord. 1991;6:288–292. https://doi.org/10.1159/000064599
17. Alvarez L., Macias R., Pavón N., López G., RodríguezOroz M.C., Rodríguez R. et al. Therapeutic efficacy of unilateral subthalamotomy in Parkinson’s disease: results in 89 patients followed for up to 36 months. J. Neurol. Neurosurg. Psychiatry. 2009;80(9):979–85. https://dx.doi.org/10.1136/jnnp.2008.154948
Psychiatry. 2009;80(9):979–85. https://dx.doi.org/10.1136/jnnp.2008.154948
18. Vitek J.L., Bakay R.A., Freeman A., Evatt M., Green J., McDonald W. et al. Randomized trial of pallidotomy versus medical therapy for Parkinson’s disease. Ann. Neurol. 2003;53:558– 569. https://doi.org/10.1002/ana.10517
19. Eskandar E.N., Shinobu L.A., Penney J.B., Jr., Cosgrove G.R., Counihan T.J. Stereotactic pallidotomy performed without using microelectrode guidance in patients with Parkinson’s disease: surgical technique and 2-year results. J. Neurosurg. 2000;92:375– 383. https://doi.org/10.1159/000068960
20. Shannon K.M., Penn R.D., Kroin J.S., Adler C.H., Janko K.A., York M. et al. Stereotactic pallidotomy for the treatment of Parkinson’s disease. Efficacy and adverse effects at 6 months in 26 patients. Neurology. 1998;50:434–438. https://doi.org/10.1212/wnl.50.2.434
21. Rand R.W. Role of Cryosurgery and MRI for Parkinson’s Disease. Stereotact. Funct. Neurosurg. 1995;65(1–4):18–22.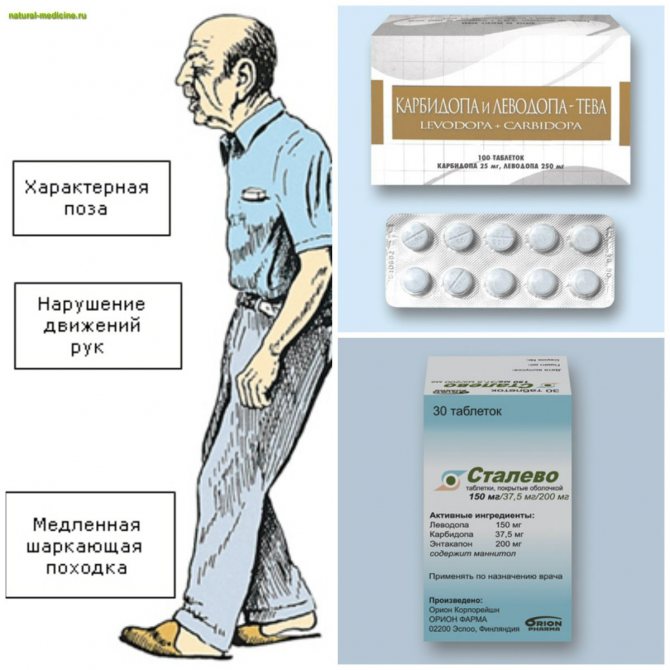 https://doi.org/10.1159/000098891
https://doi.org/10.1159/000098891
22. Koller W.C., Pahwa R., Lyons K.E., Albanese A. Surgical treatment of Parkinson’s disease. J. Neurol. Sci. 1999;167(1):1–10. https://doi.org/10.1016/S0022-510X(99)00139-2
23. Moosa S., Martínez-Fernández R., Elias W.J., Alamo M.D., Eisenberg H.M., Fishman P.S. The Role of High-Intensity Focused Ultrasound as a Symptomatic Treatment for Parkinson’s Disease. Mov. Disord. 2019;34(9):1243–1251. https://doi.org/10.1002/mds.27779. Epub 2019 Jul 10.
24. Ito H., Yamamoto K., Fukutake S., Odo T., Yamaguchi T., Taira T. Magnetic resonance imaging-guided focused ultrasound bilateral thalamotomy for essential tremor: A case report. Neurol. Clin. Neurosci. 2020;8(6):1–3. https://doi.org/10.1111/ncn3.12438
25. Alvarez L., Macias R., Pavon N., López G., RodríguezOroz M.C., Rodríguez R. et al. Therapeutic efficacy of unilateral subthalamotomy in Parkinson’s disease: results in 89 patients followed for up to 36 months. J. Neurol. Neurosurg. Psychiatry. 2009;80:979–985. https://doi.org/10.1136/jnnp.2008.154948
2009;80:979–985. https://doi.org/10.1136/jnnp.2008.154948
26. Krack P., Martinez-Fernandez R., Del Alamo M., Obeso J.A. Current applications and limitations of surgical treatments for movement disorders. Mov. Disord. 2017;32:36–52. https://doi.org/10.1002/mds.26890
27. Niranjan A., Lunsford L.D., Kano H. Leksell Radiosurgery for Movement Disorders. Leksell Radiosurgery. Prog. Neurol. Surg. Basel, Karger, 2019;34:279–288. https://doi.org/10.1159/000493075
28. Duma C.M. Movement disorder radiosurgery — planning, physics and complication avoidance. Prog. Neurol. Surg. 2007;20:249–266. https://doi.org/10.1159/000100168
29. Young R.F., Li F., Vermeulen S., Clayton D.A., Hesselgesser R.D. Gamma Knife pallidotomy for treatment of Parkinson’s disease: long term results, clinical study. Transl. Cancer Res. 2014;3:342–350. https://doi.org/10.3978/j.issn.2218-676X.2014.08.04
30. Cooper I.S. A Cryogenic Method for Physiologic Inhibition and Production of Lesions in the Brain. J. Neurosurg. 1962;19:853– 8. https://doi.org/10.3171/jns.1962.19.10.0853
J. Neurosurg. 1962;19:853– 8. https://doi.org/10.3171/jns.1962.19.10.0853
31. Кандель Э.И. Функциональная и стереотаксическая нейрохирургия. М.: Медицина, 1981:368 с.
32. Charles A., Fager M.D. Use of the Radio-Frequency Electrode in Stereotactic Surgery of Parkinson’s Disease. Surgical Clinics of North America. 1965;45(3):705–713. https://doi.org/10.1016/s0039-6109(16)37593-4
33. Watkins E.S. Heat Gains in Brain During Electrocoagulative Lesions. J. Neurosurg. 1965;23(3):319–28. https://doi.org/10.3171/jns.1965.23.3.0319
34. Schreglmann S.R., Krauss J.K., Chang J.W., Bhatia K.P., Kägi G. Functional Lesional Neurosurgery for Tremor: A Systematic Review and Meta-Analysis. J. Neurol. Neurosurg. Psychiatry. 2018;89(7):717–726. https://doi.org/10.1136/jnnp-2017-316302. Epub 2018 Jan 11.
35. Ohye C., Higuchi Y., Shibazaki T., Hashimoto T., Koyama T., Hirai T. et al. Gamma Knife thalamotomy for Parkinson disease and essential tremor: a prospective multicenter study. Neurosurgery. 2012;70:526–536. https://doi.org/10.1227/NEU.0b013e3182350893
Neurosurgery. 2012;70:526–536. https://doi.org/10.1227/NEU.0b013e3182350893
36. Young R.F., Jacques S., Mark R., Kopyov O., Copcutt B., Posewitz A. et al. Gamma Knife thalamotomy for treatment of tremor: long-term results. J. Neurosurg. 2000;93(Suppl.3):128–135. https://doi.org/10.3171/jns.2000.93.supplement
37. Kooshkabadi A., Lunsford L.D., Tonetti D., Flickinger J.C., Kondziolka D. Gamma Knife thalamotomy for tremor in the magnetic resonance imaging era. J. Neurosurg .2013;118:713–718. https://doi.org/10.3171/2013.1.JNS121111
38. Niranjan A., Kondziolka D., Baser S., Heyman R., Lunsford L.D. Functional outcomes after Gamma Knife thalamotomy for essential tremor and MS-related tremor. Neurology. 2000;55:443–446. https://doi.org/10.1212/wnl.55.3.443
39. Campbell A.M., Glover J., Chiang V.L., Gerrard J., Yu J.B. Gamma Knife stereotactic radiosurgical thalamotomy for intractable tremor: a systematic review of the literature. Radiother. Oncol. 2015;114:296–301. https://doi. org/10.1016/j.radonc.2015.01.013
org/10.1016/j.radonc.2015.01.013
40. Okun M.S., Stover N.P., Subramanian T., Gearing M., Wainer B.H., Holder C.A. et al. Complications of gamma knife surgery for Parkinson disease. Arch. Neurol. 2001;58:1995– 2002. https://doi.org/10.1001/archneur.58.12.1995
41. Witjas T., Carron R., Krack P., Eusebio A., Vaugoyeau M., Hariz M. et al. A prospective single-blind study of Gamma Knife thalamotomy for tremor. Neurology. 2015;85:1562–1568. https://doi.org/10.1212/WNL.0000000000002087
42. Moser D. MR-guided focused ultrasound technique in functional neurosurgery: targeting accuracy. J. Ther. Ultrasound. 2013;1:3. https://doi.org/10.1186/2050-5736-1-3
43. Christian E., Yu C., Apuzzo M.L. Focused ultrasound: relevant history and prospects for the addition of mechanical energy to the neurosurgical armamentarium. World Neurosurg. 2014;82:354– 365. https://doi.org/10.1016/j.wneu.2014.06.021
44. Fry W.J., Mosberg Jr.W.H., Barnard J.W., Fry F.J. Production of focal destructive lesions in the central nervous system with ultrasound. J. Neurosurg. 1954;11:471–478. https://doi.org/10.3171/jns.1954.11.5.0471
J. Neurosurg. 1954;11:471–478. https://doi.org/10.3171/jns.1954.11.5.0471
45. Jagannathan J., Sanghvi N.T., Crum L.A., Yen C.-P., Medel R., Dumont A.S. et al. High-intensity focused ultrasound surgery of the brain: part 1 — a historical perspective with modern applications. Neurosurgery 2009;64:201–210;discussion,210–211. https://doi.org/10.1227/01.NEU.0000336766.18197.8E
46. Gallay M.N., Moser D., Jeanmonod D. Safety and accuracy of incisionless transcranial MR-guided focused ultrasound functional neurosurgery: single-center experience with 253 targets in 180 treatments. J. Neurosurg. 2018;May 1. https://doi.org/10.3171/2017.12.JNS172054
47. Bond A.E., Shah B.B., Huss D.S., Dallapiazza R.F., Warren A., Harrison M.B. et al. Safety and efficacy of focused ultrasound thalamotomy for patients with medication-refractory, tremordominant Parkinson disease: a randomized clinical trial. JAMA Neurol. 2017;74:1412–1418. https://doi.org/10.1001/jamaneurol.2017.3098
48. Jung N. Y., Rachmilevitch I., Sibiger O., Amar T., Zadicario E., Chang J.W. Factors Related to Successful Energy Transmission of Focused Ultrasound through a Skull: A Study in Human Cadavers and Its Comparison with Clinical Experiences. J. Korean Neurosurg. Soc. 2019;62(6):712–722. https://doi.org/10.3340/jkns.2018.0226
Y., Rachmilevitch I., Sibiger O., Amar T., Zadicario E., Chang J.W. Factors Related to Successful Energy Transmission of Focused Ultrasound through a Skull: A Study in Human Cadavers and Its Comparison with Clinical Experiences. J. Korean Neurosurg. Soc. 2019;62(6):712–722. https://doi.org/10.3340/jkns.2018.0226
49. Mazerolle E.L., Seasonsa G.M., Warwaruk-Rogers R., Romo P., Nordal R., Sevick R.J. et al. Focused ultrasound resolves persistent radiosurgery related change in a patient with tremor. Radiology Case Reports. 2019;14(10):1233–1236. https://doi.org/10.1016/j.radcr.2019.07.010
50. Залялова З.А. Глубокая стимуляция головного мозга. Каким образом она контролирует движения при болезни Паркинсона? Нейрохирургия. 2019;21(3):93–99. https://doi.org/10.17650/1683-3295-2019-21-3-93-99
51. Benazzouz A., Hallett M. Mechanism of Action of Deep Brain Stimulation. Neurology. 2000;55(12Suppl.6):S13–6. PMID: 11188968.
52. Томский А.А., Бриль Е.В., Гамалея А.А., Федорова Н. В., Левин О.С. Функциональная нейрохирургия при болезни Паркинсона в России. Анналы клинической и экспериментальной неврологии. 2019;13(4):10–15. https://doi.org/10.25692/ACEN.2019.4.2
В., Левин О.С. Функциональная нейрохирургия при болезни Паркинсона в России. Анналы клинической и экспериментальной неврологии. 2019;13(4):10–15. https://doi.org/10.25692/ACEN.2019.4.2
53. Follett K.A., Weaver F.M., Stern M., Kwan Hur, Harris C.L., Luo P. et al. Pallidal versus subthalamic deep-brain stimulation for Parkinson’s disease. N Engl J. Med. 2010;362:2077–2091. https://doi.org/10.1056/NEJMoa0907083
54. Voon V., Kubu C., Krack P., Houeto J.-L., Tröster A.I. Deep brain stimulation: Neuropsychological and neuropsychiatric issues. Mov. Disord. 2006;21Suppl.14:S305 — 27. https://doi.org/10.1002/mds.20963
55. Vendette M., Gagnon J.-F., Decary A., Massicotte-Marquez J., Postuma R.B., Doyon J. et al. REM sleep behavior disorder predicts cognitive impairment in Parkinson’s disease without dementia. Neurology. 2007;69(19):1843–9. https://doi.org/10.1212/01.wnl.0000278114.14096.74
56. Charles P.D., Dolhun R.M., Gill C.E., Davisa T.L., Blitonc M.J., Tramontanad M.G. et al. Deep brain stimulation in early Parkinson’s disease: Enrollment experience from a pilot trial. Parkinsonism & Related Disorders. 2012;18(3):268–273. https://doi.org/10.1016/j.parkreldis.2011.11.001
et al. Deep brain stimulation in early Parkinson’s disease: Enrollment experience from a pilot trial. Parkinsonism & Related Disorders. 2012;18(3):268–273. https://doi.org/10.1016/j.parkreldis.2011.11.001
57. Schuepbach W.M., Rau J., Knudsen K., Volkmann J., Krack P., Timmermann L. еt. al. EARLYSTIM Study Group. Neurostimulation for Parkinson’s disease with early motor complications. The New England Journal of Medicine. 2013;368(7):610–22. https://doi.org/10.1056/NEJMoa1205158
58. Lhommée E., Wojtecki L., Czernecki V., Witt K., Maier F., Tonder L. et al. EARLYSTIM study group. Behavioural outcomes of subthalamic stimulation and medical therapy versus medical therapy alone for Parkinson’s disease with early motor complications (EARLYSTIM trial): secondary analysis of an open-label randomised trial. The Lancet Neurology. 2018;17(3):223–31. https://doi.org/10.1016/S1474-4422(18)30035-8
59. Greb E. Can DBS in Early Parkinson’s Disease Reduce Disease Progression? Medscape. 2020;Jul 09. https://www.medscape.com/viewarticle/933676#vp_1
2020;Jul 09. https://www.medscape.com/viewarticle/933676#vp_1
60. Бриль Е.В. Ранняя нейростимуляция подкорковых структур головного мозга при болезни Паркинсона. Споры продолжаются. Бюллетень Национального общества по изучению болезни Паркинсона и расстройств движений. 2020;3:13–15. https://doi.org/10.24412/2226-079X-2020-12236
Типы распространенных медикаментозных методов лечения
Авторы: Редакторы WebMD
- Распространенные лекарства от болезни Паркинсона
- Рекомендации по лечению болезни Паркинсона
- Оставайтесь в безопасности с вашими лекарствами
последние годы. Ученые разработали новые лекарства и лучше понимают, как использовать старые методы лечения. Это сильно изменило повседневную жизнь людей с этим заболеванием.
Большинство людей могут облегчить симптомы болезни Паркинсона с помощью лекарств. Но некоторым может потребоваться операция, если их лекарства перестанут работать достаточно хорошо.
Лекарства, которые вы принимаете в начале лечения, сильно влияют на то, как ваше состояние будет развиваться с течением времени. Поэтому важно работать с неврологом или другим специалистом по болезни Паркинсона, который поможет вам принять решение о лечении.
Поэтому важно работать с неврологом или другим специалистом по болезни Паркинсона, который поможет вам принять решение о лечении.
Общие препараты для лечения болезни Паркинсона
Леводопа и карбидопа ( Дуопа , Ритары , Синемет ) . Леводопа (также называемая L-допа) является наиболее часто назначаемым лекарством от болезни Паркинсона. Он также лучше всего справляется с симптомами заболевания, особенно с медленными движениями и жесткими частями тела.
Леводопа работает, когда клетки вашего мозга превращают ее в дофамин. Это химическое вещество, которое мозг использует для отправки сигналов, которые помогают вам двигаться. У людей с болезнью Паркинсона в мозгу недостаточно дофамина, чтобы контролировать свои движения.
Синемет представляет собой смесь леводопы и другого препарата под названием карбидопа. Карбидопа улучшает действие леводопы, поэтому вы можете принимать ее меньше. Это предотвращает многие распространенные побочные эффекты леводопы, такие как тошнота, рвота и нерегулярный сердечный ритм.
Это предотвращает многие распространенные побочные эффекты леводопы, такие как тошнота, рвота и нерегулярный сердечный ритм.
Синемет имеет наименьшее количество краткосрочных побочных эффектов по сравнению с другими препаратами для лечения болезни Паркинсона. Но это повышает ваши шансы на долгосрочные проблемы, такие как непроизвольные движения. Ингаляционная порошковая форма леводопы (INBRIJA) и истрадефиллин в таблетках (Nourianz) были одобрены для тех, у кого наблюдаются периоды выключения. Периоды выключения могут возникать, когда симптомы болезни Паркинсона возвращаются в периоды между запланированными дозами леводопы/карбидопы.
У людей, принимающих леводопу в течение 3–5 лет, в течение нескольких часов после приема лекарства могут появиться беспокойство, спутанность сознания или необычные движения. Изменение количества или времени приема дозы обычно предотвращает эти побочные эффекты.
Агонисты дофамина . Эти препараты действуют как дофамин в мозге.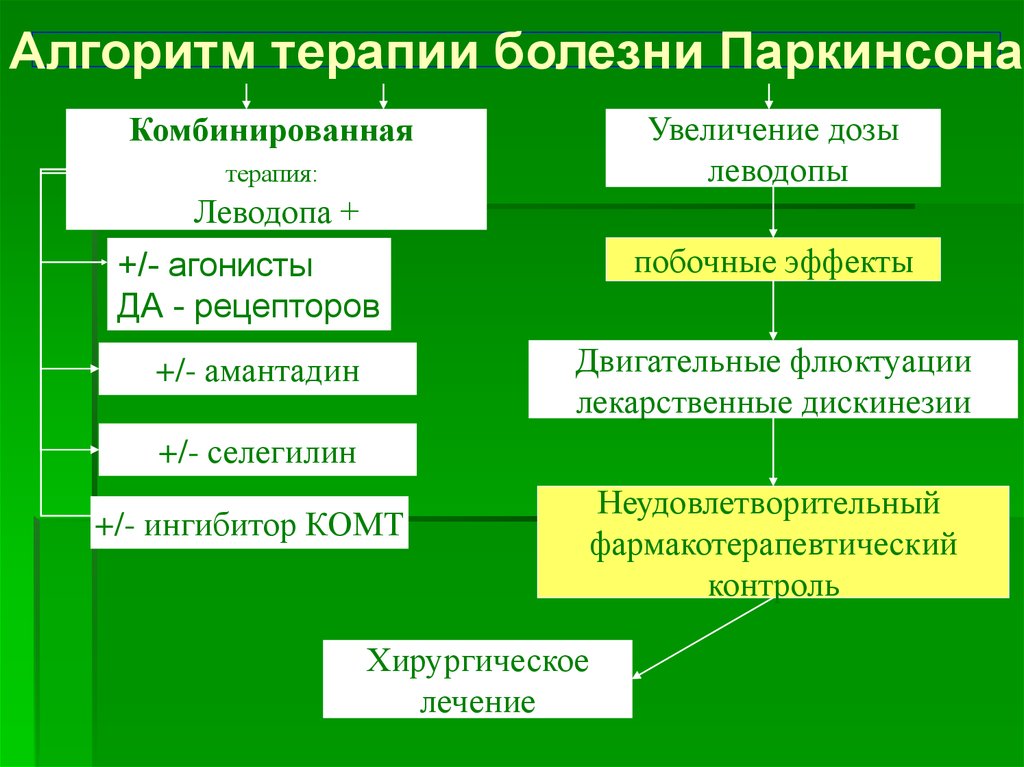 К ним относятся прамипексол (Mirapex), ротиготин (Neupro) и ропинирол (Requip).
К ним относятся прамипексол (Mirapex), ротиготин (Neupro) и ропинирол (Requip).
Вы можете принимать один из этих препаратов отдельно или вместе с Синеметом. Некоторые врачи сначала назначают агонисты дофамина, а затем добавляют леводопа, если ваши симптомы все еще не контролируются.
Агонисты дофамина не имеют такого же риска долгосрочных проблем, как терапия леводопой. Поэтому они часто являются препаратами первого выбора для лечения болезни Паркинсона.
Однако эти препараты повышают вероятность некоторых краткосрочных побочных эффектов, таких как тошнота, рвота, головокружение, предобморочное состояние, спутанность сознания и галлюцинации.
Амантадин ( Gocovri , Osmolex ER) может помочь людям с легкой формой болезни Паркинсона.
Он работает, повышая количество дофамина, которое могут использовать клетки вашего мозга, что помогает уменьшить симптомы болезни Паркинсона. Недавние исследования показали, что амантадин может помочь облегчить непроизвольные движения, которые могут возникнуть при терапии леводопой. Но это может вызвать побочные эффекты, такие как спутанность сознания и проблемы с памятью.
Но это может вызвать побочные эффекты, такие как спутанность сознания и проблемы с памятью.
Антихолинергические средства , такие как бензтропин ( Когентин ) и тригексифенидил ( Артан ) . Эти препараты восстанавливают баланс между двумя химическими веществами мозга, дофамином и ацетилхолином. Это облегчает тремор и ригидность мышц у людей с болезнью Паркинсона. Но эти лекарства могут нанести вред памяти и мышлению, особенно у пожилых людей. Из-за этого врачи редко назначают их сегодня.
Ингибиторы Мао-В , например сафинамид (Xadago), селегилин ( элдеприл , зелапар ) и разагилин . Эти препараты блокируют химические вещества мозга, расщепляющие дофамин. Это помогает вашему мозгу иметь больше дофамина для работы.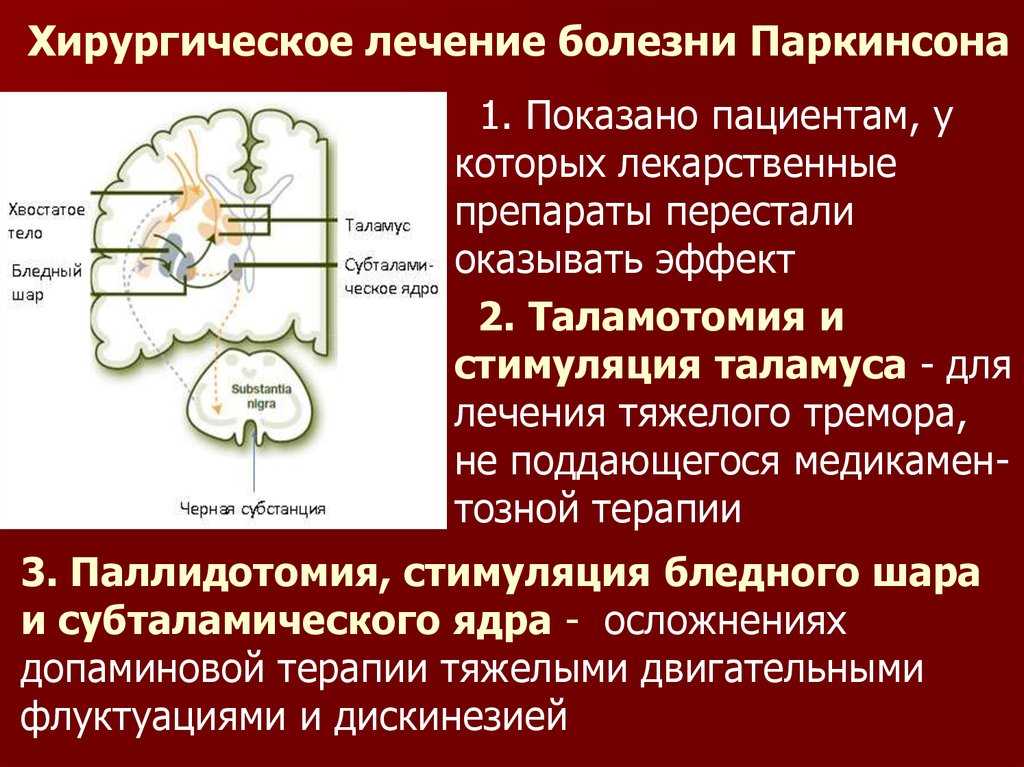
Некоторые данные показывают, что селегилин может замедлять прогрессирование болезни Паркинсона, особенно на ранних стадиях. Общие побочные эффекты включают тошноту, головокружение или обмороки и боль в животе.
Исследования на животных показывают, что разагилин может также замедлять прогрессирование болезни Паркинсона. Побочные эффекты включают головную боль, боль в суставах, расстройство желудка и депрессию.
Сафинамид является дополнительным лекарственным средством, которое может быть назначено, когда у лиц, принимающих леводопу и карбидопу, наблюдается прорыв симптомов болезни Паркинсона, которые ранее находились под контролем. Исследования показывают, что добавление этого препарата помогает людям испытывать более длительные периоды времени с уменьшенными или отсутствующими симптомами. Наиболее распространенными побочными эффектами являются проблемы с засыпанием или сном, тошнота, падения и неконтролируемые непроизвольные движения.
Ингибиторы COMT , такие как энтакапон ( Комтан ), опикапон (Онгентис), и толкапон (Тасмар) . Когда вы принимаете леводопу, химическое вещество COMT в вашем организме делает часть препарата бесполезной. Препараты блокируют COMT, поэтому мозг может более эффективно использовать леводопа, что облегчает симптомы болезни Паркинсона.
Когда вы принимаете леводопу, химическое вещество COMT в вашем организме делает часть препарата бесполезной. Препараты блокируют COMT, поэтому мозг может более эффективно использовать леводопа, что облегчает симптомы болезни Паркинсона.
Руководство по лекарствам для лечения болезни Паркинсона
Не существует наилучшего сочетания лекарств от болезни Паркинсона. Вам и вашему врачу придется попробовать несколько подходов к лечению, чтобы определить лучший для вас.
Но есть некоторые общие рекомендации по приему лекарств. Обязательно спросите своего врача или фармацевта о каких-либо конкретных советах для вашего лечения.
- Не делите таблетки и не вынимайте капсулы, если это не предписано врачом.
- Пейте от 6 до 10 стаканов воды в день.
- Физическая активность может помочь вашему организму переваривать и усваивать лекарства.
- Знайте названия ваших лекарств и то, как вы их принимаете. Знайте общие и торговые названия, ваши дозы и побочные эффекты, которые у вас могут быть.
 Всегда держите при себе список этих деталей.
Всегда держите при себе список этих деталей. - Принимайте лекарства точно так, как их прописал врач.
- Не прекращайте прием и не меняйте лекарства, если предварительно не поговорите со своим врачом. Даже если вы чувствуете себя хорошо, вам все равно нужно их принимать. Ваше состояние может ухудшиться, если вы внезапно прекратите прием лекарства.
- Соблюдайте режим приема лекарств. Принимайте их в одно и то же время каждый день. Установите будильник, чтобы напомнить вам, если вам нужно.
- Ведите календарь приема лекарств и записывайте каждый раз, когда принимаете дозу.
- Если вы пропустите дозу в назначенное время, не паникуйте. Возьми, как только вспомнишь. Но если уже почти пришло время для следующей дозы, пропустите пропущенную дозу и вернитесь к своему обычному графику приема лекарств.
- Не храните просроченные лекарства. Избавьтесь от них, следуя инструкциям на этикетке препарата или в информационном листке для пациентов. Или узнайте у своего фармацевта, как их утилизировать.

- Храните лекарства в сухом месте, вдали от влаги (если только ваш врач или фармацевт не скажет вам, что лекарство необходимо хранить в холодильнике).
- Не делитесь своими лекарствами с другими.
- Возьмите с собой дополнительные лекарства, когда вы путешествуете, на случай, если вам нужно будет оставаться дома дольше, чем планировалось. И держите его в ручной клади, а не в зарегистрированном багаже.
- Пополняйте свои рецептурные препараты до того, как они полностью закончатся. Позвоните в аптеку по крайней мере за 48 часов до того, как она закончится. Если вы не можете добраться до аптеки, у вас есть финансовые проблемы или другие проблемы, из-за которых вам трудно получить лекарства, сообщите об этом своему врачу. Вам может помочь социальный работник.
Будьте осторожны с лекарствами
Внимательно прочитайте все этикетки.
- Сообщите всем своим поставщикам медицинских услуг обо всех лекарствах и добавках, которые вы принимаете.

- Знайте все лекарства и продукты, на которые у вас аллергия.
- Ознакомьтесь со всеми побочными эффектами, которые могут вызвать ваши лекарства. Большинство реакций произойдет, когда вы начнете что-то принимать, но это не всегда так. Некоторые реакции могут быть отсрочены или могут возникнуть, когда вы добавляете лекарство к своему лечению. Немедленно позвоните своему врачу обо всем необычном.
- По возможности используйте одну аптеку. Старайтесь получать лекарства по всем рецептам в одном месте, чтобы фармацевт мог следить за лекарствами, которые могут взаимодействовать друг с другом.
- Вы можете использовать онлайн-инструменты, чтобы узнать, не будут ли какие-либо из ваших лекарств работать вместе.
Вы имеете право и обязаны знать, какие лекарства прописывает ваш врач. Чем больше вы знаете о них и о том, как они работают, тем легче вам будет контролировать свои симптомы. Вы и ваш врач можете работать вместе над созданием и изменением плана лечения. Убедитесь, что вы понимаете и разделяете одни и те же цели лечения. Поговорите о том, что вам следует ожидать от лекарств, чтобы вы могли знать, работает ли ваш план лечения.
Убедитесь, что вы понимаете и разделяете одни и те же цели лечения. Поговорите о том, что вам следует ожидать от лекарств, чтобы вы могли знать, работает ли ваш план лечения.
Руководство по болезни Паркинсона
- Обзор
- Симптомы и стадии
- Диагностика и тесты
- Лечение и симптомы. Болезнь Паркинсона
Поиск тем, статей, видео, исследований и т. д.
Нажмите Enter для поиска или ESC для закрытия
Вы ищете:
- ${результат.термин}
Домашняя страница
Лекарства и методы лечения
Пожертвовать
О болезни Паркинсона
В то время как доступные методы лечения могут лечить некоторые симптомы, люди с болезнью Паркинсона срочно нуждаются в более эффективных методах лечения, чтобы улучшить качество жизни и замедлить или остановить прогрессирование заболевания.

При двигательных симптомах
Помощь при треморе, скованности и медлительности.
Читать далее
При немоторных симптомах
Помощь в лечении симптомов — например, запора, деменции, депрессии, галлюцинаций, боли, сексуальной дисфункции и проблем со сном, — которые могут возникать на протяжении всего заболевания.
Читать далее
Глубокая стимуляция мозга
Несмотря на инвазивность, эта хирургическая терапия может уменьшить симптомы, ограничить потребность в лекарствах и уменьшить побочные эффекты, такие как дискинезия, которые могут сопровождать медикаментозное лечение.
Читать далее
Сфокусированный ультразвук
Фокусированное ультразвуковое исследование — это неинвазивная хирургическая процедура при моторных симптомах или дискинезии Паркинсона, которые не поддаются медикаментозному контролю.
Для некоторых людей сфокусированный ультразвук может быть альтернативой операции по глубокой стимуляции мозга.
Терапия в разработке
Список избранных методов лечения, которые проходят испытания (те, которые в настоящее время или ранее финансируются Фондом Майкла Дж. Фокса) для замедления или остановки прогрессирования болезни Паркинсона или для лечения симптомов.
Читать далее
Все доступные лекарства и методы лечения направлены на облегчение симптомов и улучшение качества жизни. Самой большой неудовлетворенной потребностью пациентов остается терапия, модифицирующая заболевание, — терапия, которая останавливает или замедляет прогрессирование заболевания. Фонд исследований болезни Паркинсона Майкла Дж. Фокса (MJFF) поддерживает исследования, направленные на ускорение лечения, а для тех, кто сегодня живет с болезнью Паркинсона, разрабатывает улучшенные методы лечения двигательных симптомов и расширенные варианты лечения немоторных симптомов.

Современные методы лечения подбираются с учетом уникальных симптомов каждого человека; не существует универсального подхода к лечению болезни Паркинсона. Чаще всего люди начинают медикаментозную терапию, когда симптомы мешают им делать то, что они хотят или должны делать. Глубокая стимуляция мозга может быть вариантом, когда лекарства не работают так же хорошо, или когда люди испытывают побочные эффекты, такие как дискинезия.
Упражнения также могут помочь справиться с симптомами болезни Паркинсона, и некоторые ранние исследования показывают, что они могут помочь защитить мозг. Вместе с врачом и физиотерапевтом разработайте безопасный и приятный режим упражнений.
Решение о том, когда и какое лечение следует начать, лучше всего принимать вместе с лечащим врачом. При выборе терапии учитывайте свои симптомы и то, как они мешают вашей жизни, а также потенциальные преимущества, побочные эффекты и затраты. Ваш врач также примет во внимание ваш возраст и другие заболевания и лекарства, помимо болезни Паркинсона.


 Всегда держите при себе список этих деталей.
Всегда держите при себе список этих деталей.