Острый ишемический инсульт последствия: Ишемический инсульт: прогнозы, последствия и реабилитация
Как уменьшить последствия инсульта? | Медичний часопис
Американские ученые из Медицинского центра Университета Лайолы (Loyola University Medical Center), Мэйвуд, Иллинойс, опубликовали данные о том, какие факторы могут повлиять на прогноз у пациентов, перенесших ишемический инсульт.
«Период сразу после острого ишемического инсульта является временем наибольшего риска», — отмечают неврологи, участвовавшие в исследовании. — Тщательный уход за пациентом, перенесшим инсульт, в ранний период может предотвратить дальнейшие неврологические повреждения и минимизировать общие осложнения, улучшая возможности функционального восстановления.
Ранний уход преследует две основные цели: сведение к минимуму повреждения ткани головного мозга и профилактику и лечение неврологических осложнений.
Если скорость мозгового кровообращения снижается менее 25 мл на 100 г ткани в 1 мин, функционирование нейронов ухудшается, что проявляется соответствующей неврологической симптоматикой, но нормальное функционирование может быть восстановлено при адекватной реперфузии. Если же скорость кровотока снижается и дальше, нейроны подвергаются необратимым изменениям, степень которых коррелирует со степенью и длительностью гипоперфузии. Области мозговой ткани, подверженной гипоперфузии, но в которой не развились необратимые изменения, называют ишемической полутенью (ischemic penumbra). Меры по повышению перфузии головного мозга могут предотвратить необратимые повреждения ткани. Кроме того, дополнительные факторы, такие как гипергликемия, гипертермия и эндотелиальная дисфункция могут негативно повлиять на ее сохранность, ускоряя повреждение нейронов.
Если же скорость кровотока снижается и дальше, нейроны подвергаются необратимым изменениям, степень которых коррелирует со степенью и длительностью гипоперфузии. Области мозговой ткани, подверженной гипоперфузии, но в которой не развились необратимые изменения, называют ишемической полутенью (ischemic penumbra). Меры по повышению перфузии головного мозга могут предотвратить необратимые повреждения ткани. Кроме того, дополнительные факторы, такие как гипергликемия, гипертермия и эндотелиальная дисфункция могут негативно повлиять на ее сохранность, ускоряя повреждение нейронов.
Существует много сложных факторов, влияющих на прогноз, например, имеются доказательства отношения между гипергликемией и неблагоприятными исходами после инсульта. Поэтому авторы исследования рекомендуют строгий контроль гликемии с помощью частых измерений уровня глюкозы глюкометром и агрессивное лечение инсулином.
Также у данной когорты пациентов каждый градус температуры тела выше нормы удваивает риск летального исхода или тяжелой инвалидизации. Существуют показания к терапевтическому охлаждению у пациентов кардиологического профиля. В настоящий момент проводятся испытания относительно эффективности проведения таких процедур у больных неврологического профиля. Однако еще до получения однозначных результатов ранний уход за пациентами должен включать поддержание температуры тела на уровне выше 35,5 °С и ниже 37,5 °С.
Существуют показания к терапевтическому охлаждению у пациентов кардиологического профиля. В настоящий момент проводятся испытания относительно эффективности проведения таких процедур у больных неврологического профиля. Однако еще до получения однозначных результатов ранний уход за пациентами должен включать поддержание температуры тела на уровне выше 35,5 °С и ниже 37,5 °С.
Немаловажным является положение пациента в постели, что обусловлено уменьшением притока крови к головному мозгу при, например, сидячем положении. У пациентов с острым инсультом в бассейне средней мозговой артерии при снижении изголовья от 30 до 15 °, по данным транскраниальной допплерографии, скорость кровотока увеличивалась на 12% (р=0,001) и еще на 8% — при снижении с 15 до 0 ° (р=0,016). Общепринятой практикой является удерживание лежачего положения в течение 24 ч. При наличии у пациента ортопноэ изголовье кровати должно быть на наиболее низкой комфортной для пациента высоте.
Неврологические осложнения острого инсульта включают отек головного мозга, повторный инсульт, внутричерепные кровоизлияния, судороги. Частое неврологическое обследование, а также повторные нейровизуализации при значительных повреждениях ткани могут обеспечить своевременное выявление и лечение этих осложнений.
Частое неврологическое обследование, а также повторные нейровизуализации при значительных повреждениях ткани могут обеспечить своевременное выявление и лечение этих осложнений.
Авторы исследуют и многие другие вопросы терапии пациентов с инсультом, в том числе регуляцию артериального давления, объема циркулирующей крови, применение статинов, методики лечения таких осложнений, как пневмония, сепсис, инфаркт миокарда, тромбоз, гипотрофия мышц, аспирация, отек мозга, судороги, повторный инсульт.
Flaster M., Morales-Vidal S., Schneck M. et al. (2012) Stroke: supportive care (www.medmerits.com/index.php/article/stroke_supportive_care).
Анна Городецкая
Последствия инсульта | Медицинский центр АКАДЕМИЯ VIP
21.07.2022
Последствия острого нарушения мозгового кровообращения (ОНМК) – комплекс симптомов, которые наблюдаются спустя год или более со времени перенесения острого цереброваскулярного заболевания.
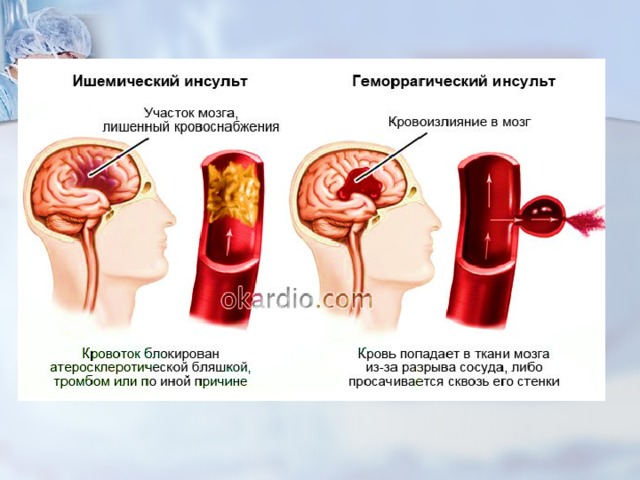
По данным статистики, после перенесённого ишемического инсульта около 60—70% больных имеют инвалидизируюшие неврологические расстройства к концу месяца. Повторный ишемический инсульт возникает в течение последующих 5 лет у 30% пациентов. После перенесённого внутримозгового кровоизлияния большинство больных имеют стойкие неврологические нарушения, однако восстановление лучше, чем при ишемическом инсульте, поскольку кровоизлияние оказывает менее разрушительное действие на ткань мозга, чем инфаркт. В связи с вышесказанным целесообразным является проведение комплекса реабилитационных мероприятий, направленных на восстановление двигательных, чувствительных расстройств, речевой функции и профилактика развития повторного ОНМК.
Дисциркуляторная энцефалопатия (ДЭ)— хроническая прогрессирующая форма цереброваскулярной патологии, характеризующаяся многоочаговым или диффузным поражением головного мозга, которая проявляется комплексом неврологических и нейропсихологических расстройств. Наибольшее значение в этиологии имеют атеросклероз, гипертония и их сочетание, приводящие к недостаточности мозгового кровообращение. Для ДЭ характерно наличие не только субъективных жалоб на головную боль, повышенную утомляемость, снижение памяти, но и наличие признаков органического поражения головного мозга, которые обнаруживаются при неврологическом и нейропсихологическом исследовании. Основными проявлениями дисциркуляторной энцефалопатии являются расстройства позновательных функций, аффективные расстройства, различные двигательные нарушения, координаторные расстройства, вегетативная недостаточность.
Наибольшее значение в этиологии имеют атеросклероз, гипертония и их сочетание, приводящие к недостаточности мозгового кровообращение. Для ДЭ характерно наличие не только субъективных жалоб на головную боль, повышенную утомляемость, снижение памяти, но и наличие признаков органического поражения головного мозга, которые обнаруживаются при неврологическом и нейропсихологическом исследовании. Основными проявлениями дисциркуляторной энцефалопатии являются расстройства позновательных функций, аффективные расстройства, различные двигательные нарушения, координаторные расстройства, вегетативная недостаточность.
Диагностика. Диагностика включает проведение неврологического осмотра, нейропсихологического исследования, использование инструментальных методов диагностики. УЗДГ позволяет сделать вывод о нарушении кровотока, состоянии сосудистой стенки, наличии атеросклеротического стеноза или закупорки сосудов, оценить коллатеральный кровоток.
КТ и МРТ.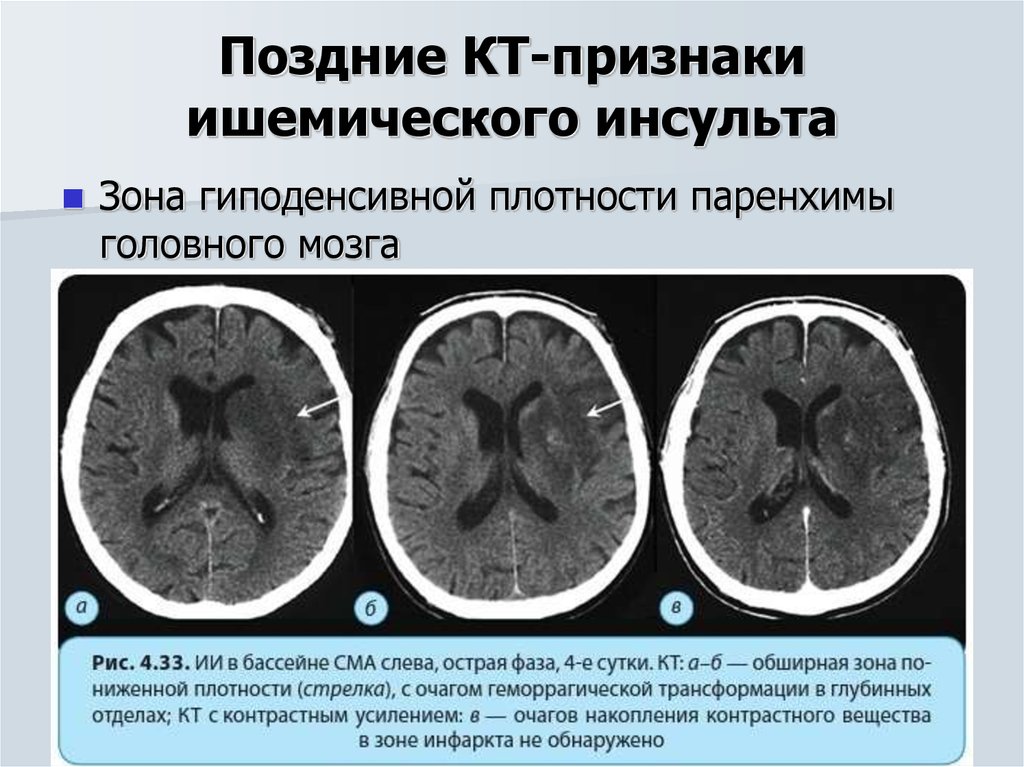 При проведении нейровизуализационного исследования выявляются мелкоочаговые изменения вещества мозга и признаки атрофии, обусловленные хронической дисциркуляцией, выраженность которых зависит от стадии заболевания.
При проведении нейровизуализационного исследования выявляются мелкоочаговые изменения вещества мозга и признаки атрофии, обусловленные хронической дисциркуляцией, выраженность которых зависит от стадии заболевания.
Лечение должно быть направлено на терапию основного заболевания, но фоне которого развивается ДЭ, устранение неврологических и психопатологических синдромов, улучшение кровоснабжения, метаболизма нервной ткани.
Другие статьи
Методы функциональной диагностики сердечно-сосудистых заболеваний
Удаление кисты яичника – лапароскопическая операция
Пред — и послеоперационное ведение пациента врачом дерматокосметологом
Поделиться в социальных сетях:
Вернуться к списку статей
Заказать обратный звонок
Оставьте ваши контактный данные и мы перезвоним Вам в ближайщее время
Имя*
Телефон*
Я согласен на обработку персональных данных
Записаться на приём
Выберите нужную специализацию врача, оставьте Ваши контактные данные, и мы запишем вас на приём:
Имя*
Телефон*
Я согласен на обработку персональных данных
Записаться на приём
Имя*
Телефон*
Я согласен на обработку персональных данных
Геморрагический инсульт и паралич лицевого нерва: История Мэгги
Талантливая актриса борется за возвращение к жизни после геморрагического инсульта и паралича лицевого нерва.

Основные моменты
- Мэгги Уиттум перенесла опасный для жизни инсульт в возрасте 33 лет. Нейрохирург Университета Джона Хопкинса Джуди Хуанг провел операцию по остановке кровотечения в стволе головного мозга Мэгги.
- После инсульта у Мэгги парализована половина лица. Пластика лица и реконструктивная хирургия помогли вернуть ее лицу подвижность.
- Сегодня Мэгги возобновила выступления и рассказывает другим о влиянии инсульта, вдохновляя пациентов, артистов, врачей и хирургов.
Разрушительный инсульт и операция по спасению жизни
«Б-Е…Г-Р-А-Т-Е-Ф-У-Л».
Пока ее сестра медленно читала алфавит, молодая женщина на кровати сжала ее руку, сигнализируя по одной букве за раз. Так теперь общалась Мэгги.
Ее семья, поспешно собравшаяся у ее постели, задавалась вопросом, будет ли это последним сообщением Мэгги для них, поскольку нейрохирургическая бригада спешила подготовить ее к экстренной операции на головном мозге.
Неделей ранее, в декабре 2014 года, у уроженки Колорадо Мэгги Уиттум, казалось, было все: здоровье, талант и блестящее будущее. Она руководила и выступала в Шотландии, Южной Корее, Тайване, Гонконге, Китае и Канаде. Она работала над получением степени магистра изящных искусств по актерскому мастерству в Вашингтоне, округ Колумбия, и была помолвлена.
Но потом появилась головная боль, из-за которой два дня спустя Мэгги, шатаясь, попала в отделение неотложной помощи в Вашингтоне, округ Колумбия. Подобно нарастающей волне, ее симптомы становились все более и более ужасающими: двоение в глазах, онемение, усиливающийся паралич. В течение 48 часов Мэгги не могла дышать самостоятельно, и ей понадобился аппарат искусственной вентиляции легких. У нее был массивный геморрагический инсульт — в возрасте 33 лет.
Причиной была кавернома, выпуклая ягодоподобная аномалия кровеносных сосудов, которая может вызвать кровотечение. В случае Мэгги расположение каверномы — в части ее ствола мозга, называемой варолиевым мостом, — делало ее особенно опасной. Ее перевели в госпиталь Джона Хопкинса, один из немногих центров нейрохирургии, готовых лечить столь серьезное заболевание.
Ее перевели в госпиталь Джона Хопкинса, один из немногих центров нейрохирургии, готовых лечить столь серьезное заболевание.
«Она замечательная», — говорит Джуди Хуанг, нейрохирург Университета Джона Хопкинса, которая провела операцию по спасению жизни Мэгги. «Кровотечение произошло в очень деликатной части нервной системы, которая контролирует основные функции, такие как дыхание и сознание.
«Поэтому, несмотря на то, что она была парализована и у нее была дыхательная трубка, она полностью осознавала, что с ней происходит», — объясняет Хуанг.
У Мэгги лишь фрагментарные воспоминания о днях, предшествовавших операции, но она вспоминает встречу с Хуаном, когда семья собралась на встречу. «[Хуан] говорил со мной, — говорит Мэгги. «Иногда люди этого не делают. Они относятся к тебе как к предмету мебели. Но она говорила прямо со мной».
Через девять часов после операции Мэгги была вне непосредственной опасности.
Хуан говорит: «Все время, пока я в операционной, я думаю: «Вот молодая, талантливая женщина, всего несколько месяцев до свадьбы, и вот мы работаем с ее стволом мозга». удалось удалить всю [каверному], это обнадёживало — мы знали, что вероятность повторного кровотечения меньше».
удалось удалить всю [каверному], это обнадёживало — мы знали, что вероятность повторного кровотечения меньше».
Но испытания Мэгги только начинались.
Восстановление после инсульта и лицевой паралич
Мэгги вспоминает: «Я была молода и здорова и мало что знала об инсульте; Я не понимал серьезности этого и не понимал, с чем столкнулся. Когда меня выписывали из реабилитационного центра, я думал: «Я не двигаюсь так, как раньше». Я думал, что вернусь туда, где был».
«Мне говорили, что только 10 процентов выживших после инсульта доживают до конца. Но я был полон решимости сделать все возможное, чтобы попасть в эти 10 процентов.
«После операции доктор Хуан не сказал, что я «никогда» не буду делать что-то конкретное. Но ей было ясно, что мое лицо больше не может двигаться. Мой лицевой нерв был полностью разрушен кровоизлиянием. Половина моего лица будто тает, как воск. Я был в ужасе от того, как я выгляжу — я не смотрел в зеркало».
Через два месяца после операции на головном мозге Хуан спросил Мэгги, думала ли она о том, чтобы проконсультироваться с командой лицевых пластических хирургов.
Операция по реанимации лица
Для актера паралич лицевого нерва может стать огромной потерей. Когда Уиттум встретилась со своим хирургом в Центре лицевой пластической и реконструктивной хирургии при Университете Джона Хопкинса, она обнаружила, что изо всех сил пытается принять свою ситуацию.
«Команда была потрясающей и чуткой, но я все еще надеялась, что через шесть месяцев я стану лучше», — говорит она. «Офис связал меня с другой молодой женщиной, которой пересадили подъязычный нерв по поводу паралича лицевого нерва. Я был так рад поговорить с ней об этом опыте. Это действительно помогло мне принять очень трудное решение сделать операцию».
Ситуация с Мэгги была сложной. Во многих случаях лицевого паралича пластический и реконструктивный хирург может реанимировать лицо, перемещая пятый черепной нерв.
Но пятый черепной нерв Мэгги был слишком поврежден кровоизлиянием, поэтому хирург применил своего рода план Б и вместо этого использовал 12-й черепной нерв, также известный как подъязычный нерв. Хирурги переместили его на ту сторону лица Мэгги, которая пострадала от инсульта, и поместили груз на ее веко, чтобы глаз мог полностью закрыться.
Хирурги переместили его на ту сторону лица Мэгги, которая пострадала от инсульта, и поместили груз на ее веко, чтобы глаз мог полностью закрыться.
Мэгги говорит: «Операция по реанимации лица прошла так хорошо, и я очень ей благодарна. Забота была феноменальной; люди такие умные». Но она знала, что результаты не будут мгновенными, и что восстановление баланса ее лица потребует месяцев терапии и тяжелой работы.
Затем еще один удар: пути Мэгги и ее жениха разошлись. Она уехала домой в Колорадо. Не имея возможности водить машину, она хотела убедиться, что у нее есть доступ к хорошему общественному транспорту, поэтому она переехала в Денвер.
Сейчас она думает о возрождении своей карьеры.
Мэгги ничего из этого не просила. Но она выступает публично, выступает и помогает другим с теми же проблемами. Она придумывает способы рассмешить их, справиться с их симптомами. Это миссия, имеющая большее значение, чем она себе представляет.
— Нейрохирург Мэгги Джуди Хуанг
Новая жизнь и миссия
За несколько лет до инсульта Мэгги побывала в уникальной театральной труппе, обосновавшейся в Денвере: отмеченной наградами театральной труппе Phamaly. В группу входят актеры с различными физическими, когнитивными и эмоциональными проблемами.
В группу входят актеры с различными физическими, когнитивными и эмоциональными проблемами.
Мэгги связалась с ними, прошла прослушивание и получила роль в музыкальной постановке. Вскоре она вышла на сцену Денверского центра исполнительских искусств в сопровождении великолепного состава и полного оркестра.
Она вернулась. Точнее, двигаться вперед.
Она говорит: «Инсульт лишает сил. Вы чувствуете стыд, горе, бесполезность. Я не мог вернуться в школу и быть независимым. Но вернуться на сцену было здорово».
Тем временем Мэгги добавила в свой репертуар еще одну роль: рассказать миру о том, что значит потерять свои физические способности, внешность и жизненные планы из-за инсульта. Она ежегодно посещает Университет Джона Хопкинса для презентации студентам-медикам, резидентам и хирургам.
Хуан отмечает, что во время разговора Мэгги даже самые крутые врачи тронуты до слез.
Хуанг удивляется: «Мэгги ничего из этого не просила. Но она выступает публично, выступает и помогает другим с теми же проблемами. Она придумывает способы рассмешить их, справиться с их симптомами. Это миссия, имеющая большее значение, чем она себе представляет».
Она придумывает способы рассмешить их, справиться с их симптомами. Это миссия, имеющая большее значение, чем она себе представляет».
Познакомьтесь с лечащей бригадой Мэгги
О геморрагическом инсульте и параличе лицевого нерва
Инсульт случается, когда приток крови к мозгу прерывается. Клетки мозга начинают умирать уже через несколько минут без крови и кислорода. Геморрагический инсульт возникает, когда кровеносный сосуд в головном мозге лопается, изливая кровь в близлежащие ткани. Возникающее в результате давление и прерывание кровотока вызывают повреждения, которые могут включать паралич лицевого нерва — неспособность двигать мышцами лица с одной или обеих сторон.
Узнайте больше об инсульте.
Узнайте больше о параличе лицевого нерва.
Лечение инсульта в Университете Джона Хопкинса
Цереброваскулярный центр Джона Хопкинса занимается обеспечением наилучшей профилактики, диагностики, лечения, ухода и лечения пациентов с рядом цереброваскулярных заболеваний, включая инсульт.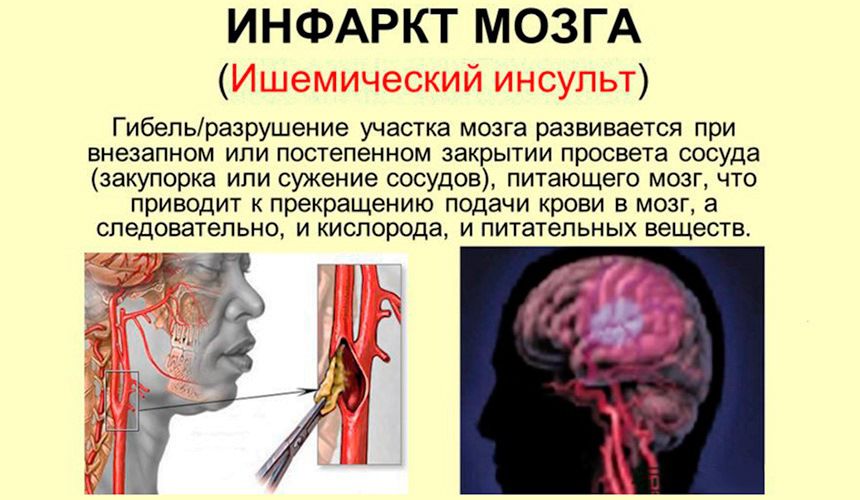 При разработке планов для наших пациентов мы ориентируемся на совместный подход.
При разработке планов для наших пациентов мы ориентируемся на совместный подход.
Узнайте больше о Цереброваскулярном центре.
Взрослая неврология: 410-955-9441
Педиатрическая неврология: 410-955-4259
Нейрохирургия взрослых: 410-955-6406
Педедиатрическая нейрохирургия: 410-955-7333333373373373737373737337337337333333333333333333333333333333337333333333373337333733373737373733н. страны или мира, мы упрощаем доступ к услугам мирового класса в Johns Hopkins.
Острый ишемический инсульт и COVID-19: опыт Комплексного центра лечения инсульта на Среднем Западе США
Введение
Вирус тяжелого острого респираторного дистресс-синдрома (SARS-CoV-2), вызывающий коронавирусную болезнь 2019 г.(COVID-19) был впервые выявлен в Ухане, Китай, и с тех пор распространился по всему миру с угрожающей скоростью, затронув более 7 миллионов человек по состоянию на 7 июня 2020 г. (1). Сообщалось о неврологическом поражении, включая инсульт (2, 3). Ишемические инсульты при COVID-19 были связаны с плохими исходами, но данные в основном ограничены азиатским и белым населением. Данных о потенциальном повышенном риске инсульта при COVID-19 пока не поступало в расово различных группах пациентов, таких как латиноамериканцы и афроамериканцы (4, 5).
(1). Сообщалось о неврологическом поражении, включая инсульт (2, 3). Ишемические инсульты при COVID-19 были связаны с плохими исходами, но данные в основном ограничены азиатским и белым населением. Данных о потенциальном повышенном риске инсульта при COVID-19 пока не поступало в расово различных группах пациентов, таких как латиноамериканцы и афроамериканцы (4, 5).
В этой рукописи мы сообщаем о клинических и лабораторных характеристиках, а также о результатах лечения пациентов с COVID-19 и острым ишемическим инсультом (ОИС), которые обратились в наш комплексный инсультный центр в Чикаго, штат Иллинойс, в период с 1 марта 2020 г. по 30 апреля 2020 г. , Наш центр третичной медицинской помощи находился в эпицентре вспышки в Чикаго на Среднем Западе США и регулярно оказывает помощь малообеспеченным и разнообразным группам пациентов с более низким уровнем грамотности в вопросах здоровья. Чтобы подтвердить наши выводы, чтобы дополнительно определить механизмы инсульта и переменные исхода, мы сравнили нашу когорту с пациентами, перенесшими инсульт, за тот же период времени в 2020 году, а также с исторической когортой за 2019 год. .
.
Methods
Мы провели ретроспективный наблюдательный анализ медицинских карт всех пациентов, поступивших в Медицинский центр Университета Раш в Чикаго, штат Иллинойс, США, в период с 1 марта 2020 г. по 30 апреля 2020 г. с подтвержденным диагнозом ПИС. на магнитно-резонансной томографии (МРТ) или компьютерной томографии (КТ) и которые были положительными на COVID-19 с анализом полимеразной цепной реакции с обратной транскриптазой в реальном времени из мазка из носоглотки. Чтобы компенсировать любые сезонные или ежемесячные колебания заболеваемости и смертности от ОИС, мы сравнили когорту с контрольной группой пациентов без COVID-19.Пациенты с ПИИ, госпитализированные в соответствующие сроки в 2020 году. Мы также сравнили с исторической когортой за 2019 год, чтобы контролировать любые изменения в популяции пациентов с течением времени. Две разные когорты использовались в качестве контроля, чтобы избежать случайных различий в демографических характеристиках между периодом до COVID и эпохой COVID.
Демографические, а также клинические и лабораторные данные были собраны посредством обзора системы электронных медицинских карт. К ним относятся возраст, пол, этническая принадлежность, ранее существовавшие сосудистые факторы риска, показатели жизненно важных функций при поступлении, лабораторные показатели и оценка по шкале инсульта Национального института здравоохранения (NIHSS) при поступлении и при выписке (или во время сбора данных для пациентов, все еще госпитализированных). ). Разделили больных COVID-19AIS в группу «COVID», определяемую как пациенты, поступившие первоначально с симптомами COVID-19, а затем у которых впоследствии развился AIS, и «нейро» группу, где пациенты были госпитализированы с AIS в качестве начальных симптомов и имели положительный результат теста на COVID-19. Группа «COVID» имела более обширное обследование на воспаление и коагулопатию. Все пациенты получали неотложную помощь при инсульте в соответствии с рекомендациями Американской кардиологической ассоциации и Американской ассоциации инсульта (6).
Мы использовали классификацию (TOAST) для определения этиологии инсульта (7). Все пациенты с AIS прошли обширную оценку, включая расширенную визуализацию сердца, панель гиперкоагуляции и длительный мониторинг сердца во время госпитализации. Мы дополнительно оценили пациентов с криптогенным инсультом для выявления эмболического инсульта неизвестной этиологии (ESUS) в соответствии с опубликованными критериями (8). Пациенты с потенциальными механизмами инсульта, которые, как считается, связаны с состоянием гиперкоагуляции из-за COVID-19.были помещены под криптогенные и/или ESUS механизмы.
Показатели исхода основывались на характере выписки и модифицированной шкале Рэнкина (mRS) (9). Тяжесть COVID-19 была определена как легкая, обычная или тяжелая/критическая на основании 7-го издания «Плана диагностики и лечения новой коронавирусной пневмонии» со следующим описанием: легкая, определяемая как незначительные клинические симптомы и отсутствие воспаления легких на визуализация; регулярные, с лихорадкой и симптомами респираторного тракта, а также с признаками видимого воспаления легких при визуализации; тяжелая, с одышкой, ЧДД более 30 вдохов в минуту или SpO2 <93% в покое при пульсоксиметрии; и критический, с необходимостью ИВЛ или наличием шока или сочетанной недостаточности других органов, требующих наблюдения в ОИТ (10).
Статистическое тестирование использовалось для выявления промежуточных различий между группами и связи отдельных переменных с предварительно выбранными результатами. Когорты сравнивались с использованием критерия Стьюдента t для параметрических непрерывных переменных, U-критерия Манна-Уитни для непараметрических непрерывных переменных и точного критерия Фишера для дихотомических переменных. Логистическая регрессия использовалась для анализа выбранных переменных (либо клинически значимых, либо со статистической связью в первом анализе) в отношении предварительно выбранных измерений результатов с поправкой на смешанные факторы. Все анализы проводились с использованием имеющегося в продаже статистического программного обеспечения SPSS (версия 21, Чикаго, Иллинойс, США). Значимость была установлена на уровне р < 0,05. Данные были собраны с помощью REDCap, электронного инструмента сбора данных, размещенного в нашем учреждении (11). Этот протокол исследования был одобрен институциональным наблюдательным советом Университета Раша.
Результаты
Демографические и клинические характеристики
В период с 1 марта 2020 г. по 30 апреля 2020 г. около 650 пациентов были госпитализированы с COVID-19, из которых 13 пациентов имели ПИС (оценочный процент 2,0%). Когорта COVID-19 AIS в основном состояла из латиноамериканцев (46,1%) и афроамериканцев (30,7%) в возрасте от 31 до 80 лет (в среднем 61,6 года). В группе «COVID» было 6 пациентов (47%), в группе «Нейро» — 7 (53%). Среднее время диагностики АИС в группе «COVID» после госпитализации составило 7,1 ± 5,1 дня. Обычные сосудистые факторы риска были общими в обеих группах без особой предрасположенности ни к группе «COVID», ни к группе «Нейро». Три наиболее распространенных фактора риска при COVID-19Когорта AIS включала артериальную гипертензию (69,2%), сахарный диабет (СД) 2 типа (69,2%) и гиперлипидемию (30,7%). COVID-19 считался тяжелым или критическим у 61,5% (
 Из 13 пациентов у 30,7% ( n = 4) также была наложенная бактериальная инфекция. Медиана госпитализации по шкале NIHSS составила 16 (IQR 4–23) у всех пациентов с COVID-AIS, с более высоким баллом 13 в группе «Нейро» по сравнению с 4,5 в группе «COVID» (таблица 1).
Из 13 пациентов у 30,7% ( n = 4) также была наложенная бактериальная инфекция. Медиана госпитализации по шкале NIHSS составила 16 (IQR 4–23) у всех пациентов с COVID-AIS, с более высоким баллом 13 в группе «Нейро» по сравнению с 4,5 в группе «COVID» (таблица 1). Таблица 1 . Демографические и клинические особенности 13 последовательных пациентов с острым ишемическим инсультом с инфекцией COVID-19.
Лабораторные характеристики
Исходные жизненные показатели и лабораторные показатели подробно представлены в таблице 2. Средняя температура 99,6 ± 1,8°F, среднее артериальное давление 82,6 ± 38,7 мм рт.ст., частота сердечных сокращений 90,6 ± 29,4 ударов в минуту, частота дыхания 22 ± 8 вдохов в минуту, сатурация кислорода 93,3 ± 7,8%. Пациенты в группе «COVID» чаще имели полиорганную недостаточность и повышенные маркеры воспаления и коагулопатии (табл. 2).
Таблица 2 . Жизненные показатели при поступлении и лабораторные показатели при поступлении у пациентов с острым ишемическим инсультом с COVID-19.
Исход Показатели
Ишемические инсульты были преимущественно корковыми (84,6%), по ходу средней мозговой артерии (76,9%), затем задней мозговой артерии (23%). Этиология инсульта была классифицирована как криптогенная и/или ЭУЗИ в 53,8% ( n = 7), кардиоэмболическая в 23% ( n = 3), атеросклероз крупных артерий в 15,3% (n = 2) и поражение мелких сосудов в 7% ( н = 1). ESUS подозревали у 71,4% «Нейро» по сравнению с 33,3% «COVID». В целом 60% ( n = 3) пациентов с признаками окклюзии крупных сосудов (LVO) подверглись эндоваскулярной тромбэктомии. В то время как в группе «COVID» было больше ЛВО (50%), большее количество пациентов в группе «Нейро» (42,8 против 16,6%) получили вмешательства при остром инсульте, при этом задержки в выявлении симптомов ПИС в группе «COVID» объясняются маскировкой симптомов системными проявлениями COVID-19. Терапевтическая антикоагулянтная терапия была начата в 38,4% ( n = 5) пациентов из-за опасений гиперкоагуляции и в 7% ( n = 1) из-за мерцательной аритмии. Медиана NIHSS при выписке для когорты COVID AIS составляла 11 (IQR 4–23) со медианой mRS 4 (IQR 3–4). Благоприятный исход с выпиской на дом или в реабилитационные учреждения наблюдался у 61,5% ( n = 3). Два пациента (15,3%) скончались от осложнений COVID-19, двое (15,3%) нуждались в длительном стационарном лечении. Один пациент остается госпитализированным (табл. 1).
Медиана NIHSS при выписке для когорты COVID AIS составляла 11 (IQR 4–23) со медианой mRS 4 (IQR 3–4). Благоприятный исход с выпиской на дом или в реабилитационные учреждения наблюдался у 61,5% ( n = 3). Два пациента (15,3%) скончались от осложнений COVID-19, двое (15,3%) нуждались в длительном стационарном лечении. Один пациент остается госпитализированным (табл. 1).
Одномерный и логистический регрессионный анализ
За исключением СД 2 типа, который был более распространен в группе пациентов с COVID-19 AIS (64,2 против 24,5%,
 0145 р 0,989 и 31 против 36%, р 0,766). В то время как медиана NIHSS при поступлении не различалась среди пациентов с AIS COVID-19 и пациентов без COVID-19 в 2020 и 2019 годах, NIHSS при выписке был значительно выше [11 (IQR 4–23) по сравнению с 3 (IQR 2–13). ), p 0,036 и 11 (IQR 4–23) против 4 (IQR 1–11), p 0,042]. Наблюдалась тенденция к меньшему введению альтеплазы у пациентов с ОИС COVID-19, хотя и не статистически значимая (7,1 против 20,7%, p 0,435 и 7,1 против 27,2%, стр 0,178). Когорта AIS COVID-19 имела худшее mRS> 2 при выписке (78,5 против 47,16%, p 0,047 и 78,5 против 40,9%, p 0,010) (таблица 3), даже после поправки на возраст и пол в логистической регрессионная модель [ p 0,046, ОШ 3,82, (ДИ 1,02–14,3)].
0145 р 0,989 и 31 против 36%, р 0,766). В то время как медиана NIHSS при поступлении не различалась среди пациентов с AIS COVID-19 и пациентов без COVID-19 в 2020 и 2019 годах, NIHSS при выписке был значительно выше [11 (IQR 4–23) по сравнению с 3 (IQR 2–13). ), p 0,036 и 11 (IQR 4–23) против 4 (IQR 1–11), p 0,042]. Наблюдалась тенденция к меньшему введению альтеплазы у пациентов с ОИС COVID-19, хотя и не статистически значимая (7,1 против 20,7%, p 0,435 и 7,1 против 27,2%, стр 0,178). Когорта AIS COVID-19 имела худшее mRS> 2 при выписке (78,5 против 47,16%, p 0,047 и 78,5 против 40,9%, p 0,010) (таблица 3), даже после поправки на возраст и пол в логистической регрессионная модель [ p 0,046, ОШ 3,82, (ДИ 1,02–14,3)]. Таблица 3 . Сравнение пациентов с острым ишемическим инсультом с инфекцией COVID-19 и пациентов с острым ишемическим инсультом без инфекции COVID-19, госпитализированных в одни и те же сроки с 1 марта 2020 г. по 30 апреля 2020 г. и 1 марта 2019 г.–30 апреля 2019 г.
по 30 апреля 2020 г. и 1 марта 2019 г.–30 апреля 2019 г.
Обсуждение
В этом одноцентровом ретроспективном обсервационном исследовании мы выявили 13 пациентов с АИС и сопутствующим COVID-19. Приблизительно у 2,0% всех пациентов с COVID-19 в нашем учреждении был диагностирован AIS, что выше, чем ранее сообщалось в литературе из США (12), но аналогично таковому из Ухани, Китай (5). Средний возраст пациентов с АИС и COVID-19 составил 61,6 года без существенной половой принадлежности. В отличие от данных, полученных из Нью-Йорка (12), в нашей когорте был более высокий процент латиноамериканцев и афроамериканцев (76,8%), что подчеркивает расовое неравенство COVID-19.в нашем столичном городе. В нескольких исследованиях подчеркивается непропорционально тяжелое бремя этого заболевания для этих сообществ. Социальное и экономическое неравенство, меньший доступ к медицинской помощи наряду с генетическими факторами, связанными с более сильным тромбовоспалительным ответом, могли способствовать более высокому уровню инфицирования и худшему исходу у латиноамериканцев и афроамериканцев (13, 14). У большинства наших пациентов была тяжелая или критическая форма COVID-19, что подтверждает ранее опубликованные данные о высокой распространенности неврологических осложнений, наблюдаемых в этой группе (2). Кроме того, тенденция к кортикальным инсультам с этиологической классификацией как ESUS отражает коагулопатию и потенциальную причинно-следственную связь между COVID-19инсульт (12).
У большинства наших пациентов была тяжелая или критическая форма COVID-19, что подтверждает ранее опубликованные данные о высокой распространенности неврологических осложнений, наблюдаемых в этой группе (2). Кроме того, тенденция к кортикальным инсультам с этиологической классификацией как ESUS отражает коагулопатию и потенциальную причинно-следственную связь между COVID-19инсульт (12).
Задержка традиционных вмешательств при инсульте, особенно среди пациентов, у которых развился ИИС во время лечения COVID-19, может быть объяснена маскировкой симптомов острого инсульта вирусным заболеванием, задержкой в распознавании симптомов инсульта и/или использованием антикоагулянтов в время оценки.
Несколько потенциальных механизмов могут привести к инсульту в условиях COVID-19. Ангиотензинпревращающий фермент, который является мишенью SARS-CoV2, экспрессируется клетками нервной системы. Это подвергает мозг риску прямой инфекции эндотелиальных клеток и диффузного эндотелиального воспаления (15). Коагулопатия, связанная с COVID, которая, вероятно, является результатом интенсивной воспалительной реакции, может привести к увеличению тромботических осложнений, включая ишемический инсульт (16). Поражение сердца также является характерной чертой COVID-19., что приводит к стрессовой кардиомиопатии, прямому повреждению миокарда и аритмиям с потенциальным повышенным риском ишемического инсульта (17). Наконец, длительная госпитализация и дисавтономия могут привести к ишемическому инсульту, особенно на фоне септического шока и гипотензии (18).
Коагулопатия, связанная с COVID, которая, вероятно, является результатом интенсивной воспалительной реакции, может привести к увеличению тромботических осложнений, включая ишемический инсульт (16). Поражение сердца также является характерной чертой COVID-19., что приводит к стрессовой кардиомиопатии, прямому повреждению миокарда и аритмиям с потенциальным повышенным риском ишемического инсульта (17). Наконец, длительная госпитализация и дисавтономия могут привести к ишемическому инсульту, особенно на фоне септического шока и гипотензии (18).
Сильные стороны и недостатки
В нашем исследовании представлено подробное описание пациентов с COVID-19 и АИС, а также подчеркивается расовое неравенство и неблагоприятные исходы, связанные с этой высококонтагиозной вирусной инфекцией. Это исследование также подчеркивает, что, несмотря на COVID-19более серьезно воздействуя на пожилых пациентов, повышенный риск ПИС при COVID-19 не зависит от возраста. Сравнение с текущими и историческими когортами предполагает прямую причинно-следственную связь COVID-19 и AIS, подчеркивая важность проверки на COVID-19 у пациентов с ESUS и / или криптогенными механизмами инсульта.
Наше исследование имеет несколько ограничений из-за небольшого размера, ретроспективного подхода и отсутствия долгосрочного наблюдения и результатов. Мы также подозреваем, что заболеваемость ПИС намного выше, так как многие пациенты с инфекцией могли умереть от болезни до выявления симптомов инсульта или, возможно, не были обследованы неврологической службой, и, таким образом, неврологические симптомы могли не быть выявлены. захвачен.
Заключение
Таким образом, ишемический инсульт при COVID-19 имеет тенденцию быть более тяжелым, в основном кортикальным, может возникать независимо от общих сосудистых факторов риска, не зависит от пола и может поражать также более молодое население. Наша группа чаще наблюдала AIS при COVID-19 в латиноамериканских и афроамериканских сообществах, что является отражением неравенства в медицинском обслуживании и ограниченного доступа к медицинской помощи среди меньшинств.
Заявление о доступности данных
Необработанные данные, подтверждающие выводы этой статьи, будут предоставлены авторами без неоправданных оговорок.
Заявление об этике
Исследования с участием людей были рассмотрены и одобрены Институциональным наблюдательным советом Университета Раш. Письменное информированное согласие на участие в этом исследовании не требовалось в соответствии с национальным законодательством и институциональными требованиями.
Вклад авторов
PG и PP в равной степени внесли свой вклад как первые авторы в сбор данных, интерпретацию данных и написание рукописи. ID и JC в равной степени, как и последние авторы, внесли свой вклад в интерпретацию данных и критический пересмотр рукописи на предмет интеллектуального содержания. JH, RD, TT, DP, RG, NO, AV и SJ участвовали в разработке и сборе данных. Все авторы несут полную ответственность за достоверность данных и результатов рукописи.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Благодарности
Мы хотели бы выразить признательность нашим координаторам данных, Анджали Астана MPH, MS, Келси Феган BS, Vikram Patel MSN, RN.
Сокращения
SARS-CoV-2, вирус тяжелого острого респираторного дистресс-синдрома; COVID-19, коронавирусная болезнь 19; NIHSS, Шкала инсульта Национального института здравоохранения.
Ссылки
1. Zhu N, Zhang D, Wang W, Li X, Yang B, Song J, et al. Новый коронавирус от пациентов с пневмонией в Китае, 2019 г. N Engl J Med.
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
2. Mao L, Jin H, Wang M, Hu Y, Chen S, He Q, et al. Неврологические проявления госпитализированных пациентов с коронавирусной болезнью 2019 года в Ухане, Китай. JAMA Нейрол . (2020) 77: 1–9. doi: 10.1001/jamaneurol.2020.1127
PubMed Abstract | CrossRef Full Text
3. Helms J, Kremer S, Merdji H, Clere-Jehl R, Schenck M, Kummerlen C, et al. Неврологические особенности при тяжелой инфекции сарков-2. N Английский J Med . (2020) 382: 2268–70. doi: 10.1056/NEJMc2008597
Неврологические особенности при тяжелой инфекции сарков-2. N Английский J Med . (2020) 382: 2268–70. doi: 10.1056/NEJMc2008597
CrossRef Полный текст | Google Scholar
4. Escalard S, Maïer B, Redjem H, Delvoye F, Hébert S, Smajda S, et al. Лечение острого ишемического инсульта вследствие окклюзии крупных сосудов при ковид-19: опыт из Парижа. Инсульт. (2020) 51:2540–3. doi: 10.1161/STROKEAHA.120.030574
PubMed Abstract | CrossRef Full Text
5. Qin C, Zhou L, Hu Z, Yang S, Zhang S, Chen M, et al. Клинические характеристики и исходы у пациентов с COVID-19 с инсультом в анамнезе в Ухане, Китай. Инсульт. (2020) 51:2219–23. doi: 10.1161/STROKEAHA.120.030365
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
6. Powers WJ, Rabinstein AA, Ackerson T, Adeoye OM, Bambakidis NC, Becker K, et al. Рекомендации по раннему ведению пациентов с острым ишемическим инсультом: 2019 г.обновление рекомендаций 2018 г. по раннему лечению острого ишемического инсульта: руководство для медицинских работников Американской кардиологической ассоциации/Американской ассоциации инсульта. Инсульт. (2019) 50:e344–418. doi: 10.1161/STR.0000000000000211
по раннему лечению острого ишемического инсульта: руководство для медицинских работников Американской кардиологической ассоциации/Американской ассоциации инсульта. Инсульт. (2019) 50:e344–418. doi: 10.1161/STR.0000000000000211
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
7. Adams HP, Bendixen BH, Kappelle LJ, Biller J, Love BB, Gordon DL, et al. Классификация подтипов острого ишемического инсульта. Определения для использования в многоцелевом клиническом исследовании. Тост. Испытание org 10172 в лечении острого инсульта.
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
8. Hart RG, Diener HC, Coutts SB, Easton JD, Granger CB, O’Donnell MJ, et al. Эмболические инсульты неопределенного происхождения: случай новой клинической конструкции. Ланцет Нейрол. (2014) 13:429–38. doi: 10.1016/S1474-4422(13)70310-7
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
9. Бродерик Дж. П., Адеой О., Элм Дж. Эволюция модифицированной шкалы Ранкина и ее использование в будущих исследованиях инсульта. Инсульт. (2017) 48:2007–12. doi: 10.1161/STROKEAHA.117.017866
Бродерик Дж. П., Адеой О., Элм Дж. Эволюция модифицированной шкалы Ранкина и ее использование в будущих исследованиях инсульта. Инсульт. (2017) 48:2007–12. doi: 10.1161/STROKEAHA.117.017866
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
10. План лечения диагностики новой коронавирусной пневмонии (предварительное 7-е изд.). Доступно в Интернете по адресу: https://www.chinalawtranslate.com/en/coronavirus-treatment-plan-7/ (по состоянию на 30 апреля 2020 г.).
11. Харрис П.А., Тейлор Р., Тильке Р., Пейн Дж., Гонсалес Н., Конде Дж.Г. Сбор электронных данных исследований (redcap) — основанная на метаданных методология и рабочий процесс для обеспечения трансляционной поддержки информатики исследований. Ж Биомед Информ. (2009) 42:377–81 doi: 10.1016/j.jbi.2008.08.010
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
12. Yaghi S, Ishida K, Torres J, Mac Grory B, Raz E, Humbert K, et al. Sars2-cov-2 и инсульт в системе здравоохранения Нью-Йорка. Инсульт. (2020). 51:2002–11. doi: 10.1161/STROKEAHA.120.030335
Инсульт. (2020). 51:2002–11. doi: 10.1161/STROKEAHA.120.030335
CrossRef Full Text
13. Yancy CW. COVID-19 и афроамериканцы. ЯМА. (2020) 323:1891–2. дои: 10.1001/jama.2020.6548
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
14. Вепа А., Бае Дж. П., Ахмед Ф., Парик М., Кхунти К. COVID-19 и этническая принадлежность: новая патофизиологическая роль воспаления. Диабетический метаболический синдром . (2020) 14:1043–51. doi: 10.1016/j.dsx.2020.06.056
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
15. Varga Z, Flammer AJ, Steiger P, Haberecker M, Andermatt R, Zinkernagel AS, et al. Инфекция эндотелиальных клеток и эндотелиит при covid-19. Ланцет. (2020) 395:1417–8 doi: 10.1016/S0140-6736(20)30937-5
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
16. Коннорс Дж.М., Леви Дж.Х. Covid-19 и его влияние на тромбоз и антикоагулянтную терапию.
